(2007•江门模拟)如图所示为电热毯电路示意图,交流电压u=311sinl00πt(v),当开关S接通时.电热丝的电功
 abcdefgzhu2022-10-04 11:39:541条回答
abcdefgzhu2022-10-04 11:39:541条回答 (2007•江门模拟)如图所示为电热毯电路示意图,交流电压u=311sinl00πt(v),当开关S接通时.电热丝的电功率为P0;下列说法正确的是( )
(2007•江门模拟)如图所示为电热毯电路示意图,交流电压u=311sinl00πt(v),当开关S接通时.电热丝的电功率为P0;下列说法正确的是( )A.开关接通时,交流电压表的读数为220V
B.开关接通时,交流电压表的读数为311V
C.开关断开时,交流电压表的读数为311V,电热丝功率为P0/2
D.开关断开时,交流电压表的读数为156V,电热丝功率为P0/2

已提交,审核后显示!提交回复
共1条回复
 k19876 共回答了27个问题
k19876 共回答了27个问题 |采纳率92.6%- 解题思路:电压表读数为有效值,开关接通时,电压表测量原线圈电压,温控器是二极管,具有正向通电性,所以开关断开后,只有一半周期的电流通过电路,根据电流的热效应求出有效值.
A、电压表读数为有效值,开关接通时,电压表测量原线圈电压,所以电压表的示数为:
311
2=220V,故A正确,B错误;
C、温控器是二极管,具有正向通电性,所以开关断开后,只有一半周期的电流通过电路,根据电流的热效应得:
2202
R•
T
2+0=
U2
RT,解得:U=
220
2=156V,
P=
U2
R=
P0
2,故C错误,D正确.
故选AD点评:
本题考点: 交流的峰值、有效值以及它们的关系.
考点点评: 本题考查有关交变电流有效值的计算问题,知道二极管具有正向通电性,难度适中. - 1年前
相关推荐
- (2011•江门一模)先化简,再求值:x2−1x2+2x+1•[1/2x−2],其中x=-[1/2].
 sellia11年前1
sellia11年前1 -
 相爱xxING 共回答了20个问题
相爱xxING 共回答了20个问题 |采纳率90%解题思路:做乘法运算时要注意先把分子、分母能因式分解的先分解,然后约分,最后代值计算.原式=
(x+1)(x−1)
(x+1)2•
1
2(x−1)
=[1/2x+2];
当x=−
1
2时,原式=1.点评:
本题考点: 分式的化简求值.
考点点评: 分子、分母能因式分解的先因式分解,分式化到最简是解答的关键.1年前查看全部
- (2009•江门一模)实验室制备纯碱的主要步骤是:
(2009•江门一模)实验室制备纯碱的主要步骤是:
①将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30-35℃,搅拌下分批加入研细的NH4HCO3固体
②加料完毕后,继续保温30分钟
③静置、过滤得NaHCO3晶体
④用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧,制得Na2CO3固体.
四种盐在不回温度下的溶解度(g/l00g水)表
①>35℃NH4HC03会有分解
0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃ 100℃ NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 39.8 NH4HCO3 11.9 15.8 21.0 27.0 -① NaHCO3 6.9 8.1 9.6 11.1 12.7 14.5 16.4 NH4Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.3 77.3
请回答:
(1)反应温度控制在30-35℃,是因为______;为控制此温度范围,采取的加热方法为______.
(2)加料完毕后,继续保温30分钟,目的是______;静置后只析出NaHCO3品体的原因是______.
(3)洗涤NaHCO3晶体的操作是______.
(4)过滤所得的母液中含有的溶质______(以化学式表示).
(5)写出本实验中制备纯碱的有关化学方程式______.
(6)测试纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1-2滴酚酞指示剂,用物质的量浓度为c (mol/L)的HCl溶液滴定至溶液由红色到无色,所用HCl溶液体积为V1 mL,再加1-2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液总体积为V2mL,写出纯碱样品中NaHCO3质量分数的计算式:
×100%c(v2−v1)106 1000w .
×100%c(v2−v1)106 1000w  vansee1年前1
vansee1年前1 -
 mzzr 共回答了20个问题
mzzr 共回答了20个问题 |采纳率95%解题思路:(1)碳酸氢铵在低于30℃时分解较少,40℃时开始大量分解,温度过高碳酸氢氨分解,若温度过低,则反应速率较慢.故反应温度控制在30-35℃之间为宜;水浴加热是把要加热的物质放在水中,通过给水加热达到给物质加热的效果.水浴加热的优点是避免了直接加热造成的过度剧烈与温度的不可控性,可以平稳地加热,水浴加热的缺点是加热温度最高只能达到100度;
(2)加料完毕后,继续保温一段时间为使反应充分进行,使反应完全.物质的溶解度,碳酸氢铵0℃时溶解度为11.3%;20℃时为21%;40℃时为35%.碳酸氢钠30℃为11.1g,30℃时碳酸氢钠的溶解度更小,故碳酸氢钠先析出;
(3)用蒸馏水洗涤NaHCO3晶体中杂质,此反应中杂质为 NaCl、NH4Cl、NH4HCO3;用过滤的方法进行洗涤晶体;
(4)过滤除去析出的碳酸氢钠后所得的母液主要成分为NaHCO3、NaCl、NH4Cl、NH4HCO3;
(5)加酚酞指示剂,指示CO32-+H+=HCO3-应的终点,再加甲基橙指示剂,指示HCO3-+H+=CO2+H2O反应的终点,样品中含有的碳酸氢钠反应消耗盐酸体积为(V2-V1 )mL,消耗盐酸的物质的量为c(V2-V1 )÷1000 mol,故碳酸氢钠的物质的量为c(V2-V1)÷1000 mol,以此来计算碳酸氢钠的质量分数;(1)碳酸氢铵10~20℃时,不易分解,30℃时开始大量分解.若温度过低,则反应速率较慢.故反应温度控制在30-35℃之间为宜.水浴加热是把要加热的物质放在水中,通过给水加热达到给物质加热的效果.一般都是把要反应的物质放在试管中,再把试管放在装有水的烧杯中,再在烧杯中插一根温度计,可以控制反应温度.水浴加热的优点是避免了直接加热造成的过度剧烈与温度的不可控性,可以平稳地加热,许多反应需要严格的温度控制,就需要水浴加热.水浴加热的缺点是加热温度最高只能达到100度.
故答案为:NH4HCO3分解;反应速率降低;水浴加热;
(2)加料完毕后,继续保温30分钟,可以使反应充分进行,使反应完全.碳酸氢铵0℃时溶解度为11.3%;20℃时为21%;40℃时为35%.碳酸氢钠0℃溶解度为6.9 g,5℃为7.45 g,
10℃为8.15 g,15℃为8.85 g,20℃为9.6 g,25℃为10.35 g,30℃为11.1g,35℃为11.9 g,40℃为12.7 g,45℃为13.55 g,50℃为14.45 g,55℃为15.4g,60℃为16.4g.30℃时碳酸氢钠的溶解度更小,故碳酸氢钠先析出.故答案为:使反应充分进行;NaHCO3的溶解度最小;
(3)用蒸馏水洗涤NaHCO3晶体的目的是为了除去杂质,此反应中杂质为 NaCl、NH4Cl、NH4HCO3;洗涤NaHC03晶体的操作是:把蒸馏水沿着玻璃棒注入到过滤器中至浸没沉淀,静置待蒸馏水滤出,重复操作2-3次;
故答案为:把蒸馏水沿着玻璃棒注入到过滤器中至浸没沉淀,静置待蒸馏水滤出,重复操作2-3次;
(4)过滤除去析出的碳酸氢钠,溶液中还有部分碳酸氢钠未析出,还有溶解在溶液中的NaCl、NH4Cl、NH4HCO3,所得的母液主要成分为NaHCO3、NaCl、NH4Cl、NH4HCO3;
故答案为:NaHCO3、NaCl、NH4Cl、NH4HCO3;
(5)加酚酞指示剂,变色范围为8-10,用物质的量浓度为c(mol/L)的HCl溶液滴定至溶液由红色到无色,指示CO32-+H+=HCO3-反应的终点,所用HCl溶液体积为V1mL;再加甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,指示HCO3-+H+=CO2↑+H2O反应的终点,所用HCl溶液体积为V2 mL.上述的两个离子方程式为①CO32-+H+=HCO3-②HCO3-+H+=CO2+H2O,故样品中含有的碳酸氢钠反应消耗盐酸体积为(V2-V1 )mL,消耗盐酸的物质的量为c(V2-V1 )÷1000 mol,故碳酸氢钠的物质的量为c(V2-V1)÷1000 mol,碳酸氢钠的质量为c(V2-V1 )M÷1000 g,碳酸氢钠的质量分数为
c(v2−v1)M
1000w×100%=
c(V2−V1)×84
1000w×100%
故答案为:
c(V2−V1)×84
1000w×100%点评:
本题考点: 纯碱工业(侯氏制碱法).
考点点评: 本题考查学生根据侯氏制碱法的基本过程进行解题,学生能利用各种物质常见的溶解度和物质的质量分数来计算是解题的关键,难度稍大.1年前查看全部
- (2013•江门二模)(1+2x)n的展开式中x3的系数等于x2的系数的4倍,则n等于______.
 劳力士戴八块1年前1
劳力士戴八块1年前1 -
 fu4year 共回答了12个问题
fu4year 共回答了12个问题 |采纳率100%解题思路:设(1+2x)n的展开式的通项公式为Tr+1,利用(1+2x)n的展开式中x3的系数等于x2的系数的4倍,得到n的关系式,解之即可.设(1+2x)n的展开式的通项公式为Tr+1,
则Tr+1=
Crn(2x)r=2r•
Crn•xr,
令r=3得展开式中x3的系数为:8
C3n,
令r=2得展开式中x2的系数为4
C2n.
依题意,8
C3n=4×4
C2n,
即
n(n−1)(n−2)
3×2×1=2×
n(n−1)
2,解得n=8.
故答案为:8.点评:
本题考点: 二项式定理的应用.
考点点评: 本题考查二项式定理的应用,着重考查展开式的通项公式,考查理解与运算能力,属于中档题.1年前查看全部
- (2009•江门一模)氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质是微溶于水的白
(2009•江门一模)氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质是微溶于水的白色固体,露置于空气中易被氧化为绿色的碱式氯化铜(Cu2(0H)3Cl),在热水中易水解生成氧化铜水合物而呈红色.以下是一种采用亚硫酸盐还原法,从含铜电镀废水中制备氯化亚铜的工艺流程如图1.

已知Ksp:CuCl:1.2×10-4 CuOH:1.4×10-15 Cu (OH) 2:1.6×10-10
请回答以下问题:
(1)写出反应①制备氯化亚铜的离子反应方程式:______.
(2)为提高CuCl的产率,常在反应①的体系中加入稀碱溶液,调节pH至3.5.这样做的目的是______.
(3)图2是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图2可知,溶液温度控制在______时,CuCl产率能达到94%,随后随温度升高CuCl产率会下降,其原因是______.
(4)若要提高Cucl的产率你认为还可采取的措施有______.
(5)写出氯化亚铜在空气中被氧化的化学方程式______.
(6)反应①也可用铁代替亚硫酸钠,写出该反应的化学方程式______. 酷狐1年前1
酷狐1年前1 -
 linxi76 共回答了26个问题
linxi76 共回答了26个问题 |采纳率92.3%解题思路:(1)根据题目信息及氧化还原反应的有关知识,书写配平离子方程式;
(2)根据平衡移动原理,减少生成物的浓度,化学平衡正向移动;
(3)根据此温度下CuCl产率最大;根据信息可知,考虑温度过高,促进了CuCl的水解,同时加快反应速率,CuCl易被氧化为绿色的高价铜盐;
(4)考虑隔绝空气条件下进行;
(5)根据氧化还原反应的化合价升降规律,结合给出的氧化产物,写出化学方程式;
(6)加入铁替代亚硫酸钠,所起的作用相同,做还原剂,把俄二价铜还原为一价铜,由于铜离子氧化性较弱,溶液中反应的铁被氧化为二价,根据原子守恒、电子守恒书写化学方程式.(1)由图示可知,反应物有:Cu2+、SO32-、Cl-,生成物有CuCl2、SO4-,由于是氧化还原反应,化合价发生了变化,根据电子得失和质量守恒进行配平:2Cu2++SO32-+2Cl-+H2O=CuCl2↓+SO4-+2H+,故答案为:2Cu2++SO32-+2Cl-+H2O=CuCl2↓+SO4-+2H+;
(2)因减少生成物的浓度,化学平衡正向移动,OH-中和了反应中的H+,有利于平衡向右移动,提高CuCl的产率.但当OH-浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜沉淀(Cu2+能与OH-结合,生成氢氧化铜沉淀),从而降低了CuCl的产率,
故答案为:OH-中和了反应中的H+,有利于平衡向右移动,提高CuCl的产率.但当OH-浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜沉淀,从而降低了CuCl的产率;
(3)根据图象可知,因在60℃时CuCl产率最大,根据信息可知,随温度升高,促进了CuCl的水解,CuCl被氧化的速度加快,
故答案为:60℃温度过高,一是促进了CuCl的水解,二是促进了CuCl与空气中氧气发生反应;
(4)因温度升高,促进了CuCl与空气中氧气发生反应,所以反应①在隔绝空气条件下(还原气氛)进行可以提高CuCl的产率,故答案为:反应①在隔绝空气条件下进行;
(5)根据氧化产物结合氧化还原反应的电子守恒和原子守恒写出化学方程式并配平:4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl,故答案为:4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl;
(6)应①也可用铁代替亚硫酸钠,铁起的作用是做还原剂,把二价铜离子还原为氯化亚铜,本身被氧化为二价铁盐,书写化学方程式为2CuSO4+2NaCl+Fe=2CuCl↓+FeSO4+Na2SO4,
故答案为:2CuSO4+2NaCl+Fe=2CuCl↓+FeSO4+Na2SO4.点评:
本题考点: 铜金属及其重要化合物的主要性质;难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题主要考查了CuCl的制备,对制备过程中的有关知识进行了考查,氧化还原反应实质和规律的应用,培养了学生分析问题的能力和运用知识的能力.1年前查看全部
- (2010•江门一模)随机抽取某中学12位高三同学,调查他们春节期间购书费用(单位:元),获得数据的茎叶图如图,这12位
 (2010•江门一模)随机抽取某中学12位高三同学,调查他们春节期间购书费用(单位:元),获得数据的茎叶图如图,这12位同学购书的平均费用是( )
(2010•江门一模)随机抽取某中学12位高三同学,调查他们春节期间购书费用(单位:元),获得数据的茎叶图如图,这12位同学购书的平均费用是( )
A.125元
B.125.5元
C.126元
D.126.5元 tianyu13145201年前1
tianyu13145201年前1 -
 yjrrg01 共回答了16个问题
yjrrg01 共回答了16个问题 |采纳率93.8%由茎叶图可以得到12个数据,
这组数据的平均数是[113+115+117+122+122+124+126+129+131+135+135+137/12]
=[1506/12]=125.5
故选B.1年前查看全部
- (2009•江门一模)下列叙述正确的是( )
(2009•江门一模)下列叙述正确的是( )
①C02的大量排放会加剧温室效应
②正常雨水的pH为5.6,主要是因为溶解了SO2
③利用太阳能、风能和氢能替代化石能源能改善空气质量
④含磷合成洗涤剂易于被细菌分解,不会导致水体污染
⑤为防止电池中的重金属离子污染土壤和水源,废电池要集中处理.
A.①②③④⑤
B.②③⑤
C.①③⑤
D.①②④⑤ 珍惜和无奈1年前1
珍惜和无奈1年前1 -
 babyface908 共回答了18个问题
babyface908 共回答了18个问题 |采纳率83.3%解题思路:①温室效应加剧主要是由于现代化工业社会燃烧过多煤炭、石油和天然气,这些燃料燃烧后放出大量的二氧化碳气体进入大气造成的;
②正常雨水的pH为5.6,是因为溶解了二氧化碳气体形成的碳酸造成;
③清洁能源替代化石燃料可以有效减少污染气体的排放;
④含磷合成洗涤剂因为会引起水生植物的快速生长 引起水污染分析;
⑤集中处理时重金属离子能更加专业的转为重金属,电池中的重金属离子会带来污染;①温室效应主要是C02的大量排放,所以大量排放二氧化碳气体会加剧温室效应,故①正确;
②正常雨水的pH为5.6,是因为溶解了二氧化碳气体,故②错误;
③太阳能、风能和氢能替代化石燃料可以有效减少污染气体的排放,故③正确;
④含磷合成洗涤剂因为会引起水生富营养化,使植物快速生长 引起水体污染,故④错误;
⑤电池中的重金属离子会带来污染,为防止电池中的重金属离子污染土壤和水源,废电池要集中处理,故⑤正确;
综上所述:①③⑤正确
故选C.点评:
本题考点: 二氧化硫的污染及治理.
考点点评: 本题考查了环境的污染和原因,主要是温室效应、酸雨、清洁能源、含磷洗衣粉、电池等对环境的污染,掌握常识理解原因是关键.1年前查看全部
- (2010•江门一模)如图,P、Q分别是正方形ABCD的边AB、AD上一点,AP=AQ.
 (2010•江门一模)如图,P、Q分别是正方形ABCD的边AB、AD上一点,AP=AQ.
(2010•江门一模)如图,P、Q分别是正方形ABCD的边AB、AD上一点,AP=AQ.
(1)作Q关于直线BD的对称点R(不写作法,保留作图痕迹);
(2)连接DP、BR,证明BRDP是平行四边形. 成人影视1年前1
成人影视1年前1 -
 bzlz14 共回答了22个问题
bzlz14 共回答了22个问题 |采纳率95.5%解题思路:(1)根据正方形的性质可得有两种方法找到Q的对称点,①过Q作直线BD的垂线l,与BD相交于M.
(2)根据ABCD是正方形得出AB=CD且AB∥CD,再结合R在DC上,AP=AQ可得出BP=DQ=DR,继而可证得结论.(1)方法一:过Q作直线BD的垂线l,与BD相交于M,
在l上截MR=MQ;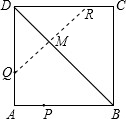
(2)∵ABCD是正方形,
∴AB=CD且AB∥CD,
依题意R在DC上,∵AP=AQ,
∴BP=DQ=DR,
∵BP∥DR,
∴BRDP是平行四边形.点评:
本题考点: 作图-轴对称变换;平行四边形的判定;正方形的性质.
考点点评: 本题考查轴对称作图及正方形的性质,难度不大,注意掌握对称轴垂直平分对称点连线.1年前查看全部
- (2012•江门一模)漂白粉是一种常用的消毒剂.
(2012•江门一模)漂白粉是一种常用的消毒剂.
(1)工业上生产漂白粉反应的化学方程式为:______,漂白粉的有效成分为______.
(2)某探究小组从市场上购买了一袋包装破损的漂白粉,对该漂白粉的成分进行探究.根据下列试剂,设计实验方案,完成实验报告(在答题卡上作答).
限选试剂:2mol•L-1NaOH溶液、2mol•L-1HCl溶液、2mol•L-1HNO3溶液、0.5mol•L-1BaCl2溶液、0.01mol•L-1AgNO3溶液、澄清石灰水、石蕊试液、酚酞试液、蒸馏水.
(3)探究小组为测定漂白粉中Ca(ClO)2的含量:称取漂白粉bg加水溶解后配制成100mL溶液,准确量取25.00mL于锥形瓶并加入足量盐酸和KI溶液,充分反应后,溶液中的游离碘用0.1000mol/L的Na2S2O3溶液滴定,滴定2次,平均消耗Na2S2O3溶液20.00ml.则该漂白粉中Ca(ClO)2的质量分数为实验步骤 预期现象与结论 步骤1:取适量漂白粉溶于足量蒸馏水,充分搅拌,静置,过滤,得沉淀和滤液. / 步骤2:向沉淀加入适量2mol•L-1HCl溶液,将产生的气体通入______ 现象:______
结论:______步骤3:取滤液分装A、B两支试管.向A试管,______ 现象:溶液先变红色,然后褪色.
结论:______步骤4:向B试管,______ 现象:产生白色沉淀.
结论:______[0.1000×20.00×143×100/4×1000×25.00b]×100%[0.1000×20.00×143×100/4×1000×25.00b]×100%.(只列算式,不做运算.已知:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,2Na2S2O3+I2=Na2S4O6+2NaI) windompan1年前1
windompan1年前1 -
 qinxy 共回答了21个问题
qinxy 共回答了21个问题 |采纳率76.2%解题思路:(1)工业上生产漂白粉是利用强化过和氯气反应生成氯化钙、次氯酸钙和水;漂白粉的有效成分为次氯酸钙;
(2)取适量漂白粉溶于足量蒸馏水,充分搅拌,静置,过滤,得沉淀和滤液,向沉淀加入适量2mol•L-1HCl溶液,将产生的气体通入氢氧化钙溶液,依据生成沉淀现象检验碳酸钙的存在;取滤液分装A、B两支试管.向A试管滴加2滴酚酞试液,溶液先变红色,然后褪色该漂白粉含有Ca(ClO)2 ,可能含有Ca(OH)2,向B试管,滴加过量2mol•L-1HNO3溶液和0.01mol•L-1AgNO3溶液,依据氯离子反应生成白色沉淀的现象分析氯化钙的存在;
(3)依据化学方程式分析计算的关系为Ca(ClO)2~2Cl2~2I2~4Na2S2O3,注意反应过程中溶液体积的变化,根据定量关系计算得到;(1)工业上生产漂白粉是利用强化过和氯气反应生成氯化钙、次氯酸钙和水,反应的化学方程式为,2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O,漂白粉的有效成分为次氯酸钙;
故答案为:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O; Ca(ClO)2;
(2)取适量漂白粉溶于足量蒸馏水,充分搅拌,静置,过滤,得沉淀和滤液,向沉淀加入适量2mol•L-1HCl溶液,将产生的气体通入氢氧化钙溶液,依据生成沉淀现象检验碳酸钙的存在;取滤液分装A、B两支试管.向A试管滴加2滴酚酞试液,溶液先变红色,然后褪色该漂白粉含有Ca(ClO)2 ,可能含有Ca(OH)2,向B试管,滴加过量2mol•L-1HNO3溶液和0.01mol•L-1AgNO3溶液,依据氯离子反应生成白色沉淀的现象分析氯化钙的存在;
故答案为:
实验步骤 预期现象与结论
适量澄清石灰水 现象:沉淀溶解,产生的气体使石灰水变浑浊(产生沉淀),或石灰水先产生白色沉淀,后沉淀溶解
结论:该漂白粉含有CaCO3
滴加2滴酚酞试液 结论:该漂白粉含有Ca(ClO)2,
可能含有Ca(OH)2
滴加过量2mol•L-1HNO3溶液和0.01mol•L-1AgNO3溶液 结论:该漂白粉含有CaCl2(3)依据化学方程式中的定量关系分析,Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,2Na2S2O3+I2=Na2S4O6+2NaI,得到计算定量关系为:
Ca(ClO)2~2Cl2~2I2~4Na2S2O3,
n[Ca(ClO)2]=[1/4]n(Na2S2O3)=[1/4]×20.0 mL×10-3 L•mL-1×0.1 000mol•L-1×[100ml/25ml],
Ca(ClO)2%=
1
4×20.0ml×10−3L/ml×0.1000mol/L×
100ml
25ml×143g/mol
bg×100%=[0.1000×20.00×143×100/4×1000×25.00b]×100%,
故答案为:[0.1000×20.00×143×100/4×1000×25.00b]×100%;点评:
本题考点: 探究物质的组成或测量物质的含量;氯、溴、碘及其化合物的综合应用.
考点点评: 本题考查了物质组成的实验分析判断,实验设计方法和反应现象的分析应用,滴定实验的有关定量分析计算,掌握基础是关键,题目难度中等.1年前查看全部
- (2014•江门模拟)如图所示,理想变压器原线圈接电压有效值不变的正弦交流电,副线圈接灯泡L1和L2,输电线的等效电阻为
 (2014•江门模拟)如图所示,理想变压器原线圈接电压有效值不变的正弦交流电,副线圈接灯泡L1和L2,输电线的等效电阻为R,开始时S断开.现接通S,以下说法正确的是( )
(2014•江门模拟)如图所示,理想变压器原线圈接电压有效值不变的正弦交流电,副线圈接灯泡L1和L2,输电线的等效电阻为R,开始时S断开.现接通S,以下说法正确的是( )
A.M、N两端输出电压U减小
B.等效电阻R的电压增大
C.灯泡L1的电流减小
D.电流表的示数减小 zxb921年前1
zxb921年前1 -
 商达 共回答了13个问题
商达 共回答了13个问题 |采纳率69.2%解题思路:本题类似于闭合电路中的动态分析问题,可以根据接通s后电路电路电阻的变化,确定出总电路的电阻的变化,进而可以确定总电路的电流的变化的情况,再根据电压不变,来分析其他的原件的电流和电压的变化的情况.A、理想变压器的输出电压是由输入电压和匝数比决定的,由于输入电压和匝数比不变,所以副线圈的输出的电压也不变,故A错误;
BC、当S接通后,两个灯泡并联,电路的电阻减小,副线圈的电流变大,所以通过电阻R的电流变大,电压变大,那么并联部分的电压减小,所以通过灯泡L1的电流减小,灯泡L1变暗,故BC正确;
D、当S接通后,两个灯泡并联,电路的电阻减小,副线圈的电流变大,所以原线圈的电流也变大,故D错误;
故选:BC.点评:
本题考点: 变压器的构造和原理;闭合电路的欧姆定律.
考点点评: 电路的动态变化的分析,总的原则就是由部分电路的变化确定总电路的变化的情况,再确定其他的电路的变化的情况,即先部分后整体再部分的方法.1年前查看全部
- (2008•江门模拟)某同学决定探究“生长素(IAA)对植物生长有何影响”.他选用了某植物的幼叶鞘作为实验材料,配制一系
(2008•江门模拟)某同学决定探究“生长素(IAA)对植物生长有何影响”.他选用了某植物的幼叶鞘作为实验材料,配制一系列不同浓度的IAA溶液进行实验.实验数据如表所示:

请回答下列问题:编号 1 2 3 4 5 6 LAA溶液浓度(mol•L-1) 0(蒸馏水) 10-12 10-10 10-8 10-6 10-4 幼叶鞘增长长度(min) 2.6 3.2 3.9 5.1 3.1 1.8
(1)实验中盛有不同浓度的小培养皿必须加盖,其原因是______.
(2)对该植物的幼叶鞘来说,最适的生长素浓度为______.
(3)假设各幼叶鞘的初始长度相等,请在坐标系绘出随IAA溶液浓度的变化幼叶鞘增长变化的曲线.
(4)分析上述实验数据得出的结论是______. yushang10141年前1
yushang10141年前1 -
 sea042181 共回答了19个问题
sea042181 共回答了19个问题 |采纳率100%解题思路:本题的实验目的是探究生长素浓度对植物生长的影响,实验的自变量是生长素的浓度,分析表格中的实验数据可知,在10-121mo1•L-l、10-10mo1•L-1、10-8mo1•L-l、10-6mo1•L-l几个浓度条件下都比空白对照组幼叶鞘增长长度大,其中10-8mo1•L-l的条件下幼叶鞘增长长度最多,这几个浓度条件下对幼叶鞘生长具有促进作用,在生长素为10-4mo1•L-l的条件下幼叶鞘增长长度小于空白对照组,该浓度抑制幼叶鞘生长.(1)由于水分蒸发会影响实验中的生长素的浓度,因此为避免水分蒸发引起溶液浓度变化,培养皿要进行加盖处理.
(2)分析表格中的数据可知,在实验控制的几个生长素浓度中10-8mo1•L-l的条件下幼叶鞘增长长度最多,因此对该植物的幼叶鞘来说,最适的生长素浓度为10-8mo1•L-l左右.
(3)分析表格中的数据可知,在10-121mo1•L-l、10-10mo1•L-1、10-8mo1•L-l、10-6mo1•L-l几个浓度条件下都比空白对照组幼叶鞘增长长度大,其中10-8mo1•L-l的条件下幼叶鞘增长长度最多,这几个浓度条件下对幼叶鞘生长具有促进作用,在生长素为10-4mo1•L-l的条件下幼叶鞘增长长度小于空白对照组,该浓度抑制幼叶鞘生长;描点做出曲线(起始位置和图线要正确)
(4)由表格中的数据得出的结论是:较低浓度范围内,随生长素浓度的增加,生长素对幼叶鞘生长的促进作用增强;继续提高生长素浓度,促进作用减弱,甚至起抑制作用(生长素对幼叶鞘生长的作用具有两重性.)
故答案应为:
(1)避免水分蒸发引起溶液浓度变化
(2)10-8mo1•L-l左右
(3)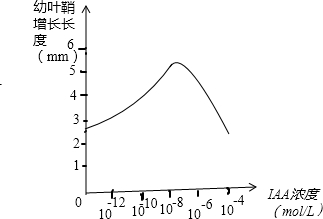
(4)较低浓度范围内,随生长素浓度的增加,生长素对幼叶鞘生长的促进作用增强;继续提高生长素浓度,促进作用减弱,甚至起抑制作用(生长素对幼叶鞘生长的作用具有两重性.)点评:
本题考点: 生长素的作用以及作用的两重性.
考点点评: 本题是对生长素作用两重性的考查,对实验室数据的分析、处理并获取结论的能力是本题考查的重点.1年前查看全部
- (2014•江门模拟)成语“蜀犬吠日”指的是:那里的狗不常见太阳,看到太阳后就觉得奇怪,就要叫.据此回答40~41题.
(2014•江门模拟)成语“蜀犬吠日”指的是:那里的狗不常见太阳,看到太阳后就觉得奇怪,就要叫.据此回答40~41题.
40.“蜀犬吠日”发生在( )
41.那里的狗为什么不常见太阳?( )
A.当地海拔高,难见太阳
B.当地群山环绕,多云雾
C.当地楼层过高,挡住阳光
D.当地常发生沙尘暴,挡住阳光 3r23j2qzjgte11年前1
3r23j2qzjgte11年前1 -
 天字无号 共回答了20个问题
天字无号 共回答了20个问题 |采纳率95%解题思路:依据成语的含义思考解答.四川盆地空气潮湿,四周群山环绕,天空多云雾,中间平原的水汽不易散开,那里的狗不常见太阳,看到太阳后就觉得奇怪,因此蜀中有“蜀犬吠日”之说.
故选:B.点评:
本题考点: 人民生活与地理环境的关系.
考点点评: 本题要知道成语的含义后理解解答即可.1年前查看全部
- (2013•江门一模)函数f(x)=lg(1-x)的定义域是( )
(2013•江门一模)函数f(x)=lg(1-x)的定义域是( )
A.(-∞,0)
B.(0,+∞)
C.(-∞,1)
D.(1,+∞) quying0457814621年前1
quying0457814621年前1 -
 纷飞蝶 共回答了26个问题
纷飞蝶 共回答了26个问题 |采纳率84.6%解题思路:通过解不等式1-x>0,求得函数的定义域.∵1-x>0⇒x<1
∴函数的定义域是(-∞,1).
故选C点评:
本题考点: 对数函数的定义域.
考点点评: 本题考查对数函数的定义域.1年前查看全部
- 描写家乡景物的句子-----江门
 nhn63101年前1
nhn63101年前1 -
 不小心过路人 共回答了17个问题
不小心过路人 共回答了17个问题 |采纳率70.6%东湖公园、东湖广场、五邑华侨广场、院士路、长堤风貌街、釜山公园、玉湖公园、体育公园、名人广场、冈州广场等,城市功能进一步完善,城市面貌日新月异.
到了江门,最不可不看的就是遍布在乡间、竹林间的碉楼.在成片开阔的绿色稻田里,弯曲的小河缓缓流过,密实挺拔的竹林中坐落着风格各异的碉楼,每一座碉楼的都有着一段动人的故事……寻迹碉楼,就像打开一幅幅侨乡画卷,走进一幕幕历史往事.
除了碉楼以外,江门山水园林比比皆是.最新评出的江门侨乡八景是:江门东湖公园的“东湖倩影”、新会天马村的“小鸟天堂”、新会圭峰山风景区的“圭峰叠翠”、台山上下川岛海滨旅游区的“川岛风情”、开平塘口镇的“立园春晓”、开平的“碉楼奇观”、恩平的“温泉仙境”、鹤山大雁山风景区的“雁影波光”等.1年前查看全部
- (2011•江门一模)设抛物线C:y2=4x的准线与对称轴相交于点P,过点P作抛物线C的切线,切线方程是______.
 luoyong961211年前1
luoyong961211年前1 -
 mwyiaetg 共回答了18个问题
mwyiaetg 共回答了18个问题 |采纳率94.4%解题思路:首先求出点P的坐标,求出抛物线在点P的导数,即得该点切线的斜率,用点斜式求得在点P的切线的方程.抛物线y2=4x的准线为x=-1,对称轴为x轴,故点P的坐标为(-1,0),
y'=±1
当切线的斜率为-1时,切线方程为 y-0=-(x+1),即x+y+1=0.
当切线的斜率为1时,切线方程为 y-0=1(x+1),即x-y+1=0.
故答案为x±y+1=0.点评:
本题考点: 抛物线的简单性质.
考点点评: 本题考查导数与切线斜率的关系,用点斜式求直线的方程,求出切线斜率是解题的关键.1年前查看全部
- (2014•江门模拟)根据原子结构示意简图的信息判断,下列说法错误的是( )
 (2014•江门模拟)根据原子结构示意简图的信息判断,下列说法错误的是( )
(2014•江门模拟)根据原子结构示意简图的信息判断,下列说法错误的是( )
A.该元素的质子数是17
B.该X=8原子核外有3个电子层
C.当x=8时,该微粒是阳离子
D.在化学变化中,该元素原子易得电子 过惯夜生活1年前1
过惯夜生活1年前1 -
 suifeng10 共回答了16个问题
suifeng10 共回答了16个问题 |采纳率87.5%解题思路:A、由结构示意图可知,圆圈内的数字表示质子数,则氯原子核内有17个质子;
B、根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可;
C、由结构示意图可知,当x=8时,核外电子数是18,核内质子数是17,带一个单位的负电荷,该微粒是阴离子;
D、根据原子中质子数等于核外电子数,由结构示意图可知,氯原子的最外层电子数为7,大于4个电子,在化学反应中易得电子,形成稳定结构.A、根据图的信息可知,氯原子的质子数是17,故说法正确;
B、根据元素周期表中的一格中获取的信息,可知该原子核外有3个电子层,故说法正确;
C、由结构示意图可知,当x=8时,核外电子数是18,核内质子数是17,带一个单位的负电荷,该微粒是阴离子,故说法错误;
D、根据原子中质子数等于核外电子数,由结构示意图可知,氯原子的最外层电子数为7,大于4个电子,在化学反应中易得电子,形成稳定结构,故说法正确.
故选:C.点评:
本题考点: 原子结构示意图与离子结构示意图.
考点点评: 理解和熟记原子结构示意图与离子结构示意图的其含义以及元素周期表提供的信息,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意,解答即可.1年前查看全部
- (2011•江门一模)1.18×104的倒数是( )
(2011•江门一模)1.18×104的倒数是( )
A.-3
B.[25/4]
C.≤2
D.<2 3362701061年前1
3362701061年前1 -
 天界的萝卜 共回答了18个问题
天界的萝卜 共回答了18个问题 |采纳率88.9%解题思路:先根据有理数的乘法法则计算出1.18×104的值,再根据倒数的定义进行解答即可.∵1.18×104=11800,
∴11800的倒数是[1/11800]<2.
故选D.点评:
本题考点: 倒数;科学记数法—原数.
考点点评: 本题考查的是有理数的乘方及倒数的定义,即乘积是1的两数互为倒数.1年前查看全部
- (2012•江门模拟)如图1所示是“探究导体在磁场中运动时产生感应电流的条件”实验 装置.铜棒油、电流表、开关
 (2012•江门模拟)如图1所示是“探究导体在磁场中运动时产生感应电流的条件”实验 装置.铜棒油、电流表、开关组成闭合电路.
(2012•江门模拟)如图1所示是“探究导体在磁场中运动时产生感应电流的条件”实验 装置.铜棒油、电流表、开关组成闭合电路.
(1)闭合开关后,要使电流表指针发生偏转,铜棒ab应向______运动,这是______种现象,利用这一原理可制成______.
(2)要使电流表指针偏转方向发生改变,可以釆取两种方法.
方法一:______;
方法二:______.
(3)某实验小组对手摇发电机非常感兴趣,他们想:发电机产生感应电流大小 跟哪些因素有关呢?于是他们开展了探究,以下是他们所用如图2的发电机和实验记录表:
根据表格可知,他们准备研究发电机产生感应电流的大小与______和______有关.实验序号 线圈转速 线圈转向 灯泡亮度 1 2 3  蓝焰黑冰1年前1
蓝焰黑冰1年前1 -
 sshe73 共回答了20个问题
sshe73 共回答了20个问题 |采纳率85%解题思路:解答此题需要知道以下几个知识点:
①什么是电磁感应现象?闭合电路的部分导体在磁场中做切割磁感线运动时,就会产生感应电流;
②产生感应电流的条件是什么?电路应该是闭合的,并且是部分导体,还要做切割磁感线运动;
③感应电流的方向和什么因素有关?感应电流的方向和两个因素有关,一个是导体的运动方向,一个是磁场方向,这两个因素中其中一个因素发生变化时,感应电流的方向就会发生变化;若两个因素都发生变化时,感应电流的方向不会发生变化;
④电磁感应现象有什么应用?我们生活中的发电机就是利用电磁感应现象的原理制成的.(1)要使电流表指针发生偏转,即要让闭合电路中产生感应电流,就要让铜棒ab做切割磁感线运动,水平向左、向右,或者斜向上、斜向下都可以切割到磁感线,这种现象就是电磁感应现象,利用它人们发明了发电机;
(2)图中的电流表可以比较出电流的方向,要使电流表指针偏转方向发生改变,也就是要改变感应电流的方向,可以从影响感应电流方向的两个因素(导体的运动方向和磁场方向)考虑,只改变其中一个因素时,感应电流的方向就会发生改变;
(3)根据表格可知,他们准备研究发电机产生感应电流的大小与线圈转速和线圈转向有关.
故答案为:(1)右(左、斜向上、斜向下); 电磁感应; 发电机
(2)改变铜棒运动方向; 改变磁场方向
(3)线圈转速;线圈转向点评:
本题考点: 产生感应电流的条件.
考点点评: 此题对于电磁感应现象的知识做了一个详细的考查,需要学生对于电磁感应现象有一个清晰的认识,是一道好题.1年前查看全部
- (2012•江门模拟)目前,“节能减排”已引起全球的关注.
 (2012•江门模拟)目前,“节能减排”已引起全球的关注.
(2012•江门模拟)目前,“节能减排”已引起全球的关注.
(1)目前***提倡“低碳生活”,实际上是为了节约能源和保护环境,并渐被人 们接受及付诸行动.下列说法中符合“低碳生活”理念cc.
a、为了卫生而使用一次性碗筷
b、为了方便而使用一次性塑料袋
c、上学时能骑单车就尽量不坐家里的汽车
d、多用洗衣机洗衣服,少用手洗
(2)如何减少能耗、提高汽车发动机的效率也越来越受到人们的重视.小明家 的汽车发动机为汽油发动机,它把汽油燃烧产生的内能部分转化为机械能,再通过传动机构将动力传给车轮使汽车行驶,如图甲是汽油机工作时的能流图,则括号内应填的是克服摩擦耗能克服摩擦耗能.小明从爸爸那里了解到他家的汽车在高速公路上每匀速行驶100km,平均耗油6kg,则汽车的效率为21.7%21.7%.(已知汽车受到的阻力为600n汽油的热值为4.6×107j/kg)
(3)小花家今年购买了一辆电动车,它通过蓄电池来提供电能,通过电动机得到动力,如图乙是电动车工作时的能流图,则括号内应填的是机械散热耗能机械散热耗能.电动车的电源采用的是48v的电压,如果使用12v的铅蓄电池,则应将44个铅蓄电池串串联. 康家四少1年前1
康家四少1年前1 -
 love_blue_wolf 共回答了17个问题
love_blue_wolf 共回答了17个问题 |采纳率100%(1)A、少用一次性木筷能减少森林的砍伐,防止废旧筷子对环境造成的污染,提倡使用一次性木筷是错误的说法,不符合“低碳生活”理念,;
B、提倡使用一次性塑料袋会间接消耗大量能源并产生污染物,不符合“低碳生活”理念;
C、骑自行车或步行上下班能减少交通工具的使用,减少石油化石的利用,从而减少二氧化碳的排放,符合“低碳生活”理念;
D、使用洗衣机洗衣服,既浪费电能,也多用水,不符合“低碳生活”理念.
(2)燃料燃烧放出的能量不可能全部转化为有用的机械能,而是大部分损失了:废气带走热量、机械散热耗能和克服摩擦耗能;
汽车发动机做的功为W=FS=fS=600N×105m=6×107J
汽油完全燃烧放出的热量为Q=qm=4.6×107J/kg×6kg=2.76×108J
汽车的效率为η=
W
Q=
6×107J
2.76×108J≈21.7%;
(3)电动车在行驶过程中,电能除转化成有用机械能和克服摩擦外,还有一部分以热的形式散失了;
电动车的电源采用的是48V的电压,所以需要将12V的蓄电池
48V
12V=4个串联使用.
故答案为:
(1)C;
(2)克服摩擦耗能;21.7%;
(3)机械散热耗能;4;串.1年前查看全部
- (2014•江门模拟)如图,矩形ABCD中,E是BC上一点,将矩形沿AE翻折后,点B恰好与CD边上的点F重合.已知AB=
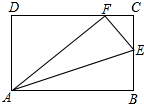 (2014•江门模拟)如图,矩形ABCD中,E是BC上一点,将矩形沿AE翻折后,点B恰好与CD边上的点F重合.已知AB=5,AD=3.
(2014•江门模拟)如图,矩形ABCD中,E是BC上一点,将矩形沿AE翻折后,点B恰好与CD边上的点F重合.已知AB=5,AD=3.
(1)求BE;
(2)求tan∠EAF. vcf3321年前1
vcf3321年前1 -
 gld17649 共回答了19个问题
gld17649 共回答了19个问题 |采纳率89.5%解题思路:(1)先根据勾股定理得到DF的长,在Rt△CEF中,CF=CD-DF=1,根据cos∠CFE=cos∠DAF,可得关于EF的方程,解得EF的长,即为BE的长;
(2)根据tan∠EAF=tan∠EAB,由正切的定义即可求解.(1)(方法一)依题意,AF=AB=5,DF=
AF2−AD2=4,
在Rt△CEF中,CF=CD-DF=1,∠CFE=∠DAF=90°-∠AFD,cos∠CFE=cos∠DAF,
所以[CF/EF=
AD
AF]
解得EF=
CF×AF
AD=
5
3,所以BE=EF=
5
3…(7分)
(方法二)依题意,AF=AB=5,DF=
AF2−AD2=4
设BE=x,
在Rt△CEF中,CF=CD-DF=1,EF=BE=x,CE=3-x
x2=12+(3-x)2,
解得BE=x=
5
3;
(2)tan∠EAF=tan∠EAB=[BE/AB=
1
3].点评:
本题考点: 翻折变换(折叠问题).
考点点评: 此题考查了折叠的性质、矩形的性质以及三角函数等知识.此题难度适中,注意掌握折叠前后图形的对应关系,注意数形结合思想与转化思想的应用.1年前查看全部
- 七年级上册英语书哪里买啊本人在江门,
 两地儿1年前1
两地儿1年前1 -
 fxy107 共回答了14个问题
fxy107 共回答了14个问题 |采纳率85.7%如果没得买就去http://www.***.com.cn/ce/czyy/qnjs/czyy/200703/t20070315_345290.htm
复印1年前查看全部
- 写景日出日落作文(好词佳句,好开头结尾)--江门白沙祠说明文---高分酬谢!
写景日出日落作文(好词佳句,好开头结尾)--江门白沙祠说明文---高分酬谢!
写景日出日落作文(好词佳句,好开头结尾)
还有--江门白沙祠说明文
---高分酬谢! 小行者1年前4
小行者1年前4 -
 370223584 共回答了15个问题
370223584 共回答了15个问题 |采纳率86.7%好词:
太阳 朝阳 曦阳 骄阳 金阳 酷阳 残阳 斜阳 红日 朝日 烈日 炎日 赤日 春日 夏日 秋日 冬日 落日 日食 日晕 日影 日轮 日夕 火轮 金轮 红轮 阳光 阳婆 晨曦 霞光 朝晖 夕晖 春晖 夕阳 余晖 斜晖 艳阳 落阳 残照 火伞 日头 红轮 火轮 金轮 金乌 落日 阳光 灿烂 夺目 耀眼 灼热 酷热 酷日 日头 日阳 日出 日落 火热 炽热 炎热 光芒 光辉 火球 金黄 鲜红 火红 微红 浅红 朱红 紫红 赭红 殷红 绯红 旭日
红艳艳 金灿灿 热烘烘 暖洋洋
明晃晃 红彤彤
红日欲出 红日未出 红日初升 红日喷薄 红日艳艳 旭日初露 旭日初升 旭日东升 旭日临窗 旭日将升 旭日当空 晓日初升 朝阳初升 朝阳灿灿 朝阳普照 朝阳火红 太阳升高 太阳高起 日出旭旭
日出东山 日出三竿 日上三竿 日高三丈 三竿日出 日色东升 日头露脸 火轮升腾 火球高升 为乌飞升 一轮红日 一轮朝日
一轮旭日 喷薄欲出 喷薄而出 徐徐上升 红日高悬 红日高照 红日当空 赤日当空 赤日当天 赤日炎炎 赤日烫人 丽日当空
丽日高照 烈日当空 烈日当头 烈日炎炎 烈日灼烈 烈日灼人 日头正顶 日已中天 日头正毒 日轮当午 日当正午 日悬高天
日悬中天 日正中天 日色过午 日头炽热 明日高挂 太阳高照 太阳毒辣 骄阳满天
太阳当空 艳阳当空 艳阳骄骄 艳阳高照
艳阳普照 春阳灿灿 秋阳明丽 秋阳明媚 秋阳高照 高悬天空 太阳偏午 雨后晴阳 太阳平西 太阳西斜 太阳偏西 太阳西沉
太阳西坠 太阳入山 太阳落山 太阳西下
太阳落坡 夕阳正美 夕阳如血 夕阳如丹 夕阳如火 太阳嫣红 夕阳欲坠 夕阳将坠
夕阳将落 夕阳西坠 夕阳西照 夕阳将沉 夕阳斜照 夕阳映照 夕阳残照 夕阳晚照 夕阳西落 夕阳西下 夕阳西沉 夕阳入山
夕阳余辉 残阳似血 残阳如血 残阳夕照
残阳消尽 斜阳淡照 斜阳落山 红日平西
红日西斜 红日西坠 红日西沉 日近黄昏
日头西落 日头偏西 日影西斜 日傍西山
日头西斜 日头压山 日头西沉 日头西坠
日薄西山 日落西山 日头刚落 日落西天
日出日落 金乌西坠 落日熔金 落日余晖
西山日落 一轮斜日 一抹夕阳 一缕夕阳
徐徐降落 阳光初照 阳光抚照 阳光普照
阳光和煦 阳光明媚 阳光明丽 阳光灿烂
波光粼粼 阳光耀阳 阳光艳丽 阳光正烈
阳光很足 阳光炽热 阳光暴热 阳光炫耀
阳光西斜 阳光暗淡 阳光直射 日光斜射
朝晖灿烂 灿烂朝晖 灿烂光辉 朝晖满地
金色阳光 金光耀目 金光万道 金光万丈
光芒四射 光芒万丈 万道金光 霞光万道
晚霞夕照 艳艳阳光 放射光芒 金辉斜照
余辉灿灿 令人目眩 色彩斑斓 一缕阳光
一团红光 一丝亮光 金盘滚动
好句:
满天红云,满海金波,红日像一炉沸腾的钢水,喷薄而出,金光耀眼.
早晨,太阳像个刚出门的新媳妇,羞答答地露出半个脸来.
太阳落山了,它那分外的强光从树梢头喷射出来,将白云染成血色,将青山染成血色.
太阳慢慢地透过云霞,露出了早已胀得通红的脸庞,像一个害羞的小姑娘张望着大地.
灿烂的阳光穿过树叶间的空隙,透过早雾,一缕缕地洒满了校园.
太阳更低了,血一般的红,水面上一条耀人眼睛的广阔的光波,从海洋的边际直伸到小船边沿.
天空被夕阳染成了血红色,桃红色的云彩倒映在流水上,整个江面变成了紫色,天边仿佛燃起大火.
春天,那太阳暖洋洋的,它伸出漫暖的大手,摩挲得人浑身舒坦.
阵阵春风,吹散云雾,太阳欣然露出笑脸,把温暖和光辉洒满湖面.
炎炎的烈日高悬当空,红色的光如火箭般射到地面上,地面着了火,反射出油在沸煎时的火焰来.
没有敢抬头看一眼太阳,只觉得到处都耀眼,空中、屋顶、地上,都是白亮亮的一片,白里透着点红,由上到下整个像一面极大的火镜,每条都是火镜的焦点,仿佛一切东西就要燃烧起来.
晚秋了,太阳懒洋洋地挂在天上,像个老公公露着笑脸在打瞌睡.
深秋的太阳像被罩上橘红色灯罩,放射出柔和的光线,照得身上、脸上,暖烘烘的.
太阳一到秋天,就将它的光芒全撒向人间.瞧,田野是金黄的,场地是金黄的,群山也是金黄的.
冬天的太阳像月亮一样苍白无力.
太阳正被薄云缠绕着,放出淡淡的耀眼的白光.
太阳一年操劳到头,忙到冬天,就筋疲力尽,几乎放不出热力来了.
和煦的阳光,透过稠密的树叶洒落下来,成了点点金色的光斑.
远处巍峨的群山,在阳光照映下,披上了金黄色的外衣,显得格外美丽.
阳光被层层叠叠的树叶过滤,漏到他身上变成了淡淡的圆圆的轻轻摇曳的光晕.
这时候正是早上八九点钟,明亮的阳光在树叶上涂了一圈又一圈金色银色的光环.
阳光透过淡薄的云层,照耀着白茫茫的大地,反射出银色的光芒,耀得人眼睛发花.
金灿灿的阳光倾泻下来,注进万顷碧波,使单调而平静的海面而变得有些色彩了.
红艳艳的太阳光在山尖上时,雾气像幕布一样拉开了,城市渐渐地显现在金色的阳光里.
那刺穿云块的阳光就像根根金线,纵横交错,把浅灰、蓝灰的云朵缝缀成一幅美丽无比的图案.
太阳刚刚升上山头,被鲜红的朝霞掩映着,阳光从云缝里照射下来,像无数条巨龙喷吐着金色的瀑布.
金色的阳光透过缝隙,洒在褐色土地滋生的小草上.
天空一碧如洗,灿烂的阳光正从密密的松针的缝隙间射下来,形成一束束粗粗细细的光柱,把飘荡着轻纱般薄雾的林荫照得通亮.
太阳泛起火红的笑脸,使朦胧的校园豁然揭去纱帐.
天际出现了一抹紫红色的朝晖,像绽开的红玫瑰.
刚刚起身的太阳呵,精神抖擞,红光四溢,把整个世界照得通亮.
火红的旭日刚刚透出海平面,给美丽恬静的大海抹上一层玫瑰色.
朝阳把它的光芒射向湖面,微风乍起,细浪跳跃,搅起满湖碎金.
忽然,迎面升起一轮红日,洒下的道道金光,就像条条金鞭,驱赶着飞云流雾.
海面上跃出一轮红日,鲜艳夺目,海空顿时洒满了金辉,海面由墨蓝一变而为湛蓝.
金灿灿的朝晖,渐渐染红了东方的天际,高高的黄山主峰被灿烂的云霞染成一片绯红.
太阳在朝霞的迎接中,露出了红彤彤的面庞,霎时,万道金光透过树梢给水面染上了一层胭脂红.1年前查看全部
- (2014•江门一模)设函数f(x)=x+sinx-2,g(x)=ex+lnx-2,若实数a,b满足f(a)=0,g(b
(2014•江门一模)设函数f(x)=x+sinx-2,g(x)=ex+lnx-2,若实数a,b满足f(a)=0,g(b)=0,则( )
A.g(a)<0<f(b)
B.f(b)<0<g(a)
C.0<g(a)<f(b)
D.f(b)<g(a)<0 dennislee1年前1
dennislee1年前1 -
 狐狸仔 共回答了18个问题
狐狸仔 共回答了18个问题 |采纳率94.4%解题思路:先判断函数f(x),g(x)在R上的单调性,再利用f(a)=0,g(b)=0判断a,b的取值范围,即可得到正确答案.∵函数f(x)=x+sinx-2的导数f′(x)=1+cosx≥0,∴函数f(x)在R上是增函数.
再由f(1)=1+sin1-2<0,f(2)=sin2>0,f(a)=0,
∴1<a<2.
∵g(x)=ex+lnx-2在(0,+∞)上是增函数,g([1/e])=e
1
e-3<0,g(1)=e-2>0,g(b)=0,
∴[1/e]<b<1.
∴f(b)<0,且 g(a)>0,
故选:B.点评:
本题考点: 函数的零点与方程根的关系.
考点点评: 本题考查了函数的性质,熟练掌握函数的单调性、函数零点的判定定理是解题的关键,体现了转化的数学思想,属于中档题.1年前查看全部
- (2012•江门模拟)某商场销售一批进价为16元的日用品,为了获得更多利润,商场需要确定适当的销售价格.调查发现:若按每
(2012•江门模拟)某商场销售一批进价为16元的日用品,为了获得更多利润,商场需要确定适当的销售价格.调查发现:若按每件20元销售,每月能卖出360件;若按每件25元销售,每月能卖出210件.假定每月销售量y(件)是销售价格x(元/件)的一次函数.
(1)试求y与x之间的函数关系式;
(2)销售价格定为多少时,商场每月获得的利润最大?每月的最大利润是多少? 的事1年前1
的事1年前1 -
 紫竹林里 共回答了22个问题
紫竹林里 共回答了22个问题 |采纳率90.9%解题思路:(1)根据每月销售量y(件)是销售价格x(元/件)的一次函数,设y=kx+b,将x=20,y=360,x=25,y=210,代入求y与x之间的函数关系式;
(2)设商场每月获利w元,根据w=每月销售量y×每件利润,列出函数关系式,根据二次函数的性质求解.(1)依题意,设y=kx+b,
则
20k+b=360
25k+b=210,
解得
k=−30
b=960.
所以y=-30x+960,16≤x≤32(不写x的取值范围不扣分);
(2)商场每月获利w=(-30x+960)(x-16)=-30x2+1440x-15360=-30(x-24)2+1920,
所以,当x=24时,w有最大值,最大值是1920元.
答:销售价格定为24元时,商场每月获得的利润最大,每月的最大利润是1920元.点评:
本题考点: 二次函数的应用.
考点点评: 本题考查了二次函数的运用.关键是根据题意列出一次函数、二次函数的关系式,根据二次函数顶点式求最大值.1年前查看全部
- (2013•江门一模)已知函数f(x)=ax2-bx-1,其中a∈(0,2],b∈(0,2],在其取值范围内任取实数a、
(2013•江门一模)已知函数f(x)=ax2-bx-1,其中a∈(0,2],b∈(0,2],在其取值范围内任取实数a、b,则函数f(x)在区间[1,+∞)上为增函数的概率为( )
A.[1/2]
B.[1/3]
C.[2/3]
D.[3/4] 逍遥笑A1年前0
逍遥笑A1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2010•江门二模)小明家有一只标有“36V 36W”的灯泡,小明想用一个电阻将它改装成能在家庭电路中正常工
(2010•江门二模)小明家有一只标有“36V 36W”的灯泡,小明想用一个电阻将它改装成能在家庭电路中正常工作的台灯(不考虑灯泡电阻随温度而变化).请你帮助小明完成:
(1)画出设计电路图.
(2)计算出这个电阻的阻值.
(3)这个电路在正常工作时消耗的总功率.
(4)你改装的台灯还有什么缺陷. hehetong1年前0
hehetong1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2009•江门一模)“神舟七号”所用动力燃料之一为氢化铿三兄弟LiH,LiD,LiTo有关下列叙述中正确的是( )
(2009•江门一模)“神舟七号”所用动力燃料之一为氢化铿三兄弟LiH,LiD,LiTo有关下列叙述中正确的是( )
A.三种物质质子数之比为1:2:3
B.三种物质中子数之比为1:1:1
C.三种物质的摩尔质量之比为8:9:10
D.三种物质的化学性质不相同 周明锋1年前1
周明锋1年前1 -
 baby0001 共回答了23个问题
baby0001 共回答了23个问题 |采纳率91.3%解题思路:Li的质子数为3,H、D、T的质子数都是1,质量数=质子数+中子数,质量数之比等于摩尔质量之比,利用组成和结构来分析物质的化学性质.A、质子数之比为(3+1):(3+1):(3+1)=1:1:1,故A错误;
B、中子数之比为(4+0):(4+1):(4+2)=4:5:6,故B错误;
C、摩尔质量之比为(7+1):(7+2):(7+3)=8:9:10,故C正确;
D、LiH、LiD、LiT的组成元素相同,结构相同,则三种物质的化学性质相同,故D错误;
故选C.点评:
本题考点: 质量数与质子数、中子数之间的相互关系.
考点点评: 本题考查原子的构成、物质的组成及原子中的数量关系,较简单,选项C、D都是学生解答中的易错点.1年前查看全部
- (2014•江门模拟)已知函数f(x)=log2x的定义域为M,N={x|x2-x-2=0},则M∩N=( )
(2014•江门模拟)已知函数f(x)=log2x的定义域为M,N={x|x2-x-2=0},则M∩N=( )
A.{-1,2}
B.{-2,1}
C.{1}
D.{2} 雨夜私语1年前1
雨夜私语1年前1 -
 abc1966容 共回答了32个问题
abc1966容 共回答了32个问题 |采纳率93.8%解题思路:求出函数f(x)=log2x的定义域,确定出M,求出N中方程的解确定出N,找出两集合的交集即可.由函数f(x)=log2x,
得到x≥0,即M=[0,+∞);
由集合N中的方程变形得:(x-2)(x+1)=0,
解得:x=2或x=-1,
即N={-1,2},
则M∩N={2}.
故选D点评:
本题考点: 交集及其运算.
考点点评: 此题考查了交集及其运算,熟练掌握交集的定义是解本题的关键.1年前查看全部
- 求大神赐教听懂纯正发音英语的方法和听出问题的重点【是高中水平的哈】 求江门练习英语听力的网站哈 是比较正统和标准的 谢谢
求大神赐教听懂纯正发音英语的方法和听出问题的重点【是高中水平的哈】 求江门练习英语听力的网站哈 是比较正统和标准的 谢谢哈
 yw_sdk1年前1
yw_sdk1年前1 -
 sam11891 共回答了15个问题
sam11891 共回答了15个问题 |采纳率100%要是为了考试就练听力题吧,掌握做题方法套路,7天速效.
要是为了真正学好英语,请听englishpod,坚持至少一年.
听力考试真正听懂了应该一分不扣,懂就是懂,只要扣一分就是没听懂,无所谓重点和理解.你听外国人考汉语的听力试试,绝对一分不扣.1年前查看全部
- (2009•江门二模)一群氢原子处于n=4的激发态,当它们自发地跃迁到较低的能级时,下列判断错误的是( )
(2009•江门二模)一群氢原子处于n=4的激发态,当它们自发地跃迁到较低的能级时,下列判断错误的是( )
A.可能辐射出六种不同频率的光子
B.从n=4的能级直接跃迁到n=1的能级时释放出的光子频率最低
C.从n=4的能级跃迁到n=3的能级时释放出的光子频率最低
D.从n=2的能级跃迁到n=1的能级时,释放出的光子波长最长 nature701年前1
nature701年前1 -
 泡沫鱼 共回答了19个问题
泡沫鱼 共回答了19个问题 |采纳率89.5%解题思路:氢原子能级间跃迁时辐射的光子能量等于两能级间的能级差,能级差越大,则辐射的光子频率越大,波长越小.A、根据数学组合公式
C24=6知,可能放出6种不同频率的光子.故A正确.
B、由n=4跃迁到n=1能级辐射的光子能量最大,频率最大.故B错误.
C、从n=4跃迁到n=3能级辐射的光子能量最小,频率最低,波长最长.故C正确,D错误.
本题选错误的,故选BD.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 解决本题的关键掌握能级间跃迁所遵循的规律,即Em−En=hv=hcλ.1年前查看全部
- (2010.江门模拟)如图为人体细胞的分裂、分化、衰老和凋亡过程的示意图,图中①~⑥为各个时期的细胞,c表示细胞所进行的
(2010.江门模拟)
如图为人体细胞的分裂、分化、衰老和凋亡过程的示意图,
图中①~⑥为各个时期的细胞,
c表示细胞所进行的生理过程,据图,下列正确的是
其中的C项是这样叙述的:
C.若⑤⑥已失去分裂能力,则其细胞内遗传信息的流动方向为
DNA → RNA → 蛋白质.

 一生简约1年前1
一生简约1年前1 -
 秋日骄阳2002 共回答了16个问题
秋日骄阳2002 共回答了16个问题 |采纳率100%失去了分裂能力,就没有了遗传信息流动了1年前查看全部
- (2009•江门二模)照明电路中,为了安全,一般在电能表后面电路上安接一漏电保护器,如图所示,当漏电保护器的ef两端没有
 (2009•江门二模)照明电路中,为了安全,一般在电能表后面电路上安接一漏电保护器,如图所示,当漏电保护器的ef两端没有电压时,脱扣开关K能始终保持接通,当ef两端有电压时,脱扣开关K立即断开,下列说法正确的是( )
(2009•江门二模)照明电路中,为了安全,一般在电能表后面电路上安接一漏电保护器,如图所示,当漏电保护器的ef两端没有电压时,脱扣开关K能始终保持接通,当ef两端有电压时,脱扣开关K立即断开,下列说法正确的是( )
A.连接火线的线圈匝数和连接零线的线圈匝数相等
B.当输入电压过低或用户电流超过一定值时,脱扣开关会自动断开,即有低压或过流保护作用
C.当站在绝缘物上的带电工作的人两手分别触到b线和d线时(双线触电)脱扣开关会自动断开,即有触电保护作用
D.“脱扣开关控制器”的线圈匝数越多,触电保护越灵敏 pollyanna5251年前1
pollyanna5251年前1 -
 基督耶稣最后nn 共回答了18个问题
基督耶稣最后nn 共回答了18个问题 |采纳率88.9%解题思路:脱扣开关K保持接通时,ef中要没有电压,保护器中火线和零线中电流产生的磁场应完全抵消,可知火线的线圈匝数和连接零线的线圈匝数应相等.只有通过火线与零线的电流有差值时,ef两端才有电压,脱扣开关K才断开.“脱扣开关控制器”的线圈匝数越多,同样的电流差值,产生的感应电动势越大,ef两端的电压越大,触电保护越灵敏.A、正常状态时,脱扣开关K保持接通,ef中要没有电压,火线和零线中电流产生的磁场应完全抵消,必须使火线的线圈匝数和连接零线的线圈匝数相等.故A正确.
B、当输入电压过低或用户电流超过一定值时,通过火线与零线的电流没有差值,不会使ef中产生感应电动势,脱扣开关不会断开.故B错误.
C、当站在绝缘物上的带电工作的人两手分别触到b线和d线时(双线触电),流过火线与零线的电流相等,保护器中火线和零线中电流产生的磁场应完全抵消,不会使ef中产生感应电动势,脱扣开关不会断开.故C错误.
D、“脱扣开关控制器”的线圈匝数越多,同样的电流差值,产生的感应电动势越大,ef两端的电压越大,触电保护越灵敏.故D正确.
故选AD点评:
本题考点: 闭合电路的欧姆定律;常见传感器的工作原理.
考点点评: 本题中火线与零线中电流相等时,磁场完全抵消,是双线并绕消除自感影响的原理.1年前查看全部
- (2009•江门二模)演示位移传感器的工作原理如图甲所示,物体M在导轨上平移时,带动滑动变阻器的金属杆P在均匀电阻丝上滑
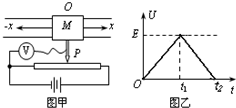 (2009•江门二模)演示位移传感器的工作原理如图甲所示,物体M在导轨上平移时,带动滑动变阻器的金属杆P在均匀电阻丝上滑动,通过理想电压表显示的数据来反映物体的位移x.设定电源电动势为E,内阻不计,若电压表的示数U随时间t的变化关系如图乙所示,则下列说法正确的是( )
(2009•江门二模)演示位移传感器的工作原理如图甲所示,物体M在导轨上平移时,带动滑动变阻器的金属杆P在均匀电阻丝上滑动,通过理想电压表显示的数据来反映物体的位移x.设定电源电动势为E,内阻不计,若电压表的示数U随时间t的变化关系如图乙所示,则下列说法正确的是( )
A.t1时刻P在最右端
B.0--t1时间内物体M向右做匀速运动
C.0--t1时间内物体M向右做匀加速运动
D.t1--t2时间内物体M向左做匀减速运动 填心1年前1
填心1年前1 -
 hujixi 共回答了30个问题
hujixi 共回答了30个问题 |采纳率83.3%解题思路:本题中理想电压表对电路没有影响,电压表测量变阻器左侧的电压.根据电压表的读数,分析滑片P的位置.根据欧姆定律和电阻定律得到电压表读数与物体位移x的关系式,再分析物体的运动情况.A、电压表测量变阻器左侧的电压.t1时刻U=0,则说明P在最左端.故A错误.
B、C设物体的位移为x时,电压表的读数为U,变阻器的总长为L,总电阻为R,则根据欧姆定律和电阻定律得
U=
x
LE,
由图知,0-t1时间内U=kt,k是比例系数,则得x=
kL
Et,x与t成正比,说明物体M向右做匀速运动.故B正确,C错误.
D、同理可知,t1--t2时间内物体M向左做匀速运动.故D错误.
故选B点评:
本题考点: 闭合电路的欧姆定律.
考点点评: 本题是力电综合题,抓住它们之间的联系.本题通过位移将力电联系起来,这是解决本题的关键.1年前查看全部
- (2014•江门模拟)用作牙膏摩擦剂的轻质碳酸钙可以石灰石来制备,工业上主要生产流程如图,请回答:
(2014•江门模拟)用作牙膏摩擦剂的轻质碳酸钙可以石灰石来制备,工业上主要生产流程如图,请回答:

(1)写出下列物质或主要成分的化学式:生石灰______,石灰乳______.
(2)“煅烧炉”中发生反应的化学方程式是:CaCO3
CaO+CO2↑高温 .CaCO3.
CaO+CO2↑高温 .
在“反应池”中主要发生反应的化学方程式是:______.
(3)从反应池中分离出轻质碳酸钙的方法是______.
(4)有人建议在上述流程中用煅烧炉排出的CO2气体替代“碳酸钠溶液”,这样做的优点是:
______.(任写1点) alangrant1年前1
alangrant1年前1 -
 homleelay 共回答了29个问题
homleelay 共回答了29个问题 |采纳率86.2%解题思路:(1)石灰乳中的溶质是氢氧化钙,生石灰是氧化钙的俗称,以及化学式的书写规则进行解答;
(2)碳酸钙高温煅烧生成氧化钙和二氧化碳和二氧化碳和氢氧化钙反应生成氢氧化钙沉淀和水,碳酸钠与氢氧化钙发生反应生成碳酸钙沉淀和氢氧化钠.根据书写化学方程式的步骤:写、配、注、等,正确书写化学方程式即可;
(3)过滤是将不溶于液体的固体分离出来的一种方法;
(4)用二氧化碳代替碳酸钠溶液,可达到降低生产成本和节能减排.(1)生石灰的化学式为:CaO;石灰乳的溶质是氢氧化钙,其化学式为:Ca(OH)2
故答案是:CaO;Ca(OH)2;
(2)煅烧炉中的反应是:石灰石经高温煅烧生成生石灰和二氧化碳,反应的化学方程式为:CaCO3
高温
.
CaO+CO2↑;
反应池中的反应是:碳酸钠与氢氧化钙发生反应,生成碳酸钙沉淀和氢氧化钠,其反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
故答案是:CaCO3
高温
.
CaO+CO2↑;Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)过滤是把不溶于溶液的固体和液体分开的一种分离混合物的方法,“反应池”中的混合物分离出生成的碳酸钙固体,可用过滤的方法;
故答案是:过滤;
(4)用二氧化碳代替碳酸钠溶液,可达到降低生产成本和节能减排.
故答案是:原料利用率高,降低生产成本,减少温室气体CO2排放.(答任一点即可,合理即给分).点评:
本题考点: 碳酸钙、生石灰、熟石灰之间的转化;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查了化学方程式的书写以及悬浊液的定义及过滤的方法,考查较为全面.1年前查看全部
- (2012•江门模拟)如图甲所示为某小组设计的模拟调光灯电路,选用的电源电压恒为6V,灯泡上标有“3.8V &
 (2012•江门模拟)如图甲所示为某小组设计的模拟调光灯电路,选用的电源电压恒为6V,灯泡上标有“3.8V1.52W”字样,变阻器上标有“20Ω1A”字样.
(2012•江门模拟)如图甲所示为某小组设计的模拟调光灯电路,选用的电源电压恒为6V,灯泡上标有“3.8V1.52W”字样,变阻器上标有“20Ω1A”字样.
(1)求灯泡正常发光1min消耗的电能;
(2)求灯泡正常发光时变阻器消耗的电功率;
(3)小明在调节灯泡的亮度时,发现灯泡有时会变得很亮甚至烧坏.为了避免出现上述情况,于是他在电路中串联了一个电阻R0,电路如图乙所示.R0的阻值多大比较合适? shuiniu1年前1
shuiniu1年前1 -
 zhaimei 共回答了19个问题
zhaimei 共回答了19个问题 |采纳率100%解题思路:(1)知道灯泡的额定功率和灯泡正常工作的时间,可利用公式W=Pt计算出灯泡消耗的电能.
(2)从甲图可知,灯泡L与滑动变阻器串联,知道灯泡L的额定电压和额定功率,可利用公式I=
计算出灯泡正常发光时电路中的电流,又知道电源电压,可利用串联电路电压的特点计算出滑动变阻器两端的电压,最后再利用公式P=UI计算出变阻器消耗的电功率.PL UL
(3)小灯泡的额定电压为3.8V,若滑动变阻器的阻值过小,很可能使小灯泡烧坏,所以要串联电阻来保护电路.即不能使灯泡由于滑动变阻器的阻值过小而烧坏,又要使灯泡能正常发光,所以乙图中,当滑动变阻器阻值为0时,电路中的电流为0.4A,小灯泡两端的电压为3.8V为宜.知道电源电压,可利用串联电路电压的特点计算出电阻R0两端的电压,再利用公式R=[U/I]计算出电阻R0的阻值.(1)∵PL=1.52W,t=1min=60s,
∴灯泡正常发光1min消耗的电能为:W=PLt=1.52W×60s=91.2J.
(2)∵UL=3.8v,
∴灯泡正常发光时电路中的电流为:I=
PL
UL=[1.52W/3.8V]=0.4A,
而电源电压恒为U=6V,
∴滑动变阻器两端的电压为:U变阻器=U-UL=6V-3.8V=2.2V,
则变阻器消耗的电功率为:P变阻器=U变阻器I=2.2V×0.4A=0.88W.
(3)要起保护作用,即不能使灯泡由于滑动变阻器的阻值过小而烧坏,又要使灯泡能正常发光,所以乙图中,当滑动变阻器阻值为0时,电路中的电流为0.4A,小灯泡两端的电压为3.8V为宜.
∴电阻R0两端的电压为:U0=U-UL=6V-3.8V=2.2V,
电阻R0的阻值为:R0=
U0
I=[2.2V/0.4A]=5.5Ω.
答:(1)灯泡正常发光1min消耗的电能为91.2J.
(2)灯泡正常发光时变阻器消耗的电功率为0.88W.
(3)电阻R0的阻值为5.5Ω时比较合适.点评:
本题考点: 电功的计算;串联电路的电流规律;串联电路的电压规律;欧姆定律的应用;电功率的计算.
考点点评: 此题主要考查了有关欧姆定律的应用及有关电功率的计算.解决此类题目的关键是注意用电器的规格型号,能够从规格中获取有用的信息.如额定电压、额定功率、额定电流值.1年前查看全部
- (2014•江门模拟)log32______log23(填“>”或“<”).
 情已皈依1年前1
情已皈依1年前1 -
 3l9kp3d9 共回答了13个问题
3l9kp3d9 共回答了13个问题 |采纳率84.6%由于log32<log33=1,log23>log22=1,
故有log32<log23,
故答案为<.1年前查看全部
- (2013•江门二模)命题“∃x0∈R,ex0≤0”的否定是∀x∈R,ex0>0∀x∈R,ex0>0.
 wwsx1年前1
wwsx1年前1 -
 tt报检员 共回答了15个问题
tt报检员 共回答了15个问题 |采纳率100%解题思路:根据命题“∃x0∈R,ex0≤0”是特称命题,其否定为全称命题,将“存在”改为“任意”,“≤“改为“>”即可得答案.∵命题“∃x0∈R,ex0≤0”是特称命题
∴命题的否定为:∀x∈R,ex0>0.
故答案为:∀x∈R,ex0>0.点评:
本题考点: 特称命题;命题的否定.
考点点评: 这类问题的常见错误是没有把全称量词改为存在量词,或者对于“>”的否定用“<”了.这里就有注意量词的否定形式.如“都是”的否定是“不都是”,而不是“都不是”.特称命题的否定是全称命题,“存在”对应“任意”.属基础题.1年前查看全部
- (2012•江门一模)聚乳酸是光和微生物双降解性高分子,有如下转化关系:
(2012•江门一模)聚乳酸是光和微生物双降解性高分子,有如下转化关系:

试回答下列问题:
(1)A中官能团的名称:羟基、羧基羟基、羧基.
(2)写出A的2种同分异构体:HOCH2CH2COOHHOCH2CH2COOH,HCOOCH2CH2OHHCOOCH2CH2OH.
(3)①的反应类型是取代反应取代反应,⑤的反应类型是消去反应消去反应.
(4)写出有关反应化学方程式③
 ,
,
④
 .
.
(5)请提出一种利用废弃的聚乳酸塑料的设想:回收塑料,在催化剂(光和微生物)作用下,降解为乳酸,用乳酸重新制塑料回收塑料,在催化剂(光和微生物)作用下,降解为乳酸,用乳酸重新制塑料. 637421471年前1
637421471年前1 -
 raulsheep 共回答了26个问题
raulsheep 共回答了26个问题 |采纳率84.6%(1)根据反应③,可以推断A为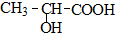 ,含有的官能团为羟基、羧基,
,含有的官能团为羟基、羧基,
故答案为:羟基、羧基;
(2)A的结构简式为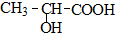 ,满足与A具有相同的分子式,本题的结构的有机物有:HOCH2CH2COOH,HCOOCH2CH2OH,HOCH2COOCH3,HOCH2COCH2OH,
,满足与A具有相同的分子式,本题的结构的有机物有:HOCH2CH2COOH,HCOOCH2CH2OH,HOCH2COOCH3,HOCH2COCH2OH,
故答案为:HOCH2CH2COOH,HCOOCH2CH2OH;
(3)①为纤维素的水解反应,属于取代反应;⑤为乳酸分子内脱水,属于消去反应,
故答案为:取代反应;消去反应;
(4)③为乳酸的缩聚反应,反应方程式为: ,
,
④为两分子乳酸分子间的酯化反应,反应的化学方程式为: ,
,
故答案为: ;
; ;
;
(5)对于废弃的聚乳酸塑料,可以先回收,然后在催化剂(光和微生物)作用下,降解为乳酸,用乳酸重新制塑料,
故答案为:回收塑料,在催化剂(光和微生物)作用下,降解为乳酸,用乳酸重新制塑料.1年前查看全部
- (2011•江门二模)下列各组离子能大量共存的是( )
(2011•江门二模)下列各组离子能大量共存的是( )
A.pH<7的溶液中:Na+、S2-、K+、MnO4-
B.pH=7的溶液中:Al3+、Cl-、SO42-、AlO2-
C.pH>7的溶液中:Na+、CO32-、SO32-、K+
D.pH=0的溶液中:Na+、Al3+、Fe2+、ClO- sirenlicai1年前1
sirenlicai1年前1 -
 chengkiong 共回答了27个问题
chengkiong 共回答了27个问题 |采纳率96.3%解题思路:A.离子之间发生氧化还原反应;
B.离子之间相互促进水解;
C.碱溶液中该组离子之间不反应;
D.pH=0的溶液,显酸性,离子之间发生氧化还原反应.A.H+、S2-、MnO4-离子之间发生氧化还原反应,不能大量共存,故A错误;
B.Al3+、AlO2-离子之间相互促进水解,不能大量共存,故B错误;
C.碱溶液中该组离子之间不反应,能大量共存,故C正确;
D.pH=0的溶液,显酸性,H+、Fe2+、ClO-离子之间发生氧化还原反应,故D错误;
故选C.点评:
本题考点: 离子共存问题.
考点点评: 本题考查离子的共存,为高考常见题型,侧重氧化还原反应、复分解反应的考查,明确离子之间的反应及抽取习题中的信息即可解答,题目难度不大.1年前查看全部
- (2012•江门一模)如图,四边形ABCD中,AB=5,AD=3,cosA=[4/5],△BCD是等边三角形.
 (2012•江门一模)如图,四边形ABCD中,AB=5,AD=3,cosA=[4/5],△BCD是等边三角形.
(2012•江门一模)如图,四边形ABCD中,AB=5,AD=3,cosA=[4/5],△BCD是等边三角形.
(1)求四边形ABCD的面积;
(2)求sin∠ABD. 独山之玉1年前0
独山之玉1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•江门模拟)如图,三棱柱ABC-A1B1C1中,侧棱垂直底面,AC⊥BC,D是棱AA1的中点,AA1=2AC=
 (2014•江门模拟)如图,三棱柱ABC-A1B1C1中,侧棱垂直底面,AC⊥BC,D是棱AA1的中点,AA1=2AC=2BC=2a(a>0).
(2014•江门模拟)如图,三棱柱ABC-A1B1C1中,侧棱垂直底面,AC⊥BC,D是棱AA1的中点,AA1=2AC=2BC=2a(a>0).
(1)证明:C1D⊥平面BDC;
(2)求三棱锥C-BC1D的体积. yjm561年前1
yjm561年前1 -
 istill 共回答了18个问题
istill 共回答了18个问题 |采纳率83.3%解题思路:(1)通过证线线垂直证明BC⊥平面CDC1,由线面垂直的性质可得BC⊥C1D1,再根据A1C1=A1D=AD=AC,证∠CDC1=[π/2],然后由线线垂直⇒线面垂直;
(2)根据VC−BDC1=VC1−BCD,求得棱锥的底面S△BCD与高C1D,代入公式计算即可.(1)证明:∵BC⊥CC1,BC⊥AC,AC∩CC1=C,∴BC⊥平面ACC1A 1,
C1D⊂平面ACC1A 1,∴BC⊥C1D,
A1C1=A1D=AD=AC,∴∠A1DC1=∠ADC=
π
4,
∴∠C1DC=
π
2,即C1D⊥DC,
又BD∩CD=C,∴C1D⊥平面BDC,
(2)三棱锥C-BC1D即三棱锥C1-BCD,由(1)知BC⊥CD,
CD=
2a,BC=a
∴△BCD的面积S=
1
2×BC×CD=
2
2a2,
由(1)知,C1D是三棱锥C1-BCD底面BDC上的高,
∴体积V=
1
3Sh=
1
3×S×C1D=
1
3×
2
2a2×
2a=
1
3a3.点评:
本题考点: 直线与平面垂直的判定;棱柱、棱锥、棱台的体积.
考点点评: 本题考查了线面垂直的判定,考查了三棱锥的体积计算,利用三棱锥的换底性求体积是常用方法.1年前查看全部
- (2010•江门一模)设{an}为递减等比数列,a1+a2=11,a1•a2=10,lga1+lga2+lga3+…+l
(2010•江门一模)设{an}为递减等比数列,a1+a2=11,a1•a2=10,lga1+lga2+lga3+…+lga10=( )
A.-35
B.35
C.-55
D.55 疾风静草1年前1
疾风静草1年前1 -
 牛头大佬 共回答了17个问题
牛头大佬 共回答了17个问题 |采纳率82.4%解题思路:设an=a1qn-1,根据a1+a2=11,a1•a2=10可知,a1和a2为方程x2-11x+10=0的两根.求出方程的两根,根据a1>a2,可求出a1和a2,进而求出q,根据对数的性质,把a1和q代入lga1+lga2+lga3+…+lga10即可得到答案.设an=a1qn-1
根据a1+a2=11,a1•a2=10可知,a1和a2为方程x2-11x+10=0的两根.求得方程两根为1和10
∵{an}为递减等比数列
∴a1>a2
∴a1=10,a2=1
∴q=
a2
a1=[1/10]
∴lga1+lga2+lga3+…+lga10=lg(a1a2…a10)=lg(a110q45)=lga110+lgq45=10-45=-35
故选A点评:
本题考点: 等比数列的性质.
考点点评: 本题主要考查了等比数列的性质和对数函数的性质等问题.属基础题.1年前查看全部
- (2009•江门一模)工业上用铝土矿(主要成分是A1203,还有少量的Fe203,SiO2)提取冶炼铝的原料氧化铝.工艺
(2009•江门一模)工业上用铝土矿(主要成分是A1203,还有少量的Fe203,SiO2)提取冶炼铝的原料氧化铝.工艺流程图如图:
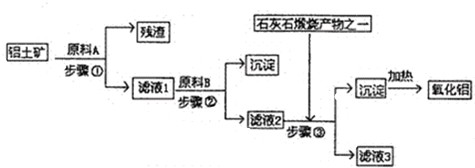
(1)原料A的名称是______,步骤①反应的离子方程式是______.
(2)滤液1中要加入稍过量原料B,原料B的化学式是______.步骤②反应的离子方程式是:______.
(3)步骤③的离子化学方程式是:______.
(4)步骤①②③的操作都是______(填操作名称),要检验Al(OH) 3沉淀是否完全的方法是______.
(5)如果省去步骤①,即溶解铝土矿是从加入原料B开始,则会对氧化铝的提取有什么影响?______. san2700211年前1
san2700211年前1 -
 善莫大焉 共回答了21个问题
善莫大焉 共回答了21个问题 |采纳率81%解题思路:SiO2和盐酸不反应,Fe2O3和氢氧化钠不反应而氧化铝能反应,向偏铝酸钠中通入过量的二氧化碳可以生成氢氧化铝沉淀.
由工艺流程可知步骤③通入的为二氧化碳,生成的沉淀为氢氧化铝,所以滤液2含有AlO2-.步骤②应加入氢氧化钠,除去铁离子,将铝离子转化为AlO2-,所以滤液1中含有Al3+,步骤①应为加入盐酸,除去SiO2.由工艺流程可知步骤③通入的为二氧化碳,生成的沉淀为氢氧化铝,所以滤液2含有AlO2-.步骤②应加入氢氧化钠,所以滤液1中含有Al3+,步骤①应为加入盐酸,除去SiO2.
(1)由上述分析可知,步骤①加入盐酸,除去SiO2,所以原料A为盐酸,
氧化铝与酸反应离子方程式为Al2O3+6H+=2Al3++3H2O,氧化铁与盐酸反应离子方程式为Fe2O3+6H+=2Fe3++3H2O.
故答案为:Al2O3+6H+=2Al3++3H2O;Fe2O3+6H+=2Fe3++3H2O.
(2)步骤①加入过量盐酸,滤液1中含有Al3+、Fe3+、H+等,应加入氢氧化钠,除去铁离子,将铝离子转化为AlO2-,反应为 H++OH-=H2O,Fe3++3OH-=Fe(OH)3↓,Al3++4OH-=AlO2-+2H2O.
故答案为:NaOH; H++OH-=H2O、Fe3++3OH-=Fe(OH)3、Al3++4OH-=AlO2-+2H2O.
(3)滤液2含有AlO2-,步骤③通入二氧化碳,与AlO2-反应生成的沉淀为氢氧化铝,
反应化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3.
故答案为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3.
(4)由工艺流程可知步骤①②③的操作都是过滤.检验Al(OH) 3沉淀是否完全,只要检验滤液3中是否含有AlO2-即可.取滤液3的上层清液,通入二氧化碳,若出现浑浊,则说明沉淀不完全;若不出现浑浊,则说明沉淀完全.
故答案为:过滤;取滤液3的上层清液,通入二氧化碳,若出现浑浊,则说明沉淀不完全;若不出现浑浊,则说明沉淀完全.
(5)若用NaOH溶液溶解铝土矿,则有部分SiO2溶解在NaOH溶液中生成硅酸钠,通入二氧化碳会生成硅酸沉淀,最后使加热制得的Al2O3混有SiO2杂质.
故答案为:若用NaOH溶液溶解铝土矿,则有部分SiO2溶解在NaOH溶液中生成硅酸钠,最后使加热制得的Al2O3混有SiO2杂质.点评:
本题考点: 镁、铝的重要化合物;硅和二氧化硅;铁的氧化物和氢氧化物;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题以框图题形式考查铝的化合物的性质,难度中等,清楚冶炼铝工艺流程原理,是对知识迁移的综合运用.1年前查看全部
- (2012•江门模拟)如图,AB和BC是由同种材料制成的长度相同、横截面积不同的两段导体,将它们串联后连入电路中.则 A
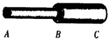 (2012•江门模拟)如图,AB和BC是由同种材料制成的长度相同、横截面积不同的两段导体,将它们串联后连入电路中.则 AB的电阻______BC的电阻;通过AB的电流______通过BC的电流;AB两端电压______BC两端电压.(选填“小于”、“大于”或“等于”)
(2012•江门模拟)如图,AB和BC是由同种材料制成的长度相同、横截面积不同的两段导体,将它们串联后连入电路中.则 AB的电阻______BC的电阻;通过AB的电流______通过BC的电流;AB两端电压______BC两端电压.(选填“小于”、“大于”或“等于”)  螽斯811年前1
螽斯811年前1 -
 w3whjf9w 共回答了18个问题
w3whjf9w 共回答了18个问题 |采纳率94.4%解题思路:(1)AB和BC是由同种材料制成的长度相同、横截面积不同的两段导体,横截面积越大,电阻越小;
(2)根据串联电路的电流特点可知通过两段导体的电流关系;
(3)根据U=IR可知两段导体两端的电压关系.(1)∵导体AB和BC由同种材料制成、长度相同,由图可知导体AB横截面积比BC的小,
∴RAB>RBC;
(2)∵两段导体串联,
∴通过两导体的电流相等,即IAB=IBC;
(3)∵U=IR,
∴UAB>UBC.
故答案为:大于; 等于; 大于.点评:
本题考点: 影响电阻大小的因素;串联电路的电流规律;欧姆定律的应用.
考点点评: 本题考查了影响电阻大小的因素和欧姆定律的应用,关键是串联电路电流特点的灵活运用.1年前查看全部
- (2013•江门模拟)将一植物放在密闭的玻璃罩内,置于室外进行培养,假定玻璃罩内植物的生理状态与自然环境中相同.CO2浓
 (2013•江门模拟)将一植物放在密闭的玻璃罩内,置于室外进行培养,假定玻璃罩内植物的生理状态与自然环境中相同.CO2浓度测定仪测得了该玻璃罩内CO2浓度的变化情况,绘制成如图的曲线.下列对曲线的分析正确的是( )
(2013•江门模拟)将一植物放在密闭的玻璃罩内,置于室外进行培养,假定玻璃罩内植物的生理状态与自然环境中相同.CO2浓度测定仪测得了该玻璃罩内CO2浓度的变化情况,绘制成如图的曲线.下列对曲线的分析正确的是( )
A.A点时叶肉细胞中产生ATP的部位只有线粒体
B.BC段较AB段CO2浓度增加减慢,是因为低温使植物呼吸作用减弱
C.D点和H点都表明植物光合作用强度和呼吸作用强度相等
D.H点CO2浓度最低,说明此时植物对CO2的吸收量多,光合作用最强 据v就会大1年前1
据v就会大1年前1 -
 我心痒ii了 共回答了12个问题
我心痒ii了 共回答了12个问题 |采纳率100%解题思路:本题主要考查呼吸作用和光合作用的过程.
1、呼吸作用是指生物体内的有机物在细胞内经过一系列的氧化分解,最终生成二氧化碳或其他产物,并且释放出能量的总过程.有氧呼吸的第一、二、三阶段的场所依次是细胞质基质、线粒体基质和线粒体内膜.有氧呼吸第一阶段是葡萄糖分解成丙酮酸和[H],合成少量ATP;第二阶段是丙酮酸和水反应生成二氧化碳和[H],合成少量ATP;第三阶段是氧气和[H]反应生成水,合成大量ATP.
2、光合作用是指绿色植物通过叶绿体,利用光能把二氧化碳和水转变成储存着能量的有机物,并释放出氧气的过程.光合作用的光反应阶段(场所是叶绿体的类囊体膜上):水的光解产生[H]与氧气,以及ATP的形成.光合作用的暗反应阶段(场所是叶绿体的基质中):CO2被C5固定形成C3,C3在光反应提供的ATP和[H]的作用下还原生成淀粉等有机物.A、A点时叶肉细胞中只进行呼吸作用,故产生ATP的部位时细胞质基质和线粒体,A错误;
B、AB段和BC段没有光照只进行呼吸作用.与AB段相比,BC段温度较低,植物呼吸作用较弱,故CO2浓度增加较慢,B正确;
C、从图可知,D、H点表示光合作用强度与呼吸强度相等,C正确;
D、DH段光合作用强度大于呼吸作用强度,H点表示光合作用强度与呼吸强度相等,有机物积累最多,但光合作用相对较弱,D错误.
故选:BC.点评:
本题考点: 光反应、暗反应过程的能量变化和物质变化;细胞呼吸的过程和意义.
考点点评: 本题考查光合作用和呼吸作用的有关知识,意在考查考生理解所学知识的要点,把握知识间的内在联系的能力.考查学生对曲线的准确解度,做出正确合理的判断,得出正确的结论的能力.1年前查看全部
- (2013•江门一模)能在水溶液中大量共存的一组离子是( )
(2013•江门一模)能在水溶液中大量共存的一组离子是( )
A.Na+、Mg2+、I-、ClO-
B.Al3+、NH
、SO+4
、Cl-2−4
C.K+、Ag+、NO
、Cl-−3
D.NH
、Na+、OH-、SiO+42−3 偶尔vv也难受1年前1
偶尔vv也难受1年前1 -
 紫面阎王 共回答了14个问题
紫面阎王 共回答了14个问题 |采纳率92.9%解题思路:如离子之间不发生复分解反应生成沉淀、气体或弱电解质或发生互促水解、氧化还原等反应,则可大量共存,反之不能.A.I-与ClO-发生氧化还原反应而不能大量共存,故A错误;
B.离子之间不发生任何反应,可大量共存,故B正确;
C.Ag+与Cl-反应生成AgCl而不能大量共存,故C错误;
D.NH4+与OH-反应而不能大量共存,故D错误.
故选B.点评:
本题考点: 离子共存问题.
考点点评: 本题考查离子共存问题,题目难度不大,注意把握离子的性质,为解答该类题目的关键,特别要注意ClO-无论在酸性还是碱性条件下都具有较强的氧化性.1年前查看全部
- (2012•江门模拟)如图表示内环境稳态的调节机制,据图分析回答下列问题:
(2012•江门模拟)如图表示内环境稳态的调节机制,据图分析回答下列问题:
 (1)图中③⑤***的物质依次是______.
(1)图中③⑤***的物质依次是______.
(2)若⑧表示促甲状腺激素,对⑧分泌具有调节作用的激素有______.
(3)外界环境温度下降,刺激皮肤感受器产生兴奋时,此过程中神经纤维膜内的电位变化是______.神经冲动传导到位于______中的体温调节中枢,通过调节作用维持体温的恒定.
(4)免疫功能过强或过弱,都会引起机体功能紊乱.当⑥再次侵入机体内环境发生的组织损伤或功能紊乱称为______.
(5)图示表明内环境稳态的维持是______共同调节的结果. smokethefish1年前1
smokethefish1年前1 -
 tqaikflaikd 共回答了20个问题
tqaikflaikd 共回答了20个问题 |采纳率85%解题思路:内环境的稳态就是指在正常生理情况下机体内环境的各种成分和理化性质只在很小的范围内发生变动.内环境的稳态是细胞维持正常生理功能的必要条件,也是机体维持正常生命活动的必要条件,内环境稳态失衡可导致疾病.内环境稳态的维持有赖于各器官,尤其是内脏器官功能状态的稳定、机体各种调节机制的正常以及血液的纽带作用.(1)神经系统释放到内环境中的物质为神经递质,免疫系统释放到内环境中的物质为抗体和淋巴因子.
(2)⑧表示促甲状腺激素,对⑧分泌具有调节作用的激素有促甲状腺激素释放激素和甲状腺激素.其中促甲状腺激素释放激素促进促甲状腺激素的分泌,甲状腺激素对促甲状腺激素的分泌起反馈作用.
(3)刺激皮肤感受器产生兴奋时,神经纤维膜内的电位变化是由负变为正,体温调节中枢在下丘脑.
(4)当⑥再次侵入机体内环境发生的组织损伤或功能紊乱,这是过敏反应.
(5)内环境的稳态是神经、体液和免疫调节共同作用的结果.
故答案为:
(1)神经递质、抗体(或淋巴因子)
(2)促甲状腺激素释放激素和甲状腺激素
(3)由负变正下丘脑
(4)过敏反应
(5)神经、内分泌、免疫系统(或神经-体液--免疫系统)点评:
本题考点: 神经、体液调节在维持稳态中的作用;人体免疫系统在维持稳态中的作用.
考点点评: 本题主要考查内环境的相关知识,意在考查学生对所学知识的理解和掌握能力,以及识图能力和运用知识解决实际问题的能力.1年前查看全部
- (2014•江门模拟)如图,质量为m的木块在水平向右的力F作用下在质量为M的木板上滑行,木板长度为L,保持静止.木块与木
 (2014•江门模拟)如图,质量为m的木块在水平向右的力F作用下在质量为M的木板上滑行,木板长度为L,保持静止.木块与木板、木板与地面间的动摩擦因数均为μ,说法正确的是( )
(2014•江门模拟)如图,质量为m的木块在水平向右的力F作用下在质量为M的木板上滑行,木板长度为L,保持静止.木块与木板、木板与地面间的动摩擦因数均为μ,说法正确的是( )
A.木板受到地面的摩擦力大小是μmg
B.木板受到地面的摩擦力大小是μ(m+M)g
C.当F>μ(m+M)g时,木板便会开始运动
D.木块滑过木板过程中,产生的内能为μmgL axddax1年前1
axddax1年前1 -
 三十三十 共回答了20个问题
三十三十 共回答了20个问题 |采纳率80%解题思路:m对M的压力等于mg,m所受M的滑动摩擦力f1=μmg,方向水平向左,M处于静止状态,水平方向受到m的滑动摩擦力和地面的静摩擦力,根据平衡条件分析木板受到地面的摩擦力的大小和方向.A、B、m所受M的滑动摩擦力大小f=μmg,方向水平向左,根据牛顿第三定律得知:木板受到m的摩擦力方向水平向右,大小等于μmg,A正确,B错误.
C、当F>μ(m+M)g时,木板受的m的滑动摩擦力不变,木板仍然静止,C错误;
D、木块滑过木板过程中,产生的内能为Q=fS相对=μmgL,D正确;
故选:AD.点评:
本题考点: 摩擦力的判断与计算.
考点点评: 本题中木板受到地面的摩擦力是静摩擦力,不能根据摩擦力求解,f2=μ2(m+M)g是错误的,不能确定此摩擦力是否达到最大值.1年前查看全部
- (2007•江门模拟)关于热机和热力学定律的讨论,下列叙述正确的是( )
(2007•江门模拟)关于热机和热力学定律的讨论,下列叙述正确的是( )
A.气体的温度升高时,分子的热运动变得剧烈,撞击器壁时对器壁的作用力增大,从而气体的压强一定增大
B.一定质量的理想气体经等温压缩后,其压强一定增大
C.物体放出热量,温度一定降低
D.只要对内燃机不断改进,就可以把内燃机得到的全部内能转化为机械能 追风78111年前1
追风78111年前1 -
 aqi_1017 共回答了18个问题
aqi_1017 共回答了18个问题 |采纳率77.8%解题思路:1、压强从微观上看,跟气体分子的平均动能和单位体积内的分子数有关,由于不清楚体积的变化,即不知道单位体积内的分子数如何变化,所以不知道气体的压强变化.
2、根据等温变化的公式PV=C,当V减小,P一定增大.
3、根据热力学第一定律的表达式△U=Q+W,物体放出热量,Q为负值,但是由于不清楚做功情况,即不知道W的正负和大小,所以内能无法确定,从而无法判断温度的升降.
4、热机的排气温度一定高于进气温度(可以无限逼近但不会相等),所以,一定有热能的损失,效率不可能为100%.A、一定质量的理想气体的温度升高时,分子的热运动变得剧烈,分子的平均动能增大,由于不清楚体积的变化,根据气体状态方程知道气体的压强变化无法确定.故A错误.
B、根据等温变化的公式PV=C,当V减小,P一定增大.即一定质量的理想气体经等温压缩后,其压强一定增大.故B正确.
C、物体放出热量,根据热力学第一定律的表达式△U=Q+W,由于不清楚W的变化,所以内能无法确定,从而无法判断温度的升降.故C错误.
D、热机在内能转化为机械能时,不可避免的要要有一部热量被传导出,所以热机效率达不到100%,即任何热机都不可以把得到的全部内能转化为机械能.故选D错误.
故选B.点评:
本题考点: 热机的工作原理;热力学第一定律;能量守恒定律.
考点点评: 要注意研究过程中哪些量不变,哪些量变化.知道气体压强产生的原理.1年前查看全部
- (2013•江门一模)如图,AB是圆O的直径,C是圆O上除A、B外的一点,△AED在平面ABC的投影恰好是△ABC.已知
 (2013•江门一模)如图,AB是圆O的直径,C是圆O上除A、B外的一点,△AED在平面ABC的投影恰好是△ABC.已知CD=BE,AB=4,tan∠EAB=
(2013•江门一模)如图,AB是圆O的直径,C是圆O上除A、B外的一点,△AED在平面ABC的投影恰好是△ABC.已知CD=BE,AB=4,tan∠EAB=
.1 4
(1)证明:平面ADE⊥平面ACD;
(2)当三棱锥C-ADE体积最大时,求三棱锥C-ADE的高. T独钓寒江T1年前1
T独钓寒江T1年前1 -
 我就随便看看 共回答了18个问题
我就随便看看 共回答了18个问题 |采纳率100%解题思路:(1)要证两个面相互垂直,可证平面ADE经过平面ACD的一条垂线DE,根据,△AED在平面ABC的投影恰好是△ABC,说明CD和BE都垂直于底面ABC,又CD=BE,可证DE∥BC,利用线面垂直的判定定理可证BC⊥面ACD,从而使问题得证;
(2)把三棱锥C-ADE体积转化为三棱锥E-ACD的体积,写出体积公式后利用基本不等式求体积最大值,并且得到使体积最大时的多面体A-BEDC的确切形状,然后利用等积法可求三棱锥C-ADE的高.(1)证明:因为AB是直径,所以BC⊥AC,因为△ABC是△AED的投影,所以CD⊥平面ABC,则CD⊥BC,
因为CD∩AC=C,所以BC⊥平面ACD,
因为CD⊥平面ABC,BE⊥平面ABC,所以CD∥BE,又因为CD=BE,所以BCDE是平行四边形,
∴BC∥DE,则DE⊥平面ACD,因为DE⊂平面ADE,所以平面ADE⊥平面ACD;
(2)在直角三角形AEB中,EB=AB•tan∠EAB=4×[1/4]=1,
由(1)知VC−ADE=VE−ACD=
1
3S△ACD•DE
=[1/3×
1
2AC•CD•DE=
1
6AC•EB•BC=
1
6AC•BC≤
1
12×(AC2+BC2)=
1
12×AB2=
4
3],
等号当且仅当AC=BC=2
2时成立,
此时,AD=
AC2+CD2=
12+(2
2)2=3,
S△ADE=
1
2AD•DE=
1
2×3×2
2=3
2,
设三棱锥C-ADE的高为h,
则VC−ADE=
1
3S△ADE•h=
4
3,
∴
1
3×3
2•h=
4
3.
∴h=
2
2
3.
所以,当三棱锥C-ADE体积最大时,三棱锥C-ADE的高为
2
2
3.点评:
本题考点: 平面与平面垂直的判定;棱柱、棱锥、棱台的体积.
考点点评: 本题主要考查了直线与平面垂直的判定和性质,考查空间想象能力、运算能力和推理论证能力,训练了利用基本不等式求最值,求棱锥体积最大时的棱锥的高时,运用了等积法,体现了数学转化思想,属于中档题.1年前查看全部
大家在问
- 1别担心,我们有足够的时间赶到那里 英语
- 2掀 是什么结构?部首是?共几画?
- 3(20分)读下面“极点日照图”(阴影部分表示黑夜),完成下列问题。
- 4根据汉语意思完成句子 1.这是标方中学学生活动调查的结果。
- 5下列事例中属于增大压强的是( ) A.将铁路的钢轨铺在枕木上 B.将书包的背带做得较宽 C.将切菜刀磨得更锋利 D.载
- 6(1)如图1所示,光线从空气射入某种液体中,入射角为45°,折射角为30°;光线射到液体中某处水平放置的平面镜上又反射回
- 7金属晶体的下列性质中,不能用金属晶体结构加以解释的是( )
- 8我们是彼此的幸福——献蓝洛的生日贺文 作文
- 9硬度HV0.1与HV区别是什么?
- 10写一篇描写小时候的一张照片的英语小作文小学水平就可以了
- 11简单英文翻译“这里也有你很多粉丝” 英文翻译,在线等
- 121256和150的最大公因数是多少
- 13把(她是一名老师,而他哥哥是一位医生)翻译成英语
- 14(2011•金东区模拟)在方格纸中,把一个图形先沿水平方向平移|a|格(当a为正数时,表示向右平移;当a为负数时,表示向
- 15金秋十月的作文,写苏州的景色和特产,拜托,拜托,请各位学霸帮帮忙吧。
