在干燥的空气中用塑料梳子梳理干燥的头发,头发跟着飘动,有时还能听到“啪啪”的响声,解释原因
 戴玫瑰花冠的公主2022-10-04 11:39:541条回答
戴玫瑰花冠的公主2022-10-04 11:39:541条回答麻烦用物理知识解答,详细点

已提交,审核后显示!提交回复
共1条回复
 yanwoniu 共回答了21个问题
yanwoniu 共回答了21个问题 |采纳率90.5%- 考点:电荷间的相互作用规律;摩擦起电.
分析:梳子和头发摩擦,由于两种物质的原子核对核外电子的束缚本领不同,在摩擦的过程中,会有电子的转移,得电子的物体带负电,失去电子的物体带正电.然后利用电荷间的作用规律,即可解决问题.
当梳子和头发相互摩擦时,由于梳子的原子核对电子的束缚能力强在摩擦的过程中得电子而带负电,头发由于失去电子而带正电.由于异种电荷相互吸引.所以头发会随着梳子飞起来. - 1年前
相关推荐
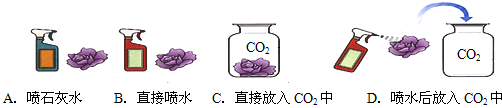
- (2013•昭通)(1)用石蕊染成紫色的干燥纸花,进行如下操作,能够观察到纸花变红的是______.
(2013•昭通)(1)用石蕊染成紫色的干燥纸花,进行如下操作,能够观察到纸花变红的是______.
(2)下列A、B是探究物质性质的实验:
二氧化碳是否可以溶于水,很难直接观察到现象,可以通过A中塑料瓶______的变化来间接感知.同样,研究氢氧化钠溶解于水时是吸热还是放热,可利用密闭的广口瓶内______的变化引起U形管内水位的变化,若______(填a或b)处的水位升高,则是放热.
(3)一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.下表是实验中可能出现的现象与对应结论,请你填写下表中空白处的相关内容:
通过实验及分析,确定该粉末为氧化铜和碳粉混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如图所示实验:现象 结论 ______ 含CuO、C 溶液颜色无明显变化,有黑色不溶物 只含______ 
①试管a中的化学方程式为C+2CuO
2Cu+CO2↑高温 .C+2CuO.
2Cu+CO2↑高温 .
②氧化铜和碳反应属于______反应.(填基本反应类型)
③最能说明a试管中氧化铜和碳已完全反应的实验现象是______. 梦的影子戚1年前1
梦的影子戚1年前1 -
 xx斗士 共回答了20个问题
xx斗士 共回答了20个问题 |采纳率80%解题思路:(1)二氧化碳与水可反应生成碳酸,碳酸可使石蕊变红,碱性溶液可使石蕊变蓝,并结合题意分析解答;
(2)气体溶于水,则瓶内气体减少,气压减小,塑料瓶变瘪;并据气体热胀冷缩引起的气压变化设计实验,据U型管内水位的变化分析物质溶于水是否放热;
(3)氧化铜与硫酸可反应生成蓝色的硫酸铜溶液和水,碳和硫酸不反应,据此并结合实验结论、实验现象进行分析;
①碳和氧化铜高温生成铜和二氧化碳,据此书写方程式;
②据反应特点分析反应类型;
③该反应生成二氧化碳,所以可据b中导管口是否产生气泡判断是否完全反应.(1)A、石灰水可使石蕊变蓝,故不符合题意;
B、石蕊试液喷水显中性,中性溶液中石蕊不变色,依然是紫色,故不符合题意;
C、二氧化碳不能使石蕊变红,故不符合题意;
D、二氧化碳可与水反应生成碳酸,碳酸可使石蕊变红,符合题意;
(2)向充满二氧化碳的软塑料瓶中注入水,若塑料瓶变瘪,则说明二氧化碳可溶于水,瓶内气体减少导致气压减小;气体具有热胀冷缩的性质,若氢氧化钠溶于水放热,则瓶内温度升高,气体膨胀,气压变大,U型管内a处水位下降,b处水位上升;
(3)取少量该黑色粉末于烧杯中,加入过量稀硫酸,若粉末中含有CuO、C,则烧杯内氧化铜与硫酸反应生成硫酸铜溶液,溶液变蓝,碳与硫酸不反应,所以烧杯内还会有黑色不溶物;若溶液颜色无变化,有黑色不溶物,说明黑色粉末中无氧化铜,只有碳;
①碳和氧化铜高温生成铜和二氧化碳,方程式是C+2CuO
高温
.
2Cu+CO2↑;
②该反应是由单质--C,和化合物CuO,生成另一种单质Cu,化合物CO2,符合置换反应的特点,属于置换反应;
③该反应生成二氧化碳,所以可据b中导管口是否产生气泡判断是否完全反应;
故答案为:
(1)D;
(2)变瘪;气压(或温度);b;
(3)溶液呈蓝色,有黑色不溶物;C;
①C+2CuO
高温
.
2Cu+CO2↑;
②置换;
③b中的导管口不再产生气泡(合理即可).点评:
本题考点: 二氧化碳的化学性质;实验探究物质的组成成分以及含量;溶解时的吸热或放热现象;酸的化学性质;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 了解二氧化碳的性质、指示剂的变色情况、碳和氧化铜反应实验等知识,才能结合题意正确分析解答.1年前查看全部
- 下列物质可以用来干燥二氧化碳气体的是( ) A、浓硫酸 B、浓盐酸 C、稀硫酸 D、氧化钙固体
下列物质可以用来干燥二氧化碳气体的是( ) A、浓硫酸 B、浓盐酸 C、稀硫酸 D、氧化钙固体
原因 彩色的鱼儿1年前2
彩色的鱼儿1年前2 -
 YOYO之妖精 共回答了15个问题
YOYO之妖精 共回答了15个问题 |采纳率100%下列物质可以用来干燥二氧化碳气体的是
A、浓硫酸,本身具有干燥的功能,可以用来干燥CO2.
B、浓盐酸,本身不具有干燥的功能,而且还极易会发出HCl气体.
C、稀硫酸 ,本身不具有干燥的功能,而且还会发出引入水蒸气.
D、氧化钙固体,碱性物质,可以吸收CO2,不能干燥酸性气体CO21年前查看全部
- 制取干燥二氧化碳装置是不是那个长颈漏斗,锥形瓶的那个装置
 zjx7257221年前1
zjx7257221年前1 -
 桂殿兰宫 共回答了20个问题
桂殿兰宫 共回答了20个问题 |采纳率90%启普发生器(盐酸和碳酸钙)+橡皮管+干燥瓶(内装浓硫酸)+集气瓶+玻璃盖1年前查看全部
- 用简短的语言介绍一下叙利亚的另一大特点——令人最不能忍受的干燥与闷热(快!)
 嘟嘟巧克力鱼1年前3
嘟嘟巧克力鱼1年前3 -
 蜩学鸠 共回答了21个问题
蜩学鸠 共回答了21个问题 |采纳率85.7%叙利亚位于亚洲西部、地中海东岸,北邻土耳其,西濒地中海并与黎巴嫩接壤,东邻伊拉克,南接约旦,西南与巴勒斯坦和以色列相连,属地中海气候,冬季下雨,夏季干旱,春秋为两个短短的过渡季.沿海地区冬季雨水多,山区冬季则是雨雪多,沙漠地区冬季雨量稀少,夏季干旱、炎热.1年前查看全部
- 干燥的玉米种子胚乳中储藏了大量的( ) A.水分 B.无机盐 C.矿物质 D.有机物
 秋思思思1年前1
秋思思思1年前1 -
 guanp1220 共回答了17个问题
guanp1220 共回答了17个问题 |采纳率70.6%选D,有机物.
解析:首先种子是干燥的,所以排出A项;无机盐和矿物质的含量只占种子干重的10%左右,其余90%的成分均为有机物,因此B和C均错;D正确,干燥种子中含量最多的是有机物,主要为淀粉,其次为蛋白质,还含有少量的维生素等等有机物.
希望能帮助你.^__^1年前查看全部
- 将一铜片在酒精灯上加热分别插入1醋酸2乙醇3石灰水溶液中,反应完毕,取出铜片洗涤,干燥,称量.为什么醋酸变使铜片质量变轻
将一铜片在酒精灯上加热
分别插入1醋酸2乙醇3石灰水溶液中,反应完毕,取出铜片洗涤,干燥,称量.为什么醋酸变使铜片质量变轻,乙醇使其不变,石灰水溶液使其变重?
卷子的答案就是这样的 海之锋1年前1
海之锋1年前1 -
 gsnacdt 共回答了24个问题
gsnacdt 共回答了24个问题 |采纳率91.7%铜经过加热后表面部分铜会变成氧化铜,放入醋酸中氧化铜会被酸碱反映掉,所以质量会变轻
乙醇把氧化铜还原了,所以质量不变
和石灰水中的水会生成氢氧化铜附着在同表面,所以质量会变重1年前查看全部
- 例句是:处处干燥,处处烫手,处处憋闷,整个老城像烧透了的砖窑,使人喘不过气来 帮忙造个句子
 再亲亲宝贝1年前1
再亲亲宝贝1年前1 -
 j01a 共回答了19个问题
j01a 共回答了19个问题 |采纳率94.7%处处清新,处处凉爽,处处湿润,整个山村想再次迎来春天,令人心情大好.
不知道行不行额
希望对您有帮助1年前查看全部
- 五氧化二磷与水反应,为何能用于干燥气体?
 potato5271年前1
potato5271年前1 -
 诎拙 共回答了15个问题
诎拙 共回答了15个问题 |采纳率93.3%能与水反应,就是能吸收水分啊.
气体中带有水分,不干燥.
通过P2O5,水被吸收,气体就干燥了.
所以
五氧化二磷与水反应,能用于干燥气体1年前查看全部
- 小明模拟自然界雨的形成做了如果4—5的实验.向锥形瓶中注入少量的温水,稍后,取一干燥的表面皿盖在瓶口,在表面皿中放置一些
小明模拟自然界雨的形成做了如果4—5的实验.向锥形瓶中注入少量的温水,稍后,取一干燥的表面皿盖在瓶口,在表面皿中放置一些冰块.稍后,观察到在瓶内出现白雾,表面皿底部看到有小水滴,小水滴逐渐变大,最终下落到瓶内.此实验展示了雨滴形成的过程和物态变化.下列说法中正确的是( )
A、水蒸气上升,遇冷时凝结成水滴,物态变化为液化
B、水蒸气下降,遇热时凝结成水滴,物态变化为液化
C、水蒸气上升,遇冷时凝结成水滴,物态变化为汽化
D、水蒸气下降,遇热时凝结成水滴,物态变化为汽化 zhoumingyue1年前1
zhoumingyue1年前1 -
 13560444455 共回答了13个问题
13560444455 共回答了13个问题 |采纳率100%A1年前查看全部
- 将一支充满干燥氨气的试管倒插入滴有几滴酚酞溶液的蒸馏水里,该实验的现象
 zyylx1年前2
zyylx1年前2 -
 巴索夫 共回答了14个问题
巴索夫 共回答了14个问题 |采纳率85.7%水柱上升,然后进入试管的溶液退色(由于氯气与水反应生成了强氧化剂HCLO)1年前查看全部
- 小明模拟大自然"雨"的形成做了如下实验.向锥形瓶中注入少量的温水,稍后,取一干燥的表面皿盖在瓶口,在表面皿中放置一些冰块
小明模拟大自然"雨"的形成做了如下实验.向锥形瓶中注入少量的温水,稍后,取一干燥的表面皿盖在瓶口,在表面皿中放置一些冰块,稍后,在瓶内出现朦胧的"白雾",表面皿底部看到有小水滴,小水滴逐渐变大,最后下落到瓶内.
(1)在瓶内出现朦胧的:白雾"是一种_____现象
(2)这个模拟实验中展示的是水循环中的_________环节
2)这个模拟实验中展示的是水循环中的___和____环节 酸的滋味1年前3
酸的滋味1年前3 -
 跳跃的火焰 共回答了23个问题
跳跃的火焰 共回答了23个问题 |采纳率78.3%(1)气化
(2)蒸发和降雨
希望对你有用.1年前查看全部
- (2013•陇南模拟)储存小麦应保持的条件是低温、干燥、通入足量的氧气.______.(判断对错)
 qjzxm8671年前1
qjzxm8671年前1 -
 无色唇彩 共回答了22个问题
无色唇彩 共回答了22个问题 |采纳率90.9%解题思路:由我们所学的知识可以知道:温度、二氧化碳、水等对种子呼吸作用有影响,据此答题.温度能影响呼吸作用,主要是影响呼吸酶的活性.一般而言,在一定的温度范围内,呼吸强度随着温度的升高而增强. 根据温度对呼吸强度的影响原理,在生产实践上储存粮食时应该降低温度,抑制种子的呼吸,以减少呼吸消耗、可延长储存时间;植物进行呼吸作用消耗氧气分解有机物,而种子内的物质必须先溶解在水里才能被种子利用,因此种子含水多,呼吸作用旺盛,含水少,种子的呼吸作用较弱.晒干的种子,水分减少,抑制了种子的呼吸作用,可以延长了种子的储存时间;增加CO2的浓度对呼吸作用有明显的抑制效应.二氧化碳浓度高呼吸作用弱,二氧化碳浓度低呼吸作用强.据此原理,在储存粮食时,增加CO2的浓度,抑制了种子的呼吸作用,以减少呼吸消耗、可延长储存时间,而通入足量的氧气则会增强种子的呼吸作用,不利于种子的保存.
故答案为:×点评:
本题考点: 种子的知识在农业生产上的应用.
考点点评: 此解答此类题目的关键是熟知温度、二氧化碳、水对呼吸作用的影响,更好的为农业生产服务.1年前查看全部
- 请问一下"混有少量HCL,H2O杂质的CO2,为使其纯净和干燥,为什么要用NaHCO3除去HCL,而不用NaOH和Na2
请问一下"混有少量HCL,H2O杂质的CO2,为使其纯净和干燥,为什么要用NaHCO3除去HCL,而不用NaOH和Na2CO3除去"
 rojy1年前1
rojy1年前1 -
 老张骑驴 共回答了18个问题
老张骑驴 共回答了18个问题 |采纳率94.4%因为CO2可与NaOH和Na2CO3反应,
CO2可与Na2CO3生成NaHCO31年前查看全部
- 无水氯化钙为什么不能干燥氨气
 冻人1年前1
冻人1年前1 -
 ronger531 共回答了21个问题
ronger531 共回答了21个问题 |采纳率90.5%氯化钙是中性的.
但是能和氨气结合生成CaCl2·8NH31年前查看全部
- 五氧化二磷、浓硫酸、氯化钙分别适用干燥哪些气体?
 1573591251年前1
1573591251年前1 -
 cyw798 共回答了23个问题
cyw798 共回答了23个问题 |采纳率95.7%五氧化二磷可以干燥酸性中性气体SO2、N2、H2、HI、H2S.
浓硫酸干燥酸性气体和中性气体,且还原性弱的气体,如:H2,CO2,SO2,Cl2,O2等
氯化钙可以干燥酸性、中性、碱性气体.
但不能干燥NH3.原因是会反应生成CaCl2·xNH3(x最大为8).这样氨气就被吸收了.1年前查看全部
- 俄罗斯主要的气候特点是( )A.终年严寒B.冬季温和多雨,夏季炎热干燥C.终年高温D.冬季长而寒冷,夏季短而温暖
 唐墨衣1年前1
唐墨衣1年前1 -
 binglizhi 共回答了15个问题
binglizhi 共回答了15个问题 |采纳率93.3%解题思路:俄罗斯幅员辽阔,面积1709.8万千米2,是世界上面积最大的国家,也是唯一地跨亚、欧两大洲和东、西两半球的国家.俄罗斯地处中、高纬度地区,以温带大陆性气候为主,冬季严寒而漫长,夏季凉爽而短促.由于领土辽阔,各地气候差异显著.北冰洋沿岸属寒带气候,太平洋沿岸属温带季风气候.西伯利亚地区冬季非常寒冷.东欧平原气候比较温和,人口和城市主要集中在这里.
故选:D.点评:
本题考点: 俄罗斯温带大陆性和亚寒带针叶林气候的特征.
考点点评: 考查俄罗斯的气候特点,要理解记忆.1年前查看全部
- 下列说法正确的是(初中化学)A、干燥的HCI气体也能与金属反应生成H2B、氰化钠气体通入水中既得盐酸C、打开盛有浓盐酸的
下列说法正确的是(初中化学)
A、干燥的HCI气体也能与金属反应生成H2
B、氰化钠气体通入水中既得盐酸
C、打开盛有浓盐酸的瓶盖会看到白雾
D、稀释浓硫酸时,只能将水缓缓倒入浓硫酸中 麸子皮1年前5
麸子皮1年前5 -
 车轮滚滚尘飞扬 共回答了16个问题
车轮滚滚尘飞扬 共回答了16个问题 |采纳率87.5%A绝对干燥的HCl在常温下不能与一般金属反应,但是如果遇到强活泼金属或高温则能反应,鉴于(初中化学)的说明,这个不正确.
B氰化钠不是气体,估计是打错字了,应该是氰化氢气体吧,通入水中得到的是氢氰酸,而不是盐酸.但不管是否打错字了,都是不正确的.
C正确
D应该反过来,将浓硫酸倒入水中,因为浓硫酸密度比水大,在考虑放热,安全.1年前查看全部
- 在一张洁白干燥的滤纸上依次喷洒 A、B、C三种无色液体,当喷洒A时滤纸无明显变化,再喷洒B时滤纸上显出一间红色小屋,最后
在一张洁白干燥的滤纸上依次喷洒 A、B、C三种无色液体,当喷洒A时滤纸无明显变化,再喷洒B时滤纸上显出一间红色小屋,最后喷洒C时红色小屋又消失了,回答下列问题:滤纸上的小屋事先是用______试剂画出的.无色液体A是______; B是______;C是______.
 bwango1年前1
bwango1年前1 -
 只是妖女 共回答了17个问题
只是妖女 共回答了17个问题 |采纳率100%解题思路:根据已有的知识进行分析解答,酚酞试液在碱性溶液中变红,在酸性和中性溶液中不变色,酸和碱能中和生成盐和水,据此解答.白色的滤纸,说明是用酚酞试液画的,酚酞在酸性和中性溶液中不变色,在碱性溶液中变红,故喷洒的A可以是水,B是氢氧化钠溶液,当喷C时红色消失,说明碱性消失,故喷洒的C是酸性溶液,可以是盐酸,故填:酚酞,水,氢氧化钠,稀盐酸.
点评:
本题考点: 酸碱指示剂及其性质.
考点点评: 本题考查了酸碱指示剂与溶液酸碱性的关系,完成此题,可以依据已有的知识进行.1年前查看全部
- 我这个化学白痴- -问题是;为了使用石灰浆抹的墙壁快点干燥.为什么常在室内生个炭火盆?为什么开始放炭火盆时,墙壁反而变潮
我这个化学白痴- -
问题是;为了使用石灰浆抹的墙壁快点干燥.为什么常在室内生个炭火盆?为什么开始放炭火盆时,墙壁反而变潮湿?
要说的明白点! 水清晓圆1年前3
水清晓圆1年前3 -
 荷包里的单人床 共回答了19个问题
荷包里的单人床 共回答了19个问题 |采纳率100%石灰浆是Ca(OH)2,炭火盆燃烧放出CO2,这两种物质反应方程式为:
Ca(OH)2+CO2=CaCO3+H2O 放出水,所以墙壁会变潮湿.1年前查看全部
- (2006•菏泽)某课外活动小组用氯酸钾和二氧化锰的混合物制取干燥、较纯净的氧气.实验步骤如下:
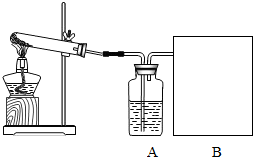 (2006•菏泽)某课外活动小组用氯酸钾和二氧化锰的混合物制取干燥、较纯净的氧气.实验步骤如下:
(2006•菏泽)某课外活动小组用氯酸钾和二氧化锰的混合物制取干燥、较纯净的氧气.实验步骤如下:
①检查装置的气密性,气密性良好;
②先在试管中放入MnO2,再放入略多于计算量的KClO3;
③连接好实验装置;
④加热;
⑤收集气体;
⑥适当的时间后,停止加热,拆卸装置.
回答下列问题:
(1)装置A中的试剂______.
(2)方框B中最好选用下列装置中的______(填字母序号).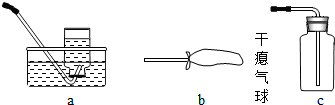
(3)实验中观察到何种现象时开始收集气体______.
(4)实验结束后,该同学发现收集到的气体比预计的少许多,百思不得其解.你认为可能的原因是______.
(5)欲从反应的残渣中回收二氧化锰(难溶于水),其操作步骤是:溶解、______、烘干. 小小香草1年前1
小小香草1年前1 -
 qulinshan 共回答了17个问题
qulinshan 共回答了17个问题 |采纳率88.2%解题思路:(1)依据图示及其作用,辨识常用药品,正确写出药品名称;
(2)根据实验要求,选择合适的实验装置;
(3)根据氧气的性质收集氧气时,掌握开始收集气体应注意的问题;
(4)在实验出现误差或失误时,会分析解决问题,找出原因.
(5)学会固体混合物的分离方法及操作步骤.(1)依据图示及其作用装置A中的试剂可用浓硫酸;因浓硫酸具吸水性,可做氧气的干燥剂.故答案为:浓硫酸
(2)根据实验要求分析方框B中最好选用的装置:a 装置是用排水法收集,得不到干燥的氧气.b装置可以收集到纯净而干燥的氧气,且能够观察收集气体的量;c 装置收集氧气时,无法排除集气瓶内空气.故答案为:b
(3)根据氧气不易溶于浓硫酸的性质收集氧气时,开始有气泡冒出因混有空气不纯,不要立即收集.看到有气泡从A中均匀冒出才能收集.故答案为:看到有气泡从A中均匀冒出
(4)实验结束后,该同学发现收集到的气体比预计的少许多,出现这样的现象可能是:装置A漏气、气球漏气、药品量少等.故答案为:装置A漏气(或气球漏气)等
(5)从反应的残渣中回收难溶于水的二氧化锰时,残渣中的氯化钾(或存在没反应完的氯酸钾)能溶于水,故其操作步骤为:溶解、过滤、烘干.故答案为:过滤
故答案为:
(1)浓硫酸
(2)b
(3)看到有气泡从A中均匀冒出
(4)装置A漏气(或气球漏气)
(5)过滤点评:
本题考点: 制取氧气的操作步骤和注意点;混合物的分离方法;过滤的原理、方法及其应用;氧气的制取装置;氧气的收集方法.
考点点评: 掌握常用气体的干燥剂、制取氧气的装置与收集方法及注意事项,学会固体混合物的分离方法及操作步骤1年前查看全部
- 澳大利亚四面临海,为什么干燥面积广大
 saltgreen1年前1
saltgreen1年前1 -
 耳机跳舞 共回答了18个问题
耳机跳舞 共回答了18个问题 |采纳率94.4%1:因为澳大利亚被南回归线穿过,深受副热带高气压带控制,所以降水比较少.
2:在澳大利亚西部滨海,由于又受寒流影响,所以降水较少
3:在中部,由于受地形影响,东部是一条很高的山脉,所以中部处在背风坡和分水岭的背面,以至降雨较少,而东部水分较多1年前查看全部
- 氯气的酒精溶液为什么不能使干燥的蓝色石蕊试纸变红又褪色?
 my稻草人1年前1
my稻草人1年前1 -
 hehelanyu 共回答了15个问题
hehelanyu 共回答了15个问题 |采纳率86.7%酒精中有水,与氯气反应生成盐酸和次氯酸,都有酸性,试纸变红,次氯酸有漂白性,可使试纸变白.我觉得1年前查看全部
- 标准状况下,在四个干燥的烧瓶中分别充入标准状况下,在四个干燥的烧瓶中分别充入
标准状况下,在四个干燥的烧瓶中分别充入标准状况下,在四个干燥的烧瓶中分别充入
标准状况下,在四个干燥的烧瓶中分别充入:①纯净的氨气 ②混有1/3体积空气的氯化氢气体 ③纯净的NO2气体 ④混有少量O2的NO2气体,然后各做喷泉实验.实验后,四个烧瓶中溶液的物质的量浓度大小关系是?(假设溶质不扩散) 请说明计算过程
请务必分析每个烧瓶内的变化以及最终结果!
答案是1=2=3>4,无法理解 九月的常春藤1年前3
九月的常春藤1年前3 -
 bluetu 共回答了11个问题
bluetu 共回答了11个问题 |采纳率72.7%① = ② = ③ > ④
①②③都是消耗的气体体积与形成溶液的体积相同;浓度相同.
④消耗的气体体积中只有部分得到溶质(O2 + 4NO2 + 2H2O = 4HNO3)1年前查看全部
- 点燃酒精灯,在火焰上方罩一个冷而且干燥的漏斗,将导气管插入盛有澄清石灰水的烧杯内,观察漏斗内是否有_______出现;澄
点燃酒精灯,在火焰上方罩一个冷而且干燥的漏斗,将导气管插入盛有澄清石灰水的烧杯内,观察漏斗内是否有_______出现;澄清石灰水是否变______.如果上述实验现象均产生,说明酒精中一定含有___元素,可能含有的元素是_______.
 潇潇殿下1年前1
潇潇殿下1年前1 -
 好钢用在枪尖上 共回答了18个问题
好钢用在枪尖上 共回答了18个问题 |采纳率83.3%小液滴
浑浊
氢、炭
氧1年前查看全部
- 质量为8.02 g的铁片,放入1.0 L 0.9 mol•L-1 CuSO4溶液中,一段时间后取出洗净,干燥后称量,质量
质量为8.02 g的铁片,放入1.0 L 0.9 mol•L-1 CuSO4溶液中,一段时间后取出洗净,干燥后称量,质量为8.66
 真水无香yql1年前1
真水无香yql1年前1 -
 littlelove4u 共回答了16个问题
littlelove4u 共回答了16个问题 |采纳率81.3%这个貌似是91年高考化学题,我先把题目补完,不知对否?将8.02g铁片放入1.0L0.90mol/L硫酸铜溶液中,过一段时间取出清洗,干燥后称量,质量变为8.66g.假设溶液的体积无变化,则铜离子浓度变为多少?设消耗的Cu2+的质量是m克F...1年前查看全部
- (2014•南通)七水硫酸镁(MgSO4•7H2O)是一种重要的化工原料,在48.1℃以下的潮湿空气中稳定,在湿热干燥空
(2014•南通)七水硫酸镁(MgSO4•7H2O)是一种重要的化工原料,在48.1℃以下的潮湿空气中稳定,在湿热干燥空气中易失去结晶水,工业上将白云石(主要成分为MgCO3,CaCO3)碳烧成粉,用于制取MgSO4•7H2O,工艺流程如图所示.

(1)煅烧过程中,MgCO3转化为MgO的基本反应类型是______;
(2)写出MgO与H2SO4反应的化学方程式:______;
(3)操作a的名称为______;
(4)将分离后的母液循环利用的目的是______;
(5)干燥得成品时,需要控制的条件是______. syhk571年前1
syhk571年前1 -
 andy_liuyong 共回答了18个问题
andy_liuyong 共回答了18个问题 |采纳率100%解题思路:根据碳酸镁煅烧反应生成氧化镁和二氧化碳进行解答;
根据碳酸镁和硫酸反应生成硫酸镁、水和二氧化碳进行解答;
根据操作a是过滤操作进行解答;(1)碳酸镁煅烧反应生成氧化镁和二氧化碳,属于分解反应;
(2)碳酸镁和硫酸反应生成硫酸镁、水和二氧化碳,化学方程式为:MgO+H2SO4=MgSO4+H2O;
(3)操作a是过滤操作;
(4)结晶后的母液是MgSO4的饱和溶液,循环利用母液可使原料中的镁元素最大可能地转化到产物中,因此将分离后的母液循环利用的目的是提高原料的利用率;
(5)由于七水硫酸镁在湿热干燥空气中易失去结晶水,因此干燥得成品时,需要控制的条件是温度,以防止七水硫酸镁水解;
故答案为:(1)分解反应;(2)MgO+H2SO4=MgSO4+H2O;(3)过滤;(4)提高原料的利用率;(5)温度.点评:
本题考点: 物质的相互转化和制备;过滤的原理、方法及其应用;酸的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了物质分离的实验设计和方法应用,主要是利用硫酸除去杂质,得到较纯净的MgSO4溶液来制备MgSO4•7H2O晶体,同时考查了物质分离方法,题目难度中等.1年前查看全部
- 高中常用干燥剂有哪些?分别适用于哪些物质的干燥?
 -ankey1年前1
-ankey1年前1 -
 流云飞袖1981 共回答了9个问题
流云飞袖1981 共回答了9个问题 |采纳率100%1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分.例如常作为H2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂.
2、无水氯化钙:因其价廉、干燥能力强而被广泛应用.干燥速度快,能再生,脱水温度473K.一般用以填充干燥器和干燥塔,干燥药品和多种气体.不能用来干燥氨、酒精、胺、酰、酮、醛、酯等.
3、无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4.7H2O.吸水作用迅速,效率高,价廉,为一良好干燥剂.常用来干燥有机试剂.
4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质.常用来干燥氢气、氧气和甲烷等气体.
5、变色硅胶:常用来保持仪器、天平的干燥.吸水后变红.失效的硅胶可以经烘干再生后继续使用.可干燥胺、NH3、 O2、 N2等
6、活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K烘烤).
7、无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差.
8、硫酸钙:可以干燥H2 .O2 .CO2 .CO 、N2 .Cl2、HCl 、H2S、 NH3、 CH4等1年前查看全部
- 某化学探究小组称取6g镁铜合金样品于烧杯中,然后将80g稀硫酸分四次加入,充分反映后过滤,洗涤,干燥,称重,得到的实验过
某化学探究小组称取6g镁铜合金样品于烧杯中,然后将80g稀硫酸分四次加入,充分反映后过滤,洗涤,干燥,称重,得到的实验过程中有关物质的用量及质量测定记录如下.
第一次加入稀硫酸的质量 20g
剩余固体的质量4.8g
第二次加入稀硫酸的质量 20g
剩余固体的质量mg
第三次加入稀硫酸的质量 20g
剩余固体的质量2.4g
第四次加入稀硫酸的质量 20g
剩余固体的质量1.8g
问题:
1.上述表格中m的值
2.该合金中Mg的质量分数
3.实验操作结束后的溶液中溶质的化学式
4.所用稀硫酸中溶质的质量分数
5.反映后所得溶液的总质量
希望能有人给出解答过程,不要只给答案,谢谢.
 发骚男人1年前1
发骚男人1年前1 -
 zihuoyanyan 共回答了13个问题
zihuoyanyan 共回答了13个问题 |采纳率100%第四次加入稀硫酸,剩余固体的质量还减小,所以第三次加入稀硫酸,镁还过量,
前后次加入稀硫酸,每次减小0.12克,所以
1.上述表格中m=3.6克
2.该合金中Mg的质量分数=(6-1.8)/6=70%
3.实验操作结束后的溶液中溶质的化学式:MgSO4
Mg + H2SO4 = MgSO4 + H2
24 98
6-4.8=1.2 X
X=4.9g
4.所用稀硫酸中溶质的质量分数=1.2/20=6%
Mg + H2SO4 = MgSO4 + H2
24 120 2
6-1.8=4.2 Y Z
Y=21g
Z=0.35g
5.反映后所得溶液的总质量=4.8+80-0.35=84.45g1年前查看全部
- I.图1是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.
I.图1是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.

(1)如何检验装置A的气密性______.若烧瓶中盛装锌片,分液漏斗中盛装稀硫酸,则:
①实验目的是验证H2的还原性并检验其氧化产物,请选择上述部分仪器(可以重复使用),组装顺序为A→C→______→______→D,D装置的作用是______.
②为使CuO可被H2充分还原,能采取多种措施,试写出其中的一种______.
(2)若烧瓶中盛装Na2O2固体,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,则:
①烧瓶内产生的气体主要有(写化学式)______.
②用产生的气体做氨的催化氧化实验,化学反应方程式为4NH3+502
4NO+6H2O催化剂 .△ 4NH3+502.
4NO+6H2O催化剂 .△
II.①以环已醇制备环已烯,环已烯粗品中含有环已醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环已烯在______层(填上或下),分液后用______(填入编号)洗涤.
a.KMnO4溶液
b.稀H2SO4
c.Na2CO3溶液
②再将环乙烯按图2装置,冷却水从______口进入.蒸馏时要加入生石灰,目的是______. 飞起来的鱼1年前1
飞起来的鱼1年前1 -
 yang_695718 共回答了14个问题
yang_695718 共回答了14个问题 |采纳率92.9%解题思路:I.(1)可利用压强差原理检验气密性,常用方法是注水法或加热法;
①装置A中产生的氢气被浓硫酸干燥后通过灼热的氧化铜,由于氢气具有还原性能将氧化铜还原为铜,通过无水硫酸铜验证水的生成,最后连接装置D是为了防止空气中的水蒸气进入盛有无水硫酸铜的装置B中,可见此实验的目的是验证氢气的还原性和检验氧化产物;
②为使CuO可被H2充分还原,通入气体的流速不能过快,且固体能与气体充分接触;
(2)①过氧化钠与水反应生成氢氧化钠和氧气,反应放热,可促进氨气的挥发;
②氨气和氧气在催化剂的作用下反应生成水和一氧化氮;
II.①环己烯的密度比水小,应在水的上层,除去酸,应用能和酸反应的物质洗涤;
②蒸馏时,冷凝水要下进上出,且用生石灰吸水,以增大蒸馏效果.I.(1)检验气密性时,可将A右端用止水夹夹紧,向分液漏斗中注入少量水,打开分液漏斗活塞,有少许水流下后,液面保持不动,则装置气密性良好,
故答案为:将A右端用止水夹夹紧,向分液漏斗中注入少量水,打开分液漏斗活塞,有少许水流下后,液面保持不动,则装置气密性良好;
①当仪器连接顺序为A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是CuO、无水CuSO4粉末,装置A中产生的氢气被浓硫酸干燥后通过灼热的氧化铜,由于氢气具有还原性能将氧化铜还原为铜,通过无水硫酸铜验证水的生成,最后连接装置D是为了防止空气中的水蒸气进入盛有无水硫酸铜的装置B中,
故答案为:B;B;防止空气中的水蒸气进入,干扰验证;
②为使CuO可被H2充分还原,通入气体的流速不能过快,且固体能与气体充分接触,故答案为:缓慢滴加稀硫酸或用石棉绒包裹CuO粉末;
(2)①氧化钠与水反应生成氢氧化钠和氧气,反应放热,可促进氨气的挥发,则烧瓶内产生的气体主要有O2、NH3,故答案为:O2、NH3;
②氨气和氧气在催化剂的作用下反应生成水和一氧化氮,反应的方程式为4NH3+502
催化剂
.
△4NO+6H2O,故答案为:4NH3+502
催化剂
.
△4NO+6H2O;
II.①环己烯的密度比水小,应在水的上层,除去酸,应用能和酸反应的物质洗涤,只有碳酸钠符合,故答案为:上;c;
②蒸馏时,冷凝水要下进上出,且用生石灰吸水,可增大蒸馏效果,
故答案为:g或下;吸收水分.点评:
本题考点: 实验装置综合;物质的分离、提纯的基本方法选择与应用;气体发生装置;气体的收集.
考点点评: 本题以氨气的催化氧化为载体考查物质制备实验,掌握反应原理,理清装置连接,把握实验气体制备、含有杂质的验证和除杂方法和步骤是解题关键,题目难度中等.1年前查看全部
- 浓硫酸不可用来干燥NH3 显什么性
 ivnana1101年前3
ivnana1101年前3 -
 play272203724 共回答了21个问题
play272203724 共回答了21个问题 |采纳率95.2%因为氨气溶解后是碱性,会与硫酸反应中和.这里浓硫酸当然显酸性了1年前查看全部
- 为什么冬天干燥,夏天潮湿? 我觉得反过来才对,冬天的太阳没夏天的热,水蒸气蒸发也就很慢
 singerp1年前1
singerp1年前1 -
 burningls 共回答了16个问题
burningls 共回答了16个问题 |采纳率93.8%冬天降水少气温低,不利于水分的蒸发,自然就形不成水蒸气,湿度就低.夏季刚好相反.1年前查看全部
- 五月时,空气潮湿,地砖上全是水,怎样使室内保持干燥?是用空调制热还是制冷?
 c_t_x1年前1
c_t_x1年前1 -
 晨光飞舞 共回答了25个问题
晨光飞舞 共回答了25个问题 |采纳率92%冷.冷之后空气水珠凝结,外界受到的蒸发大于室内,压力膨胀原理,室内的会泄出去.1年前查看全部
- 工业上制漂白粉的化学方程式为2Cl2+2Ca(OH)=Ca(ClO)2+CaCl2+2H2O.某干燥样品中有效成分(接下
工业上制漂白粉的化学方程式为2Cl2+2Ca(OH)=Ca(ClO)2+CaCl2+2H2O.某干燥样品中有效成分(接下)
(接上)Ca(ClO)2的质量分数为55%,则生产过程中Ca(OH)2的利用率为? A96.1% B86.4% C77.8% D71.3% 过程? 操之有道1年前1
操之有道1年前1 -
 pandoraeb 共回答了19个问题
pandoraeb 共回答了19个问题 |采纳率100%n(Ca(ClO)2)=55/143=0.3846mol
m(CaCl2)=0.3846*111=42.69g
m(Ca(OH)2)=100-55-42.69=2.3g
m(Ca(OH)2反应)=0.3846*2*74=56.9g
Ca(OH)2%=56.9/(56.9+2.3)=96.1%
A1年前查看全部
- 下列气体中,既可以用浓硫酸干燥,又可以用NaOH固体干燥的是( )
下列气体中,既可以用浓硫酸干燥,又可以用NaOH固体干燥的是( )
A. SO2
B. H2
C. CO2
D. NH3 yfv41年前1
yfv41年前1 -
 vvtx 共回答了23个问题
vvtx 共回答了23个问题 |采纳率82.6%解题思路:本题考查了气体的干燥,应用了两种干燥剂浓硫酸和氢氧化钠固体,要满足:气体不能与干燥剂反应这个条件;浓硫酸不能干燥氨气等溶于水显碱性的气体;氢氧化钠固体不能干燥二氧化碳、二氧化硫、氯化氢等溶于水显酸性的气体.A、二氧化硫可以和氢氧化钠反应生成亚硫酸钠和水,故A错误;
B、氢气既不与浓硫酸反应,也不与氢氧化钠反应,因此可以干燥,故B正确;
C、二氧化碳与能与氢氧化钠反应生成碳酸钠,故C错误;
D、氨气溶于水是氨水,能与浓硫酸反应,故D错误;
故选B.点评:
本题考点: 根据浓硫酸或烧碱的性质确定所能干燥的气体.
考点点评: 本题考查了气体的干燥,经常应用的干燥剂有:氢氧化钠固体、浓硫酸、生石灰和碱石灰等,属于结合课本知识的信息.常用的干燥剂要记牢,而且要掌握干燥剂的性质,了解干燥剂能与哪一类物质反应,能做哪些气体的干燥剂等.1年前查看全部
- 洁净干燥的空气中有没有水分子?
 放风去了1年前3
放风去了1年前3 -
 dybj-a 共回答了19个问题
dybj-a 共回答了19个问题 |采纳率89.5%是空气就有水分子.
洁净干燥的空气是相对来说的,一是洁净度高,二是相对湿度较低,在适宜于人的范围,一般35%~65%.在35%45%这范围都能称之为洁净干燥的空气.1年前查看全部
- 什么浓溶液可同时用于干燥一氧化炭和二氧化炭
 了我1年前1
了我1年前1 -
 wawaxyz 共回答了17个问题
wawaxyz 共回答了17个问题 |采纳率100%浓硫酸1年前查看全部
- 为什么铁钉在水盘子、盐水盘子里的铁锈最多,而在菜油盘、干燥的瓶子里且盖上盖子的器皿里却没有铁锈呢?
为什么铁钉在水盘子、盐水盘子里的铁锈最多,而在菜油盘、干燥的瓶子里且盖上盖子的器皿里却没有铁锈呢?
铁钉在不同的地方生锈情况记录表
时间 第一天 第二天 第三天 第四天
空盘子 无变化 无变化 无变化 有点生锈
水盘子 水变色 有点生锈 铁锈多了 铁锈更多了
菜油盘 无变化 无变化 无变化 无变化
盐水盘子 水变红色 铁钉生锈 铁锈更多了 铁锈很多
干燥的瓶子里且盖上盖子 无变化 无变化 无变化 无变化
回答者需要回答的答案:
我分析的结果: 泡沫爱情801年前1
泡沫爱情801年前1 -
 33901 共回答了24个问题
33901 共回答了24个问题 |采纳率75%在空盘子
与空气发生氧化反应,但是水分比较少,所以速度比较慢
在水盘子
4Fe+6H2O+5O2=4Fe(OH)3,2Fe(OH)3=Fe2O3+3H2O
金属中含有较多的杂质,这些杂质就会和金属形成化学原电池,发生电化学腐蚀,从而将金属氧化生成金属氧化物.铁钉 生锈之后产生的氧化膜稀松更加速了金属氧化,不过如果全部浸泡在水里的话,也不容易生锈,空气少.
菜油盘
油可以隔绝空气,无产生化学反应的条件.
盐水盘子
金属中含有较多的杂质,这些杂质就会和金属形成化学原电池,发生电化学腐蚀,从而将金属氧化生成金属氧化物.而盐水里的离子多,会发生离子反应,铁钉 生锈之后产生的氧化膜稀松更加速了金属氧化.1年前查看全部
- 灰分的干燥基和挥发分的干燥基加起来为什么不能超过100?
 o陆哥李o1年前1
o陆哥李o1年前1 -
 911zc 共回答了15个问题
911zc 共回答了15个问题 |采纳率93.3%因为根据公式 固定碳FCd=100-Ad-Vd1年前查看全部
- 有NaCl和KCl的混合物26.6g,溶于水形成溶液,加入含0.8摩尔硝酸银的溶液200克,充分反应后滤出沉淀,洗涤干燥
有NaCl和KCl的混合物26.6g,溶于水形成溶液,加入含0.8摩尔硝酸银的溶液200克,充分反应后滤出沉淀,洗涤干燥
称其质量为57.4g,求原混合物中NaCll,KCl的物质的量各为多少? 刘tt宇1年前2
刘tt宇1年前2 -
 彝家小妹妹 共回答了10个问题
彝家小妹妹 共回答了10个问题 |采纳率100%NaCl,KCl各有0.2mol.解析如下:
通过AgCl的质量57.4g,可得n(AgCl)=0.4mol,即原混合物中Cl为0.4mol.由于混合物可以写成XCl的形式,所以原混合物总物质的量就是0.4mol.于是我们可以算出该混合物的平均摩尔质量
M=26.6/0.4=66.5g/mol.正巧发现,NaCl和KCl二者摩尔质量的平均数(58.5+74.5)/2=66.5!所以二者物质的量之比就是1:1,各为0.2mol啦!
注:通过平均摩尔质量计算二者比例时,更普适的算法应该是十字交叉,如果楼主不懂,我可以详细解释~
希望对你有所帮助!1年前查看全部
- 关于物理的,有兴趣的过来看看.有5g的干燥的黄土泥沙,倒入一个量筒中,再倒入27.0g清水,黄土与水均匀混合后,配制成了
关于物理的,有兴趣的过来看看.
有5g的干燥的黄土泥沙,倒入一个量筒中,再倒入27.0g清水,黄土与水均匀混合后,配制成了一定密度的泥沙水,求泥沙水的含沙量,(提示:单位要化成kg/m3)
混合成后的量筒的容积示数是:30cm3 zhaoshuwei1年前1
zhaoshuwei1年前1 -
 yanpingjianan 共回答了19个问题
yanpingjianan 共回答了19个问题 |采纳率78.9%泥沙水的含沙量为
0.005kg/(30*10^-6)m^3=166.7kg/m31年前查看全部
- naoh可以吸收ne吗?ar,o2,ch4,co2呢 能否用它干燥这几种气体
 lixiaokeke1年前1
lixiaokeke1年前1 -
 人ww爱HJ 共回答了15个问题
人ww爱HJ 共回答了15个问题 |采纳率93.3%不可以.稀有气体性质稳定,不与naoh反应;ar,o2,ch4可用naoh干燥,但naoh不能干燥co2,因为co2+2NaOH=Na2CO3+H2O1年前查看全部
- 将鸡蛋壳洗净干燥并捣碎后称取10g放在烧杯里然后往烧杯中加入足量的稀盐酸90g充分反应后剩余物
将鸡蛋壳洗净干燥并捣碎后称取10g放在烧杯里然后往烧杯中加入足量的稀盐酸90g充分反应后剩余物
将鸡蛋壳洗净,干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g.充分反应后剩余物为97.14g产生二氧化碳气体多少g? 520hwx1年前1
520hwx1年前1 -
 成都亚明 共回答了28个问题
成都亚明 共回答了28个问题 |采纳率96.4%由题目可知反应物总重量为10+90=100克
反应剩余物为97.14克
可知产生CO2气体为100-97.14=2.86克
由反应方程式CaCO3+2HCl=CaCl2+H2O+CO2
100 44
x 2.86
解得CaCO3重量为6.5克
可知鸡蛋中CaCO3的质量分数为6.5/10*100=65%1年前查看全部
- 一般用浓硫酸干燥什么
 wjm-m1年前1
wjm-m1年前1 -
 zhoujim 共回答了15个问题
zhoujim 共回答了15个问题 |采纳率86.7%干燥(除了氨气)气体中的水蒸汽1年前查看全部
- 1.铁生锈的快慢和盐接触是否有关,为什么 2.铁生锈是一中常见的现象,而我们的发现,放在干燥环境中的铁生锈慢,在潮湿环境
1.铁生锈的快慢和盐接触是否有关,为什么 2.铁生锈是一中常见的现象,而我们的发现,放在干燥环境中的铁生锈慢,在潮湿环境中的铁生锈快.那么铁生锈是否与水分有关呢?请设计一个实验加以验证.第一个问题,是学习辅导,练习组合,科学教科版六年级下册p25页 第二个是p31也得
 ban9z1年前1
ban9z1年前1 -
 cenychen 共回答了21个问题
cenychen 共回答了21个问题 |采纳率90.5%两个问题 1.铁生锈的快慢和盐接触是否有关,为什么 2.铁生锈是一中常见的现象,而我们的发现,放在干燥环境中的铁生锈慢,在潮湿环境中的铁生锈快.那么铁生锈是否与水分有关呢?请设计一个实验加以验证. 第一个问题,是学习辅导,练习组合,科学教科版六年级下册p25页 第二个是p31也得1年前查看全部
- 化学中吸收杂质的溶液或干燥气体的溶液,高中奋斗中...
 asd5568851年前3
asd5568851年前3 -
 moanjoy 共回答了14个问题
moanjoy 共回答了14个问题 |采纳率100%楼主看来真是好学生,能够想到这一点已经不错了,不过你问的问题确实有点超过初中生所能理解的,你可以下课后问下你们的老师或者相关的专业人士进行咨询,在此,祝你学习进步,天天向上哦.如若还不能解决您的问题,可以继续追问,自当尽力帮您解决.1年前查看全部
- 在通常情况下能够共存,并都能用浓硫酸干燥,也能用碱石灰干燥的气体是
在通常情况下能够共存,并都能用浓硫酸干燥,也能用碱石灰干燥的气体是
a.NH3 N2 H2
b.SO2 H2S O2
c.N2 H2 CO
d.HCl Cl2 CO2
为什么啊 虫虫飞飞2000条1年前6
虫虫飞飞2000条1年前6 -
 gracie_wang 共回答了16个问题
gracie_wang 共回答了16个问题 |采纳率87.5%c 因为不反应
浓硫酸可干燥酸性和中性气体,而碱石灰可干燥碱性和中性气体
要二者都可行,只可以是中性气体
a 氨气是碱性
b 二氧化硫是酸性,硫化氢是酸性
d 全是酸性1年前查看全部
- NAOH不能干燥HCL 不是不能干燥气体么
NAOH不能干燥HCL 不是不能干燥气体么
可它不是气体啊 不懂饿..... 芯伶hana1年前6
芯伶hana1年前6 -
 rongrongzhu 共回答了20个问题
rongrongzhu 共回答了20个问题 |采纳率95%NAOH不能干燥HCL
发生酸碱中和反应
HCL标准状态下是气态
我们说的盐酸是HCL的水溶液1年前查看全部
- 菌落干燥与湿润的原因是什么?为何这一标准在四大类微生物识别中占有重要地位?
 1858241291年前3
1858241291年前3 -
 阿羊羊羊 共回答了21个问题
阿羊羊羊 共回答了21个问题 |采纳率100%因为从微观上有些菌落有荚膜层,黏液层,这两层被称为糖被,它是菌在一定营养条件下向胞外分泌的透明胶体物质,致使该菌表面湿润,而干燥的菌落无该结构,相对干燥.
它可以从视觉上直接判断是属于湿润的细菌和酵母菌,还是干燥的霉菌和放线菌.1年前查看全部
- 下列选项中,不属于表面活性剂的功能的是:() (3.00分) A.干燥 B.乳化 C.起泡 D.催化
 bwdktp61年前1
bwdktp61年前1 -
 zengjingya 共回答了18个问题
zengjingya 共回答了18个问题 |采纳率88.9%A1年前查看全部
大家在问
- 1陌上花开缓缓归 作文
- 2Jim的房间看起来真乱啊!(完成译句)
- 3与100mL0.1mol/L(NH4)2SO4溶液中NH4+离子浓度相同的是( )
- 4物理 密度推导题有甲乙两种密度分别为P1,P2的两种金属合成一块密度为P,边长为a的正方体 求合金中两金属的质量要过程
- 54分之3×5+4分之3×2+4分之3×3 递等式 还有(11+11分之9)×11 递等式 可以简便计算
- 6化合物C(C6H12)能使溴水褪色能溶于浓H2SO4,催化加氢生成2-甲基戊烷,被KMnO4氧化后生成两种羧酸.C结够
- 7含有比喻的词语就像 快如闪电这样的成语如字要在第二个
- 8从A组的备选词语中至少选用两个词语,从B组中至少选用一组关联词,写一段关于建筑物或艺术品的话.A
- 9你所在的考场里空气的质量大约是( )(已知空气的密度是1.29kg/m3)
- 10甲桶油比乙桶油多2千克,从甲桶中取出36千克加入到乙桶这时乙桶油的重量是甲的3倍,原来甲重多少千克
- 11求一道概率题的解法三人独立地去破译一份密码,已知各人能译出的概率分别为1/15、1/3、1/4,问三人中至少有一人能译的
- 12Thank you very much的回答,是OK更恰当,还是Fine更恰当,还是That's all right更恰
- 13SO2能够使品红溶液褪色,也能使高锰酸钾溶液和溴水等褪色,原理是否相同
- 142.一个正方体的一角被切去一个长方形,如图(单位:厘米).
- 15“失败乃成功之母”在英文中的地道说法是什么?
