干燥剂与水的放热反应.(1)拿一小包干燥剂用剪刀小心剪开,导入干燥的杯中,一次性滴入几滴室温下的水,观察到的现象是---
 沙场秋点兵12022-10-04 11:39:541条回答
沙场秋点兵12022-10-04 11:39:541条回答(1)拿一小包干燥剂用剪刀小心剪开,导入干燥的杯中,一次性滴入几滴室温下的水,观察到的现象是--------------------.
(2)拿一包干燥剂用剪刀小心剪开,导入干燥的杯中,一次性导入适量的室温下的水(以高出干燥剂1厘米开始尝试)最后能观察到水中冒出大量气泡,甚至沸腾吗?-------------------------------------------------------.
(3)将(2)最后得到的物质静止一小段时间后,取上层澄清液于一容器中,往溶液中加入几滴由紫色卷心菜制成的酸碱指示剂.观察其颜色,试着判断它的pH值-------------------------------------------------------------------.

已提交,审核后显示!提交回复
共1条回复
 xf131259 共回答了20个问题
xf131259 共回答了20个问题 |采纳率90%- 我是高三的化学理科生,希望答案对您有所帮助!
①可以看到白雾,和剧烈反应.因为热气干燥剂里的氧化钙和水剧烈反应,放出大量热,会蒸发一部分水出来,水遇冷凝结.
②中,能观察到大量气泡,因为会发出大量热,所以很有可能会沸腾.
③中,因为氧化钙和水反应生成Ca(OH)2,所以上层清液就是Ca(OH)2溶液,而Ca(OH)2是碱,紫色酸碱指示剂的原理 酸红碱蓝 所以显蓝色.pH值可以用pH试纸或pH测试计来测定.
祝你学习道路上一路顺风! - 1年前
相关推荐
- 月饼中除氧剂的成分在月饼中有很多什么干燥剂除氧剂的,其中有一种除氧剂里面是活性铁粉(我已经验证过了),但它的指示剂就是一
月饼中除氧剂的成分
在月饼中有很多什么干燥剂除氧剂的,其中有一种除氧剂里面是活性铁粉(我已经验证过了),但它的指示剂就是一根线,在氧浓度=0.3%时呈蓝色,我查了书可能是邻二氮菲-亚铁,或者硝基邻二氮菲-亚铁,不知道到底是什么,怎么验证
请问具体是什么,怎么验证
先谢谢了
 mejunwudi1年前1
mejunwudi1年前1 -
 淡蓝色夜14 共回答了13个问题
淡蓝色夜14 共回答了13个问题 |采纳率92.3%这么微量的氧浓度指示剂,想要业余分析其成分,恐怕不容易吧……
何况这两种物质没有多大不同.
看书上怎么说就是了.1年前查看全部
- 浓硫酸作气体的干燥剂,只能干燥与它反映的气体,为什么不能干燥氨气
 风铃之旅1年前1
风铃之旅1年前1 -
 hasu_hasu 共回答了16个问题
hasu_hasu 共回答了16个问题 |采纳率87.5%氨气是碱性气体.两者会发生反应1年前查看全部
- “CaCl2 最容易朝解,所以常用作干燥剂”这句话是对还是错,为什么
 shijunxiang1年前2
shijunxiang1年前2 -
 martin07 共回答了9个问题
martin07 共回答了9个问题 |采纳率100%错 因为吸水后生成结晶体 且吸水能力强 所以被选做干燥剂1年前查看全部
- 下列物质的用途由化学性质决定的是氢氧化钙用于图墙浓硫酸用做干燥剂
下列物质的用途由化学性质决定的是氢氧化钙用于图墙浓硫酸用做干燥剂
氢氧化钙用于图墙这是什么性质 上海乖囡囡1年前1
上海乖囡囡1年前1 -
 儒雅林枫 共回答了23个问题
儒雅林枫 共回答了23个问题 |采纳率100%遇到CO2,就转化成CaCO31年前查看全部
- 选择双锥回转真空干燥机的干燥剂来干燥液态有机化合物应注意哪几点?
 maggiesp1年前1
maggiesp1年前1 -
 灰色的思念 共回答了18个问题
灰色的思念 共回答了18个问题 |采纳率100%这个要看看有机化合物是否是正品
据我所知太仓展日搪瓷干燥就是做这个的,
能被媒体采访的应该品质不会差1年前查看全部
- 初二化学,哪些物质可做气体的吸附剂(包括干燥剂吗?还是不同的概念?),分别能吸附什么?
初二化学,哪些物质可做气体的吸附剂(包括干燥剂吗?还是不同的概念?),分别能吸附什么?
初中阶段的尽量完整一些。 556620021年前3
556620021年前3 -
 慰藉美丽 共回答了18个问题
慰藉美丽 共回答了18个问题 |采纳率94.4%干燥剂吸收的是水蒸气,碱石灰可以吸收二氧化碳和水蒸气1年前查看全部
- 食品公司通常在“XX雪饼”的包装袋内放入一小包干燥剂,其上面的部分文字见图,请仔细阅读,回答问题:
食品公司通常在“XX雪饼”的包装袋内放入一小包干燥剂,其上面的部分文字见图,请仔细阅读,回答问题:

(1)写出这包干燥剂吸收水分的反应的化学方程式.
(2)“请勿食用”是因为干燥剂吸水后具有什么样的性质? 戏王之王KEN1年前1
戏王之王KEN1年前1 -
 xinzimin 共回答了23个问题
xinzimin 共回答了23个问题 |采纳率82.6%解题思路:根据标签内容可知此干燥剂为生石灰,可与水反应生成氢氧化钙,氢氧化钙具有腐蚀性.(1)这包干燥剂吸收水分是氧化钙和水反应生成氢氧化钙,该反应的方程式为:CaO+H2O=Ca(OH)2;
(2)因为干燥剂的主要成份是生石灰,吸收水分后生成氢氧化钙,氢氧化钙属于强碱,对皮肤、织物、器皿等物质有腐蚀作用.
故答案为:(1)CaO+H2O=Ca(OH)2;
(2)氢氧化钙属于强碱,对皮肤、织物、器皿等物质有腐蚀作用.点评:
本题考点: 生石灰的性质与用途;常见碱的特性和用途;标签上标示的物质成分及其含量.
考点点评: 本题主要考查学生对氧化钙和氢氧化钙的性质的认识,了解一些常见的干燥剂.注重基础知识的考查.1年前查看全部
- 生石灰干燥剂撒入眼睛为什么会导致眼睛失明
 流浪炫篮1年前2
流浪炫篮1年前2 -
 wangbin11 共回答了26个问题
wangbin11 共回答了26个问题 |采纳率96.2%1,生石灰与到水会放出大量热,因为眼里有水
2,生石灰与水反应产生的氢氧化钙具有强腐蚀性..1年前查看全部
- 干燥剂的酸性,碱性,中性 的区别?
 刘懿德1年前2
刘懿德1年前2 -
 zxj444 共回答了15个问题
zxj444 共回答了15个问题 |采纳率100%用途不同!
1.酸性干燥剂用于干燥酸性,中性气体(如氯化氢,氟化氢,甲烷,氢气,氧气,氯气,氮气,二氧化碳,二氧化硫等等):
常见酸性干燥剂:浓硫酸,五氧化二磷,浓磷酸,硅胶(硅酸)
注意:浓硫酸不能干燥还原性气体(即使这些气体是酸性的,如:硫化氢,硒化氢,碘化氢,溴化氢等等);另外硅胶不能干燥氟化氢(生成四氟化硅)
2.碱性干燥剂用于干燥碱性中性气体:(如氨气,氢气,甲烷,甲烷,氢气,氧气,氯气,氮气)亻不能干燥酸性气体(生成盐而使其吸收)
常见碱性干燥剂:氢氧化钾,氢氧化钠,生石灰,碱石灰等
3.中性干燥剂适用于大多数气体干燥(如:无水硫酸镁,无水氯化钙,无水硫酸铜,无水高氯酸镁等等)1年前查看全部
- (2002•南京)一些食品包装袋中常用氧化钙做干燥剂,氧化钙属于( )
(2002•南京)一些食品包装袋中常用氧化钙做干燥剂,氧化钙属于( )
A.酸
B.碱
C.盐
D.氧化物 曾经拥有20001年前1
曾经拥有20001年前1 -
 学好ANSYS 共回答了20个问题
学好ANSYS 共回答了20个问题 |采纳率85%解题思路:根据氧化钙的组成元素及物质的分类中的有关概念来分析解答.A、酸是指在水中电离产生的阳离子全部为H+的化合物,酸中一般没有金属元素,则氧化钙不属于酸,故A错误;
B、碱是由金属阳离子和氢氧根离子形成的,而氧化钙中没有H元素,则不属于碱,故B错误;
C、盐是由金属离子和酸根离子形成的,而氧化钙中不含有酸根,则不属于盐,故C错误;
D、氧化物是指只有两种元素组成且含有氧元素,而氧化钙符合,则属于氧化物,故D正确;
故选D.点评:
本题考点: 物质的简单分类;从组成上识别氧化物;氧化物、酸、碱和盐的概念.
考点点评: 本题考查物质的类别的判断,学生应熟悉根据物质的组成和性质进行的分类,并熟悉酸、碱、盐的重要性质及在水中产生的离子.1年前查看全部
- (2008•金山区二模)小强同学在某食品包装袋内,发现一个装有白色颗粒状固体的小纸袋,上面写着“生石灰干燥剂,请勿食用”
(2008•金山区二模)小强同学在某食品包装袋内,发现一个装有白色颗粒状固体的小纸袋,上面写着“生石灰干燥剂,请勿食用”.小强同学随手将小纸袋拿出来放在空气中.几天后,小强同学对纸袋内的固体进行探究:
(1)取少量的块状固体放入盛有足量水的烧杯中,搅拌、静置、过滤得到少量白色固体C.你认为该白色固体C可能的组成有______.
猜测的依据是(用化学方程式表示)______.
(2)请你设计实验证明你的猜测(填写下表):
实验步骤 现象和结论 ______ ______ ______ ______  cabhe1年前1
cabhe1年前1 -
 没有爱情的鱼 共回答了25个问题
没有爱情的鱼 共回答了25个问题 |采纳率88%解题思路:(1)由生石灰的化学性质可知,CaO放置在空气中易吸收水分,变为Ca(OH)2,并能与空气中的二氧化碳发生反应,因此块状固体可能含有的成份就有Ca(OH)2或CaCO3或Ca(OH)2或CaCO3的混合物.
(2)根据物质的性质进行验证,检验熟石灰可用酚酞试液,检验碳酸钙可用稀盐酸.(1)生石灰放置在空气中易吸收水分,变为Ca(OH)2,并能吸收空气中的二氧化碳,反应生成CaCO3,因此块状固体可能含有的成份就有Ca(OH)2或CaCO3或Ca(OH)2和CaCO3的混合物.
故答案为:(1)Ca(OH)2或Ca(OH)2和CaCO3或CaCO3;CaO+H2O═Ca(OH)2;CO2+Ca(OH)2═CaCO3↓+H2O;
(2)根据猜想中物质的性质来设计实验,氢氧化钙溶液呈碱性,能使无色酚酞变红,碳酸钙不溶于水,和盐酸反应能生成二氧化碳气体;故答案为:
实验步骤 现象和结论
取样,溶解于水,取清液,加入酚酞;
样品中再加入稀盐酸. 酚酞变红,有Ca(OH)2
有气泡产生,则有Ca(OH)2和CaCO3
取样,加水,再加入酚酞;
样品中再加入稀盐酸. 酚酞不变红,但有气泡产生,则只有CaCO3点评:
本题考点: 食品干燥剂、保鲜剂和真空包装的成分探究;猜想与事实验证;书写化学方程式、文字表达式、电离方程式.
考点点评: 生石灰的主要成分是氧化钙,氧化钙极易吸收水分变成氢氧化钙,氢氧化钙吸收二氧化碳生成碳酸钙.氢氧化钙的溶液呈碱性,能使酚酞试液变红,碳酸钙与盐酸反应生成是澄清石灰水变浑浊的二氧化碳.1年前查看全部
- 磷在空气中燃烧生成的氧化物通常可作强干燥剂.已知在标准状况下,32克氧气的体积是22.4升,
磷在空气中燃烧生成的氧化物通常可作强干燥剂.已知在标准状况下,32克氧气的体积是22.4升,
在该条件下制备71克这种干燥剂所消耗的空气的体积约为多少升? jickidd1年前2
jickidd1年前2 -
 我家的小绵羊 共回答了17个问题
我家的小绵羊 共回答了17个问题 |采纳率94.1%首先要确定的是P在空气中燃烧生成的是 P2O5
即 4P + 5O2 ==== 2P2O5
物质的量之比味 4:5:2
应为M(P)=32 所以M(P2O5)=142
71g 即为0.5mol
所以由 5O2~2P2O5
推出需要消耗的氧气为1.25mol 即(1.25*22.4)L=28L
又因为空载中含O2为1/5 所以需要空气为140L
由于是在电脑上.所以无法摆出正确的格式,请楼主见谅1年前查看全部
- 验证CH4在空气中燃烧的产物,为什么要先通入干燥剂中?
验证CH4在空气中燃烧的产物,为什么要先通入干燥剂中?
CH4与氧气完全燃烧后,为了验证沼气燃烧后的产物,将生成物通入无水硫酸铜和澄清石灰水中.
为什么要先通入无水硫酸铜后通入石灰水中?
生成的CO2应该和石灰水反应生成水,所以不应该后通过无水硫酸铜吗? junxiao1101年前1
junxiao1101年前1 -
 一只H蝴蝶 共回答了18个问题
一只H蝴蝶 共回答了18个问题 |采纳率77.8%CH4燃烧产物是CO2和H2O
我们要检验这两个的存在
首先必须检验H2O,如果先CO2进入澄清石灰石的话,因为溶液中出来的气体都会带水汽出来,那么无水硫酸铜检验不出来是不是CH4燃烧产生了H2O,还是水汽.1年前查看全部
- 月饼干燥剂的成分是?为防止月饼等富含油脂的食品氧化变质,常在包装袋中放入生石灰 为什么?
 鸡蛋花881年前1
鸡蛋花881年前1 -
 gymz504 共回答了30个问题
gymz504 共回答了30个问题 |采纳率93.3%CaO1年前查看全部
- 食品吸潮和吸氧后容易变质,为了延长食品保质期.通常在包装袋中加入1小包干燥剂.某化学兴趣小组经过查阅资料,发现常见的食品
食品吸潮和吸氧后容易变质,为了延长食品保质期.通常在包装袋中加入1小包干燥剂.某化学兴趣小组经过查阅资料,发现常见的食品干燥剂主要有’两种:一种是以生石灰为主要成份的千燥剂(简称A类,下同);另一种是以硅胶为主要成份的干燥剂(简称B类,下同).请问答下列问题:
(1)将装有A类干燥剂的小纸袋打开露置于潮湿的空气中,发现纸袋发热,与出其发生反应的化学方程式______.
(2)B类干燥剂中硅胶的主要成分为SiO2•nH2O.SiO2是______(填“酸”、“碱”、“盐”、“氧化物”),其中Si的化合价为______.
(3)小组在杳阅资料中,还发现了-种新型的食品干燥剂:泡沫铁粉(铁粉包裹在泡沫塑料中).当它露置于潮湿的空气中,很快变成铁锈(主要成分为Fe2O3•nH2O),并有发热现象,说明化学反应除了生成新物质外,还伴随着______变化.与A类干燥剂比较,泡沫铁粉除了做干燥剂外,还可做______剂. 水……seaman1年前1
水……seaman1年前1 -
 虫子-虫子 共回答了16个问题
虫子-虫子 共回答了16个问题 |采纳率93.8%解题思路:氧化钙能和水反应生成氢氧化钙,根据物质的元素组成可以判断物质的类别,根据化合物中元素化合价代数和为零的原则可以求出某种元素的化合价.(1)氧化钙和水反应能生成氢氧化钙,故填:CaO+H2O=Ca(OH)2.(2)二氧化硅是由硅元素和氧元素组成的化合物,属于氧化物.故填:氧化物.二氧化硅中氧元素的化合价是-2价,可以求出硅元素的化合价是+4价.故填:+...
点评:
本题考点: 水的性质和应用;从组成上识别氧化物;有关元素化合价的计算;物质发生化学变化时的能量变化.
考点点评: 本题主要考查了化学方程式的书写、化合价的求法及其干燥剂与水或与水和氧气反应等方面的内容,可以依据已有的知识进行.1年前查看全部
- 某些食品袋中有干燥剂,主要成分是生石灰,在空气中放置一段时间后,干燥剂中的成分有哪些?请分情况解答,并写出有关反应的化学
某些食品袋中有干燥剂,主要成分是生石灰,在空气中放置一段时间后,干燥剂中的成分有哪些?请分情况解答,并写出有关反应的化学方程式.
 26shuiyin1年前2
26shuiyin1年前2 -
 听风化雨 共回答了26个问题
听风化雨 共回答了26个问题 |采纳率84.6%初中化学方程式汇总
一、 氧气的性质:
(1)单质与氧气的反应:(化合反应)
1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO
2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O4
3. 铜在空气中受热:2Cu + O2 加热 2CuO
4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O3
5. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O
6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 点燃 2P2O5
7. 硫粉在空气中燃烧: S + O2 点燃 SO2
8. 碳在氧气中充分燃烧:C + O2 点燃 CO2
9. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO
(2)化合物与氧气的反应:
10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO2
11. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O
12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O
(3)氧气的来源:
13.玻义耳研究空气的成分实验 2HgO 加热 Hg+ O2 ↑
14.加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)
15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 MnO22H2O+ O2 ↑(实验室制氧气原理2)
二、自然界中的水:
16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+ O2 ↑
17.生石灰溶于水:CaO + H2O == Ca(OH)2
18.二氧化碳可溶于水: H2O + CO2==H2CO3
三、质量守恒定律:
19.镁在空气中燃烧:2Mg + O2 点燃 2MgO
20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu
21.氢气还原氧化铜:H2 + CuO 加热 Cu + H2O
22. 镁还原氧化铜:Mg + CuO 加热 Cu + MgO
四、碳和碳的氧化物:
(1)碳的化学性质
23. 碳在氧气中充分燃烧:C + O2 点燃 CO2
24.木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑
25. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe + 3CO2↑
(2)煤炉中发生的三个反应:(几个化合反应)
26.煤炉的底层:C + O2 点燃 CO2
27.煤炉的中层:CO2 + C 高温 2CO
28.煤炉的上部蓝色火焰的产生:2CO + O2 点燃 2CO2
(3)二氧化碳的制法与性质:
29.大理石与稀盐酸反应(实验室制二氧化碳):
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
30.碳酸不稳定而分H2CO3 == H2O + CO2↑
31.二氧化碳可溶于水: H2O + CO2== H2CO3
32.高温煅烧石灰石(工业制二氧化碳):CaCO3 高温 CaO + CO2↑
33.石灰水与二氧化碳反应(鉴别二氧化碳):
Ca(OH)2 + CO2 === CaCO3 ↓+ H2O
(4)一氧化碳的性质:
34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO2
35.一氧化碳的可燃性:2CO + O2 点燃 2CO2
其它反应:
36.碳酸钠与稀盐酸反应(灭火器的原理):
Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
五、燃料及其利用:
37.甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O
38.酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O
39. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O
六、金属
(1)金属与氧气反应:
40. 镁在空气中燃烧:2Mg + O2 点燃 2MgO
41. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O4
42. 铜在空气中受热:2Cu + O2 加热 2CuO
43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3
(2)金属单质 + 酸 -------- 盐 + 氢气 (置换反应)
44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑
45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑
46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑
47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑
48. 锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑
49. 铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑
50. 镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑
51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑
(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐
52. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu
53. 锌和硫酸铜溶液反应:Zn + CuSO4 ==ZnSO4 + Cu
54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 == Cu(NO3)2 + Hg
(3)金属铁的治炼原理:
55.3CO+ 2Fe2O3 高温 4Fe + 3CO2↑
七、酸、碱、盐
1、酸的化学性质
(1)酸 + 金属 -------- 盐 + 氢气(见上)
(2)酸 + 金属氧化物-------- 盐 + 水
56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl ==2FeCl3 + 3H2O
57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O
58. 氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl2 + H2O
59. 氧化铜和稀硫酸反应:CuO + H2SO4 == CuSO4 + H2O
(3)酸 + 碱 -------- 盐 + 水(中和反应)
60.盐酸和烧碱起反应:HCl + NaOH == NaCl +H2O
61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 == CaCl2 + 2H2O
62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 == AlCl3 + 3H2O
63. 硫酸和烧碱反应:H2SO4 + 2NaOH == Na2SO4 + 2H2O
(4)酸 + 盐 -------- 另一种酸 + 另一种盐
64.大理石与稀盐酸反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑
67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl
2、碱的化学性质
(1) 碱 + 非金属氧化物 -------- 盐 + 水
68.苛性钠暴露在空气中变质:2NaOH + CO2 == Na2CO3 + H2O
69.苛性钠吸收二氧化硫气体:2NaOH + SO2 == Na2SO3 + H2O
70.苛性钠吸收三氧化硫气体:2NaOH + SO3 == Na2SO4 + H2O
71.消石灰放在空气中变质:Ca(OH)2 + CO2 == CaCO3 ↓+ H2O
72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 == CaSO3 ↓+ H2O
(2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)
(3)碱 + 盐 -------- 另一种碱 + 另一种盐
73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH
3、盐的化学性质
(1)盐(溶液) + 金属单质------- 另一种金属 + 另一种盐
74. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu
(2)盐 + 酸-------- 另一种酸 + 另一种盐
75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑
(3)盐 + 碱 -------- 另一种碱 + 另一种盐
76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH
(4)盐 + 盐 ----- 两种新盐
77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 == AgCl↓ + NaNO3
78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl1年前查看全部
- 碳酸钠用作干燥剂有什么好处有做保护剂作用的吗
 keyiko1年前2
keyiko1年前2 -
 何必你妹还好吗 共回答了26个问题
何必你妹还好吗 共回答了26个问题 |采纳率92.3%碳酸钠当然可以吸收,有机实验室里很常用的吸水试剂.比如你从水溶液中用有机溶剂萃取了产物,这样有机溶剂溶剂就要用碳酸钠来除水,然后旋蒸掉溶剂得到纯的产物.除了碳酸钠,硫酸镁也是常用的除水试剂.
保护剂啊,你说保护什么,有机化学上是没有.食品工业上就不知道了1年前查看全部
- 在浓硫酸、石墨、活性炭、纯碱等物质中,工业常用来净化某些气体和液体的是____,可用来作干燥剂的是_____.
 limi721年前1
limi721年前1 -
 袁蛟 共回答了21个问题
袁蛟 共回答了21个问题 |采纳率85.7%活性炭可以用来净化
浓硫酸和活性炭都可以用来做干燥剂1年前查看全部
- 为什么酸性干燥剂是干燥酸性气体、不干燥碱性气体,碱性干燥剂是干燥碱性气体,不干燥酸性气体?
为什么酸性干燥剂是干燥酸性气体、不干燥碱性气体,碱性干燥剂是干燥碱性气体,不干燥酸性气体?
不包括中性气体 火中雨歇1年前3
火中雨歇1年前3 -
 9113318 共回答了25个问题
9113318 共回答了25个问题 |采纳率84%酸性干燥剂干燥氨气等碱性气体会发生酸碱反应.反之同理.1年前查看全部
- 淑平同学在我市某食品厂生产的盒装饼干中,发现盒内有一小包东西,其上标有“干燥剂”主要成分生石灰,
淑平同学在我市某食品厂生产的盒装饼干中,发现盒内有一小包东西,其上标有“干燥剂”主要成分生石灰,
“请勿使用”等字样.为了提高自己的实验探究能力,淑平决定对这包干燥剂展开实验.
(1)她将这包干燥剂全部倒入一定量的水中,充分搅拌后,触摸杯壁,感觉有点热,将其过滤,得到白色沉淀物和滤液.
(2)联系到空气中成分和氧化钙的性质,她对白色沉淀物的组成提出了一下假设:
假设1:是氧化钙和碳酸钙的混合物
假设2:是氢氧化钙和碳酸钙的混合物
假设3:只有碳酸钙
假设4:只有氢氧化钙
其中假设______不合理,用化学方程式说明原因.
为什么是假设一不正确呢?解析一下
 睫毛上的钻石1年前1
睫毛上的钻石1年前1 -
 chriswu1979 共回答了17个问题
chriswu1979 共回答了17个问题 |采纳率88.2%是氯化钙和其他混合物1年前查看全部
- 铁做干燥剂的反应方程式
 风JJ毛不动1年前5
风JJ毛不动1年前5 -
 niea 共回答了23个问题
niea 共回答了23个问题 |采纳率73.9%2Fe + O2 + 2H2O 4Fe(OH)3
2Fe(OH)3=Fe2O3 +3H20
铁生锈反应很复杂,利用铁生锈可以做双吸剂,吸水和氧气.1年前查看全部
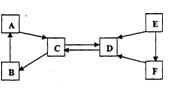
- 现有A-F六种常见物质,其中B是食品包装中常用的干燥剂,A、B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、
现有A-F六种常见物质,其中B是食品包装中常用的干燥剂,A、B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素.它们的转化关系如下图所示.请回答:
(1)下列物质的化学式为A ,B ,E ;
(2)下列转化的化学方程式为A→C:;
F→D:.
 爱上你是我的错1年前1
爱上你是我的错1年前1 -
 晴朗心1973 共回答了15个问题
晴朗心1973 共回答了15个问题 |采纳率93.3%A Ca(OH)2 B CaO C CaCO3 D CO2 E C F CO
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
2CO+O2=点燃=2CO21年前查看全部
- 气体干燥问题 下列常用的干燥剂中,不能用来干燥氯气的是A.浓硫酸 B.无水氯化钙 C.碱石灰 D.磷酸酐(P2O5)
 skel1年前6
skel1年前6 -
 罗基野山猫 共回答了18个问题
罗基野山猫 共回答了18个问题 |采纳率94.4%生石灰:CaO 遇水生成氢氧化钙 而氯气会和氢氧化钙反应,这个问题也好理解,在教材上高一第四章介绍的!就是用氯气和石灰乳反应来制漂白粉.没有水反应不容易进行,但是有水的话反应就可以进行,因此不能用生石灰、熟石灰或是碱石灰来进行干燥1年前查看全部
- 请问一道关于酸碱盐的化学题:碱石灰是化学实验室常用的干燥剂.其制法如下:在氢氧化钠溶液中加入氧化钙粉末搅拌,在90℃的烘
请问一道关于酸碱盐的化学题:
碱石灰是化学实验室常用的干燥剂.其制法如下:在氢氧化钠溶液中加入氧化钙粉末搅拌,在90℃的烘干箱中干燥30分钟左右,所得的白色固体就是碱石灰.
相关资料:氢氧化钙在250℃以下不分解;氢氧化钠在580℃以下不分解.
某学习小组在老师的指导下欲探究碱石灰的成分.请参与他们的探究.
(1)提出猜想:该碱石灰的成分可能是如下几种情况.
①氢氧化钠、氧化钙; ②氢氧化钠、氢氧化钙;③氢氧化钠、氢氧化钙、水;
④氢氧化钠、氢氧化钙、氧化钙;⑤氢氧化钠、氢氧化钙、氧化钙、水.
以上猜想中,不需要通过实验就能排除的是( ) ,
理由是 ( ).
(2)设计实验:
①称取4.0g碱石灰样品;②在250度时,加热至恒重,测质量减轻了0.6g;
③将剩余物在580度时加热至恒重,测质量又减轻0.7g.
(3)得出结论:该碱石灰的实际成分是( )
(4)应用:有些气体不能用碱石灰干燥,请列举两种:
( ) 、 ( ) qq冰季1年前1
qq冰季1年前1 -
 仁辛人爱 共回答了19个问题
仁辛人爱 共回答了19个问题 |采纳率84.2%答:5,因为水和氧化钙不共存.
250度时减轻重量可以由下面方程式解释
Ca(OH)2Na2O+H2O
Y 0.7g
Y=3.1g
X+Y=5.6g大于4.0克,说明在250度时减少的水不全都是氢氧化钙分解产生的,在碱石灰样品中本身就含有水,所以实际成分是;③氢氧化钠、氢氧化钙、水
酸性气体不可以,比如HCl,二氧化碳,二氧化硫等等1年前查看全部
- 为加快漂白粉的作用,最好办法是:A,加入烧碱溶液.B,用水湿润.C,加稀盐酸.D,加干燥剂
为加快漂白粉的作用,最好办法是:A,加入烧碱溶液.B,用水湿润.C,加稀盐酸.D,加干燥剂
我不太明白啊... superman_0081年前5
superman_0081年前5 -
 n_hao 共回答了26个问题
n_hao 共回答了26个问题 |采纳率96.2%C,加稀盐酸
Ca(ClO)2+2HCl=CaCl2+2HClO
生成HClO,发挥漂泊作用1年前查看全部
- 能不能用干燥剂制取氢氧化钙有个同学买了零食后玩干燥剂,泡水,结果把另一个同学烫了一下(不是很严重),我当天就要了他带的所
能不能用干燥剂制取氢氧化钙
有个同学买了零食后玩干燥剂,泡水,结果把另一个同学烫了一下(不是很严重),我当天就要了他带的所有的干燥剂.
整个过程用的水都是自来水(我对结果要求不大)
干燥剂是零食里带的,上面写了主要成分氧化钙,我用了好几包.
把袋子打开后放水瓶里,水有点热,并且看起来有点像牛奶.(有同学被这个反应烫到手过)
然后静置,分为2层,上面的比较澄清(还是很混浊),下面的是白色的,摇晃的时候发现有很多杂质.
把上面比较澄清的溶液过滤(自己用水瓶剪的漏斗,滤纸用卫生纸代替),得到澄清的溶液.
每次过滤后,把反应用的水瓶里加水,静置沉淀后重复上面的步骤.
我现在已经做了这些,都弄了一大瓶了.
接下来我想把这些溶液蒸发,希望可以得到氢氧化钙固体,不过考虑到氢氧化钙的溶解度很低,估计用1升溶液只能得到十几克.
现在的问题是,这样得到的溶液能不能蒸发得到氢氧化钙固体?还有,如果能,怎么收集得到的固体?
现在没什么分,下次再提高悬赏. 5648465541年前1
5648465541年前1 -
 小Magic 共回答了16个问题
小Magic 共回答了16个问题 |采纳率93.8%可以得到氢氧化钙固体.cao+2H2O=ca(HO)2.反应后的糊状物都是氢氧化钙,因为干燥剂不是纯的氧化钙,反应后沉淀物氢氧化钙含有少量杂质.澄清的氢氧化钙水溶液经蒸发后所得氢氧化钙比较纯净.1年前查看全部
- A、B、C、D、E、F、b均为初中常见他物质,其转化关系如图所示(条件略去),已知D、b为单质,B是一种常见他干燥剂.
A、B、C、D、E、F、b均为初中常见他物质,其转化关系如图所示(条件略去),已知D、b为单质,B是一种常见他干燥剂.

(四)写出B物质他化学式:______;
(2)写出C物质他一种常见用途:______;
(的)写出E和赤铁矿反应生成C和b他化学方程式:的CO+Fe2O的
2Fe+的CO2高温 .的CO+Fe2O的;该反应在工业上他用途:______.
2Fe+的CO2高温 . 徐道婧1年前1
徐道婧1年前1 -
 wdx21cn 共回答了21个问题
wdx21cn 共回答了21个问题 |采纳率95.2%解题思路:根据B是一种常见的干燥剂,B又是A分解生成的,所以B是氧化钙,A是碳酸钙,C就是二氧化碳,D为单质,和二氧化碳反应生成的E和氧化铁会生成单质G和二氧化碳,可以判断D就是碳,E就是一氧化碳,然后结合题中的转化关系,推导剩余的物质,最后代入转化图中验证即可.(1)B是他种常见的干燥剂,B又是A分解生成的,所以B是氧化钙,A是碳酸钙,C就是二氧化碳,D为单质,和二氧化碳反应生成的E和氧化铁会生成单质G和二氧化碳,根据质量守恒定律可知,G就是铁,然后可以判断D就是碳,E就是他氧化碳,他氧化碳和氧化铁反应生成铁和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应又会生成碳酸钙,推出的各种物质经过检验,所有的转化关系都是合理的,所以推导正确,B物质的化学式是:CaO;
(2)二氧化碳具有密度比空气大,不能支持燃烧,本身也不燃烧的性质,可以用来灭火;
(1)他氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,化学方程式为:1CO+Fe2O1
高温
.
2Fe+1CO2;
该反应是利用还原剂将金属从其氧化物中还原出来,经常用来冶炼金属;
故答案为:(1)CaO;
(2)灭火;
(1)1CO+Fe2O1
高温
.
2Fe+1CO2;冶炼金属.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.1年前查看全部
- 氯化钙、硅胶、五氧化二磷做干燥剂时,发生的反应是什么?
 qnly1111年前3
qnly1111年前3 -
 firefly14 共回答了19个问题
firefly14 共回答了19个问题 |采纳率89.5%CaCl2+2H2O===CaCl2·2H2O氯化钙是中性干燥剂,能干燥除氨气以外的任何气体 硅胶做干燥剂不是化学变化,是物理吸附.硅胶为酸性干燥剂,可以干燥酸性气体或中性气体.P2O5+3H2O===2H3PO4 五氧化二磷是酸性干燥剂,可以干燥酸性气体或中性气体.查看原帖1年前查看全部
- ①碱石灰是实验室常用的干燥剂,它是氧化钙、氢氧化钠的固体混合物. 除了能吸收水蒸气外,碱石灰还能吸收常见的气体是 ___
①碱石灰是实验室常用的干燥剂,它是氧化钙、氢氧化钠的固体混合物. 除了能吸收水蒸气外,碱石灰还能吸收常见的气体是 _______ (选填编号,只有一个答案,多选不得分).
A.氧气 B.一氧化碳 C.二氧化碳 D.氢气
②实验室中利用草酸亚铁晶体(FeC 2 O 4 ·2H 2 O)受热分解得到一定量的 CO,反应的方程式 为:FeC 2 O 4 ·2H 2 O→铁的氧化物+CO+CO 2 +2H 2 O该反应属于 ______ (填写基本反应类型),根据质量守恒定律,可以推知产物中“铁的氧化物”的化学式是 _______
③加热草酸亚铁可选用下列“A、B、C”三套装置中的 ______ (选填编号“A、B、C”).写出下列仪器“a”的名称是 ______ .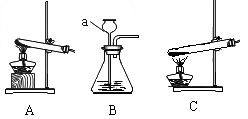
④草酸亚铁晶体的摩尔质量是 _________ (写全单位),若有1.8g 草酸亚铁晶体充分反应可得 到CO气体的物质的量是多少?请写出计算过程:
⑤草酸亚铁晶体受热分解得到的气体通过碱石灰后,用来与氧化铜反应,并检验反应得到的气体产物.整套装置如图:
写出“乙”处 反应的 现象是 ___________ ,反应的 化学方程式 为 _____________ ,该反应中还原剂是. 甲、丙两处所盛放的试液分别是 ___________ 、 _________ ,其中“甲”处所盛放该试液的作用是 ___________________ .  代代12号1年前1
代代12号1年前1 -
 精彩哥 共回答了18个问题
精彩哥 共回答了18个问题 |采纳率88.9%①C ②分解反应;FeO ③A;长颈漏斗 ④180克/摩尔;设1.8g 草酸亚铁晶体充分反应可得到CO气体的质量为x: FeC 2 O 4 ·2H 2 O FeO+CO↑+CO 2 ↑+2H 2 O 180...1年前查看全部
- 某化合物的浓溶液有强烈的腐蚀性,实验室中常用作气体的干燥剂,其稀溶液X具有如下转化关系.
某化合物的浓溶液有强烈的腐蚀性,实验室中常用作气体的干燥剂,其稀溶液x具有如下转化关系.
a、b、c、d、e、f、g、m、n都是初中常见的化学物质.已知:b、c、f都是氧化物,通常状况下它们分别是***液体、***气体和黑色粉末状固体;g是通常状况下密度最小的气体.(图中部分反应物、生成物已略去).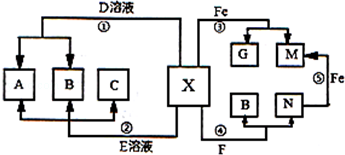
请回答下列问题:
(1)写出化学式:g ,x ;
(2)写出化学反应的类型:反应⑤ ;
(3)写出符合题意的化学方程式:
反应② ;
反应③ ;
反应④ .
(4)简答x的浓溶液稀释成稀溶液的操作方法: . shuanghuipc1年前1
shuanghuipc1年前1 -
 wusagi22 共回答了20个问题
wusagi22 共回答了20个问题 |采纳率90%(1)H 2 ;H 2 SO 4 (2)置换反应(3)H 2 SO 4 +Na 2 CO 3 ═Na 2 SO 4 +CO 2 ↑+H 2 O(其他合理答案也可);H 2 SO 4 +Fe═FeSO 4 +H 2 ↑;H 2 SO 4 +CuO═CuSO 4 +H 2 O(4)向水中缓缓加入浓硫酸,并用玻璃棒不断搅拌
1年前查看全部
- 熟石灰能作为干燥剂吗
 linda_62201年前4
linda_62201年前4 -
 水蓝湖 共回答了19个问题
水蓝湖 共回答了19个问题 |采纳率89.5%生石灰(碳酸钙)作干燥剂与水发生反应生成氢氧化钙(熟石灰)与水.
而熟石灰不能与水发生反应,所以不能作干燥剂.1年前查看全部
- 一些食品包装袋内常有一小袋干燥剂,干燥剂袋上的部分文字如图,请阅读文字,并回答问题:
一些食品包装袋内常有一小袋干燥剂,干燥剂袋上的部分文字如图,请阅读文字,并回答问题:
万一误入眼睛,请先以清水冲洗后求诊于医师谨防儿童取玩
①“请勿食用”是因为干燥剂食用后,对人体有______作用.
②写出干燥剂的主要成分吸水过程中,发生的化学反应方程式______.
③误入眼睛应该______.
 顽主林1年前1
顽主林1年前1 -
 dz2326217wx 共回答了19个问题
dz2326217wx 共回答了19个问题 |采纳率89.5%①根据干燥剂袋上的部分文字,该干燥剂的成分为生石灰,可与水反应生成氢氧化钙,同时放出大量的热,氢氧化钙具有腐蚀性.
②氧化钙与水反应生成氢氧化钙,反应的化学方程式为:CaO+H 2 O=Ca(OH) 2 .
③生石灰进入眼睛,不能用手揉眼睛,也不能直接用水冲洗,因为生石灰与水反应生成熟石灰同时产生热量,处理不当反而会灼伤眼睛.此时应用棉签或干净手绢将生石灰粉拨出,然后再用清水反复冲洗受伤的眼睛.
故答案为:①腐蚀;②CaO+H 2 O=Ca(OH) 2 ;③用棉签或干净手绢将生石灰粉拨出,然后再用清水反复冲洗受伤的眼睛.1年前查看全部
- 做干燥剂的生石灰块状变成粉末状为什么属于化学变化?
做干燥剂的生石灰块状变成粉末状为什么属于化学变化?
?为什么?
 我要去个地方1年前1
我要去个地方1年前1 -
 橡胶人体50 共回答了15个问题
橡胶人体50 共回答了15个问题 |采纳率93.3%生石灰变成熟石灰了
CaO+H2O=Ca(OH)21年前查看全部
- 酸性干燥剂 浓硫酸不能用来干燥碱性气体,
酸性干燥剂 浓硫酸不能用来干燥碱性气体,
碱性干燥剂固体氢氧化钠不能用来干燥酸性气体,但它们都能干燥氢气,氧气,氮气(请问这些都属于什么性质的气体),为什么? dan_ly1年前6
dan_ly1年前6 -
 我爱如如 共回答了16个问题
我爱如如 共回答了16个问题 |采纳率87.5%化学反应啊,酸遇碱反应生产水和盐.起不到干燥的作用的.所以碱性干燥剂不用用来干燥酸性气体(如二氧化碳,二氧化氮等);酸性干燥剂不能用来干燥碱性气体(如氨气).而氢气、氧气和氮气属于中性气体.不与碱性干燥剂和酸性干燥剂反应,所以可以用来干燥.1年前查看全部
- 下列气体中,不能用固体氢氧化钠作干燥剂的是( )
下列气体中,不能用固体氢氧化钠作干燥剂的是( )
A. 氢气
B. 氧气
C. 二氧化碳
D. 一氧化碳 美食虫子1年前1
美食虫子1年前1 -
 j49601 共回答了18个问题
j49601 共回答了18个问题 |采纳率94.4%解题思路:作干燥剂的物质应该既能吸水,又不与被干燥的气体反应,A、B、D三种物质都不能与氢氧化钠反应,所以可以用氢氧化钠来干燥.A、氢气、不与氢氧化钠反应,可以用氢氧化钠干燥;故本选项错误;
B、氧气不与氢氧化钠反应,可以用氢氧化钠干燥;故本选项错误;
C、二氧化碳是酸性气体,会与氢氧化钠反应,不能用氢氧化钠干燥:2NaOH+CO2=Na2CO3+H2O;故本选项正确.
D、一氧化碳不与氢氧化钠反应,可以用氢氧化钠干燥;故本选项错误;
故选C.点评:
本题考点: 根据浓硫酸或烧碱的性质确定所能干燥的气体.
考点点评: 本题考查了根据浓硫酸或烧碱的性质确定所能干燥的气体.完成此题,可以依据氢氧化钠的性质进行分析.1年前查看全部
- 干燥剂种类一些基本的干燥剂和其可以干燥的气体.
 wjq_433711年前2
wjq_433711年前2 -
 js_ocean 共回答了19个问题
js_ocean 共回答了19个问题 |采纳率94.7%酸性干燥剂:浓硫酸(硫化氢、碘化氢不行),五氧化二磷,可以干燥中性或酸性气体.
碱性干燥剂:碱石灰(氧化钙和氢氧化钠的混合物),氧化钙,固体氢氧化钠,金属钠(卤代烃不可)可以干燥中性或碱性气体.
中性干燥剂:氯化钙(氨气不行),硅胶,无水硝酸镁可以干燥中性、碱性或酸性气体.1年前查看全部
- Ca(OH)2能作干燥剂吗?它不是碱石灰的组成之一吗?为什么不能作干燥剂?
 xaddhhj1年前1
xaddhhj1年前1 -
 3872504 共回答了25个问题
3872504 共回答了25个问题 |采纳率100%一般不用Ca(OH)2做干燥剂,因为它的吸水性不强,常常用碱石灰(NaOH和CaO的混合物)但这类碱性物质不能用于二氧化碳等要与他们反应的气体干燥.而这些气体却常常用浓硫酸来干燥.1年前查看全部
- 什么气体能用氢氧化钠作干燥剂啊,
 insanewolf1年前1
insanewolf1年前1 -
 顾惜朝晕倒 共回答了20个问题
顾惜朝晕倒 共回答了20个问题 |采纳率95%氢氧化钠极易溶于水,易潮解,所以可以用作某些气体(如氧气,氢气)的干燥剂.
但是不能作为酸性气体的干燥剂(如二氧化碳,二氧化硫等等)1年前查看全部
- 实验室常用的干燥剂碱石灰是CaO和NaOH的固体混合物,极易与空气中的水蒸气和二氧化碳反应而变质.某同学对一瓶久置的碱石
实验室常用的干燥剂碱石灰是CaO和NaOH的固体混合物,极易与空气中的水蒸气和二氧化碳反应而变质.某同学对一瓶久置的碱石灰作了如下探究:
【提出猜想】猜想一:没有变质,只有CaO和NaOH两种固体; 猜想二:已完全变质,碱石灰全部变成了CaCO3和Na2CO3.
【实验探究】实验过程与现象如下图所示:
【做出判断】(1)若把Ca(OH)2、CaCO3和Na2CO3加入水中不会放出热量,侧由操作b中的现象可判断猜想二______(填“成立”或“不成立”).
(2)操作f中发生反应的化学方程式为______;
由操作e、f中的现象可判断滤液里含有______(填化学式),由此判断猜想一______(填“成立”或“不成立”).
(3)综合(1)、(2)中的结论,判断该碱石灰的变质情况为______.
【拓展应用】(4)由上述实验说明,在实验室存放碱石灰应______保存. 狗JB1年前1
狗JB1年前1 -
 红米411 共回答了15个问题
红米411 共回答了15个问题 |采纳率100%解题思路:(1)根据物质溶于水的温度变化情况进行分析,
(2)根据推导确定混合物的成分进行分析,
(3)根据实验现象进行分析,
(4)根据上面的实验结论进行分析.(1)混合物加水后试管壁发热,但是Ca(OH)2、CaCO3和Na2CO3加入水中不会放出热量,所以C猜想二不成立.
(2)浑浊液中的滤渣中滴加盐酸,产生气泡,说明混合物中有碳酸钙,滤液中滴加盐酸有气泡,加澄清石灰水有沉淀生成,说明滤液中有碳酸钠,但是如果只有氧化钙和氢氧化钠就不会生成碳酸钙沉淀和碳酸钠.
(3)从(2)中的推导可知,混合物中既有CaO和NaOH,也有CaCO3和Na2CO3.
(4)通过实验可知,碱石灰在空气中极易变质.
故答案为:
(1)不成立,
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 碳酸钠 不成立
(3)部分变质
(4)密封、防潮点评:
本题考点: 物质的鉴别、推断;空气中常见酸碱盐的质量或性质变化及贮存法;酸、碱、盐的鉴别;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,先根据题中的现象推出确定的物质,对于不确定的物质要设计实验进行验证.1年前查看全部
- 什么碱加什么干燥剂生成水?
 porcelethch1年前1
porcelethch1年前1 -
 xzmfls 共回答了25个问题
xzmfls 共回答了25个问题 |采纳率88%2NAOH+H2SO4=NA2SO4+2H2O1年前查看全部
- “双吸剂”主要成分是极细的铁粉,那么“双吸剂”与干燥剂相比优点有什么?
 salalaYOU1年前1
salalaYOU1年前1 -
 lindacan 共回答了26个问题
lindacan 共回答了26个问题 |采纳率80.8%双吸剂既可以干燥又可以抗氧化..1年前查看全部
- 选择干燥剂时应该注意哪些因素
 爱流浪0071年前1
爱流浪0071年前1 -
 天蝎座的男孩 共回答了17个问题
天蝎座的男孩 共回答了17个问题 |采纳率94.1%酸性干燥剂:浓硫酸(l),五氧化二磷(s)等;主要干燥酸性或中性气体,
如SO2,CO2,CO,NO2,O2
碱性干燥剂:碱石灰(s),NaOH(s)等;主要干燥碱性或中性气体,
如NH3,CO,O2
中性干燥剂:CaCl2(s),MgSO4(s)等;这类干燥剂不常用,因为很复杂,如CaCl2(s),看上去好象不和酸性气体反应,似乎可以干燥酸性气体,但它不能干燥卤化氢(HCl HBr),因会发生复杂的化学反应,中学阶段没学;再者它也不能干燥NH3,因它可以和NH3形成复杂的络合物.总之,这类干燥剂一般主要是干燥中性气体.
另:①,干燥剂的选择,既要看干燥剂的性质还要看所干燥物质的性质,如浓硫酸,是酸所以不能干燥碱性气体;另外浓硫酸还具有强氧化性,因此不能用来干燥还原性的物质,如H2S,HI ,HBr等
②对液体干燥剂来说,一般装在洗气瓶中(气体从长管进,短管出).而固体干燥剂装在干燥管或U形管中.
其次还要主意会互相发生氧化还原反应的不能干燥1年前查看全部
- 高中化学中干燥剂的原理P2o5 Hclo4 sio2 NaHO CaO CaCl的原理硅胶是什么,是二氧化硅吗,它怎么吸
高中化学中干燥剂的原理
P2o5 Hclo4 sio2
NaHO CaO CaCl
的原理
硅胶是什么,是二氧化硅吗,它怎么吸水啊,课本上说二氧化硅不跟水反应的
我的资料书上讲了以上都可以当干燥剂 pingtouchefu1年前3
pingtouchefu1年前3 -
 谁认真谁SB 共回答了19个问题
谁认真谁SB 共回答了19个问题 |采纳率94.7%P2O5:于水反应生成H3PO4
HClO4:不能作干燥剂,但可以除杂,利用氧化性
SiO2:一般不作干燥剂
NaOH:遇水潮解
CaO:与水反应生成Ca(OH)2
CaCl2:与水反应生成CaCl·H2O1年前查看全部
- 下列气体可用NaOH 做干燥剂的是( )A:CO2 B;HCL C:H2 D:SO2
下列气体可用NaOH 做干燥剂的是( )A:CO2 B;HCL C:H2 D:SO2
注意以上的“:”均为小2, veeky1年前3
veeky1年前3 -
 小李肺刀 共回答了17个问题
小李肺刀 共回答了17个问题 |采纳率94.1%C
其他三种均与NaOH反应,反应分别生成Na2CO3、NaCl、Na2SO3和水.1年前查看全部
- 化学2道填空题!________、_________、__________都能做干燥剂,(食品袋一般用其中的______
化学2道填空题!
________、_________、__________都能做干燥剂,(食品袋一般用其中的_________)这三种物质遇到水温度都会_________,遇到水温度降低的是物质是_________(名称为_________)
并不是所有的碱中都有金属离子,如______、_______(名称及化学式),酸、碱、盐的水溶液可以导电,而_______,________和蔗糖溶液等溶液不能导电. redfox3181年前2
redfox3181年前2 -
 M川酷子 共回答了20个问题
M川酷子 共回答了20个问题 |采纳率95%氢氧化钠 氧化钙 浓硫酸
氧化钙
上升
氢氧化钙
熟石灰
氨水 NH3.H2O
酒精 纯水1年前查看全部
- 高中常用干燥剂有哪些?分别适用于哪些物质的干燥?
 -ankey1年前1
-ankey1年前1 -
 流云飞袖1981 共回答了9个问题
流云飞袖1981 共回答了9个问题 |采纳率100%1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分.例如常作为H2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂.
2、无水氯化钙:因其价廉、干燥能力强而被广泛应用.干燥速度快,能再生,脱水温度473K.一般用以填充干燥器和干燥塔,干燥药品和多种气体.不能用来干燥氨、酒精、胺、酰、酮、醛、酯等.
3、无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4.7H2O.吸水作用迅速,效率高,价廉,为一良好干燥剂.常用来干燥有机试剂.
4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质.常用来干燥氢气、氧气和甲烷等气体.
5、变色硅胶:常用来保持仪器、天平的干燥.吸水后变红.失效的硅胶可以经烘干再生后继续使用.可干燥胺、NH3、 O2、 N2等
6、活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K烘烤).
7、无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差.
8、硫酸钙:可以干燥H2 .O2 .CO2 .CO 、N2 .Cl2、HCl 、H2S、 NH3、 CH4等1年前查看全部
- 制取二氧化碳是能否用生石灰做干燥剂
 ckinlove19851年前1
ckinlove19851年前1 -
 彼得文 共回答了20个问题
彼得文 共回答了20个问题 |采纳率85%不能,碱性氧化物和酸性氧化物会反应1年前查看全部
大家在问
- 1请你写出一个三项式,使它能先提公因式,再运用公式法来分解因式,你编的三项式是( ),
- 2平方得0.25的数是( ).
- 3娟娟和哥哥共存了45.6元钱,如果哥哥给娟娟2.4元,那么两人的存款数相等,娟娟和
- 4This is Jim. He is thirteen. He is from the U.S.A. He is a s
- 5我们要及时纠正自己的缺点和错误.--------改病句
- 6复称法、平衡法、原理法浮力表达式
- 7how can i thank all of you怎么读
- 8英语阅读提问,我会在以下补充,Reading comprehension 1A friend of mine was f
- 954减8除以17减十七分之九的简便运算
- 10导热油可以降温到零下十度吗
- 11人生的开关中的''光明境界指什么
- 12下列属于直接利用太阳能辐射能的方式是( )
- 13完形填空Kate Smith __1__ a student . She __2__ a brother and a _
- 14关于物体做圆周运动的说法正确的是( )
- 15我的五一假期,,英语作文,50字
