离子交换膜与反渗透膜
 juliet_wang2022-10-04 11:39:543条回答
juliet_wang2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 qiyejia2 共回答了20个问题
qiyejia2 共回答了20个问题 |采纳率85%- 反渗透又称逆渗透,一种以压力差为推动力,从溶液中分离出溶剂的膜分离操作.因为它和自然渗透的方向相反,故称反渗透.根据各种物料的不同渗透压,就可以使大于渗透压的反渗透法达到分离、提取、纯化和浓缩的目的.
EDI(Electrodeionization,连续电解除盐技术),是一种将离子交换技术、离子交换膜技术和离子电迁移技术相结合的纯水制造技术.它巧妙的将电渗析和离子交换技术相结合,利用两端电极高压使水中带电离子移动,并配合离子交换树脂及选择性树脂膜以加速离子移动去除,从而达到水纯化的目的.在EDI除盐过程中,离子在电场作用下通过离子交换膜被清除.同时,水分子在电场作用下产生氢离子和氢氧根离子,这些离子对离子交换树脂进行连续再生,以使离子交换树脂保持最佳状态. - 1年前
 freeman0201 共回答了17个问题
freeman0201 共回答了17个问题 |采纳率- 离子交换膜与反渗透膜的区别,它们各自的机理是什么 反渗透膜是在压力离子交换膜是可以可以阴阳离子分别通过的膜,是靠电压作用的. 反渗透膜是依靠
- 1年前
 cross99 共回答了2个问题
cross99 共回答了2个问题 |采纳率- 离子交换膜是在电场的作用下离子发生迁移,反渗透膜是在压力 的作用下分离溶液中的溶质和溶剂
- 1年前
相关推荐
- 电解时用的是哪种离子交换膜?为什么?
 znbird1年前1
znbird1年前1 -
 李逸姝 共回答了23个问题
李逸姝 共回答了23个问题 |采纳率100%一般是阳离子交换膜.一般反应后会让氢离子平衡溶液1年前查看全部
- (2014•洛阳模拟)电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如下图所示.已知海水中含Na+、Cl-、Ca
 (2014•洛阳模拟)电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如下图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )
(2014•洛阳模拟)电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如下图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )
A.A膜是阳离子交换膜
B.通电后,海水中阴离子往b电极处运动
C.通电后,b电极上产生无色气体,溶液中出现白色沉淀
D.通电后,a电极的电极反应式为4OH--4e-═O2↑+2H2O 无欲则痿1年前1
无欲则痿1年前1 -
 rightailring 共回答了18个问题
rightailring 共回答了18个问题 |采纳率83.3%解题思路:A、阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过;
B、依据电解原理分析,电解过程中阳离子移向阴极;
C、a电极和电源正极相连是电解池的阳极,溶液中氯离子先放电;
D、b电极氢离子放电生成氢气,氢氧根离子浓度增大结合镁离子生成白色沉淀.A、阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过,隔膜B和阴极相连,阴极是阳离子放电,所以隔膜B是阳离子交换膜,故A错误;
B、电解过程中阳离子移向阴极b极,故B错误;
C、b电极氢离子放电生成氢气,电极附近氢氧根离子浓度增大,结合镁离子生成白色沉淀,故C正确;
D、a电极和电源正极相连是电解池的阳极,溶液中氯离子先放电,电极反应为:2Cl--2e-=Cl2↑,故D错误;
故选C.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了电解原理的应用,电极反应,电极判断,题干信息的分析应用,题目难度中等.1年前查看全部
- 离子交换膜法电解饱和食盐水的原理
 葱葱太葱葱三世1年前1
葱葱太葱葱三世1年前1 -
 kd0i 共回答了18个问题
kd0i 共回答了18个问题 |采纳率88.9%+极OH根放电生成氧气
-极cl离子放电生成氯气
因为有膜所以OH根留在+极生成NaOH
同时防止cl离子与NaOH接触发生反应1年前查看全部
- 如图装置为一种可充电电池的示意图,其中的离子交换膜只允许K + 通过,该电池充、放电的化学方程式为:2K 2 S 2 +
如图装置为一种可充电电池的示意图,其中的离子交换膜只允许K + 通过,该电池充、放电的化学方程式为:2K 2 S 2 +KI 3 
K 2 S 4 +3KI.装置(Ⅱ)为电解池的示意图.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )A.闭合K时,K + 从右到左通过离子交换膜 B.闭合K时,A的电极反应式为:3I - -2e - =I 3 - C.闭合K时,X的电极反应式为:2Cl - -2e - =Cl 2 ↑ D.闭合K时,当有0.1molK + 通过离子交换膜,X电极上产生标准状况下气体1.12L 
 sxh441年前1
sxh441年前1 -
 zz孤人A 共回答了24个问题
zz孤人A 共回答了24个问题 |采纳率87.5%当闭合开关K时,X附近溶液先变红,即X附近有氢氧根生成,所以在X极上得电子析出氢气,X极是阴极,Y极是阳极.与阴极连接的是原电池的负极,所以A极是负极,B极是正极.
A、闭合K时,A是负极B是正极,电子从A极流向B极,根据异性电荷相吸原理,所以K + 从左到右通过离子交换膜,故A错误.
B、闭合K时,A是负极,负极上失电子发生氧化反应,所以其电极反应式为:I 3 - +2e - =3I - ,故B错误.
C、闭合K时,X电极是阴极,在阴极上溶液中的氢离子放电生成氢气,所以电极反应式为 2H + +2e - =H 2 ↑,故C错误.
D、闭合K时,当有0.1molK + 通过离子交换膜,即有0.1mol电子产生,根据氢气与电子的关系式知,生成的氢气体积为1.12L(标况下),故D正确.
故选D.1年前查看全部
- (2012•山东模拟)现有用离子交换膜(只允许对应的离子通过)和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH
 (2012•山东模拟)现有用离子交换膜(只允许对应的离子通过)和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和H2SO4,下列说法中正确的是( )
(2012•山东模拟)现有用离子交换膜(只允许对应的离子通过)和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和H2SO4,下列说法中正确的是( )
A.气体A是H2,溶液E是稀硫酸
B.气体B是H2,溶液D是NaOH溶液
C.Na2SO4溶液由G口加入,F口通入稀硫酸
D.靠阳极室一侧的是阳离子交换膜,阴极室导出的是氢气 104540cb440e2cb21年前1
104540cb440e2cb21年前1 -
 Boy_风 共回答了11个问题
Boy_风 共回答了11个问题 |采纳率72.7%解题思路:据题意,电解饱和Na2SO4溶液时,阳极附近是OH-放电,生成氧气,阴极附近时H+放电生成氢气,由于装置中放置了离子交换膜,在两极分别生成NaOH和H2SO4,需在阳极室一侧放置阴离子交换膜,只允许通过阴离子,在阴极一侧放置阳离子交换膜,只允许通过阳离子,D错误;接电源正极的是阳极,即A极放出氧气,A错误B正确;若由F口通入稀硫酸,则将NaOH中和,得不到产品.A、连接电源正极的是电解池的阳极,连接电源负极的是电解池的阴极,A为阳极产生的气体,是氧气,故A错误;
B、阴极发生的反应为:2H2O+2e-═H2↑+2OH-,在阴极上生成H2和NaOH溶液,故B正确;
C、若由F口通入稀硫酸,则将NaOH中和,得不到产品,故C错误;
D、由于装置中放置了离子交换膜,在两极分别生成NaOH和H2SO4,需在阳极室一侧放置阴离子交换膜,只允许通过阴离子,在阴极一侧放置阳离子交换膜,只允许通过阳离子,故D错误.
故选B.点评:
本题考点: 电解原理.
考点点评: 本题考查电解池知识,本题设置新情景,即离子交换膜,注意根据两极上的反应判断生成物.1年前查看全部
- 离子交换膜法制烧碱那块,请问为什么要往阳极室中通精制饱和NaCl,往阴极室里通H2O(含少量NaOH)特别是为什么在阴极
离子交换膜法制烧碱那块,
请问为什么要往阳极室中通精制饱和NaCl,往阴极室里通H2O(含少量NaOH)
特别是为什么在阴极室通水还要有(少量NaOH)?
请一一回答,谢谢O(∩_∩)O wyl5151年前2
wyl5151年前2 -
 莹妮 共回答了22个问题
莹妮 共回答了22个问题 |采纳率86.4%增强导电性,同时NaOH不会干扰反应1年前查看全部
- (2013•马鞍山一模)海水淡化的方法有多种,如蒸馏法、电渗析法等.电渗析法是一种利用离子交换膜进行离子交换的方法,其原
(2013•马鞍山一模)海水淡化的方法有多种,如蒸馏法、电渗析法等.电渗析法是一种利用离子交换膜进行离子交换的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )

A.B膜是阴离子交换膜
B.通电后,海水中阳离子往a电极处运动
C.通电后,a电极的电极反应式为:4OH--4e-=O2↑+2H2O
D.通电后,b电极上产生无色气体,溶液中出现少量白色沉淀 花tt121年前1
花tt121年前1 -
 snc5zf 共回答了16个问题
snc5zf 共回答了16个问题 |采纳率87.5%解题思路:A、阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过;
B、依据电解原理分析,电解过程中阳离子移向阴极;
C、a电极和电源正极相连是电解池的阳极,溶液中氯离子先放电;
D、b电极氢离子放电生成氢气,氢氧根离子浓度增大结合镁离子生成白色沉淀.A、阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过,隔膜B和阴极相连,阴极是阳离子放电,所以隔膜B是阳离子交换膜,故A错误;
B、电解过程中阳离子移向阴极,故B错误;
C、a电极和电源正极相连是电解池的阳极,溶液中氯离子先放电,电极反应为:2Cl--2e-=Cl2↑,故C错误;
D、b电极氢离子放电生成氢气,电极附近氢氧根离子浓度增大,结合镁离子生成白色沉淀,故D正确;
故选D.点评:
本题考点: 电解原理.
考点点评: 本题考查了电解原理的应用,电极反应,电极判断,题干信息的分析应用,题目难度中等.1年前查看全部
- 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42
 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是
电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是
(1)A膜是______离子交换膜.
(2)通电后,海水中阴离子往______电极处运动.
(3)通电后,a电极的电极反应式为______.
(4)通电后,b电极上产生的现象为______. 钉子神经1年前1
钉子神经1年前1 -
 yqhjsr 共回答了20个问题
yqhjsr 共回答了20个问题 |采纳率75%解题思路:(1)阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过;
(2)依据电解原理分析,电解过程中阴离子移向阳极;
(3)根据阳极是氯离子放电来书写电极反应式;
(4)阴极区是氢离子得到电子生成氢气,氢氧根离子浓度增大.(1)阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过,隔膜A和阳极相连,阳极是阴离子放电,所以隔膜A是阴离子交换膜,
故答案为:阴;
(2)依据电解原理,电解过程中阴离子移向阳极,故答案为:阳极a极;
(3)通电后,a电极为阳极,阳极是氯离子放电,生成氯气,其电极反应为:2Cl--2e-═Cl2↑;
故答案为:2Cl--2e-=Cl2↑;
(3)通电后,b电极为阴极,阴极区是氢离子得到电子生成氢气,氢氧根离子浓度增大,和钙离子,镁离子形成沉淀,
故答案为:产生无色气体,溶液中出现少量白色沉淀.点评:
本题考点: 电解原理.
考点点评: 本题考查了电解原理的应用,主要考查了电极反应的书写、电极判断、题干信息的分析应用等,题目难度不大.1年前查看全部
- 钢铁电化学腐蚀有两种类型主要区别在于水膜的ph不同.这句话是一条选择题,然后水膜是什么?离子交换膜?请各位老师赐教……
 狮人与水水1年前1
狮人与水水1年前1 -
 黑百 共回答了14个问题
黑百 共回答了14个问题 |采纳率92.9%这句话对,水膜是指附着在钢铁上的水溶液,含有各种离子,酸性强时容易析氢腐蚀,酸性弱或者中性时容易吸氧腐蚀,原理是水膜与金属表面形成许多微电池,发生电化学反应,离子交换膜是对离子具有选择透过性的高分子材料制成的薄膜,手打慢,请采纳1年前查看全部
- 电解海水(NaCl)利用离子交换膜进行海水淡化的方法的原理是什么?
电解海水(NaCl)利用离子交换膜进行海水淡化的方法的原理是什么?
在电解海水(NaCl)时,为什么在阴极区放置阳离子交换膜,在阳极区放置阴离子交换膜?这会在中间部分生成水吗?
11年武汉市五月供题1理综第28题.是海水淡化法不是氯碱工业. 娃哈哈uzd41年前1
娃哈哈uzd41年前1 -
 zzdxc 共回答了20个问题
zzdxc 共回答了20个问题 |采纳率80%首先,电解海水目的是为了制取烧碱 和氯气
那么在阴极区存在大量OH-
所以要将Na+交换到OH-富集的区域内以便提纯
阳极区Cl-变成Cl2跑出去必要补充CL-以便继续电解成为Cl21年前查看全部
- (2011•南京模拟)如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程
 (2011•南京模拟)如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程式为:2K2S2+KI3═K2S4+3KI.装置(Ⅱ)为电解池的示意图.当闭合开关K时,电极X附近溶液先变红.则闭合K时,下列说法正确的是( )
(2011•南京模拟)如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程式为:2K2S2+KI3═K2S4+3KI.装置(Ⅱ)为电解池的示意图.当闭合开关K时,电极X附近溶液先变红.则闭合K时,下列说法正确的是( )
A.K+从右到左通过离子交换膜
B.电极A上发生的反应为:3I--2e-=I3-
C.电极X上发生的反应为:2Cl--2e-=C12↑
D.当有0.1 mol K+通过离子交换膜,X电极上产生1.12 L气体(标准状况) lanbor1年前1
lanbor1年前1 -
 午后的红茶liu 共回答了14个问题
午后的红茶liu 共回答了14个问题 |采纳率92.9%解题思路:当闭合开关K时,X附近溶液先变红,说明X极生成OH-,应为电解池的阴极,发生反应为:2H2O+2e-=H2↑+2OH-,Y为电解池的阳极,发生:2Cl--2e-═Cl2↑,则A为原电池的负极,电极反应式为2K2S2-2e-═K2S4+2K+,B为原电池的正极,电极反应式为I3-+2e-═3I-,以此解答该题.当闭合开关K时,X附近溶液先变红,说明X极生成OH-,应为电解池的阴极,发生反应为:2H2O+2e-=H2↑+2OH-,Y为电解池的阳极,发生:2Cl--2e-═Cl2↑,则A为原电池的负极,电极反应式为2K2S2-2e-═K2S4+2K+,B为原电池的正极,电极反应式为I3-+2e-═3I-,
A.钾离子向正极移动,则钾离子向B电极移动,故A错误;
B.A为负极,失电子发生氧化反应,电极反应式为2K2S2-2e-═K2S4+2K+,故B错误;
C.X电极上得电子发生还原反应,电极反应式为2H2O+2e-=H2+2OH-,故C错误;
D.当有0.1 mol K+通过离子交换膜,根据2K2S2-2e-═K2S4+2K+知,转移电子的物质的量是0.1mol,根据转移电子守恒知,X电极上产生气体体积=
0.1mol
2×22.4L/mol=1.12L,故D正确.
故选D.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查了原电池和电解池原理,以X电极现象确定电解池阴阳极,从而确定原电池正负极,再结合各个电极上得失电子书写电极反应式,难点是电极反应式的书写,难度中等.1年前查看全部
- (2012•大兴区一模)工业上电解饱和食盐能制取多种化工原料,如图是离子交换膜法电解饱和食盐水示意图,下列说法中不正确的
 (2012•大兴区一模)工业上电解饱和食盐能制取多种化工原料,如图是离子交换膜法电解饱和食盐水示意图,下列说法中不正确的是( )
(2012•大兴区一模)工业上电解饱和食盐能制取多种化工原料,如图是离子交换膜法电解饱和食盐水示意图,下列说法中不正确的是( )
A.电解槽阳极的反应方程式为:2Cl--2e-═Cl2↑
B.产品 NaOH的出口是b
C.精制饱和食盐水的进口为d
D.干燥塔中应使用的液体是浓硫酸 imaray1年前1
imaray1年前1 -
 supermartingale 共回答了18个问题
supermartingale 共回答了18个问题 |采纳率94.4%解题思路:电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,阳极发生的方程式为:2Cl--2e-═Cl2↑,阴极:2H++2e-═H2↑;H2、NaOH在阴极,NaOH溶液的出口为a,Cl2在阳极,精制饱和食盐水从阳极进入,要干燥Cl2需要用酸性干燥剂或中性干燥剂.A、依据图装置可知电解槽中阳极是氯离子放电生成氯气,电极反应为:2Cl--2e-═Cl2↑,故A正确;
B、电解槽中阴极是氢离子放电生成氢气,水电离平衡正向进行氢氧根离子浓度增大,生成氢氧化钠溶液,NaOH溶液的出口为a,故B错误;
C、Cl2在阳极,依据装置图分析可知精制饱和食盐水从阳极进入,即进口为d,故C正确;
D、要干燥Cl2需要用酸性干燥剂或中性干燥剂,可以用浓硫酸干燥,故D正确;
故选B.点评:
本题考点: 电解原理.
考点点评: 本题考查电解原理的原理应用,电解反应电极判断是解题关键,题目难度中等.1年前查看全部
- (2014•威海一模)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只
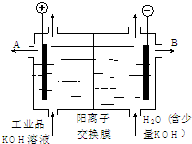 (2014•威海一模)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.下列说法中正确的是( )
(2014•威海一模)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.下列说法中正确的是( )
A.该电解槽的阳极反应式是4OH--2e-→2H2O+O2↑
B.通电开始后,阴极附近溶液pH会减小
C.除去杂质后氢氧化钾溶液从液体出口A导出
D.用氯化钾制备氢氧化钾也可采用这种离子交换膜电解法 防弹玻璃221年前1
防弹玻璃221年前1 -
 duida 共回答了17个问题
duida 共回答了17个问题 |采纳率100%解题思路:用阳离子交换膜电解法除去工业品氢氧化钾溶液中的杂质含氧酸根,相当于电解水,故电解时,阳极:4OH--4e-=2H2O+O2↑,阴极:4H++4e-=2H2↑,其中阴极区H+放电,H+浓度减小,使水的电离平衡向右移动促进水的电离,OH-浓度增大.在阴极和阳极之间有阳离子交换膜,只允许阳离子K+和H+通过,这样就在阴极区聚集大量的K+和OH-,从而产生纯的氢氧化钾溶液.A.电解除杂过程相当于电解水,阳极反应式为:4OH--4e-=2H2O+O2↑,故A错误;
B.电解时,阴极电极反应式为:4H++4e-=2H2↑,氢离子浓度减小,溶液的pH增大,故B错误;
C.在B电极附近产生氢氧根离子,钾离子向B电极移动,所以除去杂质后氢氧化钾溶液从液体出口B导出,故C错误;
D.用氯化钾制备氢氧化钾时,阴极上氢离子放电,阳极上氯离子放电,阴极附近产生氢氧化钾,所以也可采用这种离子交换膜电解法,故D正确;
故选D.点评:
本题考点: 电解原理.
考点点评: 本题考查了电解原理,明确离子放电顺序是解本题关键,再结合离子移动方向确定产物,题目难度不大.1年前查看全部
- (2009•徐州三模)如图所示装置I是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为2
 (2009•徐州三模)如图所示装置I是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为2Na2S2+NaBr3
(2009•徐州三模)如图所示装置I是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为2Na2S2+NaBr3
Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )放电 充电
A.负极反应为4Na-4e-=4Na+
B.当有0.01 mol Na+通过离子交换膜时,b电极上析出标准状况下的气体112 mL
C.闭合K后,b电极附近的pH变小
D.闭合K后,a电极上有气体产生 LJJ19681年前1
LJJ19681年前1 -
 cctofengshui 共回答了24个问题
cctofengshui 共回答了24个问题 |采纳率75%解题思路:当闭合开关K时,b附近溶液先变红,即b附近有氢氧根生成,所以在b极上得电子析出氢气,b极是阴极,a极是阳极,与阴极连接的是原电池的负极,所以B极是负极,A极是正极,再根据原电池、电解池原理判断选项.
A、原电池的负极发生失电子的氧化反应;
B、根据电子守恒知识来计算;
C、闭合K后,b电极附近溶液先变红,即b附近有氢氧根生成;
D、闭合开关K时,根据a极上发生的电极反应来看现象.当闭合开关K时,b附近溶液先变红,即b附近有氢氧根生成,所以在b极上得电子析出氢气,b极是阴极,a极是阳极,与阴极连接的是原电池的负极,所以B极是负极,A极是正极.
A、闭合K时,负极发生氧化反应,电极反应为2Na2S2-2e-=2Na++Na2S4,故A错误;
B、闭合K时,有0.01molNa+通过离子交换膜,说明有0.01mol电子转移,阴极上生成0.005molH2,标准状况下体积为0.005mol×22.4L/mol=0.112L=112 mL,故B正确;
C、闭合开关K时,b极附近先变红色,该极上是氢离子放电的过程,即b附近有氢氧根生成,pH增大,故C错误;
D、闭合开关K时,a极是阳极,该极上金属铜电极是活泼电极,发生的电极反应为:Cu-2e-=Cu2+,没有气体产生,故D错误.
故选B.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查学生原电池和电解池的工作原理知识,属于综合知识的考查,综合性较强,难度较大.1年前查看全部
- 化学电解氯化钠溶液,中间有离子交换膜.为什么要在阴极加氢氧化钠.
 miwei1年前1
miwei1年前1 -
 回尤氏道 共回答了11个问题
回尤氏道 共回答了11个问题 |采纳率90.9%上一个人回答是错误的 不知道就不要误人子弟 在阴极加氢氧化钠 是和水一起加的 主要是为了增强导电性 必要浪费更的的电能.1年前查看全部
- (2014•浙江模拟)离子交换膜是一类具有离子交换功能的高分子材料,在生产和研究中有广泛应用.一容器被离子交换膜分成左右
 (2014•浙江模拟)离子交换膜是一类具有离子交换功能的高分子材料,在生产和研究中有广泛应用.一容器被离子交换膜分成左右两部分,如图所示:
(2014•浙江模拟)离子交换膜是一类具有离子交换功能的高分子材料,在生产和研究中有广泛应用.一容器被离子交换膜分成左右两部分,如图所示:
(1)若该交换膜为阳离子交换膜(只允许阳离子自由通过).左边充满加过盐酸酸化的H2O2溶液.右边充满滴有少量KSCN溶液的FeCl2溶液(FeCl2过量),一段时间后可观察到的现象:右边______(从下列选项中选择)
A.无明显现象B.溶液有浅绿色变红色C.溶液由无色变黄色D.盐溶液由浅绿色变无色
试写出左边发生的离子方程式______
(2)若该交换膜为阴离子交换膜(只允许阴离子自由通过).左边充满1mol•L-1的NaHCO3溶液,右边充满等体积的1mol•L-1的NaAlO2溶液,一段时间后可观察到的现象:左边______(从下列选项中选择)
A.无明显现象B.有气泡产生C.有白色胶状沉淀生成D.有红褐色沉淀生成
试比较最终容器内所得溶液中离子浓度的大小______. 65个realtree1年前1
65个realtree1年前1 -
 jeffey_jun 共回答了17个问题
jeffey_jun 共回答了17个问题 |采纳率100%解题思路:(1)交换膜为阳离子交换膜,二价铁离子通过交换膜从右边进入到左边被双氧水氧化生成三价铁离子,三价铁离子通过交换膜与硫氰根离子反应生成血红色的络合物;
(2)NaHCO3溶液中碳酸氢根离子是多元弱酸的酸式根离子,水解生成碳酸和氢氧化钠,交换膜为阴离子交换膜,NaAlO2 电离出的AlO2 -通过交换膜与水解生成的碳酸反应生成氢氧化铝沉淀;
(3)碳酸氢钠和偏铝酸钠都是强电解质,完全电离产生碳酸氢根离子、偏铝酸根离子和钠离子,碳酸氢根离子水解生成碳酸,与偏铝酸根离子发生反应:2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3 ,反应后溶液主要溶质为碳酸钠,据此判断各种离子浓度大小.(1)二价铁离子通过交换膜从右边进入到左边被双氧水氧化生成三价铁离子,三价铁离子通过交换膜与硫氰根离子反应生成血红色的络合物,发生反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O;
故答案为:B;2Fe2++H2O2+2H+=2Fe3++2H2O;
(2)NaHCO3溶液中碳酸氢根离子是多元弱酸的酸式根离子,水解生成碳酸和氢氧化钠,交换膜为阴离子交换膜,NaAlO2 电离出的AlO2 -通过交换膜与水解生成的碳酸反应生成氢氧化铝沉淀,所以左边会看到有白色胶状沉淀产生,
故答案为:C;
(3)碳酸氢钠和偏铝酸钠都是强电解质,完全电离产生碳酸氢根离子、偏铝酸根离子和钠离子,碳酸氢根离子水解生成碳酸,与偏铝酸根离子发生反应:2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3 ,反应后溶液主要溶质为碳酸钠,所以最终容器内所得溶液中离子浓度的大小顺序为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+);
故答案为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).点评:
本题考点: 铁盐和亚铁盐的相互转变;镁、铝的重要化合物.
考点点评: 本题考查了铁及其化合物的转化,碳酸氢钠与偏铝酸钠的性质,题目难度中等,解题关键在于明确离子交换膜的作用.1年前查看全部
- 氯碱工业,电解nacl为什么用离子交换膜,cl2又不会从一处放出
 yuzhile1231年前1
yuzhile1231年前1 -
 hh呀 共回答了16个问题
hh呀 共回答了16个问题 |采纳率87.5%用离子交换膜的作用主要就是利用离子交换膜的选择透过性,阻止OH-从阴极穿过离子膜到阳极,同阳极的CL2反应.1年前查看全部
- 右图装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.装置(Ⅰ)的离子交换膜只允许Na+ 通过.
 右图装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.装置(Ⅰ)的离子交换膜只允许Na+ 通过.已知电池充、放电的化学反应方程式为2Na2S2+NaBr3
右图装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.装置(Ⅰ)的离子交换膜只允许Na+ 通过.已知电池充、放电的化学反应方程式为2Na2S2+NaBr3 Na2S4+3NaBr.当闭合开关K时,X极附近溶液变红色.下列说法正确的是( )
Na2S4+3NaBr.当闭合开关K时,X极附近溶液变红色.下列说法正确的是( )
A.闭合K时,钠离子从右到左通过离子交换膜
B.闭合K时,负极反应为3NaBr-2e-=NaBr3+2Na+
C.闭合K时,X电极的电极反应式为2Cl--2e-=Cl2↑
D.闭合K时,有0.1molNa+通过离子交换膜,X电极上析出标准状况下气体1.12L lmmhappy1年前1
lmmhappy1年前1 -
 nanako1983 共回答了18个问题
nanako1983 共回答了18个问题 |采纳率66.7%解题思路:当闭合开关K时,X极附近溶液变红色,说明X极生成OH-离子,为电解池的阴极,发生反应为2H2O+2e-=H2↑+2OH-,则A为原电池的负极,B为原电池的正极,根据电池充、放电的化学反应方程式为2Na2S2+NaBr3 Na2S4+3NaBr可知,负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr,Y极为电解池的阳极,
Na2S4+3NaBr可知,负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr,Y极为电解池的阳极,
电极反应为2Cl--2e-=Cl2↑,以此解答该题.A、原电池中阳离子向正极移动,则闭合K时,钠离子从左到右通过离子交换膜,故A错误;B、闭合K时,负极发生氧化反应,电极反应为2Na2S2-2e-=2Na++Na2S4,故B错误;C、闭合K时,X极附近溶液变红色,说明X极生成OH-离子...
点评:
本题考点: 化学电源新型电池;电极反应和电池反应方程式.
考点点评: 本题考查化学电源知识,题目难度中等,注意从总反应式判断两极上的变化和电极反应式的书写.1年前查看全部
- 目前电解法制烧碱通常采用离子交换膜法,阳(阴)离子交换膜不允许阴(阳)
目前电解法制烧碱通常采用离子交换膜法,阳(阴)离子交换膜不允许阴(阳)
离子通过。则以下叙述错误的是()
A.NaOH、H 2 均在Ⅰ区产生 B.图中a为阴离子交换膜 C.Ⅲ区炭棒上的电极反应式为2Cl - -2e →Cl 2 ↑ D.电解时往Ⅲ区的溶液中滴加甲基橙,溶液先变红后褪色  李紫雅1年前1
李紫雅1年前1 -
 zlbok1698 共回答了13个问题
zlbok1698 共回答了13个问题 |采纳率92.3%B
Ⅰ区是阴极,氢离子放电,生成氢气,同时促进水的电离,生成氢氧化钠,A正确。由于Ⅰ区生成氢氧化钠,所以a应该是阳离子交换膜,B不正确。Ⅲ区和电源的正极相连,则阳极,氯离子放电生成氯气,氯气溶于水显酸性,同时次氯酸还具有漂白性,所以CD都是正确的,答案选B。1年前查看全部
- 43.用氯化钾制备氢氧化钾的常用方法是离子交换膜电解法.氢氧化钾在_________极产生,
43.用氯化钾制备氢氧化钾的常用方法是离子交换膜电解法.氢氧化钾在_________极产生,
为了避免两极产物发生副反应,位于电解槽中间的离子交换膜应阻止----离子通过 opehg1年前1
opehg1年前1 -
 mample 共回答了20个问题
mample 共回答了20个问题 |采纳率85%阴极;OH-1年前查看全部
- 离子交换膜和电渗析哪个可以用作盐酸提浓,各自的原理都是什么呢
离子交换膜和电渗析哪个可以用作盐酸提浓,各自的原理都是什么呢
有大概8%的稀盐酸,想要用离子膜和电渗析进行提浓,但是两种方法哪个是可以进行提浓的,哪个方法在实际应用中更好一些呢,麻烦详细一点, 丑小魚1年前1
丑小魚1年前1 -
 m_cicy 共回答了22个问题
m_cicy 共回答了22个问题 |采纳率95.5%请参考.
专利CN101195639公开了对草甘膦母液,采用扩散渗析、电渗析以及 扩散渗析和电渗析的组合,分别回收盐酸、催化剂三乙胺和草甘膦的 工艺,该工艺所采用的扩散渗析膜,成本较高、寿命有限、分离速率比较低,不利于大规模工业化生产,并且电渗析的能效较高,并且分 离效果不理想.
==
感觉无论是离子交换膜还是电渗析用作盐酸提浓成本都非常高.现在盐酸提浓用的最多的方法应该是蒸馏.1年前查看全部
- 下列叙述正确的是( )A.天然气是一种清洁燃料,主要由石油分馏制得B.海水淡化的方法主要有蒸馏法、电渗析法、离子交换膜
下列叙述正确的是( )
A.天然气是一种清洁燃料,主要由石油分馏制得
B.海水淡化的方法主要有蒸馏法、电渗析法、离子交换膜法等
C.煤的干馏和石油的分馏都是化学变化
D.石油裂化的目的是使直链烃转化为芳香烃 bravo93511年前1
bravo93511年前1 -
 francesliang 共回答了17个问题
francesliang 共回答了17个问题 |采纳率88.2%解题思路:A.天然气的主要成分是甲烷;
B.海水淡化的方法有多种,如蒸馏法、电渗析法等;
C.有新物质生成的是化学变化;
D.石油裂化的目的是为了提高轻质液体燃料(汽油,煤油,柴油等)的产量,特别是提高汽油的产量.A.天然气的主要成分是甲烷,石油分馏得不到甲烷,故A错误;
B.海水淡化的方法有多种,如蒸馏法、电渗析法、离子交换膜法等,故B正确;
C.石油的分馏属物理变化,因为石油的分馏是利用石油中各种成分沸点不同将其分离的一种方法,没有新物质生成,所以是物理变化,煤的干馏是复杂的物理化学变化,故C错误;
D.催化重整的目的是使直链烃转化为芳香烃,故D错误.
故选B.点评:
本题考点: 化石燃料与基本化工原料;海水资源及其综合利用;石油的裂化和裂解;煤的干馏和综合利用.
考点点评: 本题考查化石燃料、石油加工、海水淡化和化学变化,题目难度不大,注意催化重整的目的是使直链烃转化为芳香烃.1年前查看全部
- 目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图.
目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图.
(1)下列说法不正确的是______
A.从E口逸出的气体是H 2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4L Cl 2 ,便产生2mol NaOH
D.粗盐水中含Ca 2+ 、Mg 2+ 、Fe 3+ 、SO 4 2- 等离子,精制时先加Na 2 CO 3 溶液
(2)现有离子交换膜A和B将电解槽分为I、II、III三个区域(下图所示),在这种电解池中电解Na 2 SO 4 溶液可制得氢氧化钠、硫酸等物质.A为______离子交换膜、B为______离子交换膜(填“阴”或“阳”),电极均为惰性电极.Na 2 SO 4 溶液应该在______区(填“I”、“II”、“III”)加入.通电电解时阴极的电极反应式为______,在III区得到______.当外电路总共通过30mol电子时,生成的NaOH 960克,则电解过程中能量的转化率为:______.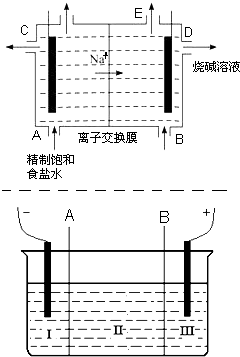
 maxreeves1年前1
maxreeves1年前1 -
 ytinter 共回答了19个问题
ytinter 共回答了19个问题 |采纳率84.2%(1)A、电解饱和食盐水时,大量的氢氧化钠在阴极附近析出,所以E极为阴极,放电的是氢离子,生成氢气,故AZ正确;
B、电解饱和食盐水时,大量的氢氧化钠在阴极附近析出,可以从B口加入含少量NaOH的水溶液以增强导电性,故B正确;
C、电解方程式为:2NaCl+2H 2 O
通电
.
2NaOH+H 2 ↑+Cl 2 ↑,标准状况下每生成22.4L 即1mol的Cl 2 ,便产生2molNaOH,故C正确;
D、粗盐提纯时,碳酸钠一定要加在氯化钡之后,可可以将多余的钡离子除掉,故D错误.
故选D.
(2)电解Na 2 SO 4 溶液时,和电源的正极相连的是阳极,该电极氢氧根离子放电生成的是氧气,和电源的负极相连的是阴极,该极上氢离子放电,生成的是氢气,所以A为阳离子交换膜,B为阴离子交换膜,Na 2 SO 4 溶液应该在Ⅱ区加入,阴极是溶液中水电离出的氢离子放电,电极反应式为:2H 2 O+2e - ═H 2 ↑+2OH - ,在III区是氢氧根放电,该极区生成硫酸和氧气,根据电极反应:2H 2 O+2e - ═H 2 ↑+2OH - ,当转移30mol电子时,生成氢氧化钠为30mol,即1200g,所以电解过程中能量的转化率=
960g
1200g ×100%=80%.
故答案为:阳;阴;Ⅱ;2H 2 O+2e - ═H 2 ↑+2OH - ;H 2 SO 4 溶液、氧气;80%.1年前查看全部
- 电渗析法为什么要用离子交换膜就算阴极区不用阳离子交换膜,阴离子也不会跑到阴极区啊,不是多此一举吗?
 lsj05131年前1
lsj05131年前1 -
 feixingyuan1 共回答了20个问题
feixingyuan1 共回答了20个问题 |采纳率85%因为溶液中阴阳离子同时存在,阴阳膜同时使用提高了除盐效率;另外,也分出浓水、淡水室,将不同离子浓度的溶液分隔开1年前查看全部
- (2013•黄冈一模)如图装置为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为:2
 (2013•黄冈一模)如图装置为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为:2K2S2+KI3
(2013•黄冈一模)如图装置为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为:2K2S2+KI3 K2S4+3KI.装置(Ⅱ)为电解池的示意图.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
K2S4+3KI.装置(Ⅱ)为电解池的示意图.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
A.闭合K时,K+从右到左通过离子交换膜
B.闭合K时,A的电极反应式为:3I--2e-=I3-
C.闭合K时,X的电极反应式为:2Cl--2e-=Cl2↑
D.闭合K时,当有0.1molK+通过离子交换膜,X电极上产生标准状况下气体1.12L 5208121年前1
5208121年前1 -
 wangztt00 共回答了20个问题
wangztt00 共回答了20个问题 |采纳率85%解题思路:当闭合开关K时,X附近溶液先变红,即X附近有氢氧根生成,所以在X极上得电子析出氢气,X极是阴极,Y极是阳极.
与阴极连接的是原电池的负极,所以A极是负极,B极是正极,再根据原电池、电解池原理判断选项.当闭合开关K时,X附近溶液先变红,即X附近有氢氧根生成,所以在X极上得电子析出氢气,X极是阴极,Y极是阳极.与阴极连接的是原电池的负极,所以A极是负极,B极是正极.
A、闭合K时,A是负极B是正极,电子从A极流向B极,根据异性电荷相吸原理,所以K+从左到右通过离子交换膜,故A错误.
B、闭合K时,A是负极,负极上失电子发生氧化反应,电极反应式为2K2S2-2e-═K2S4+2K+,故B错误.
C、闭合K时,X电极是阴极,在阴极上溶液中的氢离子放电生成氢气,所以电极反应式为 2H++2e-=H2↑,故C错误.
D、闭合K时,当有0.1molK+通过离子交换膜,即有0.1mol电子产生,根据氢气与电子的关系式知,生成的氢气体积为1.12L(标况下),故D正确.
故选D.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池及电解池工作原理,有些难度,能准确判断各电极的名称及电极反应是解本题的关键.1年前查看全部
- 有关原电池的问题槽内有一离子交换膜,只允许硫酸根离子通过,膜两边分别有硫酸锌溶液(并插入锌棒)和硫酸铜溶液(并插入铜棒)
有关原电池的问题
槽内有一离子交换膜,只允许硫酸根离子通过,膜两边分别有硫酸锌溶液(并插入锌棒)和硫酸铜溶液(并插入铜棒),为什么用导线连接锌、铜会产生电流? krees1年前1
krees1年前1 -
 狗头86年万众狂欢 共回答了15个问题
狗头86年万众狂欢 共回答了15个问题 |采纳率86.7%在两侧会有液接电位产生,所以会有电流.1年前查看全部
- (2009•茂名二模)现有用离子交换膜和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和
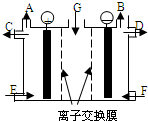 (2009•茂名二模)现有用离子交换膜和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和
(2009•茂名二模)现有用离子交换膜和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和
H2SO4,下列说法中正确的是( )
A.气体A是H2,溶液E是稀硫酸
B.气体B是H2,溶液D是NaOH溶液
C.Na2SO4 溶液由G口加入,F口通入稀硫酸
D.要定期补充水,不用补充Na2SO4 icolor31年前1
icolor31年前1 -
 川银 共回答了13个问题
川银 共回答了13个问题 |采纳率92.3%解题思路:据题意,电解饱和Na2SO4溶液时,阳极附近是OH-放电,生成氧气,阴极附近时H+放电生成氢气,由于装置中放置了离子交换膜,在两极分别生成NaOH和H2SO4,需在阳极室一侧放置阴离子交换膜,只允许通过阴离子,在阴极一侧放置阳离子交换膜,只允许通过阳离子;接电源正极的是阳极,即A极放出氧气;若由F口通入稀硫酸,则将NaOH中和,得不到产品.A、连接电源正极的是电解池的阳极,连接电源负极的是电解池的阴极,A为阳极产生的气体,是氧气,故A错误;
B、阴极发生的反应为:2H2O+2e-═H2↑+2OH-,在阴极上生成H2和NaOH溶液,故B正确;
C、若由F口通入稀硫酸,则将NaOH中和,得不到产品,故C错误;
D、电解的是饱和硫酸钠溶液,实质是电解水,在两极分别得到氢氧化钠和硫酸,需要补充饱和硫酸钠溶液,故D错误.
故选B.点评:
本题考点: 电解原理.
考点点评: 本题考查电解池知识,本题设置新情景,即离子交换膜,注意根据两极上的反应判断生成物,题目难度中等.1年前查看全部
- 电解饱和食盐水制氢氧化钠采用离子交换膜,是不是为了防止阴极室产生的氯气进入阳极?
电解饱和食盐水制氢氧化钠采用离子交换膜,是不是为了防止阴极室产生的氯气进入阳极?
不好意思,打错了,
电解饱和食盐水制氢氧化钠采用离子交换膜,是不是为了防止阳极室产生的氯气进入阴极? gnpjvc20051年前3
gnpjvc20051年前3 -
 江湖情小子刀 共回答了22个问题
江湖情小子刀 共回答了22个问题 |采纳率90.9%1年前查看全部
- 离子交换膜的原理为什么只有阴离子或者阳离子才能通过?
 doux10311年前1
doux10311年前1 -
 小文鸟 共回答了14个问题
小文鸟 共回答了14个问题 |采纳率100%离子交换树脂是一类具有离子交换功能的高分子材料.在溶液中它能将本身的离子与溶液中的同号离子进行交换.按交换基团性质的不同,离子交换树脂可分为阳离子交换树脂和阴离子交换树脂两类.
阳离子交换树脂大都含有磺酸基(—SO3H)、羧基(—COOH)或苯酚基(—C6H4OH)等酸性基团,其中的氢离子能与溶液中的金属离子或其他阳离子进行交换.例如苯乙烯和二乙烯苯的高聚物经磺化处理得到强酸性阳离子交换树脂,其结构式可简单表示为R—SO3H,式中R代表树脂母体,其交换原理为
2R—SO3H+Ca2+ (R—SO3)2Ca+2H+
这也是硬水软化的原理.
阴离子交换树脂含有季胺基[-N(CH3)3OH]、胺基(—NH2)或亚胺基(—NH2)等碱性基团.它们在水中能生成OH-离子,可与各种阴离子起交换作用,其交换原理为
R—N(CH3)3OH+Cl- R—N(CH3)3Cl+OH-
由于离子交换作用是可逆的,因此用过的离子交换树脂一般用适当浓度的无机酸或碱进行洗涤,可恢复到原状态而重复使用,这一过程称为再生.阳离子交换树脂可用稀盐酸、稀硫酸等溶液淋洗;阴离子交换树脂可用氢氧化钠等溶液处理,进行再生.
离子交换树脂的用途很广,主要用于分离和提纯.例如用于硬水软化和制取去离子水、回收工业废水中的金属、分离稀有金属和贵金属、分离和提纯抗生素等.1年前查看全部
- 现在工业上主要采用离子交换膜法电解饱和食盐水制取NaOH、H 2 和Cl 2 。请回答下列问题:
现在工业上主要采用离子交换膜法电解饱和食盐水制取NaOH、H 2 和Cl 2 。请回答下列问题:
⑴在电解过程中,与电源正极相连的电极上所发生的电极反应式为 。
⑵电解之前,食盐水需要精制,目的是除去粗盐中的、Ca 2+ 、Mg 2+ 、SO 4 2 - 等杂质离子,使用的试剂有:a.Na 2 CO 3 溶液,b.Ba(OH) 2 溶液,c.稀盐酸,其合理的加入顺序为(填试剂序号) 。
⑶如果在容积为10L的离子交换膜电解槽中,1min后在阴极可产生11.2L(标准状况)Cl 2 ,这时溶液的pH值是 (填“升高”、“降低”或“不变”),溶液中c(OH - )为(设体积保持不变) 。
⑷若没有阳离子交换膜的存在,则电解饱和食盐水的化学方程式是
。 木马速递1年前0
木马速递1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 用离子交换膜提取出Na离子溶液,蒸发后Na离子溶液,是否会获得Na离子结晶?
 fjlyxwh1年前2
fjlyxwh1年前2 -
 涞捉苍蝇的 共回答了23个问题
涞捉苍蝇的 共回答了23个问题 |采纳率91.3%用离子交换膜提取的Na离子溶液也是呈电中性的,溶液里面还有OH离子等,如果没有其他元素的离子,蒸发后会形成NaOH结晶.1年前查看全部
- 问下电解池的产生电流的问题离子交换膜只允许阳离子通过 ,也就是溶液只有阳离子能在阴阳极之间移动 阴离子不能通过,只能在一
问下电解池的产生电流的问题
离子交换膜只允许阳离子通过 ,也就是溶液只有阳离子能在阴阳极之间移动 阴离子不能通过,只能在一极附近,那为什么还能产生电流.
阴离子过不去 就没有负电荷的传递啊.. 秋云暗几重1年前1
秋云暗几重1年前1 -
 甘奇燕 共回答了16个问题
甘奇燕 共回答了16个问题 |采纳率93.8%阳离子向一个方向移动就等价于阴离子向另一个方向移动1年前查看全部
- 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42
电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是
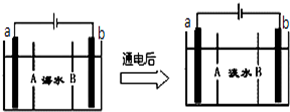
(1)A膜是______离子交换膜
(2)通电后,a电极的电极反应式为______
(3)通电后,b电极上______产生的现象为______. 面包树1年前1
面包树1年前1 -
 Elva英子 共回答了11个问题
Elva英子 共回答了11个问题 |采纳率81.8%(1)阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过,隔膜A和阳极相连,阳极是阴离子放电,所以隔膜A是阴离子交换膜,
故答案为:阴;
(2)通电后,a电极为阳极,阳极是氯离子放电,生成氯气,其电极反应为:2Cl--2e-═Cl2↑;
故答案为:2Cl--2e-=Cl2↑;
(3)通电后,b电极为阴极,阴极区是氢离子得到电子生成氢气,氢氧根离子浓度增大,和钙离子,镁离子形成沉淀,
故答案为:产生无色气体,溶液中出现少量白色沉淀.1年前查看全部
- “左侧的IO3-通过阴离子交换膜向右侧移动”,为什么?这个离子交换膜是怎回事?在这里干什么用?
“左侧的IO3-通过阴离子交换膜向右侧移动”,为什么?这个离子交换膜是怎回事?在这里干什么用?
A怎么判断不是氧气还原为氢氧根 小妍2221年前1
小妍2221年前1 -
 天地无用唯我独尊 共回答了22个问题
天地无用唯我独尊 共回答了22个问题 |采纳率95.5%离子交换膜是一种含离子基团的、对溶液里的离子具有选择透过能力的高分子膜,和细胞膜相似.阴离子交换膜只允许阴离子在溶液中移动,而阳离子不可以.1年前查看全部
- (8分)目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图。
(8分)目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图。

(1)下列说法不正确的是
(2)现有离子交换膜A和B将电解槽分为I、II、III三个区域(下图所示),在这种电解池中电解Na 2 SO 4 溶液可制得氢氧化钠、硫酸等物质。A为 离子交换膜、B为 离子交换膜(填“阴”或“阳”),电极均为惰性电极。Na 2 SO 4 溶液应该在 区(填“I”、“II”、“III”)加入。通电电解时阴极的电极反应式为 ,在III区得到 。当外电路总共通过30 mol电子时,生成的NaOH 960克,则电解过程中能量的转化率为:A.从E口逸出的气体是H 2 B.从B口加入含少量NaOH的水溶液以增强导电性 C.标准状况下每生成22.4 L Cl 2 ,便产生2 mol NaOH D.粗盐水中含Ca 2+ 、Mg 2+ 、Fe 3+ 、SO 4 2- 等离子,精制时先加 Na 2 CO 3 溶液  tangdianwei1年前1
tangdianwei1年前1 -
 心口如一 共回答了17个问题
心口如一 共回答了17个问题 |采纳率82.4%(8分)(1)D(2分)
(2)阳(1分)阴(1分) II (1分) 2H 2 O + 2e - === H 2 ↑ + 2OH - (1分)
H 2 SO 4 溶液、氧气(1分) 80%
略1年前查看全部
- 请熟悉化工的各位大侠汉译英请大侠们把这几个翻译成英语:鼓泡,阳极液浓度,离子交换膜,开停车
 不穿窑裤儿1年前1
不穿窑裤儿1年前1 -
 丁XY 共回答了15个问题
丁XY 共回答了15个问题 |采纳率73.3%鼓泡:Bubble
阳极液浓度:Concentration of anodic solution
离子交换膜:Ion-exchange membrane
开停车:Start and Stop Production1年前查看全部
大家在问
- 1读全球主要温室气体在大气中的含量变化表,完成下列问题。
- 2not any more和no more 造句(俩个词组相等.要句意一样的句子)
- 3(mary) is writing aletter to her pen pal对括号内提问
- 4过年了 作文怎么写?300-400字 详略得当
- 5I will always waiting for you and forever 这是病句吗?怎么改呢?
- 6碳素笔的英语怎么写?
- 7根据短文内容和所给汉语提示,写出短文空白处各单词的正确形式。每空限填一词。
- 8HCO3根的电离与水解的大小HCO3-水解程度大于电离程度因为他本来碳酸2元弱酸 第2步电离的难于第一步电离也就是说H2
- 9一句名言的启示 作文
- 10文言文 关伊子教射说明了什么道理?用一句名言概括.
- 11初二下册英语《全品作业本》p35-36
- 12c=15.7m d=( ) r=( )
- 13字意分析?圆滑,有时用来形容人,可圆滑本意是什么?那样的人可用圆滑来形容?
- 14一个两位数除以3余2这个两位数最小是多少?最大呢?算式怎么写?
- 15写出表示想的成语3个5分钟内给我

