用酚酞试液(填能或不能)检验氢氧化钠变质为什么?
 柏杨灵魂附体2022-10-04 11:39:541条回答
柏杨灵魂附体2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 单身汉哦 共回答了17个问题
单身汉哦 共回答了17个问题 |采纳率94.1%- 不能.
碳酸钠也是碱性的 - 1年前
相关推荐
- 酚酞试液是用多少酚酞固体配多少水?
酚酞试液是用多少酚酞固体配多少水?
那我刚才把酚酞放到NaOH水溶液里怎么变红了?而且在扩散? yatouangel1年前1
yatouangel1年前1 -
 my5969171 共回答了25个问题
my5969171 共回答了25个问题 |采纳率100%酚酞是不溶于水的,而易溶于酒精.酚酞试液是酚酞的酒精溶液,无色.酚酞试液在碱性溶液里呈红色,在酸性和中性溶液里为无色.使用酚酞试液检验溶液的酸碱性时,用试管取2mL~3mL被测溶液,滴加几滴酚酞试液,振荡后,观察溶液的颜色变化.用滤纸浸蘸酚酞试液,晾干后即为酚酞试纸.使用方法与使用石蕊试纸样.1年前查看全部
- 亚硝酸钠有咸味、水溶液呈碱性、食盐水溶液呈中性、鉴别的试剂为酚酞试液、为什么不是石蕊
 shiyingming1年前2
shiyingming1年前2 -
 风云散 共回答了18个问题
风云散 共回答了18个问题 |采纳率83.3%石蕊 要比较强的碱性溶液才变为蓝色
NaNO2水溶液碱性不够强.不变色1年前查看全部
- 【回答好的我追加分,急!】下列各组稀溶液,只用酚酞试液和互换反应就可以鉴别出来的是( ).
【回答好的我追加分,急!】下列各组稀溶液,只用酚酞试液和互换反应就可以鉴别出来的是( ).
1.下列各组稀溶液,只用酚酞试液和互换反应就可以鉴别出来的是( ).
A.稀硫酸 氢氧化钠 氯化钠 氯化钡
B.氢氧化钾 氢氧化钠 稀盐酸
C.稀盐酸 稀硝酸 氢氧化钙
D.氢氧化钡稀硫酸 稀盐酸 硫酸钠
2.
现有三组物质:①金刚石 水银 金属钠 水②五氧化二磷 干冰 生石灰 一氧化碳③食醋 白酒 加碘食盐 纯碱.每组中均有一种物质所属类别与其他三种不同,这三种物质依次是( )、( )、( );他们混合后可以发生反应得到一种重要的化工原料,其反应的化学方程式为: puppy3131年前1
puppy3131年前1 -
 秋蚕1 共回答了18个问题
秋蚕1 共回答了18个问题 |采纳率94.4%1.D:加酚酞,鉴别出氢氧化钡
把适量氢氧化钡加入剩余三种溶液,无现象的是稀盐酸
白色沉淀是稀硫酸和硫酸钠
再加酚酞,变红说明是硫酸钠(硫酸钠和氢氧化钡反应生成硫酸钡沉淀和氢氧化钠)
2.水(为化合物)、生石灰(碱性氧化物)、纯碱(纯净物)
水+生石灰====氢氧化钙
氢氧化钙+碳酸钠====碳酸钙+2氢氧化钠1年前查看全部
- 如图,做氨分子运动实验时,将滴有酚酞试液的滤纸条放在试管里.
如图,做氨分子运动实验时,将滴有酚酞试液的滤纸条放在试管里.

(1)用______吸取浓氨水,滴在管口棉花上,可观察到的现象是______.
(2)实验中往往在试管下放一张白纸,白纸的作用是______.
(3)某同学在做此实验时,发现滤纸条的颜色没有改变,而试管口的棉花却变色了,发生该现象的可能原因是______. elvia7231年前1
elvia7231年前1 -
 y大不同 共回答了15个问题
y大不同 共回答了15个问题 |采纳率86.7%解题思路:微观粒子总是不断运动的.浓氨水中的氨分子不断运动,向四周扩散,与酚酞试液相遇时,溶于水又形成氨水,氨水属于碱,碱性溶液能使无色的酚酞试液变红.(1)一般用胶头滴管取用少量液体.氨分子不断运动,向四周扩散能使酚酞试液变红.
故填:滤纸条上的酚酞试液由管口向管底逐渐变红.
(2)为了便于观察,通常铺一层白纸.
故填:便于观察实验.
(3)可能把酚酞试剂和浓氨水的位置颠倒了.
故填:把无色酚酞滴在棉花上,把氨水滴在滤纸条上.点评:
本题考点: 微粒观点及模型图的应用.
考点点评: 本题主要考查了微观粒子的特征及其碱性溶液与酚酞试液相互作用显色的情况.1年前查看全部
- 1.为什么使酚酞试液变红的不一定是碱溶液?请举例.2.为什么使石蕊试液变红的溶液却不能使酚酞试液变色
 右岸左手1年前5
右岸左手1年前5 -
 海de鱼 共回答了22个问题
海de鱼 共回答了22个问题 |采纳率90.9%使酚酞试液变红只能说明溶液显碱性,不一定是碱,如Na2CO3溶液就能使酚酞试液变红.
使石蕊试液变红的溶液显酸性,酸性溶液不能使酚酞显色.1年前查看全部
- 氢氧化钙溶液滴入石蕊试液后的现象?滴入酚酞试液后的现象?
 嫣嫣261年前2
嫣嫣261年前2 -
 daifeng_ustc 共回答了22个问题
daifeng_ustc 共回答了22个问题 |采纳率95.5%滴入石蕊后变蓝.
滴入酚酞后变红.
满意请采纳(手机版点“满意”即可)1年前查看全部
- 在盛有少量蒸馏水的注烧杯中滴入2~3滴酚酞试液,再向其中滴加浓氨水.由实验得出的结论是什么?
 乱飞的蝴蝶1年前1
乱飞的蝴蝶1年前1 -
 pgq423 共回答了26个问题
pgq423 共回答了26个问题 |采纳率69.2%无色酚酞溶液变红,结论:浓氨水呈碱性1年前查看全部
- 某无色溶液滴入酚酞试液后显红色,下列离子组中能在该溶液里大量共存的是
某无色溶液滴入酚酞试液后显红色,下列离子组中能在该溶液里大量共存的是
A.Cl-、Mg2+、Na+、NO3-
B.Ca2+ Cl- K+ NO3-
C.K+ NO3- Ba2+ MnO4-
D CO3(2-) Na+ SO4(2-) K+
我知道选D,但是从那个方面分析呢?Mg Ca Na K不都会溶于OH-根吗?那怎么还可以大量共存? 普罗旺斯的夜1年前1
普罗旺斯的夜1年前1 -
 miumiu12 共回答了14个问题
miumiu12 共回答了14个问题 |采纳率78.6%无色溶液滴入酚酞试液后显红色,证明是有OH-
A.Cl-、Mg2+、Na+、NO3-,Mg(OH)2,沉淀,Mg2+不能和OH-共存
B.Ca2+ Cl- K+ NO3-,Ca(OH)2微溶,OH-不能和Ca2+大量共存
C.K+ NO3- Ba2+ MnO4-,MnO4-是紫色
答案是D1年前查看全部
- 在含有CO2-3且能使酚酞试液变红的无色溶液中,能大量共存的离子组是( )
在含有CO2-3且能使酚酞试液变红的无色溶液中,能大量共存的离子组是( )
A.Na+、(SO3)2-、(SO4)2-、K+ x05x05B.Na+、Cu2+、Br-、Ba2+
C.K+、MnO4-、NO3-、Na+ x05x05D.K+、Ca2+、(SO3)2-、Cl- Bwtv1年前3
Bwtv1年前3 -
 27387403 共回答了12个问题
27387403 共回答了12个问题 |采纳率100%选A
B.Na+、Cu2+、Br-、Ba2+
Cu2+有颜色
Ba2+CO32-不共存
C.K+、MnO4-、NO3-、Na+
MnO4- 有颜色 x09x09
D.K+、Ca2+、(SO3)2-、Cl-
Ca2+、与(SO3)2-CO32-不共存1年前查看全部
- 鲁教版九年级全一册第二节,研究中和反应,先在氢氧化钠中滴加无色酚酞试液,试液变红,慢慢滴加稀盐酸,为什么慢慢滴加时反应不
鲁教版九年级全一册第二节,研究中和反应,先在氢氧化钠中滴加无色酚酞试液,试液变红,慢慢滴加稀盐酸,为什么慢慢滴加时反应不明显,还是红色,而到了一定时刻滴加一滴马上就变无色了吗?按理说应该是一边滴加红色一边变弱,为什么这个反应中要等到某一滴滴下时才突然变色?
为什么会有这么一个过程?log规定是什么?我们没有学到 救救工人1年前1
救救工人1年前1 -
 ak6412083 共回答了21个问题
ak6412083 共回答了21个问题 |采纳率95.2%pH中和滴定时有一个滴定突跃的过程.比如有0.1mol/L的盐酸20mL,0.1mol/L的烧碱20mL,碱滴酸.如果你算一下pH就会发现,当NaOH加到19.98mL时,那时的pH还在5左右,20mL时变成7,20.02mL时直接就变9了.因为pH的log规定是10倍关系,所以滴定完成就是那一滴不到的事,往往是一滴滴下就突然从酸变到碱了.
我来补充一下:
pH的定义是溶液中氢离子物质的量浓度的负对数.也就是说pH=-lg(c(H+)),lg是以10为底的log对数运算
比如说,10^-1=0.1,那么lg0.1=-1,10^-3=0.001,那么lg0.001=-3,也就是说它求的是指数.那么pH=1的盐酸与pH=2的盐酸,虽然pH只差1,但氢离子浓度已经差了10倍之多.
当加入19.98mLNaOH时,溶液中原有H+为20*10^-3*0.1=2*10^-3mol,加入的OH-为19.98*10^-3*0.1=1.998*10^-3,所以反应完H+还剩下了2*10^-6mol,此时溶液体积为39.98mL,所以H+的浓度为2*10^-6/0.03998=5.003*10^-5,用计算器上的log键取一下对数,pH=4.3.也就是说加入19.98mL烧碱时,pH=4.3.加入20mL时,毫无疑问完全中和,pH=7.按照上面的算法,可以算出20.02mL时,pH在9.7左右.所以pH在0.04mL这么小的范围里突然从4.3变成了9.7,这是非常快的.酚酞在一滴液体滴下的瞬间就变色了1年前查看全部
- 初三化学实验题学校实验室有A、B、C三瓶无色溶液放错了试剂瓶,它们可能是硫酸、碳酸钠、氢氧化钠溶液,现给你酚酞试液和稀盐
初三化学实验题
学校实验室有A、B、C三瓶无色溶液放错了试剂瓶,它们可能是硫酸、碳酸钠、氢氧化钠溶液,现给你酚酞试液和稀盐酸.请你设计一个实验方案,把它们一一鉴别出来.
实验操作 预计出现的现象 你的结论
 dwamd1年前1
dwamd1年前1 -
 喜欢孤独的猫 共回答了21个问题
喜欢孤独的猫 共回答了21个问题 |采纳率100%取三支洁净的试管,分别取少量上述三种溶液.
滴加酚酞,不变色的为硫酸,变红的是碳酸钠、氢氧化钠溶液.
滴加稀盐酸,颜色消失并产生气体的为碳酸钠,红色逐渐消失,无其他明显现象的是氢氧化钠.1年前查看全部
- 1、下列各组溶液中,只用酚酞试液和同组稀溶液间的相互反映就能鉴别的是( ) A、硝酸钾、氯化钠、氢氧化
1、下列各组溶液中,只用酚酞试液和同组稀溶液间的相互反映就能鉴别的是( ) A、硝酸钾、氯化钠、氢氧化
1、下列各组溶液中,只用酚酞试液和同组稀溶液间的相互反映就能鉴别的是( )
A、硝酸钾、氯化钠、氢氧化钠 B、氢氧化钠、氢氧化钾、盐酸
C、硫酸、盐酸、氢氧化钠 D、氢氧化钠、硫酸、氯化钠
2、下列各组物质在水溶液中能大量共存,且溶液为无色的有( )
A、碳酸钠、硝酸钾、氯化钠 B、硫酸钠、氯化钾、硝酸铁
C、硫酸钠、氯化钡、硝酸钠 D/硝酸钾、氯化钠、硫酸铜
3、实验室分解过氧化氢法制氧气时,加入少量二氧化锰在化学反应前后,正确的是( )
A、质量减少 B、质量增加 C、化学性质改变 D、化学性质不变 潜流天下1年前4
潜流天下1年前4 -
 万能的神 共回答了20个问题
万能的神 共回答了20个问题 |采纳率100%1.D
2.A
3.D1年前查看全部
- 用无色酚酞试液来区分盐酸、氢氧化钠溶液和水三种物质,设计实验,不增加其他实验设施和药品!
 50370071年前3
50370071年前3 -
 hogan 共回答了19个问题
hogan 共回答了19个问题 |采纳率78.9%取这三种物质分别装在三支试管中,分别滴加酚酞试液,变红者为氢氧化钠溶液,再把已经变红的氢氧化钠溶液分成两份,分别向里面滴加另外两种物质(即水和盐酸),滴加到一定量,若红色褪去,则滴加的为盐酸,若红色只是变浅而不退去,则滴加的是水.1年前查看全部
- 有一瓶溶液,它的pH值是4.5,注入少量于试管中,再滴入几滴酚酞试液,溶液呈____色.如果要使试管里的溶液
 tclzcja1年前1
tclzcja1年前1 -
 yzshgz 共回答了12个问题
yzshgz 共回答了12个问题 |采纳率91.7%无色.
酚酞遇碱显红色,在酸性溶液中无色.1年前查看全部
- 【初中化学】向滴有酚酞试液的氢氧化钠溶液中滴加过量的盐酸,溶液由红色逐渐变成无色
【初中化学】向滴有酚酞试液的氢氧化钠溶液中滴加过量的盐酸,溶液由红色逐渐变成无色
向滴有酚酞试液的氢氧化钠溶液中滴加过量的盐酸,溶液由红色逐渐变成无色。
这句话对吗?
为什么以前我学习时,被告知“指示剂是突然变色,不是随酸碱度逐渐变化”呢?
还有,红磷在空气中燃烧,产生大量白色烟雾。
这句话对吗?
以上两个是单选,只有一句是对的,应该选哪个?
 JOYCZM1年前4
JOYCZM1年前4 -
 lai713 共回答了21个问题
lai713 共回答了21个问题 |采纳率76.2%向滴有酚酞试液的氢氧化钠溶液中滴加过量的盐酸,溶液由红色逐渐变成无色。
对,先变粉红,后变无色的
红磷在空气中燃烧,产生大量白色烟雾。
不对,只是生成白色烟,没有雾的,不是白色烟雾1年前查看全部
- 浓氨水使酚酞试液变红的实验中,酚酞试液变红了,为什么氨水不变化红?
 xinyz71年前2
xinyz71年前2 -
 ellen8116 共回答了20个问题
ellen8116 共回答了20个问题 |采纳率85%氨水挥发出氨气,氨气极易溶于水,就溶到了酚酞溶液的水中,酚酞溶液遇碱(氨水是弱碱)变红了.相反,酚酞不能挥发出,再溶到氨水里,氨水就不会变红了.1年前查看全部
- 下列说法正确的是( )A. 碱溶液能使酚酞试液变红,所以能使酚酞变红的一定是碱溶液B. 向某固体中滴加稀盐酸,有气体生
下列说法正确的是( )
A. 碱溶液能使酚酞试液变红,所以能使酚酞变红的一定是碱溶液
B. 向某固体中滴加稀盐酸,有气体生成,则该固体一定是碳酸盐
C. 溶液一定是均一、稳定的混合物
D. 有盐和水生成的反应,一定是中和反应 lbbj1年前1
lbbj1年前1 -
 cara4** 共回答了25个问题
cara4** 共回答了25个问题 |采纳率92%解题思路:A、酚酞是检验溶液酸碱性的,呈碱性的不一定是碱.
B、与盐酸反应生成气体的常见的气体有二氧化碳、氢气等,可据此分析.
C、根据溶液的特征进行分析.
D、根据中和反应定义的实质进行分析.A、酚酞与碱性溶液变红色,但溶液呈碱性的不一定是碱,还有盐如碳酸钠溶液,所以错误.
B、与盐酸反应生成气体的固体很多,如活泼金属、碳酸盐、碳酸氢盐等,所以错误.
C、溶液是均一、稳定的混合物,正确.
D、中和反应的反应物必须是酸和碱,生成盐和水的反应的反应物不一定是酸和碱,如二氧化碳和氢氧化钠,氧化铜和盐酸等.所以错误.
故选C点评:
本题考点: 证明碳酸盐;溶液的概念、组成及其特点;酸碱指示剂及其性质;中和反应及其应用.
考点点评: 对概念的理解要抓住内涵和外延,不能断章取义,如中和反应必须是酸和碱反应,还必须生成盐和水;再如简单的概念单质,单质必须是由同种元素组成,还必须是纯净物,任何偷换概念都可能错误.1年前查看全部
- 有关溶解度的化学题将7.3%的稀盐酸滴入盛有10%的碳酸钠溶液(滴有两滴酚酞试液)的烧杯中,恰好完全反应时消耗此稀盐酸的
有关溶解度的化学题
将7.3%的稀盐酸滴入盛有10%的碳酸钠溶液(滴有两滴酚酞试液)的烧杯中,恰好完全反应时消耗此稀盐酸的质量为10g。计算:(1)求碳酸钠溶液的质量;(2)求所得溶液中溶质的质量分数(酚酞试液质量不计)。
急需!明天考试!!! wqfvip1年前2
wqfvip1年前2 -
 rivorivo 共回答了19个问题
rivorivo 共回答了19个问题 |采纳率78.9%1.
Na2CO3 + 2HCl= 2NaCl + H20 + CO2
106。。。。73。。。。117。。。。。。。44
x。。。100x7.3%.。。。y.。。。。。。。z
106/x=73/100x7.3%
117/y=73/100x7.3%
44/z=73/100x7.3%
x=10.6g
y=11.7g
z=4.4g
碳酸钠溶液的质量=10.6/10%=106g
反应后的溶质是NaCl,质量是11.7g
根据质量守恒定律,溶液的质量是100+106-4.4=201.6g
所以所得溶液中溶质的质量分数11.7/201.6x100%=5.8%1年前查看全部
- 有失去标签的硫酸、盐酸、氢氧化钠三瓶溶液.拟用BaCl2溶液和酚酞试液按下列步骤鉴别:
有失去标签的硫酸、盐酸、氢氧化钠三瓶溶液.拟用BaCl2溶液和酚酞试液按下列步骤鉴别:
(1)从三支试管分别移取各溶液少许作试样,向试样中分别滴加______,如发生的现象是______,所取得溶液是H2SO4,相关的化学方程式为:______;
(2)将剩余的两种试样各取少许放入另外两支试管中,分别滴加______,如发生现象为______,所取得溶液为NaOH溶液.
(3)无明显现象的为______. 秀南1年前1
秀南1年前1 -
 54lawer 共回答了21个问题
54lawer 共回答了21个问题 |采纳率81%解题思路:(1)盐酸和硫酸都是酸,都具有相同的氢离子,而它们的阴离子是不同的,可以根据硫酸根离子与氯化钡反应生成白色的沉淀,而氯离子不会与氯化钡反应进行鉴别.
(2)盐酸和氢氧化钠分别属于酸和碱,根据酸碱指示剂遇到酸碱显示不同的颜色,用酚酞区分盐酸和氢氧化钠.(1)盐酸和硫酸都是酸,都具有相同的氢离子,而它们的阴离子是不同的,可以根据硫酸根离子与氯化钡反应生成白色的沉淀,而氯离子不会与氯化钡反应,可以区分出盐酸和硫酸.
故答案为:BaCl2溶液,溶液出现白色沉淀,BaCl2+H2SO4═BaSO4↓+2HCl.
(2)盐酸和氢氧化钠分别属于酸和碱,根据酸碱指示剂遇到酸碱显示不同的颜色,酚酞遇碱变红色,酚酞遇酸不变色.
故答案为:酚酞试剂,溶液变成红色
(3)酚酞遇盐酸不变色,所以加入酚酞不变色的是盐酸,故答案为:盐酸.点评:
本题考点: 反应现象和本质的联系;酸碱指示剂及其性质;酸的化学性质;碱的化学性质;物质的鉴别、推断;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查了利用酸中阳离子的不同来鉴别酸,利用酸碱指示剂遇酸碱显示不同颜色鉴别酸碱.1年前查看全部
- 哪个氧化物的水溶液中滴入无色酚酞试液后变红色 Na2O CuO SO2 CaO
 zhangwentao10191年前3
zhangwentao10191年前3 -
 丝雨_mm 共回答了19个问题
丝雨_mm 共回答了19个问题 |采纳率78.9%Na2O溶于水生成氢氧化钠,是碱性,滴入无色酚酞试液后变红色
CuO不溶于水,不变红
SO2溶于水生成酸,不变红
CaO溶于水生成氢氧化钙,是碱性,滴入无色酚酞试液后变红色1年前查看全部
- 某工厂化验室用10.0%的氢氧化钠溶液16.0g滴加到20.0g盐酸中(含几滴酚酞试液,质量忽略不计),混合液刚好由无色
某工厂化验室用10.0%的氢氧化钠溶液16.0g滴加到20.0g盐酸中(含几滴酚酞试液,质量忽略不计),混合液刚好由无色变成粉红色时,可认为恰好反应.原盐酸中溶质的质量分数为多少?
 惊涛拍俺1年前1
惊涛拍俺1年前1 -
 半瓣眼泪 共回答了19个问题
半瓣眼泪 共回答了19个问题 |采纳率94.7%解题思路:氢氧化钠和盐酸反应生成氯化钠和水,根据氢氧化钠溶液质量、溶质质量分数可以计算氢氧化钠的质量,根据氢氧化钠质量可以计算盐酸中氯化氢的质量,进一步可以计算原盐酸中溶质的质量分数.设原盐酸中溶质氯化氢的质量为x,
NaOH+HCl═NaCl+H2O
4036.5
16.0g×10.0% x
[40/16.0g×10.0%=
36.5
x]
x=1.46g
原盐酸中溶质的质量分数为:[1.46g/20.0g]×100%=7.3%
答:原盐酸中溶质的质量分数为7.3%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.1年前查看全部
- 红色石蕊试纸和紫色石蕊试液和酚酞试液三者有那样区别
 财务ee1年前1
财务ee1年前1 -
 为梦而活 共回答了7个问题
为梦而活 共回答了7个问题 |采纳率100%石蕊试纸有红色石蕊试纸和蓝色石蕊试纸两种.红色用来检验碱性物质,蓝色用来检验酸性物质.碱性溶液使红色试纸变蓝,酸性溶液使蓝色试纸变红.石蕊试纸可以检验气体的酸碱性.
紫色石蕊试液用于帮助判断液体的酸碱性.滴入紫色石蕊试液,如果试液显红色,则说明液体显酸性;如果试液显蓝色,则说明液体显碱性.
酚酞遇酸溶液不变色,遇中性溶液也不变色,遇碱溶液变红色.用来检验碱性物质.1年前查看全部
- 在试管里加少量的氢氧化钠溶液,然后滴加几滴酚酞试液,会有什么现象
 荫道发言1年前4
荫道发言1年前4 -
 yang_zi 共回答了18个问题
yang_zi 共回答了18个问题 |采纳率83.3%溶液变红,因为碱性溶液遇酚酞试液会变红1年前查看全部
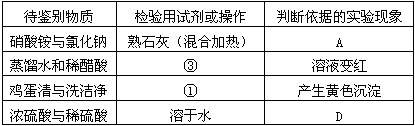
- 下表中有4组物质需要鉴别,试选择合理答案的序号填下表空格中。 ★检验用试剂或操作:①浓硫酸(微热) ②无色酚酞试液 ③紫
下表中有4组物质需要鉴别,试选择合理答案的序号填下表空格中。 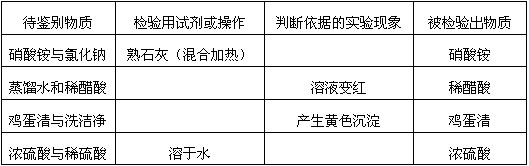
★检验用试剂或操作:①浓硫酸(微热) ②无色酚酞试液 ③紫色石蕊试液 ④饱和硫酸铵溶液
★判断依据的实验现象:A.产生能使湿润的红色石蕊试纸变蓝的刺激性气味的气体 B.溶液温度降低 C.产生能使湿润的蓝色石蕊试纸变红的刺激性气味的气体 D.溶液温度升高 流浪八月1年前1
流浪八月1年前1 -
 阿莫西林AMOR 共回答了16个问题
阿莫西林AMOR 共回答了16个问题 |采纳率93.8%1年前查看全部
- U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。下列说法正确的
U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。下列说法正确的是

A.开始时左边溶液呈蓝色,右边溶液呈红色 B.开始时左边溶液呈无色,右边溶液呈红色 C.充分反应后U形管中溶液可能呈红色 D.充分反应后U形管中溶液一定呈无色  小新心1年前1
小新心1年前1 -
 jjxxw 共回答了23个问题
jjxxw 共回答了23个问题 |采纳率82.6%C
A、氢氧化钠呈碱性,能使酚酞变红,稀盐酸呈酸性,使酚酞试液不变色,故开始时左边溶液为无色,右边溶液为红色,不是无色,故A错误;
B、氢氧化钠呈碱性,能使酚酞变红,开始时右边为红色,不是蓝色,故B错误;
C、充分反应后溶液可能呈碱性,故溶液可能为红色,故C正确;
D、由于酸碱的量不确定,所以充分反应后酸碱剩余情况不确定,所以颜色不确定,故D错误;
故选C.1年前查看全部
- 已知A是一种金属,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如下变化关系
已知A是一种金属,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如下变化关系:

(1)A的名称是 ; F的化学式是 。
(2)C+B→D反应的化学方程式为 。
(3)F+D→C反应的化学方程式为 。
(4)F在空气中遇水蒸气产生白雾现象这白雾实际上是 。 dyy03561年前1
dyy03561年前1 -
 新零距离 共回答了13个问题
新零距离 共回答了13个问题 |采纳率69.2%(10) (1)钠; HCl (2)NH 4 Cl + NaOH ="NaCl" + NH 3 ↑+ H 2 O。
(3)NH 3 + HCl=NH 4 Cl. (4)氯化氢气体与空气中水蒸气形成小液滴
1年前查看全部
- CaO会使无色酚酞试液变红吗?
 弦弦一音1年前3
弦弦一音1年前3 -
 醴陵346 共回答了26个问题
醴陵346 共回答了26个问题 |采纳率80.8%会,因为CAo与水反应生成Ca(OH)21年前查看全部
- 碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性这句话对不?
碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性这句话对不?
如题, **我痛心1年前1
**我痛心1年前1 -
 不管不顾 共回答了9个问题
不管不顾 共回答了9个问题 |采纳率100%呈碱性是对的,但不能说是碱,因碳酸钠虽然是碱,但却呈碱性.1年前查看全部
- 下列溶液的PH值最大A.滴入紫色石蕊试液呈红色的溶液 B.滴入紫色石蕊试液呈紫色的溶液C.滴入无色酚酞试液呈红色的溶液
下列溶液的PH值最大
A.滴入紫色石蕊试液呈红色的溶液 B.滴入紫色石蕊试液呈紫色的溶液
C.滴入无色酚酞试液呈红色的溶液 D.滴入无色酚酞试液呈无色的溶液
为什么? emma_1211年前4
emma_1211年前4 -
 zjw327 共回答了14个问题
zjw327 共回答了14个问题 |采纳率71.4%石蕊试液
pH ------------5-----------8-----------------------
红 紫 蓝
pH ----------------------------8------------10---------
无色 浅红 红色
A.滴入紫色石蕊试液呈红色的溶液 pH1年前查看全部
- 在氢氧化钠溶液( 色)中加入酚酞试液( 色)产生什么的现象?里面的什么颜色也帮忙回答下,
 只爱自己1年前1
只爱自己1年前1 -
 阿修罗一平 共回答了13个问题
阿修罗一平 共回答了13个问题 |采纳率76.9%在氢氧化钠溶液(无 色)中加入酚酞试液( 无 色)产生的现象:
无色酚酞试液变为红色
原因是:酚酞遇到碱性物质,能变红1年前查看全部
- 在烧杯A中装入10毫升浓氨水(氨水是一种易出氨气的液体),在烧杯B、C中分别中装入20毫升滴有2到3滴酚酞试液的蒸馏水(
在烧杯A中装入10毫升浓氨水(氨水是一种易出氨气的液体),在烧杯B、C中分别中装入20毫升滴有2到3滴酚酞试液的蒸馏水(酚酞试液遇碱性溶液变成红色,遇酸性溶液不变色),用一只大烧杯把A、B两烧杯溶液罩在一起,取另一只大烧杯把C杯溶液罩住.过一会儿发现B杯出现红色,A、C烧杯无变化.试分析出现这种现象发生上述现象的原因.
 蓝天宝贝1年前1
蓝天宝贝1年前1 -
 whw2006 共回答了15个问题
whw2006 共回答了15个问题 |采纳率73.3%浓氨水中的氨气挥发(分子运动) 酚酞试液遇氨变成红色 所以B红了
然后因为有杯子隔着 C无变化1年前查看全部
- 小梅看到滴加酚酞试液的NaOH溶液褪色,就说SO2溶于水后生成酸.小明认为这种说法不对.为什么这么说?
 5119111年前3
5119111年前3 -
 渺mang 共回答了20个问题
渺mang 共回答了20个问题 |采纳率80%上面的乱说(酚酞不会被空气里面的氧气给氧化,不然做酸碱滴定时酚酞老早没用了),使酚酞在碱性下褪色有两种方法,一种是使他变成酸性环境,另一种是使酚酞发生变化.因为二氧化硫有一定的还原性,可能会是酚酞的结构发生变化,二氧化硫使品红发生褪色就是这种机理.1年前查看全部
- 下列物质的水溶液能使无色酚酞试液变红,但物质本身不是碱的是
下列物质的水溶液能使无色酚酞试液变红,但物质本身不是碱的是
1.SO3
2.CaO
3.NaOH
4.NaCL hskj0071年前1
hskj0071年前1 -
 jinjianhui 共回答了15个问题
jinjianhui 共回答了15个问题 |采纳率93.3%选2.
1.不能使酚酞变红,酸性的.SO3+H2O=H2SO4
2.CaO+H2O=Ca(OH)2,CaO是氧化物,不是碱.
3.NaOH是碱,可以使无色酚酞试液变红.
4.NaCl是中性的,遇到无色酚酞试液不变色.1年前查看全部
- 现有两瓶滴加了酚酞试液的稀硫酸和食盐水,区分它们的最理想方法是
 kikirain1年前1
kikirain1年前1 -
 太阳绕我转 共回答了16个问题
太阳绕我转 共回答了16个问题 |采纳率75%两种溶液各取少量
滴入一滴氢氧化钠溶液,
不变红的是稀硫酸,变红的是食盐水1年前查看全部
- 以下物质中不能使酚酞试液变红的是?
以下物质中不能使酚酞试液变红的是?
A.氢氧化钠溶液 B.碳酸钠溶液 C.氢氧化铁 D.石灰水 山水芝麻1年前6
山水芝麻1年前6 -
 crazychater 共回答了22个问题
crazychater 共回答了22个问题 |采纳率86.4%答案是C
因为氢氧化铁属于难溶物,在水中溶解度很小.所以并不能使酚酞变红1年前查看全部
- 在一次实验开放日活动中,小明同学取出一无色溶液,向其中滴加酚酞试液后变红色.小明同学做出的下列结论中正确的是( )
在一次实验开放日活动中,小明同学取出一无色溶液,向其中滴加酚酞试液后变红色.小明同学做出的下列结论中正确的是( )
A. 该溶液能使石蕊试液变成红色
B. 该溶液的pH小于7
C. 该溶液中的溶质一定是某种碱
D. 该溶液显碱性 foreign_ghost1年前6
foreign_ghost1年前6 -
 老狼曰 共回答了21个问题
老狼曰 共回答了21个问题 |采纳率81%解题思路:根据指示剂的性质进行分析,酚酞试液在碱性溶液中变红,在酸性和中性溶液中不变色,石蕊试液在碱性溶液中变蓝,在酸性溶液中变红,在中性溶液中不变色.能使酚酞试液变红的溶液呈碱性,
A、碱性溶液能使石蕊试液变蓝,不是变红,故A错误;
B、碱性溶液的pH大于7,不是小于7,故B错误;
C、碱性溶液的溶质不一定是碱,也可能是某种盐,比如碳酸钠,故C错误;
D、该溶液呈碱性,正确;
故选D.点评:
本题考点: 酸碱指示剂及其性质;溶液的酸碱性与pH值的关系.
考点点评: 本题考查了常见指示剂以及与溶液酸碱性的关系,完成此题,可以依据已有的知识进行.1年前查看全部
- 紫色石蕊试液遇碱的颜色,酚酞试液遇碱的颜色?
 有生之年相逢1年前1
有生之年相逢1年前1 -
 zhsqce 共回答了22个问题
zhsqce 共回答了22个问题 |采纳率81.8%紫色石蕊试液遇碱变蓝,酚酞遇碱变红1年前查看全部
- 鉴别稀盐酸和稀硫酸最好选用 A紫色石蕊试液B无色酚酞试液C硝酸银溶液C氯化钡溶液
 老庄v1年前4
老庄v1年前4 -
 哎呀疯了25 共回答了26个问题
哎呀疯了25 共回答了26个问题 |采纳率96.2%选最后一个,氯化钡溶液,稀盐酸和稀硫酸遇到紫色石蕊试液,和无色酚酞现象都一样,因为他们都是酸性溶液,和硝酸银反应都有白色沉淀,只有稀盐酸和氯化钡没有反应,但稀硫酸和氯化钡会有沉淀,就是硫酸钡了.1年前查看全部
- 将滴有酚酞试液的滤纸条放在试管里,在试管口上塞一小团脱脂棉
将滴有酚酞试液的滤纸条放在试管里,在试管口上塞一小团脱脂棉
1、用仪器 A 吸取浓氨水,地在试管口的脱脂棉上,A 的仪器名称是什么?
2、实验中往往在试管下方一张白纸,则白纸的作用是什么?
3、实验中看到的现象是什么? runrun061年前1
runrun061年前1 -
 hy5034080 共回答了21个问题
hy5034080 共回答了21个问题 |采纳率90.5%1滴管
2方便与试纸的颜色变化进行对比
3滤纸条编成粉红色1年前查看全部
- 在石灰水中滴入几滴酚酞试液,溶液呈______色;把此显色的溶液在空气中久置后,为什么溶液的颜色又会消失变成无色?___
在石灰水中滴入几滴酚酞试液,溶液呈______色;把此显色的溶液在空气中久置后,为什么溶液的颜色又会消失变成无色?______.  chysya1年前1
chysya1年前1 -
 lion_zyf 共回答了23个问题
lion_zyf 共回答了23个问题 |采纳率87%酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色.石灰水是氢氧化钙的水溶液,显碱性,则在石灰水中滴入几滴酚酞试液,溶液呈红色.
把此显色的溶液在空气中久置后,氢氧化钙溶液能与空气中的二氧化碳反应生成碳酸钙沉淀和水,生成的水显中性,则溶液的颜色又会消失变成无色.
故答案为:红;氢氧化钙溶液能与空气中的二氧化碳反应生成碳酸钙沉淀和显中性的水.1年前查看全部
- 氢氧化钠使酚酞试液变红是物理变化还是化学变化?
 yuntao211年前7
yuntao211年前7 -
 枫叶荻 共回答了12个问题
枫叶荻 共回答了12个问题 |采纳率100%有新的物质生成·、是化学变化1年前查看全部
- 下列溶液中,能够大量共存的离子组是( ) A.使酚酞试液变红的溶液:Na + 、Cl - 、S0 2-4 、Fe
下列溶液中,能够大量共存的离子组是( ) A.使酚酞试液变红的溶液:Na + 、Cl - 、S0
、Fe 3+2-4 B.使紫色石蕊试液变红的溶液:Fe 2+ 、Mg 2+ 、N0 3 - 、Cl - C.c(H + )=10 -12 mol•L -1 的溶液:K + 、Ba 2+ 、Cl - 、Br - D.pH=2的无色溶液:K + 、S0 4 2- 、Mn0 4 - 、Na +  yuansu991年前1
yuansu991年前1 -
 gengliang 共回答了26个问题
gengliang 共回答了26个问题 |采纳率96.2%A.使酚酞试液变红的溶液,显碱性,Fe 3+ 、OH - 结合生成沉淀,不能共存,故A错误;
B.使紫色石蕊试液变红的溶液,显酸性,Fe 2+ 、H + 、N0 3 - 发生氧化还原反应,不能共存,故B错误;
C.c(H + )=10 -12 mol•L -1 的溶液,显碱性,该组离子之间不反应,能共存,故C正确;
D.Mn0 4 - 为紫色,与无色溶液不符,故D错误;
故选C.1年前查看全部
- 在烧杯里加入20mL 0.1mol•L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物
 在烧杯里加入20mL 0.1mol•L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):
在烧杯里加入20mL 0.1mol•L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):
实验现象如下:
①灯泡逐渐变暗;②烧杯中有白色沉淀生成,溶液红色变浅甚至消失.请依据实验现象回答下列问题:
(1)灯泡变暗的原因是______.
(2)有白色沉淀生成,说明______,红色变浅说明______.
(3)当Ba2+恰好完全沉淀时,消耗NaHSO4溶液的体积为______mL,溶液呈______色,离子反应方程式为______.
(4)若向(3)得到的溶液中,继续滴加NaHSO4溶液到恰好变为无色,此阶段的离子反应方程式为______. 轻吟狂啸1年前1
轻吟狂啸1年前1 -
 bdlzdq 共回答了14个问题
bdlzdq 共回答了14个问题 |采纳率78.6%解题思路:Ba(OH)2与NaHSO4发生反应:①Ba2+沉淀完全:Ba2++OH-+SO42-+H+═BaSO4↓+H2O;②溶液呈中性:Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O;反应过程中,溶液中离子的浓度减小,其导电能力减弱,灯泡变暗,以此来解答.(1)反应生成硫酸钡,使溶液中可自由移动离子的浓度变小,导电性减弱,则灯泡变暗,故答案为:溶液中可自由移动离子的浓度变小;
(2)白色沉淀为硫酸钡,是Ba2+与SO42-发生了反应,红色变浅,氢氧根离子浓度减小,发生了H+与OH-发生了反应,使溶液碱性减弱,
故答案为:Ba2+与SO42-发生了反应;发生了H+与OH-发生了反应,使溶液碱性减弱;
(3)当Ba2+恰好完全沉淀时,发生Ba2++OH-+SO42-+H+═BaSO4↓+H2O,以1:1反应,浓度相等,则体积相同,即NaHSO4溶液的体积为20mL,碱性减弱,颜色变浅,
故答案为:20;浅红;Ba2++OH-+SO42-+H+═BaSO4↓+H2O;
(4)向(3)得到的溶液中,继续滴加NaHSO4溶液到恰好变为无色,只发生H+与OH-的反应,离子反应为H++OH-═H2O,故答案为:H++OH-═H2O.点评:
本题考点: 离子方程式的书写;电解质溶液的导电性.
考点点评: 本题考查离子反应方程式的书写,为高考常见题型,明确发生的化学反应为解答的关键,把握反应的先后顺序及现象与导电性的关系,题目难度不大.1年前查看全部
- 右图表示一个电解池,电解液ɑ是足量的饱和NaCl溶液,X、Y都是石墨电极,实验开始前,在两边各滴入几滴酚酞试液,则:
 右图表示一个电解池,电解液ɑ是足量的饱和NaCl溶液,X、Y都是石墨电极,实验开始前,在两边各滴入几滴酚酞试液,则:
右图表示一个电解池,电解液ɑ是足量的饱和NaCl溶液,X、Y都是石墨电极,实验开始前,在两边各滴入几滴酚酞试液,则:
(1)X电极上的电极反应式为______,在X极附近观察到的现象是______.
(2)Y电极上的电极反应式为______,若在X电极处收集到标准状况下的气体224mL,则Y电极处生成物的质量为______ g. mcpbv1年前1
mcpbv1年前1 -
 安徽rr 共回答了19个问题
安徽rr 共回答了19个问题 |采纳率94.7%解题思路:(1)依据装置图可知X为电解池阴极,溶液中氢离子得到电子发生还原反应生成氢气,破坏了水的电离平衡,溶液中氢氧根离子浓度增大;
(2)Y电极和电源正极连接是电解池的阳极,溶液中氯离子失电子发生氧化反应失电子生成氯气;依据X电极生成的氢气物质的量计算Y电极生成的氯气;(1)装置图可知X连接电源负极,为电解池阴极,溶液中氢离子得到电子发生还原反应生成氢气,电极反应为:2H++2e-=H2↑,破坏了水的电离平衡,溶液中氢氧根离子浓度增大,酚酞变红色;
故答案为:2H++2e-=H2↑,生成无色气体,X电极附近溶液变红;
(2)Y电极和电源正极连接是电解池的阳极,溶液中氯离子失电子发生氧化反应失电子生成氯气,Y电极上的电极反应式为2Cl--2e-=Cl2↑,若在X电极处收集到标准状况下的气体224mL是氢气,物质的量为0.01mol,依据电子守恒计算得到氯气为0.01mol,生成氯气质量=0.01mol×71g/mol=0.71g;
故答案为:2Cl--2e-=Cl2↑,0.71g;点评:
本题考点: 电解原理.
考点点评: 本题考查电解原理的应用,主要是电极判断,电极反应应用,题目较简单.1年前查看全部
- 下列对实验现象的分析合理的是:A 向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱溶液B 某白色固体与熟石灰混合后加热
下列对实验现象的分析合理的是:
A 向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱溶液
B 某白色固体与熟石灰混合后加热,产生可使湿润的红色石蕊试纸变蓝色的气体,证明该固体是铵盐
这两个那个对? Candy宝贝1年前1
Candy宝贝1年前1 -
 miaozicq 共回答了26个问题
miaozicq 共回答了26个问题 |采纳率84.6%选B.
A.不一定是碱溶液,可以是强碱弱酸盐如Na2CO3.(高中会学到)
B.正确.NH4+ +OH-=△=NH3↑+H2O,NH3可以使湿润的红色石蕊试纸变蓝色,证明含有NH4+,一定是铵盐.1年前查看全部
- 《全科王》中求物理题答案某同学在一只容积为50ml的烧杯中倒入10ml的浓氨水,然后迅速将一张潮湿的并滴有无色酚酞试液的
《全科王》中求物理题答案
某同学在一只容积为50ml的烧杯中倒入10ml的浓氨水,然后迅速将一张潮湿的并滴有无色酚酞试液的滤纸放在烧杯正上方,该同学发现了:变红的现象,对于该现象的解释是______.该同学在实验时惊奇地发现变色的湿润滤纸离开烧杯上方一段时间后______,这是因为_______. YumiTT1年前1
YumiTT1年前1 -
 chenjihuai 共回答了16个问题
chenjihuai 共回答了16个问题 |采纳率93.8%浓氨水显碱性,溶于水后,氨水中氨分子易挥发且易溶于水,生成碱性氨水,所以湿的无色酚酞滤纸接触到挥发的氨气变红.一段时间后,氨气挥发,滤纸变为无色,这是因为氨分子挥发扩散到空气中了.1年前查看全部
- 将二氧化硫通到显红色的酚酞试液中,发现红色消失,主要是因为二氧化硫有
将二氧化硫通到显红色的酚酞试液中,发现红色消失,主要是因为二氧化硫有
酸性氧化物.为什么 byxok1年前3
byxok1年前3 -
 zhumin388813 共回答了21个问题
zhumin388813 共回答了21个问题 |采纳率90.5%因为二氧化硫显酸性,会与使酚酞溶液变红的碱性物质发生化学反应.从而,酚酞褪色.1年前查看全部
- 取样,加水溶解,溶液蓝色的是CuSO4.在溶液中,滴加无色酚酞试液,变红色的是NaOH.
取样,加水溶解,溶液蓝色的是CuSO4.在溶液中,滴加无色酚酞试液,变红色的是NaOH.
在溶液中再滴加AgNO3溶液,产生白色沉淀的是NaCl.
无现象的是KNO3
写出这个过程中所发生反应的化学方程式 comicon1年前1
comicon1年前1 -
 魑魅魍魉1999 共回答了21个问题
魑魅魍魉1999 共回答了21个问题 |采纳率85.7%AgNO3 HCl=AgCl(沉淀,标下箭头) HNO31年前查看全部
- 某无色溶液用酚酞试液检测,发现无色酚酞未变红,用紫色石蕊试液检验,未变色.说明该溶液的PH值不可能为()
某无色溶液用酚酞试液检测,发现无色酚酞未变红,用紫色石蕊试液检验,未变色.说明该溶液的PH值不可能为()
A.>7 B.=7 C.<7 D.=3
理由! 3L公主1年前2
3L公主1年前2 -
 gs841219 共回答了19个问题
gs841219 共回答了19个问题 |采纳率94.7%酚酞变色范围为8-10,石蕊变色范围5-8,说明小于5,只能选D1年前查看全部
大家在问
- 1请大家告诉我一句关于合作的名言!
- 2在甲、乙两个盒子中分别装有标号为1、2、3、4的四个球,现从甲、乙两个盒子中各取出1个球,每个小球被取出的可能性相等.
- 3多少克过氧化氢与98克硫酸所含氧元素的质量相等?
- 4为什么晶体形成的热力学条件是物质的自由能为负值?
- 51、假如你是Daniel,请你根据以下提示写一篇60词左右的推荐信,推荐王芳同学获本年度最佳学生奖.
- 6函数y=1/根号下(1+2cosx)再+lg(2sinx+根号3)得定义域是
- 7如图所示电流表的示数是______A.
- 8在线求指导:不留余地的狼 不留余地的狼 有一天,狼发现山脚下有个洞,各种动物由此通过.狼非常高兴,它想,守住山洞就可
- 9(2005•盐城)现规定一种新的运算“*”:a*b=ab,如3*2=32=9,则[1/2]*3=( )
- 10陈老师的电话号码从高位到低位依次是(1)即使8的因数,又是8的倍数,(2)2和3的最小公倍数(3)6和9的最
- 11我是法国人 我是德国人 转化为 我是欧洲人 与这一现象有关的事情是什么
- 12The jeans _____ fit
- 13平原,高原,丘陵 山地,盆地的地形特点.
- 14用天平找次品,从2007袋里找【其中有一袋或轻或重】
- 15挖一条水渠,以以挖米数是未挖的5分之3,未挖的长度是500米,这条水渠全长多少米?