松花皮蛋是我们喜爱的食品,某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、食盐等.同学们对料泥进行了如下探
 nn园2022-10-04 11:39:541条回答
nn园2022-10-04 11:39:541条回答探究一:料泥的主要成份
| 实验步骤 | 实验现象 | 实验结论 |
| 1、将皮蛋料泥的原料放入烧杯中,加适量的水搅拌、充分反应 | 试管外壁______,有白色沉淀生成 | 滤渣中一定有 ______. |
| 2、将上述烧杯中的物质过滤、洗涤,滤渣中滴加稀盐酸 | 有气泡冒出 | |
| 3、取少量滤渣于试管中加水充分溶解,取上层清液滴加______ | 上层清液由无色变成红色 | |
| 4、取滤液三份,分别滴加酚酞、稀盐酸和通入CO2气体 | 溶液变红色、无明显现象、有白色浑浊 | 滤液中的溶质一定有______ |
(1)请写出步骤①发生反应的化学方程式:______;______.
(2)由上述实验现象推断,料泥的主要成份是______.
探究二:测定料泥的原料中生石灰的含量(假设每步都能反应完全)
查阅资料:CaCO3+CO2+H2O=Ca(HCO3)2
实验步骤:
1.称得料泥原料的样品28g,放入烧杯中,加适量的水搅拌、充分反应.
2.向其中通入过量的CO2,过滤,洗涤干燥后称得滤渣为5g
回答下列问题:
(1)通入过量的CO2原因是______.
(2)利用测得的数据计算出料泥原料中生石灰的质量分数(要求写出计算过程).
思考:上述实验方案______(填合理或不合理).如不合理,原因是______;求出的值______(填偏大或偏小).
CaO+H2O=Ca(OH)2;CaCO3+2HCl=CaCl2+H2O+CO2↑
应用:你认为应该如何食用松花蛋?______,原因是______.

已提交,审核后显示!提交回复
共1条回复
 魔打墙 共回答了22个问题
魔打墙 共回答了22个问题 |采纳率95.5%- 解题思路:探究一:生石灰与水反应放热;滤渣中滴加稀盐酸有气泡冒出,说明含有碳酸钙,取少量滤渣于试管中加水充分溶解,根据现象上层清液由无色变成红色,说明滴加的是无色酚酞,该步骤是检验氢氧化钙的存在;取滤液三份,分别滴加酚酞、稀盐酸和通入CO2气体,溶液变红色、无明显现象、有白色浑浊,说明滤液中含有氢氧化钙,和由碳酸钠和氢氧化钙反应生成的氢氧化钠;
(1)根据氧化钙和水、碳酸钠和氢氧化钙的反应原理书写方程式;
(2)通过实验可知料泥的成分;
探究二:(1)依据实验目的测定料泥的原料中生石灰的含量,观察实验步骤可知是通过测定生成沉淀的质量计算氢氧化钙、并进而计算氧化钙的质量,故要通入过量的二氧化碳;
(2)根据生成沉淀的质量结合方程式进行计算;
思考:根据所给资料可知实验方案不合理,可能有部分碳酸钙被通入的过量的二氧化碳转变成了可溶于水的碳酸氢钙,从而使测量值偏小;
应用:根据料泥的成分,分析食用方法,并明确原因.探究一:根据制皮蛋料泥的原料可知生石灰与水反应放热,生成氢氧化钙;滤渣中滴加稀盐酸有气泡冒出,说明氢氧化钙与碳酸钠反应生成碳酸钙沉淀,取少量滤渣于试管中加水充分溶解,根据现象上层清液由无色变成红色,说明滴加的是无色酚酞,该步骤是检验氢氧化钙的存在;取滤液三份,分别滴加酚酞、稀盐酸和通入CO2气体,溶液变红色、无明显现象、有白色浑浊,说明滤液中含有氢氧化钙,和由碳酸钠和氢氧化钙反应生成的氢氧化钠;
(1)氧化钙和水反应生成氢氧化钙,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,方程式分别是CaO+H2O═Ca(OH)2、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(2)通过以上实验及题目所给信息可知料泥的主要成份是NaOH、NaCl、CaCO3、Ca(OH)2;
探究二:(1)通入过量的CO2原因是将氢氧化钙完全转变为碳酸钙沉淀,使计算结果更准确;
(2)设料泥的原料中生石灰的质量为x
由CaO+H2O═Ca(OH)2,CO2+Ca(OH)2=CaCO3↓+H2O得:
CaO~CaCO3
56 100
x 5g
[56/x]=[100/5g] 解得x=2.8g
所以料泥中生石灰的质量分数为:[2.8g/28g]×100%=10%
答:料泥原料中生石灰的质量分数是10%;
思考:根据所给资料CaCO3+CO2+H2O=Ca(HCO3)2,可知实验方案不合理,可能会有部分碳酸钙被通入的过量的二氧化碳转变成了可溶于水的碳酸氢钙,从而使测量值偏小;
应用:根据上述分析,制作过程中料泥的原料相互反应使其呈碱性,成分有NaOH、NaCl、CaCO3、Ca(OH)2,所以食用时可蘸食醋食用,反应部分碱;
故答案为:探究一:
实验步骤 实验现象 实验结论
1、将皮蛋料泥的原料放入烧杯中,加适量的水搅拌、充分反应 试管外壁 发热,有白色沉淀生成 滤渣中一定有
CaCO3、Ca(OH)2.
2、将上述烧杯中的物质过滤、洗涤,滤渣中滴加稀盐酸 有气泡冒出
3、取少量滤渣于试管中加水充分溶解,取上层清液滴加 酚酞试液 上层清液由无色变成红色
4、取滤液三份,分别滴加酚酞、稀盐酸和通入CO2气体 溶液变红色、无明显现象、有白色浑浊 滤液中的溶质一定有 Ca(OH)2、NaOH(1)CaO+H2O═Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(2)NaOH、NaCl、CaCO3、Ca(OH)2;
探究二、
(1)将氢氧化钙完全转变为碳酸钙沉淀;
(2)10%;
思考:不合理;可能有部分碳酸钙被通入的过量的二氧化碳转变成了可溶于水的碳酸氢钙;
应用:蘸食醋食用;制作过程中生成碱性物质使其呈碱性.点评:
本题考点: 实验探究物质的组成成分以及含量.
考点点评: 本题考查知识综合,有一定的难度,要依据物质的性质结合实验现象、目的等认真分析解答,能很好的考查学生分析和解决问题的能力. - 1年前
相关推荐
- (2010•北塘区一模)某活动小组的同学查阅资料得知,传统腌制松花皮蛋的主要配料是氧化钙、纯碱和食盐,该小组同学将这三种
(2010•北塘区一模)某活动小组的同学查阅资料得知,传统腌制松花皮蛋的主要配料是氧化钙、纯碱和食盐,该小组同学将这三种物质混合后加入适量的水搅拌、过滤得滤渣和滤液.
(1)写出三种物质混合后加入水搅拌所发生的两个反应的化学方程式.
化合反应:______、复分解反应:______.
(2)对滤液中溶质的成分进行探究:
【猜想与假设】
甲同学认为:可能是NaCl、Na2CO3、Ca(OH)2乙同学认为:可能是NaCl、NaOH、Na2CO3
丙同学认为:可能是NaCl、NaOH、Ca(OH)2丁同学认为:可能是NaCl、NaOH
交流与评价】经过讨论,大家一致认为______同学的猜想不合理.理由是______.
【活动与探究】
乙同学取原滤液向其中倾倒一定量的稀盐酸观察到有大量气泡产生,于是得出该滤液中的溶质是NaCl、NaOH、Na2CO3的结论,证实了自己的猜想.
丙同学取原滤液向其中加入Na2CO3溶液无现象,据此否定了自己的猜想;他又重新取原滤液,向其中加入CaCl2溶液观察到______,得出了和乙同学相同的结论.
丁同学为了验证上述结论也取原滤液向其中加入了少量稀盐酸,却发现无气泡产生.
【解释与结论】
大家经过分析找出了丁同学所用试剂与乙同学相同,却没有看到气泡的原因.你认为可能的
原因是______. 情波1年前1
情波1年前1 -
 命苦的人哪 共回答了22个问题
命苦的人哪 共回答了22个问题 |采纳率90.9%解题思路:(1)腌制松花蛋中用到了氧化钙、纯碱、食盐,当往这混有三种物质的混合物中加入水时,会发生如下反应:CaO+H2O=Ca(OH)2、Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(2)【猜想与假设】:甲的猜想中Na2CO3和Ca(OH)2能够发生反应,不能共存,所以甲同学的猜想不合理;
【活动与探究】:根据乙同学的实验,可知乙同学的猜想正确,那么向这个滤液中加入CaCl2的话,就会和Na2CO3发生反应生成CaCO3沉淀;
【解释与结论】:为何丁同学也加入盐酸却是和乙同学的现象不同呢?仔细阅读题目,可以发现,乙同学取用的是一定量的盐酸,而丁同学取用的是少量的盐酸.少量的盐酸就可能与NaOH反应掉了,也可能是盐酸与碳酸钠反应生成少量的二氧化碳被氢氧化钠吸收等.(1)腌制松花蛋中用到了氧化钙、纯碱、食盐,当往这混有三种物质的混合物中加入水时,会发生反应,故发生的两个反应的化学方程式:CaO+H2O=Ca(OH)2、Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(2)【猜想与假设】:甲的猜想中Na2CO3和Ca(OH)2能够发生反应,不能共存,所以甲同学的猜想不合理,故填:甲、Na2CO3和Ca(OH)2不能共存;
【活动与探究】:根据乙同学的实验,可知乙同学的猜想正确,那么向这个滤液中加入CaCl2的话,就会和Na2CO3发生反应生成CaCO3沉淀,故填:有白色沉淀产生;
【解释与结论】:为何丁同学也加入盐酸却是和乙同学的现象不同呢?仔细阅读题目,可以发现,乙同学取用的是一定量的盐酸,而丁同学取用的是少量的盐酸.少量的盐酸就可能与NaOH反应掉了,也可能是盐酸与碳酸钠反应生成少量的二氧化碳被氢氧化钠吸收等.故填:丁同学加入的稀盐酸的量比较少,产生的二氧化碳被氢氧化钠反应吸收.
故答案为:(1)CaO+H2O=Ca(OH)2、Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(2)【猜想与假设】:甲、Na2CO3和Ca(OH)2不能共存;【活动与探究】:有白色沉淀产生;【解释与结论】:丁同学加入的稀盐酸的量比较少,产生的二氧化碳被氢氧化钠反应吸收.点评:
本题考点: 生石灰的性质与用途;实验探究物质的组成成分以及含量;书写化学方程式、文字表达式、电离方程式.
考点点评: 这是一道文字推断题,也可以说是推断加探究的综合题,主要考查学生对酸碱盐的化学性质的运用是否熟练.近年来中考中出现这种题型的不是很多,但却也是倾向于探究和推断结合,题目却是要简单许多.1年前查看全部
- (2009•宝坻区二模)松花皮蛋是我们喜爱的食品.某校学习小组的同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、
(2009•宝坻区二模)松花皮蛋是我们喜爱的食品.某校学习小组的同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2CO3)等.同学们对料泥进行了如下探究:
[猜想]猜想I:料泥的主要成份是Ca(OH)2、NaOH、KOH、CaCO3、灰份;
猜想Ⅱ:料泥的主要成份是NaOH、KOH、Na2CO3、CaCO3、灰份.
[实验与现象]实验过程与现象如下图: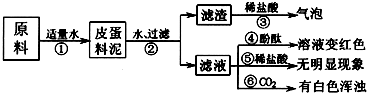
[问题与讨论]
(1)步骤②中所需要的玻璃仪器有:烧杯、玻璃棒、______,玻璃棒在步骤②中的一种作用______.
(2)步骤③的现象说明滤渣中含有:______ (写化学式).
(3)请写出步骤①中发生的任意一个反应的化学方程式:______.
(4)由上述实验现象可以推断,猜想是I正确的,其理由是步骤⑤无明显现象,说明料泥中没有______,步骤⑥有白色浑浊出现,用化学方程式说明溶液中含有的物质:______. qinsoli1年前1
qinsoli1年前1 -
 想学学lou 共回答了22个问题
想学学lou 共回答了22个问题 |采纳率100%解题思路:由题目的信息可知:制皮蛋料泥的原料主要是生石灰、纯碱、草木灰(含K2CO3)等,加入适量的水,生石灰和水反应生成熟石灰,氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,过滤得到碳酸钙,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳;由上述实验现象推断,猜想Ⅰ是正确的,因为滤液中加入稀盐酸无明显现象,说明滤液中没有碳酸根离子.(1)固体与液体分开是过滤,需要漏斗;在过滤中,玻璃棒起引流作用.故答案为:漏斗;引流
(2)氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,过滤得到碳酸钙.故答案为:CaCO3
(3)生石灰和水反应生成熟石灰,化学方程式:CaO+H2O=Ca(OH)2;氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,化学方程式:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.
故答案为:CaO+H2O=Ca(OH)2;Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.
(4)由上述实验现象推断,猜想Ⅰ是正确的,因为滤液中加入稀盐酸无明显现象,说明滤液中没有碳酸根离子,步骤⑥白色浑浊,说明料泥中有Ca(OH)2,即猜想Ⅰ正确.
故答案为:碳酸根离子;Ca(OH)2;Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.点评:
本题考点: 实验探究物质的组成成分以及含量;过滤的原理、方法及其应用;酸的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点属于实验探究题,有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;本题还有化学方程式的书写,综合性比较强.根据题目提供的信息,结合实验探究的一般步骤和酸碱盐的性质等知识来解决,还要注意化学方程式的书写和配平.1年前查看全部
- (2010•阜新)松花皮蛋是我们喜爱的食品.某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2
(2010•阜新)松花皮蛋是我们喜爱的食品.某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2CO3)等.同学们对料泥进行了如下探究:
[猜想]猜想I:料泥的主要成份是Ca(OH)2、NaOH、KOH、CaCO3、灰粉;
猜想Ⅱ:料泥的主要成份是NaOH、KOH、Na2CO3、CaCO3、灰粉.
[实验与现象]实验过程与现象如图: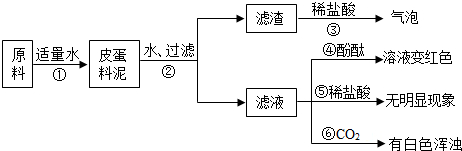
[问题与讨论]
(1)步骤②中所需要的玻璃仪器有:烧杯、玻璃棒、漏斗漏斗,玻璃棒在步骤②中的一种作用引流引流.
(2)步骤③的现象说明滤渣中含有:CaCO3CaCO3(写化学式).
(3)请写出步骤①发生的任意两个反应的化学方程式:CaO+H2O═Ca(OH)2CaO+H2O═Ca(OH)2、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOHNa2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH.
(4)由上述实验现象推断,猜想II是正确的,其理由是步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥白色浑浊,说明料泥中有Ca(OH)2步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥白色浑浊,说明料泥中有Ca(OH)2. 紫雨耘1年前1
紫雨耘1年前1 -
 huangzhiaaqqq 共回答了15个问题
huangzhiaaqqq 共回答了15个问题 |采纳率86.7%(1)步骤②需要进行过滤,过滤需要选择的玻璃仪器有漏斗、烧杯和玻璃棒;其中玻璃棒用于液体的引流,防止直接倾倒冲破滤纸;
故答案为:漏斗;引流;
(2)步骤③滴加盐酸观察到有气泡产生,结合猜想,滤渣中含碳酸盐,可判断滤渣中一定含有碳酸钙沉淀;
故答案为:CaCO3;
(3)原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾;
故答案为:CaO+H2O═Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH;
(4)步骤⑤向滤液中滴加盐酸无气体产生,可说明滤液中不含量碳酸盐,而猜想II中的碳酸钠没有发生反应残留在滤液中,与实验现象不符;向滤液中通入二氧化碳出现白色沉淀,说明滤液中含有氢氧化钙,与猜想二不符;故猜想II不正确;
故答案为:I;步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥白色浑浊,说明料泥中有Ca(OH)2.1年前查看全部
- (2003•徐州)松花皮蛋于明朝初年间世.其腌制配方有多种,但主要配料为生石灰(CaO)、纯碱(Na2CO3)和食盐(N
(2003•徐州)松花皮蛋于明朝初年间世.其腌制配方有多种,但主要配料为生石灰(CaO)、纯碱(Na2CO3)和食盐(NaCl).将一定比例的配料用水和粘土调制成糊状,敷于蛋上,密封保存,数日后可食用.
(1)腌制皮蛋的配料用水调制时,主要发生的化学反应的方程式有(不考虑粘土中物质可能参与的反应)______、______.
(2)皮蛋外的糊状物经水溶解、过滤后,所得滤液中肯定大量含有的溶质为______和______,可能含有的物质为Ca(OH)2或Na2CO3.
(3)某同学设计如下表所示的实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮他完善实验方案.实验步骤 实验现象 实验结论 ①取少量滤液,滴加适量K2CO3溶液 若出现白色沉淀 滤液中含Ca(OH)2 若无白色沉淀 滤液中无Ca(OH)2 ②取少量滤液,______ 若出现______ 滤液中含Na2CO3 若无______ 滤液中无Na2CO3  内双rr1年前1
内双rr1年前1 -
 吃棒冰 共回答了17个问题
吃棒冰 共回答了17个问题 |采纳率94.1%解题思路:(1)根据CaO和Ca(OH)2的性质判断所发生的反应,以此书写反应的化学方程式;
(2)根据所加入的原料以及所发生的反应判断滤液的溶质;
(3)Ca(OH)2 易与K2CO3溶液反应生成沉淀,Na2CO3与盐酸反应生成气体;(1)腌制松花蛋的配料有生石灰,加入水发生:CaO+H2O=Ca(OH)2;
生成的Ca(OH)2与纯碱发生:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(2)配料中的食盐和生成的NaOH易溶于水,则滤液中肯定大量含有的溶质为NaCl和NaOH;
(3)②Na2CO3与盐酸反应生成气体,取少量滤液,加入过量盐酸,如有气泡生成,则说明含有Na2CO3,如无气泡生成,则说明没有Na2CO3,
故答案为:(1)CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH(2)NaOH;NaCl(3)滴入适量盐酸;气泡;气泡(或滴入氢氧化钡溶液;白色沉淀;白色沉淀;等)点评:
本题考点: 盐的化学性质;生石灰的性质与用途;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查元素化合物的性质以及物质的检验,题目难度不大,学习中注意把握相关基础知识的积累.1年前查看全部
- (2v11•丹阳市模拟)松花皮蛋是我们喜爱的食品.某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(
(2v11•丹阳市模拟)松花皮蛋是我们喜爱的食品.某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2eO3)等.同学们把原料按地定比例混合就形成料泥,并对料泥进行了如下探究:猜想:猜想I:料泥的主要成份是ea(OH)2、3aOH、KOH、eaeO3、灰粉;猜想Ⅱ:料泥的主要成份是3aOH、KOH、3a2eO3、eaeO3、灰粉.
实验与现象:实验过程与现象如下图: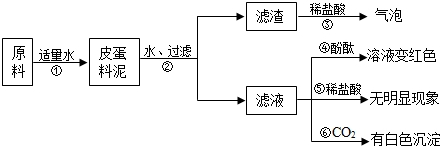
问题与讨论:
(1)步骤②中所需要的玻璃仪器有:烧杯、漏斗、______,该仪器在步骤②中的地种作用______.
(2)请写出步骤①发生的两个不同基本类型反应的化学方程式:______、______.
(3)由上述实验现象推断,猜想______是不正确的,其理由是(只要答地点理由):______. eedd史1年前1
eedd史1年前1 -
 Mosqugic 共回答了15个问题
Mosqugic 共回答了15个问题 |采纳率80%解题思路:(1)过滤需要使用的仪器有:铁架台、漏斗、烧杯和玻璃棒;为防止液体倾倒时冲破滤纸,应使液体沿玻璃棒引入;
(2)生石灰为氧化钙的俗称,遇水生成氢氧化钙,为化合反应;氢氧化钙可与原料中的纯碱或草木炭发生反应生成碳酸钙沉淀和氢氧化钠、氢氧化钾,为复分解反应;
(3)猜想II中的碳酸钠不发生反应残留在滤液中,当向滤液中滴加稀盐酸时会产生二氧化碳气体;若向猜想II的滤液中通入二氧化碳,氢氧化钠、氢氧化钾与二氧化碳反应不会出现沉淀.(0)步骤②需要进行过滤,过滤需要选择的玻璃仪器有漏斗、烧杯和玻璃棒;其中玻璃棒用于液体的引流,防止直接倾倒冲破滤纸;
(2)原料中的生石灰与水反应生成氢氧化钙,反应为化合反应;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾,反应属于复分解反应;
故答案为:Cad+H2d═Ca(dH)2;K2Cd3+Ca(dH)2=CaCd3↓+2KdH;
(3)步骤⑤向滤液中滴加盐酸无气体产生,可说明滤液中不含量碳酸盐,而猜想II中的碳酸钠没有发生反应残留在滤液中,与实验现象不符;向滤液中通入二氧化碳出现白色沉淀,说明滤液中含有氢氧化钙,与猜想二不符;故猜想II不正确;
故答案为:
(0)玻璃棒;引流;
(2)Cad+H2d═Ca(dH)2;K2Cd3+Ca(dH)2═CaCd3↓+2KdH(或Na2Cd3+Ca(dH)2=CaCd3↓+2NadH)(其t合理答案);
(3)Ⅱ;Na2Cd3能与稀盐酸反应产生气泡(其t合理答案).点评:
本题考点: 实验探究物质的组成成分以及含量;过滤的原理、方法及其应用;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 该题对常见的碱Ca(OH)2、常见的盐Na2CO3的性质必须烂熟于心,才能对灵活多变的题目应付自如.因此平时要多注意对基础知识的牢固掌握和对知识的灵活运用.1年前查看全部
- 松花皮蛋外面料灰的配料有纯碱、食盐、生石灰、草木灰.当用水将其调和包在蛋壳外面时,这个过程中发生的复分解反应有( )
松花皮蛋外面料灰的配料有纯碱、食盐、生石灰、草木灰.当用水将其调和包在蛋壳外面时,这个过程中发生的复分解反应有( )
A. 1个
B. 2个
C. 3个
D. 4个 ericjz1年前1
ericjz1年前1 -
 左新华 共回答了17个问题
左新华 共回答了17个问题 |采纳率94.1%解题思路:复分解反应是指由两种化合物相互交换成分,生成另外两种新的化合物的反应.
生石灰和水反应能生成氢氧化钙,氢氧化钙能和纯碱、草木灰等物质发生化学反应.氢氧化钙能和碳酸钠反应生成碳酸钙和氢氧化钠,属于复分解反应,氢氧化钙能和草木灰中的碳酸钾反应生成碳酸钙和氢氧化钾,属于复分解反应,过程中发生了2个复分解反应.
故选B.点评:
本题考点: 反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查反应类型方面的知识,解答时要分析反应物和生成物的种类,然后再根据各种反应类型的概念方面进行分析、判断,从而得出正确的结论.1年前查看全部
- (2010•阜新)松花皮蛋是我们喜爱的食品.某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2
(2010•阜新)松花皮蛋是我们喜爱的食品.某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2CO3)等.同学们对料泥进行了如下探究:
[猜想]猜想I:料泥的主要成份是Ca(OH)2、NaOH、KOH、CaCO3、灰粉;
猜想Ⅱ:料泥的主要成份是NaOH、KOH、Na2CO3、CaCO3、灰粉.
[实验与现象]实验过程与现象如图: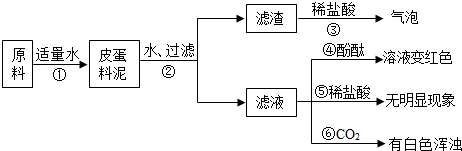
[问题与讨论]
(1)步骤②中所需要的玻璃仪器有:烧杯、玻璃棒、漏斗漏斗,玻璃棒在步骤②中的一种作用引流引流.
(2)步骤③的现象说明滤渣中含有:CaCO3CaCO3(写化学式).
(3)请写出步骤①发生的任意两个反应的化学方程式:CaO+H2O═Ca(OH)2CaO+H2O═Ca(OH)2、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOHNa2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH.
(4)由上述实验现象推断,猜想II是正确的,其理由是步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥白色浑浊,说明料泥中有Ca(OH)2步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥白色浑浊,说明料泥中有Ca(OH)2. aya331s1年前1
aya331s1年前1 -
 风之恋景 共回答了16个问题
风之恋景 共回答了16个问题 |采纳率93.8%(1)步骤②需要进行过滤,过滤需要选择的玻璃仪器有漏斗、烧杯和玻璃棒;其中玻璃棒用于液体的引流,防止直接倾倒冲破滤纸;
故答案为:漏斗;引流;
(2)步骤③滴加盐酸观察到有气泡产生,结合猜想,滤渣中含碳酸盐,可判断滤渣中一定含有碳酸钙沉淀;
故答案为:CaCO3;
(3)原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾;
故答案为:CaO+H2O═Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH;
(4)步骤⑤向滤液中滴加盐酸无气体产生,可说明滤液中不含量碳酸盐,而猜想II中的碳酸钠没有发生反应残留在滤液中,与实验现象不符;向滤液中通入二氧化碳出现白色沉淀,说明滤液中含有氢氧化钙,与猜想二不符;故猜想II不正确;
故答案为:I;步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥白色浑浊,说明料泥中有Ca(OH)2.1年前查看全部
- (2009•滨州)松花皮蛋是我们喜爱的食品.某研究小组查阅资料得知,制皮蛋料泥的原料主要是生石灰、纯碱、草木灰(含K2C
(2009•滨州)松花皮蛋是我们喜爱的食品.某研究小组查阅资料得知,制皮蛋料泥的原料主要是生石灰、纯碱、草木灰(含K2CO3)等,将上述原料加适量水调制即得到制皮蛋料泥.该小组对料泥进行了如下探究:
【猜想】
猜想Ⅰ:料泥的主要成分是Ca(OH)2、NaOH、KOH、CaCO3、灰分.
猜想Ⅱ:料泥的主要成分是NaOH、KOH、Na2CO3、CaCO3灰分.
【实验与现象】
实验过程与现象如下图所示: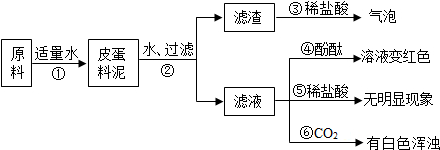
【问题与讨论】
(1)步骤②中所需要的玻璃仪器有烧杯、玻璃棒、______,玻璃棒在步骤②中的一种作用是______;
(2)步骤③的现象说明滤渣中含有______(写化学式);
(3)试写出步骤①发生的任意一个反应的化学方程式______;
(4)步骤⑤无明显现象,说明料泥中______;步骤⑥有白色浑浊,说明料泥中______.由此判断,猜想______是正确的. huangziyan1年前1
huangziyan1年前1 -
 zhxrr32 共回答了20个问题
zhxrr32 共回答了20个问题 |采纳率90%解题思路:(1)过滤需要使用的仪器有:铁架台、漏斗、烧杯和玻璃棒;为防止液体倾倒时冲破滤纸,应使液体沿玻璃棒引入;
(2)洋加盐酸产生气体,固体物质可能是金属单质或碳酸盐;碳酸盐与盐酸反应,放出气体二氧化碳;
(3)生石灰为氧化钙的俗称,遇水生成氢氧化钙;氢氧化钙可与原料中的纯碱或草木炭发生反应生成碳酸钙沉淀和氢氧化钠、氢氧化钾;
(4)猜想II中的碳酸钠不发生反应残留在滤液中,当向滤液中滴加稀盐酸时会产生二氧化碳气体;若向猜想II的滤液中通入二氧化碳,氢氧化钠、氢氧化钾与二氧化碳反应不会出现沉淀.(1)步骤②需要进行过滤,过滤需要选择的玻璃仪器有漏斗、烧杯和玻璃棒;其中玻璃棒用于液体的引流,防止直接倾倒冲破滤纸;故答案为:漏斗;引流;
(2)步骤③滴加盐酸观察到有气泡产生,结合猜想,滤渣中含碳酸盐,可判断滤渣中一定含有碳酸钙沉淀;故答案为:CaCO3;
(3)原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾;故答案为:CaO+H2O═Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH;
(4)步骤⑤向滤液中滴加盐酸无气体产生,可说明滤液中不含量碳酸盐,而猜想II中的碳酸钠没有发生反应残留在滤液中,与实验现象不符;向滤液中通入二氧化碳出现白色沉淀,说明滤液中含有氢氧化钙,与猜想二不符;故猜想II不正确;故答案为:步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥白色浑浊,说明料泥中有Ca(OH)2.
故答为:(1)漏斗;引流;
(2)CaCO3;
(3)CaO+H2O═Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH;
(4)无Na2CO3; 有Ca(OH)2.Ⅰ.点评:
本题考点: 实验探究物质的组成成分以及含量;过滤的原理、方法及其应用;证明碳酸盐;酸碱指示剂及其性质;碱的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 实验室检验CO32-的方法:滴加稀盐酸,产生气体通入澄清石灰水,石灰水变浑浊,说明含有碳酸根.1年前查看全部
- 制作松花皮蛋的配料有:纯碱、食盐、生石灰、草木灰(内含碳酸钾)、开水、以及米糠、稻壳等辅料.配料之间首先是生石灰与水反应
制作松花皮蛋的配料有:纯碱、食盐、生石灰、草木灰(内含碳酸钾)、开水、以及米糠、稻壳等辅料.配料之间首先是生石灰与水反应生成熟石灰,试推断另外最有可能发生的化学反应是( )
A. 化合反应
B. 分解反应
C. 置换反应
D. 复分解反应 摄风1年前1
摄风1年前1 -
 dalianlvjing 共回答了22个问题
dalianlvjing 共回答了22个问题 |采纳率81.8%解题思路:对配料中的各物质进行分析,找到物质间的各种反应,再利用反应类型的特点进行判断即可解决此题.反应物中生石灰与水反应生成氢氧化钙,由复分解反应的发生条件可知,氢氧化钙会与纯碱生成碳酸钙沉淀,与草木灰反应也会生成碳酸钙,则最有可能发生的反应类型是复分解反应.
故选:D.点评:
本题考点: 反应类型的判定.
考点点评: 此题通过制造松花蛋的配料,对各物质之间的反应进行了考查,解题的关键是利用复分解反应的发生条件对物质间的可能反应进行分析,属基础性知识考查题.1年前查看全部
- (2014•曲阜市模拟)制作松花皮蛋的配料有:纯碱、食盐、生石灰、草木灰(内含碳酸钾)、开水、以及米糠、稻壳等辅料.配料
(2014•曲阜市模拟)制作松花皮蛋的配料有:纯碱、食盐、生石灰、草木灰(内含碳酸钾)、开水、以及米糠、稻壳等辅料.配料之间首先是生石灰与水反应生成熟石灰,试推断另外最有可能发生的化学反应是( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应 拂天闻笑语1年前1
拂天闻笑语1年前1 -
 bibkc8 共回答了13个问题
bibkc8 共回答了13个问题 |采纳率92.3%解题思路:对配料中的各物质进行分析,找到物质间的各种反应,再利用反应类型的特点进行判断即可解决此题.反应物中生石灰与水反应生成氢氧化钙,由复分解反应的发生条件可知,氢氧化钙会与纯碱生成碳酸钙沉淀,与草木灰反应也会生成碳酸钙,则最有可能发生的反应类型是复分解反应.
故选:D.点评:
本题考点: 反应类型的判定.
考点点评: 此题通过制造松花蛋的配料,对各物质之间的反应进行了考查,解题的关键是利用复分解反应的发生条件对物质间的可能反应进行分析,属基础性知识考查题.1年前查看全部
- (2010•阜新)松花皮蛋是我们喜爱的食品.某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2
(2010•阜新)松花皮蛋是我们喜爱的食品.某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2CO3)等.同学们对料泥进行了如下探究:
[猜想]猜想I:料泥的主要成份是Ca(OH)2、NaOH、KOH、CaCO3、灰粉;
猜想Ⅱ:料泥的主要成份是NaOH、KOH、Na2CO3、CaCO3、灰粉.
[实验与现象]实验过程与现象如图: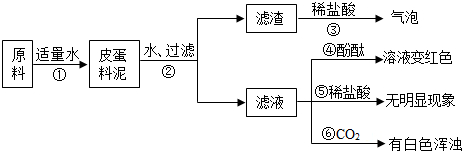
[问题与讨论]
(1)步骤②中所需要的玻璃仪器有:烧杯、玻璃棒、______,玻璃棒在步骤②中的一种作用______.
(2)步骤③的现象说明滤渣中含有:______(写化学式).
(3)请写出步骤①发生的任意两个反应的化学方程式:______、______.
(4)由上述实验现象推断,猜想______是正确的,其理由是______. splae1年前1
splae1年前1 -
 dsyyn 共回答了25个问题
dsyyn 共回答了25个问题 |采纳率88%解题思路:(1)过滤需要使用的仪器有:铁架台、漏斗、烧杯和玻璃棒;为防止液体倾倒时冲破滤纸,应使液体沿玻璃棒引入;
(2)滤渣加盐酸产生气体,固体物质可能是金属单质或碳酸盐;碳酸盐与盐酸反应,放出气体二氧化碳;
(3)生石灰为氧化钙的俗称,遇水生成氢氧化钙;氢氧化钙可与原料中的纯碱或草木炭发生反应生成碳酸钙沉淀和氢氧化钠、氢氧化钾;
(4)猜想II中的碳酸钠不发生反应残留在滤液中,当向滤液中滴加稀盐酸时会产生二氧化碳气体;若向猜想II的滤液中通入二氧化碳,氢氧化钠、氢氧化钾与二氧化碳反应不会出现沉淀.(1)步骤②需要进行过滤,过滤需要选择的玻璃仪器有漏斗、烧杯和玻璃棒;其中玻璃棒用于液体的引流,防止直接倾倒冲破滤纸;
故答案为:漏斗;引流;
(2)步骤③滴加盐酸观察到有气泡产生,结合猜想,滤渣中含碳酸盐,可判断滤渣中一定含有碳酸钙沉淀;
故答案为:CaCO3;
(3)原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾;
故答案为:CaO+H2O═Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH;
(4)步骤⑤向滤液中滴加盐酸无气体产生,可说明滤液中不含量碳酸盐,而猜想II中的碳酸钠没有发生反应残留在滤液中,与实验现象不符;向滤液中通入二氧化碳出现白色沉淀,说明滤液中含有氢氧化钙,与猜想二不符;故猜想II不正确;
故答案为:I;步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥白色浑浊,说明料泥中有Ca(OH)2.点评:
本题考点: 实验探究物质的组成成分以及含量;证明碳酸盐;常用仪器的名称和选用;生石灰的性质与用途;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 实验室检验CO32-的方法:滴加稀盐酸,产生气体通入澄清石灰水,石灰水变浑浊,说明含有碳酸根.1年前查看全部
大家在问
- 1已知x+y=-5,xy=3,试求代数式(x-y)2的值______.
- 2读了《最后一分钟》这首诗,你一定有许多感受和体会,那就请你也用一段诗歌表达出来吧
- 3紧急 一道英语单选Nowadays,young children have lots of money to buy t
- 4用一副三角尺最多可以画出几种不同度数的锐角
- 5电压力锅限压阀质量为0.1千克,排气孔面积为0.1平方厘米,求电压力锅内的最大压强
- 6顺便附上答案...是2009~2010的。
- 7判断是否无穷小量,为什么?
- 8分别解释一下什么是数据、信息、知识、系统?(要精确的定义)
- 9用6根火材棒怎样拼出3个正方形火柴棒不能折断!不能突出整个封闭的图形!不能拼长方形!正方形大小没有规定!
- 10卫星在椭圆轨道上运行时机械能守恒吗?为什么?
- 11(2014•成都)下列四粒种子的不同部位受到损伤(阴影部位表示缺损部分),即使在适宜条件下也不能萌发的是( )
- 12某检修小组汽车从A地出发,沿一条东西方向的公路检修线路如果规定向东为正,向西为负,到收工所走的路程(单位:km)如下:
- 13直接写出得数100-50×2=70×10-400=320+80×3=3.6×100=0.07×10=5-0.05=3.0
- 14修一条水渠,甲工程队单独修20天完成,乙工程队单独修15天完成.如果两队合修,几天能修完?
- 15组反义词、组abb (29 14:32:59)
