有臭鸡蛋气味的气体A和B可以相互转化,B在沸水中可以生成C,C在空气 中氧化成D,D有臭鸡蛋气味,问A,B,C,D各是什
 离恨水2022-10-04 11:39:5413条回答
离恨水2022-10-04 11:39:5413条回答A和B可以相互转化,
B在沸水中可以生成C,
C在空气 中氧化成D,
D有臭鸡蛋气味,
问A,B,C,D各是什么?

已提交,审核后显示!提交回复
共13条回复
 mdmdm1 共回答了13个问题
mdmdm1 共回答了13个问题 |采纳率92.3%- 化学中常见的臭鸡蛋味气体是硫化氢H2S
D是硫化氢H2S
其他不知道,你们太精辟了 - 1年前
 循环型dd105 共回答了23个问题
循环型dd105 共回答了23个问题 |采纳率87%- A是鸡,B是鸡蛋,C是熟鸡蛋,D是臭鸡蛋
- 1年前
 shhjy 共回答了5个问题
shhjy 共回答了5个问题 |采纳率- A:鸡
B:蛋
C:熟鸡蛋
D:臭鸡蛋 - 1年前
 米小敏 共回答了3个问题
米小敏 共回答了3个问题 |采纳率- A是鸡,B是生鸡蛋,C是熟鸡蛋,D是臭鸡蛋。
- 1年前
 bayue18 共回答了1个问题
bayue18 共回答了1个问题 |采纳率- A是鸡,B是蛋,以此类推
- 1年前
 啊祖祖 共回答了1个问题
啊祖祖 共回答了1个问题 |采纳率- A:FeCL3 B.Fe C.H2 D .H2S
- 1年前
 ribber1 共回答了3个问题
ribber1 共回答了3个问题 |采纳率- 鸡、鸡蛋、熟鸡蛋、臭掉的鸡蛋
这是一个很经典的题,据说难道爱因斯坦,却被一个修鞋匠答对了 - 1年前
 李小路 共回答了1个问题
李小路 共回答了1个问题 |采纳率- A 鸡 B 鸡蛋 C 熟鸡蛋 D 臭鸡蛋
- 1年前
 FINDU 共回答了1个问题
FINDU 共回答了1个问题 |采纳率- A鸡 B鸡蛋 C熟鸡蛋 D臭鸡蛋
- 1年前
 不行 共回答了1个问题
不行 共回答了1个问题 |采纳率- a为鸡,b为鸡蛋,c是水煮蛋,d是臭鸡蛋
- 1年前
 伤感的痛楚 共回答了128个问题
伤感的痛楚 共回答了128个问题 |采纳率- 你这不是化学题
A是鸡B是生鸡蛋C熟鸡蛋D臭鸡蛋 - 1年前
 醉心客zuixinke 共回答了875个问题
醉心客zuixinke 共回答了875个问题 |采纳率- A是鸡,B是生鸡蛋,C是熟鸡蛋,D是臭鸡蛋
- 1年前
 yc_zhou 共回答了1个问题
yc_zhou 共回答了1个问题 |采纳率- 母鸡,鸡蛋,熟鸡蛋,臭鸡蛋
- 1年前
相关推荐
- 二氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(H 2 SO 3 )。硫化氢(H2S)是一种具有臭鸡蛋气味的剧毒气体
二氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(H 2 SO 3 )。硫化氢(H2S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。现在室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为: 2H 2 S+H 2 SO 3 ===3S↓+3H 2 O。则下图中溶液的pH随通入硫化氢体积的变化曲线示意图正确的是 [ ]A. 
B.
C.
D.
 172649221年前1
172649221年前1 -
 cdrong 共回答了11个问题
cdrong 共回答了11个问题 |采纳率90.9%B1年前查看全部
- (1999•福州)在通常情况下,硫化氢(H2S)是一种没有颜色、具有臭鸡蛋气味的气体,其密度比空气大,能溶于水而形成氢硫
(1999•福州)在通常情况下,硫化氢(H2S)是一种没有颜色、具有臭鸡蛋气味的气体,其密度比空气大,能溶于水而形成氢硫酸.在实验室里常用块状固体硫化亚铁(FeS)跟稀硫酸通过复分解反应来制取硫化氢气体.
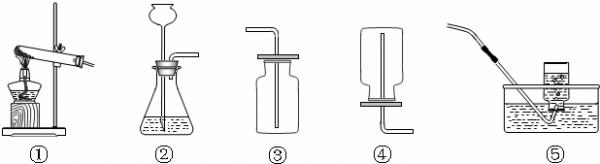
(1)实验室制取硫化氢气体的发生装置可选用______,收集硫化氢气体应选用______.(均填标号)
(2)写出实验室制取硫化氢气体的化学方程式______.
(3)向硫化氢的水溶液中滴入紫色石蕊试液时显______色,该溶液的pH______7(选填:“大于”、“小于”或“等于”). 711240601年前1
711240601年前1 -
 丹菜 共回答了18个问题
丹菜 共回答了18个问题 |采纳率94.4%解题思路:(1)根据实验室制取硫化氢的反应原理和条件选择发生装置,根据硫化氢的密度及水溶性来选择收集装置;
(2)根据题意结合质量守恒定律来书写制取硫化氢的化学方程式;
(3)紫色石蕊试液遇酸变红,酸性溶液的pH值小于7,可以据此答题.(1)在实验室里常用块状固体硫化亚铁(FeS)跟稀硫酸通过复分解反应来制取硫化氢气体,该反应无需加热,所以可以选择②作为发生装置,而硫化氢的密度比空气的大,能够溶于水,所以只能用向上排空气法来收集,即装置③;
(2)根据复分解反应的特点可以知道硫化亚铁和稀硫酸反应后生成硫酸亚铁和硫化氢,故可以写出该反应的化学方程式;
(3)硫化氢溶于水生成氢硫酸,氢硫酸是酸,其pH值小于7,可以使紫色石蕊试液变红.
故答案为:(1)②;③;
(2)FeS+H2SO4═FeSO4+H2S↑;
(3)红;小于.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;溶液的酸碱性与pH值的关系;书写化学方程式、文字表达式、电离方程式.
考点点评: 掌握常见的发生装置和收集装置,能够根据反应物的状态和反应条件,来选择合适的发生装置,根据气体的密度及水溶性来选择收集装置.1年前查看全部
- 阅读下文:在通常情况下,硫化氢是一种没有颜色,具有臭鸡蛋气味的有毒气体,比空气重,能溶于水,在空气中点燃硫化氢气体有二氧
阅读下文:在通常情况下,硫化氢是一种没有颜色,具有臭鸡蛋气味的有毒气体,比空气重,能溶于水,在空气中点燃硫化氢气体有二氧化硫和水生成,硫化氢的实验室制法:用块状硫化亚铁和稀硫酸反应,就有硫化氢气体逸出,回答:
(1)具有臭鸡蛋气味,这属于硫化氢的______(物理、化学)性质.
(2)制取硫化氢气体的装置可选用______的气体发生装置,收集时可用______法. 我是大米谁是老鼠1年前1
我是大米谁是老鼠1年前1 -
 qq316087820 共回答了17个问题
qq316087820 共回答了17个问题 |采纳率88.2%(1)具有臭鸡蛋气味,描述的是气味,不需要通过化学变化就能表现出来,属于物理性质.
(2)制取硫化氢是用的固态硫化亚铁和液态稀硫酸,而且反应不需要加热,属于固液常温型制取气体,故气体发生装置可以选择制二氧化碳的装置;硫化氢密度比空气大,且能溶于水,可以用向上排空气法来收集;
故答案为:(1)物理;(2)二氧化碳;向上排空气.1年前查看全部
- 在通常情况下,H 2 S是一种无色有臭鸡蛋的有毒气体,比空气重,能溶于水,在空气中燃烧生成一种有刺激性气味的气体SO 2
在通常情况下,H 2 S是一种无色有臭鸡蛋的有毒气体,比空气重,能溶于水,在空气中燃烧生成一种有刺激性气味的气体SO 2 和水,它的实验方法是:用块状硫化亚铁跟稀硫酸反应.请回答:
(1)具有臭鸡蛋,属于H 2 S的 _________ 性质;
(2)写出H 2 S的发生装置,可选用 _________ (填CO 2 或O 2 )的装置,收集时可采用 _________ 法.
(3)H 2 S可以燃烧,当氧气不充足时,燃烧的产物是单质硫和水,写出该条件下H 2 S燃烧的化学方程式 _________ .
(4)当氧气充足时,H 2 S燃烧的产物是二氧化硫和水,写出该条件下H 2 S燃烧的化学方程式 _________ . 18kog1年前1
18kog1年前1 -
 yxjht 共回答了16个问题
yxjht 共回答了16个问题 |采纳率87.5%1年前查看全部
- 某地天然气井发生井喷事故,喷出的天然气中H 2 S气体含量很高,H 2 S气体在臭鸡蛋气味,密度比空气大,有剧毒.井喷发
某地天然气井发生井喷事故,喷出的天然气中H 2 S气体含量很高,H 2 S气体在臭鸡蛋气味,密度比空气大,有剧毒.井喷发生不久,附近村民就闻到了臭鸡蛋气味,这体现了分子______的性质; 当村民得知这种气体有剧毒时,迅速撤离村庄.为减少村民的中毒机会,你认为村民在撤离时应尽量走______(填“低处”或“高处”).技术人员后来成功点燃了H 2 S气体,使气体不再扩散.已知H 2 S(硫化氢)燃烧时生成两种常见的氧化物,试写出H 2 S燃烧的化学方程式:______.  weiweikind1年前1
weiweikind1年前1 -
 gamekey 共回答了15个问题
gamekey 共回答了15个问题 |采纳率80%由于气体的分子不断运动,所以硫化氢会不断地扩散到空气中. 由于硫化氢密度比空气大所以会存于低处,H 2 S(硫化氢)燃烧时生成两种常见的氧化物,根据元素的种类在反应前后不变的规律,可判断生成物是二氧化硫和水,故反应的化学方程式为2H 2 S+3O 2
点燃
.
2SO 2 +2H 2 O.
故答案为:不断运动;高出;2H 2 S+3O 2
点燃
.
2SO 2 +2H 2 O.1年前查看全部
- 阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水.在空气中点燃硫化氢气体有二氧化
阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水.在空气中点燃硫化氢气体有二氧化硫和水生成.硫化氢的实验室制法是用块状硫化亚铁和液体状稀硫酸反应,则属硫化氢的化学性质的是( )
A.无色
B.有臭鸡蛋气味
C.比空气重
D.能燃烧 superangry11年前1
superangry11年前1 -
 whant928 共回答了20个问题
whant928 共回答了20个问题 |采纳率100%解题思路:化学性质主要有:可燃性、毒性、氧化性、还原性、稳定性等.物理性质主要有:颜色、状态、气味、密度、硬度、熔点、沸点等.可以根据物质的物理性质和化学性质进行综合解释.解;A、硫化氢是无色气体,颜色属于物理性质;
B、硫化氢气味有臭鸡蛋气味,气味属于物理性质;
C、硫化氢比空气重,密度属于物理性质;
D、硫化氢能燃烧,可燃性属于化学性质;
故选D.点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 本题主要考查了物质的两种性质的区别与联系的内容,可以依据题干提供的信息进行.1年前查看全部
- 2003年12月23日,川东气矿发生井喷事故,高压天然气携带一种有臭鸡蛋气味的气体--硫化氢(H2S)从地下喷出,向四周
2003年12月23日,川东气矿发生井喷事故,高压天然气携带一种有臭鸡蛋气味的气体--硫化氢(H2S)从地下喷出,向四周扩散,造成了上百人死亡.抢险队和救援队迅速进入事故地点并点燃了喷出的气体,切断有毒气体来源,并不断向空中喷洒碱水;救援队员发现,低洼地的人、蓄死亡率高,但是有一老年幸存者因摔到在水田里,头埋在和着烂泥的潮湿的草里,而幸免于中毒.若
请你根据上面的叙述,回答下列问题:
(1)硫化氢具有的物理性质:______;
(2)硫化氢具有的化学性质:______;
(3)如果你当时出在事故现场,你准备怎样保护自己?______. smilewbz1年前1
smilewbz1年前1 -
 春醇 共回答了19个问题
春醇 共回答了19个问题 |采纳率94.7%解题思路:物理性质是指物质不需要发生化学变化就表现出来的性质.化学性质是指物质在化学变化中表现出来的性质.而化学变化的本质特征是变化中有新物质生成,因此,判断物理性质还是化学性质的关键就是看表现物质的性质时是否有新物质产生.可以据此完成(1)和(2)两小题.
(3)根据该气体的物理性质考虑.(1)低洼地的人畜死亡率高,说明该气体密度比空气大,头埋在和着烂死的潮湿的草里,却幸免于中毒,说明该气体易溶于水;
(2)高压天然气携带一种有毒气体从地下喷出,所以该气体有毒;点燃了喷出的气体,说明该气体具有可燃性;(3)因为该气体易溶于水,所以要用湿毛巾捂住口鼻,又因为该气体密度比空气大,所以要向高处跑.
故该答案为:(1)密度比空气大;易溶于水;
(2)可燃性(或有毒);
(3)逃跑时要用湿毛巾捂住口鼻,向高处跑.点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 本题主要考查学生对题干信息的理解能力以及硫化氢气体性质方面的知识,是一道基础题.1年前查看全部
- 2003年12月23日,重庆川东北某天然气发生井喷事故,喷出的天然气中H2S(硫化氢)气体含量很高,H2S气体有臭鸡蛋气
2003年12月23日,重庆川东北某天然气发生井喷事故,喷出的天然气中H2S(硫化氢)气体含量很高,H2S气体有臭鸡蛋气味,密度比空气大,有剧毒.井喷发生不久,附近村民就闻到了臭鸡蛋气味,这体现了分子的性质;当村民们得知这种臭气有剧毒时,迅速撤离村庄,远离井喷地点.为减少村民的中毒机会,你认为村民在撤离井喷地点时应尽量走______(选填“低处”或“高处”);24日下午,技术人员通过原有的H2S放喷管线,成功点燃了地下喷出的H2S气体,使气体不扩散.H2S燃烧后生成了一种淡黄色的固体单质粉末和水;回答下列问题:
(1)H2S具有哪些物理性质______,
(2)点燃H2S说明它具有______性,写出该反应的化学方程式2H2S+O2
2S+2H2O点燃 ..2H2S+O2.
2S+2H2O点燃 .. yzang1年前1
yzang1年前1 -
 156430944 共回答了14个问题
156430944 共回答了14个问题 |采纳率100%解题思路:硫化氢的气味、密度、状态等属于物理性质.硫化氢具有可燃性属于化学性质,根据反应物和生成物及其质量守恒定律可以书写化学方程式.因为硫化氢的密度比空气大,所以村民在撤离井喷地点时应尽量走高处.故填:高处.
(1)硫化氢的物理性质有:是具有臭鸡蛋气味的气体,密度比空气大.故填:臭鸡蛋气味的气体,密度比空气大.
(2)硫化氢燃烧能生成水和硫,具有可燃性.故填:可燃.
硫化氢燃烧能生成水和硫,化学方程式为:2H2S+O2
点燃
.
2S+2H2O.点评:
本题考点: 化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要掌握化学方程式的书写方法和各种物质的性质方面的知识,只有这样才能对问题做出正确的判断.1年前查看全部
- 2006年3月,重庆开县发生天然气井漏事故,井漏喷出的气体含有大量的硫化氢气体.硫化氢(H 2 S)气体是一种有臭鸡蛋气
2006年3月,重庆开县发生天然气井漏事故,井漏喷出的气体含有大量的硫化氢气体.硫化氢(H 2 S)气体是一种有臭鸡蛋气味,剧毒的无色气体,密度比空气大,能溶于水,其水溶液显酸性,叫氢硫酸.把硫化氢气体通入浓硫酸中,发生的反应为:H 2 S+H 2 SO 4 (浓)=SO 2 +X↓+2H 2 O.
(1)硫化氢的一点物理性质:______.
(2)硫化氢与浓硫酸反应时,生成物中X的化学式为______.
(3)氢硫酸与盐酸一样能与氢氧化钠溶液发生中和反应,生成硫化钠和水,写出该反应的化学方程式______.
(4)为降低危害程度,消防队员可向空气中喷洒______,以减少空气中硫化氢的含量. 纳蓝容若1年前1
纳蓝容若1年前1 -
 易曦yi 共回答了15个问题
易曦yi 共回答了15个问题 |采纳率66.7%(1)硫化氢(H 2 S)气体是一种有臭鸡蛋气味,无色气体,密度比空气大,能溶于水.
(2)根据反应的化学方程式H 2 S+H 2 SO 4 (浓)=SO 2 +X↓+2H 2 O,反应物中氢、硫、氧原子个数分别为4、2、4,反应后的生成物中氢、硫、氧原子个数分别为4、1、4,根据反应前后原子种类、数目不变,则每个X分子由1个硫原子构成,则物质X的化学式为S.
(3)氢硫酸与盐酸一样能与氢氧化钠溶液发生中和反应,生成硫化钠和水,反应的化学方程式为:H 2 S+2NaOH═Na 2 S+2H 2 O.
(4)根据题意,硫化氢能溶于水,其水溶液显酸性,故可向空气中喷洒石灰水等碱性溶液或水以减少空气中硫化氢的含量.
故答案为:(1)有臭鸡蛋气味;(2)S;(3)H 2 S+2NaOH═Na 2 S+2H 2 O;(4)石灰水.1年前查看全部
- 某地天然气井发生井喷事故,喷出的天然气中H2S气体含量很高,H2S气体在臭鸡蛋气味,密度比空气大,有剧毒.井喷发生不久,
某地天然气井发生井喷事故,喷出的天然气中H2S气体含量很高,H2S气体在臭鸡蛋气味,密度比空气大,有剧毒.井喷发生不久,附近村民就闻到了臭鸡蛋气味,这体现了分子______的性质; 当村民得知这种气体有剧毒时,迅速撤离村庄.为减少村民的中毒机会,你认为村民在撤离时应尽量走______(填“低处”或“高处”).技术人员后来成功点燃了H2S气体,使气体不再扩散.已知H2S(硫化氢)燃烧时生成两种常见的氧化物,试写出H2S燃烧的化学方程式:2H2S+3O2
2SO2+2H2O点燃 .2H2S+3O2.
2SO2+2H2O点燃 . 星星一点亮1年前1
星星一点亮1年前1 -
 夜风七 共回答了14个问题
夜风七 共回答了14个问题 |采纳率100%解题思路:根据题意,结合分子的不断运动,以及硫化氢的性质进行解答.硫化氢具有可燃性属于化学性质,根据反应物和生成物及反应条件可以判断化学方程式.由于气体的分子不断运动,所以硫化氢会不断地扩散到空气中. 由于硫化氢密度比空气大所以会存于低处,H2S(硫化氢)燃烧时生成两种常见的氧化物,根据元素的种类在反应前后不变的规律,可判断生成物是二氧化硫和水,故反应的化学方程式为2H2S+3O2
点燃
.
2SO2+2H2O.
故答案为:不断运动;高出;2H2S+3O2
点燃
.
2SO2+2H2O.点评:
本题考点: 利用分子与原子的性质分析和解决问题;化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题是对硫化氢气体的考查,主要是对硫化氢的物理性质的应用,并结合质量守恒定律书写化学方程式.1年前查看全部
- 蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体(H 2 S ),H 2 S 气体是一种大气污染物,它在空气完全燃烧时,
蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体(H 2 S ),H 2 S 气体是一种大气污染物,它在空气完全燃烧时,生成了二氧化硫和水。把H 2 S 气体通入浓H 2 SO 4 中,发生的反应为:H 2 S + H 2 SO 4 ( 浓)==SO 2 + X ↓+ 2H 2 O
(1 )上述内容中,属于H 2 S 的物理性质是_______________________________________ ;
(2 )写出H 2 S 在空气中完全燃烧的化学方程式: ________________________________ ;
(3 )H 2 S 气体通入浓H 2 SO 4 中反应时,生成物中X 的化学式为________________ ;
(4 )若尾气中含有H 2 S ,用浓硫酸来吸收行吗?为什么? _____________________________ ;若你来建议,你认为使用何种试剂能达到吸收的效果?请写出相应的化学方程式________________________ 。 ss凯1234561年前1
ss凯1234561年前1 -
 盐煮咖啡 共回答了24个问题
盐煮咖啡 共回答了24个问题 |采纳率95.8%(1 )无色、有臭鸡蛋气味的气体;
(2 )2H 2 S + 3O 2 === 2SO 2 + 2H 2 O ;
(3 )S
(4 )不行,产生的SO 2 气体仍然是污染性气体; 用氢氧化钠溶液 H 2 S + 2NaOH == Na 2 S + 2H 2 O1年前查看全部
- 已知:H2S是一种无色具有臭鸡蛋气味的气体,易分解,能溶于水形成二元弱酸.某研究小组为研究H2S的性质进行了如下实验(已
已知:H2S是一种无色具有臭鸡蛋气味的气体,易分解,能溶于水形成二元弱酸.某研究小组为研究H2S的性质进行了如下实验(已知FeS为黑色难溶于水的固体).
(1)制取H2S:
(1)写出实验I中反应的离子方程式______.并用沉淀溶解平衡原理解释FeS溶解于盐酸的过程______.编号 操作 现象 Ⅰ 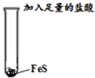
反应剧烈,试管中的黑色固体逐渐溶解,产生大量的无色具有臭鸡蛋气味的气体. Ⅱ 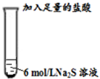
只有少量的无色臭鸡蛋气味的气体产生,但溶液中却有一定量的淡黄色沉淀产生.
该小组同学对实验Ⅱ中产生的现象发生了兴趣,首先设计实验探究沉淀的成分.实验和现象:将实验Ⅱ产生的沉淀进行______、洗涤、干燥.将沉淀放在燃烧匙中,伸入广口瓶灼烧.燃烧后向广口瓶中滴加少量品红溶液,振荡.品红溶液褪色,褪色后的溶液加热后又恢复红色.可以推知该淡黄色沉淀为______,写出沉淀燃烧产生刺激性气味气体的化学方程式S+O2
SO2点燃 .S+O2.
SO2点燃 .
(2)探究生成沉淀的原因.
提出假设:①H2S不稳定,分解生成沉淀;②______.
实验验证:
(3)重新假设并实验验证.编号 操作 现象 Ⅲ 将H2S通入蒸馏水中达到饱和,将该溶液分为两等份.一份静置,另一份在空气中不断振荡. 两份溶液在短时间内均未出现明显的浑浊现象.
查阅资料:在Na2S溶液中经常含有多硫化钠(Na2Sx),多硫化钠稳定,但在酸的作用下生成不稳定的多硫化氢,多硫化氢分解生成硫.即:Sx2-+2H+═H2SxH2Sx═H2S↑+(x-1)S
设计实验验证:
写出Na2S溶液暴露在空气里形成多硫化钠的化学方程式______.编号 操作 现象 Ⅳ 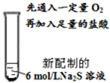
先通入一定量O2,几乎看不到明显变化;加入足量的盐酸,产生无色具有臭鸡蛋气味的气体,溶液中有大量的淡黄色沉淀产生.  邮戳与信封1年前1
邮戳与信封1年前1 -
 天仙冬不拉 共回答了18个问题
天仙冬不拉 共回答了18个问题 |采纳率94.4%解题思路:(1)实验Ⅰ时是FeS中加入足量稀盐酸反应生成氯化亚铁和硫化氢气体,硫化亚铁为难溶固体;依据沉淀溶解 平衡影响因素分析判断沉淀溶解过程;固体通过过滤从溶液中分离出,洗涤干燥,淡黄色固体燃烧生成的气体可以使品红溶液褪色,证明是二氧化硫气体,则淡黄色固体为硫单质;
(2)酸性溶液中硫离子被空气中氧气氧化为硫单质;
(3)Na2S、氧气、水反应生成Na2S2、NaOH,以此书写方程式;(1)实验Ⅰ时是FeS中加入足量稀盐酸反应生成氯化亚铁和硫化氢气体,硫化亚铁为难溶固体,反应的离子方程式为:FeS+2H+=Fe2++H2S↑;依据沉淀溶解 平衡影响因素分析判断沉淀溶解过程,硫化亚铁存在沉淀溶解平衡FeS(s)⇌Fe2++S2-,加入盐酸,氢离子结合硫离子生成硫化氢气体,促进平衡正向进行,硫化亚铁溶解;固体通过过滤从溶液中分离出,将实验Ⅱ产生的沉淀进行过滤、洗涤、干燥得到沉淀,淡黄色固体燃烧生成的气体可以使品红溶液褪色,证明是二氧化硫气体,反应的化学方程式为:S+O2
点燃
.
SO2 ;则淡黄色固体为硫单质;
故答案为:FeS+2H+=Fe2++H2S↑;硫化亚铁存在沉淀溶解平衡FeS(s)⇌Fe2++S2-,加入盐酸,氢离子结合硫离子生成硫化氢气体,促进平衡正向进行,硫化亚铁溶解;过滤,S,S+O2
点燃
.
SO2;
(2)将H2S通入蒸馏水中达到饱和,将该溶液分为两等份.一份静置,另一份在空气中不断振荡,两份溶液在短时间内均未出现明显的浑浊现象,但加入盐酸会出现硫化氢气体和硫单质,可能是硫化氢不稳定分解生成,也可能是酸溶液中硫离子被空气中氧气氧化生成硫单质;
故答案为:酸性溶液中硫离子被空气中氧气氧化为单质硫;
(3)Na2S、氧气、水反应生成Na2S2、NaOH,该反应的方程式为4Na2S+O2+2H2O═4NaOH+2Na2S2,故答案为:4Na2S+O2+2H2O═4NaOH+2Na2S2;点评:
本题考点: 性质实验方案的设计.
考点点评: 本题考查了物质性质分析,实验工厂设计和物质检验方法和反应现象的理解应用,掌握基础是关键,题目难度中等.1年前查看全部
- 硫化氢(化学式:H2S)是一种具有臭鸡蛋气味的气体,其中硫元素的化合价是( )
硫化氢(化学式:H2S)是一种具有臭鸡蛋气味的气体,其中硫元素的化合价是( )
A. +1
B. -l
C. +2
D. -2 xiaoxuesyh1年前1
xiaoxuesyh1年前1 -
 tyfans2008 共回答了21个问题
tyfans2008 共回答了21个问题 |采纳率90.5%解题思路:根据在化合物中正负化合价代数和为零,结合硫化氢(化学式:H2S)的化学式进行解答本题.氢元素显+1价,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x=0,则x=-2价.
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答本题.1年前查看全部
- 二氧化硫是造成酸雨的主要气体,其水溶液叫亚硫酸(H 2 SO 3 )。硫化氢(H 2 S)是一种具有臭鸡蛋气味的剧毒气体
二氧化硫是造成酸雨的主要气体,其水溶液叫亚硫酸(H 2 SO 3 )。硫化氢(H 2 S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为:2H 2 S+H 2 SO 3 =3S↓+3H 2 O。下列溶液的pH随通入硫化氢体积的变化曲线示意图中,正确的是()
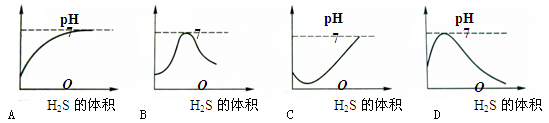
 ck888991年前1
ck888991年前1 -
 xieyishu78 共回答了17个问题
xieyishu78 共回答了17个问题 |采纳率82.4%B
1年前查看全部
- 硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空气大,可溶于水形成氢硫酸,氢硫酸具有酸的通性.实验室常用固体
 硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空气大,可溶于水形成氢硫酸,氢硫酸具有酸的通性.实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeS04.
硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空气大,可溶于水形成氢硫酸,氢硫酸具有酸的通性.实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeS04.
(1)在如图中,应选用图______作为制取H2S的装置.
(2)收集H2S气体满后,对产生尾气的处理方法是:______.
(3)实验室若制取6.8克的硫化氢气体,理论上需要多少克20%的硫酸溶液? Done1年前1
Done1年前1 -
 caozhen762695 共回答了14个问题
caozhen762695 共回答了14个问题 |采纳率92.9%解题思路:(1)根据实验室制取硫化氢的反应物状态、反应条件可以选择制取硫化氢的发生装置;
(2)氢硫酸具有酸的通性,能和碱性溶液发生反应;
(3)根据反应的化学方程式、硫化氢的质量可以计算硫酸溶液的质量.(1)固体硫化亚铁和稀硫酸反应时不需要加热,应该用B装置作为发生装置.
故填:B.
(2)氢氧化钠和硫化氢反应生成硫化钠和水,因此可以用氢氧化钠溶液吸收硫化氢气体.
故填:用氢氧化钠溶液吸收.
(3)设需要20%硫酸溶液的质量为x,
FeS+H2SO4═FeS04+H2S↑,
9834
x×20% 6.8g
[98/34]=[x×20%/6.8g],
x=98g;
答:若制取6.8g的硫化氢气体,理论上需要98g20%的硫酸溶液.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;气体的净化(除杂);根据化学反应方程式的计算.
考点点评: 本题主要考查实验装置的选择、酸碱中和反应、根据化学方程式计算的方面的知识,计算时要注意规范性和准确性.1年前查看全部
- 【化学题】:1.A和B可以相互转化,B在沸水中可以生成C,C在空气中氧化成D,D有臭鸡蛋气味,请问A,B,C,D各是什么
【化学题】:
1.A和B可以相互转化,B在沸水中可以生成C,C在空气中氧化成D,D有臭鸡蛋气味,请问A,B,C,D各是什么? 星无泪1年前4
星无泪1年前4 -
 loveluzhu 共回答了18个问题
loveluzhu 共回答了18个问题 |采纳率83.3%又一个受害者.
教科书上说
有臭鸡蛋气味的是H2S(硫化氢)
但是遗憾的是
它具有还原性
不可能有某种物质(题目中的所谓“C”)能够在空气中可以氧化成它
这题实际上是某位达人(原作者已经无从查找了,有知情者请告知,谢谢)恶搞高考化学题而编造出来的
恶搞答案是:A是鸡,B是生鸡蛋,C是熟鸡蛋,D是臭鸡蛋1年前查看全部
- 已知正盐A能与盐酸反应生成臭鸡蛋味气体,又能与Naoh反应生成气体,在一定条件下,A能实现下列转化
已知正盐A能与盐酸反应生成臭鸡蛋味气体,又能与Naoh反应生成气体,在一定条件下,A能实现下列转化
A和x生成B B和氧气生成C C和氧气生成D D和水生成E E和Cu生成C
1. A是什么
2当x为盐酸时 E与Cu反应的化学方程式为?
当x为NaOH溶液时E与Cu反应的化学方程式为? 河云1年前2
河云1年前2 -
 青鸟飞羽 共回答了21个问题
青鸟飞羽 共回答了21个问题 |采纳率100%1.A :(NH3)2S
2.x为HCl时,B:H2S,C:SO2,D:SO3,E:H2SO4,
2H2SO4(浓)+Cu==加热==CuSO4+2H2O+SO2(气体)
x为NaOH时,B:NH3,C:NO,D:NO2,E:HNO3
8HNO3(稀)+3Cu=3Cu(NO3)2+ 4H2O+ 2NO(气体)1年前查看全部
- 急求制备硫酸亚铁铵的问题.1)在制备硫酸亚铁时,为什么会有臭鸡蛋味?2)在Fe和H2SO4反应过程中,为什么要把温度控制
急求制备硫酸亚铁铵的问题.
1)在制备硫酸亚铁时,为什么会有臭鸡蛋味?
2)在Fe和H2SO4反应过程中,为什么要把温度控制在50-60℃之间?
3)在制备硫酸亚铁中,为什么要趁热过滤,并用少量水洗涤滤纸?如果不这样做,有什么后果? hjwp9119111年前1
hjwp9119111年前1 -
 aitaya 共回答了20个问题
aitaya 共回答了20个问题 |采纳率80%1.臭鸡蛋味是生成了部分的硫化氢,H2S
2.温度过高,反应速度太快,控制不住,另外,会有副产物.温度低了,反应速度慢,营销效率
3.硫酸亚铁容易被氧化成硫酸铁,趁热过滤有一个好处就是减少他和氧气接触的机会,因为温度高了,气体在水中的溶解度就要减小.1年前查看全部
- 臭鸡蛋气味的气体A与B可以相互转化,B在沸水中生成C,C在空气中氧化成D,D有臭鸡蛋气味.问ABCD 个是什么
 清茶疏影1年前5
清茶疏影1年前5 -
 ngu2002 共回答了21个问题
ngu2002 共回答了21个问题 |采纳率90.5%A鸡.B鸡蛋.C熟鸡蛋D臭鸡蛋1年前查看全部
- 硫化氢如何生成给几个化学方程式我把一个烟花棒『小孩子玩的那种』点燃,然后伸入水中,居然可以燃烧!并且闻到硫化氢的臭鸡蛋味
硫化氢如何生成
给几个化学方程式
我把一个烟花棒『小孩子玩的那种』点燃,然后伸入水中,居然可以燃烧!
并且闻到硫化氢的臭鸡蛋味,谢 那年我们正年轻1年前1
那年我们正年轻1年前1 -
 迷雾中的青绿 共回答了20个问题
迷雾中的青绿 共回答了20个问题 |采纳率70%S2-+2H+=H2S↑(氢离子只能由可溶且不是硫酸的酸来提供)
S+2H=H2S (条件:加热)
答案补充:
S+2KNO3+3C=K2S+3CO2↑+N2↑
CO2+H2O=H2O=H2CO3
H2CO3+K2S=H2S↑+K2CO31年前查看全部
- 我要问问化学题A和B分别是一个可逆反应的反应物和生成物B和水在高温条件下生成DC物质经慢性氧化生成DD是有臭鸡蛋味的物质
我要问问化学题
A和B分别是一个可逆反应的反应物和生成物
B和水在高温条件下生成D
C物质经慢性氧化生成D
D是有臭鸡蛋味的物质
请问A,B,C,D各是什么物质 心碧1年前1
心碧1年前1 -
 caizibo 共回答了22个问题
caizibo 共回答了22个问题 |采纳率81.8%题是不是错了?B和水在高温下生成C吧
那就是A母鸡B鸡蛋C熟鸡蛋D臭鸡蛋1年前查看全部
- A由B转化而来,B在沸水中生成C,C在空气中氧化成为D,D有臭鸡蛋气味,问:这四种物质分别是什么?
 fushuai3891年前1
fushuai3891年前1 -
 恋夕夕 共回答了18个问题
恋夕夕 共回答了18个问题 |采纳率94.4%A=鸡
B=鸡蛋
C=熟鸡蛋
D=臭鸡蛋1年前查看全部
- 猜ABCD各是什么?A和B经过一定的条件可以互相转化,B加热后可以生成C,C在空气中氧化生成D,D是一种有臭鸡蛋气味的物
猜ABCD各是什么?
A和B经过一定的条件可以互相转化,B加热后可以生成C,C在空气中氧化生成D,D是一种有臭鸡蛋气味的物质,请问,A、B、C、D各是什么 lc200164221年前2
lc200164221年前2 -
 淡蓝嘀海 共回答了14个问题
淡蓝嘀海 共回答了14个问题 |采纳率85.7%A:鸡(条件:会生蛋的母鸡,下的蛋)
B:鸡蛋(条件:孵化)
C:熟鸡蛋(条件:开水煮)
D:臭鸡蛋(条件:在空气中放置一定时间)1年前查看全部
- H2S是一种无色有臭鸡蛋气味的气体有剧毒H2S燃烧生成两种常见的氧化物写出该反应的化学方程式.(着急,
 roshyang1年前1
roshyang1年前1 -
 手的纹路 共回答了20个问题
手的纹路 共回答了20个问题 |采纳率85%2H2S+O2=2H2O+S
2H2S+3O2=2H2O+2SO2
如果H2S:O2>2:1 只有第一个1年前查看全部
- A和B可以相互转化,B在沸水中生成C,C在空气中氧化成D,D有臭鸡蛋味.请问这ABCD分别是什么?
 hunbecca1年前1
hunbecca1年前1 -
 dreamtrue51 共回答了23个问题
dreamtrue51 共回答了23个问题 |采纳率87%A=鸡
B=鸡蛋
C=熟鸡蛋
D=臭鸡蛋1年前查看全部
- A和B可以互相转化,B在沸水中生成C,C在空气中氧化成为D,D有臭鸡蛋味,请问ABCD分别是什么?
A和B可以互相转化,B在沸水中生成C,C在空气中氧化成为D,D有臭鸡蛋味,请问ABCD分别是什么?
我要正确答案d是硫化氢那种的,不要鸡蛋系列的那个答案
额,能把化学方程式写上么? cr04691年前1
cr04691年前1 -
 老李大 共回答了21个问题
老李大 共回答了21个问题 |采纳率90.5%好久不学化学了,给你找的答案
此题突破口应该是D具有臭鸡蛋味,由此可判断出D是H2S(硫化氢),再由C在空气中氧化成B,B在沸水生成C,可判断出C为S(硫),B为SO2(二氧化硫),又有"A由B转化而来"故A是H2SO3(亚硫酸).
所以,A是H2SO3(亚硫酸).B为SO2(二氧化硫).C为S(硫).D是H2S(硫化氢).1年前查看全部
- 猜ABCD各是什么A和B可以互相转化,B在沸水中变成C,C在空气中可以氧化成D,D有臭鸡蛋味,问,ABCD分别是什么,这
猜ABCD各是什么
A和B可以互相转化,B在沸水中变成C,C在空气中可以氧化成D,D有臭鸡蛋味,问,ABCD分别是什么,这个问题爱因斯坦一辈子也没弄清楚,化学不及格的别猜.哈哈. lyggod1年前1
lyggod1年前1 -
 Johnwayu 共回答了9个问题
Johnwayu 共回答了9个问题 |采纳率100%A母鸡B鸡蛋C熟鸡蛋D臭鸡蛋1年前查看全部
- 什么与水反应生成一种有臭鸡蛋气味的气体和一种温室气体
什么与水反应生成一种有臭鸡蛋气味的气体和一种温室气体
000 fjf0011年前2
fjf0011年前2 -
 nona_nie 共回答了16个问题
nona_nie 共回答了16个问题 |采纳率87.5%CSO 电子式
.. ..
:O::C::S :
CS2与水不互溶,据我所知很难与水反应1年前查看全部
- 在化学中有臭鸡蛋气味的是什么气体
 lijingjian1年前1
lijingjian1年前1 -
 shuaigege1234567 共回答了26个问题
shuaigege1234567 共回答了26个问题 |采纳率92.3%硫化氢 H2S
我们学到现在仅此一例!挺好记的1年前查看全部
- 求解!一道简单又复杂的化学题!A生成B,B在沸水中生成C,C氧化成D,D有臭鸡蛋味!问A、B、C、D各是什么?既简单又复
求解!一道简单又复杂的化学题!
A生成B,B在沸水中生成C,C氧化成D,D有臭鸡蛋味!
问A、B、C、D各是什么?
既简单又复杂! milaeng1年前2
milaeng1年前2 -
 wetom 共回答了21个问题
wetom 共回答了21个问题 |采纳率90.5%A和B可以相互转化,鸡和鸡蛋
B在沸水中生成C,鸡蛋和熟鸡蛋
C在空气中可以氧化成D,熟鸡蛋和臭鸡蛋
D有臭鸡蛋气味,
请问ABCD各是什么?
A 鸡
B 鸡蛋
C 熟鸡蛋
D 臭鸡蛋1年前查看全部
- 高中化学出现的各种物质特征在高中化学中有很多物质有特殊标志,比如 1.硫化氢 又臭鸡蛋味 2.二氧化碳通到澄清石灰水中变
高中化学出现的各种物质特征
在高中化学中有很多物质有特殊标志,比如 1.硫化氢 又臭鸡蛋味 2.二氧化碳通到澄清石灰水中变混浊 等本身或化学反应特征
能否给我比较全的各种物质特征
最好能是 推断题中爱出现的 裙摆舞随1年前1
裙摆舞随1年前1 -
 wangmeili98 共回答了21个问题
wangmeili98 共回答了21个问题 |采纳率100%物质鉴别题的类型和解题步骤、方法
一、鉴定、鉴别和推断的区别和联系
鉴定、鉴别和推断都属于物质的检验,它们的共同点是:依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理.
鉴定通常是指对于某一种物质的定性检验,根据物质的化学特性,分别检出阳离子、阴离子;鉴别通常是指对分别存放的两种或两种以上的物质进行定性辨认,可根据一种物质的特性区别于另一种,也可根据几种物质的颜色、气味、溶解性、溶解时的热效应等一般性质的不同加以区别;推断是通过已知实验事实,根据性质分析推求出被检验物质的组成和名称.我们要综合运用化学知识对常见物质进行鉴别和推断.
1.常见气体的检验
常见
气体 检验方法
H2 纯净的氢气在空气中燃烧呈淡蓝色火焰,混合空气点燃有爆鸣声,生成物只有水.不是只有氢气才产生爆鸣声;可点燃的气体不一定是氢气
O2 可使带火星的木条复燃
Cl2 黄绿色,能使湿润的碘化钾淀粉试纸变蓝(O3、NO2也能使湿润的碘化钾淀粉试纸变蓝)
HCl 无色有刺激性气味的气体.在潮湿的空气中形成白雾,能使湿润的蓝色石蓝试纸变红;用蘸有浓氨水的玻璃棒靠近时冒白烟;将气体通入AgNO3溶液时有白色沉淀生成.
SO2 无色有刺激性气味的气体.能使品红溶液褪色,加热后又显红色.能使酸性高锰酸钾溶液褪色.
H2S 无色有具鸡蛋气味的气体.能使Pb(NO3)2或CuSO4溶液产生黑色沉淀,或使湿润的醋酸铅试纸变黑.
NH3 无色有刺激性气味,能使湿润的红色石蕊试纸变蓝,用蘸有浓盐酸的玻璃棒靠近时能生成白烟.
NO2 红棕色气体,通入水中生成无色的溶液并产生无色气体,水溶液显酸性.
NO 无色气体,在空气中立即变成红棕色
CO2 能使澄清石灰水变浑浊;能使燃着的木条熄灭.SO2气体也能使澄清的石灰水变混浊,N2等气体也能使燃着的木条熄灭.
CO 可燃烧,火焰呈淡蓝色,燃烧后只生成CO2;能使灼热的CuO由黑色变成红色.
CH4 无色气体,可燃,淡蓝色火焰,生成水和CO2;不能使高锰酸钾溶液、溴水褪色.
C2H4 无色气体、可燃,燃烧时有明亮的火焰和黑烟,生成水和CO2.能使高锰酸钾溶液、溴水褪色.
C2H2 无色无臭气体,可燃,燃烧时有明亮的火焰和浓烟,生成水和 CO2,能使高锰酸钾溶液、溴水褪色.
2.几种重要阳离子的检验
(l)H+ 能使紫色石蕊试液或橙色的甲基橙试液变为红色.
(2)Na+、K+ 用焰色反应来检验时,它们的火焰分别呈黄色、浅紫色(通过钴玻片).
(3)Ba2+ 能使稀硫酸或可溶性硫酸盐溶液产生白色BaSO4沉淀,且沉淀不溶于稀硝酸.
(4)Mg2+ 能与NaOH溶液反应生成白色Mg(OH)2沉淀,该沉淀能溶于NH4Cl溶液.
(5)Al3+ 能与适量的NaOH溶液反应生成白色Al(OH)3絮状沉淀,该沉淀能溶于盐酸或过量的NaOH溶液.
(6)Ag+ 能与稀盐酸或可溶性盐酸盐反应,生成白色AgCl沉淀,不溶于稀 HNO3,但溶于氨水,生成〔Ag(NH3)2〕+.
(7)NH4+ 铵盐(或浓溶液)与NaOH浓溶液反应,并加热,放出使湿润的红色石蓝试纸变蓝的有刺激性气味NH3气体.
(8)Fe2+ 能与少量NaOH溶液反应,先生成白色Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色Fe(OH)3沉淀.或向亚铁盐的溶液里加入KSCN溶液,不显红色,加入少量新制的氯水后,立即显红色.2Fe2++Cl2=2Fe3++2Cl-
(9)Fe3+ 能与 KSCN溶液反应,变成血红色 Fe(SCN)3溶液,能与 NaOH溶液反应,生成红褐色Fe(OH)3沉淀.
(10)Cu2+ 蓝色水溶液(浓的CuCl2溶液显绿色),能与NaOH溶液反应,生成蓝色的Cu(OH)2沉淀,加热后可转变为黑色的 CuO沉淀.含Cu2+溶液能与Fe、Zn片等反应,在金属片上有红色的铜生成.
3.几种重要的阴离子的检验
(1)OH-能使无色酚酞、紫色石蕊、橙色的甲基橙等指示剂分别变为红色、蓝色、黄色.
(2)Cl-能与硝酸银反应,生成白色的AgCl沉淀,沉淀不溶于稀硝酸,能溶于氨水,生成[Ag(NH3)2]+.
(3)Br- 能与硝酸银反应,生成淡黄色AgBr沉淀,不溶于稀硝酸.
(4)I- 能与硝酸银反应,生成黄色AgI沉淀,不溶于稀硝酸;也能与氯水反应,生成I2,使淀粉溶液变蓝.
(5)SO42- 能与含Ba2+溶液反应,生成白色BaSO4沉淀,不溶于硝酸.
(6)SO32- 浓溶液能与强酸反应,产生无色有刺激性气味的SO2气体,该气体能使品红溶液褪色.能与BaCl2溶液反应,生成白色BaSO3沉淀,该沉淀溶于盐酸,生成无色有刺激性气味的SO2气体.
(7)S2- 能与Pb(NO3)2溶液反应,生成黑色的PbS沉淀.
(8)CO32- 能与BaCl2溶液反应,生成白色的BaCO3沉淀,该沉淀溶于硝酸(或盐酸),生成无色无味、能使澄清石灰水变浑浊的CO2气体.
(9)HCO3- 取含HCO3-盐溶液煮沸,放出无色无味CO2气体,气体能使澄清石灰水变浑浊.或向HCO3-盐酸溶液里加入稀MgSO4溶液,无现象,加热煮沸,有白色沉淀 MgCO3生成,同时放出 CO2气体.
(10)PO43- 含磷酸根的中性溶液,能与AgNO3反应,生成黄色Ag3PO4沉淀,该沉淀溶于硝酸.w.w.w.k.s.5.u.c.o.m
(11)NO3- 浓溶液或晶体中加入铜片、浓硫酸加热,放出红棕色气体.
4.几种重要有机物的检验
(1)苯 能与纯溴、铁屑反应,产生HBr白雾.能与浓硫酸、浓硝酸的混合物反应,生成黄色的苦杏仁气味的油状(密度大于1)难溶于水的硝基苯.
(2)乙醇 能够与灼热的螺旋状铜丝反应,使其表面上黑色CuO变为光亮的铜,并产生有刺激性气味的乙醛.乙醇与乙酸、浓硫酸混合物加热反应,将生成的气体通入饱和Na2CO3溶液,有透明油状、水果香味的乙酸乙酯液体浮在水面上.
(3)苯酚能与浓溴水反应生成白色的三溴苯酚沉淀.能与FeCl3溶液反应,生成紫色溶液.
(4)乙醛 能发生银镜反应,或能与新制的蓝色Cu(OH)2加热,生成红色的 Cu2O沉淀.
二、物质鉴别的几种主要类型
1、任意选择试剂的物质鉴别
这是指一般类型鉴别题.它不限所用鉴别试剂的多少,只要求能简明扼要,一一区别开来即可.比如,鉴别下列六种气体:O2、Cl2、NH3、CO2、N2、空气.对于此题可先观色,即黄绿色者为Cl2,后闻气味,即有刺激性气味的是NH3,其余再点燃,火焰无明显变化的是空气,燃烧更旺的是O2,火焰熄灭的是CO2和N2,再将CO2和N2分别通入石灰水,石灰水变浑浊的是CO2,不变的为N2.w.w.w.k.s.5.u.c.o.m
2.限用一种试剂的鉴别题
这类题较前者更复杂,它要求只允许用一种试剂加以一一区别.为此,我们所选用的那种试剂须能分别与被鉴别物反应,产生各种不同的现象才行,即被检物有几种就应产生几种不同的现象(包括没有明显变化也是一种现象).
3、不用任何试剂的鉴别题
它要求不准用任何外来试剂去参与物质鉴别.为此,须掌握待鉴物之间相互鉴别之功能,或先加热或先观察所给物质颜色,或先水溶然后再相互滴加鉴别之.如不用任何试剂,将HCl、BaCl2、NaOH、CuSO4四种溶液鉴别出来.经观察,四种溶液中只有CuSO4溶液显蓝色,其余为无色.把CuSO4溶液分别滴入另三种溶液中,有白色沉淀产生的原溶液为BaCl2溶液;有白蓝色沉淀产生的原溶液为NaOH溶液,剩余的为HCl溶液
三、物质鉴别题的解题步骤、方法
物质鉴别题的解题步骤、方法又根据物质的状态不同而又有所区别.但解答此类题的叙述程序基本相同,就是:由操作到现象再到结论最后写出有关方程式.
1、气态物质的鉴别
鉴别气态物质的步骤和方法一般遵循:
①看气体的颜色;②嗅气味;③用试纸检验;④用火点燃⑤加有关试剂.当然,在具体操作时,可根据题意省略或变动其中的某些步骤和顺序
【例1】在十个集气瓶里分别盛有Cl2、N2、O2、H2S、CO2、HCl、NO2、CO、H2、NO等气体,试用最简单的方法把它们鉴别出来.w.w.w.k.s.5.u.c.o.m
解析:①看颜色:黄绿色的为Cl2,棕红色的为NO2,瓶口附近出现棕红色的为NO;②嗅气味:有臭鸡蛋气味的为H2S,有刺激性气味的为HCl;③用湿润的蓝色石蕊试纸检验:试纸变红的为CO2(此步也可省略);④用燃着的木条试验:熄灭的为N2,燃烧更旺的为O2,气体被点燃的是CO、H2;⑤用蘸有石灰水的玻璃棒置于燃烧的火焰附近,石灰水出现浑浊的为CO,无浑浊出现的为H2.
2、固态物质的鉴别
鉴别固态物质时,一般采用如下的步骤和方法,即①分别取出试样,配成溶液;②各取少量试液,分别加入有关的试剂,根据不同现象加以区分或分组;③分组取出少量试液,各加有关的试剂,根据反应特征,加以区分 w.w.w.k.s.5.u.c.o.m
【例2】 现有十瓶白色固体,它们是Al2O3、Ca CO3、Ba(OH)2、Mg Cl2、 BaSO4、AlCl3、NH4NO3、NaNO3、 (NH4)2SO4、无水CuSO4等,是将它们一一鉴别出来.
解析:①加水配成溶液,不溶的有Al2O3、Ca CO3、BaSO4;溶液成蓝色的为无水CuSO4;溶液成无色的有Ba(OH)2、Mg Cl2、AlCl3、NH4NO3、NaNO3、 (NH4)2SO4
②在不溶物组中分别加NaOH溶液,溶解的为Al2O3,不溶的为Ca CO3、BaSO4.再向Ca CO3、BaSO4中分别加盐酸,溶解的为Ca CO3,仍不溶的为BaSO4
③在无色溶液组中分别加CuSO4溶液,出现蓝色沉淀的为Ba(OH)2;不出现沉淀的为Mg Cl2、AlCl3、NH4NO3、NaNO3、 (NH4)2SO4等
④在余下的五种溶液中,分别加Ba(OH)2溶液,无明显现象的为NaNO3;有白色沉淀且不消失的为Mg Cl2,有白色沉淀过量后消失的为AlCl3,有气体产生而无沉淀的为NH4NO3,既有气体产生又生成沉淀的为(NH4)2SO4 w.w.w.k.s.5.u.c.o.m
(溶液的鉴别在另一专题中单独归纳)
你会寻找鉴别方法吗?
“有比较才有鉴别”.可见,比较是鉴别的前提.通过比较,找出性质差异,依据性质差异寻找体现性质差异的鉴别方法,是解答鉴别物质题的常规思路.要提醒同学们的是:找差异可从整体找,也可从局部找;可从化学性质找,也可从物理性质找.对同一问题的鉴别方法可能有多种.例如:
题目:如何鉴别室温下等体积饱合食盐水、蒸馏水各一杯.
解析:饱和食盐水与蒸馏水的差异是显而易见的:即蒸馏水中不含Na+和Cl-.就是这种组成上的差别,造成它们性质上的很多差异.因而就有如下的可用鉴别方法:
1、往两液体中分别滴入AgNO3溶液,有白色沉淀产生者为饱和食盐水.
2、分别称量等体积的两液体,质量大者为饱和食盐水.
3、分别测两液体的导电性,导电能力强者为饱和食盐水.
4、分别测丙液体的沸点,高者为饱和食盐水.
5、分别加热蒸发两液体,冷却后见有晶体者为饱和食盐水.
6、分别在两液体中加入少量食盐晶体,搅拌后有不溶晶体者为饱和食盐水.
7、在两液体中分别通入HCl气体,有晶体析出者为饱和食盐水.
8、用洁净铂丝分别蘸取两液体在无色火焰上灼烧,火焰呈黄色者为饱和食盐水.
当然,还可以有其他的办法.
另外,有人认为,只要尝一下这两种液体的味道便可解决问题,岂不更简单.本来这办法也是正确的,不过,在化学上,我们总是尽可能避免去尝物质的味道,以免错尝了毒物.
高中化学——常见的特征反应现象及对应物质
常见的特征反应现象及对应物质
① 焰色反应显黄色Na显紫色(透过钴玻璃)的元素是K
② 有臭鸡蛋气味或能使湿Pb(Ac)2 试纸变黑的气体是H2S
③ 在空气中由无色迅速变为红棕色NO
④ 使品红溶液褪色SO2
⑤ 能使淀粉变蓝I2
⑥ 与碱溶液反应生成白色沉淀在空气中迅速变灰绿色最终变红褐色的离子___Fe2+
⑦ 滴入KSCN溶液显血红色以及遇苯酚显紫色的离子__Fe3+
⑧ 投入水中生成气体和难溶物(或微溶物) CaC2 Al2S3 Mg3N2
⑨ 既能跟酸反应又能跟碱反应且生成气体Al NH4HCO3 (NH4)2CO3 (NH4)2S
⑩ 能使湿润的红色石蕊试纸变蓝的气体NH3
物质的性质
1.颜色的规律
(1)常见物质颜色
① 以红色为基色的物质
红色:难溶于水的Cu,Cu2O,Fe2O3,HgO等.
碱液中的酚酞、酸液中甲基橙、石蕊及pH试纸遇到较强酸时及品红溶液.
橙红色:浓溴水、甲基橙溶液、氧化汞等.
棕红色:Fe(OH)3固体、Fe(OH)3水溶胶体等.
② 以黄色为基色的物质
黄色:难溶于水的金、碘化银、磷酸银、硫磺、黄铁矿、黄铜矿(CuFeS2)等.
溶于水的FeCl3、甲基橙在碱液中、钠离子焰色及TNT等.
浅黄色:溴化银、碳酦银、硫沉淀、硫在CS2中的溶液,还有黄磷、Na2O2、氟气.
棕黄色:铜在氯气中燃烧生成CuCl2的烟.
③ 以棕或褐色为基色的物质
碘水浅棕色、碘酒棕褐色、铁在氯气中燃烧生成FeCl3的烟等
④ 以蓝色为基色的物质
蓝色:新制Cu(OH)2固体、胆矾、硝酸铜、溶液中淀粉与碘变蓝、石蕊试液碱变蓝、pH试纸与弱碱变蓝等.
浅蓝色:臭氧、液氧等
蓝色火焰:硫、硫化氢、一氧化碳的火焰.甲烷、氢气火焰(蓝色易受干扰).
⑤ 以绿色为色的物质
浅绿色:Cu2(OH)2CO3,FeCl2,FeSO4•7H2O.
绿色:浓CuCl2溶液、pH试纸在约pH=8时的颜色.
深黑绿色:K2MnO4.
黄绿色:Cl2及其CCl4的萃取液.
⑥ 以紫色为基色的物质
KMnO4为深紫色、其溶液为红紫色、碘在CCl4萃取液、碘蒸气、中性pH试纸的颜色、K+离子的焰色等.
⑦ 以黑色为基色的物质
黑色:碳粉、活性碳、木碳、烟怠、氧化 铜、四氧化三铁、硫化亚铜(Cu2S)、硫化铅、硫化汞、硫化银、硫化亚铁、氧化银(Ag2O).
浅黑色:铁粉.
棕黑色:二氧化锰.
⑧ 白色物质
★ 无色晶体的粉末或烟尘;
★ 与水强烈反应的P2O5;
★ 难溶于水和稀酸的:AgCl,BaSO4,PbSO4;
★ 难溶于水的但易溶于稀酸:BaSO3,Ba3(PO4)2,BaCO3,CaCO3,Ca3(PO4)2,CaHPO4,Al(OH)3,Al2O3,ZnO,Zn(OH)2,ZnS,Fe(OH)2,Ag2SO3,CaSO3等;
★ 微溶于水的:CaSO4,Ca(OH)2,PbCl2,MgCO3,Ag2SO4;
★ 与水反应的氧化物:完全反应的:BaO,CaO,Na2O;
不完全反应的:MgO.
⑨ 灰色物质
石墨灰色鳞片状、砷、硒(有时灰红色)、锗等.
(2)离子在水溶液或水合晶体的颜色
① 水合离子带色的:
Fe2+:浅绿色;
Cu2+:蓝色;
Fe3+:浅紫色 呈黄色因有[FeCl4(H2O)2] 2-;
MnO4-:紫色
:血红色;
:苯酚与FeCl3的反应开成的紫色.
②主族元素在水溶液中的离子(包括含氧酸根)无色.
运用上述规律便于记忆溶液或结晶水合物的颜色.
(3)主族金属单质颜色的特殊性
ⅠA,ⅡA,ⅣA,ⅤA的金属大多数是银白色.
铯:带微黄色 钡:带微黄色
铅:带蓝白色 铋:带微红色
(4)其他金属单质的颜色
铜呈紫红色(或红),金为黄色,其他金属多为银白色,少数为灰白色(如锗).
(5)非金属单质的颜色
卤素均有色;氧族除氧外,均有色;氮族除氮外,均有色;碳族除某些同素异形体(金钢石)外,均有色.
2.物质气味的规律(常见气体、挥发物气味)
① 没有气味的气体:H2,O2,N2,CO2,CO,稀有气体,甲烷,乙炔.
② 有刺激性气味:HCl,HBr,HI,HF,SO2,NO2,NH3•HNO3(浓液)、乙醛(液).
③ 具有强烈刺激性气味气体和挥发物:Cl2,Br2,甲醛,冰醋酸.
④ 稀有气味:C2H2.
⑤ 臭鸡蛋味:H2S.
⑥ 特殊气味:苯(液)、甲苯(液)、苯酚(液)、石油(液)、煤焦油(液)、白磷.
⑦ 特殊气味:乙醇(液)、低级酯.
⑧ 芳香(果香)气味:低级酯(液).
⑨ 特殊难闻气味:不纯的C2H2(混有H2S,PH3等).
3.熔点、沸点的规律
晶体纯物质有固定熔点;不纯物质凝固点与成分有关(凝固点不固定).
非晶体物质,如玻璃、水泥、石蜡、塑料等,受热变软,渐变流动性(软化过程)直至液体,没有熔点.
沸点指液体饱和蒸气压与外界压强相同时的温度,外压力为标准压(1.01×105Pa)时,称正常沸点.外界压强越低,沸点也越低,因此减压可降低沸点.沸点时呈气、液平衡状态.
(1)由周期表看主族单质的熔、沸点
同一主族单质的熔点基本上是越向下金属熔点渐低;而非金属单质熔点、沸点渐高.但碳族元素特殊,即C,Si,Ge,Sn越向下,熔点越低,与金属族相似.还有ⅢA族的镓熔点比铟、铊低,ⅣA族的锡熔点比铅低.
(2)同周期中的几个区域的熔点规律
① 高熔点单质
C,Si,B三角形小区域,因其为原子晶体,熔点高.金刚石和石墨的熔点最高大于3550℃,金属元素的高熔点区在过渡元素的中部和中下部,其最高熔点为钨(3410℃).
② 低熔点单质
非金属低熔点单质集中于周期表的右和右上方,另有IA的氢气.其中稀有气体熔、沸点均为同周期的最低者,而氦是熔点(-272.2℃,26×105Pa)、沸点(268.9℃)最低.
金属的低熔点区有两处:IA、ⅡB族Zn,Cd,Hg及ⅢA族中Al,Ge,Th;ⅣA族的Sn,Pb;ⅤA族的Sb,Bi,呈三角形分布.最低熔点是Hg(-38.87℃),近常温呈液态的镓(29.78℃)铯(28.4℃),体温即能使其熔化.
(3)从晶体类型看熔、沸点规律
原子晶体的熔、沸点高于离子晶体,又高于分子晶体.金属单质和合金属于金属晶体,其中熔、沸点高的比例数很大(但也有低的).
在原子晶体中成键元素之间共价键越短的键能越大,则熔点越高.判断时可由原子半径推导出键长、键能再比较.如熔点:
金刚石>碳化硅>晶体硅
分子晶体由分子间作用力而定,其判断思路是:
① 结构性质相似的物质,相对分子质量大,范德华力大,则熔、沸点也相应高.如烃的同系物、卤素单质、稀有气体等.
② 相对分子质量相同,化学式也相同的物质(同分异构体),一般烃中支链越多,熔沸点越低.烃的衍生物中醇的沸点高于醚;羧酸沸点高于酯;油脂中不饱和程度越大,则熔点越低.如:油酸甘油酯常温时为液体,而硬脂酸甘油酯呈固态.
上述情况的特殊性最主要的是相对分子质量小而沸点高的三种气态氢化物:NH3,H2O,HF比同族绝大多数气态氢化物的沸点高得多(主要因为有氢键).
(4)某些物质熔沸点高、低的规律性
① 同周期主族(短周期)金属熔点.如
LiNaI.
4.物质溶解性规律
(1)气体的溶解性
① 常温极易溶解的
NH3[1(水):700(气)] HCl(1:500)
还有HF,HBr,HI,甲醛(40%水溶液—福尔马林).
② 常温溶于水的
CO2(1:1) Cl2(1:2)
H2S(1:2.6) SO2(1:40)
③ 微溶于水的
O2,O3,C2H2等
④ 难溶于水的
H2,N2,CH4,C2H2,NO,CO等.
(2)液体的溶解性
① 易溶于水或与水互溶的
如:酒精、丙酮、醋酸、硝酸、硫酸.
② 微溶于水的
如:乙酸乙酯等用为香精的低级酯.
③ 难溶于水的
如:液态烃、醚和卤代烃.
(3)固体的水溶性(无机物略)
有机物中羟基和羧基具有亲水性,烃基具有憎水性,烃基越大,则水溶性越差,反而易I溶于有机溶剂中.如:甲酸、乙酸与水互溶,但硬脂酸、油酸分子中因—COOH比例过少反而不溶于水而溶于CCl4,汽油等有机溶剂.苯酚、三溴苯酚、苯甲酸均溶于苯.
(4)从碘、溴、氯的水溶液中萃取卤素的有机溶剂
如:苯、汽油、乙醚、乙酸乙酯、CCl4、CS2等.
(5)白磷、硫易溶于CS2
(6)常见水溶性很大的无机物
如:KOH,NaOH,AgNO3溶解度在常温超过100g(AgNO3超过200g).KNO3在20℃溶解度为31.6g,在100℃溶解度为246g.溶解度随温度变化甚少的物质常见的只有NaCl.
(7)难溶于水和一般溶剂的物质
① 原子晶体(与溶剂不相似).如:C,Si,SiO2,SiC等.其中,少量碳溶于熔化的铁.
② 有机高分子:纤维素仅溶于冷浓H2SO4、铜氨溶液和CS2跟NaOH作用后的溶液中,已热固化的酚醛树脂不溶于水或一般溶剂.
5.常见的有毒物质
(1)剧毒物质
白磷、偏磷酸、氰化氢(HCN)及氰化物(NaCN,KCN等)砒霜(As2O3)、硝基苯等.
CO(与血红蛋白结合),Cl2,Br2(气),F2(气),HF,氢氟酸等.
(2)毒性物质
NO(与血红蛋白结合),NO2,CH3OH,H2S.
苯酚、甲醛、二氧化硫、重铬酸盐、汞盐、可溶性钡盐、可溶性铅盐、可溶性铜盐等.
这些物质的毒性,主要是使蛋白质变性,其中常见的无机盐如:HgCl2,BaCl2,Pb(CHCOO)2;铜盐也使蛋白质凝固变性,但毒性较小,此外铍化合物也有相当的毒性.
钦酒过多也有一定毒性.汞蒸气毒性严重.有些塑料如聚氯乙烯制品(含增塑剂)不宜盛放食品等.1年前查看全部
- 紫黑色固体.紫色溶液.棕黄色溶液.橙色溶液.黄绿色气体.臭鸡蛋气味.
紫黑色固体.紫色溶液.棕黄色溶液.橙色溶液.黄绿色气体.臭鸡蛋气味.
白色沉淀 lhm_0201年前4
lhm_0201年前4 -
 ll琳 共回答了23个问题
ll琳 共回答了23个问题 |采纳率91.3%高锰酸钾固体;高锰酸钾溶液;三价铁盐溶液;溴水;氯气;硫化氢气体1年前查看全部
- 有A、B、C、D四种元素,已知A、B单质在一定条件下,反应可生成有臭鸡蛋气味的气体X,X德溶液长期露置
有A、B、C、D四种元素,已知A、B单质在一定条件下,反应可生成有臭鸡蛋气味的气体X,X德溶液长期露置
有A、B、C、D四种元素,已知A、B单质在一定条件下,反应可生成有臭鸡蛋气味的气体X,X德水溶液长期露置在空气中又有B单质析出.C和A可形成另一化合物Y,C+和D-德电子层结构相同,且D与A原子的电子层数相同.求ABCD
我也做得和一楼一样德呃= =
也是在一个电子层上面纠结住乐、、
看样子应该是题目错乐叭(我么打错哦~题目就是这样德。) robby_liyi1年前3
robby_liyi1年前3 -
 zhangrong12 共回答了17个问题
zhangrong12 共回答了17个问题 |采纳率94.1%把“X德水溶液长期露置在空气中又有B单质析出”中的B改成A,
题目肯定是这样的,
那么A为硫,B为H,C为K,D为Cl,Y为K2S1年前查看全部
- 某强酸A和食盐固体混合物加热生成一气体B,将B溶于水制成较浓溶液后和黑色固体C反应制得有臭鸡蛋气味的气体D和淡绿色溶液,
某强酸A和食盐固体混合物加热生成一气体B,将B溶于水制成较浓溶液后和黑色固体C反应制得有臭鸡蛋气味的气体D和淡绿色溶液,D气体和E气体在常温下反应得淡黄色粉末和水,过量E气体通入NaOH溶液中的F溶液,将A和B溶液混合反应又可得E气体.试回答:(1)试写出A至F的化学式A—B—C—D—E—F—(2)写出过量E和NaOH溶液反应的离子方程式——
写出A和F反应的离子方程式—— 某君张某某KI小某1年前1
某君张某某KI小某1年前1 -
 荒於嬉 共回答了14个问题
荒於嬉 共回答了14个问题 |采纳率100%D是硫化氢,淡绿色溶液是铜离子特征,C是硫化铜,B是氯化氢,E是氧气或二氧化硫,又氧气和氢氧化钠不反应,所以E是二氧化硫,F是亚硫酸氢钠,A是硫酸
AH2SO4 B HCL C CUS D H2S E SO2 F NAHSO3
SO2+OH- = HSO3-
H+ +HSO3- = H2O+SO2(气体加箭头符号)1年前查看全部
- 急求制备硫酸亚铁铵的问题.1)在制备硫酸亚铁时,为什么会有臭鸡蛋味?2)在Fe和H2SO4反应过程中,为什么要把温度控制
急求制备硫酸亚铁铵的问题.
1)在制备硫酸亚铁时,为什么会有臭鸡蛋味?
2)在Fe和H2SO4反应过程中,为什么要把温度控制在50℃-60℃之间?
3)在硫酸亚铁的制备过程中,为什么要趁热过滤,并用少量热水洗涤滤纸?如果不趁热过滤会有什么后果? micky131年前1
micky131年前1 -
 鲜橙多vc 共回答了20个问题
鲜橙多vc 共回答了20个问题 |采纳率95%1.可能铁当中有杂质S,与H2SO4反应时生成H2S气体,臭鸡蛋气味
2.反应的最佳温度,而且Fe2+不易发生水解反应,不会生成Fe(OH)2沉淀,也不会被氧化成Fe(OH)31年前查看全部
- 常温常压下,硫化氢H2S是一种没有颜色,具有臭鸡蛋气味的有毒气体
常温常压下,硫化氢H2S是一种没有颜色,具有臭鸡蛋气味的有毒气体
“具有臭鸡蛋气味”是化学性质还是物理性质? 黑石深渊1年前2
黑石深渊1年前2 -
 songrui528 共回答了17个问题
songrui528 共回答了17个问题 |采纳率88.2%物理性质1年前查看全部
- A、B可以相互转换,B在沸水中生成C,C在空气中被氧化生成D,D有臭鸡蛋味,问ABCD是什么?
A、B可以相互转换,B在沸水中生成C,C在空气中被氧化生成D,D有臭鸡蛋味,问ABCD是什么?
速度回答吧!~
 womens1111年前1
womens1111年前1 -
 yuuboo 共回答了11个问题
yuuboo 共回答了11个问题 |采纳率72.7%如果不是脑筋急转弯的话
在高中课本中臭鸡单气味的气体是臭氧和硫化氢
C是氧气
D是臭氧
但是推不出来B然后是A
如果D是硫化氢,不可能是氧化成的
所以这道题不是出错了就是蒙人的脑筋急转弯1年前查看全部
- 化学题求A、B、C、D四种物质求A、B、C、D四种物质A能生成B,B和C能相互转化,B能通过氧化反应生成D,D有臭鸡蛋味
 gyaa1年前1
gyaa1年前1 -
 4703309 共回答了15个问题
4703309 共回答了15个问题 |采纳率93.3%A鸡,B生鸡蛋,C熟鸡蛋.D臭鸡蛋.
.
D.H2S1年前查看全部
- 求一个高二方程式在加热了的FeS上滴加HCl,生成具有臭鸡蛋气味的气体,求方程式……
 左佳韵1年前1
左佳韵1年前1 -
 3h53 共回答了12个问题
3h53 共回答了12个问题 |采纳率100%FeS+2HCl=H2S+FeCl21年前查看全部
- 有臭鸡蛋气味的气体A和B能相互转换,B在沸水中可以生成C,C在空气中氧化成D,D有种臭鸡蛋的味道.请问:A,B,C,D各
有臭鸡蛋气味的气体
A和B能相互转换,B在沸水中可以生成C,C在空气中氧化成D,D有种臭鸡蛋的味道.请问:A,B,C,D各是什么东东? 千里千寻0o1年前4
千里千寻0o1年前4 -
 茜茜宫主 共回答了20个问题
茜茜宫主 共回答了20个问题 |采纳率85%A鸡、B鸡蛋、C熟鸡蛋、D臭鸡蛋1年前查看全部
- 鸡蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体(H2S),硫化氢气体是一种大气污染物,吸入量过多会使人中毒身亡,它在
鸡蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体(H2S),硫化氢气体是一种大气污染物,吸入量过多会使人中毒身亡,它在空气中点燃完全燃烧时,生成二氧化碳和水,把硫化氢气体通入浓硫酸中,发生的反应为H2S+H2SO4(浓)═SO2+X↓+2H2O根据以上信息回答问题:
(1)硫化氢的物理性质有______
(2)硫化氢的化学性质有______.
(3)硫化氢与浓硫酸反应时,生成物中X的化学式是______
(4)若尾气中含有硫化氢气体,用浓硫酸来吸收行吗?为什么?
答:______. jiakechong1231年前1
jiakechong1231年前1 -
 十丈红尘 共回答了23个问题
十丈红尘 共回答了23个问题 |采纳率91.3%解题思路:根据题干提供的信息进行分析即可得出硫化氢的物理性质和化学性质,判断物质的化学式可以依据质量守恒定律,化学反应前后元素的种类和原子的个数不变进行.(1)根据题干叙述可知,硫化氢是无色、有臭鸡蛋气味的气体,故填:无色、有臭鸡蛋气味的气体;
(2)根据题干叙述可知,硫化氢是有毒、能燃烧、能和浓硫酸反应的气体,故填:毒性、可燃性、能与浓硫酸反应;
(3)根据质量守恒定律,化学反应前后元素的种类和原子的个数不变,反应前含有4个H原子,2个S原子和4个O原子,反应后已有1个S原子,4个H原子和4个O原子,故X为S,故填:S;
(4)硫化氢能和浓硫酸反应生成二氧化硫气体,所以不能用浓硫酸干燥硫化氢气体,故填:不可以,因为硫化氢与浓硫酸反应后生成二氧化硫污染空气.点评:
本题考点: 化学性质与物理性质的差别及应用;空气的污染及其危害;有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 本题主要考查了物质的物理性质和化学性质、根据质量守恒定律推断物质的化学式等,完成此题,可以依据题干的叙述,从中抽取有用的信息.1年前查看全部
- 阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水.在空气中点燃硫化氢气体有二氧化
阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水.在空气中点燃硫化氢气体有二氧化硫和水生成.硫化氢的实验室制法是用块状硫化亚铁和液体状稀硫酸反应,则属硫化氢的化学性质的是 [ ]A.无色
B.有臭鸡蛋气味
C.比空气重
D.能燃烧 tangelo1年前1
tangelo1年前1 -
 zwking_1981 共回答了21个问题
zwking_1981 共回答了21个问题 |采纳率85.7%D1年前查看全部
- 在通常情况下,硫化氢(H2S)是一种没有颜色、具有臭鸡蛋气味的有毒气体,比空气重,能溶于水.实验室用块状固体硫化亚铁(F
在通常情况下,硫化氢(H2S)是一种没有颜色、具有臭鸡蛋气味的有毒气体,比空气重,能溶于水.实验室用块状固体硫化亚铁(FeS)跟稀硫酸通过复分解反应来制取H2S气体,请回答:
(1)实验室制H2S气体的发生装置可选用______(填“制H2”或“制O2”)的气体发生装置;
(2)收集H2S气体应选用______法;
(3)硫化亚铁与稀硫酸反应的化学方程式为______;
(4)已知H2S水溶液的pH值小于7,向其中加入紫色石蕊试液,溶液呈______色;
(5)实验室制取H2S气体时,为防止污染和避免中毒,多余的硫化氢应该用______吸收. zzlwj1年前1
zzlwj1年前1 -
 95585 共回答了20个问题
95585 共回答了20个问题 |采纳率95%解题思路:制取装置包括加热和不需加热两种,实验室用块状固体硫化亚铁(FeS)跟稀硫酸反应制取的,因此不需要加热;实验室是用锌粒和稀硫酸在常温下反应制氢气的,因此也不需要加热;如果用双氧水和二氧化锰制氧气就不需要加热;收集H2S气体应选用向上排空气法收集,因为硫化氢气体比空气重,能溶于水;硫化亚铁与稀硫酸反应生成硫酸亚铁和硫化氢气体;H2S水溶液的pH值小于7,因此呈酸性,向其中加入紫色石蕊试液,溶液呈红色;硫化氢(H2S)是一种没有颜色、具有臭鸡蛋气味的有毒气体,为防止污染和避免中毒,多余的硫化氢应该用氢氧化钠溶液吸收.(1)实验室用块状固体硫化亚铁(FeS)跟稀硫酸反应制取的,因此不需要加热;实验室是用锌粒和稀硫酸在常温下反应制氢气的,因此也不需要加热;如果用双氧水和二氧化锰制氧气就不需要加热;故答案为:制H2或制O2
(2)收集H2S气体应选用向上排空气法收集,因为硫化氢气体比空气重,能溶于水,故答案为:向上排空气
(3)硫化亚铁与稀硫酸反应生成硫酸亚铁和硫化氢气体,故答案为:FeS+H2SO4=FeSO4+H2S↑
(4)H2S水溶液的pH值小于7,因此呈酸性,向其中加入紫色石蕊试液,溶液呈红色,故答案为:红
(5)硫化氢(H2S)是一种没有颜色、具有臭鸡蛋气味的有毒气体,为防止污染和避免中毒,多余的硫化氢应该用氢氧化钠溶液吸收,故答案为:NaOH溶液点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;酸碱指示剂及其性质;溶液的酸碱性与pH值的关系;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和溶液的酸碱性等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.1年前查看全部
- 鸡蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体(H 2 S),硫化氢气体是一种大气污染物,吸入量过多会使人中毒身亡,
鸡蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体(H 2 S),硫化氢气体是一种大气污染物,吸入量过多会使人中毒身亡,它在空气中点燃完全燃烧时,生成二氧化碳和水,把硫化氢气体通入浓硫酸中,发生的反应为H 2 S+H 2 SO 4 (浓)═SO 2 +X↓+2H 2 O根据以上信息回答问题:
(1)硫化氢的物理性质有______
(2)硫化氢的化学性质有______.
(3)硫化氢与浓硫酸反应时,生成物中X的化学式是______
(4)若尾气中含有硫化氢气体,用浓硫酸来吸收行吗?为什么?
答:______. pagon1年前1
pagon1年前1 -
 stgeorge 共回答了17个问题
stgeorge 共回答了17个问题 |采纳率82.4%(1)根据题干叙述可知,硫化氢是无色、有臭鸡蛋气味的气体,故填:无色、有臭鸡蛋气味的气体;
(2)根据题干叙述可知,硫化氢是有毒、能燃烧、能和浓硫酸反应的气体,故填:毒性、可燃性、能与浓硫酸反应;
(3)根据质量守恒定律,化学反应前后元素的种类和原子的个数不变,反应前含有4个H原子,2个S原子和4个O原子,反应后已有1个S原子,4个H原子和4个O原子,故X为S,故填:S;
(4)硫化氢能和浓硫酸反应生成二氧化硫气体,所以不能用浓硫酸干燥硫化氢气体,故填:不可以,因为硫化氢与浓硫酸反应后生成二氧化硫污染空气.1年前查看全部
- 1和2可以相互转化,2在沸水中生成3,3在空气中氧化生成4,4有臭鸡蛋气味,问1234各是什么?
1和2可以相互转化,2在沸水中生成3,3在空气中氧化生成4,4有臭鸡蛋气味,问1234各是什么?
在线等
不是脑筋急转弯啊,要化学答案不对,3到4是被还原了,不是被氧化了 怎么当了兵1年前1
怎么当了兵1年前1 -
 孙韩旭 共回答了22个问题
孙韩旭 共回答了22个问题 |采纳率104.5%1是母鸡,2是生鸡蛋,3是熟鸡蛋,4是臭鸡蛋1年前查看全部
- A由B转化而来,B在开水中生成C,C在空气中氧化成D,D有臭鸡蛋的气味,请问ABCD各是什么?
 205watin1年前1
205watin1年前1 -
 djxiaoyun 共回答了23个问题
djxiaoyun 共回答了23个问题 |采纳率82.6%a鸡
b鸡蛋
c熟鸡蛋
d臭鸡蛋
这不是个化学题,是幽默故事1年前查看全部
- 1和2可以相互转换,2在沸水中生成3,3在空气中氧化成4,4有臭鸡蛋气味
1和2可以相互转换,2在沸水中生成3,3在空气中氧化成4,4有臭鸡蛋气味
;问1,2,3 ,4 各是什么? 潇洒-人生1年前1
潇洒-人生1年前1 -
 支为 共回答了19个问题
支为 共回答了19个问题 |采纳率100%把4作为突破口就成了
很简单的题
建议你自己做1年前查看全部
- 蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体(H2S).硫化氢气体是一种大气污染物,它在空气中点燃时,生成二氧化硫和
蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体(H2S).硫化氢气体是一种大气污染物,它在空气中点燃时,生成二氧化硫和水,把硫化氢气体通人浓硫酸中,发生的反应为:H2S+H2SO4(浓)=SO2+X↓+2H2O.
(1)上述内容中,属于硫化氢物理性质的是______.
(2)硫化氢在空气中完全燃烧的化学方程式是:2H2S+3O2
2SO2+2H2O点燃 .2H2S+3O2.其中硫化氢是______(填“‘氧化剂”或“还原剂”).
2SO2+2H2O点燃 .
(3)硫化氢与浓硫酸反应时,生成物中X的化学式是______. 冬无名1年前1
冬无名1年前1 -
 飞言海声 共回答了27个问题
飞言海声 共回答了27个问题 |采纳率88.9%解题思路:(1)不需要通过化学变化表现出来的性质属于物质的物理性质;
(2)根据质量守恒定律可以书写反应的化学方程式;反应中得氧的物质是还原剂;
(3)根据质量守恒定律可以判断物质的化学式.(1)硫化氢的颜色、气味等方面的性质不需要通过化学变化表现出来,属于物理性质.
故答案为:无色、有臭鸡蛋气味的气体;
(2)硫化氢在空气中完全燃烧的化学方程式为:2H2S+3O2
点燃
.
2SO2+2H2O;该反应中硫化氢得氧,是还原剂;
故答案为:2H2S+3O2
点燃
.
2SO2+2H2O;还原剂;
(3)由H2S+H2SO4(浓)═SO2+X↓+2H2O可知,反应物中有4个氢原子、2个硫原子、4个氧原子,生成物除X外,有4个氢原子、1个硫原子、4个氧原子,根据质量守恒定律,每个X中含有1个硫原子,是硫,化学式是S.
故答案为:S.点评:
本题考点: 化学性质与物理性质的差别及应用;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查物质的性质和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.1年前查看全部
- (2013•海淀区二模)硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中.在人体的
(2013•海淀区二模)硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中.在人体的很多生理过程中也起着重要作用.
(1)某化学小组设计了制取H2S并验证其性质的实验,如下图所示.A中是CuSO4溶液,B中放有湿润的蓝色石蕊试纸,C中是FeCl3溶液.资料:①H2S可溶于水(约1:2),其水溶液为二元弱酸.
②H2S可与许多金属离子反应生成沉淀.
③H2S在空气中燃烧,火焰呈淡蓝色.
回答下列问题:
①A中有黑色沉淀(CuS)产生,A中发生反应的化学方程式为______.
②B中的现象是______.
③C中只有浅黄色沉淀产生,且溶液变浅绿色.则C中发生反应的离子方程式为______.
④D中盛放的试剂可以是______(填标号).
a.水b.盐酸c.NaCl溶液d.NaOH溶液
(2)为进一步探究-2价硫的化合物与+4价硫的化合物反应条件,小组同学又设计了下列实验.
已知:电离平衡常数:H2SKa1=1.3×10-7;Ka2=7.1×10-15实验操作 实验现象 实验1 将等浓度的Na2S和Na2SO3溶液按体积比2:1混合 无明显现象 实验2 将H2S通入Na2SO3溶液中 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 实验3 将SO2通入Na2S溶液中 有浅黄色沉淀产生
H2SO3Ka1=1.7×10-2;Ka2=5.6×10-8
①根据上述实验,可以得出结论:在______条件下,+4价硫的化合物可以氧化-2价硫的化合物.
②将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是______(填序号).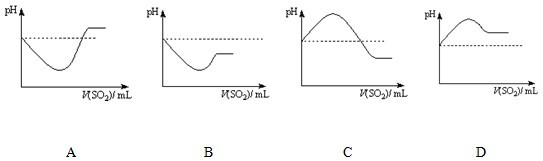
(3)文献记载,常温下H2S可与Ag发生置换反应生成H2.现将H2S气体通过装有银粉的玻璃管,请设计简单实验,通过检验反应产物证明H2S与Ag发生了置换反应______. cc11091年前1
cc11091年前1 -
 阿露儿 共回答了15个问题
阿露儿 共回答了15个问题 |采纳率86.7%解题思路:(1)①CuSO4与H2S反应生成CuS沉淀;
②H2S水溶液呈酸性;
③FeCl3具有氧化性,与H2S发生氧化还原反应生成S和Fe2+;
④H2S可与碱反应.
(2)①H2S与SO2发生氧化还原反应生成S;
②根据H2SO3 酸性比H2S强判断;
(3)如与Ag发生置换反应生成H2,可用点燃的方法检验.(1)①CuSO4与H2S反应生成CuS沉淀,反应的方程式为H2S+CuSO4=CuS↓+H2SO4,故答案为:H2S+CuSO4=CuS↓+H2SO4;
②H2S水溶液呈酸性,可使湿润的蓝色石蕊试纸变红,故答案为:蓝色石蕊试纸变红;
③FeCl3具有氧化性,与H2S发生氧化还原反应生成S和Fe2+,反应的离子方程式为H2S+2Fe3+=S↓+2H++2Fe2+,故答案为:H2S+2Fe3+=S↓+2H++2Fe2+;
④H2S有毒,不能排放到空气中,可与碱反应,故答案为:d;
(2)①由实验现象可知反应应下酸性条件下发生氧化还原反应生成S,故答案为:酸性(或酸性较强);
②H2SO3 酸性比H2S强,通入过量的SO2,溶液酸性更强,pH更小,故答案为:C;
(3)如与Ag发生置换反应生成H2,可用点燃的方法检验,但应先将H2S除去,方法是将反应后的气体通入足量氢氧化钠溶液中(或硫酸铜溶液或氯化铁溶液等),除去未反应的H2S后,点燃,若观察到火焰呈淡蓝色,说明有H2生成,从而证明H2S与Ag发生了置换反应,
故答案为:将反应后的气体通入足量氢氧化钠溶液中(或硫酸铜溶液或氯化铁溶液等),除去未反应的H2S后,点燃,若观察到火焰呈淡蓝色,说明有H2生成,从而证明H2S与Ag发生了置换反应.点评:
本题考点: 制备实验方案的设计;含硫物质的性质及综合应用.
考点点评: 本题考查实验制备方案的设计,侧重于硫化氢的性质的设计,题目难度不大,注意把握实验原理和实验的基本操作方法的学习.1年前查看全部
大家在问
- 1臭鸡蛋气味的气体A与B可以相互转化,B在沸水中生成C,C在空气中氧化成D,D有臭鸡蛋气味.问ABCD 个是什么
- 2完全平方公式运用.1.已知x-y=1,x^2+y^2=25,求xy的值.2.已知(x+y)^2=1,(x-y)^2=49
- 3暮江吟(白居易)赏析 第一人称写
- 4古诗暮江吟的诗句意思
- 5暮江吟古诗意思
- 6《暮江吟》的200字古诗赏析.
- 7小莉绕着一个长方形花坛走一周,走了980步.如果她的平均步长是0.55米,花坛的宽是124.5米,这个花坛的长是多少米?
- 8wear和dress的区别
- 9我困了,用英文怎么说 口语化一点
- 105000公顷等于多少平方千米
- 111500亩等于多少平方千米
- 12书非借不能读翻译成英文怎么说
- 13英语里可数名词与不可数名词是什么意思
- 14赏析 暮江吟
- 151 4 13 40 121有什么规律?写出后面两个数


