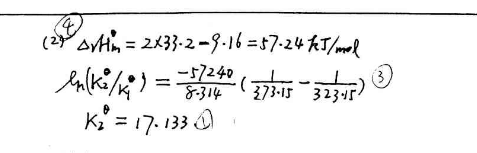在将气抽空的过程中,你听到的铃声的 (选填"音调","响度"或"音色")逐渐减小?直至听不到声音
 liyuqingqing2022-10-04 11:39:541条回答
liyuqingqing2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 扫雪怪兽 共回答了17个问题
扫雪怪兽 共回答了17个问题 |采纳率94.1%- 响度
- 1年前
相关推荐
- 还有4题,你能抽空帮我把过程发过来吗,这是其中一题,其实我都悬赏了,就是没人回答,你先解决这题,谢
 岭南墨客1年前1
岭南墨客1年前1 -
 朱明睿 共回答了18个问题
朱明睿 共回答了18个问题 |采纳率88.9%01年前查看全部
- 在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4=2NO2 ΔH>0
在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4=2NO2 ΔH>0 ,
要增大该反应的K值,可采取的措施有(填序号) D ,若要重新达到平衡时,使[NO2]/[N2O4]值变小,可采取的措施有(填序号) AB .
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
问:为什么A和B可以使[NO2]/[N2O4]值变小(重点是为什么选B?)
B中加入的NO2,平衡移动只是减小NO2,到底体系的NO2还是增加了,这样不会令到比值反而变大么? linjiarui1年前3
linjiarui1年前3 -
 xianjinghu 共回答了21个问题
xianjinghu 共回答了21个问题 |采纳率81%关键是 固定容积的密闭容器 这个前提!
假设未作任何改变时,有体积为50%的是NO2,另50%是N2O4,
现在通入NO2,会增加压强,通入的一部分NO2会反应生成N2O4,继续通入NO2,会在一定压强下,所有的NO2都反应生成N2O4,NO2不复存在!
所以你可以理解,继续通入NO2,是朝着NO2消失的状态发展,所以不用计算,就可以得出结论B.1年前查看全部
- 英语翻译在这个令人激动的时刻,感谢大家百忙之中抽空来参加我们的婚礼,带来了喜悦和快乐,也带来了真挚的祝福.此时此刻我们再
英语翻译
在这个令人激动的时刻,感谢大家百忙之中抽空来参加我们的婚礼,带来了喜悦和快乐,也带来了真挚的祝福.此时此刻我们再一次真诚地感谢父母的含辛茹苦,感谢领导的关心厚爱,感谢亲友的真诚祝福,也祝愿各位嘉宾心想事成,万事如意, 西西丁1年前2
西西丁1年前2 -
 beforelife 共回答了17个问题
beforelife 共回答了17个问题 |采纳率94.1%诸位 :日中临安,此为幸事之日,百万心激,由心多谢诸位临来吾之婚宴,给(ji)幸庆之悦,给心诚祝福,时刻谢之为娘爷至心,谢之领者至爱,谢之友人之福,幸祝诸位来者心想事成,万事如意,心激由谢!(希望你的婚礼能成功哦,祝你和你的妻子幸福哦)1年前查看全部
- 在温度为298K时,将0.10mol无色的N2O4气体放入1L抽空的密闭容器中,出现红棕色,直至建立N2O4(g)⇔2N
 在温度为298K时,将0.10mol无色的N2O4气体放入1L抽空的密闭容器中,出现红棕色,直至建立N2O4(g)⇔2NO2(g)的平衡.下图表示测定N2O4的浓度与时间关系的曲线(纵坐标为N2O4的浓度,横坐标为时间).
在温度为298K时,将0.10mol无色的N2O4气体放入1L抽空的密闭容器中,出现红棕色,直至建立N2O4(g)⇔2NO2(g)的平衡.下图表示测定N2O4的浓度与时间关系的曲线(纵坐标为N2O4的浓度,横坐标为时间).
(1)计算在2s至4s时间内,NO2的平均生成速率为______.
(2)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到同样的平衡状态,二氧化氮的起始浓度是______mol•L-1.
(3)在温度为298K时,达到平衡时四氧化二氮的转化率α1等于______.化学平衡常数为______.
(4)若在7s时向该密闭容器中再充入0.10mol N2O4气体,此时平衡向______方向移动(填“正”或“逆”);再次达平衡时,总计0.20mol N2O4的转化率为α2,正确的是______
A.α2<α1B.α2>α1C.α2=α1D.无法判断.
(5)下表是不同温度下测定的该反应的化学平衡常数.
据此判断该反应正反应是______反应(填“吸热”或“放热”)T/K 310 320 K值 0.38 0.42
(6)若其他条件不变,反应在398K条件下进行并达到平衡,此温度下N2O4的浓度随时间变化的曲线(以298K条件下进行并达到平衡的曲线作为参照)正确的是______
 yixiaotian1年前1
yixiaotian1年前1 -
 花间蝶 共回答了24个问题
花间蝶 共回答了24个问题 |采纳率95.8%解题思路:(1)根据v=[△c/△t]计算反应速率;
(2)根据等效平衡的思想可以判断;
(3)根据三段式可以计算转化率和平衡常数;
(4)根据浓度和压强对平衡的影响可以作判断;
(5)根据温度对平衡的影响可以判断;
(6)根据温度对平衡移动的影响可以判断.(1)在2s至4s时间内,NO2的平均生成速率v=[△c/△t]=
(0.07mol•L−1−0.05mol•L−1)×2
2s=0.02mol•L-1•S-1,故答案为:0.02mol•L-1•S-1;
(2)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到同样的平衡状态,即与原平衡为等效平衡,根据等效平衡的特点,充入的二氧化氮气体折算成四氧化二氮,与原浓度一样,所以折算为二氧化氮作为起始物时,其浓度0.20mol•L-1,故答案为:0.20;
(3)利用三段式
N2O4 2NO2
2NO2
起始浓度(mol•L-1)0.1 0
转化浓度(mol•L-1) 0.06 0.12
平衡浓度(mol•L-1) 0.04 0.12
∴四氧化二氮的转化率α1=
0.06mol•L−1
0.1mol•L−1×100%=60%,
化学平衡常数为
(0.12mol•L−1)2
0.04mol•L−1=0.36mol•L-1
故答案为:60%;0.36;
(4)根据平衡移动原理,增加反应物浓度平衡正向移动;在容积不变的条件下,再充入0.10mol N2O4气体,达到平衡时体系的压强比原平衡体系压强大,N2O4的转化率下降工,故α2<α1,故答案为:正;A;
(5)由图表可知温度升高K值增大,平衡正向移动,所以正反应为吸热反应,故答案为:吸;
(6)若其他条件不变,反应在398K条件下进行并达到平衡,与原平衡相比,平衡正向移动,N2O4气体的浓度下降,故C图符合要求,故答案为:C.点评:
本题考点: 物质的量或浓度随时间的变化曲线;化学平衡的影响因素;化学平衡的计算.
考点点评: 本题考查了化学平衡图象、转化率计算、平衡常数的计算、等效平衡的思想等知识,中等难度,在解题时要注意准确运用图表中信息解答相关问题.1年前查看全部
- 形容自己在百忙之中抽空来参加某事的词语
 不_知道1年前1
不_知道1年前1 -
 阳光漫漫 共回答了22个问题
阳光漫漫 共回答了22个问题 |采纳率95.5%忙里偷闲
拔冗莅临:是指推开繁杂事务,抽出时间前来参加的意思.拔冗光临1年前查看全部
- 英语翻译亲爱的,我看到了你的信.你在日本工作一定很忙,还要抽空回信,很多事都要去做,平常要好好照顾自己,保重身体.我会按
英语翻译
亲爱的,我看到了你的信.你在日本工作一定很忙,还要抽空回信,很多事都要去做,平常要好好照顾自己,保重身体.我会按照你告诉我的去努力做的 今生混沌来生再见1年前6
今生混沌来生再见1年前6 -
 风轻轻舞 共回答了19个问题
风轻轻舞 共回答了19个问题 |采纳率89.5%Dear,
Well received your mail, you must be busy in Japan and have to reply the mail in your spare time. Lots of things you need to do,so you also need to take care of yourself as well as your body. I will follow your words to do with my best.1年前查看全部
- 经典物理试验:光在真空中的变化在一个密闭的透明体中放入一光源.把这个透明体逐渐抽空至真空.观查光源的变化.如果技术上能达
经典物理试验:光在真空中的变化
在一个密闭的透明体中放入一光源.把这个透明体逐渐抽空至真空.观查光源的变化.如果技术上能达到极高真空或物理学上定义真空.那么光亮将逐渐减弱,直至看不见光源.这就是人造黑洞.
有谁能帮我做这个试验?
仁者见仁,智者见智!无知者,请自知之明! gjn20081年前1
gjn20081年前1 -
 hixibao 共回答了11个问题
hixibao 共回答了11个问题 |采纳率90.9%声学实验还有可能,如放进个闹钟,抽成真空后就听不见了,因为声音无法在真空中传播.
但光学实验不行.这个实验也好做,但你观测不到任何效果,因为光可以在真空中传播!像太阳光就是穿过太阳与地球间的真空环境到达地球.
事实上光在真空环境中传播的最好了,在空气中反而会减慢、散射.
另外,人们常说的“黑洞”确实指的是另外一回事,是把很大的质量压缩到很小的体积内使其引力大到光速也无法逃出.1年前查看全部
- 在100℃时,将0.1mol的四氧化二氮气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下数据:
在100℃时,将0.1mol的四氧化二氮气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下数据:
(1)该反应的化学方程式为______,达到平衡时四氧化二氮的转化率为______%,表中C2______C3______a______b(选填“>”、“<”、“═”).浓度时间(S) 0 20 40 60 80 100 C(N2O4)/mol•L-1 0.1 c1 0.05 C3 a b C(NO2)/mol•L-1 0 0.06 C2 0.12 0.12 0.12
(2)20s时四氧化二氮的浓度C1=______mol•l-1,在0s~20s内四氧化二氮的平均反应速率为______mol•(L•s)-1. abui1年前1
abui1年前1 -
 niy004 共回答了12个问题
niy004 共回答了12个问题 |采纳率91.7%解题思路:(1)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;60s后反应达平衡,反应混合物各组分的浓度不变;
(2)由△c(NO2),根据方程式计算△c(N2O4),20s的四氧化二氮的浓度=起始浓度-△c(N2O4);根据v=[△c/△t]计算v(N2O4).(1)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,反应的N2O4浓度为0.06mol/L,反应的化学方程式为:N2O4⇌2 NO2,
N2O4⇌2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为[0.06mol/L/0.1mol/L]×100%=60%;
60s后反应达平衡,反应混合物各组分的浓度不变,所以C3=a=b=0.04mol/L,40s时:
N2O4⇌2 NO2,
0.1mol/L 0
0.05mol/L 0.1mol/L
0.05mol/L C2=0.1mol/L
C2=0.1mol/L>C3=a=b=0.04mol/L;
故答案为:N2O4=2NO2;60;>;=;=;
(2)由表可知,20s时,c(NO2 )=0.060mol/L,所以
N2O4⇌2 NO2,
浓度变化:0.03mol/L 0.060mol/L
所以20s的四氧化二氮的浓度c1=0.1mol/L-0.03mol/L=0.07mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4)=[0.03mol/L/20s]=0.0015mol•(L•s)-1.
故答案为:0.07mol/L;0.0015mol•(L•s)-1.点评:
本题考点: 化学平衡的计算.
考点点评: 本题考查化学平衡的有关计算、等效平衡等,难度中等,注意基础知识的积累掌握.1年前查看全部
- 假如从地球的北极到南极打通一条隧道,然后把隧道里空气抽空,然后分别从南极和北极洞口向隧道内扔一同质量的石头或金属,初速度
假如从地球的北极到南极打通一条隧道,然后把隧道里空气抽空,然后分别从南极和北极洞口向隧道内扔一同质量的石头或金属,初速度为零,那么这两块石头在隧道内将做什么运动,能否到达对面洞口?或到洞外?假如向隧道内注水,能否定把隧道注满?水是否会溢出?宇宙种又是存在这样的中心空间隧道?
 poly1年前1
poly1年前1 -
 youyoujie 共回答了18个问题
youyoujie 共回答了18个问题 |采纳率83.3%.岩浆已经把隧道注满了,如果那时候地球还没毁灭的话.就算你真的扔下去了,到达地心的时候也变成岩浆了.注水?好吧,蒸发没了.1年前查看全部
- 尤今的 记在心上 中那位摊主,尽管忙得不可开交,还是抽空抬起头来,温和淡定地说“你刚才叫的是豆
尤今的 记在心上 中那位摊主,尽管忙得不可开交,还是抽空抬起头来,温和淡定地说“你刚才叫的是豆
腐鱼片汤,我已记在心上了”说明什么 snowingyang1年前1
snowingyang1年前1 -
 艾泽拉斯之泪 共回答了16个问题
艾泽拉斯之泪 共回答了16个问题 |采纳率93.8%说明,每一位顾客在他心目中都有着同样的重量1年前查看全部
- 在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到
在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s)
C(mol/L)
0
20
40
60
80
100
C(N2O4)
0.20
a
0.10
c
d
e
C(NO2)
0.00
0.12
b
0.22
0.22
0.22
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
(1)该反应的化学方程式为 ,表中b c(填“”).
(2)20s时,N2O4的的浓度为 mol/L,0~20s内N2O4的平均反应速率为 .
(3)该反应的平衡常数表达式K= ,在80℃时该反应的平衡常数K值为 (保留2位小数).
21(12分)在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s)
C(mol/L)x090x0920x0940x0960x0980x09100
C(N2O4)x090.20x09ax090.10x09cx09dx09e
C(NO2)x090.00x090.12x09bx090.22x090.22x090.22
反应进行至100s后,将反应混合物的温度降低,发现气体的颜色变浅。 折翼smile1年前1
折翼smile1年前1 -
 j100200bbb 共回答了16个问题
j100200bbb 共回答了16个问题 |采纳率87.5%N2O4=2NO2 因为是在已抽空的固定容积的密闭容器内,所以就没有氧气什么的了.即开始的时侯只有N2O4,而由数据可得出实验进行一段时间后有NO2生成.再由化学反应式的平衡原理可得出此化学式.
b>c 由数据可知,随着时间的增加N2O4逐渐减少,而NO2逐渐增多.而且c0.12,由此可得出:b>c1年前查看全部
- 英语翻译您好,感谢你百忙中抽空回复我的邮件.我8月14号购买的订单#100150029至到今日还没发货,现在已经半个月了
英语翻译
您好,感谢你百忙中抽空回复我的邮件.我8月14号购买的订单#100150029至到今日还没发货,现在已经半个月了,我非常需要我的订单.我购买订单的时候以为8月发货时确切的,.希望你明白漫无目的的等待是非常痛苦的,请你给我一个大致的发货时间,让我知道自己大概什么时候能收到货,
更正一个错别字:我购买订单的时候以为8月发货是确切的 yjeric1年前4
yjeric1年前4 -
 春夜喜雨_ 共回答了19个问题
春夜喜雨_ 共回答了19个问题 |采纳率94.7%Hello,thank you for taking the time to reply to my mail I purchased on August 14 Order # 100150029 until today has not shipped two weeks now,and I need my order when I buy ordersthought the exact ship...1年前查看全部
- 语文高考作文 很重要去年,一档《爸爸,我们去哪儿?》的电视真人秀节目,触动了繁忙中的家长:除了关注孩子的学业,也应抽空去
语文高考作文 很重要
去年,一档《爸爸,我们去哪儿?》的电视真人秀节目,触动了繁忙中的家长:除了关注孩子的学业,也应抽空去关注孩子们的成长;思考孩子的教育问题、思考孩子孩童时期的性格的塑造和培养将影响孩子的一生。让家长在各方面条件允许的情况下,带他们远离城市的喧嚣体验乡间田野中的乐趣,丰富书本上学不到的知识和感受,让孩子们生活中的娱乐方式不仅仅局限于电脑和手机的高科技,带他们体验最原始,最普通,最容易得到的快乐。
《燕赵晚报》发表了一篇《徒步日记:我陪着儿子走到北京》。讲述了河北省鹿泉市一位38岁的父亲选择陪10岁的儿子徒步到北京的经历。儿子从小跟爷爷奶奶长大,备受娇宠,不喜欢运动,身体越来越胖。怎么培养孩子吃苦耐劳的意志品质,帮孩子运动减肥?一路走来,父亲累倒了,而胖胖的儿子却咬牙坚持,知道照顾父亲了。父亲喜不自禁,把父子每天的徒步情况记录下来,表示今后会多跟孩子做一些有意义的活动。
一
你读后有什么感触?请根据自己的生活经历和切身体验,写一篇文章,可以讲述故事,抒发情感,也可以发表议论,表达见解。
【注意】①角度自选,立意自定,题目自拟。②除诗歌外,文体不限。③不少于800字。④不得抄袭。
 锤宝宝1年前1
锤宝宝1年前1 -
 sky10m 共回答了30个问题
sky10m 共回答了30个问题 |采纳率96.7%可拟题:儿子,我们去哪儿;给未来孩子的一封信;无可替代;看不见的父爱;书本之外;关注被我们忽略的;最幸运的事;我和爸爸的情人节……1年前查看全部
- 在不能抽空真空的情况下怎么证明“声音在真空中不能传播”
 大前门后1年前3
大前门后1年前3 -
 yuzhong830303 共回答了18个问题
yuzhong830303 共回答了18个问题 |采纳率88.9%目的:证明声音能在液体中传播
器材:一根足够长充满水的铁管
步骤:1.一个同学敲击铁管,另一个同学在铁管另一边听
2.听到3次响声(第1次由铁管传播,第2次由水传播,第3次由空气传播)1年前查看全部
- 在100℃时,将0.2mol的N2O4气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析
在100℃时,将0.2mol的N2O4气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析
时间(s)0x0520x0540x0560x0580x05100
C(N2O4)0.10x05ax050.05x05cx05dx05e
C(NO2) 0.00x050.06x05bx050.12x050.12x050.12
20s时,N2O4的的浓度为 mol/L,20s内N2O4的平均反应速率为 . 为爱走qq的我1年前1
为爱走qq的我1年前1 -
 三好vv 共回答了12个问题
三好vv 共回答了12个问题 |采纳率75%根据方程式N2O4=2NO2
20s时候,得到0.06mol/L的NO2,则N2O4就反应掉0.03(系数是2:1).
(1)N2O4的的浓度为0.1-0.03=0.07mol/L
(2)0~20s内N2O4的平均反应速率为0.03/20s=0.0015mol/Ls1年前查看全部
- 《母亲的日历》阅读题!做题新年前夕,母亲总爱抽空去镇上买回一本崭新的A4纸四分之一大小的日历,钉在墙上,随手一翻红红黑黑
《母亲的日历》阅读题!做题
新年前夕,母亲总爱抽空去镇上买回一本崭新的A4纸四分之一大小的日历,钉在墙上,随手一翻红红黑黑的纸张,她欢喜得像个孩子.
其实,母亲不识字,只是认识一些简单的阿拉伯数字.起初,她钟情于日历,引起我好长一段时间的疑惑,一直以为母亲看日历,只是为了记住二十四节气,以便农事耕收,或关注母猪下崽,出栏的时日.
直到去年新年前夕,我偶尔回了一趟家,恰逢母亲买回了新日历,正欢天喜地翻看着,几乎每个月,都有几页被她折叠起不同的图案,甚至有几页,她用糊鞋底的浆糊糊上红布条、白布条……看母亲虔诚幸福地忙碌着,我一时没有打扰她,只是站在一旁,静静地注视着冬阳下的母亲,看她一会儿双掌合十,一会儿满脸微笑……当时我以为母亲在做某种迷信的祷告,心想,老年人冬闲无事,寻找一些心灵的信仰,即使迷信,只要心灵得以慰藉,能带来快乐,我们做晚辈的,就随她而去吧.
一本厚厚的日历被母亲折叠、张贴得像一个待产的孕妇.她突然转身,看到回家的我,自然惊喜不已.看我注视着她手中的日历,母亲有点慌张,躲闪着把日历掖于身后,嗫嚅着说,在家闲着没事,瞎忙活!
母亲的日历还是被我拿到手中,翻到被折叠或糊上布条的页面,我好奇地问她:妈,这些都是什么日子呀?
母亲见我对她折叠过的日历感兴趣,犹豫着,喃喃而语,到时候,你就会知道了!母亲的“卖关子”更撩起我的好奇心,我激将母亲———在家没事搞什么封建迷信活动!母亲一急,马上和我争辩起来……
在争辩中,我了解到那些被母亲折叠、或糊上布条页面的含义———
2月28日、7月14日、8月17日、8月19日,那是弟弟、我、姐姐和哥哥的生日;母亲折叠这些日子,为的是到时候提醒我们为自己做一碗寿面.
元月2日、2月16日、12月18日、12月28日,那是我、弟弟、姐姐、哥哥的结婚纪念日,母亲糊上红布条,只因这些日子都是我们的大喜之日,到时候她会提醒我们在这一天好好庆祝,夫妻要相敬如宾.
6月14日、10月20日,那是祖母和外婆去世的纪念日.母亲糊上白布条,是提醒自己到那一天,到祖坟烧一些纸钱,保佑我们一大家子出行平安.
2月3日、4月5日、6月16日、8月5日、8月22日被母亲折叠成心形,那是孙子、孙女、外孙的生日,母亲折叠这些日子,是要通知我们为自己的妻子好好做一天家务,在母亲的眼里,子女的出生日就是母亲的受难日.
我翻看完所有的日历,竟没有发现母亲为自己的生日和结婚纪念日打上记号,我心隐隐地发痛.母亲把所有的爱都倾注到家人身上,却忽略了自己.
也是因母亲的那本充满母爱的日历,让我记住了家人所有的生日、祖辈的祭日,以及我们兄弟姐妹的结婚纪念日.因而,在新年到来之际,我总是满怀信心迎接新年,因为新的一年里,有那么多值得我们欣喜的日子,这种欣喜不为权利,不为金钱,而是至真亲情的牵挂和关心!我们没有理由不向新年迈出坚实的步伐!
新年的钟声敲响了,我眼前又恍惚起母亲折叠新年日历的身影,止不住拿起案头的一本新日历,学着母亲的虔诚,翻着日历折叠起来.我先折叠起的,是母亲和父亲的生日……
(1) 母亲喜买日历→(母亲)____日历→“我”____日历→“我”学母亲折叠日历
(2)从文中画线的A B两个句子任选一句赏析
A一本厚厚的日历被母亲折叠,张贴得像一个待产的孕妇
B看我注视着她手中的日历,母亲有点慌张,躲闪着把日历掖于身后,嗫嚅着说,在家闲着没事,瞎忙活!
选择___句,___________
(3)简要分析母亲这一人物形象
(4)根据你的理解,说说文章划波浪线句子中加点词语的含义
波浪线句子:我们没有理由不向新年迈出坚实的步伐
(5)文章8~10段不厌其烦的交代母亲折叠的具体日子,有何作用?请写两点
快,我现在就要, 蓝天笛1年前1
蓝天笛1年前1 -
 偶的样 共回答了19个问题
偶的样 共回答了19个问题 |采纳率100%(1)母亲喜买日历→母亲折叠日历→“我”翻日历→“我”学母亲折叠日历
(2)选择A句,A句用比喻手法,把被母亲折叠的日历比喻成待产的孕妇,写出了日历被折叠得中间部分很厚的样子.
(3)母亲是一位勤劳朴实的农村妇女,有着中华传统美德.她把所有的爱都倾注到家人身上,尊敬长辈,爱护晚辈,唯独忽略了自己.
(4)波浪线句子:我们没有理由不向新年迈出坚实的步伐!这是一个双重否定句.它表达了作者珍惜美好生活的愿望.
(5)文章8~10段不厌其烦地交代母亲折叠的具体日子,(1)体现出母亲的细心:她对所有家庭成员的所有重要日子都了然于胸,这里头包含着怎样的牵挂和关心啊!(2)体现出母亲的辛苦:事无巨细,她都承担着,做寿面,到祖坟烧纸钱,母亲的日程排得满满的,她在这些层层叠叠的忙碌的日子里享受着为家人付出的快乐.1年前查看全部
- 在抽空的玻璃罩内封入两杯液面相同的糖水A和纯水B.经历若干时间后,两杯液面的高度是
 wolfkingmen1年前3
wolfkingmen1年前3 -
 416678650 共回答了28个问题
416678650 共回答了28个问题 |采纳率85.7%因为糖水的渗透压比纯水的渗透压高,所以糖水的化学势比纯水的化学势高,所以水分子通过蒸汽方式,从糖水向纯水移动,所以纯水高,糖水低1年前查看全部
- 英语翻译您好.非常感谢您在百忙之中抽空完成此次调查.这是一份学术性问卷.旨在了解大学生在择业时对工作的态度.调查仅供研究
英语翻译
您好.非常感谢您在百忙之中抽空完成此次调查.这是一份学术性问卷.旨在了解大学生在择业时对工作的态度.调查仅供研究使用.不会对您造成任何不利影响.请您放心作答.您的意见对本研究非常重要,请您客观.真实填写.尽量回答每个问题.对您的大力支持表示感谢!
我说不要google就一堆有道…… waktvictor1年前1
waktvictor1年前1 -
 0084218 共回答了22个问题
0084218 共回答了22个问题 |采纳率90.9%Thanks for your acception for this investigation. This is an acdemic investigation. It focuses on the attitude of choosing the job of the college students. The result only uses for the study. It will not take you any trouble. Your advices are very important for us. Please answer the question wiht objectivity and rightly and try to answer every question. Thanks again.1年前查看全部
- 相律中怎么判断R撇,就是独立的限制条件数,我没有找到方法,例如这题:NH4HS(s)放入一抽空的容器中,并与其分解产物N
相律中怎么判断R撇,就是独立的限制条件数,我没有找到方法,例如这题:NH4HS(s)放入一抽空的容器中,并与其分解产物NH3(g)和H2S(s)成平衡.那么这里的独立限制条件是多少?
 microsoft_19811年前1
microsoft_19811年前1 -
 白色蝎子 共回答了19个问题
白色蝎子 共回答了19个问题 |采纳率100%首先,这个东西仅存在于同一相中,否则不算限制,其次,在同一相中观察是否存在量之间的恒等关系,有则算,这里的两个生成物和反应物都不在一个相态中,所以是01年前查看全部
- 高手来分析这几张放电曲线图说明了什么? 今天抽空用DIY的电阻箱(或叫电子负载),对自组的几组锂电池进行了放电测试,电池
高手来分析这几张放电曲线图说明了什么? 今天抽空用DIY的电阻箱(或叫电子负载),对自组的几组锂电池进行了放电测试,电池是原来充的,不满电.得出如下放电曲线(第一次做,数据不够精确),请高手分析分析,2种锂电放电曲线完全不同,在安全保护电压各设置多少伏为最佳?
 悠旎1年前1
悠旎1年前1 -
 还咳 共回答了22个问题
还咳 共回答了22个问题 |采纳率90.9%一般来说,单片电芯负载电压在3.5,空载电3.7,就算是没电了.但是这要根据具体电池来,很难讲清楚,都是基于个人使用经验的.你的用电器抽电能力也要加入这个函数里面去.这说的是30C以上的电池.你那个6C的不建议使用.查看原帖1年前查看全部
- 首先向我的冒昧打扰向您表示歉意,然后感谢您抽空看此封信件,以下是我的个人介绍。”翻译成英语是
 admany8889991年前2
admany8889991年前2 -
 实话实说的至尊宝 共回答了26个问题
实话实说的至尊宝 共回答了26个问题 |采纳率88.5%First, I am sorry to bother you, and I am very appreciate that you can spare some time to read this letter. The following is my self-introduction.1年前查看全部
- (2013•上海模拟)在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:
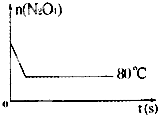 (2013•上海模拟)在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:
(2013•上海模拟)在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:
N2O4(无色)⇌2NO2(红棕色)Q<0,隔一段时间对该容器内的物质进行分析得到如下数据:
(1)计算20s-40s内用N2O4表示的平均反应速率为______.
时间(s)
n(mol)0 20 40 60 80 100 n(N2O4) 0.40 a 0.20 c d e n(NO2) 0.00 0.24 b 0.52 0.60 0.60
(2)反应进行至100s后将反应混合物的温度降低,混合气体的颜色______(填“变浅”、“变深”或“不变”).
(3)若要重新达到平衡时,使c(NO2)/c(N2O4)值变小,可采取的措施有(填序号)______.
A. 增大N2O4的起始浓度B.向混合气体中通入NO2 C.使用高效催化剂D.升高温度
(4)如果在80℃、将0.40mol的N2O4气体放入一个起始体积为2L、且压强维持不变的容器中发生上述反应.则达到平衡时n(NO2)______0.60mol(填“大于”“等于”或“小于”).
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线. miluco1年前1
miluco1年前1 -
 孤独ZY 共回答了18个问题
孤独ZY 共回答了18个问题 |采纳率83.3%解题思路:(1)先根据二氧化氮物质的量计算20s内反应的四氧化二氮的物质的量,进而计算20s时容器内四氧化二氮的物质的量,再计算20s~40s参加反应的四氧化二氮的物质的量,再根据速率定义式计算四氧化二氮的平均反应速率;
(2)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小;
(3)若使c(NO2)/c(N2O4)值变小,需使平衡向逆反应方向移动;
(4)压强不变则比原平衡的压强大,平衡向生成四氧化二氮的方向移动,使压强减小;
(5)降低温度,化学反应速率减小,平衡向放热方向移动.(1)20s时△n(NO2)=0.24mol,故△n(N2O4)=[1/2]△n(NO2)=[1/2]×0.24mol=0.12mol,所以a=0.4mol-0.12mol=0.28mol,故20s~40s参加反应的四氧化二氮的物质的量为0.28mol-0.2mol=0.08mol,所以20s-40s内用N2O4表示的平均反应速率为
0.08mol
2L
20s=0.002mol/(L•S),
故答案为:0.002mol/(L•S);
(2)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小,气体的颜色变浅,
故答案为:变浅;
(3)若使c(NO2)/c(N2O4)值变小,需使平衡向逆反应方向移动,
A、增大N2O4的起始浓度,按勒夏特列原理,平衡移动的结果只能减弱这种改变,不能消除,所以,c(NO2)/c(N2O4)值变小,故A正确;
B、向混合气体中通入NO2 时,因为同时增大了体系的压强,平衡移动的结果,会使c(NO2)/c(N2O4)值变小,故B正确;
C、催化剂只能加快化学反应速率,不会影响平衡移动,故C错误;
D、升高温度会使平衡向生成二氧化氮的方向移动,会使c(NO2)/c(N2O4)值变大,故D错误;
故选:AB;
(4)压强不变则比原平衡的压强小,平衡向体积增大的方向移动,即向生成二氧化氮的方向移动,所以,n(NO2)增大,
故答案为:大于;
(5)当降低温度,化学反应速率减小,到达平衡所需时间增大,平衡向逆反应方向移动,所以到达新平衡时四氧化二氮的物质的量比第一次平衡时少,60℃曲线为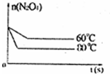 .
.
故答案为:
点评:
本题考点: 化学平衡的影响因素;反应速率的定量表示方法;化学平衡建立的过程.
考点点评: 本题考查了化学反应速率、平衡移动、外界条件对化学平衡的影响图象,题目难度不大.1年前查看全部
- 1.\x05在体积为1dm3的抽空容器中充入0.03458mol N2O4(g),发生如下分解反应:N2O4(g) 2N
1.x05在体积为1dm3的抽空容器中充入0.03458mol N2O4(g),发生如下分解反应:N2O4(g) 2NO2(g),
在323.15K条件下,分解反应的平衡总压为130.0kPa,
(1)x05计算N2O4(g)的解离度及分解反应的标准平衡常数Kθ.
(2)x05计算373.15K条件下,反应的标准平衡常数Kθ.
已知:NO2(g)和N2O4(g)的 (298K)分别为33.2 kJ•mol-1、9.16 kJ•mol-1,并假设反应的 ΔrCp,m = 0 . lqr2hl1年前1
lqr2hl1年前1 -
 zrchyy 共回答了15个问题
zrchyy 共回答了15个问题 |采纳率86.7%1年前查看全部
- 英语翻译“好久没去那里了,今天抽空去了一下,景色依旧,空气也清新”
 lwqin01年前1
lwqin01年前1 -
 绫小路彦麻吕 共回答了12个问题
绫小路彦麻吕 共回答了12个问题 |采纳率100%Haven't been there for a long time, but made some time for the visit today, everthing is just like the old times and with fresh air. 希望采纳谢谢1年前查看全部
- 英语翻译1.清炉、装炉;2.抽空、充气、预热;3.化料、引晶;4.生长细颈;5.扩肩;6.转肩、保持及夹持器释放;7.收
英语翻译
1.清炉、装炉;
2.抽空、充气、预热;
3.化料、引晶;
4.生长细颈;
5.扩肩;
6.转肩、保持及夹持器释放;
7.收尾、停炉; joanne731年前1
joanne731年前1 -
 yaohua66 共回答了14个问题
yaohua66 共回答了14个问题 |采纳率85.7%1.Clean furnace,installed furnace;
2.The time to inflate,preheat;
3.Of material,seeding;
4.The growth of narrow neck;
5.Expanding the shoulder;
6.Shoulder turn,maintain and gripper release;
7.Closure,shutdown;1年前查看全部
- 这英语句子怎么造啊?我希望你们能抽空去看看那部电影I hope that you can _____ _____ ___
这英语句子怎么造啊?
我希望你们能抽空去看看那部电影
I hope that you can _____ _____ _____ _____see the film. bijiasuo39261年前2
bijiasuo39261年前2 -
 小精灵LUY 共回答了19个问题
小精灵LUY 共回答了19个问题 |采纳率78.9%I hope you can find a time to see the film1年前查看全部
- 在100℃时,将0.100mol的N 2 O 4 气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到
在100℃时,将0.100mol的N 2 O 4 气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:时间/s
浓度mol·L -10 20 40 60 80 100 c(N 2 O 4 )mol·L -1 0.100 c 1 0.050 c 3 a b c(NO 2 )/mol·L -1 0.000 0.060 c 2 0.120 0.120 0.120
(1)达到平衡时N 2 O 4 的转化率为 %,表中c 2 c 3 ,a b (选填“>”“<”“=”)。
(2)20s的四氧化二氮的浓度c 1 = mol·L -1 ,在0s~20s内四氧化二氮的平均反应速率为 mol·(L·s) -1 ;。
(3)若在相同情况下最初向该容器充入的是二氧化氮气体要达到上述同样的平衡状态,二氧化氮的起始浓度是 mol·L -1 。 sam1982cn1年前1
sam1982cn1年前1 -
 zhenghuifang 共回答了14个问题
zhenghuifang 共回答了14个问题 |采纳率92.9%(1)60,>,="" (2)0.070,0.0015 (3)0.200
略1年前查看全部
- 在100℃时,将0.100mol N2O4气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行
在100℃时,将0.100mol N2O4气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到如表数据:
(1)该反应的平衡常数表达式为时间(s) 0 20 40 60 80 c(N2O4)/mol•L-1 0.100 c1 0.050 c3 c4 c(NO2)/mol•L-1 0.000 0.060 c2 0.120 0.120 [NO2]2 [N2O4] ;从表中分析:[NO2]2 [N2O4]
c1______c2,c3______c4(填“>”、“<”或“=”).
(2)在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为______mol•L-1•s-1.
(3)达平衡后下列条件的改变可使NO2气体浓度增大的是______(填字母序号).
A.扩大容器的容积B.再充入一定量的N2O4C.分离出一定量的NO2D.再充入一定量的He
(4)若在相同条件下,起始时只充入0.080mol NO2气体,则达到平衡时NO2气体的转化率为______. 6299841年前1
6299841年前1 -
 xuzhh1314 共回答了24个问题
xuzhh1314 共回答了24个问题 |采纳率91.7%解题思路:(1)平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,根据方程式计算c2、c1,据此解答;60s后反应达平衡,反应混合物各组分的浓度不变;
(2)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),依据化学反应速率V=[△c/△t]计算得到;
(3)依据化学平衡原理分析改变条件提高NO2转化率的选项;
(4)依据平衡浓度计算平衡常数,结合化学平衡三段式列式计算,转化率=[消耗量/起始量]×100%;(1)N2O4(g)⇌2NO2(g),反应的平衡常数K=
[NO2]2
[N2O4];
20s时c(NO2)=0.060mol/L
N2O4⇌2 NO2,
浓度变化 0.030mol 0.060mol/L
c1=0.10mol/L-0.03mol/L=0.070mol/L;
由表可知,40s时,c(N2O4)=0.050mol/L,
N2O4⇌2 NO2,
浓度变化:(0.1-0.05)mol/L 0.10mol/L
所以c2=0.10mol/L
所以c2>c1;
故答案为:
[NO2]2
[N2O4];<;=;
(2)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4⇌2 NO2,
浓度变化:0.06mol/L 0.120mol/L
V(N2O4)=[0.060mol/L/60s]=0.001mol/(L•s);
故答案为:0.001;
(3)N2O4=2 NO2 反应是气体体积减小的放热反应,依据化学平衡原理分析选项,增大二氧化氮浓度的条件;
A、增大容器体积,各组分浓度均减小,故A错误;
B、再充入四氧化二氮,平衡正向移动,二氧化氮浓度增大,故B正确;
C、减小NO2的浓度,平衡虽正向进行,但二氧化氮的浓度减小,故C错误;
D、再充入一定量的He,总压增大,气体分压不变,平衡不变,二氧化氮浓度不变,故D错误;
故选B;
(4)依据平衡浓度计算平衡常数,结合化学平衡三段式列式计算;
N2O4⇌2 NO2,
起始量(mol/L) 0.10 0
变化量(mol/L) 0.06 0.12
平衡量(mol/L) 0.04 0.12
K=
0.122
0.04=0.36
若起始时充入N02气体0.080mol,设消耗二氧化氮物质的量浓度为x,2 NO2=N2O4 ,K=[1/0.36]
2 NO2=N2O4
起始量(mol/L) 0.0800 0
变化量(mol/L) x 0.5x
平衡量(mol/L) 0.080-x 0.5x
K=[0.5x
(0.080−x)2=
1/0.36]
x=0.020mol/L
则达到平衡时N02气体的转化率=[0.020/0.080]×100%=25%,
故答案为:25%.点评:
本题考点: 化学平衡的计算;化学平衡的影响因素.
考点点评: 本题考查化学平衡的有关计算、化学平衡的影响因素,题目综合性较大,注意基础知识的积累掌握.1年前查看全部
- 希望百忙之中抽空参加的文言文怎么说
 一品搜1年前1
一品搜1年前1 -
 canfengxie 共回答了16个问题
canfengxie 共回答了16个问题 |采纳率100%望拨冗出席——多用于邀请平级者,如客户、同事,等等。
望拨冗莅临——多用于邀请领导。1年前查看全部
- 有关压强的化学题在常温下四个容积相同的抽空的密闭容器内,分别注入下列各组气体(先注入一种,再注入另一种),全部气体注入完
有关压强的化学题
在常温下四个容积相同的抽空的密闭容器内,分别注入下列各组气体(先注入一种,再注入另一种),全部气体注入完毕后,容器中的压强从大到小的顺序是(C )
①2mol二氧化硫和1mol氧气 ②2mol硫化氢和1mol二氧化硫
③2mol硫化氢和1mol氯气 ④2mol氨和lmol氯化氢
A.③>④>①>② B.①>②=③>④ C.①=③>④>② D.①=②=③>④
硫化氢和二氧化硫恰好反应完全,生成什么,为什么它的压强最小.
只有气体才有压强?固体和液体的压强是0吗?
压强与什么有关? 俊11年前2
俊11年前2 -
 maidiken 共回答了32个问题
maidiken 共回答了32个问题 |采纳率90.6%1、常温SO2和O2只有极小部分反应生成SO3,可以忽略,所以气体总物质的量是3mol.
2、常温下完全反应:2H2S+SO2=3S↓+2H2O,而常温下水是液态,所以气体总物质的量是0.
3、气体状态时不反应,所以气体总物质的量是3mol.
4、部分NH3和HCl结合:NH3+HCl=NH4Cl,剩下1molNH3,所以气体总物质的量是1mol.
综上,答案选C.
一般在化学中谈到压强都是指气压,因为气压在一定温度下是正比于气体物质的量的.而固体和液体都有压强且不0,但是不能直接计算(需要用力和受力面积计算),且与化学关系不大,所以一般化学中不考虑固体和液体的压强.1年前查看全部
- 在80℃时,将0.4mol的N2O4气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如
在80℃时,将0.4mol的N2O4气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.时间(s)
C(mol/L)0 20 40 60 80 100 C(N2O4) 0.20 a 0.10 c d e C(NO2) 0.00 0.12 b 0.24 0.24 0.24
(1)该反应的化学方程式为______,
(2)表中b=______mol/L,c______d(填“<”、“=”、“>”).
(3)20s时,N2O4的浓度为______mol/L,0~20s内N2O4的平均反应速率为______.
(4)该反应的平衡常数表达式K=c2(NO2) c(N2O4) ,在80℃时该反应的平衡常数K值为______.c2(NO2) c(N2O4)
(5)在其他条件相同时,若该反应的K值越大,表明建立平衡时______.(多选)
A.N2O4的转化率越高 B.NO2的产量越大C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
E.所耗时间越少F.容器内气体压强越大. 27080031年前1
27080031年前1 -
 与天无缘 共回答了18个问题
与天无缘 共回答了18个问题 |采纳率83.3%解题思路:(1)依据反应条件分析判断,结合化学平衡的三段式列式计算分析比较;
(2)结合平衡三段式列式计算分析比较判断;
(3)化学平衡的三段式列式计算N2O4的浓度,结合化学反应速率概念计算0~20s内N2O4的平均反应速率;
(4)依据化学方程式和平衡常数概念写出平衡常数表达式,依据80°C平衡状态下结合三段式列式计算平衡浓度计算平衡常数;
(5)反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅,说明反应逆向进行,逆向是放热反应,正向是吸热反应;该反应的K值越大,说明平衡正向进行,是温度降低的原因,结合反应特征分析选项.(1)将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,反应的化学方程式为:N2O4⇌2NO2,故答案为:N2O4⇌2NO2 ;
(2)隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅,说明反应逆向进行,逆向是放热反应,正向是吸热反应;依据化学平衡三段式列式计算分析判断;进行到40S和进行到80S时;
N2O4⇌2NO2
起始量(mol) 0.4 0
变化量(mol) 0.2 0.4
40S末(mol) 0.2 0.4
得到b=0.2mol/L;
进行进行到60s到80S时,反应达到平衡状态,c=d=e;
N2O4⇌2NO2
起始量(mol) 0.4 0
变化量(mol) 0.24 0.48
80S末(mol) 0.16 0.48
d=c=e=[0.16mol/2L]=0.08 mol/L
故答案为:0.2;=;
(3)进行到20S;
N2O4⇌2NO2
起始量(mol) 0.4 0
变化量(mol) 0.12 0.24
20S末(mol) 0.28 0.24
20s时,N2O4的浓度=[0.28mol/2L]=0.14mol/L;
0~20s内N2O4的平均反应速率=
0.12mol
2L
20s=0.003mol/(L•s);
故答案为:0.14;0.003mol/(L•s);
(3)N2O4⇌2NO2,平衡常数K=
c2(NO2)
c(N2O4);
80°C平衡状态下,平衡浓度c(NO2)=0.24mol/L,c(N2O4)=0.08mol/L;
平衡常数K=
c2(NO2)
c(N2O4)=
0.242
0.08=0.72mol/L;
故答案为:
c2(NO2)
c(N2O4);0.72;
(5)反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅,说明反应逆向进行,逆向是放热反应,正向是吸热反应;该反应的K值越大,说明平衡正向进行,是温度降低的原因;
A、平衡正向进行N2O4的转化率越高,故A正确;
B、平衡正向进行NO2的产量越大,故B正确;
C、依据上述计算分析平衡正向进行,N2O4与NO2的浓度之比越小,故C错误;
D、该反应的K值越大,说明平衡正向进行,正反应进行的程度越大,故D正确;
F、反应正向进行是气体体积增大的反应,容器内气体压强越大,故F正确;
故答案为:ABDF.点评:
本题考点: 化学平衡的计算;化学平衡的影响因素.
考点点评: 本题考查了化学平衡的建立判断,平衡常数的计算应用,平衡移动原理的分析判断,题目难度中等.1年前查看全部
- 英语翻译:我们想邀请你来观看我们表演的节目,希望你能抽空来观看我们的表演.急
 sdfad22er1年前1
sdfad22er1年前1 -
 好大一棵树111 共回答了19个问题
好大一棵树111 共回答了19个问题 |采纳率94.7%We would like to invite you to watch our show program, I hope you can find time to watch our performance1年前查看全部
- 科学家将黑猫卵的核物质注入内部已抽空的白猫的卵内,激活后,移植入花猫的子宫中,花猫最终产下一只克隆猫
科学家将黑猫卵的核物质注入内部已抽空的白猫的卵内,激活后,移植入花猫的子宫中,花猫最终产下一只克隆猫
这个克隆猫的体色和性别是____.要分析.不要直接答案 xiaokang341年前1
xiaokang341年前1 -
 kenlmsoft 共回答了16个问题
kenlmsoft 共回答了16个问题 |采纳率93.8%体色是黑,性别为雌性.决定体色和性别的只有DNA(在黑猫卵的核物质中),所以体色和黑猫相同,性别亦然.(黑猫是雌猫).1年前查看全部
- 在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下表格
在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:时间/s
浓度mol•L-10 20 40 60 80 100 c(N2O4)mol•L-1 0.100 c1 0.050 c3 a b c(NO2)/mol•L-1 0.000 0.060 c2 0.120 0.120 0.120
(1)达到平衡时N2O4的转化率为______%.
(2)20s的四氧化二氮的浓度c1=______mol•L-1,在0s~20s内四氧化二氮的平均反应速率为______mol•(L•s)-1;. surewheel1年前1
surewheel1年前1 -
 奶_瓶 共回答了22个问题
奶_瓶 共回答了22个问题 |采纳率86.4%解题思路:(1)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;60s后反应达平衡,反应混合物各组分的浓度不变;
(2)由△c(NO2),根据方程式计算△c(N2O4),20s的四氧化二氮的浓度=起始浓度-△c(N2O4);根据v=[△c/△t]计算v(N2O4).(1)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4⇌2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为[0.06mol/L/0.10mol/L]×100%=60%,
故答案为:60;
(2)由表可知,20s时,c(NO2 )=0.060mol/L,所以
N2O4⇌2 NO2,
浓度变化:0.03mol/L 0.060mol/L
所以20s的四氧化二氮的浓度c1=0.1mol/L-0.03mol/L=0.07mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4)[0.03mol/L/20s]═0.0015mol•(L•s)-1,
故答案为:0.07;0.0015.点评:
本题考点: 化学平衡的计算.
考点点评: 本题考查化学平衡的有关计算应用,主要是平衡转化率、反应速率概念的计算应用,难度中等,注意基础知识的积累掌握.1年前查看全部
- 英语翻译请帮忙翻译下面这句话谢谢您能在百忙之中抽空回信
 jinyinglai1年前3
jinyinglai1年前3 -
 poinmo 共回答了21个问题
poinmo 共回答了21个问题 |采纳率85.7%Thank you very much for replying me out of your busy schedule.
Thank you for writing back to me from your busy schedule.
Thank you for taking time out of your busy schedule to reply me1年前查看全部
- 在100℃时,将0.200mol的四氧化二氮气体充入2L抽空的密闭容器中,每隔一定时间对该容器内的物质进行分析,得到如下
在100℃时,将0.200mol的四氧化二氮气体充入2L抽空的密闭容器中,每隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:时间 0 20 40 60 80 100 c(N2O4) 0.100 c1 0.050 c3 a b c(NO2) 0.000 0.060 c2 0.120 0.120 0.120
(1)该反应的化学方程式为______,达到平衡时四氧化二氮的转化率为______%.
(2)20s时四氧化二氮的浓度c1=______mol•L-1,在0~20s时间段内,四氧化二氮的平均反应速率为______mol•L-1•s-1.
(3)若在相同情况下最初向容器中充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的初始浓度为______mol•L-1. 曾那么接近幸福1年前1
曾那么接近幸福1年前1 -
 whj0880 共回答了16个问题
whj0880 共回答了16个问题 |采纳率93.8%解题思路:(1)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;60s后反应达平衡,反应混合物各组分的浓度不变.
(2)由△c(NO2),根据方程式计算△c(N2O4),20s的四氧化二氮的浓度=起始浓度-△c(N2O4);根据v=[△c/△t]计算v(N2O4).
(3)恒温恒容条件下,且反应前后气体的物质的量发生变化,起始向容器中充入的是二氧化氮气体,要达到相同的平衡状态,按化学计量数转化到N2O4一边,满足N2O4的浓度为0.1mol/L.(1)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4⇌2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为[0.06mol/L/0.1mol/L]×100%=60%;
故答案为:60;
(2)由表可知,20s时,c(NO2 )=0.060mol/L,所以
N2O4⇌2 NO2,
浓度变化:0.03mol/L 0.060mol/L
所以20s的四氧化二氮的浓度c1=0.1mol/L-0.03mol/L=0.070mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4)=[0.03mol/L/20S]=0.0015mol•(L•s)-1.
故答案为:0.070mol/L;0.0015mol•(L•s)-1;
(3)恒温恒容条件下,且反应前后气体的物质的量发生变化,起始向容器中充入的是二氧化氮气体,要达到相同的平衡状态,按化学计量数转化到N2O4一边,满足N2O4的浓度为0.1mol/L,由N2O4(g)⇌2 NO2(g)可知,二氧化氮的初始浓度=2×0.1mol/L=0.2mol/L,
故答案为:0.2.点评:
本题考点: 化学平衡的计算;反应速率的定量表示方法.
考点点评: 本题考查化学反应速率、化学平衡常数、化学平衡的有关计算、等效平衡等,难度中等,注意基础知识的积累掌握.1年前查看全部
- "感谢您百忙之中抽空来." 这句英文怎么说?
 lyd831年前4
lyd831年前4 -
 0o鼠标 共回答了23个问题
0o鼠标 共回答了23个问题 |采纳率87%是个人简历里常用到的句子了:
"感谢您百忙之中抽空来." 英文可以这么说:)
Thank you for sparing a time to.(in the midst of pressing affairs)
如:
感谢您百忙之中抽空阅读我的自荐材料.
Thank you for sparing a time to read my recommending material in the midst of pressing affairs,
感谢您在百忙之中抽空阅读我的自荐材料,我希望在贵公司谋求一份职业.
Thank you for sparing a time to read my recommending material in the midst of pressing affairs,I hope to seek a job in your company.1年前查看全部
- 在100℃时,将0.200mol的四氧化二氮气体充入2L抽空的密闭容器中,每隔一定时间对该容器内的物质进行分析,得到如下
在100℃时,将0.200mol的四氧化二氮气体充入2L抽空的密闭容器中,每隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:时间 0 20 40 60 80 100 c(N2O4) 0.100 c1 0.050 c3 a b c(NO2) 0.000 0.060 c2 0.120 0.120 0.120
(1)该反应的化学方程式为______,达到平衡时四氧化二氮的转化率为______,该温度时,平衡常数值为______.
(2)80s时四氧化二氮的浓度a=______,在0~20s时间段内,四氧化二氮的平均反应速率为______.
(3)若在相同情况下最初向容器中充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的初始浓度为______. 假冒黑客1年前1
假冒黑客1年前1 -
 13825421314 共回答了17个问题
13825421314 共回答了17个问题 |采纳率76.5%解题思路:(1)由表可知,60s时反应达平衡,利用三段式计算各组分的浓度变化量、平衡浓度,转化率=浓度变化量÷起始浓度,据此计算四氧化二氮的转化率,平衡常数k=c2(NO2)c(N2O4);(2)80s时处于平衡状态,根据(1)计算可知a的值;根据浓度变化量之比等于化学计量数之比计算△c(N2O4),再根据v=△c△t计算v(N2O4);(3)恒温恒容条件下,且反应前后气体的物质的量发生变化,起始向容器中充入的是二氧化氮气体,要达到相同的平衡状态,按化学计量数转化到N2O4一边,满足N2O4的浓度为0.1mol/L.(1)反应的化学方程式为:N2O4⇌2NO2,
由表可知,60s时反应达平衡,平衡时c(NO2)=0.120mol/L,N2O4的起始度为0.1mol/L,则:
N2O4(g)⇌2NO2(g)
起始(mol/L):0.1 0
变化(mol/L):0.06 0.12
平衡(mol/L):0.04 0.12
所以平衡时N2O4的转化率=[0.06mol/L/0.1mol/L]×100%=60%,
平衡常数K=
c2(NO2)
c(N2O4)=
0.122
0.04=0.36,
故答案为:N2O4⇌2NO2;60%;0.36;
(2)80s时处于平衡状态,根据(1)计算可知a=0.04;
由表中数据可知,20s时c(NO2 )=0.06mol/L,浓度变化量之比等于化学计量数之比,所以,在0~20s时间段内,△c(N2O4)=[1/2]×0.06mol/L=0.03mol/L,故v(N2O4)=[0.03mol/L/20s]=0.0015mol/(L•s),
故答案为:0.04;0.0015mol/(L•s);
(3)恒温恒容条件下,且反应前后气体的物质的量发生变化,起始向容器中充入的是二氧化氮气体,要达到相同的平衡状态,按化学计量数转化到N2O4一边,满足N2O4的浓度为0.1mol/L,由N2O4(g)⇌2 NO2(g)可知,二氧化氮的初始浓度=2×0.1mol/L=0.2mol/L,
故答案为:0.2mol/L.点评:
本题考点: 化学平衡建立的过程;化学平衡的计算.
考点点评: 本题考查化学反应速率、化学平衡常数、化学平衡的有关计算、等效平衡等,难度中等,注意基础知识的积累掌握.1年前查看全部
- 一水池,池底有一打开的出水口,不停地向外排着水,另外再用5台抽水机,20小时可将水抽空;用8台抽水机,
一水池,池底有一打开的出水口,不停地向外排着水,另外再用5台抽水机,20小时可将水抽空;用8台抽水机,
15小时可将水抽空,如果仅靠出水口排水,多久能把水排完? qxbh30511年前1
qxbh30511年前1 -
 vincent14 共回答了24个问题
vincent14 共回答了24个问题 |采纳率91.7%设每台抽水机每小时排水a立方米,出水口每小时排水b立方米,则排水总量:
(5a+b)*20=(8a+b)*15
即20a+4b=24a+3b
得b=4a
所以排水总量为(5a+b)*20=(5a+4a)*20=180a=45b立方米
如果仅靠出水口排水,所需时间为:45b/b=45小时1年前查看全部
- 英语翻译你是上班时间抽空过来的吗,英文怎么说
 yuanbangyin1年前5
yuanbangyin1年前5 -
 螃蟹1 共回答了12个问题
螃蟹1 共回答了12个问题 |采纳率100%你是上班时间抽空过来的吗? Are you use office hours evacuation to come here ?其中:evacuation 英[ɪ,vækjʊ'eɪʃ(ə)n] 美[ɪ,vækjʊ'e&...1年前查看全部
- 三元系爆炸极限测定实验结束后,为什么必须将系统抽空?
 陪你到uu55661年前1
陪你到uu55661年前1 -
 YOYOHHH 共回答了15个问题
YOYOHHH 共回答了15个问题 |采纳率80%如果不抽空的话,实验装置内会有可燃气体,有发生危险的可能1年前查看全部
- 英语翻译1.我有绘画天赋,我画什么像什么.2.由于路途颠簸,我呕吐得快要把胃都抽空了.麻烦不要用翻译器啊.
 zhangyangchao1年前3
zhangyangchao1年前3 -
 你家后院着火了 共回答了26个问题
你家后院着火了 共回答了26个问题 |采纳率80.8%1.I have talent in painting ,and my paintings are really true to life and vivid indeed.
2.As we bumped over the track,i nearly vomited my stomach out.1年前查看全部
- 把发声物体放在玻璃罩里,用抽气筒把罩里空气抽空,如果用秒表计时,怎么计算抽空罩内空气的时间?
 toty20051年前4
toty20051年前4 -
 susan0755 共回答了24个问题
susan0755 共回答了24个问题 |采纳率83.3%从开始抽气计时一直到听不见玻璃罩内物体发声为止!
为什么要直到听不见物体发声为止呢?因为声音的传播是需要介质的,我们生活在空气之中,我们平日里说话大家都能听见.就是因为有空气这种介质.而声音是无法在没有介质的真空中传播的.所以直到听不见声音了,说明玻璃罩里已经全部是真空了,无传播声音的介质--空气了.此时空气也就抽完了.
声音传播的介质是多种多样的.我们生活中的许多物体都可做为声音传播的介质,包括谁也可以做为声音传播的介质.而光的传播是不需要介质的.它在任何情况下都是可以传播的.1年前查看全部
- 1995年,联合国教科文组织将每年的4月23日定为“世界读书日”,然而,抽空认真读书的人越来越少.但读书的
 决不罢手1年前1
决不罢手1年前1 -
 dby_dai 共回答了16个问题
dby_dai 共回答了16个问题 |采纳率81.3%我喜欢看《查理九世》1年前查看全部
- 在100℃时,将0.100mol的四氧化二氮气体充入1L抽空的密闭容器中.隔一定时间对该容器内的物质浓度进行分析得到如下
在100℃时,将0.100mol的四氧化二氮气体充入1L抽空的密闭容器中.隔一定时间对该容器内的物质浓度进行分析得到如下表数据:
时间(S) 0 20 40 60 80
c(N2O4)/mol/L 0.100 a 0.050 c d
c(NO2)/mol/L 0.000 0.06 b 0.120 0.120
(1).20s时N2o4浓度a=( ) ;在0-20s内N2O4的平均反应速率为( );
表中b()c()d (填>.<.= )
(2.)该反应到达平衡时N2O4的转化率为( ) 平衡时容器内压强与开始时压强之比是() 衔杯袒腹1年前2
衔杯袒腹1年前2 -
 ay2137 共回答了23个问题
ay2137 共回答了23个问题 |采纳率82.6%一个N2O4可逆变成两个NO2,20S时产生NO2 0.06mol/l,
因此消耗N2O4 0.03mol/l.还剩0.07mol/l.即a=0.07,同理b=0.1,c=d=0.04.
然后根据各个问的定义进行计算即可.1年前查看全部
- 《母亲的日历》阅读题!新年前夕,母亲总爱抽空去镇上买回一本崭新的A4纸四分之一大小的日历,钉在墙上,随手一翻红红黑黑的纸
《母亲的日历》阅读题!
新年前夕,母亲总爱抽空去镇上买回一本崭新的A4纸四分之一大小的日历,钉在墙上,随手一翻红红黑黑的纸张,她欢喜得像个孩子.
其实,母亲不识字,只是认识一些简单的阿拉伯数字.起初,她钟情于日历,引起我好长一段时间的疑惑,一直以为母亲看日历,只是为了记住二十四节气,以便农事耕收,或关注母猪下崽,出栏的时日.
直到去年新年前夕,我偶尔回了一趟家,恰逢母亲买回了新日历,正欢天喜地翻看着,几乎每个月,都有几页被她折叠起不同的图案,甚至有几页,她用糊鞋底的浆糊糊上红布条、白布条……看母亲虔诚幸福地忙碌着,我一时没有打扰她,只是站在一旁,静静地注视着冬阳下的母亲,看她一会儿双掌合十,一会儿满脸微笑……当时我以为母亲在做某种迷信的祷告,心想,老年人冬闲无事,寻找一些心灵的信仰,即使迷信,只要心灵得以慰藉,能带来快乐,我们做晚辈的,就随她而去吧.
一本厚厚的日历被母亲折叠、张贴得像一个待产的孕妇.她突然转身,看到回家的我,自然惊喜不已.看我注视着她手中的日历,母亲有点慌张,躲闪着把日历掖于身后,嗫嚅着说,在家闲着没事,瞎忙活!
母亲的日历还是被我拿到手中,翻到被折叠或糊上布条的页面,我好奇地问她:妈,这些都是什么日子呀?
母亲见我对她折叠过的日历感兴趣,犹豫着,喃喃而语,到时候,你就会知道了!母亲的“卖关子”更撩起我的好奇心,我激将母亲———在家没事搞什么封建迷信活动!母亲一急,马上和我争辩起来……
在争辩中,我了解到那些被母亲折叠、或糊上布条页面的含义———
2月28日、7月14日、8月17日、8月19日,那是弟弟、我、姐姐和哥哥的生日;母亲折叠这些日子,为的是到时候提醒我们为自己做一碗寿面.
元月2日、2月16日、12月18日、12月28日,那是我、弟弟、姐姐、哥哥的结婚纪念日,母亲糊上红布条,只因这些日子都是我们的大喜之日,到时候她会提醒我们在这一天好好庆祝,夫妻要相敬如宾.
6月14日、10月20日,那是祖母和外婆去世的纪念日.母亲糊上白布条,是提醒自己到那一天,到祖坟烧一些纸钱,保佑我们一大家子出行平安.
2月3日、4月5日、6月16日、8月5日、8月22日被母亲折叠成心形,那是孙子、孙女、外孙的生日,母亲折叠这些日子,是要通知我们为自己的妻子好好做一天家务,在母亲的眼里,子女的出生日就是母亲的受难日.
我翻看完所有的日历,竟没有发现母亲为自己的生日和结婚纪念日打上记号,我心隐隐地发痛.母亲把所有的爱都倾注到家人身上,却忽略了自己.
也是因母亲的那本充满母爱的日历,让我记住了家人所有的生日、祖辈的祭日,以及我们兄弟姐妹的结婚纪念日.因而,在新年到来之际,我总是满怀信心迎接新年,因为新的一年里,有那么多值得我们欣喜的日子,这种欣喜不为权利,不为金钱,而是至真亲情的牵挂和关心!我们没有理由不向新年迈出坚实的步伐!
新年的钟声敲响了,我眼前又恍惚起母亲折叠新年日历的身影,止不住拿起案头的一本新日历,学着母亲的虔诚,翻着日历折叠起来.我先折叠起的,是母亲和父亲的生日……
(1) 母亲喜买日历→(母亲)____日历→“我”____日历→“我”学母亲折叠日历
(2)从文中画线的A B两个句子任选一句赏析
A一本厚厚的日历被母亲折叠,张贴得像一个待产的孕妇
B看我注视着她手中的日历,母亲有点慌张,躲闪着把日历掖于身后,嗫嚅着说,在家闲着没事,瞎忙活!
选择___句,___________
(3)简要分析母亲这一人物形象
(4)根据你的理解,说说文章划波浪线句子中加点词语的含义
波浪线句子:我们没有理由不向新年迈出坚实的步伐
(5)文章8~10段不厌其烦的交代母亲折叠的具体日子,有何作用?请写两点
快,我现在就要, vivian52008591年前1
vivian52008591年前1 -
 言文行远 共回答了21个问题
言文行远 共回答了21个问题 |采纳率81%在网上去查1年前查看全部
- 在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如表格:
在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如表格:
试填空:时间/s
浓度mol•L-10 20 40 60 80 100 c(N2O4)mol•L-1 0.100 c1 0.050 c3 a b c(NO2)/mol•L-1 0.000 0.060 c2 0.120 0.120 0.120
(1)达到平衡时N2O4的转化率为______%,表中c2______c3,a______b (选填“>”“<”“=”).
(2)20s的四氧化二氮的浓度c1=______mol•L-1,在0s~20s内四氧化二氮的平均反应速率为______mol•(L•s)-1.
(3)若在相同情况下最初向该容器充入的是二氧化氮气体要达到上述同样的平衡状态,二氧化氮的起始浓度是______mol•L-1. yueliang5201年前1
yueliang5201年前1 -
 杨念 共回答了22个问题
杨念 共回答了22个问题 |采纳率90.9%解题思路:(1)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;
根据方程式计算,计算c2、c3,据此解答;
60s后反应达平衡,反应混合物各组分的浓度不变.
(2)由△c(NO2),根据方程式计算△c(N2O4),20s的四氧化二氮的浓度=起始浓度-△c(N2O4);
根据v=[△c/△t]计算v(N2O4).
(3)达到上述同样的平衡状态,为等效平衡,按化学计量数换算到N2O4一边,满足c(N2O4)为0.100mol/L.(1)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4⇌2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为[0.06mol/L/0.1mol/L]×100%=60%;
c3=0.1mol/L-0.06mol/L=0.04mol/L,
由表可知,40s时,c(N2O4)=0.050mol/L,
N2O4⇌2 NO2,
浓度变化:(0.1-0.05)mol/L 0.10mol/L
所以c2=0.10mol/L
所以c2>c3;
60s后反应达平衡,反应混合物各组分的浓度不变,所以a=b.
故答案为:60;>;=
(2)由表可知,20s时,c(NO2)=0.060mol/L,所以
N2O4⇌2 NO2,
浓度变化:0.03mol/L 0.060mol/L
所以20s的四氧化二氮的浓度c1=0.1mol/L-0.03mol/L=0.07mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4)=[0.03mol/L/20s]=0.0015mol•(L•s)-1.
故答案为:0.07mol/L;0.0015mol•(L•s)-1.
(3)达到上述同样的平衡状态,为等效平衡,按化学计量数换算到N2O4一边,满足c(N2O4)为0.100mol/L.
所以 N2O4⇌2 NO2,
0.1mol/L 0.20mol/L
故答案为:0.20mol/L点评:
本题考点: 化学平衡的计算.
考点点评: 考查化学平衡的有关计算、等效平衡等,难度中等,注意基础知识的积累掌握.1年前查看全部
- 在80℃时,将0.20mol的四氧化二氮气体充入1L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得
在80℃时,将0.20mol的四氧化二氮气体充入1L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
根据本题内容和表格中提供的数据填空(C1、C2、C3、A、B表示相应的浓度)请回答下列各小题:时间(s)
浓度(mol•L-1)0 20 40 60 80 100 c(N2O4) 0.20 C1 0.10 C3 A B c(NO2) 0.00 0.12 C2 0.22 0.22 0.22
(1)该反应的化学方程式为______;达到平衡时四氧化二氮的转化率为______%,表中C2______C3______A(填“<”、“>”=)
(2)20s时,四氧化二氮的浓度C1=______mol•L-1,在0s~20s内四氧化二氮的平均反应速率为______. 马申亚1年前1
马申亚1年前1 -
 blackcomet_711 共回答了18个问题
blackcomet_711 共回答了18个问题 |采纳率100%解题思路:(1)依据图表数据分析,反应物和生成物分析判断;由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;60s后反应达平衡,反应混合物各组分的浓度不变;
(2)化学平衡的三段式列式计算,结合化学反应速率概念计算0~20s内N2O4的平均反应速率.(1)由表可知,60s时反应达平衡,c(NO2)=0.22mol/L,反应的N2O4浓度为0.11mol/L,反应的化学方程式为:N2O4⇌2 NO2,
N2O4⇌2 NO2,
浓度变化:0.11mol/L 0.22mol/L
所以平衡时N2O4的转化率为[0.11mol/L/0.20mol/L]×100%=55%;
60s后反应达平衡,反应混合物各组分的浓度不变,所以C3=A=B=0.20mol/L-0.11mol/L=0.09mol,40s时:
N2O4⇌2 NO2,
0.2mol/L 0
0.1mol/L 0.2mol/L
0.1mol/L C2=0.2mol/L
C2=0.2mol/L>C3=A=B=0.09mol/L;
故答案为:N2O4⇌2NO2;55%;>;=;
(2)进行到20s;
N2O4 ⇌2NO2
起始量(mol/L) 0.20 0
变化量(mol/L) 0.06 0.12
20S末(mol/L) 0.14 0.12
20s时,N2O4的浓度=C1=0.14mol/L;
0~20s内N2O4的平均反应速率=[0.06mol/L/20s]=0.003mol/(L•s),
故答案为:0.14;0.003mol/(L•s).点评:
本题考点: 化学平衡建立的过程;化学平衡的计算.
考点点评: 本题考查了化学反应速率的计算、化学平衡常数的含义等知识点,注意化学平衡常数只与温度有关,与物质的浓度无关.1年前查看全部
- 把发声体放在玻璃罩里,用抽气机把罩里面的空气抽空,在抽空的过程中,玻璃瓶内压强的变化会怎么样
把发声体放在玻璃罩里,用抽气机把罩里面的空气抽空,在抽空的过程中,玻璃瓶内压强的变化会怎么样
q 溪桥度晚霜1年前5
溪桥度晚霜1年前5 -
 湘颐 共回答了22个问题
湘颐 共回答了22个问题 |采纳率95.5%逐渐减少 直到里面没有气体1年前查看全部
大家在问
- 1小明问妈妈借了500,问爸爸借了500.去买了一双鞋970.还了爸爸10元.还了妈妈10元.自己留10元.欠爸爸490.
- 2枫桥夜泊 作者住在哪 从哪个字看出的
- 3灯L与电阻R串联,电压表测电阻电压.
- 4怎样用电压表测小灯泡电阻
- 5真核生物的遗传物质都是DNA吗?除了一些病毒什么生物的遗传物质是RNA?
- 6自行车6小时能行驶72千米,汽车的速度是自行车的4倍,汽车的速度是多少?(列算式)
- 7概括凿壁偷光这个故事的内容
- 8大家帮忙将下列英语单词变复数
- 9已知集合A={l,3,5},B={l,2,x的平方减一}若AUB={l,2,3,5}求x及A交B
- 10根据统计图统计图计算:这次英语考试的及格率
- 11小明借父亲500 又向母亲借500买双鞋970,还父亲10快和母亲10快,欠父亲490,欠母亲4
- 12英语翻译用英语怎么说例 他不喜欢吃这个 但我一下就选着他不喜欢吃的了 别只翻译例句 我想知道 文法
- 13《我们的错误》联系诗句,对“曲曲折折”一词的理解是:
- 14apple的复数形式
- 15幸福照见了谁的伤痕 那时,他还是个年轻力壮的男人,希望能够在繁华的北京混上几年,攒下一笔钱,再光鲜亮丽地回老家,盖一所像