(2014•桓台县一模)某同学用双氧水和二氧化锰来做制取氧气的实验.请回答下列问题.
 黑鸭子7772022-10-04 11:39:541条回答
黑鸭子7772022-10-04 11:39:541条回答 (2014•桓台县一模)某同学用双氧水和二氧化锰来做制取氧气的实验.请回答下列问题.
(2014•桓台县一模)某同学用双氧水和二氧化锰来做制取氧气的实验.请回答下列问题.(1)要检查A装置的气密性是否良好,通常是把导管口插入水中,然后双手紧握锥形瓶外壁,观察导管口是否有气泡产生.请你回答这种做法的依据是什么(用微粒的观点解释):______;
(2)A装置内发生反应的化学方程式为
| ||
| ||
(3)在实验过程中,某同学由于动作太慢,氧气还没有收集满,锥形瓶内的反应就已经停止(如图所示).若想集满这瓶氧气,在不拆卸装置的前提下,请你帮他想出两种方法:①______②______.

已提交,审核后显示!提交回复
共1条回复
 江湖jh 共回答了22个问题
江湖jh 共回答了22个问题 |采纳率100%- 解题思路:(1)熟悉微粒的性质之二:运动性、微粒之间有间隔,知道宏观与微观的联系,即:宏观上体积的膨胀与微观上粒子的运动和微粒之间的空隙变大有着密切的关系;
(2)熟记教材中的双氧水制取氧气的反应方程式,知道反应物是过氧化氢,生成物是水合氧气,二氧化锰是催化剂;不溶性固体与液体分离的方法常用过滤;
(3)学生实验中出现这样的问题,解决时就会首先想到反应物是谁就再加谁,反应就会继续;再者就是将生成物全都收集起来.(1)根据受热时微粒运动加快,间隔变大的原理,故答案为:(1)手握锥形瓶,使瓶内气体受热,微粒运动速率增大,间隔变大,气体体积膨胀,能从导管口逸出.
(2)依据教材中用双氧水和二氧化锰制取氧气的实验原理以及二氧化锰是催化剂的事实,又因为二氧化锰是固体,双氧水是液体,固体和液体分离要用过滤的方法.故答案为:2H2O2
MnO2
.
2H2O+O2↑ 催化剂 过滤
(3)①因为二氧化锰在化学反应前后化学性质不变,所以再加入适量的双氧水反应又会继续.故答案为:再加入适量的双氧水使反应继续进行
②因为反应结束后,锥形瓶内仍然有氧气停留.故答案为:从分液漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中
答案:
(1)手握锥形瓶,使瓶内气体受热,微粒运动速率增大,间隔变大,气体体积膨胀,能从导管口逸出.
(2)2H2O2
MnO2
.
2H2O+O2↑ 催化剂 过滤
(3)
①再加入适量的双氧水使反应继续进行
②从分液漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中点评:
本题考点: 氧气的制取装置;氧气的收集方法;催化剂的特点与催化作用;分子的定义与分子的特性;书写化学方程式、文字表达式、电离方程式.
考点点评: 该题主要考查实验室制取氧气的原理、二氧化锰的催化作用、装置气密性检查的依据,题目中所问的问题正是同学们在实验操作过程中经常遇到的,所以此题正适合学生的做题口味. - 1年前
相关推荐
- (2014•桓台县一模)某化学小组同学要测定某石灰石样品中碳酸钙的质量分数,进行如下实验:取25g石灰石样品放入烧杯,然
 (2014•桓台县一模)某化学小组同学要测定某石灰石样品中碳酸钙的质量分数,进行如下实验:取25g石灰石样品放入烧杯,然后向里面逐滴加入一定质量、某溶质质量分数的稀盐酸,直至与样品充分反应(杂质不反应).产生二氧化碳质量随反应时间的变化关系如图所示.请分析并完成下列问题:
(2014•桓台县一模)某化学小组同学要测定某石灰石样品中碳酸钙的质量分数,进行如下实验:取25g石灰石样品放入烧杯,然后向里面逐滴加入一定质量、某溶质质量分数的稀盐酸,直至与样品充分反应(杂质不反应).产生二氧化碳质量随反应时间的变化关系如图所示.请分析并完成下列问题:
(1)反应生成二氧化碳的质量是______;
(2)至完全反应所需时间是______min;从图中可看出,随着反应的进行,产生二氧化碳的速率越来越慢.请分析原因:______;
(以上直接填空即可)
(3)计算石灰石样品中碳酸钙的质量分数______. 象棋大师1年前1
象棋大师1年前1 -
 jxzxd8887 共回答了20个问题
jxzxd8887 共回答了20个问题 |采纳率95%解题思路:(1)根据反应曲线图,充分反应放出二氧化碳的质量为8.8g;
(2)根据化学反应速率和温度、以及反应物的浓度有关进行解答;
(3)用反应的化学方程式,由生成二氧化碳的质量计算样品中碳酸钙的质量,碳酸钙质量与样品质量比即为样品中碳酸钙含量;(1)根据反应曲线图,充分反应放出二氧化碳的质量为8.8g;
(2)根据反应曲线图,至完全反应所需时间是4min;从图中可看出,随着反应的进行,产生二氧化碳的速率越来越慢,原因是稀盐酸溶液浓度减小;
(3)设样品中CaCO3的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
10044
x 8.8g
[100/44=
x
8.8g]
x=20g
样品中CaCO3的质量分数为:
20g
25g×100%=80%
答案:
(1)8.8g
(2)4 稀盐酸溶液浓度减小
(3)80%点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 在对数形结合类问题中的表示变化的曲线进行分析时,曲线的折点的特殊意义是分析的重点.1年前查看全部
- (2014•桓台县模拟)如图,▱ABCD中,E为AD的中点.已知△DEF的面积为1,则▱ABCD的面积为( )
 (2014•桓台县模拟)如图,▱ABCD中,E为AD的中点.已知△DEF的面积为1,则▱ABCD的面积为( )
(2014•桓台县模拟)如图,▱ABCD中,E为AD的中点.已知△DEF的面积为1,则▱ABCD的面积为( )
A.9
B.12
C.15
D.18 hmz331年前1
hmz331年前1 -
 yu986464 共回答了14个问题
yu986464 共回答了14个问题 |采纳率85.7%解题思路:由于四边形ABCD是平行四边形,那么AD∥BC,AD=BC,根据平行线分线段成比例定理的推论可得△DEF∽△BCF,再根据E是AD中点,易求出相似比,从而可求△BCF的面积,再利用△BCF与△DEF是同高的三角形,则两个三角形面积比等于它们的底之比,从而易求△DCF的面积,进而可求▱ABCD的面积.如图所示,
∵四边形ABCD是平行四边形,
∴AD∥BC,AD=BC,
∴△DEF∽△BCF,
∴S△DEF:S△BCF=([DE/BC])2,
又∵E是AD中点,
∴DE=[1/2]AD=[1/2]BC,
∴DE:BC=DF:BF=1:2,
∴S△DEF:S△BCF=1:4,
∴S△BCF=4,
又∵DF:BF=1:2,
∴S△DCF=2,
∴S▱ABCD=2(S△DCF+S△BCF)=12.
故选B.点评:
本题考点: 相似三角形的判定与性质;平行四边形的性质.
考点点评: 本题考查了平行四边形的性质、平行线分线段成比例定理的推论、相似三角形的判定和性质.解题的关键是知道相似三角形的面积比等于相似比的平方、同高两个三角形面积比等于底之比,先求出△BCF的面积.1年前查看全部
- (2014•桓台县一模)溶质质量分数相同的①碳酸钠溶液②氯化钠溶液③稀盐酸④氢氧化钠溶液中,PH最小的是______,分
(2014•桓台县一模)溶质质量分数相同的①碳酸钠溶液②氯化钠溶液③稀盐酸④氢氧化钠溶液中,PH最小的是______,分别向四种溶液中滴加石蕊试液,溶液变蓝色的是______(以上填写序号);把质量各为10g的①、③溶液先后倒入同一个烧杯中,搅拌,过一会儿称量,烧杯内物质质量为______,再向烧杯中滴加石蕊,发现溶液呈现红色,此时溶液中的溶质是______(写化学式).
 vest1001年前1
vest1001年前1 -
 百日登山望烽火 共回答了28个问题
百日登山望烽火 共回答了28个问题 |采纳率89.3%解题思路:根据已有的知识进行分析,pH小于7的溶液呈酸性,pH等于7的溶液呈中性,pH>7的溶液呈碱性,据此解答.①碳酸钠溶液显碱性,pH大于7,②氯化钠溶液显中性,pH等于7,③稀盐酸显酸性,pH小于7,④氢氧化钠溶液显碱性,pH大于7,pH最小的是稀盐酸;碱性溶液能使紫色石蕊试液变蓝;碳酸钠与稀盐酸反应生成二氧化碳气体,二氧化碳气体逃逸到空气中;再向烧杯中滴加石蕊,发现溶液呈现红色,此时溶液显酸性,说明酸过量,因此溶液中的溶质是氯化钠和氯化氢.
故填:③;①④;减小;NaCl、HCl.点评:
本题考点: 溶液的酸碱性与pH值的关系;酸碱指示剂及其性质;盐的化学性质.
考点点评: 本题考查了溶液的酸碱性与pH的关系,完成此题,可以依据已有的知识进行.1年前查看全部
- (2014•桓台县一模)某校的化学兴趣小组制作了一面化学五环旗,图中A、B、C、D、E各代表铁、氧气、氢气、稀硫酸、氢氧
 (2014•桓台县一模)某校的化学兴趣小组制作了一面化学五环旗,图中A、B、C、D、E各代表铁、氧气、氢气、稀硫酸、氢氧化钠溶液中的一种物质.相连环物质间在一定条件下都能发生反应,不相连环物质间不发生反应,且A的相对分子质量小于E的.请填写下列空白:
(2014•桓台县一模)某校的化学兴趣小组制作了一面化学五环旗,图中A、B、C、D、E各代表铁、氧气、氢气、稀硫酸、氢氧化钠溶液中的一种物质.相连环物质间在一定条件下都能发生反应,不相连环物质间不发生反应,且A的相对分子质量小于E的.请填写下列空白:
(1)写出下列物质的化学式:B______ D______;
(2)写出B与C反应的化学方程式2O2+3Fe
Fe3O4点燃 .2O2+3Fe;
Fe3O4点燃 .
(3)上述物质中属于新型燃料的是______. 景红叶1年前1
景红叶1年前1 -
 大江东去浪淘尽了 共回答了19个问题
大江东去浪淘尽了 共回答了19个问题 |采纳率89.5%解题思路:根据铁会与氧气、稀硫酸反应,氧气会与铁、氢气反应,氢气会与氧气反应,稀硫酸会与铁、氢氧化钠反应,氢氧化钠会与稀硫酸反应等知识进行分析.(1)铁会与氧气、稀硫酸反应,氧气会与铁、氢气反应,氢气会与氧气反应,稀硫酸会与铁、氢氧化钠反应,氢氧化钠会与稀硫酸反应,通过分析可知,氢气和氢氧化钠都只会与一种物质反应,A、E是氢气或氢氧化钠中的一种,且A的相对分子质量小于E的,所以A是氢气,E是氢氧化钠,氢气会与氧气反应,氢氧化钠会与硫酸反应,所以B是氧气,D是稀硫酸,剩余的C就是铁,所以B是O2,D是H2SO4;
(2)B与C的反应是铁和氧气在点燃的条件下生成四氧化三铁,化学方程式为:2O2+3Fe
点燃
.
Fe3O4;
(3)通过分析可知,属于新型燃料的是氢气.
故答案为:(1)O2,H2SO4;
(2)2O2+3Fe
点燃
.
Fe3O4;
(3)氢气.点评:
本题考点: 物质的鉴别、推断;氧气的化学性质;金属的化学性质;酸的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.1年前查看全部
- (五f11•桓台县二模)下列事件中是必然事件的是( )
(五f11•桓台县二模)下列事件中是必然事件的是( )
A.一个直角三角形的两锐角分别是40°和50°
B.抛掷一枚硬币,落地后正面朝上
C.当x是实数时,x2≥0
D.长为5cm、5cm、11cm的三条线段能围成一个三角形 左岸生活1年前1
左岸生活1年前1 -
 simone_ma 共回答了30个问题
simone_ma 共回答了30个问题 |采纳率73.3%解题思路:一定会发生的事情称为必然事件.依据定义即可解答.A、是随机事件,故不符合题意,
B、是随机事件,故不符合题意,
C、是必然事件,符合题意,
D、是不可能事件,故不符合题意.
故选C.点评:
本题考点: 随机事件.
考点点评: 本题主要考查了必然事件为一定会发生的事件,解决此类问题,要学会关注身边的事物,并用数学的思想和方法去分析、看待、解决问题,提高自身的数学素养,难度适中.1年前查看全部
- (2014•桓台县一模)下列除杂质的方法不正确的是( )
(2014•桓台县一模)下列除杂质的方法不正确的是( )
选 项 物 质 杂 质 除杂方法 A CaO CaCO3 加适量的稀盐酸 B CaCO3 KNO3 溶解、过滤 C N2 O2 通过灼热的铜网 D NaCl NH4HCO3 加热
A.A
B.B
C.C
D.D 454353611年前1
454353611年前1 -
 幸福小生 共回答了24个问题
幸福小生 共回答了24个问题 |采纳率91.7%解题思路:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.A、CaO和CaCO3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、硝酸钾易溶于水,CaCO3难溶于水,可采取加水溶解、过滤的方法进行分离除杂,故选项所采取的方法正确.
C、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、NH4HCO3在加热条件下生成氨气、水和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:A.点评:
本题考点: 物质除杂或净化的探究;常见气体的检验与除杂方法;盐的化学性质.
考点点评: 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.1年前查看全部
- (2011•桓台县二模)汽车前排座位中安装有高低档的电加热,其工作原理相当于如图所示的电路图,其中R1=12Ω,R2=6
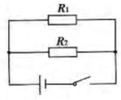 (2011•桓台县二模)汽车前排座位中安装有高低档的电加热,其工作原理相当于如图所示的电路图,其中R1=12Ω,R2=6Ω,闭合开关后,通过R1的电流为2A,求:
(2011•桓台县二模)汽车前排座位中安装有高低档的电加热,其工作原理相当于如图所示的电路图,其中R1=12Ω,R2=6Ω,闭合开关后,通过R1的电流为2A,求:
(1)R1两端的电压;
(2)通过R2的电流.
(3)R1 R2同时工作时的总功率是多少?
项目 数值 整机质量(kg) 5000 标准斗容(m3) 0、5 A最大挖掘深度(m) 3 B最大卸料高度(m) 5 两履带与地面接触的总面积(m2) 4  大a阿宝1年前1
大a阿宝1年前1 -
 katakamen 共回答了17个问题
katakamen 共回答了17个问题 |采纳率88.2%解题思路:由电路图可知,R1、R2并联,根据欧姆定律可求R1两端的电压,即为电源的电压;再根据欧姆定律求出通过R2的电流;根据并联电路的电流特点求出干路电流,利用P=UI求出R1 R2同时工作时的总功率.(1)R1两端的电压:
U1=I1R1=2A×12Ω=24V,
(2)因R1、R2并联,
所以电源的电压:
U=U1=24V;
通过R2的电流为:
I2=[U
R2=
24V/6Ω]=4A;
(3)电路的总电流为:
I=I1+I2=2A+4A=6A,
R1 R2同时工作时的总功率为:
P=UI=24V×6A=144W.
答:(1)R1两端的电压为24V;
(2)通过R2的电流为4A;
(3)R1 R2同时工作时的总功率为144W.点评:
本题考点: 电功率的计算;欧姆定律的应用.
考点点评: 本题考查了并联电路的特点和欧姆定律、电功率的简单计算,因题中条件已给出是一道较为简单的计算题.1年前查看全部
- (2014•桓台县一模)实验室要配制50g溶质质量分数是10%的氯化钠溶液,有如下步骤:
 (2014•桓台县一模)实验室要配制50g溶质质量分数是10%的氯化钠溶液,有如下步骤:
(2014•桓台县一模)实验室要配制50g溶质质量分数是10%的氯化钠溶液,有如下步骤:
(1)计算:需要氯化钠的质量是______,水为______mL(常温下水的密度取1g/mL);
(2)称量:用______ 称取所需氯化钠质量,倒入烧杯; 用______(填“10mL”或“50mL”)的量筒量取所需的水量.量筒内液面接近刻度时的操作是______.读数时,视线要与______保持水平;
(3)溶解:将水倒入烧杯,同时用玻璃棒搅拌至食盐全部溶解.在搅拌过程中,溶液的溶质质量分数会______;食盐全部溶解后,溶质质量分数______.请在图中画出搅拌过程中溶质质量分数随时间变化的曲线(横坐标是时间,纵坐标是溶质质量分数/%);
(4)贴上标签,装瓶保存. 斯文一点1年前1
斯文一点1年前1 -
 wx小光 共回答了15个问题
wx小光 共回答了15个问题 |采纳率73.3%解题思路:(1)根据溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量减去溶质质量计算;
(2)根据称量一定量的固体选用天平和量筒规格的选择依据及用量筒量取一定量的液体的基本操作解答;
(3)根据溶质质量分数的计算公式判断.(1)需要氯化钠的质量为50g×10%=5g;需要水的质量为50g-5g=45g,需要水的体积为45g×1g/mL=45mL;
(2)称量固体用天平;需要水45mL所以选用50mL的量筒,当倒入量筒中的水接近刻度时改用胶头滴管滴加,视线与凹液面的最底部保持水平;
(3)溶解过程中,随着食盐的逐渐溶解,溶液溶质质量分数增大;当食盐全部溶解后再搅拌溶液溶质质量分数不改变;
故答案:(1)5;45;
(2)天平;50;改用胶头滴管滴加;凹液面的最底部;
(3)增大;不改变; .
.点评:
本题考点: 一定溶质质量分数的溶液的配制;测量容器-量筒;称量器-托盘天平.
考点点评: 配制溶液两种常见操作:固体溶质加水溶解,配制步骤计算-称量-溶解;液体加水稀释,配制步骤计算-量取-溶解-装瓶存放.1年前查看全部
- (2014•桓台县一模)下列关于海洋开发利用的说法中不正确的是( )
(2014•桓台县一模)下列关于海洋开发利用的说法中不正确的是( )
A.海洋是个巨大的资源库,人们可以无节制的向她索取各种资源
B.海水“晒盐”是利用蒸发结晶的方法从海水中得到食盐
C.海洋本身就是个巨大的水资源库,如何获取廉价的淡水对缓解淡水危机意义重大
D.海水“制碱”是利用向饱和氨盐水中通入二氧化碳过滤,加热过滤后固体得到纯碱 水123451年前1
水123451年前1 -
 广论_ 共回答了17个问题
广论_ 共回答了17个问题 |采纳率88.2%解题思路:A、海洋是个巨大的资源库,人们不可以无节制的向她索取各种资源,应适量为之;
B、海水“晒盐”是利用蒸发结晶的方法从海水中得到食盐;
C、可以通过淡化海水的方法获得淡水;
D、根据海水制碱的过程分析.A、海洋是个巨大的资源库,人们不可以无节制的向她索取各种资源,应适量为之,故错误;
B、海水“晒盐”是利用蒸发结晶的方法从海水中得到食盐,正确;
C、海洋本身就是个巨大的水资源库,如何获取廉价的淡水对缓解淡水危机意义重大,正确;
D、海水“制碱”是利用向饱和氨盐水中通入二氧化碳过滤,加热过滤后固体得到纯碱,正确.
故选A.点评:
本题考点: 海洋中的资源;结晶的原理、方法及其应用;纯碱的制取.
考点点评: 海洋是巨大的资源宝库,本题主要考查对海洋资源的开发利用.1年前查看全部
- (2014•桓台县模拟)下列变形正确的是( )
(2014•桓台县模拟)下列变形正确的是( )
A.
=x3x6 x2
B.[x+m/x+n]=[m/n]
C.
=x+yx2+y2 x+y
D.[−x+y/x−y]=-1 爱上孔夫子1年前1
爱上孔夫子1年前1 -
 达莱 共回答了22个问题
达莱 共回答了22个问题 |采纳率90.9%解题思路:根据分式的基本性质进行约分即可.A、结果为x4,故本选项错误;
B、[x+m/x+n]不能约分,故本选项错误;
C、
x2+y2
x+y不能约分,故本选项错误;
D、结果是-1,故本选项正确;
故选D.点评:
本题考点: 分式的基本性质.
考点点评: 本题考查了分式的基本性质的应用,主要考查学生对分式的基本性质的理解能力和应用能力.1年前查看全部
- (2014•桓台县模拟)在直角坐标系中,坐标轴上到点P(-3,-4)的距离等于5的点共有______个.
 neptune05111年前1
neptune05111年前1 -
 伪兵 共回答了15个问题
伪兵 共回答了15个问题 |采纳率100%解题思路:利用勾股定理列式求出OP=5,再判断即可.∵点P(-3,-4),
∴OP=
32+42=5,
∴坐标轴上到点P的距离等于5的点有原点和x轴、y轴上一个点,共3个点.
故答案为:3.点评:
本题考点: 坐标与图形性质;勾股定理.
考点点评: 本题考查了坐标与图形性质,勾股定理的应用,求出OP的长是解题的关键.1年前查看全部
- (2014•桓台县一模)化学科学的发展促进了人类社会的进步,提高了人们的生活质量.以下分析不正确的是( )
(2014•桓台县一模)化学科学的发展促进了人类社会的进步,提高了人们的生活质量.以下分析不正确的是( )
A.新材料的开发和利用极大的丰富和方便了人们的生活,但有些废弃材料也对环境造成了不利的影响
B.绿色化学有助于解决环境污染问题,实现人与自然的和谐相处
C.合成药物的研发和使用保障了人体健康
D.化石燃料的直接利用促进了低碳经济的发展 longtaoa1年前1
longtaoa1年前1 -
 gfthr 共回答了13个问题
gfthr 共回答了13个问题 |采纳率100%解题思路:A、从新材料的开发和利用极大的丰富和方便了人们的生活,但有些废弃材料也对环境造成了不利的影响去分析;
B、从绿色化学减少了污染物的产生去分析;
C、从合成药物的研发和使用提供了更多的药物去分析;
D、从化石燃料的直接利用产生了大量的二氧化碳去分析.A、新材料的开发和利用极大的丰富和方便了人们的生活,但有些废弃材料也对环境造成了不利的影响;故正确;
B、绿色化学减少了污染物的产生,实现人与自然的和谐相处;故正确;
C、合成药物的研发和使用提供了更多的药物,保障了人体健康;故正确;
D、化石燃料的直接利用产生了大量的二氧化碳,妨碍了低碳经济的发展;故错误;
由于题目要求选出分析不正确的,故答案为:D.点评:
本题考点: 新材料的开发与社会发展的密切关系;化学的研究领域;绿色化学;常用燃料的使用与其对环境的影响.
考点点评: 化学与生活生产有着紧密联系,学会用所学的化学知识,解决生活中的实际问题.1年前查看全部
- (2011•桓台县二模)如图所示,两支完全相同的试管,内盛等质量的水和酒精.甲管竖直放置,乙管倾斜放置,两管液面相平,比
 (2011•桓台县二模)如图所示,两支完全相同的试管,内盛等质量的水和酒精.甲管竖直放置,乙管倾斜放置,两管液面相平,比较两管中的液体对管底压强的大小p甲______p乙.若h=10cm,则甲试管受到的压强是______Pa.
(2011•桓台县二模)如图所示,两支完全相同的试管,内盛等质量的水和酒精.甲管竖直放置,乙管倾斜放置,两管液面相平,比较两管中的液体对管底压强的大小p甲______p乙.若h=10cm,则甲试管受到的压强是______Pa.  心中的唯一1年前1
心中的唯一1年前1 -
 winzip00 共回答了13个问题
winzip00 共回答了13个问题 |采纳率76.9%解题思路:知道两管液面相平、h相同,知道液体密度的大小关系,根据液体压强公式判断液体对管底压强的大小关系;
知道深度h大小和水的密度,利用液体压强公式求甲试管受到的压强.由题知,h水=h酒精,
∵p=ρgh,ρ水>ρ酒精,
∴两管中的液体对管底压强:
p甲>p乙;
甲试管受到的压强:
p甲=ρ水gh=1×103kg/m3×9.8N/kg×0.1m=980Pa.
故答案为:>;980.点评:
本题考点: 液体的压强的计算;液体的压强的特点.
考点点评: 本题考查了学生对液体压强公式的掌握和运用,知道深度h的含义(从液体内某点到液面的垂直距离)是本题的关键.1年前查看全部
- (2014•桓台县一模)元素观是化学的重要观念之一.下列有关元素的说法不正确的是( )
(2014•桓台县一模)元素观是化学的重要观念之一.下列有关元素的说法不正确的是( )
A.物质都是由元素组成的
B.同种元素的原子核内中子数相同
C.元素周期表中原子序数等于该元素原子核内的质子数
D.原子核内的质子数如果发生变化,则元素种类就会发生变化 yun7891年前1
yun7891年前1 -
 闪啦 共回答了18个问题
闪啦 共回答了18个问题 |采纳率94.4%解题思路:A、根据在宏观上,物质都是由元素组成的考虑;
B、根据决定元素种类的是核内质子数考虑;
C、根据元素周期表中原子序数等于该元素原子核外的电子数考虑.
D、根据决定元素种类的是核内质子数考虑;A、物质是由元素组成的属于宏观解释;故A正确;
B、同种元素的原子核内质子数相同,中子数不一定相同,例如C-12、C-13、C-14,故错;
C、元素周期表中原子序数等于该元素原子核内的质子数;故正确.
D、元素的各类取决于原子核内质子数,原子核内的质子数如果发生变化,则元素种类就会发生变化,故正确;
故选:B.点评:
本题考点: 元素的概念;元素周期表的特点及其应用.
考点点评: 决定元素种类的是质子数,同种元素的原子核内质子数相同,中子数不一定相同,并能灵活运用.1年前查看全部
- (200z•桓台县一模)目前市场上出现的木糖醇(化学式为C中H02O中)是一种新型甜味剂,它不能被细菌分解,添加在6香糖
(200z•桓台县一模)目前市场上出现的木糖醇(化学式为C中H02O中)是一种新型甜味剂,它不能被细菌分解,添加在6香糖里取代糖分,可防止蛀牙.十列关于木糖醇的说法正确的是( )
A.木糖醇中含有5个碳原子、12个氢原子和5个氧原子
B.木糖醇中碳、氢、氧元素的质量比为5:12:5
C.木糖醇中氢元素的质量分数最大
D.木糖醇由碳、氢、氧三种元素组成 上hh迪1年前1
上hh迪1年前1 -
 nanyeorange 共回答了23个问题
nanyeorange 共回答了23个问题 |采纳率100%解题思路:A、根据木糖醇的微观构成进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据化合物中元素的质量分数=[相对原子质量×原子个数/相对分子质量]×100%,进行分析判断.
D、根据木糖醇化学式的含义进行分析判断.A、木糖醇是由木糖醇分子构成的,1个木糖醇分子是由地个碳原子、1e个氢原子和地个氧原子构成的,故选项说法错误.
B、木糖醇中碳、氢、氧三种元素的质量比是(1e×地):(1×1e):(16×地)=1地:三:e0,故选项说法错误.
C、木糖醇中碳原子的相对原子质量之和为1e×地=60,氢原子的相对原子质量之和为1×1e=1e,氧原子的相对原子质量之和为16×地=80,氧元素的相对原子质量之和最大,则氧元素的质量分数最大,故选项说法错误.
D、木糖醇是由碳、氢、氧三种元素组成的,故选项说法正确.
故选:D.点评:
本题考点: 化学式的书写及意义;元素质量比的计算;元素的质量分数计算.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.1年前查看全部
- (2014•桓台县一模)多吃蔬菜、水果可以调节身体健康,提高人体的免疫力,主要原因是蔬菜、水果中富含人体需要的( )
(2014•桓台县一模)多吃蔬菜、水果可以调节身体健康,提高人体的免疫力,主要原因是蔬菜、水果中富含人体需要的( )
A.油脂
B.维生素
C.蛋白质
D.淀粉 kiss520me1年前1
kiss520me1年前1 -
 鼠标碍手 共回答了25个问题
鼠标碍手 共回答了25个问题 |采纳率88%解题思路:从水果蔬菜中含有大量的维生素及维生素的作用去分析.维生素在人体内的含量虽然很小,但它可以起到调节新陈代谢,预防疾病、维持身体健康的重要作用;水果蔬菜中含有大量的维生素;故答案为:B.
点评:
本题考点: 食品、药品与健康食品中的有机营养素.
考点点评: 化学与生活生产有着紧密联系,学会用所学的化学知识,解决生活中的实际问题.1年前查看全部
- (2011•桓台县二模)弹簧测力计下挂着物体A静止,如图所示.请画出物体A所受重力的示意图.(要求:表示出重力的三要素)
 王燕红1年前0
王燕红1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•桓台县一模)水是人类生存的物质基础,也是经济发展的重要资源.下列做法你认为不合理的是( )
(2014•桓台县一模)水是人类生存的物质基础,也是经济发展的重要资源.下列做法你认为不合理的是( )
A.淡水资源有限,需要我们科学合理的开发利用,杜绝浪费和污染
B.为保护地表环境,把污水注入地下排放
C.当前城市实行的雨污分流是减少污染,有效利用资源的重要举措
D.农业生产中的滴水灌溉、科学使用化肥农药都是增收节支的好办法 火星妞妞1年前1
火星妞妞1年前1 -
 deeeepblue 共回答了13个问题
deeeepblue 共回答了13个问题 |采纳率92.3%解题思路:A、科学合理的开发利用,杜绝浪费和污染,可以节约用水,保护水资源;
B、把污水注入地下排放,会污染地下水;
C、雨污分流可以减少污染,有效利用资源;
D、农业生产中的滴水灌溉、科学使用化肥农药,可以增收节支,并且保护环境,A、科学合理的开发利用,杜绝浪费和污染,可以节约用水,保护水资源,合理;
B、把污水注入地下排放,会污染地下水,不合理;
C、雨污分流可以减少污染,有效利用资源,合理;
D、农业生产中的滴水灌溉、科学使用化肥农药,可以增收节支,并且保护环境,合理.
故选B.点评:
本题考点: 保护水资源和节约用水;水资源的污染与防治.
考点点评: 保护水资源,节约用水,人人有责.1年前查看全部
- (2014•桓台县模拟)圆锥的高是4cm,母线长5cm,则其侧面展开图的面积为( )
(2014•桓台县模拟)圆锥的高是4cm,母线长5cm,则其侧面展开图的面积为( )
A.30πcm2
B.24πcm2
C.15πcm2
D.18πcm2 shaziershaoye1年前1
shaziershaoye1年前1 -
 依楚情 共回答了19个问题
依楚情 共回答了19个问题 |采纳率84.2%解题思路:首先根据圆锥的高和母线长求得圆锥的底面半径,然后利用圆锥的侧面积=底面周长×母线长÷2.∵圆锥的高是4cm,母线长5cm,
∴圆锥的底面半径为3cm,
∴则底面周长=6πcm,侧面面积=[1/2]×6π×5=15πcm2.
故选C.点评:
本题考点: 圆锥的计算.
考点点评: 本题利用了圆的周长公式和扇形面积公式求解.解题的关键是了解圆锥的有关元素与扇形的有关元素的对应.1年前查看全部
- (2014•桓台县一模)钢铁的锈蚀主要是铁与空气中的______、______等物质发生化学反应的结果,铁绣的主要成分是
(2014•桓台县一模)钢铁的锈蚀主要是铁与空气中的______、______等物质发生化学反应的结果,铁绣的主要成分是______(写化学式).金属属于______(填“再生”或“不可再生”)资源,废旧金属属于______(填“可回收”或“不可回收”)垃圾,解决金属腐蚀以及有效利用废旧金属的问题,既可以节约资源,又能实现节能减排.请说出一种防止铁制品锈蚀的具体方法______.
 ma045967600541年前1
ma045967600541年前1 -
 yic76c 共回答了19个问题
yic76c 共回答了19个问题 |采纳率94.7%解题思路:根据铁锈蚀的条件、铁锈的主要成分及金属资源回收利用及防止锈蚀的等知识分析回答.钢铁的锈蚀主要是铁与空气中的氧气、水等物质发生化学反应的结果,钢铁锈蚀后生成铁锈(主要成分是氧化铁).金属属于可再生资源,废旧金属属于可回收垃圾,防止铁制品锈蚀的方法有在铁制品表面刷保护漆,防止铁制品受潮等;
故答为:氧气;水;Fe2O3;再生;可回收;在铁制品表面刷保护漆.点评:
本题考点: 金属锈蚀的条件及其防护;铁锈的主要成分;金属的回收利用及其重要性.
考点点评: 本题重在重在考查身边化学,更加贴近生活和生产,可以使学生感受到“生活处处有化学”.这也是中考的题型之一.1年前查看全部
- (2014•桓台县一模)微粒观是化学“三重表征”的内容之一.下列认识错误的是( )
(2014•桓台县一模)微粒观是化学“三重表征”的内容之一.下列认识错误的是( )
A.化学变化中原子核不发生变化,因此化学变化前后元素种类不变
B.化学变化中原子不可分,因此原子是构成物质的最小粒子
C.构成物质的微粒:分子、原子、离子都是不断运动的
D.化学变化的微观实质是构成分子的原子进行重新组合而形成新的分子 股海金牛9101年前1
股海金牛9101年前1 -
 _ice_sun_ 共回答了14个问题
_ice_sun_ 共回答了14个问题 |采纳率92.9%解题思路:A、一切化学反应都遵循质量守恒定律;
B、根据分子、原子的定义进行分析;
C、构成物质的微粒都是在不断运动的;
D、化学反应的过程就是分子分成原子,原子不再分,而是重新组合得新的分子的过程.A、化学变化是核外电子的变化,原子核没有发生变化,则化学变化前后元素种类不变.故A认识正确;
B、在化学反应中分子分成原子,原子再重新组合成新的分子,所以说原子是化学变化中的最小粒子,而不是构成物质的最小粒子.故B认识错误;
C、构成物质的微粒:分子、原子、离子都是不断运动的.故C认识正确;
D、化学变化的实质是分子分成原子,原子再重新组合成新分子的过程.故D认识正确.
故选:B.点评:
本题考点: 元素在化学变化过程中的特点;分子、原子、离子、元素与物质之间的关系;原子的定义与构成;化学反应的实质.
考点点评: 了解分子、原子、离子、元素与物质之间的关系;了解化学变化的实质是解答本题的关键.1年前查看全部
大家在问
- 1请给我一篇关于“春节习俗”的英语作文(80---120字)!谢谢了,大神帮忙啊
- 2英语翻译要求:不要用传统的翻译句子的方法,答案将采用最新颖、搞笑的一种.
- 3初一数学小明、小亮、小颖家恰好依次住在一条笔直的大街上,若小明家离小颖家600米,小刚家到小明家的距离是到小颖家距离的1
- 4《墨池记》中的小问题(请行家指点)
- 5英语翻译
- 6英语.if i ain't got you.中的ain't等于don't吗?
- 7四个水的字读什么?
- 8芳草碧连天(诗一首) 作文
- 9文言文“与”的一词多义不要粘贴的.各位大大具体翻译几个苏子与客泛舟,游于赤壁之下而吾与子之所共食悠悠乎与颢气具知可以战与
- 10波尔模型如何解决了原子结构的稳定性问题
- 11(x+y分之y)-(y²-x²分之xy)
- 12将下面长方形沿AB遍旋转一周,得到什么图形?它的体积是多少立方米?
- 13峨眉山月半轮秋中的半轮是什么意思
- 14、“生活是美好的,但生活也是复杂的.”尤其是未成年人,面对陌生人,一不小心可能就会使自已的合法权益甚
- 15“两个半小时” 到底是两个小时+半个小时 还是两个半小时(半个小时+半个小时)?
