三氯化磷,三氯化硼用杂化轨道理论解释其空间构型.
 吃葡萄吐西瓜皮2022-10-04 11:39:541条回答
吃葡萄吐西瓜皮2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 hh人观hh事 共回答了15个问题
hh人观hh事 共回答了15个问题 |采纳率86.7%- 三氯化磷,价层对数为4,有一对孤对电子,不等性sp3杂化,四面体结构,和氨分子类似.
三氯化硼,价层对数为3,没有孤对电子,平面三角结构,sp2杂化 - 1年前
相关推荐
- 三氯化磷和甲醇反应方程式三氯化磷和甲醇反应生成亚磷酸二甲酯和氯甲烷 这个化学方程式怎么写啊?十万火急!我需要一个最终平衡
三氯化磷和甲醇反应方程式
三氯化磷和甲醇反应生成亚磷酸二甲酯和氯甲烷 这个化学方程式怎么写啊?十万火急!
我需要一个最终平衡的方程式,可能还有一些副产物生成,我这边没有写出来 太监631年前1
太监631年前1 -
 王会才yy 共回答了15个问题
王会才yy 共回答了15个问题 |采纳率80%3CH3OH+PCL3=====C2H7O3P+CH3CL+2HCL1年前查看全部
- 为什么磷元素能形成三氯化磷和五氯化磷,但氮元素只能形成三氯化磷
 wangli8406231年前2
wangli8406231年前2 -
 文化跑 共回答了18个问题
文化跑 共回答了18个问题 |采纳率88.9%1、简单的解释办法:
P和Cl反应,因为P的电负性小于Cl,所以P是正的,而Cl是负的;水解是得到的是HCl;N和P反应,按照鲍林的数据N小于Cl,但实际反应得到的NCl3水解后得到的NH3和HClO,也就是说N是负的;
因为N最多只能是-3价;
2、中等的解释办法:
刚才的方法有些赖皮;用价键理论,NCl5如果成立,那么N势必要和五个Cl共用电子对,这就出现了N周围有10个电子的情况,对于第二周期的N来说这是不可能出现的;但P有3d轨道,外层有9条轨道,可以形成5条共价键;
3、正规的解释方法:
其实真正的还是应该要用分子轨道去解释,最终就是证明NCl5的电子填充在反键轨道上,能量太高,是极其不稳定的;分子轨道的一个很好的地方就是,它不认为哪一种物质绝对不存在,只是说如果有这种物质,势能太高,但是基础知识很多;
看您需要哪种解释方法了1年前查看全部
- 三氯化磷和三氯化硼中所有原子的最外层达到8电子了吗?
三氯化磷和三氯化硼中所有原子的最外层达到8电子了吗?
三氯化磷和三氯化硼中所有原子的最外层达到8电子稳定结构了吗?五氯化磷呢? shuaiaiok1年前4
shuaiaiok1年前4 -
 fychenhb 共回答了17个问题
fychenhb 共回答了17个问题 |采纳率70.6%三氯化磷达到了,但三氯化硼中硼的最外层只够6个电子.五氯化磷不符合要求.1年前查看全部
- 磷与氯气按物质的量1:1.8反应生成的三氯化磷与五氯化磷的物质的量之比是多少?
 samar1年前3
samar1年前3 -
 风不再起 共回答了19个问题
风不再起 共回答了19个问题 |采纳率89.5%反应可视为:2P+3Cl2==2PCl3,PCl3+Cl2==PCl5
设有磷1mol
第一步反应消耗氯气1.5mol,还有0.3mol
故剩余的氯气可继续反应生成0.3mol五氯化磷
由磷守恒,三氯化磷共1-0.3=0.7mol
所以三氯化磷与五氯化磷的物质的量之比是 7:31年前查看全部
- 用杂化轨道理论解释为何三氯化磷是三角锥形,且键角为101°,而三氯化铍却是平面三角形的几何构型.
 这答儿忒1年前1
这答儿忒1年前1 -
 忉力天宫 共回答了16个问题
忉力天宫 共回答了16个问题 |采纳率93.8%三氯化磷中磷原子sp3杂化,三个sp3杂化轨道分别与三个氯原子成键,还有一个sp3杂化轨道上有一对孤对电子.如果算上孤对电子,是近似正四面体构型,键角接近正四面体的109.5度.
三氯化铍中铍原子是sp2杂化,三个sp2杂化轨道分别与三个氯原子成键,呈平面正三角型的构型.1年前查看全部
- 除去三氯化磷中的亚磷酸
 夜舞婆娑1年前1
夜舞婆娑1年前1 -
 凄然北望 共回答了15个问题
凄然北望 共回答了15个问题 |采纳率93.3%三氯化磷沸点76度,亚磷酸沸点200度(分解),利用沸点的差异,在80度进行真空分馏,控制好馏份.1年前查看全部
- 电子式 帮忙找一下氢气 氧气 卤素气体 氮气 一氧化碳卤化氢 二氧化碳 二硫化碳 水 硫化氢 三氟化硼 氨气 三氯化磷
电子式 帮忙找一下
氢气 氧气 卤素气体 氮气 一氧化碳
卤化氢 二氧化碳 二硫化碳 水 硫化氢 三氟化硼 氨气 三氯化磷 甲烷
四氯化碳 SiH4 四氟化硅 四氯化硅
谢谢了
 彭转转941年前1
彭转转941年前1 -
 云想衣裳 共回答了20个问题
云想衣裳 共回答了20个问题 |采纳率95%在化学反应中,一般是原子的最外层电子数目发生变化。为了简便起见,化学中常在元素符号周围用小黑点“·”或小叉“×”来表示元素原子的最外层电子,相应的式子叫做电子式。
一、原子的电子式
原子的最外层有多少个电子就在其元素符号周围画多少个小黑点“·”或小叉“×”。原子的最外层电子有成对电子和单电子之别,写原子的电子式时,应使元素符号周围各个方向的电子尽量均匀分布。严格地讲,成对电子要排在同一个方位上,单电子分别排在不同的方位上。如锂原子写成·Li(或×Li)、氮原子写成··。
二、离子的电子式
阳离子 简单的阳离子(一般指单原子形成的阳离子)是元素原子失去最外层电子后形成的,此时若原最外层没有电子,其电子式就是它的离子符号,如钠离子写成Na+、钡离子写成Ba2+;复杂的阳离子是原子团失去一个或几个电子形成的,不仅要画出各原子的最外层电子以及它们的成键关系,而且要用“?眼 ?演”将原子团括起来,并在其右上角标明所带的正电荷数,电子式中的小黑点和小叉总数为原子团中各原子最外层电子总数减去原子团所带的电荷数值。如铵根离子写成?眼H H?演。
阴离子 简单阴离子,一般最外层是2个电子或8个电子的稳定结构,在元素符号周围画出最外层电子,并用“?眼 ?演”将其括起来,并在右上角标明所带的负电荷数,其中小黑点和小叉总数为各原子的最外层电子总数加上所带的电荷数值的绝对值,如氯离子的电子式为?眼 ?演;复杂的阴离子,要根据各原子的成键关系画出所有原子的最外层电子,然后用“?眼 ?演”将它们括起来,并在右上角标明所带的负电荷数,其小黑点和小叉总数为原子团中各原子的最外层电子数之和加上所带的电荷数值的绝对值。如氢氧根离子?眼 H?演。
三、单质分子的电子式
根据原子的最外层电子数和分子的组成判断出成键电子数和各原子的成键关系,再画出所有原子的最外层电子。如H2写成HH。
四、化合物的电子式
共价化合物 原子间通过共价键形成的化合物,原子间的单键即为一对共用电子,若为双键则有两对共用电子,依此类推。一般来说,8减去原子的最外层电子数等于该原子的成键数目(H、P例外)。写电子式时,共用电子对写在两成键原子之间,未成键的最外层电子,也应在元素符号周围画出。在共价化合物中,各元素原子最外层一般都达到了8电子(或2电子)的稳定结构。如HCl写成H 、H2O2写成H H。
离子化合物 由阴、阳离子的电子式组成,但相同的离子不能合并,若有多个阳离子或多个阴离子,书写时要使每一个离子都与带相反电荷的离子直接相邻,并注意对称、规范。如K2S写成K+?眼 ?演 K+,NaOH写成Na+?眼 H ?演 。
五、游离基的电子式
游离基是由分子失去一个或多个原子所形成的活性基团,它显电中性,电子式中的小黑点和小叉总数为各原子的最外层电子数之和。如甲基的电子式为H C H,羟基的电子式为 H。1年前查看全部
- 苯与三氯化磷以三氯化铝为催化剂反应后为什么要加入氯化钾
苯与三氯化磷以三氯化铝为催化剂反应后为什么要加入氯化钾
据说是为了把产物分离出来,但是原理是什么 2005爱过你1年前1
2005爱过你1年前1 -
 爱与不爱都痛苦 共回答了18个问题
爱与不爱都痛苦 共回答了18个问题 |采纳率88.9%我认为氯化钾的作用是提供氯离子,与三氯化铝形成AlCl4-,从而起到催化作用1年前查看全部
- 化学过量计算16g含磷77.5%的某红磷在56.8g氯气中充分燃烧.问生成三氯化磷多少克?(设杂质不参与反应)
 safdghawrjkgrsth1年前7
safdghawrjkgrsth1年前7 -
 gg掘烂地XO 共回答了23个问题
gg掘烂地XO 共回答了23个问题 |采纳率95.7%P的量:16g*77.5%/31g/mol=0.4mol
Cl2的量:56.8g/71g/mol=0.8mol
第一步:生成PCl3
从以上计算,可是Cl2能使P完全反应
用去Cl2的量为:0.4*3/2=0.6mol
同时生成的PCl3的量为0.4mol
第二步:生成的PCl3与过量Cl2反应生成PCl5
剩余的Cl2量为0.8-0.6=0.2mol
因此,反应掉的PCl3的量为0.2mol
剩余的PCl3的量为0.4-0.2=0.2mol
所以生成PCl3的量为0.2mol*(31+35.5*3)g/mol=27.5g1年前查看全部
- 特殊双水解方程式氮化镁Mg3N2 三氯化磷PCl3 五氯化磷PCl5 氯化硅SiCl4 CaC2
 悠游小舟1年前1
悠游小舟1年前1 -
 badnoon 共回答了16个问题
badnoon 共回答了16个问题 |采纳率75%Mg3N2+6H2O=3Mg(OH)2$+2NH3#($沉淀,#气体,这是少量水的情况,水多氨气溶于水,不用气体符号,以下自己看着办不一一赘述)
PCl3+3H2O=H3PO3+3HCl
PCl5+5H2O=H3PO4+5HCL
SiCL4+3H2O=H2SiO4$+4HCl
CaC2+2H2O=Ca(OH)2$+C2H2#(制乙炔)
(pcl3那个有点忘了,好像没有这个双水解,H3PO3很不稳定,亚磷酸在水里溶解度很高)1年前查看全部
- 判断三氯化铁,氯化亚铁,五氯化磷,三氯化磷的熔点,为什么
判断三氯化铁,氯化亚铁,五氯化磷,三氯化磷的熔点,为什么
是四个一起比较 demo**1年前3
demo**1年前3 -
 月夜阳光 共回答了16个问题
月夜阳光 共回答了16个问题 |采纳率93.8%按顺序升高:三氯化磷 五氯化磷 三氯化铁 氯化亚铁,因为,化合物的共价倾向越明显则溶沸点越低.楼下的那位仁兄,这几个化合物里面只有氯化亚铁是较明显的离子化合物肯定熔点最高,剩下的三者中氯化铁属于金属氯化物,所以熔点高于剩下的二者,对于磷我们知道共价化合物分子间仅受到范德华力,其大小与分子量成正比(相同元素组成的情况下),所以五氯化磷大于三氯化磷~
不想多说,“宝木沉香”我哪句说错了吧?你自己说的和我的有何区别?你不是也承认三氯化铁的共价倾向大于氯化亚铁?然后再拿金属氯化物和非金属氯化物比较,接着拿两个非金属氯化物比较范德华力而得到答案么?我哪句不合适了?自己也是读过大学的吧,你觉得我有错误就指出来啊,自己又说不出= =不知道在纠结些什么.我勒个去的1年前查看全部
- 关于化学的一些结构问题三氯化磷是三角锥结构,甲烷是正四面体结构,据说,注意是据说 三角锥就是四面体,可是甲烷和三氯化磷分
关于化学的一些结构问题
三氯化磷是三角锥结构,甲烷是正四面体结构,据说,注意是据说 三角锥就是四面体,可是甲烷和三氯化磷分子数不同啊?分子结构中三角锥三棱锥四面体到底都有什么区别呀? 蓝心爱玄1年前3
蓝心爱玄1年前3 -
 gg猪扎西 共回答了21个问题
gg猪扎西 共回答了21个问题 |采纳率85.7%甲烷分子有5个原子,一个C连着4个H,每一个C-H键都是相同的,且C没有未共用电子对,所以甲烷的分子结构是个均匀的正四面体结构,C在中心,4个H为正四面体的4个顶点.三氯化磷分子有4个原子,1个P连着4个Cl,每一个P-Cl键都是相同的,所以三氯化磷的结构本应是正三角形,一个P在中心,3个Cl为3个顶点.但是由于P原子有未共用电子对,具有空间效应,因而对结构具有压迫作用,将整个三角形给扯了起来,成为了三角锥形.又如三氯化硼,它和三氯化磷的区别只在于B原子没有未共用电子对,所以其结构为正三角形,一个B在中心,3个Cl为3个顶点.1年前查看全部
- 求解PCl3(三氯化磷),PCl5(五氯化磷),[PCl6]- 的空间结构式
 八月结1年前1
八月结1年前1 -
 Rubylily0914 共回答了20个问题
Rubylily0914 共回答了20个问题 |采纳率95%PCl3 sp3杂化 三角锥
PCl5 sp3d杂化 三角双锥
[PCl6](-) sp3d2杂化 正八面体1年前查看全部
- [紧急求助]三氯化磷和氯气反应生成什么?
 tata_mo1年前4
tata_mo1年前4 -
 夏末虫鸣 共回答了19个问题
夏末虫鸣 共回答了19个问题 |采纳率78.9%少量的磷和氯气反应生成三氯化磷
大量的磷和氯气反应生成五氯化磷
大量的磷和氯气反应生成五氯化磷,怎么理解呢?你可以这么认为:
首先磷和氯气反应生成三氯化磷,之后三氯化磷和多余的氯气生成五氯化磷1年前查看全部
- 三氯化磷各原子最外层电子为什么不满足8电子稳定结构?
三氯化磷各原子最外层电子为什么不满足8电子稳定结构?
如题,还有 BF3
奇怪,那我做的题目的答案不是这个啊,怎么回事 yanjin050311年前1
yanjin050311年前1 -
 yayoyu 共回答了27个问题
yayoyu 共回答了27个问题 |采纳率92.6%我现在也是一高三学生!我们马上就要上大学了!安逸!
PCL3都满足!有个方法可以判断:如果该元素的化合价的绝对值和他的族序数相加的和是8,那么这就是满足8电子稳定.
BF3你自己判断嘛!很容易的1年前查看全部
- 用杂化轨道理论解释:硫化氢分子(H2S)的键角为什么为92度,而三氯化磷分子(PCl3)键角为102度
用杂化轨道理论解释:硫化氢分子(H2S)的键角为什么为92度,而三氯化磷分子(PCl3)键角为102度
<<普通化学>>第34页,化学工业出版社 wenrouzhanshen1年前1
wenrouzhanshen1年前1 -
 allenyl 共回答了23个问题
allenyl 共回答了23个问题 |采纳率73.9%H2S的S几乎没有杂化,S直接使用3p轨道和H的1s轨道重叠成键,键角仍是3p轨道的90°左右.
PCl3的P采用sp3杂化,形成接近正四面体的电子结构,但由于孤对电子对成键电子的斥力较大,3个P-Cl相比于正四面体更远离孤对电子,键角比正四面体的109.5°略小.1年前查看全部
- 三氯化磷和五氯化磷的形成区别,以及他们的颜色和状态
 秀-CooL1年前1
秀-CooL1年前1 -
 aardvark2003 共回答了21个问题
aardvark2003 共回答了21个问题 |采纳率85.7%当Cl2不足时:2P+3Cl2=2PCl3(液态)
当Cl2充足时:PCl3+Cl2=PCL5(固态)
所以才会有白色烟(PCL5)雾(PCL3)
三氯化磷
1.英 文 名:Phosporus Trichloride
2.分 子 式:PCL3
3.分 子 量:137.3
4.CAS No.:7719-12-2
5.物化性质:
无色透明的发烟液体,相对密度1.574,熔点-112℃,沸点75.5℃,能溶于乙醚、苯、二硫化碳和四氯化碳,在潮湿空气中发烟,有强烈的刺激性,遇水发生剧烈分解,放出氯化氢气体,有毒、腐蚀性强.
6.产品用途:
主要用于制造敌百虫、甲胺磷和乙酰甲胺磷以及稻瘟净等有机磷农药的原料.医药工业用于生产磺胺嘧啶(S.D)、磺胺五甲氧嘧啶(S.M.D).染料工业用于色酚类的缩合剂.
五氯化磷
1.物质的理化常数:
国标编号 81042
CAS号 10026-13-8
中文名称 五氯化磷
英文名称 Phosphorus pentachloride
别 名
分子式 PCl5 外观与性状 淡黄色结晶,有刺激性气味,易升华
分子量 208.23 沸 点 升华
熔 点 148℃(加压) 溶解性 溶于水、二硫化碳、四氯化碳
密 度 相对密度(水=1)3.60 稳定性 稳定
危险标记 20(酸性腐蚀品) 主要用途 用作氯化剂,催化剂,脱水剂1年前查看全部
- 一个超难的化学方程式的书写.甲磷酸一甲酯,与三氯化磷及氯气反应得甲基氧二氯化磷甲基氧二氯化磷+2-二异丙氨基乙硫醇钠+乙
一个超难的化学方程式的书写.
甲磷酸一甲酯,与三氯化磷及氯气反应得甲基氧二氯化磷
甲基氧二氯化磷+2-二异丙氨基乙硫醇钠+乙醇得β—二异丙氨基乙基甲基硫代磷酸乙酯.
请帮我把这两个化学方程式配平. 游离微笑的鱼1年前1
游离微笑的鱼1年前1 -
 aozz555 共回答了29个问题
aozz555 共回答了29个问题 |采纳率93.1%一
2CH3P(OH)OCH3+4PCl3+3Cl2==3CH3POCl2+3POCl3+CH3Cl+2HCl
生成的副产物三氯氧磷难以除去
所以建议使用格利雅试剂
三氯氧磷加少量镁粉在乙醚环境中得POCl2MgCl
再与氯甲烷反应而成甲基氧二氯化磷
二
CH3POCl2+(i-Pr)2NC2H4SNa+EtOH=VX+2HCl
其中Et表示乙基,i-Pr表示异丙基
但这里的硫原子极易在空气中氧化得亚硫砜或硫砜类化合物
不如做环沙林好
甲基氧二氯化磷加无水氢氟酸加环己醇(环己醇由苯酚和氢气在镍催化下制的)
总之这类实验还是不建议你做
那个比它们毒性都弱的沙林仅需1公斤就可以杀死一百万人
你要考虑后果
神经毒素不是闹着玩的
我们学化学的目的是为了造福人,懂吗1年前查看全部
- PCl3三氯化磷为什么是分子晶体?
 大王胡子1年前1
大王胡子1年前1 -
 tzh_dnr 共回答了17个问题
tzh_dnr 共回答了17个问题 |采纳率82.4%CaCl2,NaCl,是离子晶体,剩下的是分子晶体.金属化合物一般分子间是离子键.除了AlCl3,而非金属化合物一般是共价键,除了NH3Cl1年前查看全部
- 三氯化氮与五氯化氮,三氯化磷与五氯化磷,这两组中分别那个更稳定?为什么?
三氯化氮与五氯化氮,三氯化磷与五氯化磷,这两组中分别那个更稳定?为什么?
本问题是竞赛要求的内容,答案上有一句说五氯化氮中氮原子是激发态,所以能形成5个键,但是不稳定。 8fkpn1年前1
8fkpn1年前1 -
 hasemiayko 共回答了21个问题
hasemiayko 共回答了21个问题 |采纳率95.2%不存在NCl5,
NCl3是易爆的危险品
PCl3,PCl5都还算稳定,但是前者会与氧化剂反应相对不如后者稳定1年前查看全部
- 五氧化二磷,三氯化磷,五氯化磷的电子式及结构式,
 cfuch1年前1
cfuch1年前1 -
 简单呆呆 共回答了15个问题
简单呆呆 共回答了15个问题 |采纳率86.7%电子式太麻烦了吧.点死了
气态P2O5:
O═P—O—P═O
…║………║
…O………O
固态时是P4O10分子
4P就是正四面体的四个顶点,6O在六条棱边上(成一定角度),另外4O在4P的正外侧以双键结合
PCl3:
Cl—P—Cl
……│
……Cl
PCl5:
……Cl
……|
Cl—P—Cl
…╱╲
Cl……Cl
//…为占位符号
电子式就把线改成两点:1年前查看全部
- 脂肪酰氯的制备哪们高手能帮我解决:用植物油与三氯化磷可以反就生成混合脂肪酰氯吗?请详细讲试验过程及要点
 li-kevin1年前1
li-kevin1年前1 -
 明阳天下 共回答了14个问题
明阳天下 共回答了14个问题 |采纳率85.7%植物油的主要成分是脂肪,而脂肪由饱和脂肪酸、单不饱和脂肪酸、多不饱和脂肪酸及甘油组成.先用氢氧化钠溶液水解植物油,分离上层溶液得到脂肪酸,再加入三氯化磷,然后加热(温度不要太高)进行反应,得到混合脂肪酰氯和磷酸.(得到的一分子脂肪酸可与三分子三氯化磷反应)
酰氯非常容易水解,所含无机杂质不能水洗除去,只能用蒸馏方法分离.三氯化磷适用于制备低沸点酰氯,可便于蒸馏出来.1年前查看全部
- 氯气如何生成三氯化磷,四氯化磷
 妖精7851年前2
妖精7851年前2 -
 流浪的青云 共回答了16个问题
流浪的青云 共回答了16个问题 |采纳率93.8%磷足量2P+3Cl2==2PCl3
磷不足:2P+5Cl2==2PCL5
应该没有四氯化磷吧1年前查看全部
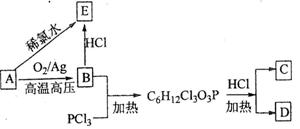
- 2010海南高考化学第16题.主要想问一下三氯化磷与B反应生成中间那个产物的方程式.
2010海南高考化学第16题.主要想问一下三氯化磷与B反应生成中间那个产物的方程式.
16、(8分)有机物A可作为植物生长调节剂,为便于使用,通常将其制成化合物D
,D在弱酸性条件下会缓慢释放出A.合成D的一种方法及各物质间
转化关系如下图所示:
请回答下列问题:
(1)A的名称是_____________,A与氯气反应可生成C,C的名称是_____________;
(2)经测定E中含有氯元素,且E可以与乙酸发生酯化反应,则E的结构简式为_________,由A直接生成E的反应类型是_____________;
(3)在弱酸性条件下,D与水反应生成A的化学方程式为_________________________;
(4)写出E的两个同分异构体的结构简式__________________________.
 小玫15841年前1
小玫15841年前1 -
 世纪飞鹰 共回答了14个问题
世纪飞鹰 共回答了14个问题 |采纳率100%那么我就直接说 B +PCl3
B为 环氧乙烷 3 (CH2)2O +PCl3 → (ClCH2CH2O)3P 即 C6H12Cl3O3P
一个P上连 3个 ClCH2CH2O- 基团 ,机理是环氧乙烷的O进攻Pcl3中的P 而开环1年前查看全部
- 用杂化轨道理论解释为何三氯化磷是三角锥形,且键角为101°,而三氯化硼却是平面三角形的几何构型.
 xunzhaoqiji1年前1
xunzhaoqiji1年前1 -
 hkyxhy 共回答了8个问题
hkyxhy 共回答了8个问题 |采纳率87.5%磷有五个电子,棚只有三个1年前查看全部
- 磷与氯气反应生成三氯化磷和五氯化磷现象一样吗?
 咿呀咿1年前1
咿呀咿1年前1 -
 yongzhi100 共回答了12个问题
yongzhi100 共回答了12个问题 |采纳率100%不一样
PCl3液体,白雾
PCl5固体,白烟1年前查看全部
- 为什么不能用过滤的方法分解 三氯化磷与五氯化磷
 冰面上的奶牛1年前1
冰面上的奶牛1年前1 -
 雪碧可可 共回答了20个问题
雪碧可可 共回答了20个问题 |采纳率95%三氯化磷:无色澄清液体
五氯化磷:白色固体
两者状态不同
PCl3和PCl5都极易和空气中的H2O发生水解反应
释放出大量HCl白雾
不可以在空气中有过滤方法分开1年前查看全部
- 一道不懂的化学题6、下列分子中所有原子不能都满足最外层8电子结构的是( )A、光气(COCl2) B、白磷 C、三氯化磷
一道不懂的化学题
6、下列分子中所有原子不能都满足最外层8电子结构的是( )
A、光气(COCl2) B、白磷 C、三氯化磷 D、三氟化硼 思念未知1年前4
思念未知1年前4 -
 ying_su 共回答了15个问题
ying_su 共回答了15个问题 |采纳率93.3%其中硼不满足,其最外层为3个电子,每个电子与一个氟原子形成一对共用电子对,一共是三对,6个.
遇到这种问题先看氢元素和硼元素,这两个元素是无论如何也不可能形成8电子稳定结构的,再看有没有五氯化磷、一氧化碳、氮氧化物之类的特殊结构.这类结构只要画出电子式就一目了然了1年前查看全部
- 红磷放在氯气中燃烧,若磷和氯气按物质的量之比为1∶1.8混合,充分反应后生成物中三氯化磷与五氯化
红磷放在氯气中燃烧,若磷和氯气按物质的量之比为1∶1.8混合,充分反应后生成物中三氯化磷与五氯化
红磷放在氯气中燃烧,若磷和氯气按物质的量之比为1∶1.8混合,待充分反应后生成物中三氯化磷与五氯化磷的物质的量之比为 大黑牡丹1年前1
大黑牡丹1年前1 -
 烟雨江南雪 共回答了25个问题
烟雨江南雪 共回答了25个问题 |采纳率96%设磷1mol那么氯气1.8mol,
那么直接设生成的物质中有xmol三氯化磷,ymol三氯化磷
由x+y=1,3x+5y=3.6
解得x=0.7,y=0.3
所以物质的量之比为7:31年前查看全部
- 2.0摩尔三氯化磷和1.0摩氯气充入体积 不变的固定容器中生成五氯化磷.达平衡时.
2.0摩尔三氯化磷和1.0摩氯气充入体积 不变的固定容器中生成五氯化磷.达平衡时.
五氯化磷为0.4摩尔.如果此时移走1.0摩尔三氯化磷和0.5摩氯气.在相同温度再达平衡时.五氯化磷的物质的量为A0.40摩尔B0.20摩尔 C小于0.20摩尔D大于0.20摩.小于0.40摩尔.为什么选C laowang1231年前2
laowang1231年前2 -
 xing8008 共回答了8个问题
xing8008 共回答了8个问题 |采纳率87.5%PCl5是固体,浓度越大,平衡越向体积减少方移动,所以全部减半时平衡时浓度没有浓度大时的多1年前查看全部
- 为什么PCl3(三氯化磷)没有PCl5(五氯化磷)稳定?
 连珠泡泡1年前1
连珠泡泡1年前1 -
 xiepinzan 共回答了22个问题
xiepinzan 共回答了22个问题 |采纳率95.5%三氯化磷中磷原子的p轨道上还有一对孤对电子,而五氯化磷中磷原子的p轨道上的一对孤对电子也与氯成键,所以五氯化磷更稳定1年前查看全部
- 1.1mol氯气跟白磷完全反应生成三氯化磷和五氯化磷,其物质的量比为2:1,则生成物中五氯化磷的物质的量为( )
1.1mol氯气跟白磷完全反应生成三氯化磷和五氯化磷,其物质的量比为2:1,则生成物中五氯化磷的物质的量为( )
A.0.4mol
B.0.1mol
C.0.2mol
D.0.05mol lalaking1591年前1
lalaking1591年前1 -
 小奇0129 共回答了18个问题
小奇0129 共回答了18个问题 |采纳率94.4%解题思路:1.1mol氯气跟白磷完全反应生成三氯化磷和五氯化磷,其物质的量比为2:1,设五氯化磷的物质的量为xmol,根据三氯化磷和五氯化磷的物质的量之比知三氯化磷的物质的量为2xmol,根据氯原子守恒计算五氯化磷的物质的量.1.1mol氯气跟白磷完全反应生成PCl3、PCl5,其物质的量比为2:1,设五氯化磷的物质的量为xmol,根据三氯化磷和五氯化磷的物质的量之比知三氯化磷的物质的量为2xmol,根据氯原子守恒得2xmol×3+xmol×5=1.1mol,x=0.1,所以五氯化磷的物质的量为0.1mol,
故选B.点评:
本题考点: 化学方程式的有关计算.
考点点评: 本题考查了物质的量的计算,根据氯原子守恒进行计算即可,题目难度不大.1年前查看全部
大家在问
- 1图书馆在公用电话的对面 求学霸翻译英语
- 2今年六年级期末考最难的题是哪种?
- 3根据下边的概念图可知,下列叙述正确的是( )
- 4甲图是某科研所在探究“影响植物光合作用速率的因素”的实验装置图.乙图是某植物在恒温(30℃)时光合作用速率与光照强度的关
- 5要除去硫酸钠中混有的少量碳酸钠,应加入的物质是
- 63又8分之5减去2又9分之8怎样简便计算?
- 7鲶鱼效应在不在生物科学的范围中呢?
- 8如图已知三角形abc中,Ac=BC,F为底边AB上一点,BF:AF=m:n(m>0,n>0)取cF
- 9哥哥身高1.68米,在地面上的影子长是2.1米,同一时间测得弟弟的影子长1.8米,则弟弟身高是______米.
- 10一点一横长,一撇到南洋,左长右长,两边脚丝丝.马字站中堂.一点一勾腔如题 谢谢了
- 11屠格涅夫 乞丐为什么要感谢这位作家呢?
- 12在数学符号中,大括号像一张弓,小括号像弯弯的月牙,那中括号像什么
- 13童童是一名四年级的小朋友,可是他没见过大城市是什么样子,请你为他写一封信吧写作文急需
- 14我喜欢数学,为什么最近有点怕数学了 已经休息了两天了,还是不怎么想学.
- 15求定积分:∫(上标是+∞ ,下标是-∞)dx/[(1+x^2)^(3/2)]=
