铝热反应的强光是谁发出的?是引燃剂Mg?铝热反应为什么要加入滤纸?铝热反应是吸热反应还是放热反应?
 老苍鹰2022-10-04 11:39:542条回答
老苍鹰2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 lf186ceo 共回答了15个问题
lf186ceo 共回答了15个问题 |采纳率100%- 反应本身放出的.好比你问氢气氧气燃烧放出的光是谁发的一样,
镁是耀眼的白光,跟铝热反应放的光不太一样.
滤纸折成一个碗状,就是为了盛那些试剂而已.
放热,铝热反应生成的铁是融化的. - 1年前
 lys1858 共回答了1个问题
lys1858 共回答了1个问题 |采纳率- 强光是由于铝剧烈燃烧产生的,因为其燃烧温度达到三千多度。至于虑纸是为了观察该反应的生成物,当虑纸被烧穿,熔融物落入蒸发皿的沙中,出去熔渣,可以观察到是铁珠。该反应是放热反应,放出强光和强热。
- 1年前
相关推荐
- 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀
 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Ⅰ.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金.你认为他的解释是否合理?答:______(填“合理”或“不合理”)物质 Al Al2O3 Fe Fe2O3 熔点/℃ 660 2054 1535 1462 沸点/℃ 2467 2980 2750 --
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是______,反应的离子方程式为______.
(3)实验室溶解该熔融物,下列试剂中最好的是______(填序号).
A.浓硫酸B.稀硫酸C.稀硝酸D.氢氧化钠溶液
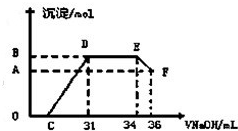
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.则B点对应的沉淀的物质的量为______mol. sknyea1年前1
sknyea1年前1 -
 wjh-jack 共回答了19个问题
wjh-jack 共回答了19个问题 |采纳率78.9%解题思路:Ⅰ.(1)铝的熔点比铁低,生成铁和液态铝一起滴落至盛有沙子的容器中形成合金;
(2)根据铝与NaOH溶液反应的性质设计实验方案;
(3)A.浓硫酸易使铁、铝钝化,不能使合金溶解;
B.活泼金属与稀硫酸反应;
C.稀硝酸与金属反应生成污染性气体;
D.铁不与NaOH溶液反应;
Ⅱ.沉淀的总量可根据NH4+的量,根据NH4++OH-═NH3•H2O 得出n(NH4+),根据氧化还原反应,N元素由+5价变为-3价,而金属都由0价变为+3价,可以运用电子守恒得出金属的物质的量.Ⅰ.(1)铝的熔点比铁低,生成铁和液态铝一起滴落至盛有沙子的容器中形成合金,所以铝热反应所得到的熔融物应是铁铝合金,
故答案为:合理;
(2)铝与NaOH溶液反应生成气体,反应的化学方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,所以可用NaOH溶液检验所得的块状熔融物中含有金属铝,
故答案为:NaOH溶液;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)A.浓硫酸易使铁、铝钝化,不能使合金溶解,故A错误;
B.活泼金属与稀硫酸反应,熔融物可溶解于稀硫酸中,故B正确;
C.稀硝酸与金属反应生成污染性气体,不是最佳选择,故C错误;
D.铁不与NaOH溶液反应,不能将熔融物全部溶解,故D错误;
故答案为:B;
Ⅱ.图中OC段没有沉淀生成,此阶段发生的离子方程式为H++OH-=H2O;在DE段沉淀的物质的量没有变化,应为NH4+和OH-的反应,此阶段发生反应的离子方程式为NH4++OH-═NH3•H2O;根据NH4++OH-═NH3•H2O 得:n(NH4+)=(34-31)×10-3L×4mol/L=0.012 mol,根据氧化还原反应,N元素由+5价变为-3价,而金属都由0价变为+3价,可以运用电子守恒得出金属的物质的量为:[0.012mol×8/3]=0.032mol,所以生成沉淀的物质的量为0.032mol,
故答案为:0.032.点评:
本题考点: 探究铝热反应.
考点点评: 本题考查较为综合,涉及铝热反应,金属与硝酸的反应、离子方程式的书写、氧化还原反应、化学计算等知识点,属于中等难度试题;解答此题关键是判断出硝酸的还原产物以及电子转移守恒的运用.1年前查看全部
- 铝热反应能否冶炼钨?
 feeel_cn1年前3
feeel_cn1年前3 -
 guoyu03 共回答了15个问题
guoyu03 共回答了15个问题 |采纳率100%楼上说错了
不可以的
WO3相当稳定,以至于即使反应,放热也不足以熔化W1年前查看全部
- 冶炼金属常用以下几种方法:①以C、CO或H 2 做还原剂还原 ②以较活泼金属Na、Mg等还原 ③利用铝热反应原理还原 ④
冶炼金属常用以下几种方法:①以C、CO或H 2 做还原剂还原 ②以较活泼金属Na、Mg等还原 ③利用铝热反应原理还原 ④电解法 ⑤热分解法
下列金属各采用哪种方法还原最佳。
(1)Fe、Zn、Cu等中等活泼金属________。
(2)Na、Mg、Al等活泼或较活泼金属________。
(3)Hg、Ag等不活泼金属________。
(4)V、Cr、Mn、W等高熔点金属________。
(5)K、Rb、Cs、Ti等金属通常还原方法是________。 猫筱鹤1年前0
猫筱鹤1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2005•岳阳)火车提速后,要求使用大量超长无缝钢轨.工人在野外常用铝热反应:2Al+Fe2O3 高温
(2005•岳阳)火车提速后,要求使用大量超长无缝钢轨.工人在野外常用铝热反应:2Al+Fe2O3
2Fe+Al2O3所得到的熔化的铁水来修补钢轨裂缝.下列有关该反应的说法中正确的是( )高温 .
A.Fe2O3是氧化剂
B.Fe是氧化产物
C.Al是氧化剂
D.这是一个复分解反应 水若耶1年前1
水若耶1年前1 -
 boliwawa668 共回答了16个问题
boliwawa668 共回答了16个问题 |采纳率87.5%解题思路:物质跟氧发生的反应叫氧化反应;氧化物中的氧被夺去的反应叫还原反应;发生氧化反应的物质做还原剂,发生还原反应的物质做氧化剂.A、氧化铁在反应中失去了氧,发生了还原反应,做氧化剂.正确;
B、铁是还原产物.故选项错误;
C、铝发生了氧化反应,做还原剂.故选项错误;
D、该反应属于氧化还原反应,不属于复分解反应.故选项错误.
故选A.点评:
本题考点: 氧化反应;复分解反应及其应用.
考点点评: 解答本题要充分理解氧化还原反应的含义,只有这样才能对关于氧化还原反应方面的问题做出正确的判断.1年前查看全部
- 请问氧化铝是金属氧化物吗?在铝热反应中能用三氧化二铝代替金属氧化物吗?
 lvvvv121年前2
lvvvv121年前2 -
 283432312 共回答了14个问题
283432312 共回答了14个问题 |采纳率92.9%氧化铝是金属氧化物.
在铝热反应中能用三氧化二铝代替金属氧化物吗?
不能.1年前查看全部
- 下列变化过程,不属于化学变化的是( ) A.石油的裂化 B.煤的干馏 C.石油的分馏 D.铝热反应
 xhsang1年前1
xhsang1年前1 -
 ganyan2004 共回答了18个问题
ganyan2004 共回答了18个问题 |采纳率72.2%A.石油裂化是由大分子经裂化而得的小分子的汽油,属于化学变化,故A错误;
B.煤的干馏是指将煤隔绝空气加强热使之分解的过程,属于化学变化,故B错误;
C.石油的分馏是根据物质的沸点不同进行分离,物理变化,故C正确;
D.铝热反应有新物质铁生成,属于化学变化,故D错误.
故选C.1年前查看全部
- 2AI+Fe2O3==AI2O3+2Fe为什么铝热反应是熵减小的反应.
 r33eere1年前1
r33eere1年前1 -
 硫171 共回答了21个问题
硫171 共回答了21个问题 |采纳率85.7%对于像这样的反应前后都是固体(在标准状态下)的化学反应,要看其标准熵变,就要定量计算了.
查表,得铝的标准熵为28.83KJ/mol;氧化铁的标准熵为87.40KJ/mol;氧化铝的标准熵为50.92KJ/mol;铁的标准熵为27.28KJ/mol,经计算,此反应的标准熵变为-39.58KJ/mol<0,即生成物在标准状态下的熵值之和小于反应物在标准状态下的熵值之和.因此当反应物和生成物都处于标准状态下时可认为此反应是熵减小的反应.
说明:
“标准状态“有很多参考状态,以上提到的“标准状态“均为25摄氏度、100千帕的状态,这与高中化学课本中提到的标准状态不同.
以上数据取自《无机化学》.1年前查看全部
- .取等物质的量的MgO和Fe2O3 的混合物进行铝热反应,写出反应的化学方程式. (2)铝与氧化铁
.取等物质的量的MgO和Fe2O3 的混合物进行铝热反应,写出反应的化学方程式. (2)铝与氧化铁
.取等物质的量的MgO和Fe2O3 的混合物进行铝热反应,写出反应的化学方程式.
(2)铝与氧化铁在高温下的反应可用于工业上冶炼铁(铝热法).将一定量的铝溶于足量的NaOH溶液,产生气体的体积为a L(标准状况).若等质量的铝与氧化铁发生反应,计算得到铁的物质的量(用含a的代数式表示).
 做孽1年前0
做孽1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 爹,帮我查个东西.铝热反应中硝酸钾的作用.
爹,帮我查个东西.铝热反应中硝酸钾的作用.
是实验室反应,铝热法炼铁.不对,是氯酸钾. zijieyun1年前1
zijieyun1年前1 -
 易篇文章 共回答了16个问题
易篇文章 共回答了16个问题 |采纳率81.3%硝酸钾受热放出氧气,生成亚硝酸钾,2KNO3==2KNO2+O2,可以做引燃的氧化剂.1年前查看全部
- (2012•白下区二模)高铁的快速发展方便了人们的出行.工业上利用铝热反应焊接钢轨间的缝隙,化学方程式为2Al+Fe2O
(2012•白下区二模)高铁的快速发展方便了人们的出行.工业上利用铝热反应焊接钢轨间的缝隙,化学方程式为2Al+Fe2O3
A.该反应属于置换反应
B.该反应利用铝的还原性,在高温下把铁从氧化铁里还原出来
C.铝是地壳中含量最多的元素
D.铝、铁均是由原子构成的单质 angelwcy1年前1
angelwcy1年前1 -
 q287106945 共回答了22个问题
q287106945 共回答了22个问题 |采纳率86.4%解题思路:A、根据置换反应是一种单质和一种化合物反应生成另外一种单质和化合物的反应进行解答;B、根据铝的还原性,在高温下把铁从氧化铁里还原成单质铁进行解答;C、根据氧是地壳中含量最多的元素而铝是地壳中含量最多的金属元素进行解答;D、根据铝、铁均是由原子构成的进行解答.A、由单质和化合物反应生成另外的单质和化合物,符合置换反应,故A正确;
B、利用铝的还原性,在高温下把铁从氧化铁里还原成单质铁,故B正确;
C、氧是地壳中含量最多的元素,而铝是地壳中含量最多的金属元素,故C错误;
D、铝、铁均是由原子构成的单质,故D正确.
故选:C.点评:
本题考点: 置换反应及其应用;地壳中元素的分布与含量;物质的构成和含量分析.1年前查看全部
- 粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.进行如下实验:①取适量A进行铝热反应,产物中有单质B生成.(
粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.进行如下实验:①取适量A进行铝热反应,产物中有单质B生成.(提示:铝与氧化铁发生的反应称为铝热反应)②另取20g A全部溶于0.15L 6.0mol/L盐酸中,得溶液C.③将①中得到的单质B和溶液C反应,放出气体1.12L(标准状况下),同时生成溶液D,还残留固体B.④用KSCN溶液检验时,溶液D不变色.
(1)反应①的产物中的单质B是______.
(2)②所发生各反应的化学方程式是:
Ⅰ______
Ⅱ______.
(3)若溶液D的体积仍为0.15L,则该溶液中c(Mg2+)为______,c(Fe2+)为______. 飞天堂1年前1
飞天堂1年前1 -
 liulujun198202 共回答了19个问题
liulujun198202 共回答了19个问题 |采纳率78.9%解题思路:(1)①铝热反应本质是置换反应,金属性Mg>Al>Fe,所以发生的反应为Al与Fe2O3反应,置换出的B是铁;
(2)②MgO与盐酸反应生成氯化镁与水,Fe2O3与盐酸反应生成氯化铁与水;
(3 设MgO和Fe2O3的物质的量都为xmol,根据二者质量计算x的值,溶液D为氯化镁、氯化亚铁的混合溶液,根据镁元素守恒可知n(Mg2+)=n(MgO);亚铁离子来自反应Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+,根据题中数据计算出亚铁离子的物质的量,再根据c=[n/V]计算镁离子、亚铁离子浓度.(1)①MgO和Fe2O3组成的混合物行铝热反应,发生Al与Fe2O3反应方程式为:Fe2O3+2Al
高温
.
Al2O3+2Fe,所以B为铁,故答案为:Fe;
(2)②MgO与盐酸反应生成氯化镁与水,反应的方程式为:MgO+2HCl=MgCl2+H2O;Fe2O3与盐酸反应生成氯化铁与水,反应方程式为:Fe2O3+6HCl=2FeCl3+3H2O,
故答案为:MgO+2HCl=MgCl2+H2O;Fe2O3+6HCl=2FeCl3+3H2O;
(3 设MgO和Fe2O3的物质的量都为xmol,则40x+160x=20,解得x=0.1,溶液D为氯化镁、氯化亚铁的混合溶液,根据镁元素守恒可知,n(Mg2+)=n(MgO)=0.1mol,溶液D的体积仍视为0.15L,所以c(Mg2+)=[0.1mol/0.15L]≈0.67mol/L;
0.1mol氧化铁溶于盐酸生成0.2mol氯化铁,根据反应Fe+2Fe3+=3Fe2+可知,生成亚铁离子的物质的量为:n(Fe2+)=0.2mol×[3/2]=0.3mol,
标况下l.12L(标况)气体的物质的量为:[1.12L/22.4L/nol]=0.05mol,根据反应Fe+2H+=Fe2++H2↑可知,生成0.05mol氢气会生成0.05mol亚铁离子,则溶液D中含有亚铁离子的物质的量为:0.3mol+0.05mol=0.35mol,则:c(Fe2+)=[0.35mol/0.15L]≈2.3mol/L,
故答案为:0.67mol/L;2.3mol/L.点评:
本题考点: 有关混合物反应的计算.
考点点评: 本题考查混合物反应的计算、物质的量浓度计算,题目难度中等,掌握氧化镁、氧化铁以及铁和三价铁离子的反应原理为解答的关键,(5)中计算亚铁离子的物质的量时,不可忽略了铁与氢离子的反应.1年前查看全部
- 铝热反应是吸热还是放热反应,还有怎么判断反应是吸热还是放热
 aprilzhao1年前1
aprilzhao1年前1 -
 zhuliangbo66 共回答了16个问题
zhuliangbo66 共回答了16个问题 |采纳率93.8%反应本身放出的.好比你问氢气氧气燃烧放出的光是谁发的一样,镁是耀眼的白光,跟铝热反应放的光不太一样.滤纸折成一个碗状,就是为了盛那些试剂而已.放热,铝热反应生成的铁是融化的.o(∩_∩)o 记得采纳哦,感激不尽.1年前查看全部
- 铝和四氧化三铁发生铝热反应的化学方程式
 kkDIY1年前3
kkDIY1年前3 -
 12570227 共回答了19个问题
12570227 共回答了19个问题 |采纳率89.5%4Al+3Fe3O4=高温=9Fe+4Al2O31年前查看全部
- 做铝热反应时为何在内层纸制漏斗底部剪个小口?
 就此一回1年前1
就此一回1年前1 -
 glctgu 共回答了19个问题
glctgu 共回答了19个问题 |采纳率89.5%纸制漏斗下面不是放了一个盛有细沙的蒸发皿么
实验第三步就是检验落在蒸发皿中的熔融物
其实,小口就是让反应的物体落下而已.否则直接在漏斗中检验的话,干扰因素太多物质比较杂,而且不方便1年前查看全部
- 问一高中化学题:铝热反应实验中内层漏斗为什么要剪孔并且润湿?目的是什么?
 遙遠哥哥1年前1
遙遠哥哥1年前1 -
 嫦娥的qq赛玉兔 共回答了17个问题
嫦娥的qq赛玉兔 共回答了17个问题 |采纳率100%剪孔并且润湿的只要目的是:为了让得到的铁水能够顺利地流到装有沙子的蒸发皿中!
镁条的作用是为了提高反应的温度,氯酸钾的目的也是为了加快镁条的燃烧,提高足够高的温度!使得反应能顺利发生!
该反应尽管是放热反应,但需要高度条件下才能发生!1年前查看全部
- 铝热反应中氧化铁换成氯化铁行吗?
 dao10201年前1
dao10201年前1 -
 -黄家强- 共回答了27个问题
-黄家强- 共回答了27个问题 |采纳率88.9%“不可以,铝热反应就是铝和金属氧化物
因为氧化铝的熔点很高
氯化铝是共价化合物的说 ”三楼讲得最靠谱
Al2O3比氯化铝稳定,从能量的角度来说,AI+Fe2O3=Fe+Al2O3 这个反应熵值更小更易进行,
且Cl-离子缺少负二价氧的一些性质,不可能完成铝热反应1年前查看全部
- 铝热反应加冰晶石的作用
 童眼颜vv1年前3
童眼颜vv1年前3 -
 dclq 共回答了19个问题
dclq 共回答了19个问题 |采纳率100%助熔剂
就像食盐溶于水是一个道理,冰晶石是溶剂,而氧化铝是溶质.氧化铝的的电解不是是真正意义上的“熔融电解”,其实,熔融的是冰晶石,氧化铝只是分散质,分散于液态的冰晶石中而已,熔液中的阴离子是复杂的原子团,并非简单氧离子.1年前查看全部
- 煤的干馏,石油的分馏,石油的裂化和铝热反应哪个属于物理变化?
 另一个我1年前1
另一个我1年前1 -
 dazhfp 共回答了20个问题
dazhfp 共回答了20个问题 |采纳率85%煤的干馏 化学变化
石油的分馏 物理变化石油的炼制一般有石油的分馏、催化裂化、催化裂解等 石油的分离是利用加热和冷凝的方法将石油分成沸点范围不同的馏分,如石油气、汽油、煤油和重油等 将重油中的大分子在催化剂作用下断裂成小分子的过程叫裂化,其目的是提高液态轻质燃料的产量和质量. 裂解是采用比裂化更高的温度进行深度裂化,以获得短链不饱和烃作为化工原料. 显然石油的分馏未涉及到新物质的生成,属物理变化 石油的裂化 化学变化铝热反应 化学变化1年前查看全部
- 急 ! 在铝热反应中 可以将氧化铁换成氧化镁么 为什么 ..
 蓝色陌子1年前1
蓝色陌子1年前1 -
 deadeyel 共回答了14个问题
deadeyel 共回答了14个问题 |采纳率100%不能,因为还原性Mg>Al>Fe,铝热反应是Al与氧化铁的反应1年前查看全部
- 铝热反应中纸漏斗蘸湿有什么用?在弄滤纸时把内层的拿出剪掉角,又蘸水..
 nandayo1年前1
nandayo1年前1 -
 laozilili_520 共回答了23个问题
laozilili_520 共回答了23个问题 |采纳率91.3%铝热反应中不仅纸漏斗蘸湿而且要用双层的滤纸.因为铝热反应是剧强的放热反应,要采取以上措施防止漏斗被烧坏,建议不要在有易燃、易爆的场所实验.1年前查看全部
- 铝热反应润湿滤纸的作用拜托各位了 3Q
 davidslee1年前1
davidslee1年前1 -
 ilwort 共回答了18个问题
ilwort 共回答了18个问题 |采纳率100%防止漏斗被烧坏 (549722397)1年前查看全部
- 怎样证明铝热反应实验产生的熔融物中含有金属铝
怎样证明铝热反应实验产生的熔融物中含有金属铝
RT 第4个ID1年前1
第4个ID1年前1 -
 yhesong1 共回答了17个问题
yhesong1 共回答了17个问题 |采纳率88.2%产物中只有铝溶于NaOH ...之后质量减轻..得证1年前查看全部
- 为什么铝和氧化镁不能发生铝热反应
 嚣dd的ee1年前4
嚣dd的ee1年前4 -
 dapiwawa2008 共回答了12个问题
dapiwawa2008 共回答了12个问题 |采纳率75%k ca na mg al zn fe sn pb (h) cu hg ag pt au---金属活性表1年前查看全部
- 铝热反应实验中加入氯酸钾做助燃剂,它助燃的原理是什么
 米白的冬天1年前1
米白的冬天1年前1 -
 雪之流 共回答了21个问题
雪之流 共回答了21个问题 |采纳率85.7%2KClO3=(催化剂,加热)2KCl+3O2↑生成氧气助燃1年前查看全部
- 铝热反应能不能用二氧化硅制硅?
 newajic1年前1
newajic1年前1 -
 cooltea83 共回答了17个问题
cooltea83 共回答了17个问题 |采纳率88.2%不能,硅可以发生铝热反应但工业制硅一般是用是用二氧化硅和炭粉在高温条件下反应,生成粗硅:SiO2+2C==Si(粗)+2CO !实验室中一般用 SiO2+2Mg==2MgO+Si(粗)主要是因为要考虑硅的纯度!1年前查看全部
- 能用电解法冶炼的金属有哪些,能用热分解法冶炼的金属有哪些,能用铝热反应冶炼的金属有哪些
 离人倾1年前1
离人倾1年前1 -
 kd8g1nlwimc2sk 共回答了15个问题
kd8g1nlwimc2sk 共回答了15个问题 |采纳率86.7%常见单质活泼性:钾钙钠镁铝,锌铁锡铅氢,铜汞银铂金 铝以前的都用电解,以后的锌到铜可以用铝热法,汞以后的用热分解法,金还可以用物理方法(淘金)1年前查看全部
- 铝热反应 金属氧化物作用请问 铝热反应中的金属氧化物 为什么必须是高熔点金属的氧化物?
 犬公子1年前1
犬公子1年前1 -
 kxwzspb 共回答了16个问题
kxwzspb 共回答了16个问题 |采纳率87.5%相对低熔点的氧化物反应也可以进行,只是通常使用铝被氧化时产生的高温来熔化一些难熔的高熔点金属1年前查看全部
- 粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物,引起铝热反应的实验操作是?
 jhtu5eytresh1年前1
jhtu5eytresh1年前1 -
 Sakura小樱 共回答了17个问题
Sakura小樱 共回答了17个问题 |采纳率94.1%点燃镁条1年前查看全部
- 为什么铝热反应冶炼高熔点金属
 swj19866171年前2
swj19866171年前2 -
 quail_z 共回答了17个问题
quail_z 共回答了17个问题 |采纳率94.1%Al具有较强的还原性
2.铝热反应能释放大量的热量1年前查看全部
- 煤的干馏,石油的分馏,石油的裂化和铝热反应哪个属于物理变化?
 daystar0111年前1
daystar0111年前1 -
 戎嘉乔 共回答了18个问题
戎嘉乔 共回答了18个问题 |采纳率94.4%煤的干馏 化学变化
石油的分馏 物理变化石油的炼制一般有石油的分馏、催化裂化、催化裂解等 石油的分离是利用加热和冷凝的方法将石油分成沸点范围不同的馏分,如石油气、汽油、煤油和重油等 将重油中的大分子在催化剂作用下断裂成小分子的过程叫裂化,其目的是提高液态轻质燃料的产量和质量.裂解是采用比裂化更高的温度进行深度裂化,以获得短链不饱和烃作为化工原料.显然石油的分馏未涉及到新物质的生成,属物理变化 石油的裂化 化学变化铝热反应 化学变化1年前查看全部
- 铝热反应为什么纯度高?金属可以融化,氧化铝还不是要融化啊,他们要混在一起啊
铝热反应为什么纯度高?金属可以融化,氧化铝还不是要融化啊,他们要混在一起啊
我查了下氧化铝的熔点是2015℃ 而钨的熔点是 3 410 ℃ 所以他们的熔融物应该是混合物才对啊?那为什么铝热反应纯度高?还有书上说:用铝热反应冶炼熔点高的金属,是因为反应要放出大量的热,足以使高熔点的金属熔融成液态,这样就可以分离出熔融态的金属,难道低熔点的就不行吗?低熔点的要气化吗? lekai12231年前3
lekai12231年前3 -
 夜归狼迹 共回答了19个问题
夜归狼迹 共回答了19个问题 |采纳率89.5%其实我也是跟你一样认为的,反应物是混合物,而产物的状态也是一样的并没有脱离体系,同时我看一些人焊铁路时并没有产生一堆“氧化铝”在旁边,而是都掺在里面,同时我们经常看到的烧焊也是用同样的原理来进行,也没有出现一堆铁,一堆氧化铝,只是按照一定的比例成为了“杂质”掺附在里面!
PS:书上所说得不一定对,因为只要有人类参与的事物都有可能出现错误.假如工业上有特殊的处理就另当别论了,1年前查看全部
- 用铝热反应原理从V2O5冶炼金属V的化学方程式
 曾_经_有_过1年前1
曾_经_有_过1年前1 -
 夜来香魂 共回答了14个问题
夜来香魂 共回答了14个问题 |采纳率100%5Al+3V2O5=5Al2O3+3V(反应条件为高温)1年前查看全部
- 铝热反应中引燃剂可以用硝酸钾吗?
铝热反应中引燃剂可以用硝酸钾吗?
如果可以用,大概要用多少? jxzyp1231年前1
jxzyp1231年前1 -
 没铺的独行侠 共回答了16个问题
没铺的独行侠 共回答了16个问题 |采纳率81.3%3KNO3+2Al=(加热)=3KNO2+Al2O3 硝酸钾加热生成亚硝酸钾和氧气,高温下氧气与铝反应生成氧化铝.反应最好用铝粉和硝酸钾粉末混合,如果用体积过大的铝片,会生成致密的氧化铝覆盖铝片,阻止继续反应1年前查看全部
- 氯酸钾在铝热反应中的应用?
 木彩1年前1
木彩1年前1 -
 wuyuhui999 共回答了21个问题
wuyuhui999 共回答了21个问题 |采纳率95.2%对,作为氧化剂,提供氧气,支持镁带燃烧.1年前查看全部
- 铝热反应中,氧化镁会不会影响所炼金属的纯度?
 3709468121年前1
3709468121年前1 -
 xiangjin2008 共回答了21个问题
xiangjin2008 共回答了21个问题 |采纳率85.7%氧化镁的熔点高达2800℃,所以在铝热反应中不会溶解的,因而不会影响所炼金属的纯度.1年前查看全部
- 铝热反应适合什么样的金属?课本上没说清楚~
铝热反应适合什么样的金属?课本上没说清楚~
冶炼铝能用还原法吗?课本上只标出了电解法~而镁却标出了电解法和还原法~镁不是比铝活泼么?电解法成本高为什么还要用电解法冶炼铝?
为什么不用炭,氢气或一氧化碳还原铝呢?这种不是便宜么?
有一道题说高熔点的金属用铝热法还原最佳~铁锌铜等金属用炭,氢气或一氧化碳还原最佳,为什么?
百科上的东西和我的问题有关系么? 不羁的孤狼1年前7
不羁的孤狼1年前7 -
 2001myth 共回答了23个问题
2001myth 共回答了23个问题 |采纳率65.2%铝热法一般用来制备高熔点且活泼性小于铝的金属,比如Cr、Mn、Fe、Mo等等.Al是否可以用CO等还原性气体还原还没见过,不过铝可以用C还原,其还原需要相当高的温度,大约是2000度,要达到这么高的温度成本更高,另外Al和O的...1年前查看全部
- 铝热反应生成的铝是离子化合物还是公价化合物
铝热反应生成的铝是离子化合物还是公价化合物
三氧化二铝,写错了,我猜是共价化合物。 dd波子21年前5
dd波子21年前5 -
 wangjianyi18 共回答了22个问题
wangjianyi18 共回答了22个问题 |采纳率86.4%是共价化合物.1年前查看全部
- 引发铝热反应的实验操作是什么
 做梦都哭笑不得1年前1
做梦都哭笑不得1年前1 -
 Lydia_Dee 共回答了15个问题
Lydia_Dee 共回答了15个问题 |采纳率86.7%引发铝热反应操作为
实验操作:
1.取一张圆形滤纸,倒入氧化铁粉沫,再倒入铝粉.
2.将两者混合均匀.用两张圆形滤纸,分别折叠成漏斗状,将其中一个取出,在底部剪一个孔,用水润湿,再跟另一个漏斗套在一起,使四周都有四层.
3.架在铁圈上,下面放置盛沙的蒸发皿,把混合均匀的氧化铁粉沫和铝粉放在纸漏斗中,上面加少量氯酸钾,并在混合物中间插一根镁条,点燃镁条,观察发生的现象.
4.可以看到镁条剧烈燃烧,放出一定的热量,使三氧化二铁粉沫和铝粉在较高的温度下发生剧烈的反应,放出大量的热,同时纸漏斗被烧穿,有熔溶物落入沙中,待熔溶物冷却后,除去外层溶渣,仔细观察,可以看到,落下的是铁珠,这个反应叫铝热反应.反应生成铁和三氧化铝.利用铝的强还原性和铝转化为氧化铝时能放出大量热的性质,工业上常用铝粉来还原一些氧化物,这类反应被称为铝热反应.
若将氧化铁换成氧化镁 反应能否发生 理由
引燃这个反应用镁条点燃吗,那当然可以.
在使用镁条时请注意,镁条必须打磨光亮,并且要10厘米左右,太短热量不够,太长燃烧时间太长,并造成浪费.建议不要在承接容器中加水,否则水高温分解的氢气容易产生化学火暴火乍.切忌不能在反应物附近放可燃物,易燃物或玻璃等易爆物品.当用氯酸钾作氧化剂时,切不可加大剂量,否则会引起物理火暴火乍和化学火暴火乍,在点燃反应物之前,先撤离周围人员,并保持一段距离.在点燃镁带时,可使用高温打火机,喷火枪或酒精灯.发现镁条逐渐变黑和闪火星时,说明镁条已经吸收了够多的热量,马上要燃烧了,这时要继续加热,并准备撤离.点燃镁带后,要赶快离至适合的距离,实验者必须戴墨镜或防强光的设备观察实验现象,以防止被铝热反应的强光灼伤眼睛.绝对不允许在反应物旁观察反应现象.反应时,会有900~1500摄氏度的高温的金属熔融物喷出,这时要隔离周围人员,不得靠近.反应结束后,不可用水浇灭,要等其自然冷却.进行反应时,容易造成剧烈反应的金属氧化物,如二氧化锰等,建议不要用相机进行拍摄,如需拍摄分析,最好用耐强光的镜头,或在镜头上装上黑色胶片等.冷却结束后,可看见被还原的金属,该金属可收藏或再使用.1年前查看全部
- 粉末式样A是由等物质的量的MgO,Fe2O3组成的混合物.取适量A进行铝热反应有B生成,则单质B是 .
 顺势而买1年前3
顺势而买1年前3 -
 kegq1l 共回答了16个问题
kegq1l 共回答了16个问题 |采纳率93.8%金属活动性顺序是Mg>Al>Fe
因此镁不会被置换出来
只有铁会被置换
2Al+Fe2O3=加热=2Fe+Al2O31年前查看全部
- Al能和Ago发生铝热反应吗?和金属硫化物(例如Ags)发生铝热反应吗?
 zzjjffzjf1年前1
zzjjffzjf1年前1 -
 蛋挞我爱吃 共回答了14个问题
蛋挞我爱吃 共回答了14个问题 |采纳率92.9%可以.
但和AgS反应时,S元素会因为高温而被氧气氧化生成二氧化硫.最终产物是Al2O3、Ag和SO2.1年前查看全部
- 请问:铝热反应是铝和那些金属反应呢?
请问:铝热反应是铝和那些金属反应呢?
麻烦例举所有能和铝发生铝热反应的金属. 捣蛋妹妹1年前4
捣蛋妹妹1年前4 -
 邹金良 共回答了13个问题
邹金良 共回答了13个问题 |采纳率69.2%铝热反应常用于冶炼高熔点的金属,并且它是一个放热反应
实验反应化学方程式:
氧化铁:
2Al+Fe2O3=Al2O3+2Fe
四氧化三铁:
8Al+3Fe3O4=4Al2O3+9Fe
二氧化锰:
4Al+3MnO2=2Al2O3+3Mn
(反应条件都为高温)1年前查看全部
- 为适应火车提速,一些铁路线上原有的短轨需要连接为超长轨,工人们利用铝热反应原理焊接钢轨下列有关该反应的说法中正确的是(
为适应火车提速,一些铁路线上原有的短轨需要连接为超长轨,工人们利用铝热反应原理焊接钢轨下列有关该反应的说法中正确的是( )
A.该反应属于化合反应
B.该反应属于复分解反应
C.该反应属于置换反应
D.该反应中铝被还原 22sjgw1年前1
22sjgw1年前1 -
 floratanjj 共回答了20个问题
floratanjj 共回答了20个问题 |采纳率90%解题思路:反应原理为2Al+Fe2O3
Al2O3+2Fe,结合反应物质的所含元素化合价的变化判断.高温 .反应的方程式为2Al+Fe2O3
高温
.
Al2O3+2Fe,反应中铝被氧化生成氧化铝,为还原剂,反应的特点是单质和化合物反应生成另一种单质和另一种化合物,为置换反应.
故选C.点评:
本题考点: 探究铝热反应;化学基本反应类型.
考点点评: 本题考查铝的性质,侧重于铝热反应的考查,判断反应类型关键是要掌握反应类型的特点,平时要对反应类型进行归类总结.1年前查看全部
- 铍和二氧化锰的反应方程式条件是高温,好象是类是铝热反应.
 lianp0011年前2
lianp0011年前2 -
 挥动翅膀的猫 共回答了18个问题
挥动翅膀的猫 共回答了18个问题 |采纳率94.4%铍与Al相似(也可以由对角线法则推出)
Be的稳定价和最高价为+2价,所以有:2Be+MnO2=高温=2BeO+Mn1年前查看全部
- 氧化铁与铝高温下发生铝热反应的方程式
 小--宇--一1年前3
小--宇--一1年前3 -
 ahbjm 共回答了18个问题
ahbjm 共回答了18个问题 |采纳率83.3%Fe2O3+2Al=2Fe+Al2O3,条件为高温1年前查看全部
- 铝热反应的装置中,为什么镁条会引起氯酸钾分解,氯酸钾会引发铝热反应.
 vvde烟灰111年前1
vvde烟灰111年前1 -
 xsfpy 共回答了14个问题
xsfpy 共回答了14个问题 |采纳率92.9%镁条点燃是放热的,氯酸钾受热分解出氧气,促使镁条燃烧更充分,放出热量更多,此时氧化铁被加热到熔融状态,金属铝置换出铁单质1年前查看全部
- 铝热反应是否可以用在冶炼金属镁
 evilweng1年前1
evilweng1年前1 -
 wfhe 共回答了18个问题
wfhe 共回答了18个问题 |采纳率100%不可,铝热反应只可以炼不如铝活泼的的金属,而镁比铝还活泼,比铝更易得电子,因此不可用铝炼镁(倒是可以用镁炼铝,但似乎经济上不划算,镁比铝贵)1年前查看全部
- 粉末状态试样A是由等物质的量的MgO和Fe2O3组成混合物.进行如下实验:(1)取适量A进行铝热反应,产物中有单质B生成
粉末状态试样A是由等物质的量的MgO和Fe2O3组成混合物.进行如下实验:(1)取适量A进行铝热反应,产物中有单质B生成;(2)另取20 g A全部溶于0,15,L 6.0 m0l
 dillon41151年前1
dillon41151年前1 -
 舞蝶小精灵 共回答了21个问题
舞蝶小精灵 共回答了21个问题 |采纳率100%步骤一:MgO、Fe2O3铝热反应后产物为:MgO、Fe、Al2O3,故单质B为Fe.
步骤二:20g的A中两种物质的物质的量相等,可推断出两者皆为0.1mol;
0.15L 6mol/L 的盐酸中,HCl物质的量:0.90mol
反应后有0.1molMgCl2,0.2molFeCl3,0.1molHCl.
步骤三、四:根据步骤四,得到步骤三反应后产物中不含Fe3+,只有Fe,Fe2+,可推断出:
单质B(Fe)先与溶液C余下的0.1mol盐酸反应,
2Fe+6HCl=2FeCl3+3H2(上升符号)
0.1 a 0.05 (为了方便计算,先用a代替)
得到0.05mol氢气,氯化铁,然后
所有氯化铁与铁反应:
2FeCl3+Fe=3FeCl2a+0.2 0.35因此反应完毕,n(Mg2+)=0.1mol n(Fe2+)=0.35mol1年前查看全部
- 高铁的快速发展方便了人们的出行.工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:2Al+Fe2O3 高温&
高铁的快速发展方便了人们的出行.工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:2Al+Fe2O3
Al2O3+2Fe,其中Fe2O3是( )高温 .
A. 氧化剂
B. 还原剂
C. 既是氧化剂又是还原剂
D. 既不是氧化剂又不是还原剂 zheng6291年前1
zheng6291年前1 -
 parmachiesa 共回答了18个问题
parmachiesa 共回答了18个问题 |采纳率94.4%解题思路:2Al+Fe2O3
Al2O3+2Fe,该反应中铝元素化合价由0价变为+3价,铁元素的化合价由+3价变为0价,得电子化合价降低的是氧化剂,失电子化合价升高的反应物是还原剂.高温 .2Al+Fe2O3
高温
.
Al2O3+2Fe,该反应中铁元素的化合价由+3价变为0价,所以氧化铁得电子化合价降低是氧化剂,故选A.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查了氧化还原反应中氧化剂、还原剂的判断,根据元素化合价变化与氧化剂、还原剂之间的关系解答即可,难度不大.1年前查看全部
- 铝热反应生成铁amol,请问该反应至少需要氧化剂 mol?
铝热反应生成铁amol,请问该反应至少需要氧化剂 mol?
铝和氧化铁反应 大热点中1年前4
大热点中1年前4 -
 lqrwblyd 共回答了19个问题
lqrwblyd 共回答了19个问题 |采纳率94.7%0.5a
Fe2O3+2Al=Al2O3+2Fe
0.5a a1年前查看全部
大家在问
- 1有ch4,c2h4,c2h6的混合气体2.24L(标准状况),完全燃烧後得到二氧化碳的体积为原混合气体的1.8倍,生成的
- 2国际会议论文和国际期刊论文的区别?
- 3Millie is a good student.She is in the (nine)grade this term
- 4已知三角形的三边长为a、b、c,如果(a-5)2+|b-12|+c2-26c+169=0,则△ABC是( )
- 5水翻煤气灶上怎么办烧水拿水的时候翻在那上面怎么处理 我家是液化气瓶来人
- 6(2008•抚州)在水溶液中,一般不会与其它物质发生复分解反应的是( )
- 7CH3COOH与甘油的反应方程式
- 8Listen and number the people 1-3 in the picture above.快
- 9大自然的启示的结尾怎么写?
- 10(2014•温州模拟)定义:如果函数y=f(x)在定义域内给定区间[a,b]上存在x0(a<x0<b),满足f(x0)=
- 11五张纸上分别写有数字 1 2 3 4 5,从中任取两张,其中一张上的数为另一张上的数的整数倍的可能性为( )
- 12a cake please l have can怎样连词成句
- 13下列有关铁及其化合物的说法中,正确的是( ) A.Fe 3 O 4 是一种红棕色粉末,俗称铁红 B.Fe(OH) 2
- 14《咏雪》文中用"柳絮"比喻雪花妙在哪里
- 15Hong kong is a busy city on the__of the South China Sea and
