无水硫酸钠吸水时间做实验 用无水硫酸钠 说吸水要过夜,问下一定量的无水硫酸钠吸水要多少时间?
 月风1632022-10-04 11:39:541条回答
月风1632022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 zuuanda 共回答了12个问题
zuuanda 共回答了12个问题 |采纳率83.3%- 这跟试验时所用硫酸钠颗粒大小有关的.为了能方便定量和过滤,我们常常使用颗粒比较大的硫酸钠来干燥,但是这却增加了吸水时间,同时也降低了干燥效果
- 1年前
相关推荐
- 如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K时开始分解为无水硫酸钠.现有14
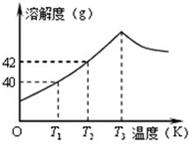
如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K时开始分解为无水硫酸钠.现有142g温度为T2 K的饱和硫酸钠溶液,当温度降为T1K或升为T4K(T4>T3)时析出晶体的质量相等,则温度为T4K时Na2SO4的溶解度为( )
 A. 小于40g
A. 小于40g
B. 等于40g
C. 等于42g
D. 大于42g linbinjordan1年前2
linbinjordan1年前2 -
 jew1 共回答了23个问题
jew1 共回答了23个问题 |采纳率95.7%解题思路:由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4•10H2O肯定要大于2g.由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4•10H2O肯定要大于2g.那么在T4K时析出的晶体是无水硫酸钠,质量是大于2g.所以温度为T4K时Na2SO4的溶解度应该小于T1时的溶解度,即小于40g.
故选:A.点评:
本题考点: 固体溶解度曲线及其作用;固体溶解度的概念;晶体和结晶的概念与现象.
考点点评: 本题考查溶解度、饱和溶液的概念,对于有关溶解度的计算题,找出该温度的饱和溶液,弄清楚硫酸钠晶体(Na2SO4•10H2O)在温度为T3K 时开始分解为无水硫酸钠是解题的关键.1年前查看全部
- 基础化学实验 实验96 从铬盐生产的废渣中提取无水硫酸钠 的实验原理~
基础化学实验 实验96 从铬盐生产的废渣中提取无水硫酸钠 的实验原理~
如果有完整的实验报告最好呀~如果好的话再加30分呀! oneloverain1年前1
oneloverain1年前1 -
 绯村玥 共回答了20个问题
绯村玥 共回答了20个问题 |采纳率95%将废渣配成溶液,加入FeSO4,和适量的稀硫酸,先除去Na2Cr2O7,用量要按照方程式的需要加:6FeSO4+Na2Cr2O7+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+Na2SO4+7H2O然后加NaOH,可以沉淀Mg2+,Fe3+和Cr3+离子,具体反应式很简单.再加Na2C...1年前查看全部
- 无水硫酸钠融于稀硫酸遇铅有什么化学反映
无水硫酸钠融于稀硫酸遇铅有什么化学反映
无水硫酸钠作为蓄电池添加剂能起到什么效果 之所以叫阿毛1年前2
之所以叫阿毛1年前2 -
 tianviv 共回答了13个问题
tianviv 共回答了13个问题 |采纳率46.2%铅酸蓄电池充放电的过程是电化学反应的过程,充电时,硫酸铅形成氧化铅,放电时氧化铅又还原为硫酸铅.而硫酸铅是一种非常容易结晶的物质,当电池中电解溶液的硫酸铅浓度过高或静态闲置时间过长时,就会“抱成”团,结成小晶体,这些小晶体再吸引周围的硫酸铅,就象滚雪球一样形成大的惰性结晶,结晶后的硫酸铅充电时不但不能再还原成氧化铅,还会沉淀附着在电极板上,造成了电极板工作面积下降,这一现象叫硫化
而无水硫酸钠的作用就是为了解决电池的硫化问题特地加入的一种物质
它的机理是,因为钠比铅活泼,加入少量的硫酸钠,在放电的时候生成的大部分最终物质都是硫酸钠,生成硫酸铅的比较少,且硫酸钠不结晶,充电的时候就没有大块的硫酸铅结晶了,这样就可以减小电池的硫化的产生,延长电池的使用寿命.1年前查看全部
- 1在25℃时,向足量的饱和碳酸钠溶液中加入1.06克无水硫酸钠,搅拌后静置,最终析出晶体的质量( )
1在25℃时,向足量的饱和碳酸钠溶液中加入1.06克无水硫酸钠,搅拌后静置,最终析出晶体的质量( )
A等于1.06克
B大于1.06克而小于2.86克
C等于2.86克
D大于2.86克
为什么不是A是D
2澄清石灰水敞口放在空气中,溶液的质量和PH将( )
B变小,变小
D变大,变小
为什么不是B啊 laitianya1年前1
laitianya1年前1 -
 qirimingquan 共回答了25个问题
qirimingquan 共回答了25个问题 |采纳率76%D大于2.86克
因为还要考虑温度.水合要吸热,所以水会降温,使溶解度变小.
B变小
吸收二氧化碳
CO2+Ca(OH)2========CaCO3+H2O1年前查看全部
- 图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K 时开始分解为无水硫酸钠
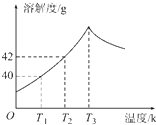 图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K 时开始分解为无水硫酸钠.现有142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K或升为T4K(T4>T3)时析出晶体的质量相等,则温度为T4K时Na2SO4的溶解度为( )
图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K 时开始分解为无水硫酸钠.现有142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K或升为T4K(T4>T3)时析出晶体的质量相等,则温度为T4K时Na2SO4的溶解度为( )
A.小于40g
B.等于40g
C.等于42g
D.大于42g 854405191年前1
854405191年前1 -
 tss9990 共回答了14个问题
tss9990 共回答了14个问题 |采纳率100%由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4•10H2O肯定要大于2g.那么在T4K时析出的晶体是无水硫酸钠,质量是大于2g.所以温度为T4K时Na2SO4的溶解度应该小于T1时的溶解度,即小于40g.
故选A.1年前查看全部
- 用14.2g无水硫酸钠配制成500ml溶液,其物质的量浓度为?
 娃哈哈5n1461年前6
娃哈哈5n1461年前6 -
 番外765 共回答了15个问题
番外765 共回答了15个问题 |采纳率93.3%1ml=1g
所以题目就是用14.2ml无水硫酸钠配制成500ml溶液
500-14.2=485.8 这是有多少水
因为(溶液除以水等于浓度),所以(14.2/485.8)约等于0.029=2.9%1年前查看全部
- 无水硫酸钠 制备无水硫酸钠的制备过程中的干燥阶段采用什么干燥方式最好马上要用了
 顾白衣1年前3
顾白衣1年前3 -
 qq876666874 共回答了16个问题
qq876666874 共回答了16个问题 |采纳率100%放在烘箱里烘干!然后放在干燥箱中冷却.没有干燥箱也可以放在盛有干燥剂(如生石灰)的密闭容器中冷却.如果原来是硫酸钠的溶液,要先加热蒸发溶剂1年前查看全部
- 六公斤无水硫酸钠能在八点六公斤水里面溶解吗?
 122wfe3w1年前1
122wfe3w1年前1 -
 只有失败吗 共回答了11个问题
只有失败吗 共回答了11个问题 |采纳率90.9%不能,六公斤无水硫酸钠大概需要21升水左右1年前查看全部
- 为什么提纯乙酸乙酯时要加入无水硫酸钠?
为什么提纯乙酸乙酯时要加入无水硫酸钠?
注:杂质有乙醇 *** 和水 站在金矿上1年前1
站在金矿上1年前1 -
 拘束的qq 共回答了12个问题
拘束的qq 共回答了12个问题 |采纳率83.3%是吸收乙酸乙酯中的水的!
无水硫酸钠可以作为干燥剂使用1年前查看全部
- 硫酸钠与无水硫酸钠一样吗
 海之蓝08981年前3
海之蓝08981年前3 -
 ycyty 共回答了15个问题
ycyty 共回答了15个问题 |采纳率100%硫酸钠不含结晶水,但易吸水潮解.
严格意义的无水硫酸钠和硫酸钠是一样的.但在实验要求中如果这样写,是为了保证不被潮解.1年前查看全部
- 碳酸氢钠与无水硫酸钠会发生反应吗?为什么
 shixiaofan1年前3
shixiaofan1年前3 -
 许波菜 共回答了13个问题
许波菜 共回答了13个问题 |采纳率92.3%这个不反应,无水碳酸钠分子式Na2CO3,碳酸氢钠分子式:NaHCO3,无水碳酸钠在受潮的情况下会生成碳酸氢钠,而碳酸氢钠在加热干燥的过程中也会生成无水碳酸钠,两者之间应该属于可逆变化,你应该知道在中学化学中我们学过化学的反应的进行是因为根的不同,然而CO3(碳酸根)与HCO3(碳酸氢根)是属于同族根,同族根的反应主要是看C(碳)这个原子的价态,两个物质中C都是正4价,所以不反应.如果是S(硫)S有很多价态(-2,0,+4,+6),要反应也必须是-2价和+4价或者-2与+6价再或者0价与+6价反应,-2价与0价无法反应,0与+4也无法反应!不知道你能不能看懂!1年前查看全部
- 大家好无水硫酸钠在什么里面溶解和亚硫酸钠是一样的成份和效果嘛?
 御士中丞1年前1
御士中丞1年前1 -
 lyd100728 共回答了15个问题
lyd100728 共回答了15个问题 |采纳率86.7%你的意思是说要让NA2SO4变成NA2SO3咯
冒似还要没杂质```
H2S溶液,应该是这答案了,不过也许是大苏打也可以吧,不确定1年前查看全部
- 无水硫酸钠跟无水亚硫酸钠是一样的吗?
无水硫酸钠跟无水亚硫酸钠是一样的吗?
它们用途是一样的,请知情人士告知.谢谢0.0 guilin1141年前4
guilin1141年前4 -
 纯咖啡04 共回答了21个问题
纯咖啡04 共回答了21个问题 |采纳率95.2%无水硫酸钠 白色均匀细颗粒或粉末.无嗅,味咸而带苦.密度2.68g/cm.熔点884℃.易溶于水,溶解度在0-30.4℃内随温度的升高而迅速增大.溶于甘油,不溶于乙醇.水溶液呈中性.当水溶液低于32.38℃时,则以十水物结晶析出.高于32.38℃时开始以无水硫酸钠结晶析出.主要用作染料和助剂的填充剂以调整染料和助剂浓度,使能达到标准浓度.也可用作直接染料、硫化染料、还原染料在染棉布时的促染剂,直接酸性染料在染丝绸和羊毛类动物纤维时的缓染剂,还可用作印花丝织物精炼时的底色保护剂等.造纸工业用作制造硫酸盐纸浆时的蒸煮剂.医药工业用作钡盐中毒时的解毒剂.此外,还用于玻璃、建筑工业等方面.
无水亚硫酸钠 白色六方棱柱形晶体,溶于水(0℃时,12.54g/100ml水;80℃时283g/100ml水),在33.4℃时溶解度最高约为28%,水溶液呈碱性,PH值约为9~9.5.微溶于醇,不溶于液氯、氨.在空气中易被氧化成硫酸钠,遇高温则分解成硫化钠.为强化还原剂,与二氧化硫作用生成亚硫酸氢钠,与强酸反应生成相应盐.CAS号为7757-83-7.
化学用途
无水亚硫酸钠用于胶片显影1年前查看全部
- 用14.2g无水硫酸钠配制成500毫升溶液,其物质的量浓度为 接上面的,若从中取出10毫升,其物质的量浓度
 阳光8531年前1
阳光8531年前1 -
 狼惊梦 共回答了9个问题
狼惊梦 共回答了9个问题 |采纳率77.8%硫酸钠分子量为142
14.2/142/0.5=0.2mol/L
取出10ml物质的量浓度仍然为0.2mol/L1年前查看全部
- 有100亳升液体要加多少无水硫酸钠抽湿水分,无水硫酸钠会溶化吗?
 gaoyonglu1年前1
gaoyonglu1年前1 -
 oyyfhe 共回答了10个问题
oyyfhe 共回答了10个问题 |采纳率100%这个要看你的液体里面含水多少了.
一般来说,无水硫酸钠吸水变成十水硫酸钠
需要的量根据你需要干燥的液体里面的含水量计算一下
然后过量一些就可以了
无水硫酸钠不会溶化,会形成晶体
过滤出来即可1年前查看全部
- 如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K时开始分解为无水硫酸钠.现有14
如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K时开始分解为无水硫酸钠.现有142g温度为T2 K的饱和硫酸钠溶液,当温度降为T1K或升为T4K(T4>T3)时析出晶体的质量相等,则温度为T4K时Na2SO4的溶解度为( )
 A. 小于40g
A. 小于40g
B. 等于40g
C. 等于42g
D. 大于42g cs123cs1年前1
cs123cs1年前1 -
 dangwenyuan 共回答了23个问题
dangwenyuan 共回答了23个问题 |采纳率91.3%解题思路:由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4•10H2O肯定要大于2g.由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4•10H2O肯定要大于2g.那么在T4K时析出的晶体是无水硫酸钠,质量是大于2g.所以温度为T...
点评:
本题考点: 固体溶解度曲线及其作用;固体溶解度的概念;晶体和结晶的概念与现象.
考点点评: 本题考查溶解度、饱和溶液的概念,对于有关溶解度的计算题,找出该温度的饱和溶液,弄清楚硫酸钠晶体(Na2SO4•10H2O)在温度为T3K 时开始分解为无水硫酸钠是解题的关键.1年前查看全部
- 无水硫酸钠是否可以代替无水碳酸钠?
 花妃1年前3
花妃1年前3 -
 永远有多远203 共回答了12个问题
永远有多远203 共回答了12个问题 |采纳率91.7%不能,碳酸钠是碱性的,而硫酸钠是中性的.而且两都的吸水性能也不同.1年前查看全部
- 用14.2g无水硫酸钠配制成500ml溶液,其物质的量浓度为多少
 野英1年前2
野英1年前2 -
 buddy1110 共回答了12个问题
buddy1110 共回答了12个问题 |采纳率91.7%物质的量浓度=(14.2/142)/0.5=0.2mol/L1年前查看全部
- 在相同温度下,100克水最多能够溶解的无水硫酸钠质量为a克,能够溶解芒硝的质量是b克,则a、b之间关系为?
在相同温度下,100克水最多能够溶解的无水硫酸钠质量为a克,能够溶解芒硝的质量是b克,则a、b之间关系为?
xiexie 逍遥折梅手1年前2
逍遥折梅手1年前2 -
 angela_yu666 共回答了20个问题
angela_yu666 共回答了20个问题 |采纳率85%A小于B
因为芒硝是硫酸钠的结晶水合物,溶解后增加水质量,同时即使溶解同质量的硫酸钠分子,芒硝的质量也要大(结晶水的质量)1年前查看全部
- 某温度下硫酸钠的溶解度为5.8g,在该温度下,把无水硫酸钠粉末5.8g加到105.8g饱和硫酸钠溶液中,可析出多少克十水
某温度下硫酸钠的溶解度为5.8g,在该温度下,把无水硫酸钠粉末5.8g加到105.8g饱和硫酸钠溶液中,可析出多少克十水合硫酸钠晶体?
 aaluo1年前1
aaluo1年前1 -
 g2l8 共回答了14个问题
g2l8 共回答了14个问题 |采纳率85.7%析出来的水和Na2SO4再重新溶解,一定也是饱和溶液
饱和溶液质量分数=5.8/105.8
设析出xg十水合硫酸钠晶体
其中水的质量180x/(142+180)
Na2SO4的质量=142x/(142+180)
从原溶液中析出的Na2SO4的质量=[142x/(142+180)]-5.8
原溶液中析出物质的质量分数={[142x/(142+180)]-5.8}/(x-5.8)=5.8/105.8 解出x就是答案1年前查看全部
- 硫酸钡的密度大于无水硫酸钠的密度,为什么在相同体积下,无水硫酸钠的质量比硫酸钡的质量大呢、、、、、?
硫酸钡的密度大于无水硫酸钠的密度,为什么在相同体积下,无水硫酸钠的质量比硫酸钡的质量大呢、、、、、?
两种都是AR分析纯 最后一个总是我1年前1
最后一个总是我1年前1 -
 云想衣裳j 共回答了13个问题
云想衣裳j 共回答了13个问题 |采纳率92.3%硫酸钡晶体密谋4.5,硫酸钠晶体密度2.7,只要比较钡离子和钠离子的密度就可以了,前者肯定大于后者(相对原子质量越大,密度越大).而做成粉体后,会有一个堆密度,因为粉末颗粒形貌并不相同,颗粒之间密实的密实度有差异,...1年前查看全部
- 如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K时开始分解为无水硫酸钠.现有14
 如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K时开始分解为无水硫酸钠.现有142g温度为T2 K的饱和硫酸钠溶液,当温度降为T1K或升为T4K(T4>T3)时析出晶体的质量相等,则温度为T4K时Na2SO4的溶解度为( )
如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为T3K时开始分解为无水硫酸钠.现有142g温度为T2 K的饱和硫酸钠溶液,当温度降为T1K或升为T4K(T4>T3)时析出晶体的质量相等,则温度为T4K时Na2SO4的溶解度为( )
A.小于40g
B.等于40g
C.等于42g
D.大于42g jude8212171年前1
jude8212171年前1 -
 eye2008 共回答了14个问题
eye2008 共回答了14个问题 |采纳率100%解题思路:由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4•10H2O肯定要大于2g.由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4•10H2O肯定要大于2g.那么在T4K时析出的晶体是无水硫酸钠,质量是大于2g.所以温度为T4K时Na2SO4的溶解度应该小于T1时的溶解度,即小于40g.
故选:A.点评:
本题考点: 固体溶解度曲线及其作用;固体溶解度的概念;晶体和结晶的概念与现象.
考点点评: 本题考查溶解度、饱和溶液的概念,对于有关溶解度的计算题,找出该温度的饱和溶液,弄清楚硫酸钠晶体(Na2SO4•10H2O)在温度为T3K 时开始分解为无水硫酸钠是解题的关键.1年前查看全部
- (2014•徐汇区一模)硫化钠是由无水硫酸钠与炭粉在高温下反应制得.反应的化学方程式为:
(2014•徐汇区一模)硫化钠是由无水硫酸钠与炭粉在高温下反应制得.反应的化学方程式为:
①Na2SO4+4C→Na2S+4CO↑;
②Na2SO4+4CO→Na2S+4CO2↑.
(1)要制取Na2S 15.6g,需原料芒硝(Na2SO4•10H2O)______mol.
(2)制得的Na2S固体中含少量Na2SO4、碳粉等杂质.称取该固体0.200g,加适量水溶解后加入25.0mL0.100mol/L的I2标准液,待反应完全后用0.100mol/L Na2S2O3溶液滴定,消耗Na2S2O3溶液16.0mL(已知:滴定时Na2S2O3转化为Na2S4O6),则该Na2S的纯度为______.
(3)①若在反应过程中,产生CO和CO2混合气体的体积为44.8L(标准状况),生成Na2S的物质的量(nmol)的范围是______<n<______;
②若在上述过程中生成Na2S的质量为62.4g,则混合气体中CO和CO2的体积比是多少?
(4)硫化钠晶体(Na2S•9H2O)放置在空气中,会缓慢氧化成Na2SO3•7H2O和Na2SO4•10H2O.现称取在空气中已部分氧化的硫化钠晶体25.76g溶于水,加入足量用盐酸酸化的BaCl2溶液,过滤得沉淀5.62g,放出H2S气体1.12L(标准状况),求原硫化钠晶体的质量. swetncn1年前1
swetncn1年前1 -
 mabin1566 共回答了13个问题
mabin1566 共回答了13个问题 |采纳率100%解题思路:(1)结合反应转化物质的转化利用元素守恒思想来解决;
(2)根据氧化还原反应中电子守恒,得出碘单质和硫代硫酸钠、以及硫化钠之间的关系,代入数据计算即可;
(3)①根据极限假设法利用元素守恒的思想来计算即可;
②计算CO和CO2各自的物质的量,再根据化学方程式列等式,确定结果;
(4)Na2S与Na2SO3在酸性条件下发生反应:2Na2S+Na2SO3+6HCl=NaCl+3S↓+3H2O,故5.62g为硫和硫酸钡的质量,放出H2S气体1.12L,还发生反应2HCl+Na2S=2NaCl+H2S↑,根据n=[m/M]计算S的物质的量,进而计算生成S的反应中参加反应的Na2S、Na2SO3各自的物质的量,根据n=[V/Vm]计算H2S的物质的量,进而计算与盐酸反应生成H2S气体需要Na2SO3的物质的量,再根据m=nM计算样品中Na2S的质量.(1)根据物质间的转化关系知道:Na2SO4~Na2S~Na2SO4•10H2O,所以制取Na2S15.6g(0.2mol),需原料芒硝(Na2SO4•10H2O)的物质的量是0.2mol,
故答案为:0.2;
(2)根据电子守恒,剩余碘单质和硫代硫酸钠之间反应的关系为:I2~2S2O32-,用0.100mol/L Na2S2O3溶液滴定,消耗Na2S2O3溶液16.0mL,所以剩余碘单质的量是[1/2]×0.100mol/L×0.016L=0.0008mol,消耗掉的碘单质物质的量0.025L×0.100mol/L-0.0008mol=0.0017mol,碘单质和硫离子之间反应的关系为:S2-~I2,所以固体中含有硫化钠的物质的量是0.0017mol,硫化钠的质量分数=[0.0017mol×78g/mol/0.2g]×100%=66.3%,故答案为:66.3%;
(3)①若在反应过程中,产生CO和CO2混合气体的体积为44.8L即2mol(标准状况),假设气体全部是CO,则根据硫元素守恒和化学反应①,硫化钠的物质的量是0.5mol,假设气体全部是CO2,将反应①②相加,根据硫元素守恒,得出硫化钠的物质的量是1.0mol,故生成Na2S的物质的量(nmol)的范围是0.5<n<1.0,故答案为:0.5;1.0;
②设混合气体中CO和CO2的物质的量分别是x、y,则根据方程式Na2SO4+4C=Na2S+4CO↑和Na2SO4+4CO=Na2S+4CO2↑,x+y=2mol,[x+y/4+
y
4]=[62.4/78],解得x=0.8mol,y=1.2mol,所以混合气体中CO和CO2的体积比是0.8:1.2=2:3,
答:混合气体中CO和CO2的体积比是2:3;
(4)Na2S与Na2SO3在酸性条件下发生反应:2Na2S+Na2SO3+6HCl=NaCl+3S↓+3H2O,故5.62g为硫和硫酸钡的质量,还发生反应2HCl+Na2S=2NaCl+H2S↑,放出H2S气体1.12L及0.05mol,消耗硫化钠的物质的量是0.05mol,所以剩余硫化钠的物质的量是0.05mol,设晶体混合物中硫化钠晶体、硫酸钠晶体的物质的量是x、y,根据方程式2Na2S+Na2SO3+6HCl=NaCl+3S↓+3H2O知道亚硫酸钠晶体的物质的量是[x−0.05/2]mol,生成硫单质的物质的量是
3(x−0.05)
2mol,根据5.62g为硫和硫酸钡的质量,得出x=0.1mol,所以原来硫化钠晶体的质量m=nM=0.1mol×240g/mol=24g,
故答案为:24g.点评:
本题考点: 含硫物质的性质及综合应用.
考点点评: 本题涉及含硫化合物的性质以及元素守恒思想的计算,属于综合知识的考查题,要求学生具有分析和解决问题的能力,难度大.1年前查看全部
- 无水硫酸钠的作用是什么
 rongll1年前2
rongll1年前2 -
 椰岛之风 共回答了14个问题
椰岛之风 共回答了14个问题 |采纳率92.9%无水硫酸钠又称无水芒硝,元明粉;
英文:Sodium sulfate.
化学分子式:Na2SO4
分子量:142.04
白色均匀细颗粒或粉末.无嗅,味咸而带苦.密度2.68g/cm.熔点884℃.易溶于水,溶解度在0-30.4℃内随温度的升高而迅速增大.溶于甘油,不溶于乙醇.水溶液呈中性.当水溶液低于32.38℃时,则以十水物结晶析出.高于32.38℃时开始以无水硫酸钠结晶析出.
编辑本段
无水硫酸钠的应用领域
主要用作染料和助剂的填充剂以调整染料和助剂浓度,使能达到标准浓度.也可用作直接染料、硫化染料、还原染料在染棉布时的促染剂,直接酸性染料在染丝绸和羊毛类动物纤维时的缓染剂,还可用作印花丝织物精炼时的底色保护剂等.造纸工业用作制造硫酸盐纸浆时的蒸煮剂.医药工业用作钡盐中毒时的解毒剂.此外,还用于玻璃、建筑工业等方面.1年前查看全部
- 实验室分离乙酸,乙醇,乙酸乙酯为什么加无水硫酸钠?
 wxf0624781年前1
wxf0624781年前1 -
 理解和掌握 共回答了15个问题
理解和掌握 共回答了15个问题 |采纳率80%干燥剂
除去有机液体中溶解的少量水分1年前查看全部
- 无水硫酸钠加盐加工业硝酸钠一起搅拌有毒吗
 dus2011年前1
dus2011年前1 -
 xiali710 共回答了19个问题
xiali710 共回答了19个问题 |采纳率100%有毒硫酸钠和硝酸钠都有毒1年前查看全部
- 称取0.4g不纯的无水硫酸钠(所含杂质不与酸反应),加入50ml 0.1mol/l的硫酸溶液中,加热使其充分反应完全;再
称取0.4g不纯的无水硫酸钠(所含杂质不与酸反应),加入50ml 0.1mol/l的硫酸溶液中,加热使其充分反应完全;再加入0.1mol/L烧碱溶液40ml,恰好中和,问:)在上述过程中可得二氧化碳气体多少毫升(S.T.P)?
(2)无水硫酸钠的纯度是多少? bobo0o1年前1
bobo0o1年前1 -
 rainbowlan 共回答了22个问题
rainbowlan 共回答了22个问题 |采纳率86.4%是无水碳酸钠吧?
1参加中和反应的NaOH的物质的量是:0.1*0.04=0.004 mol
2NaOH+H2SO4==Na2SO4+H2O
2^^^^^^1
0.004^^X
X=0.002 mol
H2SO4的物质的量是:0.05*0.1=0.005 mol
则与Na2CO3反应的H2SO4的物质的量是:0.005-0.002=0.003 mol
Na2CO3+H2SO4==Na2SO4+CO2+H2O
106^^^^^1^^^^^^^^^^^^22.4
X^^^^^^0.003 Y
X= 0.318 g Y=0.0672 L=67.2 ml
2无水碳酸钠钠的纯度是:0.318/0.4=79.5%
很坦率的说,这已经是很详细的过程了.1年前查看全部
- 请问怎么样将无水硫酸钠变为10水硫酸钠?
请问怎么样将无水硫酸钠变为10水硫酸钠?
芒硝能溶在已六醇中吗? liquidst1年前2
liquidst1年前2 -
 tianyapat 共回答了22个问题
tianyapat 共回答了22个问题 |采纳率86.4%第一个问题
将无水硫酸钠容于水中,放在蒸发皿中加热,就可结晶成10水硫酸钠
第二个
不能
根据相似相溶原理,芒硝是离子晶体,六醇是共价化合物1年前查看全部
- 无水硫酸钠怎么用处干燥?直接丢进溶液里面吗?那干燥完之后怎么去掉?
无水硫酸钠怎么用处干燥?直接丢进溶液里面吗?那干燥完之后怎么去掉?
RT,还有 氯化钙作为干燥剂的时候 也是丢尽溶液里面吗?干燥完之后 也是可以过滤掉? johnny31881年前1
johnny31881年前1 -
 qingl1002 共回答了15个问题
qingl1002 共回答了15个问题 |采纳率100%如果是用于有机液体的干燥,一般就是直接放入液体中就可以了,然后将有机液体过滤或者蒸馏就可以了,不过滤纸的选择却是有讲究的(这里就不细讲了)而且具体使用蒸馏还是过滤就要看具体的情况.
同样无水CaCL2也是,
不过上述两种物质大多是用于气体的干燥,用于液体的干燥却不是很常见.1年前查看全部
- 乙酸乙酯的制取装置中,乙醇过量的目的?边滴加醋酸,变加热蒸馏的目的?加无水硫酸钠,震荡、过滤的目?
 鲁小妹儿1年前1
鲁小妹儿1年前1 -
 真干冰之剑 共回答了12个问题
真干冰之剑 共回答了12个问题 |采纳率83.3%乙醇过量乙醇回流带出反应的水分
滴加醋酸蒸馏防治乙酸乙酯分解
加无水硫酸钠干燥脱除水分1年前查看全部
- 无水硫酸钠和六水合氯化钴反应吗
 feifeiamm1年前1
feifeiamm1年前1 -
 看你几眼就不疼 共回答了17个问题
看你几眼就不疼 共回答了17个问题 |采纳率94.1%六水合氯化钴结合能力不强,但无水硫酸钠吸水能力也一般般.二者磨成粉充分混合的话肯定会发生一定程度的反应,但要使六水合氯化钴完全变成无水氯化钴是不可能的,1年前查看全部
- 请问怎么样将无水硫酸钠变为10水硫酸钠?1克无水硫酸钠需要加多少水变为10水硫酸钠?
 zhaoerjj1年前5
zhaoerjj1年前5 -
 xiyule 共回答了18个问题
xiyule 共回答了18个问题 |采纳率100%在硫酸钠溶液中不停加硫酸钠固体.直至有晶体析出,析出的就是10水硫酸钠.
约需要1.27g水1年前查看全部
- 称取0.4g不纯的无水碳酸钠称取0.4g不纯的无水硫酸钠(所含的杂质不与酸反应),加入50毫升0.1mol/L的硫酸溶液
称取0.4g不纯的无水碳酸钠
称取0.4g不纯的无水硫酸钠(所含的杂质不与酸反应),加入50毫升0.1mol/L的硫酸溶液,加热使其反应完全,在加入0.1mol/L烧碱溶液40毫升,恰好中和.问,(1)在上述过程中可得二氧化碳气体多少毫升?2)无水碳酸钠的纯度是多少? 孤军1年前1
孤军1年前1 -
 yudepei 共回答了18个问题
yudepei 共回答了18个问题 |采纳率100%0.1mol/L烧碱溶液40ml含OH-0.004mol,可与0.004molH+(0.002mol硫酸)反应.
硫酸溶液共含硫酸0.005mol,所以有0.003mol硫酸和碳酸钠反应
H2SO4 + Na2CO3=Na2SO4+H2O+CO2
1 106 22.4*1000
0.003 0.318 67.2
mol g ml
生成二氧化碳67.2ml
无水碳酸钠纯度0.318/0.4*100%=79.5%1年前查看全部
- 无水硫酸钠在镍水回收的作用
 卞丽华1年前1
卞丽华1年前1 -
 孙涵 共回答了23个问题
孙涵 共回答了23个问题 |采纳率87%吸收水(H2O)1年前查看全部
- 无水硫酸钠的密度是多少?
 男人糊涂1年前1
男人糊涂1年前1 -
 maowei_8777 共回答了24个问题
maowei_8777 共回答了24个问题 |采纳率95.8%相对密度(水=1):2.681年前查看全部
- 哪位朋友知道:无水氯化钙与无水硫酸钠的区别?
 juliajiang1年前1
juliajiang1年前1 -
 denyling 共回答了20个问题
denyling 共回答了20个问题 |采纳率100%无水氯化钙进入溶剂后具有弱酸性,属于路易斯酸,弱电解质,易水解,结合水中的氢氧根离子,生成氢氧化钙及氢、氯离子,反应可逆.
无水硫酸钠是强酸强碱盐,不属于路易斯酸,强电解质,易电离,电离生成硫酸根离子和钠离子.1年前查看全部
- 怎样鉴别碳酸镁、碳酸钡、无水硫酸钠、无水碳酸钠、无水氯化钙
 KM_annia1年前3
KM_annia1年前3 -
 向前22 共回答了15个问题
向前22 共回答了15个问题 |采纳率73.3%在不用其他试剂的情况下是不可能实现的!
用其他试剂的情况下:
①对各种样品编号取样,分别配置为溶液.
由于碳酸钡是不溶的,碳酸镁是微溶的,所以很容易就把这两种物质与其他的物质区分开了
②加入适量的盐酸到 碳酸镁、碳酸钡的“溶液”,使沉淀溶解,然后向溶液加入稀氢氧化钠,有沉淀生成的原物质是碳酸镁,另者是碳酸钡
③另取无水硫酸钠、无水碳酸钠、无水氯化钙
所配置的溶液两份,一份加入稀盐酸,有气泡冒出的是碳酸钠,第二份加入氢氧化钡,有沉淀生成的是硫酸钠1年前查看全部
- CuSe是什么颜色铁、硫酸铜、硫代硫酸钠、无水硫酸钠、高锰酸钾、七钼酸铵,怎样配制才能得到黑色物质牢固附着在铁上
 飘渺无轩1年前1
飘渺无轩1年前1 -
 老人不老 共回答了11个问题
老人不老 共回答了11个问题 |采纳率90.9%CuSe,性质:黑色粉末.有两种变体:110℃以下为四方晶系结构,110℃以上为立方晶系结构.密度6.749~6.84g/cm3.熔点1113℃.易为硝酸、王水等强氧化剂氧化.由元素硒和铜直接反应,或由碳还原硒酸铜等方法制取.1年前查看全部
- 无水硫酸钠的作用无水硫酸钠在水泥中起什么作用
 绝地-1年前2
绝地-1年前2 -
 sherry1209 共回答了21个问题
sherry1209 共回答了21个问题 |采纳率81%晶体无水硫酸钠(元明粉国标III类一等) 产品主要为生产粉体混凝土外加剂、水泥工艺外加剂企业提供原料.同时,该工艺生产的无水硫酸钠在形成过程中吸收和积聚了大量自然能量.在生产硫化碱.泡花碱.苛性钠.硫磺等需要发生氧化还原反应时,可释放能量加快反应速度,降低能耗增加效益.应用于水泥助磨剂时,效果特别明显.1年前查看全部
- 用无水硫酸钠干燥一般要多长时间?
 jessie_8611年前1
jessie_8611年前1 -
 jhy123 共回答了20个问题
jhy123 共回答了20个问题 |采纳率95%zhlfang(站内联系TA)要看你准备做什么,如果下步是无水操作当然要干燥彻底些,很多时候不用干燥那么久.而且无水硫酸钠的干燥能力也有限,如果真要很干燥,建议换干燥剂.zhouy23(站内联系TA)干燥过夜是为了干燥的充分点luoyueyouqing(站内联系TA)我一般是干燥过夜,至于真空干燥,貌似不可以.还有就是如果产品在有机溶剂里面,要看什么溶剂.干燥剂建议还是选无水硫酸钠,别的有可能会破坏产品lovehappy2008(站内联系TA)我都干燥过夜了,一般四小时就差不多了duoan(站内联系TA)Originally posted by luoyueyouqing at 2008-1-5 19
是在溶剂里面,二氯甲烷,一般几个小时可以?有时候要做下一步无水反应,有时候是最终产品.二氯甲烷在5个小时左右吧,如果无水硫酸钠有结块的话就放长一点的时间1年前查看全部
- 如何用无水硝酸钠和无水硫酸钠制取一氧化二氮?
 风海流翼1年前1
风海流翼1年前1 -
 也是翁迷 共回答了18个问题
也是翁迷 共回答了18个问题 |采纳率88.9%好像只有硝酸钠和无水硫酸铵才能制.
由加热硝酸钠和无水硫酸铵的混合物来制备.
2NaNO3+(NH4)2SO4=2N2O+Na2SO4+4H2O1年前查看全部
大家在问
- 1《红楼梦》分上、中、下三册,全书共108元.上册比中册贵11元,下册比中册便宜2元,上、中、下各多少元?
- 2生日聚会 英语怎么讲
- 3以下哪一项不是威胁生物多样性的原因?( )
- 4无理式如何裂项相消求和
- 5how was the plane able to clear the mountains中clear是飞过的意思吗?为
- 6用行走造句
- 7图中氢气球重为10N,空气对它的浮力为16N.由于受到水平向左的风力的作用,使系气球的绳子与地面成60°,试求:
- 8某研究性学习小组为了制作一个传感器,需要选用某种电学元件.实验中首先要描绘该元件的伏安特性曲线,实验室备有下列器材:
- 9He was found___ the next morning .A.die B.death C.dead D.dyi
- 10计算C5:H5和的公式是
- 11I am your antidote是我是你的解药的意思吗?或者我是你的解药英语怎么说的?
- 12妈妈决定给我买一辆新自行车 英文翻译
- 13已知一个角的补角是它本身的3倍,求这个角
- 14在一元2次方程中,知道A,B,C的符号,怎么判断他的根的符号啊?
- 15干冰升华为何说明粒子间存在间隔?轮胎爆胎不能说明粒子运动吗?
