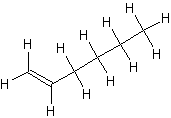
非极性共价键和极性共价]键怎么分别?
 7790894882022-10-04 11:39:541条回答
7790894882022-10-04 11:39:541条回答是两种不同元素之间形成的键都是非极性吗?还是对称的才是呢?
那,极性呢?怎么分别呢?

已提交,审核后显示!提交回复
共1条回复
 mouse-mouse 共回答了20个问题
mouse-mouse 共回答了20个问题 |采纳率95%- 1、非极性共价键:由同种元素的原子间通过共用电子对形成的共价键,又称为非极性键.
存在于非金属单质中.某些共价化合物分子中也有非极性键,如:H2O2中的O-O键,C2H6中的C-C键等.少数离子化合物中也有非极性键,如:Na2O2中的O-O键,CaC2中的碳碳三键等.
2、极性共价键:不同种元素的原子形成分子时共用电子对偏向吸引电子能力强的原子而形成的共价键,又称为极性键.
所有的共价化合物分子中都存在极性键,离子化合物的原子团中也存在极性键. - 1年前
相关推荐
- 非极性共价键的电负性差范围刑其毅先生在《基础有机化学》里,说“电负性差在0~0.6之间是共价键,0.1.7之间是典型极性
非极性共价键的电负性差范围
刑其毅先生在《基础有机化学》里,说“电负性差在0~0.6之间是共价键,0.1.7之间是典型极性共价键”,那电负性差0~0.6之间的共价键,能不能称之为非极性键呢?
比如甲烷里的C-H键,C、H泡林标度的电负性差只有0.35,这个键算极性键还是非极性键?
注意,一共两问哦:
1.电负性差0~0.6之间的共价键,能不能称之为非极性键?
2.甲烷里的C-H键,C、H泡林标度的电负性差只有0.35,这个键算极性键还是非极性键? 小鱼要吃大鱼1年前3
小鱼要吃大鱼1年前3 -
 7az7 共回答了17个问题
7az7 共回答了17个问题 |采纳率100%电负性差0~0.6之间的共价键,一般能称之为非极性键.当然,如果数值在边缘,如0.56,那么将视具体反应来决定它是否算非极性.
.甲烷里的C-H键算非极性键1年前查看全部
- 怎样判断物质是否含有极性共价键和非极性共价键
 ss冷月刀1年前1
ss冷月刀1年前1 -
 5987950 共回答了12个问题
5987950 共回答了12个问题 |采纳率83.3%从分子(结构)式中可以看出:
1、非极性共价键:同种元素的原子之间形成.因为同种元素,吸引电子的能力一样,所以电子不偏不倚,没有极性;
2、极性共价键:不同种的原子形成的共价键,因为原子不同,吸引电子的能力不一样,所以电子偏向于吸引电子能力强的一方,化学键显极性.1年前查看全部
- 碳与碳原子之间可以有4个非极性共价键吗?它构成什么物质?
碳与碳原子之间可以有4个非极性共价键吗?它构成什么物质?
是构成碳单质吗?构成碳单质要【所有】的碳原子都是碳碳双键?那最两边的碳原子呢?
请回答以上五个问题.会几个回答几个. w-jc1年前2
w-jc1年前2 -
 kingwjj1984 共回答了21个问题
kingwjj1984 共回答了21个问题 |采纳率95.2%如果分子中存在但不是所有C是与4个C 相连,那该分子中有叔丁基,也可形成石墨 C60.如果所有的C都是的话则可以形成金刚石,等.是不是单质要判断是否为纯净物,具体是否有混杂,我也说不清,石墨和金刚石在一定条件下可以相互转化,不过一般条件下都是稳定单质.不可能都是CC双键的,如果都是CC双键,那么这个分子团将是直链,而且分子键张力很大,极不稳定,很显然石墨 金刚石 C60均不是直链,他们其中会有CC双键,或复合键存在,但不可能都是.1年前查看全部
- 化学在线提问麻烦问你几个问题希望你能帮我解决一下,谢谢了!下列各物质中,只含有非极性共价键的是A. H2S B. NaO
化学在线提问
麻烦问你几个问题希望你能帮我解决一下,谢谢了!
下列各物质中,只含有非极性共价键的是
A. H2S B. NaOH C. KCl D. Cl2
非极性共价键指的是什么?
下列过程中不可逆的是
A氨的合成 B氯化铁的分解 C蛋白质的变质 D蛋白质的盐析 麻烦说下原因 暂时在这儿混1年前4
暂时在这儿混1年前4 -
 qq78001943 共回答了15个问题
qq78001943 共回答了15个问题 |采纳率93.3%D.1年前查看全部
- 下列物质中既有离子键又有非极性共价键的化合物是( )
下列物质中既有离子键又有非极性共价键的化合物是( )
A.H2SO4
B.NaOH
C.N2
D.Na2O2 cmjsdkfoiasufous1年前1
cmjsdkfoiasufous1年前1 -
 zhx7528 共回答了15个问题
zhx7528 共回答了15个问题 |采纳率86.7%解题思路:一般来说,活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性共价键,不同非金属元素之间易形成极性共价键,由两种或两种以上元素组成的纯净物为化合物,据此分析解答.A.硫酸中只含共价键不含离子键,故A错误;
B.氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在极性共价键,所以氢氧化钠中不含非极性共价键,故B错误;
C.氮气为单质,氮气中只含非极性共价键,故C错误;
D.氢氧化钠中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在非极性共价键,故D正确;
故选D.点评:
本题考点: 离子化合物的结构特征与性质;极性键和非极性键.
考点点评: 本题考查了化学键和化合物的判断,明确化学键和化合物的概念是解本题关键,第IA、IIA族元素和第VIA、第VIIA族元素之间易形成离子键,难度不大.1年前查看全部
- H+离子与H2O分子反应生成H3O+离子,它们之间的相互作用是( )A.分子间作用力B.非极性共价键C.离子
H+离子与H2O分子反应生成H3O+离子,它们之间的相互作用是( )A.分子间作用力B.非极性共价键C.离子
H+离子与H2O分子反应生成H3O+离子,它们之间的相互作用是( )
A.分子间作用力
B.非极性共价键
C.离子键
D.配位键
 9流浪鱼1年前1
9流浪鱼1年前1 -
 眼镜上的泪水 共回答了23个问题
眼镜上的泪水 共回答了23个问题 |采纳率100%氢离子中不含电子只含空轨道,水分子中O原子含有孤电子对,所以氢离子和水分子生成的水合氢离子中存在配位键,故选D.1年前查看全部
- 次氯酸钠中含有什么化学键我认识 所含的化学键有非极性共价键、记性共价键和离子键.但是我错了,.那它含有什么键/?.没有含
次氯酸钠中含有什么化学键
我认识 所含的化学键有非极性共价键、记性共价键和离子键.但是我错了,.那它含有什么键/?.没有含什么化学键呢、、 为什么呢?如何判断? 萍水相逢19881年前6
萍水相逢19881年前6 -
 lovelace06 共回答了18个问题
lovelace06 共回答了18个问题 |采纳率100%NaClO中含离子键和极性共价键.
Na+与ClO-有离子键;
Cl与O有极性共价键.
判断:1.金属与酸根之间形成的是离子键;
2.相同的非金属之间形成的是非极性共价键;
3.不同的非金属之间形成的是极性共价键.
特例,1.铵根NH4+看作金属,N和H极性共价键,NH4+与酸根之间形成的是离子键;
2.AlCl之间是共价键.1年前查看全部
- 下列说法错误的是( )A.原子晶体中只能存在非极性共价键B.离子晶体在熔化状态下能导电C.金属晶体通常具有导电、导热和
下列说法错误的是( )
A.原子晶体中只能存在非极性共价键
B.离子晶体在熔化状态下能导电
C.金属晶体通常具有导电、导热和良好的延展性
D.分子晶体的状态变化,只需克服分子间作用力 dase751年前1
dase751年前1 -
 cctv5yumen 共回答了14个问题
cctv5yumen 共回答了14个问题 |采纳率92.9%解题思路:A.同种元素原子之间形成非极性键,不同原子之间形成极性键;
B.离子晶体在熔化状态下能电离出自由移动的离子;
C.金属的物理通性;
D.只需克服分子间作用力,则晶体为分子晶体;A.二氧化硅是原子晶体,晶体中存在极性键,故A错误;
B.离子晶体在熔化状态下能电离出自由移动的离子,所以在熔融状态下能导电,故B正确;
C.金属晶体通常具有导电、导热和良好的延展性,故C正确;
D.分子晶体的状态变化,只需克服分子间作用力即可,故D正确;
故选:A;点评:
本题考点: 离子晶体;原子晶体;分子晶体;金属晶体.
考点点评: 本题主要考查了晶体的性质,难度不大,注意知识的积累.1年前查看全部
- 求教一下如何辨别是极性共价键还是非极性共价键,或者是既有离子键又有共价键
 清秀俗不1年前3
清秀俗不1年前3 -
 风遗言 共回答了11946个问题
风遗言 共回答了11946个问题 |采纳率0.6%分子中或原子团中不同种原子之间是极性共价键,同种原子之间如果有键一般是非极性共价键。单质O3(臭氧除外,有一个离子键) 阴阳离子之间是离子键 酸的分子,氢与酸根之间是极性共价键,水溶液中则以氢离子和酸根离子形式存在,之间没有键 望采纳!!!...1年前查看全部
- 请帮忙判断下是否有极性共价键,非极性共价键,离子键的断裂和形成,2NaOH+Cl2==NaClO+H2O+NaCl
请帮忙判断下是否有极性共价键,非极性共价键,离子键的断裂和形成,2NaOH+Cl2==NaClO+H2O+NaCl
2Na2O2+2CO2==2Na2CO3+O2 bier11年前1
bier11年前1 -
 我爱四叶 共回答了21个问题
我爱四叶 共回答了21个问题 |采纳率85.7%断键:极性共价键:O-H
非极性共价键:Cl-Cl
离子键:Na+与OH-
成键:极性共价键:O-H,O-Cl
离子键:Na+与ClO-,Na与Cl-
无非极性共价键1年前查看全部
- 下列反应过程中,同时有离子键、极性共价键和非极性共价键断裂的是( )
下列反应过程中,同时有离子键、极性共价键和非极性共价键断裂的是( )
A. NH4Cl
NH3↑+HCl↑△ .
B. NH3+CO2+H2O=NH4HCO3
C. 2NaOH+Cl2=NaCl+NaClO+H2O
D. 2Na2O2+2CO2=2Na2CO3+O2 WQDGY1年前1
WQDGY1年前1 -
 dalls4141 共回答了23个问题
dalls4141 共回答了23个问题 |采纳率87%解题思路:根据活泼金属和活泼非金属之间易形成离子键,同种非金属元素之间易形成非极性共价键,不同种非金属元素之间易形成极性共价键,化学反应的实质是旧化学键的断裂和新化学键的形成,据此分析解答.A.NH4Cl中含有离子键和极性共价键,则反应物中只有极性共价键、离子键的断裂,故A错误;
B.NH3、CO2、H2O中只含有极性共价键,则反应物中只有极性共价键的断裂,故B错误;
C.NaOH中含有离子键和极性共价键,Cl2中含有非极性共价键,则反应物中有离子键、非极性共价键断裂,没有极性键的断裂,故C错误;
D.Na2O2为含有非极性键的离子化合物,CO2中含有极性键,则反应物中离子键、极性共价键和非极性共价键断裂,故D正确;
故选:D.点评:
本题考点: 化学键.
考点点评: 本题以化学反应与化学键的关系,难度不大,明确物质中存在化学键的类型是解答本题的关键,注意非金属元素之间易形成共价键,但铵盐除外,铵盐中含有离子键.1年前查看全部
- 过氧化氢 过氧化钠 都有什么化学键?离子键,共价键 极性共价键,非极性共价键?
过氧化氢 过氧化钠 都有什么化学键?离子键,共价键 极性共价键,非极性共价键?
这几个化学键,有什么区别? longwen1231年前3
longwen1231年前3 -
 吓狗的猫 共回答了19个问题
吓狗的猫 共回答了19个问题 |采纳率89.5%过氧化氢中有极性共价键和非极性共价键 .
过氧化钠 有离子键和非极性共价键.
离子键:使阴、阳离子结合成化合物的静电作用.
共价键:原子之间通过共用电子对所形成的相互作用.
非 极 性 键.
共用电子对不偏向任何成键原子的共价键.
存在同种元素的原子间
极 性 键
共用电子对偏向某一成键原子的共价键.
存在不同种元素的原子间1年前查看全部
- IBr分子是 极性共价键?还是非极性共价键
 Hoverinlife1年前3
Hoverinlife1年前3 -
 神aa英 共回答了14个问题
神aa英 共回答了14个问题 |采纳率92.9%极性共价键,只要是不同元素的双原子分子一般都是极性共价键1年前查看全部
- 2Ca+2H2O=2Ca(OH)2+O2为什么破坏了非极性共价键?
2Ca+2H2O=2Ca(OH)2+O2为什么破坏了非极性共价键?
RT yuyuantan1年前1
yuyuantan1年前1 -
 cyr2006 共回答了24个问题
cyr2006 共回答了24个问题 |采纳率95.8%2Ca+2H2O=2Ca(OH)2+H2反应破坏的是H-O-H中的氧氢键1年前查看全部
- 同时有离子键,极性共价键,非极性共价键的断裂和形成的反应是?
 sally_zhanghehe1年前3
sally_zhanghehe1年前3 -
 流浪的CAPO 共回答了22个问题
流浪的CAPO 共回答了22个问题 |采纳率77.3%解答2Na2O2+2H2O==4NaOH+O2↑
离子键 极性共价 非极性共价
断裂 NA-O O--OH O--O
形成 NA-OH O-H O--O1年前查看全部
- 极性共价键非极性共价键离子键区别怎么区分
 凯歌51年前4
凯歌51年前4 -
 haydeeyu 共回答了18个问题
haydeeyu 共回答了18个问题 |采纳率72.2%离子之间形成的是离子键,一般是金属与非金属元素形成的,如Na2O中含有离子键,但需要记住AlCl3和FeCl3是共价键.
极性共价键是不同元素之间形成的共价键,如C2H6中的C-H键.
非极性共价键是相同元素之间形成的共价键,如C2H6中的C-C键,单质中的共价键都是非极性共价键.1年前查看全部
- 一个己烯分子中含5个非极性共价键,
一个己烯分子中含5个非极性共价键,
0.5mol丙烯中,共价键的数目为4NA, 鲍斯0071年前2
鲍斯0071年前2 -
 shrekandfiona 共回答了20个问题
shrekandfiona 共回答了20个问题 |采纳率85%1年前查看全部
- 1 只含非极性共价键的物质:同种非金属元素构成的物质,如:____
1 只含非极性共价键的物质:同种非金属元素构成的物质,如:____
2 只含有极性共价键的物质:一般是不同的非金属元素构成的共价化合物,如:____
3 既含有有极性共价键的物质又有非极性共价键的物质:如:____ liujian33101年前1
liujian33101年前1 -
 飞天少女猪 共回答了18个问题
飞天少女猪 共回答了18个问题 |采纳率94.4%放电脑着…………………………
1:非金属单质 氧气 白磷 红磷 一类的 高三就用这些吧?
2:水 氨气 甲烷 好多……
3:双氧水 ……
对了都是化学式……这地方不好打呢玩意……1年前查看全部
- 离子键 共价键…的区别离子键 共价键 极性共价键 非极性共价键 氢键的区别,怎么区分,最好举几个例子…谢谢了
 吾境不远1年前2
吾境不远1年前2 -
 sheqs 共回答了16个问题
sheqs 共回答了16个问题 |采纳率87.5%离子键是阴阳离子之间形成的化学键,如Na+与Cl-.
共价键是原子之间形成的,如果是同种元素的原子形成的是非极性键,不同种元素原子形成的是极性键.
氢键是X-H...Y的类型的键,X、Y只能是N、O、F.1年前查看全部
- 怎样判断物质是否含有极性共价键和非极性共价键
怎样判断物质是否含有极性共价键和非极性共价键
越简洁易懂越好,急...一定要教会我,.. 独自在行走1年前3
独自在行走1年前3 -
 THXHT 共回答了29个问题
THXHT 共回答了29个问题 |采纳率93.1%一、由同种非金属元素形成的化学键是非极性键.如氧气中O—O键就是非极性键
成因:
由于两个成键原子对共用电子对的作用力相同,所以共用电子对位于两原子中间
存在:
1、非金属单质中,一定是非极性键
2、某些共价化合物中,过氧化氢(H—O—O—H)中的O—O键就是非极性键
3、某些离子化合物中,过氧化钠中的O—O键也是非极性键
二、由不同种非金属元素形成的化学键是极性键.如氯化氢中H—Cl键是极性键
成因:
由于两个原子得电子能力不同,使共用电子对偏向得电子能力强的原子一方,使这个原子显负电,另外一个得电子能力弱的原子则显正电.
存在:
1、共价化合物中都有极性键存在.如水(H—O—H)中的H—O键
2、离子化合物中,氢氧根、各种酸根、铵根中都存在极性键1年前查看全部
- 有什么常见物质是既含极性共价键又含非极性共价键?
有什么常见物质是既含极性共价键又含非极性共价键?
举一些常见的物质既含极性共价键又含非极性共价键的.
最好多提一些容易让人出错的!
NA2O2是吗? 样尤氏道1年前4
样尤氏道1年前4 -
 maoxuming 共回答了26个问题
maoxuming 共回答了26个问题 |采纳率96.2%双氧水H2O2
乙烷:CH3-CH3等烷烃1年前查看全部
- 由非极性共价键和极性共价键构成的物质是
 我命问我不问天1年前3
我命问我不问天1年前3 -
 娘子_ 共回答了16个问题
娘子_ 共回答了16个问题 |采纳率81.3%过氧化氢:H2O2 结构式:H-O=O-H 两个氧原子在中间,共用两对电子,是非极性键构成的;而两边的氢原子和氧原子直接是极性键,共用电子对会偏向氧原子那侧1年前查看全部
- 非极性共价键是否只存在于双原子单质分子里?
 浑身是毛1年前3
浑身是毛1年前3 -
 手指缠上微 共回答了21个问题
手指缠上微 共回答了21个问题 |采纳率85.7%非极性共价键不仅存在于双原子单质分子里,而且存在多原子的共价化合物(双氧水、乙烯···),还存在离子化合物在(过氧化钠、二硫化亚铁···)1年前查看全部
- 具有非极性共价键的共价化合物是电解质么
 lenovolove1年前1
lenovolove1年前1 -
 huang1hui 共回答了17个问题
huang1hui 共回答了17个问题 |采纳率94.1%高二课本说某些具有极性键的共价化合物是弱电解质 那么1年前查看全部
- 不含非极性共价键的分子晶体一定是共价化合物?
不含非极性共价键的分子晶体一定是共价化合物?
RT.判断对错+理由. 啊妹妹1年前1
啊妹妹1年前1 -
 光碟ll商 共回答了27个问题
光碟ll商 共回答了27个问题 |采纳率88.9%错,稀有气体分子为单原子分子,不含非极性共价键,而且是分子晶体,但它不是化合物1年前查看全部
- 水算极性共价键还是非极性共价键?
水算极性共价键还是非极性共价键?
RT,说明下原因, 缘遇-1年前4
缘遇-1年前4 -
 dcqwzw 共回答了18个问题
dcqwzw 共回答了18个问题 |采纳率94.4%极性,水结构呈V型,两个氢原子对氧原子的吸引力不能抵消,故为极性分子如果分子中中心原子所受分子引力平衡的话,就是非极性分子,不平衡就是极性分子
非极性共价键是由对电子吸引能力相同粒子产生,一般为同种原子间的共价键.
所以水分子是含极性键的极性分子1年前查看全部
- co2分子内存在极性共价键.h2o分子内存在非极性共价键.这两句话对吗?
 AnGeL__Lee1年前2
AnGeL__Lee1年前2 -
 jluedu01 共回答了17个问题
jluedu01 共回答了17个问题 |采纳率94.1%前一句正确,后一句错误1年前查看全部
- 二氧化硅非极性共价键还是极性共价键
 fere20081年前1
fere20081年前1 -
 crystaltennis 共回答了25个问题
crystaltennis 共回答了25个问题 |采纳率88%非极性共价键1年前查看全部
- 下列叙述正确的是:A.氧气分子间存在着非极性共价键 B.二氧化碳分子内存在着极性共价键
 xysr14erx_24b71年前2
xysr14erx_24b71年前2 -
 vianzhao603 共回答了17个问题
vianzhao603 共回答了17个问题 |采纳率70.6%B正确.二氧化碳分子内存在两个碳氧极性共价键.A错,氧气分子间没用非极性共价键,氧气分子间作用是范德华力,分子内则存在氧氧非极性共价键.1年前查看全部
- 比如书上说:两个原子(ΔEN在0~0.4之间),共用电子对产生的化学键为非极性共价键
 nweli0001年前1
nweli0001年前1 -
 67894545 共回答了20个问题
67894545 共回答了20个问题 |采纳率90%这个指的是两种元素电负性的差值.1年前查看全部
- MgCl2是否含离子键和非极性共价键?
MgCl2是否含离子键和非极性共价键?
同上.. 今年不宜恋爱1年前1
今年不宜恋爱1年前1 -
 Monicapan1018 共回答了20个问题
Monicapan1018 共回答了20个问题 |采纳率80%不是,只含两个氯镁离子键!1年前查看全部
- “氧气分子之间存在非极性共价键”这句话为什么错
 gxcyl1年前1
gxcyl1年前1 -
 你说我说都说吧 共回答了22个问题
你说我说都说吧 共回答了22个问题 |采纳率86.4%氧气分子之间存在的是(分子间作用力)
而非极性共价键存在于氧气分子内的原子之间1年前查看全部
- 氧气分子间存在的化学键氧气分子 间 存在的化学键都有什么?不是非极性共价键么?为什么?同种原子组成的,不是应该存在非极性
氧气分子间存在的化学键
氧气分子 间 存在的化学键都有什么?
不是非极性共价键么?
为什么?同种原子组成的,不是应该存在非极性共价键么? 溪有源1年前4
溪有源1年前4 -
 wang19970 共回答了25个问题
wang19970 共回答了25个问题 |采纳率84%氧气分子间仅存在范德华力
在氧分子中,两个氧原子之间才存在非极性共价键1年前查看全部
- 怎样区分极性共价键、非极性共价键、离子键和金属键
 ingodwetrust1年前1
ingodwetrust1年前1 -
 wusi112233 共回答了13个问题
wusi112233 共回答了13个问题 |采纳率100%一、离子键 离子键是由电子转移(失去电子者为阳离子,获得电子者为阴离子)形成的.即正离子和负离子之间由于静电引力所形成的化学键.离子既可以是单离子,如Na+、CL-;也可以由原子团形成;如SO4 2-,NO3-等.离子键的作用力强,无饱和性,无方向性.离子键形成的矿物总是以离子晶体的形式存在.二、共价键 共价键的形成是相邻两个原子之间自旋方向相反的电子相互配对,此时原子轨道相互重叠,两核间的电子云密度相对地增大,从而增加对两核的引力.共价键的作用力很强,有饱和性与方向性.因为只有自旋方向相反的电子才能配对成键,所以共价键有饱和性;另外,原子轨道互相重叠时,必须满足对称条件和最大重叠条件,所以共价键有方向性.共价键又可分为三种:(1)非极性共价键 形成共价键的电子云正好位于键合的两个原子正中间,如金刚石的C—C键.(2)极性共价键 形成共价键的电子云偏于对电子引力较大的一个原子,如Pb—S 键,电子云偏于S一侧,可表示为Pb→S.(3)配价键 共享的电子对只有一个原子单独提供.如Zn—S键,共享的电子对由锌提供,Z:+ ¨..S:=Z n→S 共价键可以形成两类晶体,即原子晶体共价键与分子晶体.原子晶体的晶格结点上排列着原子.原子之间有共价键联系着.在分子晶体的晶格结点上排列着分子(极性分子或非极性分子),在分子之间有分子间力作用着,在某些晶体中还存在着氢键.关于分子键精辟氢键后面要讲到.1年前查看全部
- 下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A. NH4Cl═NH3↑+HCl↑
B. NH3+CO2+H2O═NH4HCO3
C. 2NaOH+Cl2
NaCl+NaClO+H2O△ .
D. 2Na2O2+2CO2═2Na2CO3+O2 十二ly1年前2
十二ly1年前2 -
 domanya 共回答了14个问题
domanya 共回答了14个问题 |采纳率100%解题思路:根据活泼金属和活泼非金属之间易形成离子键,同种非金属元素之间易形成非极性共价键,不同种非金属元素之间易形成极性共价键,化学反应的实质是旧化学键的断裂和新化学键的形成,据此分析解答.A.NH4Cl中含有离子键和极性共价键,则反应物中只有极性共价键、离子键的断裂,故A错误;
B.NH3、CO2、H2O中只含有极性共价键,则反应物中只有极性共价键的断裂,故B错误;
C.NaOH中含有离子键和极性共价键,Cl2中含有非极性共价键,则反应物中有离子键、非极性共价键断裂,没有极性键的断裂,故C错误;
D.Na2O2为含有非极性键的离子化合物,CO2中含有极性键,则反应物中离子键、极性共价键和非极性共价键断裂,故D正确;
故选:D.点评:
本题考点: 分子、原子、离子、元素与物质之间的关系.
考点点评: 本题以化学反应与化学键的关系,难度不大,明确物质中存在化学键的类型是解答本题的关键,注意非金属元素之间易形成共价键,但铵盐除外,铵盐中含有离子键.1年前查看全部
- 如何判断物质存在哪些化学键?比如说NaOH又含离子键又含非极性共价键,而MgCI2只含有离子键呢?
 威海海景楼盘1年前1
威海海景楼盘1年前1 -
 肖蓝 共回答了14个问题
肖蓝 共回答了14个问题 |采纳率92.9%稀有气体不存在化学键,稀有气体是单原子分子,没有化学键,存在的是分子间作用力.1年前查看全部
- 『问』什么是离子键什么是共价件,又什么是极性共价件和非极性共价键?如何区分…
 魅力投影1年前1
魅力投影1年前1 -
 飞哥的传说 共回答了19个问题
飞哥的传说 共回答了19个问题 |采纳率89.5%离子键一般情况下是金属与非金属所构成的化合物(铵根离子除外),其中,有一种元素完全失去电子形成相应的阳离子,同时另一种物质得到电子形成相应的阴离子.
共价键指的是由两种物质共用电子对所形成的化学键.
离子化合物中可能含有共价键,有离子键的化合物一定是离子化合物
1.离子键是由离子组成的,是由于阴阳离子的电性作用形成的,由活泼金属与非金属化合得来,例如:CaCl2,NaOH,NaH
2.共价键是由原子组成的,是由于共用电子对(电子云重叠)对两原子核产生的电性作用形成的,由非金属元素间形成单质或化合物时形成共价键,例如:Cl2,CCl4,H2O,HF
3.同种元素的原子间形成的共价键,共用电子对在成键两原子的中间,不向任何一方偏转,这种共价键叫非极性键.
4.不同种元素的原子间形成的键,都是极性键.共用电子对偏向非金属性强原子一方,这种带部分正负电荷叫极性键.1年前查看全部
- NH3中有非极性共价键么
 帅天帆123_gg1年前1
帅天帆123_gg1年前1 -
 紫羽安卡 共回答了22个问题
紫羽安卡 共回答了22个问题 |采纳率81.8%没有,三个N-H都是极性共价键.既含有极性键又含有非极性键的四原子分子有乙炔(C-C间是非极性键,C-H间是极性共价键).1年前查看全部
- 下列元素的院子在形成不同物质时,既能形成离子键又能形成极性共价键和非极性共价键得失
下列元素的院子在形成不同物质时,既能形成离子键又能形成极性共价键和非极性共价键得失
A 钾
B 钙
C 碘 丹上校1年前1
丹上校1年前1 -
 zhxfpek 共回答了18个问题
zhxfpek 共回答了18个问题 |采纳率94.4%K Ca形成离子化合物不形成共价化合物
I:NaI 离子化合物
I2 非极性共价键
HI0 极性共价键
选C1年前查看全部
- 某种离子化合物中可以同时含有离子键极性共价键和非极性共价键
某种离子化合物中可以同时含有离子键极性共价键和非极性共价键
什么物质三个都有? 田野足迹1年前3
田野足迹1年前3 -
 s278523640 共回答了23个问题
s278523640 共回答了23个问题 |采纳率95.7%硫代硫酸铵(NH4)2S2O3是.其中 S=S是非极性键,S=O是极性键,与NH4+是离子键
CH3COONa 也是,所有的羧酸盐都是.1年前查看全部
- 离子化合物中有没有含有非极性共价键的
 051blue1年前1
051blue1年前1 -
 天街星雨 共回答了23个问题
天街星雨 共回答了23个问题 |采纳率95.7%①离子键:阴阳离子间的强烈的相互作用.如NaCl,NaOH等(Na+与Cl-,OH-间);判断依据:一般活泼金属与活泼非金属间的就是;当然有特例:铵盐如NH4SO4,NH4Cl等的NH4+与SO42-,Cl-间的就是离子键,再者AlCl3,BeCl2等间的是共价键.
②共价键:通过共有电子对形成的.如HCl,Cl2,HNO3等;判断依据:一般非金属与非金属间的化学键就是.特例:AlCl3,BeCl2等
共价键又可分:极性共价键(简称极性键)和非极性共价键(简称非极性键),其中极性键和非极性键的判断依据就是看是否是由同种元素构成,如果是,则为极性键,否则就是非极性键.当然判断的前提是他们是共价键.
③金属键:金属阳离子与电子形成的;判断:金属单质中
(2)对于共价化合物来说,根据工价键的极性和分子的空间构型可将分子分为极性分子和非极性分子.
判断一个分子是极性分子还是非极性分子,(前提是共价化合物)通常有三个规律:
1.①由极性键构成的双原子分子就是极性分子,如HCl,HBr;全部由非极性键构成的分子就是非极性分子,如Cl2,I2,P4
②由极性键构成的多原子分子:如果其空间构型是对称的,就是非极性分子,否则就是极性分子.常见的是对称结构的有CO2,CS2,CCl4,CH4,BF3,C2H4,C2H2,苯等等,这些都是非极性分子.
2.多原子分子ABx型的,一般来说如果A的化合价的绝对值=最外层电子数,则这个分子就是非极性分子,如CO2,C为+4=4(最外层电子数),因此CO2是非极性分子
3.多原子分子ABx型的,看A是否有孤对电子,如果有,一般就是极性分子,否则就是非极性的.如:NH3,N的5个电子中有3个和H共用,剩下一对没共用的电子(孤对电子),因此NH3是极性分子.1年前查看全部
- 有两种元素组成的共价化合物可能含有非极性共价键吗
 tt哆嘞咪1年前2
tt哆嘞咪1年前2 -
 331900 共回答了15个问题
331900 共回答了15个问题 |采纳率100%可以使极性共价键CO CO2 SO2 SO3 NO也可以是非极性共价键N2 O2 CL2 H21年前查看全部
- C60是分子晶体 有没有非极性共价键
 wwh22861年前1
wwh22861年前1 -
 忘记可见光 共回答了19个问题
忘记可见光 共回答了19个问题 |采纳率89.5%有,而且有很多C-C 非极性共价键1年前查看全部
- H2分子中只有非极性共价键 这句话对吗?
H2分子中只有非极性共价键 这句话对吗?
答案是不对,很疑惑,是答案错了吗 夜深人静xf1年前2
夜深人静xf1年前2 -
 yuxinsh 共回答了17个问题
yuxinsh 共回答了17个问题 |采纳率88.2%对是非极性共价键1年前查看全部
- 1mol异丁烷有含多少非极性共价键
 乐涩鱼1年前3
乐涩鱼1年前3 -
 myzpced926 共回答了19个问题
myzpced926 共回答了19个问题 |采纳率73.7%(CH3)2CHCH3
有 3个 C-C单键
有 3 mol 非极性键1年前查看全部
- 极性共价键非极性共价键和极性分子非极性分子有什么不同?
 bt雪1年前2
bt雪1年前2 -
 13166294155 共回答了21个问题
13166294155 共回答了21个问题 |采纳率90.5%对于双原子分子,如果由极性键构成则为极性分子,反之为非极性分子 判断极性分子和非极性分子的最本质方法是:极性分子一个分子内正负电荷中心不重合而非极性分子内正负电荷中心是重合的.比如二氧化碳C=O=C正负电荷中心重合于O所以是非极性分子;H-O-H不是直线形的分子,正负电荷中心不重合,所以是极性分子.(1)非极性键:同种原子形成共价键,两个原子吸引电子的能力相同,共同电子对不偏向任何一个原子,电荷在两个原子核附近对称地分布,因此成键的原子都不显电性.这样的共价键称为非极性键.判断方法:由相同元素的原子形成的共价键是非极性键.如单质分子(Xn,n>1),如H2、Cl2、O3、P4等)和某些共价化合物(如C2H2、C2H4、CH3CH2OH等)、某些离子化合物(如Na2O2、CaC2等)含有非极性键.(2)极性键:不同种原子形成共价键,由于不同原子吸引电子的能力不同,使得分子中共用电子对的电荷是非对称分布的.这样的共价键叫做极性键.判断方法:由不同元素的原子形成的共价键一般是极性键.如HCl、CO2、CCl4、SO42-、OH-等都含有极性键.(3)极性键和非极性键的关系:①有的分子中只有非极性键,如H2、Cl2、O3等.②有的分子中只有极性键,如HCl、H2S、CO2、CH4等.③也有的分子中既有极性键、又有非极性键,如H2O2、C2H2、CH3CH2OH等.1年前查看全部
- 下列说法正确的是( )A.气态水中一定无氢键作用B.原子晶体中只存在非极性共价键C.含两种元素的化合物中可能含有非极性
下列说法正确的是( )
A.气态水中一定无氢键作用
B.原子晶体中只存在非极性共价键
C.含两种元素的化合物中可能含有非极性键
D.金属元素和非金属元素形成的化合物一定是离子化合物 小欧飞雁1年前1
小欧飞雁1年前1 -
 燃烧的宇宙 共回答了15个问题
燃烧的宇宙 共回答了15个问题 |采纳率93.3%解题思路:A.气态水分子间距离太远,分子间氢键氢键较难形成,但不是没有没有;
B.原子晶体是原子之间通过共价键形成的晶体,同种元素原子之间形成非极性键,不同原子之间形成极性键,如二氧化硅是原子晶体,晶体中存在极性键;
C.同种元素原子之间形成非极性键,含两种元素的化合物中可能含有非极性键,如H2O2;
D.金属元素和非金属元素形成的化合物不一定是离子化合物.A.气态水分子间距离太远,分子间氢键氢键较难形成,但仍然含有氢键,故A错误;
B.原子晶体是原子之间通过共价键形成的晶体,同种元素原子之间形成非极性键,不同原子之间形成极性键,如二氧化硅是原子晶体,晶体中Si-O键是极性键,故B错误;
C.H2O2中含有氢氧极性键和氧氧非极性键,故C正确;
D.金属元素和非金属元素形成的化合物不一定是离子化合物,如AlCl3,故D错误;
故选C.点评:
本题考点: 极性键和非极性键;离子化合物的结构特征与性质.
考点点评: 本题考查了化合物中存在的化学键以及氢键,难度不大,注意非极性键和极性键的区别.1年前查看全部
- 只有非金属原子才能构成共价键吗举个例子 什么叫极性非极性共价键和配位键
 idmeid1年前1
idmeid1年前1 -
 zhkun1 共回答了23个问题
zhkun1 共回答了23个问题 |采纳率87%氯化铝是特例,金属化合物形成的共价.极性非极性是按分子结构是否对称来划分,对称是非极性,不对称是极性.要想在这点上高分或全分,就要熟悉基本的化合物的分子结构是否对称.1年前查看全部
- 【【化学】什么是极性共价键和非极性共价键?本人上海高一下,化学中等偏上,请用通俗语言解释~
【【化学】什么是极性共价键和非极性共价键?本人上海高一下,化学中等偏上,请用通俗语言解释~
RT looda1年前3
looda1年前3 -
 freesleet 共回答了11个问题
freesleet 共回答了11个问题 |采纳率100%原子间共用电子对而形成的化学键称为共价键
所谓极性,是指原子对共用电子对的吸引,也就是电子云在分子中的偏向.
同种原子形成的分子,原子对共用电子对的吸引力相同,电子没有偏向,所以形成非极性共价键.1年前查看全部
大家在问
- 1英语翻译all pallets and or cartons must arrive as agreed to or a
- 2如图所示,已知AB比AC长2cm,BC的垂直平分线交AB于D,交BC于E,△ACD的周长是14cm,则AB=______
- 3why should we improve our EQ?
- 4一个容器(上小下大)中装有密度分别为 ρ1、ρ2(ρ1<ρ2)的不同液体,它们的分界明显(图甲).这时液体对容
- 5若黄赤交角变大,北京的正午太阳高度和昼长夜短怎么变化? 若角度变小,则地球上太阳直射的范围及北半球副
- 6请说明下列式子是等式,还是方程,或是方程式.
- 7(多选)用现代生物进化理论的观点解释病菌抗药性不断增强的原因是
- 8在下列语句中,其中正确的语句是( ) A.在统计中应用扇形统计图 B.在统计中应用条形统计图 C.在统计中应用哪种统计
- 9what s on the table A.It s a circle B.There is a circle
- 10作文要求:在学习汉字的过程中,你遇到了什么困难,选一件事写一写.
- 112的负(2k+1)次方减2的负(2k-1)次方加2的负2k次方等于多少?
- 12中国历史上为什么盛世王朝之前就有一个短命王朝啊
- 13The hotel wasn’t particularly good.But I _________ in many w
- 14小学语文一年级下学期有哪些课文
- 15将下列词语排列成通顺的语句.1.景色 哩 依然 夏天的 不让 原野 一片青 春天2.只有 时候 樱花 树叶的 花朵 盛开