丁烷在一定条件下可以按两种方式裂解:C4H10→C2H6+C2H4;C4H10→CH4+C3H6,某石油公司实验室对丁烷
 zz花魁2022-10-04 11:39:541条回答
zz花魁2022-10-04 11:39:541条回答)另取丁烷完全裂解后的气体与H2的混合气体10L,已知其中H2的体积分数为x,在一定条件下使其充分反应,反应后气体的体积为VL。请列出V与x的函数关系式。

已提交,审核后显示!提交回复
共1条回复
 ycysmile 共回答了17个问题
ycysmile 共回答了17个问题 |采纳率82.4%- x1/3 V=10 - 10(1-x)/2
- 1年前
相关推荐
- 同分异构体是同种化合物吗?例如:新丁烷 异丁烷不是混在一起,分开就是“新丁烷 异丁烷是同种化合物吗?”
 ee在唱歌9991年前5
ee在唱歌9991年前5 -
 yy老鱼 共回答了22个问题
yy老鱼 共回答了22个问题 |采纳率86.4%看来你也是高一生
化学上,同分异构体是一种有相同化学式,有同样的化学键而有不同的原子排列的化合物.简单地说,化合物具有相同分子式,但具有不同结构的现象,叫做同分异构现象;具有相同分子式而结构不同的化合物互为同分异构体.很多同分异构体有相似的性质. 同分异构体的组成和分子量完全相同而分子的结构不同、物理性质和化学性质也不相同,如乙醇和甲醚.1年前查看全部
- 丁烷和2-甲基丙烷的关系请问是同系物还是同分异构体?
 恨海狂风1年前2
恨海狂风1年前2 -
 al2aasa 共回答了25个问题
al2aasa 共回答了25个问题 |采纳率88%同分异构体
同系物是相差几个CH2性质相同(有共同官能团)的一系列物质
同分异构体是化学是相同,结构式不同的物质1年前查看全部
- 求画出 2-乙基丁烷 的链图画到纸上拍下来谢谢,(我知道这个是错的)
 zhanggengyun1年前0
zhanggengyun1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 以1 溴丁烷和必要的无机试剂制取1,2 二溴丁烷
以1 溴丁烷和必要的无机试剂制取1,2 二溴丁烷
方程式
两个方程式 abai991年前2
abai991年前2 -
 省级分站 共回答了19个问题
省级分站 共回答了19个问题 |采纳率94.7%1 溴丁烷 + Br2 = 1,2 二溴丁烷 + HB1年前查看全部
- 关于丁烷的二溴代物有哪些,请写出它们的结构简式
关于丁烷的二溴代物有哪些,请写出它们的结构简式
正丁烷的二溴代物是有6种吗?异丁烷的二溴代物是有3种吗?求结构简式 面条玉米1年前0
面条玉米1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 丁烷燃烧生成气体分子数计算1.737克的丁烷和氧气完全燃烧 需要氧气几克?生成几摩尔水?总共生成气体摩尔数多少?
 itcyj1年前1
itcyj1年前1 -
 ww有名的人 共回答了24个问题
ww有名的人 共回答了24个问题 |采纳率91.7%1.737克的丁烷物质的量是0.03mol
2C4H10+13O2=8CO2+10H2O
所以需要0.195molO2,即6.24gO2
生成0.15molH2O,即2.7gH2O
总共生成气体摩尔数0.27mol1年前查看全部
- 这个有机物命名对不对,2,3,3-三甲基丁烷
 踏云踩浪1年前1
踏云踩浪1年前1 -
 61132559 共回答了20个问题
61132559 共回答了20个问题 |采纳率85%2,2,3-三甲基丁烷1年前查看全部
- 据报道,北京奥运会“祥云”火炬燃料为丙烷,悉尼奥运会火炬燃料为丁烷和丙烷混合气.
据报道,北京奥运会“祥云”火炬燃料为丙烷,悉尼奥运会火炬燃料为丁烷和丙烷混合气.
(1)常温、同压下,等体积的丙烷和丁烷完全燃烧恢复到原状态,生成二氧化碳的体积比为______
(2)已知丁烷的燃烧热为2880kJ/mol,1mol丙烷和丁烷(物质的量之比1:1)的混合气完全燃烧生成液态水放出的热量为2550kJ.写出丙烷燃烧的热化学方程式______.
(3)标准状况下,1.0mol丙烷和丁烷的混合气和足量氧气混合完全燃烧后,恢复至原状态,混合气体的体积减小了70.0L,混合气体中丙烷和丁烷的体积比为______
(4)标准状况下,a L的某丙烷和丁烷的混合气体,在b L足量氧气中完全燃烧后,恢复到原状态体积为V L,所得气体体积V为______(用a和b表示). 祁连放勋1年前2
祁连放勋1年前2 -
 citiven 共回答了17个问题
citiven 共回答了17个问题 |采纳率100%解题思路:(1)常温、同压下,等体积的丙烷和丁烷物质的量相同,依据碳元素守恒计算;
(2)依据丁烷燃烧热写出热化学方程式,聚合混合物的物质的量和放出热量计算丙烷放出的热量,依据热化学方程式的书写原则写出;
(3)标准状况下,水是液体根据化学方程式的定量系计算;
(4)根据(3)的计算结合碳元素守恒的特征计算得到关系式.(1)常温、同压下,等体积的丙烷和丁烷物质的量相同,完全燃烧恢复到原状态,水为液体,生成二氧化碳的体积比为物质的量之比,依据碳元素守恒得到二氧化碳气体的体积比为3:4;故答案为:3:4;
(2)丁烷的燃烧热为2880kJ/mol,依据燃烧热概念写出热化学方程式为:C4H10(g)+[13/2]O2(g)→4CO2(g)+5H2O(l)△H=-2880kJ/mol;
1mol丙烷和丁烷(物质的量之比1:1)的混合气中丙烷为0.5mol,丁烷为0.5mol;0.5mol丁烷放热1440KJ,所以0.5mol丙烷燃烧放热1110KJ;丙烷燃烧的热化学方程式为;
C3H8(g)+5O2(g)→3CO2(g)+4H2O(l)△H=-2220KJ/mol,
故答案为:C3H8(g)+5O2(g)→3CO2(g)+4H2O(l)△H=-2220KJ/mol;
(3)标准状况下,1.0mol丙烷和丁烷的混合气和足量氧气混合完全燃烧后,恢复至原状态,混合气体的体积减小了70.0L,物质的量为3.125mol;
设丙烷物质的量为X,丁烷物质的量为1-X;
C3H8(g)+5O2(g)→3CO2(g)+4H2O(l)△n
1 3
X 3X
2C4H10(g)+13O2(g)→8CO2(g)+10H2O(l)
2 7
1-X 3.5(1-X)
3X+3.5(1-X)=3.125
X=0.75mol
所以混合气体中丙烷和丁烷的体积比=0.75:(1-0,75)=3:1,
故答案为:3:1;
(4)标准状况下,a L的某丙烷和丁烷的混合气体,在b L足量氧气中完全燃烧后,恢复到原状态体积为V L,所得气体体积V依据化学方程式计算得到:
假设气体全部是丙烷体积为a
C3H8(g)+5O2(g)→3CO2(g)+4H2O(l)△V减小
1 3
a3a
3a=a+b-V
V=b-2a
假设气体全部是丁烷体积为a
2C4H10(g)+13O2(g)→8CO2(g)+10H2O(l)△V减小
2 7
a 3.5a
3.5a=a+b-V
V=b-2.5a
a L的某丙烷和丁烷的混合气体,在b L足量氧气中完全燃烧后,恢复到原状态体积为V L,所得气体体积V为:b-2.5a<V<b-2a,
故答案为:b-2.5a<V<b-2a.点评:
本题考点: 烷烃及其命名;热化学方程式;有关混合物反应的计算.
考点点评: 本题考查了阿伏伽德罗定律的计算应用,混合物的计算应用和判断,烷烃燃烧的热化学方程式的书写方法,燃烧热的概念应用,燃烧前后气体体积的变化计算,题目难度中等.1年前查看全部
- 简单的1道科学题在常温下使用到无气体放出时,钢瓶中常剩余一些液态物质,这些物质最有可能是( )A.乙烷,丙烷和丁烷 B.
简单的1道科学题
在常温下使用到无气体放出时,钢瓶中常剩余一些液态物质,这些物质最有可能是( )
A.乙烷,丙烷和丁烷 B.乙烷和丙烷
C.只有乙烷 D.戊烷和已烷 wendychou1年前1
wendychou1年前1 -
 红桥烟雨 共回答了18个问题
红桥烟雨 共回答了18个问题 |采纳率94.4%D
无气体放出时,刚瓶内压力是大气压.
在正常的压力和温度下只有D的两种烷才能保持液态.
你打错字了,是己烷,不是已烷.1年前查看全部
- 请问怎么用化学方法鉴别环丁烷和丁烷,
 出言成章q1年前1
出言成章q1年前1 -
 心灵之幻 共回答了25个问题
心灵之幻 共回答了25个问题 |采纳率88%使用溴水,环丁烷会褪色,丁烷不褪色1年前查看全部
- 2,2,3 三甲基丁烷有哪几种等效氢
 紫火人生1年前3
紫火人生1年前3 -
 千年白狐狸 共回答了25个问题
千年白狐狸 共回答了25个问题 |采纳率96%有两种1年前查看全部
- 丁烷是液化石油气的成分之一另外完全燃烧后与甲烷完全燃烧后的产物相同写化学
 狗尾巴草的游乐场1年前1
狗尾巴草的游乐场1年前1 -
 fobqi 共回答了22个问题
fobqi 共回答了22个问题 |采纳率95.5%甲烷的化学式:CH4
点燃
CH4+2O2====CO2+2H2O
丁烷的化学式:C4H10
点燃
2C4H10+13O2====8CO2+10H2O1年前查看全部
- 化学燃烧热计算已知丁烷的燃烧热(生成液态水)为2880kj/mol,1mol丙烷和丁烷(物质的量之比为1:1)的混合起完
化学燃烧热计算
已知丁烷的燃烧热(生成液态水)为2880kj/mol,1mol丙烷和丁烷(物质的量之比为1:1)的混合起完全燃烧放出的热量为2550kj.
我想问的是丙烷燃烧的△值怎么算的
 rodman19811年前1
rodman19811年前1 -
 s_2robbit 共回答了27个问题
s_2robbit 共回答了27个问题 |采纳率92.6%2550*2-2880=22201年前查看全部
- 反-1-甲氧基-3-溴环丁烷 手性碳的构型?
反-1-甲氧基-3-溴环丁烷 手性碳的构型?
(就像这样对称位置有取代基的二取代环丁烷或二取代环己烷,手性碳怎样命名?)就是怎样比较手性碳的四个键的大小!
1
CH2—CH—CH3
∣ ∣
CH —CH2
∣3
Br
C1位连接的是甲基,不是甲氧基! 506663771年前1
506663771年前1 -
 521mm521 共回答了18个问题
521mm521 共回答了18个问题 |采纳率94.4%首先按原子序数,序数越小,原子团越小.其次看C链长度,越长的原子团越大.1年前查看全部
- 有一罐气体,重38吨,其中丁烷和丙烷的比是95:5,另一罐气体重20吨它们的比是60:40.要用这两罐气体配置24吨的气
有一罐气体,重38吨,其中丁烷和丙烷的比是95:5,另一罐气体重20吨它们的比是60:40.要用这两罐气体配置24吨的气体,要其比例为70:30.要从这两罐气体中取混合气体各为多少吨?
 baidusha1年前2
baidusha1年前2 -
 pinkyoyo 共回答了17个问题
pinkyoyo 共回答了17个问题 |采纳率82.4%假设从甲罐中取x吨.则从乙罐取了24-x
[0.95x+0.6(24-x)]:[0.05x+0.4(24-x)]=70:30
x=48/7
所以从甲罐中取48/7吨.则从乙罐取了120/7吨1年前查看全部
- 由燃烧热判断相对储能大小,已知:丁烷>异丁烷,石墨
 星际中的等待1年前1
星际中的等待1年前1 -
 朱哥 共回答了19个问题
朱哥 共回答了19个问题 |采纳率89.5%根据已知的话,我们可以判断出:物质排列组成越紧凑(不带支链),则相对的储能就越大.
所以可以得出石墨的相对储能应小于金刚石的相对储能1年前查看全部
- 2,3- 二甲基丁烷的 二氯代物数目多少
2,3- 二甲基丁烷的 二氯代物数目多少
三甲苯的二氯代物几种 我爱步非烟1年前2
我爱步非烟1年前2 -
 liwh_99 共回答了17个问题
liwh_99 共回答了17个问题 |采纳率88.2%2,3- 二甲基丁烷的 二氯代物数目6种
均三甲苯二氯代4种
连三甲苯二氯代9种
偏三甲苯二氯代18种1年前查看全部
- 2,3-二甲基丁烷和2,2,3,3-四甲基 丁烷哪个稳定?
 coolbrain1年前2
coolbrain1年前2 -
 yuyanwifelo 共回答了16个问题
yuyanwifelo 共回答了16个问题 |采纳率81.3%烷烃不存在稳定一说,因为都很稳定,燃烧的话都产生二氧化碳和水.
如果真要比稳定性,那支链多的稳定性差(2,2,3,3-四甲基).1年前查看全部
- 有机物命名的问题 求教!氢我没画出来是2-甲基-3-氯丁烷对还是3-甲基-2-氯丁烷对?该从哪边数起?为什么?还有当卤代
有机物命名的问题 求教!
 氢我没画出来
氢我没画出来
是2-甲基-3-氯丁烷对还是3-甲基-2-氯丁烷对?该从哪边数起?为什么?
还有当卤代烷里同时含有Cl和Br取代基 比如说是2-氯-3-溴戊烷对还是3-溴-2-氯戊烷对?哪一个应该先写前面 为什么.
真心不懂 虚心求教!希望能讲详细点,先谢过了!
氢没画出来 少打了个氢字。 修依果1年前1
修依果1年前1 -
 武儿文秀 共回答了12个问题
武儿文秀 共回答了12个问题 |采纳率100%是2-甲基-3-氯丁烷对
最低原则,写在前面的为大,除非取代基构成词尾,比如3-甲基-2-丁醇,羟基构成词尾【醇】.
2-氯-3-溴戊烷对
优先次序原则.溴原子序数大,优先,写在后面.1年前查看全部
- 只能有一个答案,液化石油气里是加丙烷好还是丁烷好?丁烷的沸点只有负0.5摄氏度,冬天不会很难用吗?
只能有一个答案,液化石油气里是加丙烷好还是丁烷好?丁烷的沸点只有负0.5摄氏度,冬天不会很难用吗?
只能有一个答案,液化石油气里是加丙烷好还是丁烷好?丁烷的沸点只有负0.5摄氏度,冬天不会很难用吗?(这是一道化学题) peyerchang1年前3
peyerchang1年前3 -
 ww_aa 共回答了11个问题
ww_aa 共回答了11个问题 |采纳率100%液化石油气中主要成分就是丙烷和丁烷,现实中也存在你所说的问题,一般一瓶气中总是丙烷用的多,丁烷用的少,用一段时间后比例越来越大.可以想象,一瓶液化石油气中丙烷越多越好,主要是气化速度不一样,温度也不一样,所以,加丙烷好.1年前查看全部
- 详见补充实验证明顺-2-丁烯和反-2-丁烯都能和H2发生反应,你认为生成的丁烷会有区别吗?问什么?请祥答.
 k4smile1年前1
k4smile1年前1 -
 肥瘦搭配 共回答了12个问题
肥瘦搭配 共回答了12个问题 |采纳率91.7%没的,因为碳链的构成是一样的,最后生成的烷即是一样的1年前查看全部
- 用化学方法鉴别下列各组化合物1)丁烷,1-丁炔,2-丁炔2)2-戊烯,1,4-戊二烯,1-戊炔
 雪舞祺洲1年前1
雪舞祺洲1年前1 -
 haiji101 共回答了15个问题
haiji101 共回答了15个问题 |采纳率100%丁烷中加溴水不褪色,另两个褪色.
1-丁炔与溴化氢在过氧化物存在的情况下,反马式加成,将Br加在端C上,然后水解.可以得到羧酸.2-丁炔则不是酸.
再通过任意方法鉴别酸即可.
1-戊炔可以将气体通入银氨溶液中,能生成(紫)红色沉淀的是戊炔,不能的是戊烯.
取2个相等物质的量的HCl,在取没鉴定且同等容量2-戊烯,1,4-戊二烯分别放入,再用PH试纸测,PH值高的是二烯1年前查看全部
- 求助醋酸钠与卤代烃酯化反应!最近在做醋酸钠与3,3-二甲基-1-氯丁烷的酯化反应,催化剂苄基三乙基氯化铵,加部分水溶解醋
求助醋酸钠与卤代烃酯化反应!
最近在做醋酸钠与3,3-二甲基-1-氯丁烷的酯化反应,催化剂苄基三乙基氯化铵,加部分水溶解醋酸钠,反应温度94度,但是几乎没有产物生成. adde08191年前3
adde08191年前3 -
 忆纷飞 共回答了17个问题
忆纷飞 共回答了17个问题 |采纳率100%氯代烃的活性要足够 才能获得满意的结果1年前查看全部
- 高2烯烃题某液态烃和溴水发生加成反应生成2,3一二溴一2一甲基丁烷.则该烃是:A3一甲基一1一丁烯B2一甲基一2一丁烯C
高2烯烃题
某液态烃和溴水发生加成反应生成2,3一二溴一2一甲基丁烷.则该烃是:
A3一甲基一1一丁烯
B2一甲基一2一丁烯
C2一甲基一1一丁烯
D1一甲基一2一丁烯
将2L乙烯和1l甲烷的混合气体在150c,1.01*10的5次方Pa下与20升空气充分燃烧后,所得混合气体的体积是;
A13L
B23L
C11L
D9L benben39731731年前1
benben39731731年前1 -
 gogozj 共回答了17个问题
gogozj 共回答了17个问题 |采纳率100%B
B1年前查看全部
- 如何检验甲丙醚及丁烷大神们帮帮忙
 我在水里游1年前1
我在水里游1年前1 -
 显蓝儿 共回答了25个问题
显蓝儿 共回答了25个问题 |采纳率92%1、通入少量氧气或加入少量过氧化氢;2、往所得物中注入硫酸亚铁溶液,充分震荡 溶液颜色加深的是甲丙醚,反之则是丁烷1年前查看全部
- 将0.4mol丁烷完全燃烧后生成的气体全部缓慢通入1L 2mol/L的NaOH中,生成的Na2CO3和NaHCO3的物质
将0.4mol丁烷完全燃烧后生成的气体全部缓慢通入1L 2mol/L的NaOH中,生成的Na2CO3和NaHCO3的物质的量之比为?
 m_j_j_20051年前3
m_j_j_20051年前3 -
 心情舞墨 共回答了23个问题
心情舞墨 共回答了23个问题 |采纳率87%额 楼上失误了 过程结果自相矛盾
1:3
丁烷化学式C4H10,因此0.4mol完全燃烧生成0.4x4=1.6molCO2 跟2molNaOH,
假设生成Na2CO3 Xmol,NaHCO3 Ymol,根据Na元素守恒,我们知道2X+ Y=2
根据C元素守恒,我们知道 X + Y=1.6 所以X=0.4mol,Y=1.2mol 两者之比为1比3
还有分步反应法 因为是缓慢通过
所以可以分别写出2NaOH+CO2=Na2CO3+H2O
Na2CO3+CO2+H2O=2NaHCO3
注意比例系数 计算可得出同样答案1年前查看全部
- 某液化石油气由丙烷和丁烷组成,其质量分数分别为80%和20%,它们燃烧的热化学方程式分别为:
某液化石油气由丙烷和丁烷组成,其质量分数分别为80%和20%,它们燃烧的热化学方程式分别为:
C3H8(g)+5O2(g)=3CO2(g)+4H2O(g)+2200kJ
2C4H10(g)+13O2(g)=8CO2(g)+10H2O(g)+5800kJ
有一质量为0.80kg,容积为4.0L的铝壶,将一壶20℃的水烧开需消耗液化石油气0.056kg,试计算该燃料的利用率,已知水的比热为4.245kJ/(kg·℃),铝的比热为0.88kJ/(kg·℃) 麻木的心何时复苏1年前1
麻木的心何时复苏1年前1 -
 caoxiuming2466 共回答了19个问题
caoxiuming2466 共回答了19个问题 |采纳率89.5%Q(H2O)=4.245*4.0*80=1358.4kJ
Q(壶)=0.88*0.8*80=56.32kJ
Q(丙)=0.056*1000*80%*2200/44=2240kJ
Q(丁)=0.056*1000*20%*5800/116=560kJ
利用率:(1358.4+56.3)/(2240+560)=50.5%1年前查看全部
- 丁烷受热分解可生成CH4、C2H6、C2H4、C3H6四者的混合气体,此混合气体对H2的相对密度是( )
丁烷受热分解可生成CH4、C2H6、C2H4、C3H6四者的混合气体,此混合气体对H2的相对密度是( )
A. 29
B. 14.5
C. 10
D. 无法确定 beyondcz0011年前1
beyondcz0011年前1 -
 lovefei03 共回答了29个问题
lovefei03 共回答了29个问题 |采纳率89.7%解题思路:在裂化过程中气体的质量守恒,平均摩尔质量大小取决于裂化后混合气体的物质的量的大小.丁烷结构简式为:CH3-CH2-CH2-CH3,断键位置只有两种,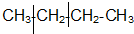 ,故可生成甲烷、丙烯、乙烷、乙烯四种物质,设丁烷的物质的量为1mol,裂解成CH4和C3H6为xmol,裂解成C2H6和C2H4为ymol,根据
,故可生成甲烷、丙烯、乙烷、乙烯四种物质,设丁烷的物质的量为1mol,裂解成CH4和C3H6为xmol,裂解成C2H6和C2H4为ymol,根据
=[m/n]结合相对密度等于摩尔质量之比求解..M 设丁烷的物质的量为1mol,裂解成CH4和C3H6为xmol,裂解成C2H6和C2H4为ymol,x+y=1mol,
依题意:C4H10
△
CH4+C3H6 C4H10
△
C2H6+C2H4
xmol xmol xmol ymol ymol ymol
则裂解后生成CH4、C2H6、C2H4、C3H6四者的混合气体总物质的量为:2x+2y=2mol,
混合气体的
.
M=[m/n]=[1mol×58g/mol/2mol]=29g/mol,根据相对密度之比等于摩尔质量之比,此混合气体对H2的相对密度是29:2=14.5:1,
故选B.点评:
本题考点: 化学方程式的有关计算.
考点点评: 本题考查了丁烷的裂解的计算,掌握裂解原理是解题的关键,注意丁烷总是1分子丁烷裂解成2分子气态烃,题目难度中等.1年前查看全部
- 个苯环上连了一个甲基,甲基上一个氢原子被一个环丁烷取代,该化合物是脂环化合物还是芳香化合物?
 aouhoo1年前1
aouhoo1年前1 -
 依山之水 共回答了15个问题
依山之水 共回答了15个问题 |采纳率93.3%芳香化合物.
希望对你有帮助O(∩_∩)O~1年前查看全部
- 应该是2—氯—3—甲基丁烷还是3—甲基—2—氯丁烷
 myjdlove1年前1
myjdlove1年前1 -
 Q选择 共回答了21个问题
Q选择 共回答了21个问题 |采纳率95.2%中文命名按顺序规则,个人觉得应该是2-甲基-3-氯丁烷1年前查看全部
- 有机物沸点越高越容易液化吗比如丙烷和丁烷
 dxjx1年前1
dxjx1年前1 -
 野狼2008 共回答了26个问题
野狼2008 共回答了26个问题 |采纳率100%是的,沸点越高,比如物质甲沸点30度,物质乙沸点0度,则常温下甲物质呈液态而乙物质呈气态.1年前查看全部
- (Ⅰ)在室温下,向某一容积固定的真空容器内充入丁烷(气)和氧气,使容器内混合气的总压强达到p 1 ,点火燃烧,氧气反应完
(Ⅰ)在室温下,向某一容积固定的真空容器内充入丁烷(气)和氧气,使容器内混合气的总压强达到p 1 ,点火燃烧,氧气反应完全,冷却至室温后容器内气体的总压强为p 2 。
(1)若丁烷燃烧的生成物只有H 2 O(液)和CO 2 ,则p 2 /p 1 = 。
(2)若 =0.64,则反应前混合气中丁烷的物质的量分数= 。
=0.64,则反应前混合气中丁烷的物质的量分数= 。
(Ⅱ)设阿伏加德罗常数为N A ,在常温常压下气体的摩尔体积为V m L·mol -1 ,O 2 和N 2 的混合气体a g含有b个分子,则c g该混合气体在常温常压下所占的体积应是 L。 冰点丫丫不哭1年前1
冰点丫丫不哭1年前1 -
 lszhf 共回答了19个问题
lszhf 共回答了19个问题 |采纳率78.9%(Ⅰ)(1) (2)16% (Ⅱ)
(2)16% (Ⅱ)
(Ⅰ)2C 4 H 10 +13O 2 点燃,8CO 2 +10H 2 O
(1)由于室温下水为液体,所以 =
= =
= 。
。
(2)由于 =0.64>
=0.64> ,所以丁烷过量,产物为CO、CO 2 和H 2 O(l),根据碳元素守恒,CO和CO 2 的物质的量之和等于4倍的C 4 H 10 的物质的量,设C 4 H 10 、O 2 的物质的量分别为a、b,则
,所以丁烷过量,产物为CO、CO 2 和H 2 O(l),根据碳元素守恒,CO和CO 2 的物质的量之和等于4倍的C 4 H 10 的物质的量,设C 4 H 10 、O 2 的物质的量分别为a、b,则 =0.64,
=0.64, =
= ,所以丁烷的物质的量分数为
,所以丁烷的物质的量分数为 ×100%=16%。
×100%=16%。
(Ⅱ)设该混合气体的摩尔质量为M,则: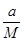 ·N A =b,则M=
·N A =b,则M= (g·mol -1 ),所以c g该气体在常温常压下所占的体积应是
(g·mol -1 ),所以c g该气体在常温常压下所占的体积应是 ·V m =
·V m = ·V m =
·V m = 。
1年前查看全部
。
1年前查看全部
- 下列有机物命名正确的是( )A. 3,3-二甲基丁烷B. 3-甲基-2-乙基戊烷C. 2,3-二甲基戊烯D. 3-甲基
下列有机物命名正确的是( )
A. 3,3-二甲基丁烷
B. 3-甲基-2-乙基戊烷
C. 2,3-二甲基戊烯
D. 3-甲基-1-戊烯 weis1年前1
weis1年前1 -
 鬼树 共回答了18个问题
鬼树 共回答了18个问题 |采纳率72.2%解题思路:A、丁烷的命名中出现:3.3-二甲基,说明没有满足取代基编号之和最小原则;
B、命名中出现2-乙基,说明选取的主链不是碳原子数最多的;
C、烯烃的命名,必须指出官能团碳碳双键的位置;
D、根据烯烃的命名原则进行判断.A、3,3-二甲基丁烷,编号时必须满足取代基的编号之和最小,正确命名为:2,2-二甲基丁烷,故A错误;
B、3-甲基-2-乙基戊烷,有机物的命名中不能出现2-乙基,说明选取的主链不是最长的,正确命名为:3,4-二甲基己烷,故B错误;
C、2,3-二甲基戊烯,没有写出官能团双键的位置,正确命名如:2,3-二甲基-1-戊烯,故C错误;
D、3-甲基-1-戊烯,烯烃命名,编号从碳碳双键一端开始,找出双键的位置,该命名符合要求,故D正确;
故选D.点评:
本题考点: 有机化合物命名.
考点点评: 本题考查了有机物的命名,注意烯烃、炔烃的命名,必须指出官能团碳碳双键、碳碳三键的位置,本题难度不大.1年前查看全部
- 丁烷受热裂解可生成CH4、C2H6、C2H4、C3H6四种气体的混合气体,此混合气体的平均相对分子质量为
丁烷受热裂解可生成CH4、C2H6、C2H4、C3H6四种气体的混合气体,此混合气体的平均相对分子质量为
A:58 B:29 C:20 D:无定值
我只求解题思路,至于答案是什么都无所谓. 孤烟白驹1年前1
孤烟白驹1年前1 -
 风铃33 共回答了16个问题
风铃33 共回答了16个问题 |采纳率93.8%29
丁烷的分子量为58
丁烷裂解生成甲烷和丙烯:或乙烷和乙烯
不论是以上那种,1mol丁烷都会分解成2mol气体,所以分子量=58/2=291年前查看全部
- 求助一道高二化学题1L 丁烷与不饱和烃A(同温同压下为气态)的混合气体完全燃烧后在同温同压下得到3.4LCO2,请填写该
求助一道高二化学题
1L 丁烷与不饱和烃A(同温同压下为气态)的混合气体完全燃烧后在同温同压下得到3.4LCO2,请填写该混合气体可能的组合 和体积比 龚xx1年前1
龚xx1年前1 -
 守侯SUN 共回答了21个问题
守侯SUN 共回答了21个问题 |采纳率90.5%丁烷为C4H10,1L完全燃烧可以生成4LCO2,那么这个不饱和烃A的C肯定小于4,如果是乙烯和乙炔,那么体积比为:C4H10:C2H4(C2H2)=7:3:;如果是如果是丙烯或者丙炔,那么体积比为:C4H10:C3H4(C3H6)=2:3.1年前查看全部
- (2005•芜湖)有一种气体打火机,内装燃料是液态丁烷.通常情况下,丁烷是气体,人们是用______的方法将其变为液态的
(2005•芜湖)有一种气体打火机,内装燃料是液态丁烷.通常情况下,丁烷是气体,人们是用______的方法将其变为液态的.从微观角度看,丁烷能从气态变为液体说明丁烷分子______.
 放逐的云1年前1
放逐的云1年前1 -
 cheery_xxr 共回答了7个问题
cheery_xxr 共回答了7个问题 |采纳率100%解题思路:使气体液化的方式有两种:降低温度和压缩体积;
丁烷由气态变为液态,体积减小,说明了分子之间有空隙.丁烷是气体,在常温下压缩体积可以使气体液化;
气态可以变为液态,体积减小就说明分子之间存在空隙.
故答案为:压缩体积;分子间存在间隙.点评:
本题考点: 分子动理论的基本观点;液化方法及其应用.
考点点评: 打火机是生活中常见的物体,应用了液化和分子动理论的知识,体现了物理知识来源于生活并应用于生活的物理理念.1年前查看全部
- 有关丙烷,叙述正确的是A 是天然气的主要成分 B 光照条件下能够发生取代反应 C 与丁烷互为同分异构体 D分子中碳原子在
有关丙烷,叙述正确的是
A 是天然气的主要成分 B 光照条件下能够发生取代反应 C 与丁烷互为同分异构体 D分子中碳原子在一条直线上 dzj_dzj1年前2
dzj_dzj1年前2 -
 lichengyu198412 共回答了20个问题
lichengyu198412 共回答了20个问题 |采纳率90%【B】
天然气主要成分是甲烷CH4,故A错;丙烷3个碳原子,丁烷4个碳原子,应该属于同系物,同分异构是只化学式相同,结构不同的两个分子,故C错;碳原子是SP3杂化类型所以丙烷只有两个碳原子是在一条直线上,1年前查看全部
- 1.丁烷受热完全分解可生成CH4.C2H6.C2H4.C3H6四者的混合气体,此混合气体对H2的相对密度为( )
1.丁烷受热完全分解可生成CH4.C2H6.C2H4.C3H6四者的混合气体,此混合气体对H2的相对密度为( )
A.29 B.14.5 C.10 D.无法确定
2.石油气是含有碳原子数目较少的烷烃,某石油气充分燃烧后,在相同条件下测得生成的CO2的体积是该石油气的1.2倍,则石油气中一定含有( )
A.甲烷 B.丁烷 C.戊烷 D.己烷
3.1体积某烃的蒸汽完全燃烧生成的CO2比水蒸气少1体积(在同温、同压下测定).0.1mol该烃完全燃烧的产物被碱石灰吸收,碱石灰增重39克.求该烃的分子式. 2886592001年前2
2886592001年前2 -
 tanghuab 共回答了21个问题
tanghuab 共回答了21个问题 |采纳率95.2%1、选B.无论哪种方式分解,都是气体物质的量增加1倍,所以平均相对质量减小一半.
2、选A.因为可以看出分子内平均含1.2个碳原子,而只有甲烷碳原子数少于1.2.
3、1体积某烃的蒸汽完全燃烧生成的CO2比水蒸气少1体积,说明这是烷烃.0.1mol该烃完全燃烧的产物被碱石灰吸收,碱石灰增重39克,说明生成二氧化碳和水一共39克.
设分子式为CxH2x+2,则4.4x+1.8*(x+1)=39,x=6,所以该烃的分子式是C6H121年前查看全部
- 一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能
一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料说法正确的是( )
A. 在熔融电解质中,O2-由负极移向正极
B. 电池的总反应是:2C4H10+13O2═8CO2+10H2O
C. 通入空气的一极是负极,电极反应为:O2+4e-=2O2-
D. 通入丁烷的一极是负极,电极反应为:C4H10-26e-+13O2-=4CO2+5H2O 2005jie111年前3
2005jie111年前3 -
 保持专注 共回答了20个问题
保持专注 共回答了20个问题 |采纳率85%解题思路:在丁烷燃料电池中,负极发生氧化反应,电极反应式为C4H10-26e-+13O2-=4CO2+5H2O,正极发生还原反应,电极反应式为O2+4e-=2O2-,总反应式为2C4H10+13O2═8CO2+10H2O,在原电池中,阴离子向负极移动,阳离子向正极移动.A、在原电池中,阴离子向负极移动,阳离子向正极移动,故A错误;
B、燃料电池的总反应与燃料燃烧的化学方程式相同,为2C4H10+13O2═8CO2+10H2O,故B正确;
C、通入空气的一极是正极,发生还原反应,电极反应为:O2+4e-=2O2-,故C错误;
D、丁烷具有还原性,在丁烷燃料电池中,负极发生氧化反应,电极反应式为C4H10-26e-+13O2-=4CO2+5H2O,故D正确.
故选BD.点评:
本题考点: 化学电源新型电池;电极反应和电池反应方程式.
考点点评: 本题考查化学电源新型电池,侧重于电极反应方程式的考查,题目难度中等,注意从正负极发生的变化结合电解质的特点书写电极反应式.1年前查看全部
- 下列大小关系正确的是A.熔点:乙烷>2,2—二甲基戊烷>2,3—二甲基丁烷>丙烷B.含氢量:甲烷>乙烷>乙烯>乙炔>苯C
下列大小关系正确的是
A.熔点:乙烷>2,2—二甲基戊烷>2,3—二甲基丁烷>丙烷
B.含氢量:甲烷>乙烷>乙烯>乙炔>苯
C.密度:CCl4>H2O>苯
D.相同物质的量物质完全燃烧耗O2量:己烷>环己烷>苯 yaya_swy1年前4
yaya_swy1年前4 -
 thn9h 共回答了13个问题
thn9h 共回答了13个问题 |采纳率84.6%选C,D
A看支链,支链越多,熔点越低,写一下
B都化成CHx的形式,就可以比较
C萃取实验中,四氯化碳沉在水底,苯浮在水面上
D上述三个全是烃,写出化学式,己烷C6H14,环己烷,相当于己烯C6H12,苯C6H6,1mol烃所需氧气的公式:CxHy所(x+y/4)mol O21年前查看全部
- 下列物质的沸点的排列顺序正确的是:1.2-甲基丙烷 2.丁烷 3.乙醛 4.乙酸 5·乙醇 A.1 > 2 >
下列物质的沸点的排列顺序正确的是:1.2-甲基丙烷 2.丁烷 3.乙醛 4.乙酸 5·乙醇 A.1 > 2 >
(在不知道各物质的具体沸点的情况下)
有没有人知道啊 在阳光中拥抱1年前1
在阳光中拥抱1年前1 -
 zhijieli121 共回答了24个问题
zhijieli121 共回答了24个问题 |采纳率79.2%1、2都是气体,后面都是液体,所以1、2应该小于后面物质的熔沸点.
1是异丁烷,2是正丁烷,支链越多,熔沸点越低,所以1乙醇>乙醛
所以由大到小的顺序为:4>5>3>2>1.1年前查看全部
- 下列五种烷烃:(1)2-甲基丁烷(2)2,2一二甲基丙烷(3)戊烷(4)丙烷(5)丁烷把他们沸点从高到低排列
下列五种烷烃:(1)2-甲基丁烷(2)2,2一二甲基丙烷(3)戊烷(4)丙烷(5)丁烷把他们沸点从高到低排列
写明原因, 安乐卫生巾1年前1
安乐卫生巾1年前1 -
 tykecn 共回答了13个问题
tykecn 共回答了13个问题 |采纳率92.3%3>1>2>5>4
比较原则:
1.先看C原子数,C原子数多的沸点高.
2.C原子数相同,支链越多,沸点越低.
原因:烷烃是通过分子间作用力形成晶体的.分子间作用力的大小与分子间的距离成反比,支链多,分子必不能靠得很近,也即距离比没有支链或支链少的分子间距离要大,则分子间作用力就小,分子间作用力小,则熔沸点低.1年前查看全部
- 2,2,3-三甲基丁烷的一氯代物有多少种?
 augustthird1年前1
augustthird1年前1 -
 mm 共回答了14个问题
mm 共回答了14个问题 |采纳率92.9%3种1年前查看全部
- 丁烷(X)燃烧的化学方程式:2X+13O 2 =8CO 2 +10H 2 O,则丁烷的化学式为( ) A.C 5 H
丁烷(X)燃烧的化学方程式:2X+13O 2 =8CO 2 +10H 2 O,则丁烷的化学式为( ) A.C 5 H 10 B.C 4 H 8 C.C 4 H 10 D.C 5 H 12  梦幻海韵1年前1
梦幻海韵1年前1 -
 compaqnc4010 共回答了14个问题
compaqnc4010 共回答了14个问题 |采纳率92.9%由反应的化学方程式2X+3O 2 ═8CO 2 +10H 2 O,可判断反应后8CO 2 、10H 2 O中总共含有碳原子数为8、氢原子数为20、氧原子数为26,而反应前的13O 2 中含有氧原子数为26.根据化学变化前后原子的种类、数目不变,可判断物质X的2个分子中含8个碳原子、20个氢原子,则每个X的分子由4个碳原子、10个氢原子构成,则物质X的化学式为C 4 H 10 .
故选C.1年前查看全部
- (急)丁烷气体是怎样被密封在打火机中的?
 北极星星光灿烂1年前1
北极星星光灿烂1年前1 -
 记事本1314 共回答了20个问题
记事本1314 共回答了20个问题 |采纳率80%高压使其液化而密封1年前查看全部
- 1.以丁烷为例说明同分异构现象2.有机化合物的简单计算
 55660131年前1
55660131年前1 -
 默默0504 共回答了21个问题
默默0504 共回答了21个问题 |采纳率100%CH3-CH2-CH2-CH3 丁烷
CH3-CH-CH3
……1
……CH3 异丁烷
省略号为了占位子的忽略它
设有机物为CxHyOz
燃烧用方程式CxHyOz+(x-y/4-z/2)O2=xCO2+(y/2)H2O
其他条件就要看具体题目了,比如式量,STP下相对于氢气的密度等等,情况太多了一天一夜讲不完1年前查看全部
- 丁烷的一氯代物(高中化学)丁烷的一氯代物有几种,分别是哪几种,简要描述一下取代位置就可以了
 顶花带刺的萝卜1年前7
顶花带刺的萝卜1年前7 -
 zoudg 共回答了10个问题
zoudg 共回答了10个问题 |采纳率80%一共有4种!
首先要找有几种c链异构 ,一共有2种
C-C-C-C C-C-C
|
C
在找对称
C-C-|-C-C 所以此种C链有2种氯代物C-C-C-C 或C-C-C-C
对称 | |
根据CH4的分子结构可知C上的4个氢都是等位的和
C-C-C 带*号的3个C都是等位的就是说还有两种是
* | * C-C-C- 和 |
C | C-C-C
* C |
C 共4种1年前查看全部
- 城市居民用的石油气主要成分是丁烷,在使用的过程中,常有一些杂质以液态沉积于钢瓶中,这种杂质是
城市居民用的石油气主要成分是丁烷,在使用的过程中,常有一些杂质以液态沉积于钢瓶中,这种杂质是
A.丙烷和丁烷
B.乙烷和丙烷
C.乙烷和戊烷
D.戊烷和己烷 珊瑚_6603091年前1
珊瑚_6603091年前1 -
 泰山樵夫 共回答了23个问题
泰山樵夫 共回答了23个问题 |采纳率91.3%答案D
常温下,烃中含碳原子数不大于4的以气体形式存在,故液态杂质中,烃分子中的碳原子数必大于4,故选D.1年前查看全部
- 生活中的化学 简单选择题城市居民用的石油气主要成分是丁烷,在使用过程中,常有一些杂质以液态沉积于钢瓶中,这些杂质是?丙烷
生活中的化学 简单选择题
城市居民用的石油气主要成分是丁烷,在使用过程中,常有一些杂质以液态沉积于钢瓶中,这些杂质是?
丙烷和丁烷 乙烷和丙烷 乙烷和戊烷 戊烷的己烷 br179021年前1
br179021年前1 -
 四月祭魂 共回答了16个问题
四月祭魂 共回答了16个问题 |采纳率87.5%戊烷的己烷
戊烷的沸点为36.1
己烷的沸点为69.2
常温下(约20摄氏度)无法达到1年前查看全部
大家在问
- 1a乘6/7=b乘6/5=c乘1,其中abc为自然数,切都不为零,吧abc三个数从小到大排列顺序
- 2我们都乐意分享我们的快乐用英语怎么说
- 3三棱锥表面积一道数学题,一个正方体 棱长1M截去一个三棱锥 求三棱锥的表面积是从棱长的一半截下去的有图..dd
- 4多元隐函数求二阶偏导数
- 5陈胜吴广策划起义所采取的策略是
- 6已知x-12的平方根是正负根号13,2x+y-6的立方根是2,求-3xy的算术平方根
- 7下列开发建设的做法,与可持续发展不相符的是 [ ] A.华北地区农业生产
- 8已知x的2次方+y的2次方=7,XY=-1,求式子4x的2次方-(3xy+4y的2次方)-(11xy-5y2的次方)-3
- 9(2011•武昌区)递等式计算:
- 10适当形式填空,1.Children feel (exciting)on Childre,s day.2.Thanks f
- 11work短语
- 124/5=12/15=28/35=( )除以10
- 13我的世界你曾来过 作文
- 14是否开运动会是天气而定,英语翻译,语法要正确
- 15Does She Love You Like I Do?
