50%有效成分的多菌灵,每50克兑多少升水
 chewang60292022-10-04 11:39:542条回答
chewang60292022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 留恋云眉 共回答了17个问题
留恋云眉 共回答了17个问题 |采纳率94.1%- 按1000倍算是50×1000÷1000=50公斤 约为两喷壶
- 1年前
 belinevip 共回答了6个问题
belinevip 共回答了6个问题 |采纳率- 5o斤
- 1年前
相关推荐
- 肥皂的成分请问肥皂的主要成分是什么?就是能够洗干净东西的成分是什么?它是碱性的吗?那么碱性和肥皂的有效成分有什么关系吗?
 wuqingming1年前1
wuqingming1年前1 -
 jasmine8282 共回答了13个问题
jasmine8282 共回答了13个问题 |采纳率92.3%肥皂是一种羧酸的钠盐,R-CO2Na,其中R基团一般是不同的,是各种烃基.R-是憎水基,羧基是亲水基.在硬水中肥皂与Ca2+,Mg2+等形成了凝乳状物质,脂肪酸钙盐等,即通常说的“钙肥皂”而成为了无用的除垢剂.将软化剂加入硬水中可以除去硬水离子,使肥皂发挥作用.1年前查看全部
- 怎样检测盐酸的有效成分
 梦思1年前1
梦思1年前1 -
 小蒙嘎 共回答了19个问题
小蒙嘎 共回答了19个问题 |采纳率94.7%加入过量硝酸银,将沉淀干燥后称量,将其质量除以143.5,及得氯离子物质的量,则盐酸的物质的量可得1年前查看全部
- (2002•长沙)人的胃液中含有少量盐酸,胃酸过多时常服用“胃舒平”[其有效成分为Al(OH)3]来治疗,其治疗的原理是
(2002•长沙)人的胃液中含有少量盐酸,胃酸过多时常服用“胃舒平”[其有效成分为Al(OH)3]来治疗,其治疗的原理是(用化学方程式表示)______.
 yhrlovesxx1年前1
yhrlovesxx1年前1 -
 liangcai 共回答了17个问题
liangcai 共回答了17个问题 |采纳率82.4%解题思路:书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据客观事实、遵守质量守恒定律.氢氧化铝与稀盐酸反应生成氯化铝和水.
该反应的化学方程式为:3HCl+Al(OH)3═AlCl3+3H20.
故答案为:3HCl+Al(OH)3═AlCl3+3H20.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;酸的化学性质.
考点点评: 本题主要考查化学方程式的书写,难度较小.1年前查看全部
- 草木灰是很好的农家肥料(其有效成分是KCO),下图
 我是ss张老五1年前1
我是ss张老五1年前1 -
 kissboy3314 共回答了25个问题
kissboy3314 共回答了25个问题 |采纳率92%1设实际消耗稀盐酸的质量为X
K2CO3 + 2 HCl = = = = 2 KCl + H2O +CO2
2*36.5 44
X 2.2g
2*36.5 / X = 44/ 2.2g
X=3.65g
2.设50g草木灰中K2CO3的质量为Y
K2CO3 + 2 HCl = = = = 2 KCl + H2O +CO2
138 44
Y 2.2g
138 / Y = 44 / 2.2g
Y=6.9g
K2CO3的质量分数为= (6.9g/50g) *100% =13.8%
3.K2CO3中 含K量= (39*2/138) *100%
K2CO3的质量分数= 50kg * 13.8%
K元素的质量 m(K)= 50kg*13.8% *(39 *2 /138 )*100% = 3.9kg
答:略1年前查看全部
- 草木灰是农村常心的一种肥料(其有效成分是K2CO3).某兴趣小组为了测定草木灰中K2CO3的含量,取现有的草木灰138g
草木灰是农村常心的一种肥料(其有效成分是K2CO3).某兴趣小组为了测定草木灰中K2CO3的含量,取现有的草木灰138g,逐滴加入足量的稀盐酸,共得到22gCO2.
请计算:
(1)K2CO3的相对分子质量
(2)该草木灰中K2CO3的质量分数 1jianqingxin1年前1
1jianqingxin1年前1 -
 ericxuek 共回答了13个问题
ericxuek 共回答了13个问题 |采纳率100%(1)39*2+12+16*3=138
(2)设生成22g的CO2要Xg K2CO3.
K2CO3+HCl=KCl+H2O+ CO2 ↑
138 44
xg 22g
138/xg = 44/ 22g
解得:x=69g
69/138*100%=50%
答:该草木灰中K2CO3的质量分数为50% .1年前查看全部
- 消毒用的白醋中有效成分是醋酸,其化学式为CH3COOH,质量分数是6.25%.请依次写
消毒用的白醋中有效成分是醋酸,其化学式为CH3COOH,质量分数是6.25%.请依次写
出组成醋酸的元素名称——- 其元素质量比为-—— C元素的质量分数是———
若八(2)班用白醋1000克,则实际用醋酸——克 fsfdfdf1年前1
fsfdfdf1年前1 -
 黄金女 共回答了19个问题
黄金女 共回答了19个问题 |采纳率94.7%HCO,4:24:32; 24/60=40%; 62.5g1年前查看全部
- 草木灰是农村常用的一种肥抖(其有效成分是K2CO3).某兴趣小组为了测定草木灰中K2CO3的含量,取现有的草木灰7.5g
草木灰是农村常用的一种肥抖(其有效成分是K2CO3).某兴趣小组为了测定草木灰中K2CO3的含量,取现有的草木灰7.5g,逐滴加入稀盐酸至恰好完全反应,消耗稀盐酸45 g,过滤除去杂质,得到溶液45.5 g,〔已知K2CO3的化学性质与Na2CO3,化学性质相似.假设草木灰中除K2CO3外,其它物质均不溶于水,也不与盐酸反应〕
试计算:①该草木灰中K2CO3的质量分数.
②反应后所得溶液中溶质的质量分数. 北三环马甸1年前1
北三环马甸1年前1 -
 szszlty 共回答了21个问题
szszlty 共回答了21个问题 |采纳率85.7%(1)
设7.5g该草木灰中K2CO3为xg.
K2CO3+2HCl=2KCl+CO2+H2O
138 149 44
x
产生CO2的质量为:44*x/138g
所以:x+45-44*x/138=45.5
x=0.734g
该草木灰中K2CO3的质量分数为:0.734*100%/7.5=9.79%
(2)
产生KCl的质量为:0.734*149/138=0.793g
反应后所得溶液中溶质的质量分数:0.793*100%/45.5=1.74%1年前查看全部
- 下列4种有机物是某些药物中的有效成分,对此4种有机物的有关说法正确的是 [
下列4种有机物是某些药物中的有效成分,对此4种有机物的有关说法正确的是  [ ]
[ ]A.4种有机物都是芳香化合物
B.4种有机物环上的氢原子若被氯原子取代,其一氯代物都只有2种
C.等物质的量的4种有机物与足量的NaOH溶液反应,阿司匹林消耗的NaOH最多
D.4种有机物都能与Na反应,也都能发生水解反应 sealzsj1年前1
sealzsj1年前1 -
 非天游人 共回答了13个问题
非天游人 共回答了13个问题 |采纳率100%C1年前查看全部
- 某补钙品(有效成分为碳酸钙,其它成分不含钙元素)的说明中标明含钙量为30%.李琳同学为了检验该产品,取l0g补钙品放入1
某补钙品(有效成分为碳酸钙,其它成分不含钙元素)的说明中标明含钙量为30%.李琳同学为了检验该产品,取l0g补钙品放入100g稀盐酸中,HCI与补钙品的有效成分刚好完全反应(其它成分不与盐酸反应).反应后剩余固体和液体的总质量比反应前减少了2.2g.求:(1)补钙品中实际含钙的质量分数是多少?(2)所用稀盐酸中溶质的质量分数是多少?
 88757971年前1
88757971年前1 -
 小旦 共回答了26个问题
小旦 共回答了26个问题 |采纳率96.2%CaCO3+2HCl=CaCl2+H2O+CO2
40(Ca)73 44↑
2 3.65 2.2
(1)补钙品中实际含钙的质量分数是多少?
2/10=20%
(2)所用稀盐酸中溶质的质量分数是多少?
3.65/100=3.65%1年前查看全部
- 大蒜有增味、杀菌等作用,被誉为“天然广谱抗菌素.”大蒜中的两种有效成分大蒜辣素和蒜氨酸的相关资料如下表所示:
大蒜有增味、杀菌等作用,被誉为“天然广谱抗菌素.”大蒜中的两种有效成分大蒜辣素和蒜氨酸的相关资料如下表所示:
成 分 性 质
大蒜辣素 C6HloS20 无色油状液体,有臭味,难溶于水
蒜氮酸 C6HloNOaS 无色针状晶体,元气味,易溶于水
(1)大蒜辣素的相对分子质量为————,蒜氨酸中碳、氢元素的质量比为————.
(2)表格中提供的是大蒜辣素和蒜氨酸的 ———— 性质(填“物理”或“化学”),从宏观和微观角度分析它们属于不同物质的原因 ——————. wa4979450521年前1
wa4979450521年前1 -
 flying2488 共回答了15个问题
flying2488 共回答了15个问题 |采纳率86.7%大蒜辣素的相对分子质量为162.27
蒜氨酸中碳、氢元素的质量比为72:10
物理性质 属于不同物质的原因:元素种类不同 原子个数不同1年前查看全部
- 英语翻译气相色谱测定气雾杀虫剂中的混合有效成分.
 ywbguan1年前1
ywbguan1年前1 -
 xueliangsz 共回答了23个问题
xueliangsz 共回答了23个问题 |采纳率87%In gas chromatography determination gas spray pesticide mix effective component1年前查看全部
- 次氯酸钙是漂白粉的有效成分,是一种应用广泛的消毒剂,其化学式为Ca(CIO)2,请回答下列问题 (1)次氯
次氯酸钙是漂白粉的有效成分,是一种应用广泛的消毒剂,其化学式为Ca(CIO)2,请回答下列问题 (1)次氯
次氯酸钙是漂白粉的有效成分,是一种应用广泛的消毒剂,其化学式为Ca(CIO)2,请回答下列问题
(1)次氯酸钙中,钙元素的质量分数为多少?28.6g次氯酸钙中含钙元素多少克?
(2)多少克次氯酸钙中含氧元素48g? 飞翔的阿六1年前1
飞翔的阿六1年前1 -
 萧飞VS木鱼 共回答了19个问题
萧飞VS木鱼 共回答了19个问题 |采纳率94.7%次氯酸钙分子量:143,钙的质量分数40/143=27.97% ; 28.6*27.97=8克
含氧元素48克,需要次氯酸钙48*143/32=214.5克1年前查看全部
- 细菌的细胞壁破碎剂的有效成分是什么物质?
 美丽心情22271年前2
美丽心情22271年前2 -
 zouyp1982 共回答了12个问题
zouyp1982 共回答了12个问题 |采纳率100%细菌细胞壁破碎可以采用溶菌酶破壁,不过一般可以采用物理方法比如反复冻融,渗透压,超声波等等,1年前查看全部
- 下列三种有机物是某些药物中的有效成分.
下列三种有机物是某些药物中的有效成分.

下列说法正确的是( )
a. 三种有机物都能发生水解反应
b. 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
c. 将等物质的量的三种物质加入氢氧化钠溶液中,对羟基桂皮酸消耗氢氧化钠最多
d. 使用fecl3溶液和稀***鉴别这三种有机物 daichaojian1年前3
daichaojian1年前3 -
 mshuang06 共回答了23个问题
mshuang06 共回答了23个问题 |采纳率91.3%解题思路:A、能水解的有机物中含有:酯基、肽键或是卤代烃等;
B、苯环上有几种类型的氢原子,其一氯代物就有几种;
C、酚羟基、酯基、羧基均能和氢氧化钠发生反应;
D、酚类物质与FeCl3溶液发生显色反应,稀硫酸作用下能让酯水解.A、只有阿司匹林能水解,故A错误;
B、阿司匹林苯环上有4种类型的氢原子,其一氯代物就有4种,其余的两个一氯代物有2种,故B错误;
C、酚羟基、酯基、羧基均能和氢氧化钠发生反应,假设有机物的物质的量均为1mol,对羟基桂皮酸消耗氢氧化钠2mol,布洛芬消耗氢氧化钠1mol,阿司匹林消耗氢氧化钠3mol,故阿司匹林最多,故C错误;
D、与FeCl3溶液发生显色反应,变为紫色的为对羟基桂皮酸,稀硫酸作用下阿司匹林水解会出现和氯化铁发生显色反应的酚类物质,故D正确.
故选D.点评:
本题考点: 有机物分子中的官能团及其结构.
考点点评: 本题是一道有关有机物基础知识点考查的题目,可以根据所学知识来回答,难度不大.1年前查看全部
- 工业上用纯净的消石灰与滤器反应制取漂白粉,已知漂白粉的有效成分为55.17%,求消石灰的利用率
工业上用纯净的消石灰与滤器反应制取漂白粉,已知漂白粉的有效成分为55.17%,求消石灰的利用率
工业上用纯净的消石灰与滤器反应制取漂白粉,已知漂白粉的有效成分为55.17%,求消石灰的利用率 愕然1年前1
愕然1年前1 -
 perrywang 共回答了18个问题
perrywang 共回答了18个问题 |采纳率100%2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O 设 生成物总质量是x,则漂白粉的质量可以求出来 根据漂白粉次氯酸钙的式量可以求出次氯酸钙的物质的量 为n,则其中钙元素的物质的量为n,相应的参与反应生成次氯酸钙的氢氧化钙的物质的量就是n mol,根据方程式 次氯酸钙是n mol,可以求出总的参与反应的氢氧化钙的物质的量m mol.用n除以 m就行了1年前查看全部
- 天然药物有效成分的提取方法有几种?采取这些方法提取的依据是什么
 nschem1年前1
nschem1年前1 -
 人工顶帖真累 共回答了25个问题
人工顶帖真累 共回答了25个问题 |采纳率96%①溶剂提取法:利用溶剂把天然药物中所需要的成分溶解出来,而对其它成分不溶解或少溶解.
②水蒸气蒸馏法:利用某些化学成分具有挥发性,能随水蒸气蒸馏而不被破坏的性质.
③升华法:利用某些化合物具有升华的性质.1年前查看全部
- 4.天然药物研究中有效成分不适于用加热法提取的是( )
4.天然药物研究中有效成分不适于用加热法提取的是( )
A.酯 类 B.挥 发 油
C.甾 醇 D.生 物 碱
某中药总生物碱中含有季铵碱(A)、酚性叔胺碱(B)、非酚性叔胺碱(C)及水溶性多糖(D)和脂肪烷烃(E)
分离的时候会出现碱水层和氯仿层 其中碱水层里会弄出沉淀,这些沉淀是分离出了哪个物质? xzzq1年前1
xzzq1年前1 -
 xx-湘西xx 共回答了18个问题
xx-湘西xx 共回答了18个问题 |采纳率94.4%A.酯 类,不适合,加热会发生脂水解反应
B.挥 发 油,必须加热
C.甾 醇 ,甾醇热稳定加不加热都行
D.生 物 碱,这个种类很多,提取方法不一
季铵碱(A)季铵碱极性较大,不溶于氯仿,加酸成盐溶于水,加碱沉淀1年前查看全部
- 某补钙品(有效成分为碳酸钙其他成分不含钙元素)的说明中表明含钙量为30% 某同学为了检验该产品取10g补钙品放入100g
某补钙品(有效成分为碳酸钙其他成分不含钙元素)的说明中表明含钙量为30% 某同学为了检验该产品取10g补钙品放入100g稀盐酸中 HCl与该补钙品的有效成分刚好完全反应 (其他成分不于盐酸反应)反应后剩余固体和液体的总质量比反应前减少了2.2g (1)补钙品中实际含钙的质量分数是多少(2)所用碳酸钙中溶质的质量分数是多少
 TY76639771年前1
TY76639771年前1 -
 lulujan 共回答了15个问题
lulujan 共回答了15个问题 |采纳率73.3%设补钙品中碳酸钙的质量为x,稀盐酸中HCl的质量为y
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 73 44
x y 2.2g
100:44=x:2.2g
x=5g
73:44=y:2.2g
y=3.65g
CaCO3中钙元素的质量分数是:
补钙品中钙元素的实际含量:
盐酸的溶质质量分数:
答:该补钙品实际含钙量为20%,所用盐酸的溶质质量分数为3.65%1年前查看全部
- 几个化学常识人造刚玉是什么?熔点很高吗?玛瑙研钵干什么用?可以磨擦固体反应物进行无溶剂合成吗?.变色眼镜的有效成分
 benniaolk1年前1
benniaolk1年前1 -
 wyh017 共回答了14个问题
wyh017 共回答了14个问题 |采纳率85.7%人造刚玉是三氧化二铝,熔点是 很高.玛瑙研钵是用来固体小颗粒磨成粉末,不能.
变色眼镜地有效成分是硝酸银.1年前查看全部
- 天然药物有效成分的提取方法有几种?采取这些方法提取的依据是什么
 1514161年前1
1514161年前1 -
 jyk666 共回答了16个问题
jyk666 共回答了16个问题 |采纳率87.5%①溶剂提取法:利用溶剂把天然药物中所需要的成分溶解出来,而对其它成分不溶解或少溶解.
②水蒸气蒸馏法:利用某些化学成分具有挥发性,能随水蒸气蒸馏而不被破坏的性质.
③升华法:利用某些化合物具有升华的性质.1年前查看全部
- 下列三种有机物是某些药物中的有效成分.
下列三种有机物是某些药物中的有效成分.

下列说法正确的是( )
a. 三种有机物都能发生水解反应
b. 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
c. 将等物质的量的三种物质加入氢氧化钠溶液中,对羟基桂皮酸消耗氢氧化钠最多
d. 使用fecl3溶液和稀***鉴别这三种有机物 想念漂泊的日子1年前4
想念漂泊的日子1年前4 -
 梦毁qq 共回答了12个问题
梦毁qq 共回答了12个问题 |采纳率66.7%解题思路:A、能水解的有机物中含有:酯基、肽键或是卤代烃等;
B、苯环上有几种类型的氢原子,其一氯代物就有几种;
C、酚羟基、酯基、羧基均能和氢氧化钠发生反应;
D、酚类物质与FeCl3溶液发生显色反应,稀硫酸作用下能让酯水解.A、只有阿司匹林能水解,故A错误;
B、阿司匹林苯环上有4种类型的氢原子,其一氯代物就有4种,其余的两个一氯代物有2种,故B错误;
C、酚羟基、酯基、羧基均能和氢氧化钠发生反应,假设有机物的物质的量均为1mol,对羟基桂皮酸消耗氢氧化钠2mol,布洛芬消耗氢氧化钠1mol,阿司匹林消耗氢氧化钠3mol,故阿司匹林最多,故C错误;
D、与FeCl3溶液发生显色反应,变为紫色的为对羟基桂皮酸,稀硫酸作用下阿司匹林水解会出现和氯化铁发生显色反应的酚类物质,故D正确.
故选D.点评:
本题考点: 有机物分子中的官能团及其结构.
考点点评: 本题是一道有关有机物基础知识点考查的题目,可以根据所学知识来回答,难度不大.1年前查看全部
- 为了保证病人血液中的有效成分不流失,血液透析仪内的溶液,除什么外,其成分和浓度应与什么完全一致,
为了保证病人血液中的有效成分不流失,血液透析仪内的溶液,除什么外,其成分和浓度应与什么完全一致,
并保持多少度? maintop1年前1
maintop1年前1 -
 忧郁女王 共回答了22个问题
忧郁女王 共回答了22个问题 |采纳率95.5%为了保证病人血液中的有效成分不流失,血液透析仪内的溶液,除尿素外,其成分和浓度应与血浆完全一致,并保持37度.1年前查看全部
- 一瓶100ml的赤霉素有效成分为4%怎么稀释成0.01%
一瓶100ml的赤霉素有效成分为4%怎么稀释成0.01%
一瓶100ml的赤霉素有效成分为4%,需要加多少水能稀释成0.01%赤霉素 世玉20031年前1
世玉20031年前1 -
 兰夜随想 共回答了25个问题
兰夜随想 共回答了25个问题 |采纳率100%这瓶100ml溶液中有4g赤霉素.
0.01%就是万分之一.笨一点想,把这100ml放到300ml水里,共400ml,里面有4g,是1%,再加到3600ml(3.6升或3.6公斤)水里,就是又稀释了10倍,就是0.1%了.再取36.4公斤水,把这3.6公斤的稀释液倒进去,总量是40公斤,里面有4g赤霉素,浓度就是0.01%了.
如果对浓度要求不是太高的话,直接把这100ml倒入40公斤(或40升)水里,混合均匀,赤霉素浓度大致就是0.01%.1年前查看全部
- 某补钙品(有效成分为碳酸钙,其它成分不含钙元素)的说明中标明含钙量为30%.
某补钙品(有效成分为碳酸钙,其它成分不含钙元素)的说明中标明含钙量为30%.
李琳同学为了检验该产品,取l0g补钙品放入100g稀盐酸中,HCI与补钙品的有效成分刚好完全反应(其它成分不与盐酸反应).反应后剩余固体和液体的总质量比反应前减少了2.2g.求:(1)补钙品中实际含钙的质量分数是多少?(2)所用稀盐酸中溶质的质量分数是多少? gxfuq1年前1
gxfuq1年前1 -
 scouts 共回答了22个问题
scouts 共回答了22个问题 |采纳率95.5%反应后剩余固体和液体的总质量比反应前减少了2.2g——放出的二氧化碳的质量.
CaCO3+2HCl=CaCl2+H2O+CO2
100 73 44
X Y 2.2
X=5克;Y=3.65克.
(1)补钙品中实际含钙的质量分数=5*40/(100*10)=20%;
(2)所用稀盐酸中溶质的质量分数=3.65/100=3.65%.1年前查看全部
- 工业上用纯净的消石灰与滤器反应制取漂白粉,已知漂白粉的有效成分为55.17%,求消石灰的利用率
 lizhen58021年前1
lizhen58021年前1 -
 开心吗 共回答了25个问题
开心吗 共回答了25个问题 |采纳率92%消石灰与氯气的反应2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O,有效成分为Ca(ClO)2,分子量为143,同时还产生了氯化钙,分子量为111.现在漂白粉中的Ca(ClO)2含量为55.17%,即可知CaCl2的含量为55.17%*111/143=42.82%,由于消石灰纯净,因此反应后剩余的消石灰含量为100%-55.17%-42.82%=2.01%,而Ca(OH)2分子量为74,设有100g漂白粉,则其中含有55.17gCa(ClO)2,2.01g未反应的消石灰,而产生这么多Ca(ClO)2已反应的消石灰量为55.17g*(74*2)/143=57.10g,因此消石灰的利用率=57.10/(57.10+2.01)=96.60%1年前查看全部
- 煤固硫剂的有效成分及固硫原理是什么?
煤固硫剂的有效成分及固硫原理是什么?
煤固硫剂的种类很多,但原理应是一致的,即使单质硫以化合物的形式固定,防止其生成二氧化硫,但我想知道其具体是如何反应,而把硫固定的 巴雷西郑1年前1
巴雷西郑1年前1 -
 泡和 共回答了14个问题
泡和 共回答了14个问题 |采纳率71.4%比如煤中加入钙基(CaO) 固硫原理为:
CaO+SO2=CaSO3
2CaSO3+O2=2CaSO4
(CaSO4与水作用生成生石膏CaSO4·2H2O)
1,烟气湿淋.用石灰乳喷淋含SO2烟气.
2,有效直接利用.用Na2SO3吸收SO2,又利用NaHSO3分解产生高浓度的SO2,作为制取硫酸的原料.1年前查看全部
- 有一不纯的尿素样品,测知含氮元素44.8%,若已知杂质不含氮元素,此化肥的有效成分尿素的质量分数为?
 ed_sws_sws1年前1
ed_sws_sws1年前1 -
 yu2008-2008 共回答了20个问题
yu2008-2008 共回答了20个问题 |采纳率85%纯尿素的含氮量为:2*14/60=46.67%
尿素的质量分数为:44.8%/46.67%=95.99%1年前查看全部
- 标况下VL氯气与过量消石灰完全反应所得漂白粉中有效成分次氯酸钙的质量为
 梦妍11051年前1
梦妍11051年前1 -
 海豚湾恋人SM 共回答了23个问题
海豚湾恋人SM 共回答了23个问题 |采纳率73.9%2CA(OH)2+2CL2=CACL2+CA(CLO)2+2H2O
44.8L 143
vl x=143*VL/44.8L1年前查看全部
- 开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示。下列有关说法正确的是
开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示。下列有关说法正确的是
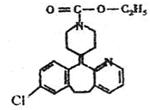
A.该有机物易溶于水 B.分子中含有四个六元环,其中有一个是苯环 C.1mol分子水解后只能得到2mol产物 D.1mol分子最多能与7molH 2 发生加成反应  一恋清风1年前1
一恋清风1年前1 -
 网上通辑犯 共回答了21个问题
网上通辑犯 共回答了21个问题 |采纳率85.7%D
根据有机物的结构和所含的官能团判断有机物的性质。该有机物不易溶于水,所以A错误;分子中含有三个六元环,一个七元环,所以B错误;1mol分子水解后可以得到2mol产物,所以C错误。1年前查看全部
- 初2下.科学题目人体缺钙容易产生骨质疏松症,每天服用某种钙片5片(每片1克)可以补充钙元素0.4克,已知该钙片的有效成分
初2下.科学题目
人体缺钙容易产生骨质疏松症,每天服用某种钙片5片(每片1克)可以补充钙元素0.4克,已知该钙片的有效成分是葡萄糖酸钙其化学式为(C6H11O7)2Ca,回答下面的问题.
(1)每片钙片中含葡萄糖酸钙的质量分数为多少?
请列出标准的计算格式.懂的请回答.
问题(1) 忘记补上了, sd8807251年前1
sd8807251年前1 -
 Anson_su 共回答了18个问题
Anson_su 共回答了18个问题 |采纳率83.3%(C6H11O7)2Ca的相对分子质量为:430
Ca占(C6H11O7)2Ca的百分数为:4/43
五片钙片补0、4g,每片补0、08g,即每片钙片含钙量为0、08g.
那么,每片钙片里含(C6H11O7)2Ca为0、08/(4/43)=0、86g
每片钙片为1g,即含葡萄糖酸钙的质量分数为86%1年前查看全部
- 为防止为川地震灾区的病菌传播,防疫人员大量使用了“漂白粉”来杀菌消毒,“漂白粉”的有效成分为次氯酸
为防止为川地震灾区的病菌传播,防疫人员大量使用了“漂白粉”来杀菌消毒,“漂白粉”的有效成分为次氯酸
Ca(Clo)2 .请回答:(1)次氯酸钙中金属元素是 (写元素符号);氧、氯、钙三种元素的质量比为 ;(2)次氯酸钙中氯元素的质量分数是多少(精确到0.1%); (3)若灾区饮用水每50kg至少需要漂白粉250g,则消毒一桶水(约20kg)至少须加漂白粉多少g? 夜行动物不飞刀1年前1
夜行动物不飞刀1年前1 -
 海风子 共回答了24个问题
海风子 共回答了24个问题 |采纳率95.8%金属元素是Ca
钙.氯.氧的质量比是40:(2*35.5):(2*16)=40:71:32
次氯酸钙(Ca(ClO)2)中的氯元素的质量分数=100%*35.5*2/(40+35.5*2+16*2)=49.7%
消毒一桶水(约20千克)至少需要漂白粉250*20/50=100(g)1年前查看全部
- 米醋是家庭常用的调味品 某同学通过上网查询 得知米醋的有效成分是醋酸 (化学式为
 传奇英雄加里波第1年前1
传奇英雄加里波第1年前1 -
 秋叶飘如雪 共回答了19个问题
秋叶飘如雪 共回答了19个问题 |采纳率84.2%2CH3COOH+Na2CO3=2CH3COONa+CO2+H2O
120 106 44
x 5.3g y
120/x=106/5.3g=44/y
x=6g
y=2.2g
(1)放出二氧化碳2.2克
(2)醋中醋酸的质量分数 6g/180g*100%=3.3%1年前查看全部
- 漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙[Ca(ClO)2].次氯酸钙可发生如下反应、
漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙[Ca(ClO)2].次氯酸钙可发生如下反应、
Ca(ClO)2+X+H2O=CaCO3↓+2HCiO,则X的化学式为?次氯酸钙中氯元素的化合价为? 待浮花浪蕊都尽1年前2
待浮花浪蕊都尽1年前2 -
 louie_wht 共回答了15个问题
louie_wht 共回答了15个问题 |采纳率93.3%2HCiO应该是2HClO
X的化学式为CO2
次氯酸钙中氯元素的化合价为+1价.1年前查看全部
- 我国固有的领土钓鱼岛海域,海底蕴藏着丰富的宝藏,包括石油,稀土金属,可燃冰.可燃冰的有效成分主要是___(填化学式)
 亚伊欧1年前1
亚伊欧1年前1 -
 hongxiaoli 共回答了16个问题
hongxiaoli 共回答了16个问题 |采纳率87.5%co21年前查看全部
- 下列说法符合事实的是( )A. 漂白精的有效成分是NaClOB. 碘化钾的水溶液遇淀粉现蓝色C. 硫在空气中燃烧生成S
下列说法符合事实的是( )
A. 漂白精的有效成分是NaClO
B. 碘化钾的水溶液遇淀粉现蓝色
C. 硫在空气中燃烧生成SO2,在纯氧中生成SO3
D. 漂白精露置空气中变质,既发生氧化反应又发生非氧化还原反应 八成新人类1年前1
八成新人类1年前1 -
 wangjunyue 共回答了25个问题
wangjunyue 共回答了25个问题 |采纳率88%解题思路:A、次氯酸盐是漂粉精的有效成分;
B、碘单质遇到淀粉会变蓝色;
C、硫在空气中、氧气中燃烧生成的都是SO2;
D、漂白精露置空气中变质,先是发生复分解反应生成次氯酸,再是次氯酸分解的过程.A、漂白精的有效成分是NaClO,故A正确;
B、碘单质遇到淀粉会变蓝色,碘化钾遇到淀粉不会变色,故B错误;
C、硫在空气中、氧气中燃烧生成的都是SO2,不会得到三氧化硫,故C错误;
D、漂白精露置空气中变质,先是次氯酸盐和空气成分之间发生复分解反应生成次氯酸,该反应为非氧化还原反应,再是次氯酸分解的过程,该反应是氧化还原反应,故D错误.
故选A.点评:
本题考点: 氯、溴、碘及其化合物的综合应用.
考点点评: 本题综合考查学生卤素单质以及化合物的性质和应用知识,注意知识的归纳和梳理是解题的关键,难度中等.1年前查看全部
- 科学家在海洋中发现了一种冰状物质可燃冰?其有效成分为甲烷,下列说法不正确的是( )
科学家在海洋中发现了一种冰状物质可燃冰?其有效成分为甲烷,下列说法不正确的是( )
A. 甲烷是烃类物质中相对分子质量最小的物质
B. 点燃甲烷前,不用检验其纯度
C. 甲烷难溶于水
D. 可燃冰是一种极具潜力的能源 duje1231年前1
duje1231年前1 -
 鄱湖虾草 共回答了18个问题
鄱湖虾草 共回答了18个问题 |采纳率83.3%解题思路:A.甲烷由C、H元素组成的最简单的烃;
B.可燃性气体点燃前需要检验纯度;
C.甲烷密度比空气小,难溶于水;
D.甲烷为清洁能源.A.甲烷是由C、H元素组成的最简单的烃,故A正确;
B.甲烷易燃,点燃前需要检验纯度,故B错误;
C.甲烷难溶于水,故C正确;
D.甲烷完全燃烧生成二氧化碳和水,为清洁能源,故D正确.
故选B.点评:
本题考点: 甲烷的化学性质;化石燃料与基本化工原料.
考点点评: 本题考查甲烷的性质,难度不大,注意基础知识的积累.1年前查看全部
- 以下是我们日常生活中常用各种清洗剂.名称洗涤灵洁厕灵炉具清洁剂活氧彩漂污渍爆炸盐产品样式有效成分或
以下是我们日常生活中常用各种清洗剂.名称洗涤灵洁厕灵炉具清洁剂活氧彩漂污渍爆炸盐产品样式有效成分或
以下是我们日常生活中常用各种清洗剂.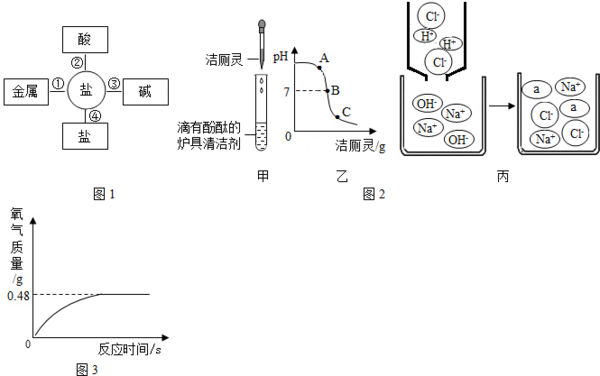
(1)我们使用洗涤灵清洗餐具上的油污,这是因为它具有______的功能.名称 洗涤灵 洁厕灵 炉具清洁剂 活氧彩漂 污渍爆炸盐 产品样式 




有效成分
或功能清洗油污 盐酸 氢氧化钠 过氧化氢 过碳酸钠
(2)清除以下物质,可以使用洁厕灵的是______填字母序号).
A.铁锈B.水垢(主要成分为碳酸钙和氢氧化镁)
C.油渍D.氢气还原氧化铜实验后,试管内壁残留的红色固体
(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2.将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,这一反应了体现如图1中______(选填①②③④)性质关系.
(4)将洁厕灵滴入炉具清洁剂中,如图2甲所示.
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外)______;此时溶液可用如图2乙中______点处(选填A、B、C)表示.
②若反应后溶液pH为7,如图2丙中a微粒的化学式为______.
(5)①“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(-O-O-).据此推测,下列物质中,可用作杀菌消毒剂的是______(填序号).
②氧化氢溶液常用于医用消毒,某兴趣小组为测定一瓶久置的医用过氧化氢溶液中溶质质量分数.他们取该溶液51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图3所示.试计算该过氧化氢溶液中溶质的质量分数.(写出计算过程)______.H-O-H 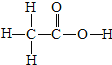
O=C=O 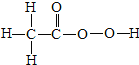
A B C D
 雪白兔子1年前1
雪白兔子1年前1 -
 潇郁 共回答了25个问题
潇郁 共回答了25个问题 |采纳率92%(1)洗洁精洗涤餐具上的油污主要是利用洗涤剂可以将油污和水溶在一起而除去,这种作用称作乳化作用.故填:乳化;
(2)洁厕灵的成分是盐酸,可以和铁锈反应生成溶于水物质除去,可以和水垢反应生成易溶于水的物质除去,但不能和油污反应,故填:AB;
(3)据题给信息可以知道爆炸盐和水反应生成了碳酸钠和双氧水,而碳酸钠可以和盐酸反应生成二氧化碳,这是体现了盐与酸反应的性质;
(4)氢氧化钠溶液呈碱性,而酚酞遇碱变红色,所以将酚酞滴入溶液变为红色,说明反应过程中,氢氧化钠有剩余,故此时溶质为氯化钠和氢氧化钠;此时溶液可用如图2乙中的A点表示;氢氧化钠可以和稀盐酸反应生成氯化钠和水,反应方程式为:HCl+NaOH=NaCl+H2O.而氯化钠在溶液中以钠离子和氯离子的形式存在,结合图中信息可以知道a为水;
(5)①A、该物质的分子结构中不含“过氧基”结构,该物质不可作杀菌消毒剂;故A不正确;
B、该物质的分子结构中不含“过氧基”结构,该物质不可作杀菌消毒剂;故B不正确;
C、该物质的分子结构中不含O原子,因此没有“过氧基”结构,该物质不可作杀菌消毒剂;故C不正确;
D、该物质的分子结构中含有“过氧基”结构,该物质可作杀菌消毒剂;故D正确;
故选D.
②[解]设:过氧化氢溶液中溶质的质量为X
2H2O2
MnO2
.
2H2O+O2↑…(1分)
68 32
X 0.48g
68/32=X/0.48g…(1分)X=1.02g…(1分)
过氧化氢溶液中溶质的质量分数=1.02g/51g×100%=2% …(1分)
答:过氧化氢溶液中溶质的质量分数2%.…设及答 合计(1分)
故答案为:(1)乳化(2)AB (3)②(4)①NaClNaOH;A②H2O(5)①D
②[解]设:过氧化氢溶液中溶质的质量为X
2H2O2
MnO2
.
2H2O+O2↑…(1分)
68 32
X 0.48g
68/32=X/0.48g…(1分)X=1.02g…(1分)
过氧化氢溶液中溶质的质量分数=1.02g/51g×100%=2% …(1分)
答:过氧化氢溶液中溶质的质量分数2%.…设及答 合计(1分)1年前查看全部
- 为防止汶川地震灾区的病菌传播,防疫人员大量使用了“漂白粉”来杀菌消毒,“漂白粉”的有效成分为次氯酸钙{Ca(ClO)2}
为防止汶川地震灾区的病菌传播,防疫人员大量使用了“漂白粉”来杀菌消毒,“漂白粉”的有效成分为次氯酸钙{Ca(ClO)2}.若灾区饮用水每50Kg至少需要加漂白粉250K,则消毒一桶水(约20Kg)至少需要加漂白粉多少克?
 jrx331年前5
jrx331年前5 -
 littleduck01 共回答了21个问题
littleduck01 共回答了21个问题 |采纳率85.7%是不是九年级,不过这与本题看来关系不大.这个直接按比例计算就行了.
饮用水每50Kg至少需要加漂白粉250K,50Kg=50000g,20Kg=20000g.
设消毒一桶水(约20Kg)至少需要加漂白粉X克.
由已知,得
50000:250=20000:X
解之,得X=250*20000/50000=100克
答略.1年前查看全部
- 次氯酸盐是一些 ,和 的有效成分,如次氯酸钠是84消毒液的有效成分,次氯酸钙是漂白粉的有效成分,
次氯酸盐是一些 ,和 的有效成分,如次氯酸钠是84消毒液的有效成分,次氯酸钙是漂白粉的有效成分,
他们与 反应生成次氯酸,起到漂白的作用,有关反应方程式为 . wang13yu101年前3
wang13yu101年前3 -
 月伴弯 共回答了20个问题
月伴弯 共回答了20个问题 |采纳率90%消毒剂 漂白剂
CO2和水
Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO
2NaClO + H2O+CO2=2HClO + Na2CO31年前查看全部
- 语文病句改错:感冒利咽冲剂的有效成分是板蓝根、桔梗、金银花、蔗糖和焦糊颗粒组成的.请问哪里错了?
 blueblitz1年前1
blueblitz1年前1 -
 唯一的爱人 共回答了20个问题
唯一的爱人 共回答了20个问题 |采纳率100%有效成分与是.组成的有重复,可改为:
感冒利咽冲剂的有效成分是板蓝根、桔梗、金银花、蔗糖和焦糊颗粒
或者:
感冒利咽冲剂是由板蓝根、桔梗、金银花、蔗糖和焦糊颗粒组成的1年前查看全部
- (2012•资阳)漂白粉常用于灾区消毒杀菌,其有效成分为Ca(ClO)2,其中氯元素的化合价为______;工业上制漂白
(2012•资阳)漂白粉常用于灾区消毒杀菌,其有效成分为Ca(ClO)2,其中氯元素的化合价为______;工业上制漂白粉,是将氯气通入石灰乳发生如下反应制得:2Ca(OH)2+2Cl2=X+Ca(ClO)2+2H2O,产物中X的化学式为______;漂白粉易吸收空气中的水分和二氧化碳而硬化变质,最终生成的硬化物是(填写化学式)______,所以漂白粉要密封保存,开封及时使用.
 hainan-hx1年前1
hainan-hx1年前1 -
 Antigone_H 共回答了15个问题
Antigone_H 共回答了15个问题 |采纳率93.3%解题思路:根据在化合物中正负化合价代数和为零,结合Ca(ClO)2的化学式进行解答.
由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
根据漂白粉的有效成分、质量守恒定律进行分析解答.钙元素显+2价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+2x+(-2)×2=0,则x=+1.
根据反应的化学方程式2Ca(OH)2+2Cl2=X+Ca(ClO)2+2H2O,反应物中钙、氧、氢、氯原子个数分别为2、4、4、4,反应后的生成物中钙、氧、氢、氯原子个数分别为1、4、4、2,根据反应前后原子种类、数目不变,则每个X分子由1个钙原子和2个氯原子构成,则物质X的化学式为CaCl2.
漂白粉的有效成分为Ca(ClO)2,吸收空气中的水分和二氧化碳而硬化变质,最终生成的硬化物是碳酸钙.
故答案为:+1;CaCl2;CaCO3.点评:
本题考点: 有关元素化合价的计算;质量守恒定律及其应用.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、原子守恒来确定物质的化学式等即可正确解答.1年前查看全部
- (2012•诏安县质检)被医学界誉为“天然广谱抗菌素”的大蒜,它的辛辣味正是其中的有效成分--大蒜辣素产生的,已知大蒜辣
(2012•诏安县质检)被医学界誉为“天然广谱抗菌素”的大蒜,它的辛辣味正是其中的有效成分--大蒜辣素产生的,已知大蒜辣素的化学式为C6H10S2O,则该物质由______种元素组成,其中碳元素与氧元素的质量比是______,硫元素的质量分数为______.
 只看一二1年前0
只看一二1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 这杀虫水怎样算水的比例?注:(1)公顷用制剂量=亩用制剂量X15 (2)总有效成分量浓度值(毫克/千
这杀虫水怎样算水的比例?

注:(1)公顷用制剂量=亩用制剂量x15
(2)总有效成分量浓度值(毫克/千克)=(制剂含量x1000000)÷制剂稀释倍数
高效氯***菊酯有效成分含量:4.5% 剂型:乳油
问那个“5-27毫升/亩”究竟一亩地要用多少毫升的水来兑? 凭轩孤闻雪压霜1年前1
凭轩孤闻雪压霜1年前1 -
 halfaton 共回答了17个问题
halfaton 共回答了17个问题 |采纳率76.5%“5-27毫升/亩”,就是要保证一亩地内打进去该药5-27毫升,通常人工背负喷雾器,每喷壶水量在14-15公斤(每公斤=1升=1000毫升),每亩地用两喷壶药水混合液,能够打完.所以一亩地要用2喷壶水,将5-27毫升的药液(为保证药效建议取上限27毫升)平分到2喷壶内即可.1年前查看全部
- 氯气和石灰乳反应化学方程式,漂白粉的有效成分,
氯气和石灰乳反应化学方程式,漂白粉的有效成分,
还有漂白粉溶于水后,受空气中CO2作用的离子方程式 wingning1年前1
wingning1年前1 -
 两面赔 共回答了20个问题
两面赔 共回答了20个问题 |采纳率100%Ca(OH)2 + Cl2 = CaCl2 + Ca(ClO)2 + H2O
Ca(ClO)2 + H2O + CO2 = CaCO3↓+ 2HClO
Ca2+ + 2ClO2- + H2O + CO2 = CaCO3↓+ 2HClO1年前查看全部
- 71gCI2制备漂白粉[有效成分Ca(ClO)2]时转移电子数是?
 婉夕1年前2
婉夕1年前2 -
 理科男生 共回答了26个问题
理科男生 共回答了26个问题 |采纳率96.2%工业上将Cl2通入石灰乳中得到漂白粉,反应为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可知:一份Cl2 可得到一份Ca(ClO)271gCl2 为 1mol,即生成0.5molCa(ClO)2现在问的是转移的电子数那么方程式中化合价变化的只有Cl,C...1年前查看全部
- 1.漂白粉与漂粉精有区别吗【漂白粉的有效成分是什么,漂粉精的有效成分是什么,它们各自的反应方程式分别是什么】
1.漂白粉与漂粉精有区别吗【漂白粉的有效成分是什么,漂粉精的有效成分是什么,它们各自的反应方程式分别是什么】
2.那么次氯酸钠是什么的有效成分,其反应方程式是
3.那么次氯酸是什么的有效成分,其反应方程式是
4.新制氯水、久置氯水有什么区别【请具体讲一讲】
5.为什么在实验室制氯气中,能够用饱和的食盐水吸收氯化氢气体【疑问---氯化氢、食盐水都含有氯离子,怎么能反应】
6.请将以下标准状况下,气体体积的算法及概念 melanl1年前3
melanl1年前3 -
 gamgfahang 共回答了17个问题
gamgfahang 共回答了17个问题 |采纳率88.2%漂白粉就是漂粉精,有效成分是次氯酸钙反应生成的次氯酸,次氯酸钠,次氯酸也一样
新制氯水主要成分为氯气,盐酸,次氯酸,水,久制氯水主要成分为盐酸,水
新制氯水成分中含次氯酸,而久置氯水没有 因为2HClO=见光分解=2HCl+O2
饱和的食盐水吸收氯化氢不是它们之间会反应,而是根据它们的溶解度来的
Cl2 + H2O == H+ + Cl- + HClO是可逆的,即氯气在饱和食盐水中溶解度很小,而氯化氢是完全溶解的.
气体体积=气体摩尔体积(即22.4l/mol)*物质的量 其它算法都是根据这个演变而来的1年前查看全部
- 问一道高中生物学问题动物的角主要是由死亡细胞的角化(变性)蛋白质组成的,而羚羊角等的有效成分最可能是AA.微量元素类 B
问一道高中生物学问题
动物的角主要是由死亡细胞的角化(变性)蛋白质组成的,而羚羊角等的有效成分最可能是A
A.微量元素类 B.大量元素类
不知为什么选A不选B? SuperFlyCat1年前3
SuperFlyCat1年前3 -
 jerrywanfei 共回答了20个问题
jerrywanfei 共回答了20个问题 |采纳率85%你没有把这一题写完整,在原题中,强调了“极少”一词,“极少”是与“微量元素”对应1年前查看全部
- 下列用品的有效成分及用途对应错误的是( )
下列用品的有效成分及用途对应错误的是( )

A.A
B.B
C.C
D.D liu_hong_bin1年前1
liu_hong_bin1年前1 -
 kedai1818 共回答了13个问题
kedai1818 共回答了13个问题 |采纳率92.3%解题思路:物质的性质决定物质的用途,氯化钠可用作调味品;小苏打是碳酸氢钠;氢氧化铝属于碱,可用于治疗胃酸过多;次氯酸钙和水、二氧化碳反应生成次氯酸,次氯酸能够消毒杀菌;据此进行分析判断.A、氯化钠可做调味品,故选项说法正确.
B、小苏打是碳酸氢钠,故选项说法错误.
C、氢氧化铝属于碱,可用于治疗胃酸过多,故选项说法正确.
D、二氧化碳反应生成次氯酸,次氯酸能够消毒杀菌,故选项说法正确.
故选:B.点评:
本题考点: 常用盐的用途;常见碱的特性和用途.
考点点评: 本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.1年前查看全部
- 工业上制漂白粉的化学方程式为2Cl2+2Ca(OH)=Ca(ClO)2+CaCl2+2H2O.某干燥样品中有效成分(接下
工业上制漂白粉的化学方程式为2Cl2+2Ca(OH)=Ca(ClO)2+CaCl2+2H2O.某干燥样品中有效成分(接下)
(接上)Ca(ClO)2的质量分数为55%,则生产过程中Ca(OH)2的利用率为? A96.1% B86.4% C77.8% D71.3% 过程? 操之有道1年前1
操之有道1年前1 -
 pandoraeb 共回答了19个问题
pandoraeb 共回答了19个问题 |采纳率100%n(Ca(ClO)2)=55/143=0.3846mol
m(CaCl2)=0.3846*111=42.69g
m(Ca(OH)2)=100-55-42.69=2.3g
m(Ca(OH)2反应)=0.3846*2*74=56.9g
Ca(OH)2%=56.9/(56.9+2.3)=96.1%
A1年前查看全部
大家在问
- 1足球的五边形方块一个足球,不是都五边行小块的吗? 你能从头到尾用一根线串起来吗?不漏下一个方块,也不重复一个方块.
- 2我听说一个螺丝帽就可以使一个宇宙飞船
- 3五棵松体育馆容纳多少人?看了奥运篮球比赛之后发现,五棵松体育馆还真有点像那么回事,看上去挺大.
- 418米增加它的六分之一,再减去六分之一米,是( )米
- 5已知函数f(x)=1/2m(x-1)²-2x+3+lnx,m属于R,当m=0时,求函数f(x)的单调增区间
- 65700立方分米=《 》立方
- 7节日里安装彩灯,现在手头有几十个彩灯泡,工作时两端的电压都不超过6.3V,只能用家庭电路供电,则可行的办法是( )
- 8朝发白帝暮到江陵这句花话是为了突出三峡的什么特点
- 9用5.2与2.1的积去除5.46,商是几?
- 10下列关于工农业节水的叙述,不正确的是( )
- 11高中数学题目,在线等,急!cos(-45∏/4)的三角函数值
- 12已知,如图,在▱ABCD中,延长DA到点E,延长BC到点F,使得AE=CF,连接EF,分别交AB,CD于点M,N,连接D
- 13若直线4x-3y+12=0过椭圆x^2/a^2+y^2/b^2=1(a>b>0)的一个焦点,且离心率为3/5,求此椭圆方
- 14如何证明任一函数可以 唯一的 写成一个奇函数和一个偶函数的和
- 15为什么摩尔曼斯克位于北极圈内,纬度很噶哦,濒临北冰洋,港湾终年不冻?
