①烧碱 ②氨水 ③SO3 ④水银 ⑤食盐水 ⑥纯醋酸晶体 ⑦碳酸钙 ⑧盐酸 ⑨蔗糖
 忘了唱歌2022-10-04 11:39:541条回答
忘了唱歌2022-10-04 11:39:541条回答其中能导电的是
属于电解质的是
属于非电解质的是

已提交,审核后显示!提交回复
共1条回复
 xt886 共回答了13个问题
xt886 共回答了13个问题 |采纳率100%- 其中能导电的是 ②氨水 ④水银 ⑤食盐水⑧盐酸
属于电解质的是 ①烧碱 ⑥纯醋酸晶体 ⑦碳酸钙
属于非电解质的是 ③SO3 ⑨蔗糖 - 1年前
相关推荐
- 用少量烧碱和过量亚硫酸反应
 一棵想静的树1年前2
一棵想静的树1年前2 -
 抱着太阳嫌冷 共回答了12个问题
抱着太阳嫌冷 共回答了12个问题 |采纳率91.7%NaOH+H2SO3=NaHSO3+H2O1年前查看全部
- 验证RX为碘代烷,把RX与烧碱水溶液混合加热,将溶液冷却后再加入硝酸银溶液 为什么错?
 yy29588981年前2
yy29588981年前2 -
 小破孩色 共回答了18个问题
小破孩色 共回答了18个问题 |采纳率83.3%错误.
必须先酸化.
因为NaOH是过量的,NaOH能与AgNO3产生Ag2O沉淀.干扰AgI的生成.1年前查看全部
- 体积和物质的量浓度相同的1.醋酸,2.盐酸,3.硫酸三溶液,分别与同浓度的烧碱反应,要使反应后的溶液呈中性,所需烧碱溶液
体积和物质的量浓度相同的1.醋酸,2.盐酸,3.硫酸三溶液,分别与同浓度的烧碱反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为 (1
我觉得老师给的这个答案是错的
虽然说醋酸不能完全电离,但是和烧碱反应到最后电离出的离子和盐酸也是一样,是不是呢
硫酸的我明白了 zhtoto0071年前9
zhtoto0071年前9 -
 lvyucheng 共回答了15个问题
lvyucheng 共回答了15个问题 |采纳率93.3%因为醋酸是一元酸,而且是弱酸,如果有1:1的烧碱跟醋酸反应,之后的溶液的PH>7
估计你们还没学强碱弱酸盐的电离.这么说吧,把醋酸钠放在水里,理论上就会有1:1的醋酸根和Na+.但是由于醋酸根是弱酸的根,一部分会跟水反应,生成醋酸,留下OH-,所以溶液就是弱碱性的了.这就是为什么1:1的醋酸跟烧碱反应,会是弱碱性的.
而盐酸是一元酸,是强酸.与1:1 的烧碱反应,之后的溶液是PH=7
硫酸是二元酸,是强酸.与2:1 的烧碱反应,之后的溶液是PH=7.如果与1:1的烧碱反应,之后还剩下一半的H+.1年前查看全部
- A铝是还原剂.B水是氧化剂.C烧碱和水是氧化剂.D偏铝酸钠是氧化产物.
 傩小咒1年前1
傩小咒1年前1 -
 鱼与自行车 共回答了15个问题
鱼与自行车 共回答了15个问题 |采纳率93.3%B 其实是因为铝和水反应是可逆的生成的氢氧化铝和氢气,水中氢化合价降低做氧化剂,氢氧化铝是两性氢氧化物可以和氢氧化钠反应生成偏铝酸钠,促使上面的可逆反应向右进行,2AL+6H2O=2AL(OH)3+3H2 这个反应是可逆反应),产生的AL(OH)3再和NAOH反应,AL(OH)3+NaOH=NaALO2+2H2O 一楼的总反应方程式是没有错误的 但是很明显生成的三分氢气在我的第一个方程式中就很明显的知道氢气中的氢是来源于水 而不是氢氧化钠1年前查看全部
- 含A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应
含A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)在元素周期表中,A位于 族,与A同族但相对原子质量比A小的元素B的原子结构示意图为 ,A与B在原子的电子层结构上的相同点是 。
(2)易与C发生化学反应的酸是 ,反应的化学方程式是 。
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①写出生成D和F的化学反应方程式: 。
②要将纯碱高温熔化,下列坩埚中可选用的是 。
A.普通玻璃坩埚B.石英玻璃坩埚
C.氧化铝坩锅D.铁坩锅
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是 。 紫菜汤汤1年前1
紫菜汤汤1年前1 -
 织造局 共回答了17个问题
织造局 共回答了17个问题 |采纳率82.4%(1)ⅣA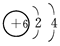 最外层均有4个电子,最内层均有2个电子
最外层均有4个电子,最内层均有2个电子
(2)氢氟酸 SiO 2 +4HF=SiF 4 ↑+2H 2 O
(3)①SiO 2 +Na 2 CO 3 Na 2 SiO 3 +CO 2 ↑,
Na 2 SiO 3 +CO 2 ↑,
Na 2 SiO 3 +CO 2 +H 2 O=Na 2 CO 3 +H 2 SiO 3 ↓
②D (4)50%
(1)A元素单质可作半导体材料,含A元素的某化合物是制造光导纤维的原料,可知A为硅元素,C为SiO 2 ,D为Na 2 SiO 3 。比硅相对原子质量小的同族元素B为碳。
(2)C为SiO 2 ,能与SiO 2 反应的酸只有氢氟酸。
(3)SiO 2 与Na 2 CO 3 高温下反应生成Na 2 SiO 3 和CO 2 ,含SiO 2 的材料(普通玻璃、石英玻璃)以及Al 2 O 3 等都能与Na 2 CO 3 在高温下反应,故不能用以上材质的坩埚熔融Na 2 CO 3 。
(4)若SiO 2 恰好完全反应或过量,与CaCO 3 反应的化学方程式只有一个,即CaCO 3 +SiO 2 CaSiO 3 +CO 2 ↑。若CaCO 3 过量,除发生上述反应外,还会发生反应:
CaSiO 3 +CO 2 ↑。若CaCO 3 过量,除发生上述反应外,还会发生反应:
CaCO 3 CaO+CO 2 ↑。总之,CaCO 3 的多少决定了CO 2 的产量,可通过以下关系列式求
CaO+CO 2 ↑。总之,CaCO 3 的多少决定了CO 2 的产量,可通过以下关系列式求
CaCO 3 ~ CO 2
100 g 22.4 L
m(CaCO 3 ) 11.2 L
m(CaCO 3 )=50 g
混合物中CaCO 3 的质量分数: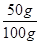 ×100%=50%。
1年前查看全部
×100%=50%。
1年前查看全部
- 烧碱,苛性钠 纯碱,石灰石,小苏打
 freeone1年前1
freeone1年前1 -
 mfr518 共回答了19个问题
mfr518 共回答了19个问题 |采纳率89.5%烧碱,苛性钠:NaOH,还一个名称叫火碱
纯碱:Na2CO3,又称苏打,化学里说的:纯碱不是碱,说的就是它,溶液呈碱性而得名
石灰石:CaCO3
小苏打:NaHCO3
希望对你有所帮助,亲!欢迎追问!1年前查看全部
- 用相关序号填空:可选物质:A.蛋白质;B.活性炭;C.干冰;D.熟石灰;E.烧碱(1)可除去冰箱中异味的是:______
用相关序号填空:
可选物质:A.蛋白质;B.活性炭;C.干冰;D.熟石灰;E.烧碱
(1)可除去冰箱中异味的是:______;
(2)可用于人工降雨的是:______;
(3)牛奶中的主要营养物质是:______;
(4)溶于水时显著放热的是:______;
(5)常用于改良酸性土壤的是:______. kzesl1年前1
kzesl1年前1 -
 selenequin 共回答了18个问题
selenequin 共回答了18个问题 |采纳率88.9%解题思路:熟记常用物质的性质及其用途;如蛋白质;活性炭;干冰;熟石灰;烧碱等物质的性质及其用途.
(1)除去冰箱中异味,考虑具有吸附作用的活性炭;
(2)用于人工降雨的物质,考虑升华,吸收周围的热量的干冰;
(3)牛奶中的主要营养物质是蛋白质;
(4)溶于水时显著放热的,考虑溶解放热的物质氢氧化钠;
(5)用于改良酸性土壤的是廉价易得的氢氧化钙.(1)可除去冰箱中异味的是:活性炭,它疏松多孔,表面积大,吸附作用好,故选B;
(2)可用于人工降雨的是:干冰,干冰升华,吸收周围的热量,故选C;
(3)牛奶中的主要营养物质是:蛋白质,故选A;
(4)溶于水时显著放热的是:烧碱,故选E;
(5)常用于改良酸性土壤的是:氢氧化钙,因为它廉价易得,故选D.
故答为:(1)B;(2)C;(3)A;(4)E;(5)D点评:
本题考点: 酸碱盐的应用;溶解时的吸热或放热现象;生命活动与六大营养素.
考点点评: 本题考查了生活中许多做法都与化学有着密切的联系,正确使用化学知识解释某些生活做法体现了化学的学习对生活有很大帮助.1年前查看全部
- 试从物质溶解过程解释下列现象(1)NH4NO3溶于水时明显吸热(2)烧碱固体溶于水时明显放热
 ymym5181年前1
ymym5181年前1 -
 这周真长啊 共回答了14个问题
这周真长啊 共回答了14个问题 |采纳率85.7%溶解是吸热的
烧碱遇水放热1年前查看全部
- 有下列8种物质,A干冰 B氧化镁 C氯化钙 D固态碘 E烧碱 F冰 G过氧化钾
有下列8种物质,A干冰 B氧化镁 C氯化钙 D固态碘 E烧碱 F冰 G过氧化钾
H金刚石
1,熔化时破坏共价键的是____为什么?
2,只含有极性键的是______为什么?
3,含非极性键的是______为什么?
请问H是否含有非极性键? 飘雪时节1年前1
飘雪时节1年前1 -
 2008dhy 共回答了22个问题
2008dhy 共回答了22个问题 |采纳率95.5%1,熔化时破坏共价键的是H金刚石,因为他是原子晶体,相邻原子间以共价键结合而形成的空间网状结构的晶体
2,只含有极性键的是A干冰.F冰.分子内仅有的氢氧键和碳氧键都是极性键
3,含非极性键的是D固态碘,分子内仅有的碘碘键是非极性键;G过氧化钾过氧离子中的氧氧键是非极性键;H金刚石 ,里面的碳碳键是非极性键1年前查看全部
- 一固体混和物,可能有氯化钙、碳酸铵、烧碱、硫酸铵,将它溶解于水得到无色澄清溶液,无其它明显现象,向溶液中加入硝酸钡溶液,
一固体混和物,可能有氯化钙、碳酸铵、烧碱、硫酸铵,将它溶解于水得到无色澄清溶液,无其它明显现象,向溶液中加入硝酸钡溶液,产生白色沉淀,再加入硝酸,沉淀部分消失,原混和物中肯定有( )
A. CaCl2 和(NH4)2SO4
B. (NH4)2SO4 和(NH4)2CO3
C. NaOH和CaCl2
D. NaOH和(NH4)2SO4 sunshime1年前2
sunshime1年前2 -
 sophia198577 共回答了20个问题
sophia198577 共回答了20个问题 |采纳率95%解题思路:溶解于水得到无色澄清溶液,则氯化钙不能与碳酸铵、硫酸铵同时存在,向溶液中加入硝酸钡溶液,产生白色沉淀,再加入硝酸,沉淀部分消失,则白色沉淀为硫酸钡和碳酸钡,以此来解答.溶解于水得到无色澄清溶液,则氯化钙不能与碳酸铵、硫酸铵同时存在,向溶液中加入硝酸钡溶液,产生白色沉淀,再加入硝酸,沉淀部分消失,则白色沉淀为硫酸钡和碳酸钡,由原子守恒可知,原固体中一定含碳酸铵、硫酸铵,则一定不含氯化钙,可能含烧碱,
故选B.点评:
本题考点: 物质的检验和鉴别的实验方案设计.
考点点评: 本题考查物质的鉴别和检验,为高频考点,把握白色固体为硫酸钡和碳酸钡为解答的关键,侧重复分解反应及离子检验的考查,题目难度不大.1年前查看全部
- 陶瓷坩埚为什么不可以熔融烧碱?陶瓷不是由硅酸盐制成的么?硅酸盐不是不和烧碱反应么?少帅花荣~烧碱跟空气反应生成盐吧~怎么
陶瓷坩埚为什么不可以熔融烧碱?
陶瓷不是由硅酸盐制成的么?硅酸盐不是不和烧碱反应么?
少帅花荣~烧碱跟空气反应生成盐吧~怎么和硅酸盐反应啊?
liuayang_2008 陶瓷里有二氧化硅吗? tenent1年前1
tenent1年前1 -
 aomaiga 共回答了16个问题
aomaiga 共回答了16个问题 |采纳率93.8%陶瓷里的二氧化硅会和烧碱反应生成硅酸钠
陶瓷是由粘土、石英及长石等天然矿物原料按不同配方配制,经加工、成型及烧成而得.有石英当然就有二氧化硅SiO2了!1年前查看全部
- 盐酸,硝酸,烧碱,安水,高孟酸钾,
 nicky_z1年前0
nicky_z1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 氢氧化钠,苛性钠,烧碱,片碱,的区别.
 查爱民1年前5
查爱民1年前5 -
 梨庭 共回答了17个问题
梨庭 共回答了17个问题 |采纳率82.4%氢氧化钠是化学术语!苛性钠,烧碱都是氢氧化钠,是氢氧化钠的俗称!片碱,是氢氧化钠(主要成分,也即有效成分)和少量碳酸钠的混合物!也即片碱是混合物!氢氧化钠,苛性钠,烧碱属于纯净物且是化合物!1年前查看全部
- 以苯、水、溴、浓硫酸、烧碱为原料制取2-溴苯酚
 tb811151年前2
tb811151年前2 -
 剃头刀2002 共回答了26个问题
剃头刀2002 共回答了26个问题 |采纳率96.2%苯
苯磺酸
2-溴-苯磺酸
2-溴-苯磺酸钠
2-溴苯酚
最后一步是碱熔融条件,不过可能出问题,溴可能保不住,具体看实验结果吧1年前查看全部
- 一 ) 1 盐酸 ; 2 烧碱 ;3 熟石灰 ;4五氧化二磷 ;5氨气 ;6硫酸铜 ;7 氢氧化铁 ,用化学式表示填入下
一 ) 1 盐酸 ; 2 烧碱 ;3 熟石灰 ;4五氧化二磷 ;5氨气 ;6硫酸铜 ;7 氢氧化铁 ,用化学式表示填入下列空格.
(1)属于酸性氧化物的是_________
(2)其水溶液能使分太试液变红的是_________
(3)有颜色的不溶物_________
(4)能中和土壤酸性的是_________
(5) 能干燥除酸性气体以外的某些气体是______
【思路 】
二) 用氧化铜制请氧化铜,可先加入___,化学方程式为________;再加入_______,化学方程式为_________;最后经_______方法分离.
三)在焊接铁制品之前,要在焊接处用稀盐酸清洗,其目的是_________,反应的化学方程式是______________ 暗香_1631年前1
暗香_1631年前1 -
 坚坚坚坚坚坚坚 共回答了20个问题
坚坚坚坚坚坚坚 共回答了20个问题 |采纳率90%一
1 P2O5
2 NaOH Ca(OH)2 NH3
3 Fe(OH)3红褐色
4 Ca(OH)2 不用NaOH
5 NaOH固体 P2O5
二
HCl 2HCl +CuO=CuCl2+H2O NaOH 2NaOH+CuCl2=Cu(OH)2沉淀+2NaCl 过滤
三
除去表面的铁锈 6HCl+Fe2O3=2FeCl3+3H2O1年前查看全部
- 下列叙述正确的是 A.电解饱和食盐水制烧碱采用离子交换膜法,可以阻止阳离子通过 B.在铁上镀锌时,锌棒作阴极,且电解液硫
下列叙述正确的是
A.电解饱和食盐水制烧碱采用离子交换膜法,可以阻止阳离子通过 B.在铁上镀锌时,锌棒作阴极,且电解液硫酸锌的浓度是不变的 C.用惰性电极电解Na 2 SO 4 溶液,阴阳两极产物的物质的量之比为1: 2 D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH  十月听雨1年前1
十月听雨1年前1 -
 谁也不会ff 共回答了13个问题
谁也不会ff 共回答了13个问题 |采纳率76.9%D
1年前查看全部
- 1.清新的空气2.水银3.二氧化锰4.铝合金5.过氧化氢溶液6.澄清石灰水7.冰水混合物8.高锰酸钾9.烧碱10.硫酸
1.清新的空气2.水银3.二氧化锰4.铝合金5.过氧化氢溶液6.澄清石灰水7.冰水混合物8.高锰酸钾9.烧碱10.硫酸
混合物—— 化合物—— 单质—— 添下序号,谢谢
 子潇1681年前1
子潇1681年前1 -
 小洛宝贝 共回答了19个问题
小洛宝贝 共回答了19个问题 |采纳率78.9%154——36879.10——2.顺便指点一下:空气再怎么纯净都是由氮气,氧气等气体组成,所以是混合物,合金呢这个是金属混合,他们不能组成化合物.过氧化氢主要是溶液两个字,则证明它是由过氧化氢和水组成的.至于化合物就是由几种元素构成,以分子形式存在,具体我相信你们的化学老师会讲的,如果不懂加我Q7707272691年前查看全部
- 写出硝酸,氯化铵,氯化铷,小苏达,灰锰氧,纯碱,烧碱的电离方程式
写出硝酸,氯化铵,氯化铷,小苏达,灰锰氧,纯碱,烧碱的电离方程式
还有硫酸氢娜和草木灰的电离方程式 小小4211年前1
小小4211年前1 -
 Love_Mallory 共回答了15个问题
Love_Mallory 共回答了15个问题 |采纳率80%HNO3 == H+ + NO3-
NH4CL == NH4+ + CL-
NaHCO3 == Na+ +HCO3-
kMnO4 == K+ + MnO4+
NaCO3 == Na+ +CO32-
NaOH == Na+ + OH-
NaHSO4 == Na+ + H+ + SO4 2-
K2CO3 == K+ +CO3 2-
❤您的问题已经被解答~~(>^ω^1年前查看全部
- 烧碱可用于处理硫酸泄漏,反应的化学方程式
 xiexiaozs1年前2
xiexiaozs1年前2 -
 ljcsx 共回答了14个问题
ljcsx 共回答了14个问题 |采纳率92.9%2NaOH+H2SO4==Na2SO4+2H2O
H+ + OH- == H2O
简单的酸碱中和1年前查看全部
- 取20克烧碱放入180克水中,制成烧碱溶液.向200克食醋中滴加该溶液.至恰好完全反应.共用去烧碱溶液40克.
取20克烧碱放入180克水中,制成烧碱溶液.向200克食醋中滴加该溶液.至恰好完全反应.共用去烧碱溶液40克.
已知反应化学方程式为;CH3COOH+NaOH=CH3COONa+H2O
求烧碱溶液中溶质的质量分数和食醋中醋酸的质量分数 叫天1年前1
叫天1年前1 -
 foxxiaoya 共回答了25个问题
foxxiaoya 共回答了25个问题 |采纳率96%烧碱溶液中溶质的质量分数是20/(20+180)*100%=10%
设食醋中醋酸的质量为x.
CH3COOH+NaOH=CH3COONa+H2O
60 40
x 40*10%g
60/x=40/4
x=6g
食醋中醋酸的质量分数是6/200*100%=3%
答:烧碱溶液中溶质的质量分数是10%,食醋中醋酸的质量分数是3%1年前查看全部
- 用固体烧碱配制500ML0.1mol/L的NAOH溶液,需要称量多少克NAOH,为什么我算的与答案不符
用固体烧碱配制500ML0.1mol/L的NAOH溶液,需要称量多少克NAOH,为什么我算的与答案不符
大家算算看 不是500/0.1 然后乘NAOH分子质量吗 逛逛看看侃侃1年前2
逛逛看看侃侃1年前2 -
 林家龙 共回答了14个问题
林家龙 共回答了14个问题 |采纳率100%注意单位
他的物质的量浓度为 0.1mol/L
单位为L
所以要把溶液的浓度化为L
所以为 500/1000*0.1*40=2g1年前查看全部
- 氧化铁、三氧化二铁可否与烧碱反应?苯环上的卤素可否与氢氧化钠发生取代反应生成苯酚?
 t13041年前2
t13041年前2 -
 xff11 共回答了11个问题
xff11 共回答了11个问题 |采纳率90.9%不可
可1年前查看全部
- 以下各物质中,前者属于单质,后者属于混合物的是( ) A.食盐、液氧 B.镁、空气 C.水、矿泉水 D.烧碱、纯碱
 fcyyx1年前1
fcyyx1年前1 -
 chenfei001 共回答了23个问题
chenfei001 共回答了23个问题 |采纳率87%A、食盐是由钠元素和氯元素组成的化合物,不符合题意;
B、镁 是由一种元素组成的纯净物,属于单质,空气是由氧气、氮气等多种物质组成的混合物,符合题意;
C、水是由氢氧两元素组成的化合物,不符合题意;
D、烧碱是氢氧化钠的俗名,是由氢、氧、钠三种元素组成的化合物,不符合题意;
故选B1年前查看全部
- 烧碱熔化为何破坏了离子键?
 万古人间四月天1年前3
万古人间四月天1年前3 -
 daisy1678 共回答了12个问题
daisy1678 共回答了12个问题 |采纳率91.7%电离为钠和氢氧根离子,破坏了离子健,氢氧共价健完好1年前查看全部
- 目前世界上比较先进的电解法制烧碱技术-阳离子交换膜法.
目前世界上比较先进的电解法制烧碱技术-阳离子交换膜法.
(1)电解精制饱和食盐水时,产生的氯气比理论值少的原因是______;电解总反应方程式为2NaCl+2H2O
Cl2↑+H2↑+2NaOH电解 .2NaCl+2H2O
Cl2↑+H2↑+2NaOH电解 .
(2)为有效除去粗盐中的Ca2+、Mg2+、SO42-,加入试剂的合理顺序为______(填字母).
a.先加NaOH,再加Na2CO3,最后加钡试剂;
b.先加NaOH,再加钡试剂,最后加Na2CO3;
c.先加钡试剂,再加Na2CO3,最后加NaOH.
(3)现有1000ml食盐水,用石墨电极电解.当阴极产生气体的体积为112mL(标准状态)时停止电解,阳极的电极反应式为______,电解后,溶液在常温下的pH约为______.(溶液体积变化忽略不计) ifiona21年前1
ifiona21年前1 -
 往高处流的水 共回答了20个问题
往高处流的水 共回答了20个问题 |采纳率95%解题思路:(1)电解食盐水生成NaOH、氢气、氯气,且氯气与NaOH溶液能发生反应;
(2)除去粗盐中的Ca2+、Mg2+、SO42-,为除去杂质又不引入新的杂质,先除去Mg2+,再除去SO42-,最后除Ca2+,或先除去SO42-也可;
(3)根据电解时阳极氯离子放电及电解反应来计算.(1)电解氯化钠溶液的生成物是氢氧化钠、氯气和氢气,即:2NaCl+2H2O
电解
.
Cl2↑+H2↑+2NaOH,因氯气与NaOH溶液能发生反应,则产生的氯气比理论值少,
故答案为:氯气与NaOH溶液能发生反应;2NaCl+2H2O
电解
.
Cl2↑+H2↑+2NaOH;
(2)根据除去钙离子用碳酸根离子进行沉淀,除去镁离子用氢氧根离子进行沉淀,除去硫酸根离子用钡离子沉淀,过量的钡离子需要用碳酸根离子除去,加入Na2CO3的顺序必须在加入钡离子的后面即可,显然只有a不符合,故答案为:bc;
(3)阴极生成氢气,阳极上生成氯气,阳极电极反应式为2Cl--2e-═Cl2↑,由2NaCl+2H2O
电解
.
Cl2↑+H2↑+2NaOH可知,Cl2↑~H2↑~2NaOH,则n(NaOH)=[0.112L/22.4L/mol]=0.01mol,所以c(NaOH)=[0.01mol/1L]=0.01mol/L,所以pH=12,故答案为:2Cl--2e-═Cl2↑;12.点评:
本题考点: 电解原理;物质的分离、提纯和除杂.
考点点评: 本题考查电解原理,明确电解食盐水发生的电极反应及除杂时试剂的先后顺序是解答本题的关键,题目难度中等.1年前查看全部
- 用于制肥皂的碱选项有a.烧碱b.氢氧化镁乳剂c.氢氧化铝d.熟石灰e.尼古丁f.氨水
 人力三轮1年前3
人力三轮1年前3 -
 山东大地 共回答了18个问题
山东大地 共回答了18个问题 |采纳率88.9%a.烧碱
肥皂就是用脂肪酸和烧碱(氢氧化钠)共煮,水解为高级脂肪酸钠和甘油,前者经加工成型后就是肥皂.1年前查看全部
- 铝与炭棒在烧碱中形成原电池、负极反应怎么写?只写负极!
 大海滩上1年前2
大海滩上1年前2 -
 无限接近于蓝 共回答了14个问题
无限接近于蓝 共回答了14个问题 |采纳率100%Al - 3e- +4OH- ===[Al(OH)4]-
或者Al -3e- +4OH- ===AlO2- +2H2O1年前查看全部
- 下列物质按酸、碱、盐顺序排列的是( ) A.烧碱、盐酸、食盐 B.纯碱、火碱、硫酸 C.硝酸、熟石灰、纯碱 D.盐酸、
下列物质按酸、碱、盐顺序排列的是( )
A.烧碱、盐酸、食盐 B.纯碱、火碱、硫酸 C.硝酸、熟石灰、纯碱 D.盐酸、纯碱、碳酸钙  12wq1年前1
12wq1年前1 -
 racewind 共回答了23个问题
racewind 共回答了23个问题 |采纳率91.3%C
1年前查看全部
- 把干冰,生石灰,硝酸,烧碱,碳酸氢钠,纯碱,胆钒,氢硫酸分类
 丘灵素十三号1年前4
丘灵素十三号1年前4 -
 蓝橘lessia 共回答了25个问题
蓝橘lessia 共回答了25个问题 |采纳率88%酸:硝酸 氢硫酸
碱:烧碱
盐:碳酸氢钠,纯碱,胆钒
氧化物:干冰,生石灰1年前查看全部
- 氯化钡能分别与:1.纯碱,2.烧碱,3.硫酸,这三种物质的溶液发生反应每吗?请说出理由.
氯化钡能分别与:1.纯碱,2.烧碱,3.硫酸,这三种物质的溶液发生反应每吗?请说出理由.
如果能告诉我盐与盐能发生反应的规律的话,那就太感谢了.
对回答1的提问:
烧碱与氯化钡不可以生成氯化钠与氢氧化钡么?为什么. zkisp1年前4
zkisp1年前4 -
 icewind80 共回答了20个问题
icewind80 共回答了20个问题 |采纳率95%1、能反应 BaCl2 + Na2CO3 = BaCO3 (沉淀) + 2NaCl
2、不能反应,因为 BaCl2 + NaOH = Ba(OH)2 + NaCl
Ba(OH)2 和NaCl 都能溶于水,也没沉淀或者气体或者水生成.
3、能反应 BaCl2 + H2SO4 = BaSO4 (沉淀)+ 2HCL1年前查看全部
- 下列说法正确的是( )A.光导纤维的主要成份是硅B.制普通玻璃的主要原料是烧碱、石灰石、石英C.常用氢氟酸(HF)来刻
下列说法正确的是( )
A.光导纤维的主要成份是硅
B.制普通玻璃的主要原料是烧碱、石灰石、石英
C.常用氢氟酸(HF)来刻蚀玻璃
D.实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液 情绪波动1年前1
情绪波动1年前1 -
 维城 共回答了17个问题
维城 共回答了17个问题 |采纳率94.1%解题思路:A、光导纤维成分是二氧化硅;
B、制普通玻璃的主要原料是纯碱、石灰石、石英;
C、氢氟酸和玻璃中的二氧化硅反应;
D、氢氧化钠和玻璃中的二氧化硅反应生成硅酸钠是矿物胶;A、光导纤维成分是二氧化硅,硅是太阳能电池的材料,故A错误;
B、制普通玻璃的主要原料是纯碱、石灰石、石英;故B错误;
C、氢氟酸和玻璃中的二氧化硅反应;常用氢氟酸(HF)来刻蚀玻璃,故C正确;
D、实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液,氢氧化钠和玻璃中的二氧化硅反应生成硅酸钠是矿物胶把瓶塞和瓶口粘结在一起,故D错误;
故选C.点评:
本题考点: 硅和二氧化硅;玻璃的主要化学成分、生产原料及其用途.
考点点评: 本题考查了二氧化硅的性质应用,工业制玻璃的原料,氢氟酸的特征性质,试剂保存方法,基础题较简单.1年前查看全部
- 在18.6克烧碱和纯碱的混合物中加入100克稀盐酸刚好完全反应,产生气体4.4克,求混
 cs5601年前4
cs5601年前4 -
 skl610 共回答了22个问题
skl610 共回答了22个问题 |采纳率81.8%Na2CO3+2HCl==2NaCl+H2O+CO2↑
106g 44g
X 4.4g
X=10.6g
含NaOH:18.6-10.6=8.0(g)
不能用盐酸带进来,因为盐酸是混合物.1年前查看全部
- 由A元素组成的一种单质是重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料,C与烧碱反应生成含A元素
由A元素组成的一种单质是重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料,C与烧碱反应生成含A元素的化合物D.
(1)列举化合物D的两种用途:______.
(2)下列物质的主要成分为C的有______(填字母).
a.沙子b.水玻璃c.黏土d.玛瑙
(3)将C与纯碱混合,高温熔融时也能发生反应生成D,同时还生成B元素的最高价氧化物E;将E通入足量D的水溶液中,又发生反应生成含A元素的化合物F.
①C与纯碱混合高温熔融时发生反应的化学方程式为SiO2+Na2CO3
Na2SiO3+CO2↑高温 .SiO2+Na2CO3.
Na2SiO3+CO2↑高温 .
②E与足量D的水溶液反应的离子方程式为______. 秘密tt20061年前1
秘密tt20061年前1 -
 wf1ove 共回答了24个问题
wf1ove 共回答了24个问题 |采纳率91.7%解题思路:含A元素的一种单质是一种重要的半导体材料,则A为Si,含A元素的一种化合物C可用于制造高性能的现代通讯材料--光导纤维,则C为SiO2,C与烧碱反应生成含A元素的化合物D为Na2SiO3.
(1)C为SiO2,D为Na2SiO3,根据Na2SiO3的性质进行解答;
(2)C为SiO2,沙子、玛瑙的主要成分为SiO2,水玻璃、黏土主要成分为硅酸盐;
(3)将SiO2与纯碱混合,高温熔融时生成DNa2SiO3,同时还生成E为CO2;将E物质CO2通入足量DNa2SiO3的水溶液中,碳酸比硅酸强,二氧化碳和硅酸钠反应生成硅酸和碳酸氢钠;生成含A元素的化合物H2SiO3,
①C为SiO2,与纯碱混合高温熔融时生成硅酸钠和二氧化碳;
②E为CO2,通入足量DNa2SiO3的水溶液中,生成硅酸沉淀;含A元素的一种单质是一种重要的半导体材料,则A为Si,含A元素的一种化合物C可用于制造高性能的现代通讯材料:光导纤维,则C为SiO2,C与烧碱反应生成含A元素的化合物D为Na2SiO3,
(1)C为SiO2,与烧碱反应SiO2+2NaOH=Na2SiO3+H2O,生成含A元素的化合物D,D为Na2SiO3,
Na2SiO3(硅酸钠)俗称水玻璃具有广泛的用途,是建筑水泥快干等工业的粘合剂,也是一种溶雪剂的成分之一,也可制备硅胶、木材防火剂,
故答案为:制备硅胶、木材防火剂;
(2)a.沙子主要成分为二氧化硅;b.水玻璃是硅酸钠的水溶液;c.黏土主要成分为硅酸盐;d.玛瑙主要成分为二氧化硅,C为SiO2,所以a、d符合,
故答案为:a、d;
(3)将SiO2与纯碱混合,高温熔融时SiO2+Na2CO3
高温
.
Na2SiO3+CO2↑,生成DNa2SiO3,同时还生成E为CO2;将E物质CO2通入足量DNa2SiO3的水溶液中,碳酸比硅酸强,二氧化碳和硅酸钠反应生成硅酸和碳酸氢钠;反应为:2CO2+Na2SiO3+2H2O═2NaHCO3+H2SiO3↓,生成含A元素的化合物H2SiO3,
①C为SiO2,与纯碱混合高温:SiO2+Na2CO3
高温
.
Na2SiO3+CO2↑,
故答案为:SiO2+Na2CO3
高温
.
Na2SiO3+CO2↑;
②E为CO2,通入足量DNa2SiO3的水溶液中2CO2+Na2SiO3+2H2O═2NaHCO3+H2SiO3↓,离子反应为:2CO2+SiO32-+2H2O═2HCO3-+H2SiO3↓,
故答案为:2CO2+SiO32-+2H2O═2HCO3-+H2SiO3↓;点评:
本题考点: 硅和二氧化硅.
考点点评: 本题考查无机物的推断,题目难度中等,本题中侧重于物质的应用为考查点,注意把握Si的单质及化合物的性质和用途,为高频考点.1年前查看全部
- 下列归类错误的是( )选项归类物质A化石燃料煤、汽油、天然气B同一物质烧碱、火碱、苛性钠C营养物质淀粉、蛋白质、维生素
下列归类错误的是( )
选项 归类 物质 A 化石燃料 煤、汽油、天然气 B 同一物质 烧碱、火碱、苛性钠 C 营养物质 淀粉、蛋白质、维生素 D 无机材料 合金、玻璃、陶瓷
A.A
B.B
C.C
D.D wheleer1年前1
wheleer1年前1 -
 nixonnixon 共回答了19个问题
nixonnixon 共回答了19个问题 |采纳率89.5%解题思路:A、根据煤、石油、天然气属于化石燃料进行分析;
B、根据氢氧化钠俗称火碱、烧碱、苛性钠,纯碱是碳酸钠的俗称进行分析;
C、根据人类需要的营养物质有糖类、油脂、蛋白质、维生素、水和无机盐进行分析;
D、根据材料包括金属材料、无机非金属材料、有机合成材料、复合材料进行分析.A、化石燃料包括煤、石油、天然气,故A正确;
B、火碱、烧碱是指氢氧化钠,纯碱是指碳酸钠,火碱、烧碱和纯碱不是同种物质,故B错误;
C、淀粉、蛋白质、维生素属于人体需要的营养物质,故C正确;
D、合金、玻璃、陶瓷都属于无机材料,故D正确.
故选:B.点评:
本题考点: 化石燃料及其综合利用;常见碱的特性和用途;新材料的开发与社会发展的密切关系;生命活动与六大营养素.
考点点评: 化学来源于生产、生活,也服务于生产、生活,与生产、生活相关的化学知识,是中考热点之一.1年前查看全部
- 下列物质中不属于碱的是 A烧碱 B苛性钠 C熟石灰 D纯碱
 小tt甲马小1年前7
小tt甲马小1年前7 -
 呼在 共回答了17个问题
呼在 共回答了17个问题 |采纳率94.1%D纯碱
碳酸钠是盐1年前查看全部
- 请问:小苏打、苏打、烧碱、纯碱分别是什么东西?
 幽谷翠筱1年前2
幽谷翠筱1年前2 -
 aaaabbbbccccdddd 共回答了21个问题
aaaabbbbccccdddd 共回答了21个问题 |采纳率95.2%NaHCO3
Na2CO3
NaOH
Na2CO31年前查看全部
- 工业烧碱2克,制成250ml溶液,取50ml可与0.2mol/L硫酸20ml完全中和,求烧碱纯度?
 赵小片1年前1
赵小片1年前1 -
 樱木花道就是我 共回答了16个问题
樱木花道就是我 共回答了16个问题 |采纳率87.5%烧碱纯度=(((0.2*20/1000)*40)/(2*50/250))*100
=80%1年前查看全部
- 将40g烧碱溶于水得溶液甲,再向甲中通入1molHCl得溶液乙,则在相同温度下甲和乙的导电能力一样.为什么?
 Phonixsong1年前1
Phonixsong1年前1 -
 兜兜多多 共回答了18个问题
兜兜多多 共回答了18个问题 |采纳率94.4%如果不考虑溶液体积变化,那麼甲有1molNaOH,乙有1molNaCl,大家阴阳离子的总量以及带电都是一样的,那麼导电能力当然相同.1年前查看全部
- 初 三 化 学 ( 紧 急 )一:写出造成下列现象的原因:1.某同学在量筒中溶解固体烧碱,发现量筒炸裂:2.用高锰酸钾制
初 三 化 学 ( 紧 急 )
一:写出造成下列现象的原因:
1.某同学在量筒中溶解固体烧碱,发现量筒炸裂:
2.用高锰酸钾制取氧气并用排水法收集,发现水槽中的水略带红紫色: 上杉景虎1年前3
上杉景虎1年前3 -
 sunyajing 共回答了19个问题
sunyajing 共回答了19个问题 |采纳率89.5%1.烧碱溶解放出大量的热,从而造成量筒的炸裂
2.有高锰酸钾进入到了水槽中的水中,从而显示红紫色1年前查看全部
- 化学物质推断题.A元素氢化物的核外电子总数为10个.A的最高价氧化物B与烧碱反应生成盐C.C受热分解出新盐D和气体E.问
化学物质推断题.
A元素氢化物的核外电子总数为10个.A的最高价氧化物B与烧碱反应生成盐C.C受热分解出新盐D和气体E.问A.B.C.D.E各是什么.并给出所有反应的化学方程式和离子方程式.
我推断出A是碳..但是E跟B物质就是一样的了?是不是有问题..请高手给出推断依据.. yl761年前3
yl761年前3 -
 40009024110 共回答了29个问题
40009024110 共回答了29个问题 |采纳率86.2%A不一定是碳,氮、氧、氟均有可能(NH3、H2O、HF的核外电子总数都是10个,不信你数数),通过第二、三句话,把氧和氟排除掉.当A是氮时,B是N2O5(五氧化二氮,硝酸的酸酐),C是NaNO3,硝酸盐不稳定,受热会分
2NaNO3==2NaNO2(亚硝酸钠)+O2
则D是NaNO2,E是氧气1年前查看全部
- 1 现有石灰石、水、残酸钠,怎样制取烧碱(不能引入其他物质),写出有关化学式.
1 现有石灰石、水、残酸钠,怎样制取烧碱(不能引入其他物质),写出有关化学式.
2 用锌粒、盐酸、氧化铁、硫酸铜为原料制取硫酸亚铁,写出有关化学式.
3 试用6种不同的方法制备氯化锌,写出有关化学式. lkmnjq21341年前1
lkmnjq21341年前1 -
 mafst 共回答了19个问题
mafst 共回答了19个问题 |采纳率89.5%1.高温煅烧石灰石生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙.氢氧化钙和碳酸钠反应生成氢氧化钠和碳酸钙沉淀.
2. Fe2O3+6HCl=2FeCl3+3H2O
3Zn+2FeCl3=3ZnCl2+2Fe
Fe+CuSO4=Cu+FeSO4
3. Zn+2HCl=ZnCl2+H2 气体
ZnO+2HCl=ZnCl2+H2O
Zn(OH)2+2HCl=ZnCl2+2H2O
锌放如氯化铜中
Zn+FeCl2=ZnCl2+Fe
硫化锌放如稀盐酸中1年前查看全部
- 熔融烧碱时,为何不能使用普通的玻璃,石英,或陶瓷坩埚,而用铁坩埚
熔融烧碱时,为何不能使用普通的玻璃,石英,或陶瓷坩埚,而用铁坩埚
带上化学方程式 hly25891年前1
hly25891年前1 -
 多毛猫 共回答了24个问题
多毛猫 共回答了24个问题 |采纳率87.5%玻璃,陶瓷的主要成分都是硅酸盐和铝酸盐,在熔融状态下会与氢氧化钠反应,铁就不存在这种情况
主要反应方程式
2NaOH+SiO2====Na2SiO3+H2O
Al2O3+2NaOH====2NaAlO2+H2O1年前查看全部
- 某同学在量筒中熔解固体烧碱,发现量筒炸裂:.
某同学在量筒中熔解固体烧碱,发现量筒炸裂:.
写出原因 XXSMILE1年前1
XXSMILE1年前1 -
 风拥云 共回答了21个问题
风拥云 共回答了21个问题 |采纳率90.5%烧碱遇到水会放热,热量使量筒炸裂1年前查看全部
- 怎样用酸碱洗工业废油,块状烧碱先要水溶解吗
 zhaoshx1年前1
zhaoshx1年前1 -
 黎叔0531 共回答了13个问题
黎叔0531 共回答了13个问题 |采纳率84.6%一般是先加热水溶解,块状烧碱必须要水溶解1年前查看全部
- (2007•番禺区一模)某化工厂常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经浓缩、蒸发等步骤制造固体烧碱.某化学兴
(2007•番禺区一模)某化工厂常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经浓缩、蒸发等步骤制造固体烧碱.某化学兴趣小组要分析该化工厂仓库里的固体烧碱样品.
(1)小组成员猜测该样品中含有碳酸钠,支持这种猜测的依据是(用化学方方程式表示)______.小组成员选用了三种不同类别的试剂,进行实验,验证猜想,并得出结论,碳酸钠确实存在.请你将实验过程中涉及的化学方程式填在下表中.
(2)现已知样品中含有氯化钠、氢氧化钠、碳酸钠,设计一个实验方案,来证实一定含有氯化钠存在.化学方程式 试剂1 试剂2 试剂3 
请写出试剂X的化学式______
请写出①反应的化学方程式______
请写出②反应的化学方程式______. 烟雨楼家族之烟灰1年前1
烟雨楼家族之烟灰1年前1 -
 钱之光 共回答了20个问题
钱之光 共回答了20个问题 |采纳率85%解题思路:(1)烧碱易潮解,潮解之后容易和空气中的二氧化碳反应,检验烧碱变质的方法就是根据碳酸钠的化学性质来选择合适的试剂来鉴别
(2)加入试剂A后生成了气体可知X为酸,但是考虑到后边的反应中加入了硝酸银,所以此时要排除氯离子和硫酸根离子的干扰,故应该选择稀硝酸,可以据此答题(1)烧碱露置于空气中时易于空气中的二氧化碳反应而变质,在验证烧碱是否变质实际上就是验证碳酸钠的存在,故可以据其性质来区分,要注意的是当用盐酸时要向把氢氧化钠反应掉,然后才会有气体产生,故本题的答案为:CO2+2NaOH=Na2CO3+H2O
化学方程式
试剂1 Na2CO3 +CaCl2═2NaCl+CaCO3↓
试剂2 Na2CO3+Ca(OH)2═2NaOH+CaCO3↓
试剂3
NaOH+HCl=NaCl+H2O
Na2CO3+2HCl=2NaCl+CO2↑+H2O (2)加入X生成了气体可知X为酸,但是考虑到后边的反应中加入了硝酸银,所以此时要排除氯离子和硫酸根离子的干扰,故应该选择稀硝酸,当加入稀硝酸时除了和碳酸钠反应,还要和氢氧化钠发生中和反应,在混合物中能和硝酸银生成白色沉淀的是氯化钠,
故本题答案为:HNO3 NaOH+HNO3=NaNO3+H2O; Na2CO3+2HNO3=2NaNO3+CO2↑+H2ONaCl+AgNO3=AgCl↓+NaNO3点评:
本题考点: 酸、碱、盐的鉴别;电解水实验.
考点点评: 解答本题要求学生熟练掌握酸、碱、盐的化学性质,并能根据物质之间能否反应及其反应的实验现象来得出结论,熟记化学方程式:CO2+2NaOH=Na2CO3+H2O;Na2CO3+Ca(OH)2═2NaOH+CaCO3↓; NaOH+HCl=NaCl+H2O.1年前查看全部
- (u008•辽宁)海洋是r个巨大的资源库,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的烧碱.其制取的主要工艺
(u008•辽宁)海洋是r个巨大的资源库,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的烧碱.其制取的主要工艺流程如下:
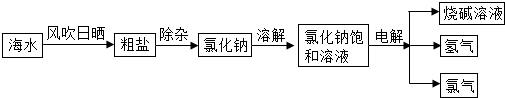
(1)利用风吹日晒可以从海水中提取粗盐,风吹日晒的主要作用是______.
(u)要除去食盐水中混有的少量泥沙,操作方法是______.
(1)写出电解氯化钠溶液的化学方程式umaCl+uHuO
umaOH+Hu↑+Clu↑通电 .umaCl+uHuO.
umaOH+Hu↑+Clu↑通电 .
(他)该化工厂将副产品氢气和氯气加以利用:氢气在氯气中燃烧生成氯化氢,氯化氢溶于水得到盐酸.写出氢气在氯气中燃烧的化学方程式:Hu+Clu
uHCl点燃 .Hu+Clu,通过这个化学反应,你对燃烧的新认识是______.
uHCl点燃 . 轩轩55号1年前1
轩轩55号1年前1 -
 qianj555 共回答了17个问题
qianj555 共回答了17个问题 |采纳率88.2%解题思路:(1)根据晒盐的原理分析即可;
(2)根据混合物分离的方法分析;
(3)根据题意再结合元素守恒分析即可;
(4)根据题目信息与燃烧的概念进行分析即可作答.(r)从海水中提取食盐采用蒸发结晶的方法,风吹日晒是为了加速水分的蒸发,故答案为:蒸发水分;(2)因为泥沙不溶于水,而氯化钠溶于水,所以可以采用过滤的方法滤去泥沙,故答案为:过滤;(五)根据题意:电解氯...
点评:
本题考点: 对海洋资源的合理开发与利用;过滤的原理、方法及其应用;结晶的原理、方法及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 可燃物在氧气中可以燃烧,但燃烧不一定需要氧气氧气参加,如:H2+Cl2 点燃 . 2HCl,同学们需要注意!1年前查看全部
- 化学会考题:为除去水中的硝基苯,应向水净化池中加入的物质是:A.烧碱 B.活性炭 C.硫酸 D.食盐
化学会考题:为除去水中的硝基苯,应向水净化池中加入的物质是:A.烧碱 B.活性炭 C.硫酸 D.食盐
答案是D食盐 但是为什么用食盐?而且查了很多资料都表明应该用活性炭... 苏州板刷头1年前1
苏州板刷头1年前1 -
 elvisliang 共回答了19个问题
elvisliang 共回答了19个问题 |采纳率105.3%加入电解质可以减小硝基苯溶解度,但由于是向水净化池投料,烧碱,硫酸不考虑
选D食盐
但是我个人还是认为B更好,因为有吸附性,可以吸附硝基苯
祝你学习进步!1年前查看全部
- 关于物质分类(化学)下列物质的分类完全正确的一组是( )A 酸性氧化物:CO,CO2,SO2B 碱:纯碱,烧碱,熟石灰C
关于物质分类(化学)
下列物质的分类完全正确的一组是( )
A 酸性氧化物:CO,CO2,SO2
B 碱:纯碱,烧碱,熟石灰
C 盐:碱式碳酸铜,碳酸氢氨,碳酸钙
D 无氧酸:盐酸,硫酸,氢硫酸
酸性氧化物和碱式碳酸铜都是什么意思啊?
回答请写分析过程, 梦醒无眠1年前1
梦醒无眠1年前1 -
 笑话狼 共回答了15个问题
笑话狼 共回答了15个问题 |采纳率93.3%A 酸性氧化物:CO,CO2,SO2
CO没有相对应的酸,所以不是
B 碱:纯碱,烧碱,熟石灰
纯碱是Na2CO3,是盐不是碱
C 盐:碱式碳酸铜,碳酸氢氨,碳酸钙
D 无氧酸:盐酸,硫酸,氢硫酸
硫酸H2SO4,显然是含氧酸
所以,选C1年前查看全部
- 向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
A. CO32-
B. Cl-
C. OH-
D. Cu2+ 望太白1年前1
望太白1年前1 -
 hgz1314 共回答了17个问题
hgz1314 共回答了17个问题 |采纳率88.2%解题思路:分别加入烧碱固体,溶液中OH-的浓度增大,与OH-反应的离子不能大量共存,以此解答该题.分别加入烧碱固体,溶液中OH-的浓度增大,因Cu2+与OH-反应,它的浓度减小,而A、B中离子浓度不变,故选D.
点评:
本题考点: 离子反应发生的条件.
考点点评: 本题考查离子的性质,侧重于元素化合物知识的综合考查,难度不大,注意把握常见与OH-反应的离子的性质以及反应类型的判断.1年前查看全部
大家在问
- 1用勾股定理求高?已知 直角三角形斜边为a,一直角边为二分之a,求高?
- 2称取含少量杂质(杂质不与酸碱反应)的硫酸铵肥料1.49g,加入足量的碱溶液,加热放出的
- 3加热碱……什么样的碱在加热时会分解?ps:生成相应的金属氧化物和水。
- 4I go swimming in summer 对 in swimming 划线提问
- 5已知5的a次方等于3,5的b次方等于15,5的c次方等于375,请你想想a、b、c之间的关
- 6用勾股定理求角度P为等边三角形ABC内一点,且PA=5,PB=4,PC=3.求角BPC的度数
- 7怎么计算42%浓度三氯化铁稀释到10%的时候所加的量
- 8将下列词语分别造句.1、折服——————2、悲悯——————3、景仰——————4、唐突——————5、顶礼膜拜————
- 9班字可以换成什么偏旁?是去掉了偏旁部首“王”后再添加部首组成新字呀··· 急呀··
- 101、给短文加上合适的题目.2、“我越来越觉得有些不是滋味”,从这句话可以看出“我”当时的心情是怎样的?请你体会着写一写(
- 11加热硫酸铵的化学反应式
- 12将ag氨气溶于bL水中形成密度为cg/cm^3的氨水求其质量分数,量浓度
- 13有向量a、b、c且|a|=|b|=1,a·b=1/2,夹角=60°,则|c|的最大值是?
- 14the rain came in through a crevice in the cabin wall 求大神的准确翻
- 15高中外语短语,一个词有很多种搭配,我想知道各自的汉译,例如:take in take out take away 等等.
