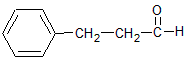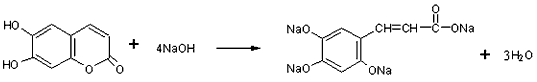有10瓶消炎药片,其中一瓶吃了3片,用天平称,至少称几次就一定能找出吃了3片的那瓶药
 最好没有2022-10-04 11:39:541条回答
最好没有2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 llgame 共回答了17个问题
llgame 共回答了17个问题 |采纳率88.2%- 四次.
第一次:任意5瓶
第二次:剩余5瓶 找出较轻的那五瓶,进行第二次称量,同时根据重的那个可以估计出一瓶的重量为w.
第三次:任意两瓶 如果小于2w,说明吃了三片的那瓶在这两个里面,否则在另三瓶里.因为说至少几次,所以就假定在这两瓶里.
第四次:称量两瓶中的任意一瓶,小于w的话就是这瓶,等于w的话就是另一瓶. - 1年前
相关推荐
- 金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )
 金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )
金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )
A.绿原酸的分子式为C16H8O9
B.1mol绿原酸最多与7molNaOH反应
C.1个绿原酸分子中含有4个手性碳原子
D.绿原酸分子中有4种化学环境不同的氢原子 最烦注册填名字1年前1
最烦注册填名字1年前1 -
 悠悠我心827 共回答了17个问题
悠悠我心827 共回答了17个问题 |采纳率100%解题思路:该有机物含有酚羟基,可发生取代、氧化反应,含有羧基,具有酸性可发生中和、取代反应,含有酯基,可发生水解反应,含有羟基,可发生取代、消去、氧化反应,含有碳碳双键,可发生加成、氧化反应,以此解答该题.A.由有机物的结构简式可知该有机物的分子式为C16H18O9,故A错误;
B.由分子中羧基和酚羟基都能与碱反应,在碱性条件下生成羧基,也消耗NaOH,则1mol绿原酸最多与4molNaOH反应,故B错误;
C.连4各不同基团的C为手性C原子,则环己烷中除2各亚甲基外的4各C均为手性C原子(与-OH或与-COOC-相连的C),故C正确;
D.结构不对称,含15种H,则绿原酸分子中有15种化学环境不同的氢原子,故D错误.
故选C.点评:
本题考点: 有机物的结构和性质.
考点点评: 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系为解答的关键,侧重酚、酯性质的考查,选项CD为解答的难点,题目难度不大.1年前查看全部
- (2010•四川)中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是( )
 (2010•四川)中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是( )
(2010•四川)中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是( )
A.M分子式为180
B.1mol M最多能与2mol Br2发生反应
C.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H5O5Na3
D.1mol M与足量NaHCO3反应能生成2molCO2 晓之林1年前1
晓之林1年前1 -
 my100ing 共回答了18个问题
my100ing 共回答了18个问题 |采纳率94.4%解题思路:A、根据结构简式书写化学式,进而计算相对分子质量;
B、酚羟基的临位和对位氢原子易被卤素原子取代;
C、酚羟基具有酸性,能和氢氧化钠反应生成对应的盐,酯基水解得到对应的钠盐;
D、酚羟基和碳酸氢钠不能发生反应.A、根据结构简式可得化学式为C9H6O4,相对分子质量为178,故A错误;
B、1molM含有酚羟基的临位和对位氢原子2mol,这些氢原子易被卤素原子取代,碳碳双键还可以和溴发生加成反应,所以一共消耗消耗3molBr2,故B错误;
C、酚羟基和酯基均能能和氢氧化钠反应生成对应的盐,所得有机产物的化学式为C9H4O5Na3,故C正确;
D、酚羟基和碳酸氢钠不能发生反应,故D错误.
故选C.点评:
本题考点: 有机物分子中的官能团及其结构;分子式.
考点点评: 本题是一道有机物的化学性质和推断的题目,可以根据所学知识来进行,难度不大.1年前查看全部
- 题开头是靛玉红是一种暗红色针状结晶,具有抗菌消炎抗肿瘤等作用,某校合作学习小组的同学拟测定其组成,已知靛玉红由C.H.O
题开头是靛玉红是一种暗红色针状结晶,具有抗菌消炎抗肿瘤等作用,某校合作学习小组的同学拟测定其组成,已知靛玉红由C.H.O.N四种元素组成,相对分子质量为147,实验流程如下

 ngngfsfn1年前1
ngngfsfn1年前1 -
 恐龙战记 共回答了16个问题
恐龙战记 共回答了16个问题 |采纳率93.8%1、物质的量=2.94÷147=0.02摩尔
2、氮气物质的量=224÷22400=0.01摩尔
3、碳的质量分数=7.04X12÷(44X2.94)=65.31%
4、氧元素质量=2.94-(7.04X12÷44)-0.9X2÷18-0.01X28=0.64克
5、碳、氢、氧、氮原子个数比=1.92/12:0.1/1:0.64/16:0.28/14=16:10:4:2,分子式C16H10O4N21年前查看全部
- 乙酰水杨酸(俗称阿司匹林)是一种常见的解热、消炎、镇痛药物。以苯为主要原料,可以通过下图所示途径可以制取阿司匹林和冬青油
乙酰水杨酸(俗称阿司匹林)是一种常见的解热、消炎、镇痛药物。以苯为主要原料,可以通过下图所示途径可以制取阿司匹林和冬青油 
请按要求回答:
(1)请写出有机物的结构简式:A_____________;B_____________;C_____________。
(2)写出变化过程中①.⑥的化学方程式(注明反应条件)
反应①__________________________________;
反应⑥__________________________________。
(3)变化过程中的②属于____________反应,⑦属于___________反应。
(4)怎样从化学平衡移动的观点理解用乙酸酐代替乙酸可以提高阿司匹林产率?
__________________________________ cambridge1年前1
cambridge1年前1 -
 陆斌ww研究 共回答了18个问题
陆斌ww研究 共回答了18个问题 |采纳率94.4%1年前查看全部
- 小明在运动时不小心把左手的食指弄伤了,伤口红肿,为了消炎,医生在他的右臂注射了青霉素.请问这些药品首先到达心脏的部位是(
小明在运动时不小心把左手的食指弄伤了,伤口红肿,为了消炎,医生在他的右臂注射了青霉素.请问这些药品首先到达心脏的部位是( )
A.右心房
B.左心房
C.左心室
D.右心室 kalayang2581年前0
kalayang2581年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示,下列叙述正确的是( )
中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示,下列叙述正确的是( )
 A. M的相对分子质量是180
A. M的相对分子质量是180
B. 1mol M最多能与2mol Br2发生反应
C. M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4
D. 1mol M与足量NaHCO3反应能生成2mol CO2 皮尔丘1年前1
皮尔丘1年前1 -
 胸毛再生 共回答了16个问题
胸毛再生 共回答了16个问题 |采纳率100%解题思路:A.M的分子式为C9H6O4,以此计算相对分子质量;
B.M中含有2个酚羟基和1个碳碳双键;
C.酚羟基与酯基都能与NaOH溶液反应;
D.M在碱性条件下水解生成的-COOH能与NaHCO3反应.A.M的分子式为C9H6O4,则相对分子质量为12×9+1×6+16×4=178,故A错误;
B.M中含有2个酚羟基和1个碳碳双键,则1 mol M最多能与3molBr2发生反应,故B错误;
C.酚羟基与酯基都能与NaOH溶液反应,则M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4,故C正确;
D.M在碱性条件下水解生成的-COOH能与NaHCO3反应,所以1mol M与足量NaHCO3反应能生成1molCO2,故D错误;
故选C.点评:
本题考点: 有机物分子中的官能团及其结构.
考点点评: 本题考查有机物的结构和性质,明确M中的官能团及结构中酯基水解后的产物为解答的关键,选项CD为解答的难点和易错点.1年前查看全部
- (2012•迪庆州模拟)我们经常可以看到在一些动物受伤后,会用舌头舔自己受伤的部位,能起到一定的消炎止痛的作用.这是因为
(2012•迪庆州模拟)我们经常可以看到在一些动物受伤后,会用舌头舔自己受伤的部位,能起到一定的消炎止痛的作用.这是因为唾液中含有的溶菌酶能杀灭一些细菌,这是一种( )
A.特异性免疫
B.非特异性免疫
C.计划免疫
D.人工免疫 kanily1111年前1
kanily1111年前1 -
 chycmm 共回答了21个问题
chycmm 共回答了21个问题 |采纳率90.5%解题思路:体液中的杀菌物质和吞噬细胞是保卫人体的第二道防线,例如杀菌物质中的溶菌酶能够破坏病菌的细胞壁,使病菌溶解,人体内的吞噬细胞,可以将侵入人体的病原体吞噬和消灭.受伤的动物经常用舌去舔伤口,这是因为口腔里的唾液含有溶菌酶,能破坏进入伤口处的病菌的细胞壁,进而杀灭病菌,这种免疫力是天生就具有的,对多种病原体都有作用,属于非特异性免疫.
故选:B点评:
本题考点: 人体特异性免疫和非特异性免疫;各种消化腺的位置和功能.
考点点评: 知道人体三道防线的组成和特点,特别是第二道防线的作用:通过杀菌物质消灭进入人体的病菌是解答此类题目的关键.1年前查看全部
- (15分)乙酰水杨酸(俗称阿司匹林)是一种常见的解热、消炎、镇痛的药物。以苯为主要原料,可通过下图所示途径来合成:
(15分)乙酰水杨酸(俗称阿司匹林)是一种常见的解热、消炎、镇痛的药物。以苯为主要原料,可通过下图所示途径来合成:

已知:R-X+H 2 O→R-OH+HX(R为烃基,X为卤素原子)
请回答下列问题:
(1)写出有机物的结构简式:A ,B 。
(2)下列关于阿司匹林的叙述正确的是 (填序号)。
E. 使溴的四氯化碳溶液因发生加成反应而褪色A.可与Na 2 CO 3 溶液作用生成CO 2 B.一定条件下,可发生加成、取代、酯化、氧化反应等 C.属于芳香烃类化合物 D.可使滴有酚酞的NaOH溶液褪色
(3)变化过程中反应⑦的反应类型是 。
(4)写出反应①、⑥的化学方程式(有机物写结构简式、注明反应条件):① ;
⑥ 。
(5)冬青油具有多种同分异构体,请写出一种符合下列条件的同分异构体: 。(分子结构中含
有苯环、属于醇类(-OH不能直接连接在苯环上)且1mol该同分异构体与足量金属钠作用能够生成1molH 2 )。 cuteclear1年前1
cuteclear1年前1 -
 xyd6 共回答了26个问题
xyd6 共回答了26个问题 |采纳率100%(1)A: B:
B: (2)ABD(3)取代反应(或酯化反应)
(2)ABD(3)取代反应(或酯化反应)
(4)①: ⑥
⑥ 
(5) 或
或 或
或 等。
等。
(1)由题中信息知:A为溴苯与水发生反应生成的 ;结合⑥、⑦反应知道,B中应即含有-OH、又含有-COOH,所以B的结构简式为:
;结合⑥、⑦反应知道,B中应即含有-OH、又含有-COOH,所以B的结构简式为: 。(2)阿司匹林中含有羧基和酯基,故应具有羧酸和酯类物质的性质,可见A、B、D选项叙述正确而E选项错误;分子中含有氧元素,故不能属于烃类,C选项错。
。(2)阿司匹林中含有羧基和酯基,故应具有羧酸和酯类物质的性质,可见A、B、D选项叙述正确而E选项错误;分子中含有氧元素,故不能属于烃类,C选项错。
(3)反应⑦是酯化反应(或取代反应)。(4)反应①是苯与溴的取代反应,反应条件是以铁粉或FeBr 3 为催化剂;反应⑥羧酸与醇的酯化反应,反应条件为:浓硫酸作催化剂并加热。(5)冬青油的分子式为:C 8 H 8 O 3 ,结合限定条件知符合条件的同分异构体中应有: ,结合分子式知还有一个-COOH连接在苯环上,所以可写出邻、间、对三种符合条件的异构体。
1年前查看全部
,结合分子式知还有一个-COOH连接在苯环上,所以可写出邻、间、对三种符合条件的异构体。
1年前查看全部
- (2014•镇江二模)金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的
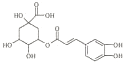 (2014•镇江二模)金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
(2014•镇江二模)金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
A.绿原酸分子中有4个手性碳原子
B.绿原酸能发生显色反应、取代反应和加成反应
C.每摩尔绿原酸最多与4 mol NaOH反应
D.绿原酸分子中所有碳原子都能在同一平面上 一片喜欢秋天叶子1年前1
一片喜欢秋天叶子1年前1 -
 changsha601 共回答了13个问题
changsha601 共回答了13个问题 |采纳率84.6%解题思路:该有机物含有酚羟基,可发生取代、氧化反应,含有羧基,具有酸性可发生中和、取代反应,含有酯基,可发生水解反应,含有羟基,可发生取代、消去、氧化反应,含有碳碳双键,可发生加成、氧化反应,以此解答该题.解;A.连4个不同基团的C为手性C原子,则环己烷中除2各亚甲基外的4个C均为手性C原子(与-OH或与-COOC-相连的C),故A正确;
B.含有酚羟基,可发生显色、取代反应,含有碳碳双键,可发生加成反应,故B正确;
C.由分子中羧基和酚羟基都能与碱反应,在碱性条件下生成羧基,也消耗NaOH,则1mol绿原酸最多与4molNaOH反应,故C正确;
D.分子中含有6个饱和碳原子,由甲烷的结构可知并不是所有的碳原子都在同一个平面上,故D错误.
故选D.点评:
本题考点: 有机物的结构和性质.
考点点评: 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系为解答的关键,侧重酚、酯性质的考查,选项CD为解答的难点,题目难度不大.1年前查看全部
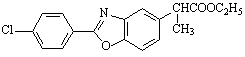
- (2008•江苏)苯噁布洛芬是一种消炎镇痛的药物.它的工业合成路线如下:
(2008•江苏)苯噁布洛芬是一种消炎镇痛的药物.它的工业合成路线如下:
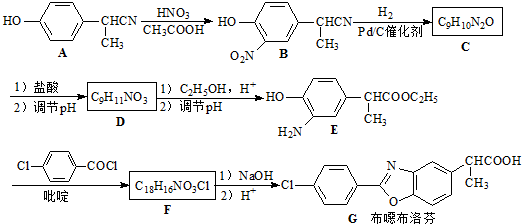
请回答下列问题:
(1)A长期暴露在空气中会变质,其原因是______.
(2)由A到B的反应通常在低温进行.温度升高时,多硝基取代副产物会增多.下列二硝基取代物中,最可能生成的是______.(填字母)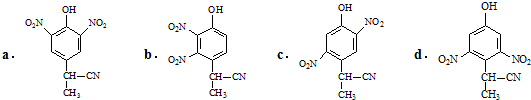
(3)在E的下列同分异构体中,含有手性碳原子的分子是______.(填字母)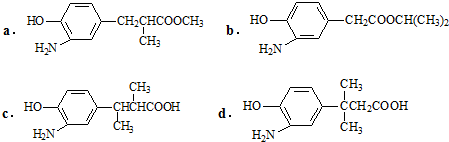
(4)F的结构简式______.
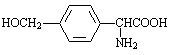
(5)D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,则H的结构简式是______.高聚物L由H通过肽键连接而成,L的结构简式是______. 晴空一鹤是也1年前1
晴空一鹤是也1年前1 -
 bm372 共回答了13个问题
bm372 共回答了13个问题 |采纳率84.6%解题思路:(1)根据苯酚在空气中易被氧化而显粉红色这一现象,可以推知含有酚羟基物质的不稳定性;
(2)根据一硝基取代物可知,硝基取代位置在酚羟基所连碳的邻位,由邻、对位取代原理解答;
(3)手性碳原子是指所连4个基团或原子互不相同的碳原子;
(4)由E、G结构,结合转化关系及F的分子式可知,利用逆推法可知F的结构简式为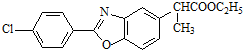 ;
;
(5)由B的结构及C的分子式可知,B中的硝基被还原为氨基,故C为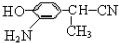 ,结合C、E的结构及D的分子式可知,C中-CN水解为-COOH,故D为
,结合C、E的结构及D的分子式可知,C中-CN水解为-COOH,故D为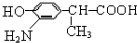 ,D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,由于酚羟基易被氧化,故H中取代基为HOCH2-、-CH(NH2)COOH,处于对位位置,H通过缩聚反应得到高聚物L.
,D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,由于酚羟基易被氧化,故H中取代基为HOCH2-、-CH(NH2)COOH,处于对位位置,H通过缩聚反应得到高聚物L.
(1)根据苯酚在空气中易被氧化而显粉红色这一现象,可以推知酚类化合物易被空气中的O2氧化,故A长期暴露在空气中会变质,
故答案为:酚类化合物易被空气中的O2氧化;
(2)根据一硝基取代物可知,硝基取代位置在酚羟基所连碳的邻位,由邻、对位取代原理可知a物质最有可能生成,
故答案为:a;
(3)手性碳原子是指所连4个基团或原子互不相同的碳原子,b、d中的饱和碳原子所连接的基团有相同部分,不存在手性碳原子,a中含有1个手性碳原子,c中含有2个手性碳原子,
故答案为:ac;
(4)由E、G结构,结合转化关系及F的分子式可知,利用逆推法可知F的结构简式为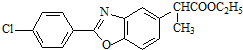 ,
,
故答案为: ;
;
(5)由B的结构及C的分子式可知,B中的硝基被还原为氨基,故C为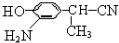 ,结合C、E的结构及D的分子式可知,C中-CN水解为-COOH,故D为
,结合C、E的结构及D的分子式可知,C中-CN水解为-COOH,故D为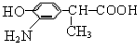 ,D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,由于酚羟基易被氧化,故H中取代基为HOCH2-、-CH(NH2)COOH,处于对位位置,则H的结构简式是
,D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,由于酚羟基易被氧化,故H中取代基为HOCH2-、-CH(NH2)COOH,处于对位位置,则H的结构简式是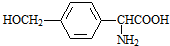 ;聚物L由H通过肽键连接而成,L的结构简式是
;聚物L由H通过肽键连接而成,L的结构简式是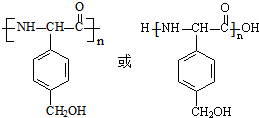 ,
,
故答案为: ;
; .
.点评:
本题考点: 有机物的推断.
考点点评: 本题考查有机物的推断与合成,充分利用合成路线中有机物的分子式、结构式,根据逆推法确定物质的结构,侧重考查学生的推理能力与分析、判断能力,难度中等.1年前查看全部
- 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图,下列叙述正确的是( )
中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图,下列叙述正确的是( )

A.M的相对分子质量为180
B.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4
C.1mol M与足量NaHCO3溶液反应能生成2mol CO2
D.1mol M最多能与2mol Br2发生反应 寻找质量人员1年前1
寻找质量人员1年前1 -
 因为偶然 共回答了11个问题
因为偶然 共回答了11个问题 |采纳率100%解题思路:根据有机物的结构简式判断分子式,进而可确定有机物的相对分子质量,分子中含有酚羟基,可发生取代、氧化和显色反应,含有酯基,可发生水解,水解产物为酚羟基和羧基,含有碳碳双键,可发生加成、加聚和氧化反应,以此解答该题.A.根据结构简式可得化学式为C9H6O4,相对分子质量为178,故A错误;B.酚羟基与酯基都能与NaOH溶液反应,则M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4,故B正确;C.NaHCO3溶液呈碱性,M在碱性...
点评:
本题考点: 有机物的结构和性质.
考点点评: 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,难度不大.1年前查看全部
- (2006•威海)小明患了急性肠炎,医生在他的上臂静脉注射消炎药物进行治疗,请问药物到达患病部位需要经过心脏的次数是(
(2006•威海)小明患了急性肠炎,医生在他的上臂静脉注射消炎药物进行治疗,请问药物到达患病部位需要经过心脏的次数是( )
A.1次
B.2次
C.3次
D.4次 紫浣花1年前1
紫浣花1年前1 -
 bettywawa 共回答了17个问题
bettywawa 共回答了17个问题 |采纳率94.1%解题思路:人体内的血液循环是指血液在心脏和血管组成的密闭系统中循环流动,可分为体循环和肺循环.体循环是从左心室开始依次经过主动脉、体动脉、全身毛细血管、体静脉、上下腔静脉至右心房终止;肺循环是从右心室开始依次经过肺动脉、肺部毛细血管、肺静脉至左心房终止.小明患了急性肠炎,医生在他的上臂静脉注射消炎药物进行治疗,药物到达患病部位需要经过上肢静脉→上腔静脉→右心房→右心室→肺动脉→肺部毛细血管→肺静脉→左心房→左心室→主动脉→肠动脉→肠内毛细血管.药物到达患病部位两次经过心脏.所以A、C、D、选项均不合题意,B选项符合题意.
故选:B点评:
本题考点: 血液循环的途径.
考点点评: 此题考查血液循环的途径,具有一定的综合性.难度偏大.要求学生认真体会分析.1年前查看全部
- 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示,下列叙述正确的是( )
 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示,下列叙述正确的是( )
中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示,下列叙述正确的是( )
A.M的相对分子质量是180
B.1mol M最多能与2mol Br2发生反应
C.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4
D.1mol M与足量NaHCO3反应能生成2mol CO2 依爱zz1年前1
依爱zz1年前1 -
 版主001 共回答了15个问题
版主001 共回答了15个问题 |采纳率93.3%解题思路:A.M的分子式为C9H6O4,以此计算相对分子质量;
B.M中含有2个酚羟基和1个碳碳双键;
C.酚羟基与酯基都能与NaOH溶液反应;
D.M在碱性条件下水解生成的-COOH能与NaHCO3反应.A.M的分子式为C9H6O4,则相对分子质量为12×9+1×6+16×4=178,故A错误;
B.M中含有2个酚羟基和1个碳碳双键,则1 mol M最多能与3molBr2发生反应,故B错误;
C.酚羟基与酯基都能与NaOH溶液反应,则M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4,故C正确;
D.M在碱性条件下水解生成的-COOH能与NaHCO3反应,所以1mol M与足量NaHCO3反应能生成1molCO2,故D错误;
故选C.点评:
本题考点: 有机物分子中的官能团及其结构.
考点点评: 本题考查有机物的结构和性质,明确M中的官能团及结构中酯基水解后的产物为解答的关键,选项CD为解答的难点和易错点.1年前查看全部
- 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示下列叙述正确的是( )
 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示下列叙述正确的是( )
中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示下列叙述正确的是( )
A.M的相对分子质量是178
B.1mol M最多能与2mol Br2发生反应
C.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4
D.1mol M与足量NaHCO3反应能生成2mol CO2 huanayue1年前1
huanayue1年前1 -
 清淡烟草味道 共回答了28个问题
清淡烟草味道 共回答了28个问题 |采纳率96.4%解题思路:A.M的分子式为C9H6O4,以此计算相对分子质量;
B.M中含有2个酚羟基和1个碳碳双键;
C.酚羟基与酯基都能与NaOH溶液反应;
D.酚羟基和酯基都不与碳酸氢钠反应.A.M的分子式为C9H6O4,则相对分子质量为12×9+1×6+16×4=178,故A正确;
B.苯环上酚羟基邻对位共有两个H,另外一个环上还有一个 ,最多消耗3mol Br2,故B错误;
,最多消耗3mol Br2,故B错误;
C.M中含有酯基,发生水解后,苯环上含有3个酚羟基,还生成一个羧基,所以1mol M共与4mol NaOH反应,所得有机物的化学式为C9H4O5Na4,故C正确;
D.酚羟基和酯基都不与碳酸氢钠反应,故D错误;
故选AC.点评:
本题考点: 有机物分子中的官能团及其结构.
考点点评: 本题考查有机物的结构和性质,明确M中的官能团及结构中酯基水解后的产物为解答的关键,选项CD为解答的难点和易错点.1年前查看全部
- 医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al 3+ 、Fe 3+ 等杂质)生产医用二水合氯
医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al 3+ 、Fe 3+ 等杂质)生产医用二水合氯化钙的工艺流程为:(已知二水合氯化钙在温度超过160°C时分解为氯化钙和水) 
已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
(1)在实验室进行溶解时玻璃棒的作用是______,过滤时用到的玻璃仪器有烧杯、玻璃棒、______.氢氧化物 Fe(OH) 3 Al(OH) 3 开始沉淀时的pH 2.3 4.0 开始溶解:7.8 完全沉淀时的pH 3.7 5.2 完全溶解:10.8
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al 3+ 、Fe 3+ 全部转化为沉淀,此时应该控制溶液的pH(X)范围是______;滤渣A的主要成分的化学式为______.
(3)酸化时加盐酸的主要目的为了______.
(4)蒸发结晶时,必须控制温度低于160℃的原因是______.
(5)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少? 东方63871年前1
东方63871年前1 -
 scof12 共回答了20个问题
scof12 共回答了20个问题 |采纳率90%(1)在实验室进行溶解时玻璃棒的作用是加快溶解(速度),过滤时用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)根据表格中的数据,则可知加入稍过量的氢氧化钙,调节溶液的pH使Al 3+ 、Fe 3+ 全部转化为沉淀,此时应该控制溶液的pH(X)范围是5.2<X<7.8(或5.2-7.8);因为氢氧化钙与Al 3+ 、Fe 3+ 全部转化为沉淀,故滤渣A的主要成分的化学式为 Fe(OH) 3 、Al(OH) 3 .
(3)利用中和反应的应用,则酸化时加盐酸的主要目的为除去过量的氢氧化钙[(Ca(OH) 2 或OH - ].
(4)“已知二水合氯化钙在温度超过160°C时分解为氯化钙和水”,则蒸发结晶时,必须控制温度低于160℃的原因是防止二水合氯化钙分解(或防止产物分解).
(5)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则设CaCO 3 最大质量为x.
CaCO 3 +2HCl═CaCl 2 +H 2 O+CO 2 ↑
100 111
x 11.1kg
则
100
x =
111
11.1kg ,解得x=10kg
10kg
12.5kg ×100%=80%
答:样品中碳酸钙的质量分数最大为80%.
故答案为:
(1)加快溶解(速度),漏斗
(2)5.2<X<7.8(或5.2-7.8); Fe(OH) 3 、Al(OH) 3 (少一种不给分)
(3)除去过量的氢氧化钙[(Ca(OH) 2 或OH - ];
(4)防止二水合氯化钙分解(或防止产物分解)
(5)80%.1年前查看全部
- (2005•益阳)安比先是一种常见的消炎药品,其主要成分氨苄西林的化学式为C16H19N3O4S•3H2O,其中含有__
(2005•益阳)安比先是一种常见的消炎药品,其主要成分氨苄西林的化学式为C16H19N3O4S•3H2O,其中含有______ 种元素.
 ww哥哥1年前1
ww哥哥1年前1 -
 樱桃飞啊飞 共回答了20个问题
樱桃飞啊飞 共回答了20个问题 |采纳率95%解题思路:根据氨苄西林的化学式C16H19N3O4S•3H2O判断,先找出元素符号,再判断元素种类.氨苄西林的化学式为C16H19N3O4S•3H2O,可见,它是由碳、氢、氮、氧、硫共5种元素组成的.
故答案为:5.点评:
本题考点: 物质的元素组成.
考点点评: 化学是研究物质的组成、结构、性质及其变化规律的科学,物质的组成和结构决定物质的性质,物质的性质决定物质的用途,所以了解物质的组成和结构,是研究物质的基础.1年前查看全部
- 医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙为原料含量为(97.5%,含有少量Na+、Al3+、Fe3+等
医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙为原料含量为(97.5%,含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙的主要流程如下:

(1)除杂操作时加入试剂A,调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+.试剂A可以选择______.a.Ca(OH)2b.NaOH c.NH3d.Na2CO3
(2)检验溶液1中是否含Fe3+的方法是______.
(3)请指出下列操作的名称:操作1______;操作2______;请指出操作1中所用的玻璃仪器的名称______.
(4)写出加入碳酸铵所发生的反应的离子方程式______;写出溶液2的一种用途______.
(5)准确称取100g工业碳酸钙粉末,通过上述方法理论上可以制得质量分数为99%的医药级二水合氯化钙的质量为______. 她怕我抢了1年前1
她怕我抢了1年前1 -
 zhuogyue 共回答了19个问题
zhuogyue 共回答了19个问题 |采纳率94.7%解题思路:工业碳酸钙加入盐酸可完全溶解生成氯化钙、氯化铁以及氯化铝等,加入试剂A溶液调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+,然后在加入碳酸铵生成碳酸钙沉淀,过滤得碳酸钙固体,再加盐酸酸化,在酸性条件下蒸发结晶可得到CaCl2•2H2O,
(1)加入试剂A溶液调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+,则从不引入新的杂质分析;
(2)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液;
(3)根据以上分析,操作1为过滤,操作2为蒸发浓缩、冷却结晶,过滤需要烧杯、玻璃棒和普通漏斗;
(4)加入碳酸铵,碳酸根与钙离子结合成碳酸钙沉淀;过滤出碳酸钙后得溶液2为氯化铵溶液,可用作氮肥;
(5)根据钙守恒进行计算.工业碳酸钙加入盐酸可完全溶解生成氯化钙、氯化铁以及氯化铝等,加入试剂A溶液调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+,然后在加入碳酸铵生成碳酸钙沉淀,过滤得碳酸钙固体,再加盐酸酸化,在酸性条件下蒸发结晶可得到CaCl2•2H2O,
(1)加入试剂A溶液调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+,则试剂A具有碱性,但又不能引入新的杂质,而且后面还加入碳酸铵,所以ac都符合,故选:ac;
(2)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液,操作为取少量溶液于试管中,加入硫氰化钾溶液,若溶液不变血红色,说明溶液中不含Fe3+;若溶液变血红色,说明溶液中含Fe3+;故答案为:取少量溶液于试管中,加入硫氰化钾溶液,若溶液不变血红色,说明溶液中不含Fe3+;若溶液变血红色,说明溶液中含Fe3+;
(3)根据以上分析,操作1为过滤,操作2为蒸发浓缩、冷却结晶,过滤需要烧杯、玻璃棒和普通漏斗,故答案为:过滤;蒸发浓缩、冷却结晶;漏斗、玻璃棒、烧杯;
(4)加入碳酸铵,碳酸根与钙离子结合成碳酸钙沉淀,离子方程式为:Ca2++CO32-═CaCO3↓;过滤出碳酸钙后得溶液2为氯化铵溶液,可用作氮肥;故答案为:Ca2++CO32-═CaCO3↓;作氮肥;
(5)根据钙守恒,则有CaCO3~CaCl2•2H2O,设理论上可以制得质量分数为99%的医药级二水合氯化钙的质量为ag
100 147
100×97.5% a×99%
[100/100×97.5%]=[147/a×99%],解得a=144.8g,故答案为:144.8g;点评:
本题考点: 探究物质的组成或测量物质的含量;物质的分离、提纯和除杂.
考点点评: 本题主要考查实验的基本操作、实验仪器的选择、离子的检验,为高频考点,侧重于学生的分析、实验和计算能力的考查,注意离子的检验方法和常见仪器的使用,样品纯度的分析要注意溶液中可能发生的反应,难度中等.1年前查看全部
- 若腮腺发炎,为了消炎在上臂进行静脉注射后,药物最先到达心脏的四个腔中的
 leilei84651年前1
leilei84651年前1 -
 紫云叶子 共回答了10个问题
紫云叶子 共回答了10个问题 |采纳率100%经上臂静脉,经腋静脉、锁骨下静脉回流至右心房,从右心室泵出经肺动脉至肺循环,经肺静脉回流至左心房,然后从左心室经主动脉泵出至全身,其中一部分经颈动脉-颈外动脉到腮腺.1年前查看全部
- 布噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
布噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
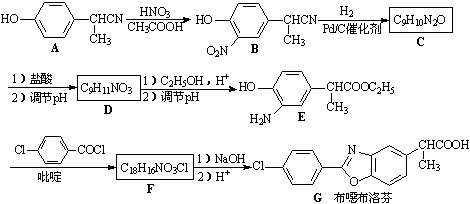
请回答下列问题:
(1)化合物A的分子式为 。
(2)A长期暴露在空气中会变质,其原因是 。
(3)由A到B的反应通常在低温时进行。温度升高时,多硝基取代副产物会增多。下列二硝基取代物中,最可能生成的是 (填字母,2分)。
a.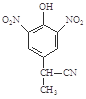 b.
b.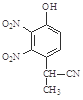 c.
c.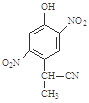 d.
d.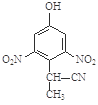
(4)B被H 2 还原的产物C的结构简式为 。
(5)D→E的化学方程式为: 。
(6)F的结构简式 。
(7)D的同分异构体H是一种α-氨基酸,H可被酸性KMnO 4 溶液氧化成对苯二甲酸,则H的结构简式是 。 天冷穿大yy1年前1
天冷穿大yy1年前1 -
 麻杏石甘汤 共回答了23个问题
麻杏石甘汤 共回答了23个问题 |采纳率82.6%1年前查看全部
- 乙酰水杨酸(俗称阿司匹林)是一种常见的解热、消炎、镇痛药物,它是一种有机弱酸,其结构简式: ,易溶于水,能和碱反应。当1
乙酰水杨酸(俗称阿司匹林)是一种常见的解热、消炎、镇痛药物,它是一种有机弱酸,其结构简式:
 ,易溶于水,能和碱反应。当1mol阿司匹林和足量氢氧化钠溶液反应时最多需氢氧化钠
,易溶于水,能和碱反应。当1mol阿司匹林和足量氢氧化钠溶液反应时最多需氢氧化钠A.2mol B.3mol C.4mol D.5mol  edmundding1年前1
edmundding1年前1 -
 常掏出来看看 共回答了15个问题
常掏出来看看 共回答了15个问题 |采纳率73.3%1年前查看全部
- 医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有 少量Na + 、Al 3+ 、Fe 3+ 等杂质)生产
医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有 少量Na + 、Al 3+ 、Fe 3+ 等杂质)生产医药级二水合氯化钙(CaCl 2 ·2H 2 O的质量分 数为97.0%~103.0%)的主要流程如下: 
(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0一8.5,以除去溶液中的少量 Al 3+ 、Fe 3+ 。检验Fe(OH) 3 是否沉淀完全的实验操作是_____________________________________________。
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①将溶液中的少量 Ca( OH) 2 转化为CaCl 2 ;②防止Ca 2+ 在蒸发时水解;③____。
(3)测定样品中Cl - 含量的方法是:a称取0.7500 g样品,溶解在250 mL容量瓶中定容;b量取25.00 mL待测溶液于锥形瓶中;c用0.05000 moI/LAgNO 3 溶液滴定至终点,消耗AgNO 3 溶液体积的平均值为20. 39 mL。
①述测定过程中需用溶液润洗的仪器有_______________ 。
②计算上述样品中CaCl 2 ·2H 2 O的质量分数为___________________。
③若用上述方法测定的样品中CaCl 2 ·2H 2 O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有___________________________;_____________________ 。 见证这一刻1年前1
见证这一刻1年前1 -
 清波钱塘门 共回答了13个问题
清波钱塘门 共回答了13个问题 |采纳率100%(1)取少量上层清液,滴加KSCN溶液,若不出现血红色,表明Fe( OH) 3 沉淀完全
(2)防止溶液吸收空气中的CO 2
(3)①酸式滴定管 ;②99.9% ;③样品中存在少量的NaCl ;少量CaCl 2 ·2H 2 O失水1年前查看全部
- 某人手指发炎,护士在其臀部肌肉注射消炎药物,此药物运至手指的途径是( )
某人手指发炎,护士在其臀部肌肉注射消炎药物,此药物运至手指的途径是( )
①左心房、左心室 ②右心房、右心室 ③肺部毛细血管网 ④主动脉 ⑤肺动脉 ⑥肺静脉 ⑦下腔静脉 ⑧上肢动脉 ⑨上肢毛细血管网.
A. ⑦②⑤③⑥①④⑧⑨
B. ⑦①⑤③⑥②④⑨⑧
C. ⑧⑨⑦②⑤③⑥①④
D. ③①⑤⑧⑥②④⑨⑦ yingbij1年前0
yingbij1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 阿司匹林能迅速解热、镇痛和消炎.长效缓释阿司匹林可在人体内逐步水解使疗效更佳用苯酚和丙酮为主要原料合成长效缓释阿司匹林的
阿司匹林能迅速解热、镇痛和消炎.长效缓释阿司匹林可在人体内逐步水解使疗效更佳用苯酚和丙酮为主要原料合成长效缓释阿司匹林的流程如下图.

已知: 回答下列问题:
回答下列问题:
(1)写出下列反应的类型:反应①______;反应④______.
(2)写出下列物质结构简式:A:______; G:______.
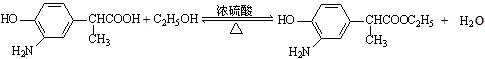
(3)写出B→C的反应方程式(CH3)2C(OH)COOH
CH2=C(CH3)COOH+H2O浓硫酸 △ (CH3)2C(OH)COOH.反应⑤是合成长效缓释阿司匹林的方程式______.
CH2=C(CH3)COOH+H2O浓硫酸 △  xiangzulian1年前1
xiangzulian1年前1 -
 aixiaoxi 共回答了20个问题
aixiaoxi 共回答了20个问题 |采纳率95%解题思路:(1)由信息可知,反应①是丙酮与HCN在碱性条件下发生加成反应生成A,G与乙酸酐反应生成阿司匹林与乙酸,结构阿司匹林的结构可知,G为 ,故反应④发生取代反应;
,故反应④发生取代反应;
(2)由信息可知,反应①是丙酮与HCN在碱性条件下发生加成反应生成 ,由(1)中分析可知G为
,由(1)中分析可知G为 ;
;
(3)由长效缓释阿司匹林的结构、结合乙二醇、阿司匹林的结构可知,D为 ,故C为CH2=C(CH3)COOH,结合A的结构,B在浓硫酸、加热条件下生成C,可以推断A酸化是-CN基团转化为-COOH生成B,故B的结构简式为(CH3)2C(OH)COOH.
,故C为CH2=C(CH3)COOH,结合A的结构,B在浓硫酸、加热条件下生成C,可以推断A酸化是-CN基团转化为-COOH生成B,故B的结构简式为(CH3)2C(OH)COOH.
(1)由信息可知,反应①是丙酮与HCN在碱性条件下发生加成反应生成A,G与乙酸酐反应生成阿司匹林与乙酸,结构阿司匹林的结构可知,G为
 ,故反应④发生取代反应,
,故反应④发生取代反应,
故答案为:加成反应;取代反应;
(2)由信息可知,反应①是丙酮与HCN在碱性条件下发生加成反应生成A,A的结构简式为 ,由(1)中分析可知G为
,由(1)中分析可知G为 ,
,
故答案为: ;
; ;
;
(3)由长效缓释阿司匹林的结构、结合乙二醇、阿司匹林的结构可知,D为 ,故C为CH2=C(CH3)COOH,结合A的结构,B在浓硫酸、加热条件下发生消去反应生成C,可以推断A酸化是-CN基团转化为-COOH生成B,故B的结构简式为(CH3)2C(OH)COOH,
,故C为CH2=C(CH3)COOH,结合A的结构,B在浓硫酸、加热条件下发生消去反应生成C,可以推断A酸化是-CN基团转化为-COOH生成B,故B的结构简式为(CH3)2C(OH)COOH,
故B→C的反应方程式为:(CH3)2C(OH)COOH
浓硫酸
△CH2=C(CH3)COOH+H2O,
反应⑤的方程式为: ,
,
故答案为:(CH3)2C(OH)COOH
浓硫酸
△CH2=C(CH3)COOH+H2O; .
.点评:
本题考点: 有机物的推断.
考点点评: 本题考查有机物的推断与合成,根据阿司匹林与长效缓释阿司匹林的结构推断G、C的结构是解题的关键,注意对反应信息的利用,酸化时-CN基团转化为-COOH,需要学生根据转化关系判断,注重对学生的自学能力、理解能力、分析归纳能力、知识迁移能力的考查.1年前查看全部
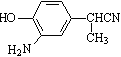
- 原儿茶醛是制造医药及染料的中间体,可用于制造多种抗菌素和消炎药物.其结构如图:
原儿茶醛是制造医药及染料的中间体,可用于制造多种抗菌素和消炎药物.其结构如图:
请回答:
(1)原儿茶醛中含氧官能团的名称是______.
(2)1mol原儿茶醛最多能与______mol H 2 发生加成反应.
(3)下列关于原儿茶醛的说法正确的是______(填序号).
①分子式为 C 7 H 8 O 3 ②能发生银镜反应 ③能与氢氧化钠溶液反应
(4)写出满足下列条件的原儿茶醛的同分异构体的结构简式:______.
①能发生水解反应②苯环上的一氯代物有两种.
 even20101年前1
even20101年前1 -
 dragon03262 共回答了17个问题
dragon03262 共回答了17个问题 |采纳率70.6%1年前查看全部
- (2014•江苏模拟)金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说
 (2014•江苏模拟)金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )
(2014•江苏模拟)金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )
A.绿原酸的分子式为C16H8O9
B.1mol绿原酸最多与4mol NaOH反应
C.1个绿原酸分子中含有4个手性碳原子
D.绿原酸分子中有4种化学环境不同的氢原子 nngoods1年前1
nngoods1年前1 -
 不会睡觉的树熊 共回答了11个问题
不会睡觉的树熊 共回答了11个问题 |采纳率81.8%解题思路:该有机物含有酚羟基,可发生取代、氧化反应,含有羧基,具有酸性可发生中和、取代反应,含有酯基,可发生水解反应,含有羟基,可发生取代、消去、氧化反应,含有碳碳双键,可发生加成、氧化反应,以此解答该题.A.由有机物的结构简式可知该有机物的分子式为C16H18O9,故A错误;
B.由分子中羧基和酚羟基都能与碱反应,在碱性条件下生成羧基,也消耗NaOH,则1mol绿原酸最多与4molNaOH反应,故B正确;
C.连4各不同基团的C为手性C原子,则环己烷中除2各亚甲基外的4各C均为手性C原子(与-OH或与-COOC-相连的C),故C正确;
D.结构不对称,含15种H,则绿原酸分子中有15种化学环境不同的氢原子,故D错误.
故选BC.点评:
本题考点: 有机物的结构和性质;有机物分子中的官能团及其结构.
考点点评: 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系为解答的关键,侧重酚、酯性质的考查,选项CD为解答的难点,题目难度不大.1年前查看全部
- [化学---有机化学基础]香豆素是广泛存在于植物中的一类芳香族化合物,具有抗菌和消炎作用.它的核心结构
[化学---有机化学基础]香豆素是广泛存在于植物中的一类芳香族化合物,具有抗菌和消炎作用.它的核心结构
[化学---有机化学基础]
香豆素是广泛存在于植物中的一类芳香族化合物,具有抗菌和消炎作用.它的核心结构是芳香内酯,其结构简式为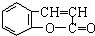 .
.
(1)下列关于芳香内酯的叙述正确的是______.
A.分子式为C9H8O2 B.可发生加聚反应
C.能与溴水发生反应D.1mol芳香内酯最多能和5mol氢气发生加成反应
(2)写出芳香内酯在酸性条件下水解的化学方程式:______.
(3)芳香内酯经下列步骤可转变为水杨酸等物质: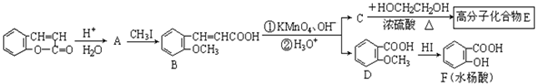
提示:CH3CH=CHCH2CH3
CH3COOH+CH3CH2COOH①KMnO4、OH? ②H30+
请回答下列问题:
①指出D→F的反应类型为______.
②请写出反应C→E的化学方程式:______.
③在一定条件下阿司匹林(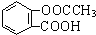 )可由水杨酸制得.下列可检验阿司匹林样品中混有水杨酸的试剂是______.
)可由水杨酸制得.下列可检验阿司匹林样品中混有水杨酸的试剂是______.
a.三氯化铁溶液b.碳酸氢钠溶液c.石蕊试液d.氢氧化钠溶液
④水杨酸的同分异构体中含有酚羟基且属于酯类的共有3种,写出其中一种同分异构体的结构简式______.
 lshding1年前1
lshding1年前1 -
 Jinnnn 共回答了22个问题
Jinnnn 共回答了22个问题 |采纳率90.9%(1)A、根据结构简式可以得出分子式为:C9H6O2,故A错误;
B、有机物中含有碳碳双键,能发生加聚反应,故B正确;
C、有机物中含有碳碳双键,能和溴水发生加成反应,故C正确;
D、有机物中含有不饱和键,能发生加成反应,但是酯基不能加成,所以1mol芳香内酯最多能和4mol氢气发生加成反应,故D错误.
故选BC.
(2)芳香内酯在酸性条件下水解的原理方程式为: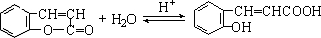 ,故答案为:
,故答案为: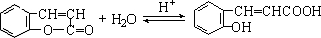 ;
;
(3)①D→F的转化过程是有机物D中的H被甲基取代的过程,属于取代反应,故答案为:取代反应;
②根据提示信息:CH3CH=CHCH2CH3
①KMnO4、OH?
②H30+CH3COOH+CH3CH2COOH,有机物质B被氧化的产物中有一种是乙二酸,可以和乙二醇之间发生缩聚反应,即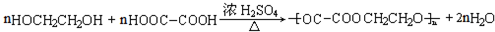 ,故答案为:
,故答案为: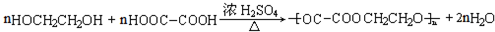 ;
;
③水杨酸中含有酚羟基,但是阿司匹林中不含有酚羟基,酚羟基的检验可以用氯化铁来检验,故选a.
④含有酚羟基且属于酯类的分子式为C7H603的同分异构体有: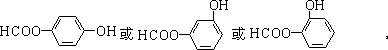 ,故答案为:
,故答案为: .
1年前查看全部
.
1年前查看全部
- 初三化学题急求!医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少.
初三化学题急求!医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少.
医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al3+、Fe3+等杂质)生产医用二水合氯化钙的工艺流程为:碳酸钙样品--溶解(盐酸)--除杂(氢氧化钙)--过滤(滤渣)--酸化(盐酸)--蒸发结晶(160度)(Cacl2.h2o) (已知二水合氯化钙在温度超过160°C时分解为氯化钙和水) 已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
氢氧化物 Fe(OH)3 Al(OH)3
开始沉淀时的pH 2.3 4.0开始溶解:7.8
完全沉淀时的pH 3.7 5.2完全溶解:10.8
(2)除杂操作是加入氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的的pH(X)范围是 ;滤渣A的主要成分的化学式为 . (3)酸化时加盐酸的主要目的为了 . .()若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少 ?
 注册5帮助1年前1
注册5帮助1年前1 -
 10cfbr 共回答了15个问题
10cfbr 共回答了15个问题 |采纳率100%(2)控制pH为8到8.5.滤渣为Fe(OH)3
(3)将溶液中的Ca(OH)2转化为CaCl2;防止Ca2+在蒸发时水解;放置溶液吸收空气中的CO2
(4)氯化钙100mol,反推回去碳酸钙也是100mol,碳酸钙的质量为10kg,碳酸钙的质量分数为10/12.5*100%=80%1年前查看全部
- 英语翻译经常饮用加糖的红茶、加牛奶的红茶,能消炎、保护胃黏膜.而且特别适宜秋冬季节饮用.
 FBLA1年前5
FBLA1年前5 -
 Kris_ZHU 共回答了23个问题
Kris_ZHU 共回答了23个问题 |采纳率87%Drinking black tea added with sugar or milk often can prevent gastricism.Also,it's very suitable for drinking on fall and winter.
医学词太难了,建议你再查查,那个保护胃黏膜,我只能翻译为防止胃黏膜发炎什么的...
一楼的最后一句和第一句好像不对吧?不过我觉得那个digest 用得很好1年前查看全部
- 对药物的认识和使用正确的是( ) A.感冒时服用适量阿司匹林 B.大部分药物没有副作用 C.创可贴不能用于伤口消炎 D
对药物的认识和使用正确的是( ) A.感冒时服用适量阿司匹林 B.大部分药物没有副作用 C.创可贴不能用于伤口消炎 D.胃酸过多只要冲服板蓝根冲剂即可治愈  看看太阳的人1年前1
看看太阳的人1年前1 -
 zhm_7aa09 共回答了21个问题
zhm_7aa09 共回答了21个问题 |采纳率100%A.阿司匹林是解热镇痛药,感冒时服用适量阿司匹林,故A正确;
B.药物都有副作用,应合理使用,故B错误;
C.创可贴没有消炎作用,不能用于伤口消炎,故C正确;
D.板蓝根冲剂有清热解毒作用,不是抗酸药,故D错误.
故选AC.1年前查看全部
- 乙酰水杨酸(俗称阿司匹林)是一种常见的解热、消炎、镇痛药物,它是一种有机弱酸,其结构简式为
乙酰水杨酸(俗称阿司匹林)是一种常见的解热、消炎、镇痛药物,它是一种有机弱酸,其结构简式为
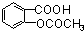
易溶于水,能和碱反应.当1mol阿司匹林和足量氢氧化钠溶液反应时最多需氢氧化钠( )
A.2mol
B.3mol
C.4mol
D.5mol 你牛不牛1年前1
你牛不牛1年前1 -
 何人是我 共回答了22个问题
何人是我 共回答了22个问题 |采纳率81.8%解题思路:该有机物含有羧基和酯基,水解产物为水杨酸和乙酸,水杨酸中含有酚羟基和羧基,乙酸含有羧基,结合有机物官能团的性质解答该题.该有机物含有羧基和酯基,水解产物为水杨酸和乙酸,水杨酸中含有酚羟基和羧基,乙酸含有羧基,都能与氢氧化钠发生中和反应,则当1mol阿司匹林和足量氢氧化钠溶液反应时最多需氢氧化钠3mol,
故选B.点评:
本题考点: 有机物的结构和性质.
考点点评: 本题考查有机物的结构和性质,题目难度不大,注意把握有机物的水解产物的官能团的性质.1年前查看全部
- 中药秦皮中含有的七叶内酯属于香豆素类,具有显著的消炎作用,是抗痢疾杆菌的有效成分。其结构简式如下 (1)七叶内酯的含氧官
中药秦皮中含有的七叶内酯属于香豆素类,具有显著的消炎作用,是抗痢疾杆菌的有效成分。其结构简式如下 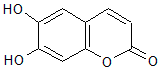
(1)七叶内酯的含氧官能团的结构简式为___________。
(2)七叶内酯可以发生的反应类型有___________(填序号)。
a.加成反应 b.取代反应 c.消去反应
(3)香豆素类物质常被看做是肉桂酸的衍生物。工业上可用物质A制备肉桂酸和肉桂醇。反应关系如下
A的结构简式为__________。
(4)七叶内酯与足量氢氧化钠稀溶液充分反应。化学方程式为_______________。 疼痛忧伤1年前1
疼痛忧伤1年前1 -
 yhf616 共回答了24个问题
yhf616 共回答了24个问题 |采纳率87.5%1年前查看全部
- 乙酰水杨酸(俗称阿司匹林)是一种常见的解热,消炎,镇痛药物,
乙酰水杨酸(俗称阿司匹林)是一种常见的解热,消炎,镇痛药物,
乙酰水杨酸(俗称阿司匹林)是一种常见的解热,消炎,镇痛药物,俗称阿司匹林,科学家试图把它连接在某种高分
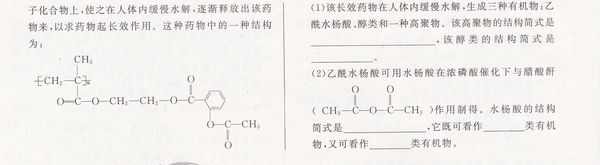
 秋爽19781年前1
秋爽19781年前1 -
 驿亭缘 共回答了19个问题
驿亭缘 共回答了19个问题 |采纳率84.2%1年前查看全部
- 某人脚背发炎,护士在他的臀部肌肉注射消炎药物,此药物运至足部的途径是( )
某人脚背发炎,护士在他的臀部肌肉注射消炎药物,此药物运至足部的途径是( )
①左心房、左心室 ②右心房、右心室 ③肺部毛细血管网 ④主动脉
⑤肺动脉 ⑥肺静脉 ⑦下腔静脉 ⑧下肢动脉.
A. ⑦①⑥③⑤②④⑧
B. ⑦②⑤③⑥①④⑧
C. ⑦⑥③⑤①②④⑧
D. ⑥①⑤③⑦②④⑧ llzlucky1年前2
llzlucky1年前2 -
 独慕斯文 共回答了26个问题
独慕斯文 共回答了26个问题 |采纳率76.9%解题思路:血液在心脏和全部血管所组成的管道系统中的循环流动叫做血液循环.体循环的路线为:左心室→主动脉→全身各级动脉→全身各处毛细血管→全身各处经脉→上下腔静脉→右心房;肺循环的路线为:右心室→肺动脉→肺部毛细血管→肺静脉→左心房.体循环和肺循环是同时进行的,并在心脏处连通在一起,构成一条完整的血液循环路线.如某同学脚背受伤发炎,医生在他的左臀部注射消炎药.此药剂到达足部的历程是,⑦下腔静脉→②右心房、右心室→⑤肺动脉→③肺部毛细血管→⑥肺静脉→①左心房、左心室→④主动脉→⑧下肢动脉→脚部毛细血管(病灶).
故选B点评:
本题考点: 血液循环的途径.
考点点评: 解答此类题目的关键是理解掌握体循环和肺循环路线.1年前查看全部
- 青霉素是一种常用的临床消炎用药,下列相关的说法中不正确的是( ) A.分泌青霉素的生物是一种细菌 B.青霉素是抗生素的
青霉素是一种常用的临床消炎用药,下列相关的说法中不正确的是( ) A.分泌青霉素的生物是一种细菌 B.青霉素是抗生素的一种 C.青霉素可利用微生物发酵技术进行规模化生产 D.青霉素的作用能抑制细菌的生长  折别1年前1
折别1年前1 -
 美杜莎mm 共回答了23个问题
美杜莎mm 共回答了23个问题 |采纳率91.3%青霉属于真菌,发酵能产生青霉素,因此可以利用微生物的发酵技术大规模生产青霉素.青霉素属于抗生素,抗生素可以用来治疗相应的细菌性疾病.可见A符合题意.
故选:A.1年前查看全部
- 香豆素是广泛存在于植物中的一类芳香族化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式
香豆素是广泛存在于植物中的一类芳香族化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C 9 H 6 O 2 。该芳香内酯A经下列步骤转变为水杨酸和乙二酸。
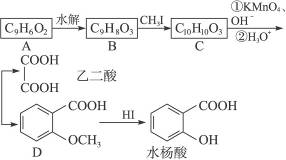
提示:
①CH 3 CH==CHCH 2 CH 3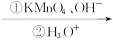 CH 3 COOH+CH 3 CH 2 COOH
CH 3 COOH+CH 3 CH 2 COOH
②R—CH==CH 2 H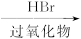 R—CH 2 —CH 2 —Br
R—CH 2 —CH 2 —Br
请完成下列问题:
(1)写出化合物C的结构简式____________。
(2)化合物D有多种同分异构体,其中一类同分异构体是苯的二取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体共有_________种。
(3)在上述转化过程中,反应步骤BC的目的是_________________________。
(4)请设计合理方案从 合成
合成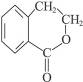 (用反应流程图表示,并注明反应条件)。
(用反应流程图表示,并注明反应条件)。 难以置信西安1年前1
难以置信西安1年前1 -
 趁我还爱你 共回答了15个问题
趁我还爱你 共回答了15个问题 |采纳率93.3%(1) (2)9 (3)保护酚羟基,使之不被氧化 充分理解题目的提示。(1)据乙二酸和D的结构可推知A的结构式;(2)中据水解产物能发生银镜反应可知原物质为甲酸酯类的物质,逐一写出 还有间位、对...1年前查看全部
- (2009•江苏)医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂志)
(2009•江苏)医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂志)生产医药级二水合氯化钙(CaCl2•2H2O的质量分数为97.0%~103.0%)的主要流程如下:

(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以出去溶液中的少量Al3+、Fe3+.检验Fe(OH)3是否沉淀完全的试验操作是______.
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2; ②防止Ca2+在蒸发时水解;③______.
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05000mol•L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL.
①上述测定过程中需要溶液润洗的仪器有______.
②计算上述样品中CaCl2•2H2O的质量分数为______.
③若用上述办法测定的样品中CaCl2•2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有______;______. izyb1年前1
izyb1年前1 -
 HN猴哥 共回答了16个问题
HN猴哥 共回答了16个问题 |采纳率100%解题思路:(1)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液;
(2)Ca(OH)2易吸收空气中的CO2,生成CaCO3沉淀,如果吸收大量的CO2 会导致最终质量分数偏低;
(3)①标准液为硝酸银溶液,所以用酸式滴定管.在使用前应先用硝酸银溶液进行润洗;
②根据到达滴定终点生成氯化银的物质的量等于消耗的硝酸银的物质的量这一关系求出消耗硝酸银的物质的量,则n(AgCl)=2n(CaCl2.2H2O),
据此可以算出实际上的CaCl2.2H2O的物质的量,进而求出质量.注意的是我们是从250mol中取25ml,所以在计算时要注意这一点;
③样品中存在少量的NaCl,根据 n(AgCl)2n(CaCl2.2H2O)可知,CaCl2.2H2O的物质的量增大.同样若CaCl2.2H2O失水导致分母变小,值偏大.(1)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液.
故答案为:取少量上层清液,滴加KSCN溶液,若不出现血红色,则表明Fe(OH)3 沉淀完全;
(2)Ca(OH)2易吸收空气中的CO2,生成CaCO3沉淀,故答案为:防止溶液吸收空气中CO2;
(3)①标准液为硝酸银溶液,所以用酸式滴定管,如用碱式滴定管会腐蚀橡胶管,故答案为:酸式滴定管;
②样品中n(Cl-)=0.05000mol•L-1×0.02039L×10=0.010195mol,根据n(AgCl)=2n(CaCl2.2H2O),则
n(CaCl2.2H2O)=0.0050975mol,所以m(CaCl2.2H2O)=0.0050975mol×147g/mol=0.7493325g,
则有:[0.7493325/0.7500]×100%=99.9%,故答案为:99.9%;
③样品中存在少量的NaCl会导致CaCl2.2H2O的物质的量增大.同样若CaCl2.2H2O失水导致分母变小,值偏大.
故答案为:样品中存在少量的NaCl;少量的CaCl2.2H2O失水点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用;中和滴定.
考点点评: 此题主要考查实验的基本操作、实验仪器的选择、实验误差分析.注意离子的检验方法和常见仪器的使用,样品纯度的分析要注意溶液中可能发生的反应,注意有效数字问题.1年前查看全部
- (初中生物)急性肠炎的病人,除消炎治疗外,一般还要滴注生理盐水,原因是
(初中生物)急性肠炎的病人,除消炎治疗外,一般还要滴注生理盐水,原因是
A.病人体内大量水随尿排出,造成体内缺水
B.肠炎的病人不能喝水
C.病人出汗多,身体虚弱
D.病人喝进的水不能被吸收 紫藤恋_jl1年前3
紫藤恋_jl1年前3 -
 ljazi176 共回答了21个问题
ljazi176 共回答了21个问题 |采纳率95.2%分析题目,生理盐水有关的考点不外乎渗透压(水盐平衡问题)和生理盐水的适用症状,这显然属于后者
关键字:急性肠炎、滴注
我们知道小肠是吸收食物中各种物质的主要器官,初中生物不需要研究太深,以下是答题技巧:
题目中明确标注是滴注,而且病变部位是小肠,A选项不能解释滴注,因为多喝水也能补充水,B选项题目没有给出,而且生物不是医学,这么绝对这么细节的东西是不会学的,因此B条件不足,C同A
因此选D,小肠病变,无法吸收水,只能滴注,而且为了维持水盐平衡必须是生理盐水1年前查看全部
- 金银花是治疗和预防感冒的常见中草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构简式见图,下列有关绿
金银花是治疗和预防感冒的常见中草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构简式见图,下列有关绿原酸的说法不正确的是
( )A.分子式为C 16 H 18 O 9 B.含有羧基、羟基、酯基等含氧官能团 C.1mol绿原酸最多与5molH 2 加成 D.绿原酸可发生氧化、加成、消去等反应 
 财经演义1年前1
财经演义1年前1 -
 战姜 共回答了21个问题
战姜 共回答了21个问题 |采纳率90.5%A.由有机物的结构简式可知该有机物的分子式为C 16 H 18 O 9 ,故A正确;
B.由有机物的结构简式可知该有机物含有羧基、羟基、酯基等含氧官能团,故B正确;
C.能与氢气发生加成反应的有苯环、碳碳双键,则1mol绿原酸最多与4molH 2 加成,故C错误;
D.该有机物含有酚羟基,可发生取代、氧化反应,含有碳碳双键,可发生加成反应,含有羟基,可发生取代、消去、氧化反应,故D正确.
故选C.1年前查看全部
- “绿色广告”,恢复以下词语的容貌(1)某消炎药厂广告词:快治人口,改为?
 等待OPERA1年前1
等待OPERA1年前1 -
 失忆qq 共回答了19个问题
失忆qq 共回答了19个问题 |采纳率100%脍炙人口1年前查看全部
- 医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂志)生产医药级二水合氯
医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂志)生产医药级二水合氯化钙(CaCl2•2H2O的质量分数为97.0%~103.0%)的主要流程如下:

(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以出去溶液中的少量Al3+、Fe3+.检验Fe(OH)3是否沉淀完全的试验操作是______.
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2; ②防止Ca2+在蒸发时水解;③______.
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05000mol•L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL.
①上述测定过程中需要溶液润洗的仪器有______.
②计算上述样品中CaCl2•2H2O的质量分数为______.
③若用上述办法测定的样品中CaCl2•2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有______;______. 若水20051年前1
若水20051年前1 -
 球场军师 共回答了13个问题
球场军师 共回答了13个问题 |采纳率100%解题思路:(1)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液;
(2)Ca(OH)2易吸收空气中的CO2,生成CaCO3沉淀,如果吸收大量的CO2 会导致最终质量分数偏低;
(3)①标准液为硝酸银溶液,所以用酸式滴定管.在使用前应先用硝酸银溶液进行润洗;
②根据到达滴定终点生成氯化银的物质的量等于消耗的硝酸银的物质的量这一关系求出消耗硝酸银的物质的量,则n(AgCl)=2n(CaCl2.2H2O),
据此可以算出实际上的CaCl2.2H2O的物质的量,进而求出质量.注意的是我们是从250mol中取25ml,所以在计算时要注意这一点;
③样品中存在少量的NaCl,根据 n(AgCl)2n(CaCl2.2H2O)可知,CaCl2.2H2O的物质的量增大.同样若CaCl2.2H2O失水导致分母变小,值偏大.(1)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液.
故答案为:取少量上层清液,滴加KSCN溶液,若不出现血红色,则表明Fe(OH)3 沉淀完全;
(2)Ca(OH)2易吸收空气中的CO2,生成CaCO3沉淀,故答案为:防止溶液吸收空气中CO2;
(3)①标准液为硝酸银溶液,所以用酸式滴定管,如用碱式滴定管会腐蚀橡胶管,故答案为:酸式滴定管;
②样品中n(Cl-)=0.05000mol•L-1×0.02039L×10=0.010195mol,根据n(AgCl)=2n(CaCl2.2H2O),则
n(CaCl2.2H2O)=0.0050975mol,所以m(CaCl2.2H2O)=0.0050975mol×147g/mol=0.7493325g,
则有:[0.7493325/0.7500]×100%=99.9%,故答案为:99.9%;
③样品中存在少量的NaCl会导致CaCl2.2H2O的物质的量增大.同样若CaCl2.2H2O失水导致分母变小,值偏大.
故答案为:样品中存在少量的NaCl;少量的CaCl2.2H2O失水点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用;中和滴定.
考点点评: 此题主要考查实验的基本操作、实验仪器的选择、实验误差分析.注意离子的检验方法和常见仪器的使用,样品纯度的分析要注意溶液中可能发生的反应,注意有效数字问题.1年前查看全部
- 非甾体类消炎镇痛药有哪些
 千帆舞661年前1
千帆舞661年前1 -
 蔡_ 共回答了24个问题
蔡_ 共回答了24个问题 |采纳率100%阿司匹林、扑热息痛、非那西丁、保泰松、吲哚美辛、双氯芬酸、布洛芬、氯诺昔康
以上等等,都属于非甾体类消炎镇痛药.1年前查看全部
- 谁知道这种蔓生植物是什么球形果 心状叶 可消炎 花穂生 求解答.
谁知道这种蔓生植物是什么
球形果 心状叶 可消炎 花穂生 求解答.


 正宗花岗岩1年前1
正宗花岗岩1年前1 -
 hellocxl 共回答了20个问题
hellocxl 共回答了20个问题 |采纳率95%黄独,有毒植物.多年生缠绕草本.地下导体茎球形或逐年增大为圆柱形,外皮棕黑色,密生须根.茎圆柱形,平滑,淡绿色,稍带红紫色;叶腋内常生球形或卵圆形珠芽(或称零余子),大小不一,外皮黄褐色.叶互生,心状卵形,长7-15厘米,宽6-14厘米,先端急尖,基部心形,全缘,上面暗绿色,下面淡绿色,叶脉明显,7-9条,基出;叶柄基部扭曲而稍宽,与叶片等长或稍短.花单性,雌雄异株;穗状花序腋生;雄花序纤弱,1-5条,下垂,长3-10厘米,花被6片,披针形,雄蕊6枚,花丝甚短;雌花序长10-25厘米,下垂,.雌花直立,退化雄蕊6枚,子房下位,3室,柱头不规则2-3裂.蒴果下垂,长圆形,有3翅,3瓣裂.种子菱形.呈镰刀状,褐色,有膜质翅.花期8-9月,果期9-10月.
 1年前查看全部
1年前查看全部
- 用3%的硼酸溶液敷脸,可以对皮肤消炎吗?
 兰色_ww1年前1
兰色_ww1年前1 -
 piggy1971 共回答了19个问题
piggy1971 共回答了19个问题 |采纳率94.7%4%溶液用于皮肤、粘膜(腔)、膀胱、角膜伤口的冲洗清洁,口腔炎和咽喉炎时含漱,急性湿疹和急性皮炎伴大量渗液时湿敷.
但是硼酸有毒,大量和长期的时候会损伤人体,尤其是人体的易受伤部位,比如眼睛.还是不建议使用.1年前查看全部
- 用3硼酸溶液敷脸,可以对皮肤消炎吗?
 songlei82031年前3
songlei82031年前3 -
 阿荣旗 共回答了21个问题
阿荣旗 共回答了21个问题 |采纳率81%硼酸溶液有抑菌消炎作用,皮肤红肿时可以做湿敷.硼酸水溶性比较好,使用3%硼酸溶液湿敷,每日3-5次,每次10分钟左右.用毛巾或者面膜巾沾3%硼酸水敷脸,消肿褪红效果很好 价格便宜,而且没有副作用1年前查看全部
- 搞笑的谐音成语,例如消炎杀菌(萧炎沙军)、最好可以弄成人名的.就象我发的那样的那种.不是成语的也Ok、反正就是弄成四个字
搞笑的谐音成语,
例如消炎杀菌(萧炎沙军)、最好可以弄成人名的.就象我发的那样的那种.
不是成语的也Ok、反正就是弄成四个字的搞笑的成语或词语、却可以拆成2个名字的. 心情不好专用mm1年前1
心情不好专用mm1年前1 -
 wugui2635581 共回答了14个问题
wugui2635581 共回答了14个问题 |采纳率92.9%马勒戈壁
词义:比喻天下太平,不再用兵.现形容思想麻痹.
出处:《尚书.武成》:“王来自商,至于丰,乃偃武修文,归马于戈壁之阳,放牛于桃林之野,示天下弗服.”
卧槽泥马:形容识人不明.表示明明其能力不足.但上位者因为种种原因或糊涂.任其肆意妄为.
⑵形容虚有其表,窃居名位者.表示即使给某人相应的地位.但其能力不足是无法改变的.(等同于烂泥扶不上墙.沐猴而冠)
⑶形容模仿不到家,反而不伦不类.
卧槽泥马
出自《战国策·楚策四》
伯乐多良马.其有邻亚犁.曾与人言.“我亦善识马.有一骏马.伯乐不及.”人皆疑.欲观之.亚犁恐.乃以草泥置一卧马于槽中.众人视之笑其蠢.皆曰:“此何良驹.卧槽泥马尔.”
中国语言博大精深,楼主给分1年前查看全部
- 95%乙醇怎么稀释我刚打的耳洞,买了瓶酒精想消消炎,可是买回来的是95%的,怎么能把它稀释成75%的,一共有五百毫升~
 lisiyi331年前2
lisiyi331年前2 -
 minmin2333 共回答了17个问题
minmin2333 共回答了17个问题 |采纳率88.2%加水稀释
500ml*95%=(V+500)*75%
V=133.33ML
加1/4酒精体积的水.1年前查看全部
- 医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程
医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:
已知:查阅资料得知氢氧化物沉淀时的pH为:
(1)CaCO3与盐酸反应的离子方程式______.氢氧化物 Fe(OH)3 Al(OH)3 开始沉淀时的pH 2.3 4.0 开始溶解:7.8 完全沉淀时的pH 3.7 5.2 完全溶解:10.8
(2)除杂操作是加入氢氧化钙,调节溶液的pH为______,目的是除去溶液中少量的Al3+、Fe3+.检验Fe(OH)3是否沉淀完全的实验操作是______.
(3)过滤时需用的玻璃仪器有______.滤渣主要成分的化学式______.
(4)酸化时加盐酸的目的为:①______,②防止Ca2+在蒸发时发生水解.
(5)为什么蒸发结晶要保持在160℃:______.
(6)若所测样品 CaCl2•2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为______.
 BaBaSky1年前1
BaBaSky1年前1 -
 李美雯 共回答了16个问题
李美雯 共回答了16个问题 |采纳率100%解题思路:工业碳酸钙加入盐酸可完全溶解生成氯化钙、氯化铁以及氯化铝等,加入氢氧化钙溶液调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+,然后在酸性条件下蒸发结晶可得到CaCl2•2H2O,
(1)碳酸钙可以和盐酸发生反应生成氯化钙、水以及二氧化碳;
(2)根据铁离子完全沉淀、铝离子完全沉淀、氢氧化铝开始溶解的pH判断需要体积的pH范围;Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液;
(3)加入氢氧化钙生成氢氧化铝、氢氧化铁沉淀,过滤需要烧杯、玻璃棒和普通漏斗;
(4)加入过量盐酸,可中和氢氧化钙以及防止Ca2+在蒸发时发生水解;
(5)从溶液中得到晶体,加热温度不能过高,防止晶体分解;
(6)样品中存在少量的NaCl,根据 n(AgCl)2n(CaCl2.2H2O)可知,CaCl2.2H2O的物质的量增大.同样若CaCl2.2H2O失水导致分母变小,值偏大.(1)碳酸钙可以和盐酸发生反应生成氯化钙、水以及二氧化碳,反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O,
故答案为:CaCO3+2H+═Ca2++CO2↑+H2O;
(2)根据表中数据可知,氢氧化铁完全沉淀的pH为3.7,氢氧化铝开始沉淀的pH为5.2,氢氧化铝开始溶解的pH为7.8,所以将铁离子、铝离子完全转化成沉淀的pH范围为:5.2~7.8;
Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液,操作为取少量上层清液于小试管中,滴加KSCN溶液,若不显红色,则Fe(OH)3沉淀完全,
故答案为:5.2~7.8(或之间的任意值);取少量上层清液于小试管中,滴加KSCN溶液,若不显红色,则Fe(OH)3沉淀完全;
(3)过滤时需用的玻璃仪器有烧杯、玻璃棒和普通漏斗;加入氢氧化钙生成氢氧化铝、氢氧化铁沉淀,所以滤渣的主要成分为:Fe(OH)3、Al(OH)3,
故答案为:烧杯、玻璃棒、普通漏斗;Fe(OH)3、Al(OH)3;
(4)因除去铁离子、铝离子需加入过量的氢氧化钙,加入盐酸,可中和氢氧化钙以及防止Ca2+在蒸发时发生水解,
故答案为:除去过量的氢氧化钙;
(5)从溶液中得到晶体,加热温度不能过高,防止因温度太高CaCl2•2H2O会失水,
故答案为:温度太高CaCl2•2H2O会失水;
(6)品中存在少量的NaCl,对氯化钙晶体加热使之失去结晶水操作中,干燥温度过高时CaCl2•2H2O 晶体失去部分结晶水,会给实验带来误差,
故答案为:样品中存在少量的NaCl或干燥温度过高时CaCl2•2H2O晶体失去部分结晶水.点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题主要考查实验的基本操作、实验仪器的选择、实验误差分析等知识,为高频考点,侧重于学生的分析、实验和计算能力的考查,注意离子的检验方法和常见仪器的使用,样品纯度的分析要注意溶液中可能发生的反应,难度中等.1年前查看全部
- 英语翻译蓝莓因具有独特风味及营养保健功能,如抗氧化防衰老、改善记忆和视力、消炎抗菌、治疗心血管疾病等,被联合国粮农组织列
英语翻译
蓝莓因具有独特风味及营养保健功能,如抗氧化防衰老、改善记忆和视力、消炎抗菌、治疗心血管疾病等,被联合国粮农组织列为人类五大健康食品之一【1】.
目前对于蓝莓中生物活性物质的研究主要围绕花色苷类物质,关于蓝莓中多糖的研究还较少.本文拟采用微波技术对蓝莓中的多糖进行提取,确定最佳工艺条件,以为后续研究奠定基础.
微波辅助提取技术,无论是提取速度、提取效率还是提取品质,均比常规工艺优秀得多【2】.本实验在传统溶剂提取法的基础上,利用微波提取技术,对多糖提取工艺条件进行优化,筛选出一套较为成熟的微波辅助提取工艺路线.
利用微波辅助技术进行蓝莓多糖提取,通过考察微波功率、微波处理时间、料液比的工艺条件对提取蓝莓多糖的影响,确定单因素实验的因素与水平,通过实验选出最优的3因素3水平,分别为400w、500w、600w,5min、6min、7min,1:15、1:20、1:25.在此基础上,采用正交法建立对微波提取时间、料液比和微波功率等因素优化组合,确定微波提取蓝莓多糖的最佳工艺参数为600W、1/25、5min. 梅子咸1年前1
梅子咸1年前1 -
 gxp6880 共回答了17个问题
gxp6880 共回答了17个问题 |采纳率94.1%Blueberry has a unique flavor and nutrition for health functions,such as resistance to oxidation aging,improve memory and vision,inflammation,cardiovascular disease,by the United Nations FAO as one of the human five healthy foods 【1】.
At present,for blueberry research in bioactive substances mainly around the anthocyanin,blueberry Polysaccharides on is still less.This paper uses microwave technology to the blueberries in the polysaccharides were extracted to determine the optimal conditions that lay the foundation for future research.
Microwave-assisted extraction,extraction speed either,extraction or the extraction efficiency of quality,excellent technology is much more than conventional 【2】.The experiment in the traditional solvent extraction method based on microwave extraction technology,to optimize the extraction conditions of polysaccharide,selected a more mature line of microwave-assisted extraction.
Microwave-assisted technology blueberry polysaccharides,by investigating the microwave power,treatment time,solid to liquid ratio of processing conditions on polysaccharide of blueberry extract to determine the single factor experiment factors and levels,selecting the best of the three experiments factors and 3 levels,respectively,400w,500w,600w,5min,6min,7min,1:15,1:20,1:25.On this basis,the establishment of the microwave method using orthogonal extraction time,solid to liquid ratio and microwave power were optimized to determine the optimum microwave extraction process of polysaccharide blueberry parameters 600W,1 / 25,5min.1年前查看全部
- 医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯
医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2•2H2O的质量分数为97.0%-103.0%)的主要流程如下:
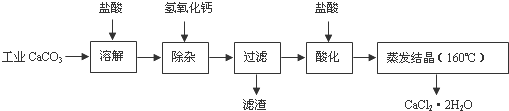
(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0-8.5,以除去溶液中的少量Al3+、Fe3+.检验Fe(OH)3是否沉淀完全的试验操作是______.
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①______
______;②______.
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05000mol•L-1 AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL.
①计算上述样品中CaCl2•2H2O的质量分数为______.
②若用上述办法测定的样品中CaCl2•2H2O的质量分数有时超过100.0%(测定过程中产生的误差可忽略),其可能原因有______. 兰心远1年前1
兰心远1年前1 -
 chsq00 共回答了16个问题
chsq00 共回答了16个问题 |采纳率87.5%解题思路:(1)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液;
(2)因在除杂过程中加入了Ca(OH)2,故加入盐酸与溶液中的少量Ca(OH)2反应使其转化为CaCl2;另Ca(OH)2易吸收空气中的CO2,生成CaCO3沉淀,故加入盐酸还可以防止溶液吸收空气中CO2,Ca(OH)2吸收空气中的CO2,生成CaCO3沉淀,如果吸收大量的CO2 会导致最终质量分数偏低;
(3)①根据到达滴定终点生成氯化银的物质的量等于消耗的硝酸银的物质的量这一关系求出消耗硝酸银的物质的量,则n(AgCl)=2n(CaCl2.2H2O),
据此可以算出实际上的CaCl2.2H2O的物质的量,进而求出质量.注意的是我们是从250mol中取25ml,所以在计算时要注意这一点;
②样品中存在少量的NaCl,根据 n(AgCl)2n(CaCl2.2H2O)可知,CaCl2.2H2O的物质的量增大.同样若CaCl2.2H2O失水导致分母变小,值偏大.(1)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在的,选用KSCN溶液,
故答案为:取少量上层清液,滴加KSCN溶液,若不出现血红色,则表明Fe(OH)3 沉淀完全;
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2; ②防止Ca2+在蒸发时水解;③防止溶液吸收空气中CO2,
故答案为:将溶液中的少量Ca(OH)2转化为CaCl2;防止Ca2+在蒸发时水解;防止溶液吸收空气中CO2;
(3)①样品中n(Cl-)=0.05000mol•L-1×0.02039L×10=0.010195mol,根据n(AgCl)=2n(CaCl2.2H2O),则n(CaCl2.2H2O)=0.0050975mol,所以m(CaCl2.2H2O)=0.0050975mol×147g/mol=0.7493325g,则有:[0.7493225g/0.7500g]×100%=99.9%,
故答案为:99.9%;
②样品中存在少量的NaCl会导致CaCl2.2H2O的物质的量增大.同样若CaCl2.2H2O失水导致分母变小,值偏大,
故答案为:样品中存在少量的NaCl或少量的CaCl2.2H2O失水.点评:
本题考点: 探究物质的组成或测量物质的含量.
考点点评: 本题考查混合物中含量的测定,涉及实验的基本操作、实验仪器的选择、实验误差分析、混合物分离及含量测定的计算等,注意离子的检验方法和常见仪器的使用,样品纯度的分析要注意溶液中可能发生的反应,注意有效数字问题,题目综合性较强,难度中等.1年前查看全部
大家在问
- 1世界有多大?地球的面积有多大?撒旦
- 2地球的海洋面积为多少?谢谢了,大神帮忙啊
- 3如何测一卷铁丝的质量
- 4在调整水费的听证会上,一位代表提出以下方案:“每月用水在5吨以下(包括5吨),按每吨1.2元收费;用水超出5吨;但不超出
- 5死海里有没有生物?
- 6在山雨这篇文章中,奇妙无比的琴键是指什么,轻捷柔软的手指是指什么.优雅的小曲实际是指什么.在这里,
- 7要载重量相同的运油车将一罐油运走,如装满8车,罐内还剩总数的7分之6,如装满9车后,罐内还剩112吨,原来这罐油多少吨?
- 8用细线把小石块拴好,使其浸没在天平的左盘上的烧杯内的水中,小石块不接触杯底,为什么天平的示数会增大
- 9这里选项A和B怎么区分?_____the beautiful gift,Alice let out an excited
- 10用涣然冰释,不虞之誉,安之若素一起造一个句子.希望精彩一点谢谢!
- 11为什么农业上可以用NaCl来选种
- 12求不虞之誉的近义词及近义词的解释.
- 13深圳市是个严重缺水的城市,为了保护环境,充分利用水资源,经过深圳市“调整水费听证会”讨论后决定,从2004年8月1日起居
- 14为了保护环境,充分利用水资源,某市经过“调整水费听证会”讨论后决定:水费由过去的每立方米0.8元调整为
- 15甲乙两个裁缝共同时加工1800套服装.如果甲单独做,8天就可以完成.如果乙单独做,需10天可以完成.如果要两人同时完工,