崇明县2010学年第一学期教学质量调研测试卷答案
 皮皮7875612022-10-04 11:39:541条回答
皮皮7875612022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 82kou 共回答了18个问题
82kou 共回答了18个问题 |采纳率100%- 崇明 2010学年 初二
在“百度文库”中键入以上三个关键词,即可搜索到.第一个文档就是. - 1年前
相关推荐
- (2012•崇明县二模)化学符号及含义正确的是( )
(2012•崇明县二模)化学符号及含义正确的是( )
A.铵根:NH3
B.2个氮原子:2N2
C.胆矾:CuSO4•5H2O
D.氧化钡:Ba2O 醉花吟月1年前1
醉花吟月1年前1 -
 城市美容师 共回答了17个问题
城市美容师 共回答了17个问题 |采纳率88.2%解题思路:化学式表示的宏观意义有:一种物质;这种物质是由哪些元素组成;微观意义有:一个分子;一个分子由哪些原子构成;原子的个数比等.一个铵根离子是由一个氮原子和四个氢原子构成的,并且一个铵根离子带一个单位的正电荷,2个氮原子:2N;胆矾是硫酸铜晶体,即硫酸铜带5个结晶水;氧化钡中氧元素是-2价,钡元素是+2价,因此化学式为BaO.A、一个铵根离子是由一个氮原子和四个氢原子构成的,并且一个铵根离子带一个单位的正电荷,故选项错误;
B、2个氮原子:2N,故选项错误;
C、胆矾是硫酸铜晶体,即硫酸铜带5个结晶水,故选项正确;
D、氧化钡中氧元素是-2价,钡元素是+2价,因此化学式为BaO,故选项错误;
故选:C.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本考点考查了化学符号表示的意义,化学式书写的一般规律是:正前负后,然后利用十字交叉法.根据在化合物中,正负化合价的代数和为零的原则,得出物质的化学式.本考点主要出现在选择题和填空题中.1年前查看全部
- (2013•崇明县二模)若抛物线y2=2px(p>0)的焦点与双曲线x2-y2=2的右焦点重合,则p的值为______.
 苏莫1年前1
苏莫1年前1 -
 想不通了1 共回答了15个问题
想不通了1 共回答了15个问题 |采纳率93.3%解题思路:将双曲线化成标准方程,求得a2=b2=2的值,从而得到双曲线的右焦点为F(2,0),该点也是抛物线的焦点,可得[p/2]=2,所以p的值为4.∵双曲线x2-y2=2的标准形式为:
x2
2−
y2
2=1
∴a2=b2=2,可得c=
a2+b2=2,双曲线的右焦点为F(2,0)
∵抛物线y2=2px(p>0)的焦点与双曲线x2-y2=2的右焦点重合,
∴[p/2]=2,可得p=4
故答案为:4点评:
本题考点: 双曲线的简单性质;抛物线的简单性质.
考点点评: 本题给出抛物线与双曲线右焦点重合,求抛物线的焦参数的值,着重考查了双曲线的标准方程和抛物线简单几何性质等知识点,属于基础题.1年前查看全部
- (2012•崇明县一模)回答下列有关植物光合作用和呼吸作用及其生命活动调节的问题.
(2012•崇明县一模)回答下列有关植物光合作用和呼吸作用及其生命活动调节的问题.

实验一:探究单株番茄光合作用强度与种植密度的关系,结果如甲图所示.
(1)与M点相比,N点限制单株光合作用强度的外界因素是______、______.实验还发现,不仅单株番茄光合作用强度与种植密度成负相关,番茄植株的生长也与种植密度成负相关.
(2)番茄生长的调节方式是______,与番茄果实发育关系最密切的调节物质是______,环境温度降低时,该物质运输速度会______.
实验二:测量种植番茄的密闭大棚内一昼夜空气中的CO2含量变化,结果如乙图所示.
(3)图中表示番茄光合作用和呼吸作用强度相等的点是______.B→C段曲线变化的原因是______,
若在B点突然停止光照,叶绿体内ADP含量将______;C3含量将______.
实验三:采用“半叶法”对番茄叶片的光合作用强度进行测定,其原理是:将对称叶片的一部分(A)遮光,另一部分(B)不做处理,并采用适当的方法阻止两部分的物质和能量转移.在适宜光照下照射6小时后,在A、B的对应部位截取相等面积的叶片,烘干称重,分别记为MA、MB,获得相应数据,则可计算出该叶片的光合作用强度,其单位是mg/(dm2•h)(实验步骤如图丙).(4)研究小组对记录的多组实验数据进行了统计分析,取______值进行计算,得出了M值.若M=MB-MA.则M表示______. 卜商1年前1
卜商1年前1 -
 古灵精怪23 共回答了14个问题
古灵精怪23 共回答了14个问题 |采纳率92.9%解题思路:主要考查你对光合作用的过程,呼吸作用的理解.探究:环境因素对光合作用强度的影响、生长素的生理作用等考点的理解.本题Ⅰ考查了有关光合作用和呼吸作用相关的知识.对于对于光合作用的影响因素主要是光照强度、CO2浓度、温度、水分和矿质元素等.通过甲图可以看出影响其与M点相比,N点限制单株光合作用强度的外界因素只有光照强度和CO2浓度,而不可能是温度和水分及矿质元素.本题Ⅱ中有关基因工程和胚胎工程的综合问题.(1)在相同的条件下,只有种群密度的不同,随着种群密度的增大,植物相互遮光,透气性不好,所以影响因素为:光照强度和CO2浓度.
(2)植物体没有神经系统,只能通过激素调节对自身的生命活动进行调节.生长素促进果实生长发育,在植物体通过极性运输.极性运输是细胞的主动运输.主动运输需要能量和载体蛋白的协助.环境温度降低时,植物体的新陈代谢降低产生能量较少.生长素运输速度会减慢.
(3)对于实验二中B→C时间段,是随着光照强度的增强,光合速率逐渐增加,所以含量应该降低.光合速率与呼吸速率相等点是乙图中的拐点,也就是B、D两点.B点突然停止光照,光反应停止,叶绿体内ADP不能合成ATP,则ADP的量增加,ATP量减少.无ATP生成,就不能为三碳化合物的还原过程供能,但二氧化碳的固定依然正常进行,则三碳化合物量有所增加.
(4)对于实验三中测定的数值,MA表示呼吸速率,MB表示净光合速率是,题干中的假定实验选定的叶片数目为3,所以要测定这三个叶片中的数值求其平均值,而M=MB-MA表示是净光合速率与呼吸速率之和,所以是真正光合速率.
故答案为:
(1)光照强度 CO2浓度
(2)激素调节 生长素
(3)BD光合作用强度大于呼吸作用强度,植物大量吸收CO2增加增加
(4)平均值B叶片被截取部分在6小时内光合作用合成的有机物总量点评:
本题考点: 影响光合作用速率的环境因素;细胞呼吸的过程和意义.
考点点评: 主要考查你对光合作用的过程,呼吸作用的理解.意在考查考生能运用所学知识与观点,通过比较、分析与综合等方法对某些生物学问题进行解释、推理,做出合理的判断或得出正确的结论的能力;识图能力和具备验证简单生物学事实的能力,并能对实验现象和结果进行解释、分析和处理的能力.1年前查看全部
- (2009•崇明县模拟)如图所示,水平固定的汽缸封闭了体积为V=2×10-3m3的理想气体,已知外面的大气压为p0=1×
 (2009•崇明县模拟)如图所示,水平固定的汽缸封闭了体积为V=2×10-3m3的理想气体,已知外面的大气压为p0=1×105Pa,活塞的横截面积为S=1×10-2m2,活塞质量和摩擦忽略不计.最初整个装置处于静止状态.现用手托住质量为m=5Kg的重物,使其缓慢升高到绳刚要松弛,(g=10m/s2)求:
(2009•崇明县模拟)如图所示,水平固定的汽缸封闭了体积为V=2×10-3m3的理想气体,已知外面的大气压为p0=1×105Pa,活塞的横截面积为S=1×10-2m2,活塞质量和摩擦忽略不计.最初整个装置处于静止状态.现用手托住质量为m=5Kg的重物,使其缓慢升高到绳刚要松弛,(g=10m/s2)求:
(1)重物需要升高多少高度?
(2)如果从绳子松弛时开始释放m,当m下落到最低点时,m共下降了H=1.6×10-2m高度,求这一过程中汽缸内气体作了多少功?
(3)重物到达最低点时的加速度a的大小和方向(设在整个过程中气体温度保持不变). 不能寻短见1年前1
不能寻短见1年前1 -
 mimu0223 共回答了19个问题
mimu0223 共回答了19个问题 |采纳率94.7%解题思路:(1)重物缓慢升高的过程中,气缸内封闭气体发生等温变化,先对活塞研究,由力平衡知识求出原来气缸内气体的压强,当绳刚松弛时,气缸内气体的压强等于大气压,再由玻意耳定律列式,求出绳刚要松弛时气缸内气体的体积,由体积变化与活塞的横截面积即可求重物上升的高度.
(2)对活塞和重物整体研究,有大气压、重力和气缸内气体压力三个力做功,动能变化量为零,根据动能定理列式即可求出汽缸内气体作功.
(3)根据重物下降的高度,得到重物到达最低点时气体的体积,由玻意耳定律列式,求出气体的压强,即可由牛顿第二定律重物到达最低点时的加速度a.(1)初态:p1=p0−
mg
S=0.95×105pa,v1=2×10−3m3
末态:p2=1×105pa,
由玻意耳定律得:p1V1=p2V2
则得 v2=
p1v1
p2=1.9×10−3m3
重物升高的高度 h=
v1−v2
S=0.01m
(2)对活塞和重物整体,根据动能定理得:
W-p0SH+mgH=0
解得,汽缸内气体作功 W=15.2J
(3)重物到达最低点时气体的体积 v3=v2+SH=2.06×10−3m3
则有 p3=
p1v1
v3=0.92×105pa
活塞质量不计,则对重物和活塞,根据牛顿第二定律得:(p0-p3)S-mg=ma
解得,a=6m/s2 方向向上
答:
(1)重物需要升高0.01m.
(2)汽缸内气体作了15.2J的功.
(3)重物到达最低点时的加速度a的大小为6m/s2,方向向上.点评:
本题考点: 封闭气体压强;理想气体的状态方程.
考点点评: 本题是玻意耳定律和力学知识的综合,要注意题中条件:活塞质量不计,运用整体法求加速度.1年前查看全部
- (2008•崇明县一模)设数列{an}的前n项和为Sn,已知a1=a(a≠3),Sn+1=2Sn+3n,n∈N*.
(2008•崇明县一模)设数列{an}的前n项和为Sn,已知a1=a(a≠3),Sn+1=2Sn+3n,n∈N*.
(1)设bn=Sn-3n,n∈N*,证明数列{bn}为等比数列;
(2)求数列{an}的通项公式;
(3)若an+1≥an,n∈N*,求a的取值范围. 緈緮豬豬1年前1
緈緮豬豬1年前1 -
 娃哈哈c921 共回答了15个问题
娃哈哈c921 共回答了15个问题 |采纳率86.7%解题思路:(1)由已知中Sn+1=2Sn+3n,bn=Sn-3n,n∈N*,我们可以得到
为定值2,根据等比数列的定义,即可得到数列{bn}为等比数列;bn+1 bn
(2)由(1)中结论,我们易求出数列{bn}的通项公式,进而得到Sn的表达式,进而根据an=Sn-Sn-1,n≥2,可以求出数列{an}的通项公式;
(3)根据数列an+1≥an,n∈N*,我们可(2)中数列{an}的通项公式,构造出一个关于a的不等式组,解不等式组,即可得到a的取值范围.(1)当a≠3时,
bn+1
bn
Sn+1−3n+1
Sn−3n=
2Sn+3n−3n+1
Sn−3n=2
所以{bn}为等比数列. (4分)
(2)b1=S1-3=a-3,(1分)bn=(a-3)×2n-1. (2分)
所以Sn-3n=(a-3)×2n-1(3分)an=Sn-Sn-1,n≥2,n∈N*an=
a
2×3n−1+(a−3)×2n−2,
n=1
n≥2;(6分)
(3)an+1≥an,
a2>a1
an+1>an,
n>2,(2分)
a≥-9(5分)
所以a≥-9,且a≠3. &点评:
本题考点: 等比关系的确定;数列的函数特性;数列递推式.
考点点评: 本题考查的知识点是等比关系的确定,数列的函数特征,数列递推式,其中(1)的关键是根据等比数列的定义,证得bn+1bn为定值,但要注意由限制首项不为0,(2)的关键是根据an=Sn-Sn-1,n≥2求通项,要注意对n=1时的判断;(3)的关键是根据(2)的结论,构造关于a的不等式组,同样要注意a1<a21年前查看全部
- (2011•崇明县二模)某实验报告记录了如下数据,其中数据合理的是( )
(2011•崇明县二模)某实验报告记录了如下数据,其中数据合理的是( )
A.用pH试纸测得氯水的pH为2.1
B.用50mL量筒量取23.00mL浓盐酸
C.用温度计测量出酒精的沸点为78.5℃
D.用托盘天平称量氧化铜粉末为11.70g 成吉思汗2221年前1
成吉思汗2221年前1 -
 雾雨迷朦 共回答了20个问题
雾雨迷朦 共回答了20个问题 |采纳率75%解题思路:A、氯水会把pH试纸漂泊,所以测氯水的pH不可以用pH试纸,并且数据不合理;
B、从量筒的精确度考虑,量筒只能精确到0.1;
C、温度计精确到0.1;
D、托盘天平只能精确到0.1.A、氯水会把pH试纸漂泊,所以测氯水的pH不可以用pH试纸,并且PH试纸精确到整数,数据也不合理,故A错误;
B、量筒只能精确到0.1,不能用50mL量筒量取23.00mL浓盐酸,故B错误;
C、温度计精确到0.1,并且酒精的沸点较低,数据合理,故C正确;
D、托盘天平只能精确到0.1,用托盘天平称量氧化铜粉末为11.70g,数据不合理,故D错误.
故选C.点评:
本题考点: 计量仪器及使用方法;试纸的使用.
考点点评: 本题考查常用计量仪器的精确度问题,题目难度不大,本题易错点为A项.1年前查看全部
- (2013•崇明县二模)不等式[1/x−x<0成立的充分不必要条件是( )
(2013•崇明县二模)不等式[1/x−x<0
 ID被杀1年前1
ID被杀1年前1 -
 郁美净专卖店 共回答了28个问题
郁美净专卖店 共回答了28个问题 |采纳率85.7%解题思路:先求出不等式的解集,即使不等式成立的充要条件,使其成立的充分不必要条件x的取值集合应为A的真子集.不等式
1
x−x<0可以化为
1−x2
x<0,等价于下面的两个不等式组:
1−x2>0
x<0]①或
1−x2<0
x>0②
解得
−1<x<1
x<0①或
x<−1或x>1
x>0②
∴-1<x<0,或x>1.
∴不等式
1
x−x<0的解集为A={x|-1<x<0,或x>1}.
使其成立的充分不必要条件x的取值集合应为A的真子集.
只有D符合.
故选D.点评:
本题考点: 其他不等式的解法;必要条件、充分条件与充要条件的判断.
考点点评: 本题考查了充要条件的判定,关键是分式不等式的解法.本题先考察命题p与命题q所表示的范围,再根据“谁大谁必要,谁小谁充分”的原则,判断出了命题p与命题q的关系.1年前查看全部
- 求一些2013年崇明县七年级期末测试卷语文的题目:可能出到的课外古文、作文题目、课内阅读和课外阅读.
求一些2013年崇明县七年级期末测试卷语文的题目:可能出到的课外古文、作文题目、课内阅读和课外阅读.
阅读的最好要有答案!谢谢
 ilikehome1年前1
ilikehome1年前1 -
 一剑渡江 共回答了12个问题
一剑渡江 共回答了12个问题 |采纳率100%作文题目1 爱(母爱 父爱 同学爱 陌生爱……)2 未来(写给xx年后的自己 写给2xxx的xxx……)3 理想(我的理想……)4 季节(走过四季 四季的美好……)5 假期(_____的假期……)6 议论 (对______发表看法……)7 ...1年前查看全部
- (2013•崇明县二模)如图所示,一对平行光滑轨道放置在水平面上,两轨道间距L=0.20m,电阻R=8Ω,有一电阻r=2
 (2013•崇明县二模)如图所示,一对平行光滑轨道放置在水平面上,两轨道间距L=0.20m,电阻R=8Ω,有一电阻r=2Ω,质量m=1kg的金属棒ab垂直平放在轨道上,轨道电阻可忽略不计,整个装置处于垂直轨道平面向下的匀强磁场中,磁感应强度B=5T,现用一外力F沿轨道方向拉金属棒,使之做初速为零的匀加速直线运动,加速度a=1m/s2.试求:
(2013•崇明县二模)如图所示,一对平行光滑轨道放置在水平面上,两轨道间距L=0.20m,电阻R=8Ω,有一电阻r=2Ω,质量m=1kg的金属棒ab垂直平放在轨道上,轨道电阻可忽略不计,整个装置处于垂直轨道平面向下的匀强磁场中,磁感应强度B=5T,现用一外力F沿轨道方向拉金属棒,使之做初速为零的匀加速直线运动,加速度a=1m/s2.试求:
(1)2s内通过电阻R的电量Q大小;
(2)外力F与时间t的关系;
(3)求当t=5s时电阻R上的电功率PR和F的功率PF的大小,并用能量守恒的观点说明两者为何不相等? 动物学aa1年前1
动物学aa1年前1 -
 goooon 共回答了19个问题
goooon 共回答了19个问题 |采纳率100%解题思路:(1)金属棒做初速为零的匀加速直线运动,由运动学公式位移求出2s通过的位移,由Q=I△t、I=[E/R+r]、E=[△Φ/△t]结合求解电量Q;
(2)推导出安培力的表达式,根据牛顿第二定律得到外力F与时间t的关系式;
(3)当t=5s时,求出感应电流,即可求出电阻R上的电功率PR,PF=Fv.分析能量如何转化来解释:外力F的功率转化为用于导体棒动能增加的机械功率和电阻上的发热功率,而发热功率还包括电阻R上的功率和导体棒电阻r的功率,所以有PR<PF.(1)t=2s时,金属棒通过的位移为 x=[1/2at2=2m
回路磁通量的变化量为△Φ=BxL=2Wb
感应电流为 I=
BLv
(r+R)]
则电量 Q=I△t=
△φ
R+r
代入解得 Q=0.2C
(2)安培力表达式为FA=BIL=B[BLv/R+r]L=
B2L2at
R+r
代入解得,FA=
B2L2at
(r+R)=0.1t
根据牛顿第二定律得 F-FA=ma
则得F=1+0.1t
(3)当t=5s时,I=
BLat
(R+r)=0.5A,
则PR=I2R=2W,
因F=1.5N,v=at=5m/s,则PF=Fv=7.5W.
外力F的功率转化为用于导体棒动能增加的机械功率和电阻上的发热功率,而发热功率还包括电阻R上的功率和导体棒电阻r的功率,所以有PR<PF.
答:(1)2s内通过电阻R的电量Q大小是0.2C;
(2)外力F与时间t的关系是F=1+0.1t;
(3)当t=5s时电阻R上的电功率PR是2W,F的功率PF的大小是7.5W,外力F的功率转化为用于导体棒动能增加的机械功率和电阻上的发热功率,而发热功率还包括电阻R上的功率和导体棒电阻r的功率,所以有PR<PF.点评:
本题考点: 导体切割磁感线时的感应电动势;闭合电路的欧姆定律;电功、电功率;电磁感应中的能量转化.
考点点评: 本题中用到两个经验公式:一是感应电荷量公式q=[△Φ/R+r];二是安培力公式FA=B2L2vR+r.对于能量问题,关键要分析能量有几种形式,把握能量是如何转化的.1年前查看全部
- (2011•崇明县二模)如图所示为______发现质子的实验装置.M是显微镜,S是荧光屏,窗口F处装有银箔,气体可从阀门
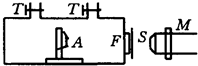 (2011•崇明县二模)如图所示为______发现质子的实验装置.M是显微镜,S是荧光屏,窗口F处装有银箔,气体可从阀门T充入,A是放射源.下列说法中正确的是
(2011•崇明县二模)如图所示为______发现质子的实验装置.M是显微镜,S是荧光屏,窗口F处装有银箔,气体可从阀门T充入,A是放射源.下列说法中正确的是
(A)放射源A放出的是α粒子
(B)充入氮气前,调整银箔厚度,使S上能见到质子引起的闪烁
(C)充入纯净的氧气后,会在S上见到质子引起的闪烁
(D)该实验的核反应方程为:24He+714N→816O+11H. 帅到头发不乱1年前1
帅到头发不乱1年前1 -
 vbgfrty 共回答了17个问题
vbgfrty 共回答了17个问题 |采纳率88.2%解题思路:明确卢瑟福发现质子的实验装置以及各部分的作用,注意F处装的银箔刚好能阻止α粒子穿过,而不能阻止其它粒子如质子穿过.卢瑟福通过用α粒子轰击氮核发现了质子;
装置中A为放射源,放出的为α粒子,由于F处装的银箔刚好能阻止α粒子穿过,因此没有充入氮气之前无质子产生,不可能在S上见到质子引起的闪烁,故AB错误;
充入氮气后,α粒子轰击氮核产生质子,质子穿过银箔,引起荧光屏S的闪烁,故C正确;
根据质量数和电荷数守恒可知D正确.
故选CD.
故答案为:卢瑟福,CD.点评:
本题考点: 原子核的人工转变.
考点点评: 卢瑟福用α粒子轰击氮核发现质子并实现原子核人工转变在近代物理上有着重要意义,要了解这一事件.1年前查看全部
- (2011•崇明县一模)重力为9牛的物体A静止在水平地面上,用力的图示法在右图中画出地面受到的压力.
 青铜时代XP1年前1
青铜时代XP1年前1 -
 greenboard 共回答了22个问题
greenboard 共回答了22个问题 |采纳率100%1年前查看全部
- (2014•崇明县二模)下列实验过程中,始终无明显现象的是( )
(2014•崇明县二模)下列实验过程中,始终无明显现象的是( )
A.Cl2通入Na2CO3溶液中
B.CO2通入CaCl2溶液中
C.NH3通入AgNO3溶液中
D.SO2通入Ba(NO3)2溶液中 hamlet197811221年前1
hamlet197811221年前1 -
 阿依朵朵娜 共回答了20个问题
阿依朵朵娜 共回答了20个问题 |采纳率80%解题思路:根据物质的性质来分析发生的化学反应,若化学反应中有气体、沉淀、颜色变化等明显现象,则不符合该题的题意.A、Cl2通入Na2CO3溶液中,Cl2和水反应生成盐酸和次氯酸,盐酸与Na2CO3反应产生二氧化碳气体,现象明显,故A错误;
B、因CO2和CaCl2不反应,无明显现象,故B正确;
C、NH3通入溶液中转化为氨水,与AgNO3反应生成氢氧化银沉淀,现象明显,故C错误;
D、SO2通入酸化的硝酸钡中,硝酸根离子在酸性条件下具有氧化性,则亚硫酸根离子被氧化为硫酸根离子,该反应生成硫酸钡沉淀,现象明显,故D错误;
故选:B.点评:
本题考点: 二氧化硫的化学性质;氯气的化学性质;氨的化学性质.
考点点评: 本题考查常见的化学反应及反应的现象,熟悉常见元素化合物知识即可解答;解答此题的易错点是:不能正确理解CO2和CaCl2能否反应,由于盐酸是强酸,碳酸是弱酸,故将CO2通入CaCl2溶液中时,因碳酸钙沉淀能溶于盐酸则CO2和CaCl2不反应.1年前查看全部
- (2010•崇明县二模)如图是一对夫妇和几个子女的简化DNA指纹,据此图判断,下列选项正确的是 ( )
(2010•崇明县二模)如图是一对夫妇和几个子女的简化DNA指纹,据此图判断,下列选项正确的是 ( )
①基因Ⅰ和基因Ⅱ肯定在同一对染色体上基因标记 母亲 父亲 女儿1 女儿2 儿子 Ⅰ - - - Ⅱ - - Ⅲ - - - Ⅳ - - Ⅴ - -
②基因Ⅳ与基因Ⅱ可能位于同一条染色体上
③基因Ⅲ可能位于X染色体上
④基因Ⅴ可能位于Y染色体上.
A.①②
B.①③
C.②④
D.②③ vampirezy1年前1
vampirezy1年前1 -
 亵神 共回答了15个问题
亵神 共回答了15个问题 |采纳率80%解题思路:分析表中信息,只有基因Ⅱ和基因Ⅳ的遗传情况一致,说明只有基因Ⅱ与基因Ⅳ最可能位于同一条染色体上.父亲的基因Ⅲ遗传给了女儿,没有遗传给儿子,则基因Ⅲ很有可能位于X染色体上.父亲的基因Ⅴ遗传给了女儿,说明基因Ⅴ不可能位于Y染色体上.①由表中信息可知,基因I和Ⅱ均存在于母亲体内,后代中有且只有这两个基因中的一个,所以基因I和Ⅱ最可能位于一对同源染色体上,但不能肯定在同一对染色体上,①错误;
②基因Ⅳ和Ⅱ的遗传情况是一样的,同时出现,所以基因Ⅳ和Ⅱ最可能位于一条染色体上,②正确;
③基因Ⅲ的遗传特点是父亲传给了两个女儿,没有传给儿子,所以最可能位于X染色体上,③正确;
④如果基因V位于Y染色体上,那么遗传特点是父亲只能传给儿子,但女儿1也有此基因,所以基因Ⅴ不可能位于Y染色体上,④错误.
所以正确的有②③.
故选:D.点评:
本题考点: 伴性遗传.
考点点评: 本题考查基因的遗传特点,意在考查考生能运用所学知识与观点,通过比较、分析与综合等方法对某些生物学问题进行解释、推理,做出合理的判断或得出正确的结论的能力.1年前查看全部
- (2014•崇明县二模)取自同种生物的不同类型的正常细胞,检测其基因表达,结果如图.关于此图说法不正确的是( )
(2014•崇明县二模)取自同种生物的不同类型的正常细胞,检测其基因表达,结果如图.关于此图说法不正确的是( )
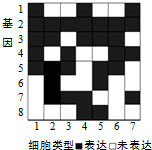
A.若基因1~8中只有一个是控制核糖体蛋白质合成的基因,则该基因最有可能是基因2
B.图中7种细胞的遗传物质一定相同,mRNA一定完全不同
C.图中8种基因的不同主要表现在组成这些基因的脱氧核苷酸的排列顺序不同
D.此图可用于说明基因的选择性表达 apapapap1年前1
apapapap1年前1 -
 echolinyan 共回答了14个问题
echolinyan 共回答了14个问题 |采纳率92.9%解题思路:据图分析,7种不同细胞表达的基因不同,说明细胞分化的本质,即基因的选择性表达;7种细胞中基因2都表达,而每个活细胞中都有核糖体,因此基因2是控制核糖体蛋白质合成的基因或呼吸酶基因.A、蛋白质是生命活动的承担者,合成场所是核糖体,而2基因在每种细胞中都表达,所以控制核糖体蛋白质合成的基因最有可能是基因2,A正确;
B、细胞分化的实质是基因的选择性表达,使得不同细胞RNA不完全相同,但管家基因,如呼吸酶基因等每个细胞都表达,B错误;
C、图中8种基因的不同主要表现在基因的脱氧核苷酸的排列顺序不同,C正确;
D、此图可用于说明基因的选择性表达,使得不同细胞表达的基因不完全相同,D正确.
故选:B.点评:
本题考点: 细胞的分化;基因、蛋白质与性状的关系.
考点点评: 本题考查基因表达和细胞分化的相关知识,意在考查考生获取图文信息和分析问题的能力,解答该题的关键是识图.1年前查看全部
- (2014•崇明县二模)如果⊙O1与⊙O2相交于点A、B,⊙O1的半径是5,点O1到AB的距离为3,那么⊙O2的半径r的
(2014•崇明县二模)如果⊙O1与⊙O2相交于点A、B,⊙O1的半径是5,点O1到AB的距离为3,那么⊙O2的半径r的取值范围是______.
 惠心意1年前0
惠心意1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•崇明县一模)人类的生产、生活都离不开水.兴趣课上同学们分组研究水的净化及组成(装置如图).
(2013•崇明县一模)人类的生产、生活都离不开水.兴趣课上同学们分组研究水的净化及组成(装置如图).

(1)一组同学用自制简易净水器(图②所示)净化河水,其中活性炭的作用是______.
(2)实验③中通电一段时间后,试管b中的气体是______(填写化学式),反应的化学方程式为2H2O
2H2↑+O2↑通电 .2H2O.
2H2↑+O2↑通电 .
(3)从微观角度分析,实验①和③两个变化中最本质的区别是______.
(4)2mol水中约有______个水分子. west52111年前1
west52111年前1 -
 相逢一笑百媚生 共回答了25个问题
相逢一笑百媚生 共回答了25个问题 |采纳率76%解题思路:(1)根据活性炭有吸附性分析活性炭的作用;
(2)根据通电分解水实验的现象和结论分析;
(3)根据分子在物理变化和化学变化中的变化分析;
(4)根据阿伏伽德罗常数进行计算.(1)由于活性炭有吸附性,在简易净水器中活性炭的作用是吸附作用;
(2)由电解水的装置图可知,试管b中的气体是电源的正极上产生的气体,是O2,通电分解水生成了氢气和氧气,反应的化学方程式是:2H2O
通电
.
2H2↑+O2↑;
(3)在实验①中是水的蒸发,水分子没有变化,只是分子的间隔变大了,在实验③中是水的分解,水分子发生了变为氢分子和氧分子;
(4)由阿伏伽德罗常数可知,2mol水中约有的水分子数约是:6.02×1023mol-1×2mol=1.204×1024.
故答为:(1)吸附作用;(2)O2,2H2O
通电
.
2H2↑+O2↑;(3)①中只是水分子的间隙变大,③中水分子变为氢分子和氧分子(4)1.204×1024.点评:
本题考点: 水的净化;电解水实验;利用分子与原子的性质分析和解决问题.
考点点评: 本题难度不是很大,综合性较强,考查了水的净化、电解水的实验、分子在物理变化和化学变化中的变化实质等,灵活运用所学知识是正确解题的关键.1年前查看全部
- (2014•崇明县二模)美国普度大学的研究人员开发出一种利用铝镓合金制备氢气的新工艺(如图所示). 下列有关该
 (2014•崇明县二模)美国普度大学的研究人员开发出一种利用铝镓合金制备氢气的新工艺(如图所示). 下列有关该工艺的说法错误的是( )
(2014•崇明县二模)美国普度大学的研究人员开发出一种利用铝镓合金制备氢气的新工艺(如图所示). 下列有关该工艺的说法错误的是( )
A.能量的转化形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金与水反应的化学方程式为:2Al+3H2O
Al2O3+3H2↑一定条件 .
D.总反应式为:2H2O
H2↑+O2↑一定条件 . ohmylord1年前1
ohmylord1年前1 -
 会唱歌的叶子 共回答了21个问题
会唱歌的叶子 共回答了21个问题 |采纳率85.7%解题思路:A、太阳能转化为电能、电能转化为化学能、化学能转变为热能.
B、开始的反应物中和最终的生成物中含有的物质就可循环使用.
C、铝镓合金与水的反应实际上是铝和水的反应.
D、根据每一步的反应方程式得出总反应方程式.A、该工艺中能量的转化形式有:太阳能转化为电能、电能转化为化学能、电能转化为热能,所以有三种形式的能量转化,故错误.
B、开始的反应物是铝镓合金,最终的生成物是铝镓合金,所以铝镓合金能循环使用,故正确.
C、铝镓合金与水的反应中生成物是氧化铝、氢气和镓,相当于镓未参加反应,所以实际上发生的反应是2Al+3H2O
一定条件
.
Al2O3+3H2↑,故正确.
D、该工艺中发生的反应有:2Al+3H2O
一定条件
.
Al2O3+3H2↑①,2Al2O3
电解
.
4Al+3O2②,将方程式①×12+②得方程式2H2O
一定条件
.
H2↑+O2↑,故D正确.
故选A.点评:
本题考点: 制备实验方案的设计;常见的能量转化形式.
考点点评: 本题考查了工艺中的信息给予题,难度不大,易错选项是A,注意电解过程中部分电能转化为热能,所以能量转化有三种形式.1年前查看全部
- (2011•崇明县一模)有关碳单质及其氧化物的说法中错误的是( )
(2011•崇明县一模)有关碳单质及其氧化物的说法中错误的是( )
A.燃着的木条可区分CO和CO2
B.金刚石、石墨、C60互称为碳的同素异形体
C.二氧化碳和一氧化碳在一定条件下可以相互转化
D.碳具有可燃性,因此在常温下其化学性质比较活泼 深南20041年前1
深南20041年前1 -
 hwy8345 共回答了12个问题
hwy8345 共回答了12个问题 |采纳率100%解题思路:A、根据一氧化碳和二氧化碳的性质分析;
B、金刚石和石墨C60互称为碳的同素异形体;
C、根据一氧化碳和二氧化碳的化学性质分析;
D、根据碳的化学性质分析.A、二氧化碳能使燃着的木条熄灭,一氧化碳能被燃着的木条点燃,说法正确;
B、同素异形体是由相同的元素组成的不同单质,说法正确;
C、一氧化碳燃烧能生成二氧化碳,二氧化碳与碳在高温下反应生成一氧化碳,说法正确;
D、碳常温下化学性质稳定,错误.
故选D.点评:
本题考点: 二氧化碳的化学性质;一氧化碳的化学性质;碳的化学性质;碳元素组成的单质.
考点点评: 本题考查知识比较全面,可根据碳单质及其氧化物的性质进行判断.1年前查看全部
- (2011•崇明县一模)下列离子方程式正确的是( )
(2011•崇明县一模)下列离子方程式正确的是( )
A.向氯化亚铁溶液中通入氯气:Fe2++Cl2→Fe3++2Cl-
B.用氢氧化钠溶液吸收少量二氧化碳:2OH-+CO2→CO32-+H2O
C.向碳酸氢钙溶液中加入足量的氢氧化钠溶液:Ca2++HCO3-+OH-→CaCO3↓+H2O
D.向过量的氨水中滴入少量氯化铝溶液:Al3++4NH3.H2O→AlO2-+4NH4++2H2O gigiyiyi1年前1
gigiyiyi1年前1 -
 凌波翩翩 共回答了15个问题
凌波翩翩 共回答了15个问题 |采纳率93.3%解题思路:A.电荷不守恒;
B.反应生成碳酸钠和水;
C.碳酸氢钙完全反应,生成碳酸钙、碳酸钠、水;
D.反应生成氢氧化铝和氯化铵.A.向氯化亚铁溶液中通入氯气的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故A错误;
B.用氢氧化钠溶液吸收少量二氧化碳的离子反应为2OH-+CO2═CO32-+H2O,故B正确;
C.向碳酸氢钙溶液中加入足量的氢氧化钠溶液的离子反应为Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故C错误;
D.向过量的氨水中滴入少量氯化铝溶液的离子反应为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故D错误;
故选B.点评:
本题考点: 离子方程式的书写.
考点点评: 本题考查离子反应方程式的书写,明确发生的反应是解答本题的关键,注意与量有关的离子反应中量少的完全反应,题目难度不大.1年前查看全部
- (2009•崇明县一模)如图所示,两个完全相同的圆柱形容器内分别盛有质量相同的水和酒精.现将两块密度相同的木块分别放入两
 (2009•崇明县一模)如图所示,两个完全相同的圆柱形容器内分别盛有质量相同的水和酒精.现将两块密度相同的木块分别放入两个圆柱形容器内,(已知ρ水>ρ酒精>ρ木)使水和酒精对容器底部压强相等,放进水里的木块体积为V甲,放进酒精里的木块体积为V乙,则其大小关系是( )
(2009•崇明县一模)如图所示,两个完全相同的圆柱形容器内分别盛有质量相同的水和酒精.现将两块密度相同的木块分别放入两个圆柱形容器内,(已知ρ水>ρ酒精>ρ木)使水和酒精对容器底部压强相等,放进水里的木块体积为V甲,放进酒精里的木块体积为V乙,则其大小关系是( )
A.V甲>V乙
B.V甲=V乙
C.V甲<V乙
D.以上都有可能 李女兆1年前1
李女兆1年前1 -
 lxw760319 共回答了22个问题
lxw760319 共回答了22个问题 |采纳率81.8%解题思路:甲、乙为相同的圆柱形容器,液体对容器底的压力等于液体重,因为原来盛有质量相同的水和酒精,所以原来两容器底受到的压强相等;
将两木块浸入后,水和酒精对容器底部的压强相等,可见增加的压强相等,因为水的密度大于酒精的密度,由液体压强公式可得液面升高值的关系,进而得出排开液体的体积关系.∵甲、乙为圆柱形容器,
∴液体对容器底的压力等于液体重,
∵原来盛有质量相同的水和酒精,
∴原来两容器底受到的压力相等,
∵p=[F/S],两容器相同、底面积S相同,
∴原来两容器底受到的压强相等;
∵将两木块浸入后,水和酒精对容器底部的压强相等,
∴增加的压强△p甲=△p乙,
∵p=ρgh,
∴ρ水g△h水=ρ酒精g△h酒精,
两木块所受的浮力关系ρ水gS△h水=ρ酒精gS△h酒精,
所以两木块的重力相等,质量相等,
也就是说体积相等.
故选B.点评:
本题考点: 液体的压强的计算.
考点点评: 本题考查了学生对压强公式、液体压强公式的掌握和运用,知道对于圆柱形容器液体对容器底的压力等于液体重是本题的关键.1年前查看全部
- (2011•崇明县二模)将2.8克Fe在一定量稀硝酸中恰好完全溶解后,往溶液中滴加NaOH 溶液立即产生沉淀,
(2011•崇明县二模)将2.8克Fe在一定量稀硝酸中恰好完全溶解后,往溶液中滴加NaOH 溶液立即产生沉淀,滴加至沉淀量最大时,再将所得溶液和沉淀一起加热蒸干,并在空气中灼烧至恒重,所得固体成分和可能的质量为( )
A.FeO3.6gNaNO312.75g
B.Fe2O34gNaNO26.9g
C.Fe3O43.87gNaNO310.25g
D.Fe2O34gNaNO29.8g 剁粉条1年前1
剁粉条1年前1 -
 张大伦 共回答了16个问题
张大伦 共回答了16个问题 |采纳率81.3%解题思路:根据2.8gFe与稀硝酸反应可能生成硝酸亚铁或硝酸铁两种情况计算,2.8gFe的物质的量为[2.8g/56g/mol]=0.05mol,加入氢氧化钠后蒸干,得到0.05mol氢氧化铁(氢氧化亚铁会被空气氧化)和0.1mol硝酸钠,或硝酸钠0.15mol,最后得到0.025mol氧化铁和0.1mol硝酸钠或0.15mol亚硝酸钠,可分别计算出亚硝酸钠的质量范围.如果2.8gFe的物质的量为[2.8g/56g/mol]=0.05mol铁全部恰好生成硝酸亚铁,
则硝酸亚铁物质的量为0.05mol,加入氢氧化钠后蒸干,
得到0.05mol氢氧化铁(氢氧化亚铁会被空气氧化)和0.1mol硝酸钠,
根据元素质量守恒可得加热生成0.025mol氧化铁和0.1mol亚硝酸钠,
质量是:氧化铁0.025mol×160g/mol=4g,亚硝酸钠0.1mol×69g/mol=6.9g
如果恰好生成硝酸铁0.05mol,则氧化铁依然是0.025mol,硝酸钠是0.15mol,
灼烧有氧化铁4g,根据Na元素守恒可得亚硝酸钠0.15mol,质量为0.15mol×69g/mol=10.35g
所以氧化铁质量肯定是4g,亚硝酸钠质量应该在[6.9,10.35]区间内.
故选BD.点评:
本题考点: 有关混合物反应的计算;铁的化学性质;铁的氧化物和氢氧化物.
考点点评: 本题考查混合物的计算,题目难度较大,注意本题考虑2.8gFe与稀硝酸反应可能生成硝酸亚铁或硝酸铁两种情况计算,利用端值法求解.1年前查看全部
- (2013•崇明县二模)下列有关实验操作中,正确的是( )
(2013•崇明县二模)下列有关实验操作中,正确的是( )
A.测定溶液的pH时,将试纸直接放入待测液中
B.固体药品都可以直接放在天平的托盘上称量
C.在未说明用量时,一般液体取1-2毫升左右,固体盖满试管底部
D.用燃着的酒精灯去点燃其他的酒精灯 cy02671年前1
cy02671年前1 -
 海岱青人 共回答了19个问题
海岱青人 共回答了19个问题 |采纳率94.7%解题思路:A、正确的测定溶液pH的方法是用玻璃棒蘸取待测液,将其滴在pH试纸上;
B、托盘天平的使用过程中,若称量具有腐蚀性的药品时,一定要放在玻璃器皿上;
C、在未说明用量时,一般液体取1-2毫升左右,固体盖满试管底部;
D、点燃酒精灯应用火柴,不能用燃着的酒精灯去点燃其它的酒精灯.A、把pH试纸直接浸入待测液中来测定溶液的pH,会污染原试剂,故错误;
B、托盘天平的使用过程中,若称量具有腐蚀性的药品时,一定要放在玻璃器皿上,例如氢氧化钠,故错误;
C、为节约药品,在未说明用量时,一般液体取1-2毫升左右,固体盖满试管底部,故正确;
D、点燃酒精灯应用火柴,不能用燃着的酒精灯去点燃其它的酒精灯,以防着火,故错误.
故选C.点评:
本题考点: 溶液的酸碱度测定;称量器-托盘天平;加热器皿-酒精灯;液体药品的取用.
考点点评: 本题主要考查实验仪器及基本实验操作等相关内容,了解酒精灯、托盘天平的使用,了解溶液的酸碱度测定的方法及其注意书写是解题关键.1年前查看全部
- (2005•崇明县模拟)A.夏季的雷雨天气,云团带电使云团间形成电场,在一次闪电中,两云团间的平均电场强度为2.0×10
(2005•崇明县模拟)A.夏季的雷雨天气,云团带电使云团间形成电场,在一次闪电中,两云团间的平均电场强度为2.0×106N/C,两云团间的距离为500m,则两云团间的电势差为______V,若从一块云团移到另一云团的电量为30C,那么在这次闪电中释放的电势能约为______ J.
 onlyjbr1年前1
onlyjbr1年前1 -
 萍-聚 共回答了14个问题
萍-聚 共回答了14个问题 |采纳率100%由题意可知两云团之间为匀强电场,符合公式U=Ed适用条件,所以U=Ed=2×106×500=1.0×109V,释放能量为:W=qU=1.0×109×30=3.0×1010J.
故答案为:1.0×109,3.0×1010.1年前查看全部
- (2007•崇明县二模)世界卫生组织把铝列为食品污染源之一,指出每人每日铝的摄入量应控制在4毫克下.某饮食店用1000克
(2007•崇明县二模)世界卫生组织把铝列为食品污染源之一,指出每人每日铝的摄入量应控制在4毫克下.某饮食店用1000克面粉、4克明矾[明矾的化学式为KAl(SO4)2•12H2O]、适量的小苏打、食盐、水等辅料,做成油条24根,平均每根约50克.请问答以下问题:
(1)在酸、碱、盐三种物质类别中,明矾属于______;
(2)明矾中铝的质量百分含量为5.7%,那么4克明矾中含铝______克;
(3)假设在烹炸过程中铝元素不损失,那么每根油条中约含铝元素______克;如果我们每天食用这种油条一根,是否超过世界卫生组织提出的安全摄入量______(填是或否);
(4)请你再列举一种日常生活中铝进入人体的途径:______. 575295301年前1
575295301年前1 -
 相信自己相信你 共回答了17个问题
相信自己相信你 共回答了17个问题 |采纳率94.1%解题思路:根据已有的知识进行分析,盐是指由金属离子和酸根离子组成的化合物,根据物质的化学式可以进行有关的计算.(1)明矾中含有铝离钾离子和硫酸根离子,由金属离子和酸根离子组成,属于盐类物质,故填:盐;
(2)4克明矾中含铝的质量为:4g×5.7%=0.228g,故填:0.228;
(3)每根油条中铝元素的质量为:0.228g÷24=0.0095g,0.0095g=9.5mg>4mg,超标,故填:0.0095,是;
(4)日常生活中铝进入人体的途径有使用铝制炊具烧饭做菜等,故填:用铝锅煮饭烧菜.点评:
本题考点: 常见的氧化物、酸、碱和盐的判别;化合物中某元素的质量计算.
考点点评: 本题考查了化学与人体健康的知识以及物质种类的判断和有关的计算,完成此题,可以依据已有的知识进行.1年前查看全部
- (2014•崇明县二模)为方便黑夜开灯,家中可安装一种带有指示灯的开关,如图(a)所示.这种开关是由一个指示灯和一个电键
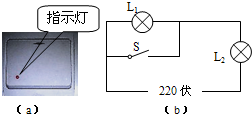 (2014•崇明县二模)为方便黑夜开灯,家中可安装一种带有指示灯的开关,如图(a)所示.这种开关是由一个指示灯和一个电键S构成.将该开关和照明灯连入电路,如图(b)所示.请根据以下工作特点,对有关电路元件进行判断.
(2014•崇明县二模)为方便黑夜开灯,家中可安装一种带有指示灯的开关,如图(a)所示.这种开关是由一个指示灯和一个电键S构成.将该开关和照明灯连入电路,如图(b)所示.请根据以下工作特点,对有关电路元件进行判断.
①当电键S闭合时,电路中的照明灯正常发光、指示灯不发光,则图(b)电路中的灯L1是______(选填“照明灯”或“指示灯”).
②当电键S断开时,电路中的照明灯不发光,指示灯正常发光,说明此时指示灯的电阻______照明灯的电阻(选填“大于”、“等于”或“小于”).
③照明灯的额定功率______指示灯的额定功率(选填“大于”、“等于”或“小于”). Lihao23115601年前1
Lihao23115601年前1 -
 6133340 共回答了24个问题
6133340 共回答了24个问题 |采纳率87.5%解题思路:①当电键S闭合时,L1被短路,电路为L2的基本电路,据此分析L1的类别;
②根据P=I2R进行分析;
③灯泡的实际功率决定了灯泡的明暗,根据指示灯和灯泡正常发光的亮度进行比较即可.①根据电路图可知,电键S闭合时,L1被短路,电路为L2的基本电路,并且照明灯正常发光、指示灯不发光,所以L1是指示灯;
②当电键S断开时,电路中的照明灯不发光,指示灯正常发光,说明指示灯的实际功率大,由P=I2R可知,指示灯的电阻大于照明灯泡的电阻;
③因为照明灯正常发光的亮度远远大于指示灯正常发光的亮度,因此照明灯的额定功率大于指示灯的额定功率.
故答案为:①指示灯;②大于;③大于.点评:
本题考点: 电路的基本连接方式.
考点点评: 本题考查电路的基本连接方式以及功率计算公式的应用,知道实际功率决定了灯泡的明暗.1年前查看全部
- (2013•崇明县二模)已知:Fe5O7可以看作Fe2O3和Fe3O4的混合物.现有Fe、Fe2O3、Fe5O7混合物共
(2013•崇明县二模)已知:Fe5O7可以看作Fe2O3和Fe3O4的混合物.现有Fe、Fe2O3、Fe5O7混合物共0.1mol,加盐酸后固体全部溶解,共收集到0.01mol H2,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为( )
A.0.05 mol
B.0.06 mol
C.0.07 mol
D.0.08 mol 9505131年前1
9505131年前1 -
 千秋孤寂 共回答了25个问题
千秋孤寂 共回答了25个问题 |采纳率92%解题思路:加盐酸后固体全部溶解,共收集到0.01mol H2,得到与盐酸反应生成氢气的铁物质的量为0.01mol;反应后的溶液中加入KSCN溶液不显红色说明不含铁离子,溶液中全部为亚铁离子,依据极值法计算判断.铁和盐酸反应Fe+2HCl=FeCl2+H2↑,生成0.01mol氢气消耗铁物质的量为0.01mol;反应后的溶液中加入KSCN溶液不显红色说明不含铁离子,溶液中全部为亚铁离子,铁和三价铁离子全部反应生成亚铁离子;
假设混合物0.1mol为Fe、Fe2O3的混合物;设原混合物铁物质的量为x,则Fe2O3的物质的量为(0.1-x)mol,Fe3+物质的量2(0.1-x)mol;
Fe+2Fe3+=3Fe2+;
12
(x-0.01)mol 2(0.1-x)mol
计算得到x=0.06mol;
假设混合物0.1mol为Fe、Fe5O7混合物,设原混合物中铁物质的量为y,则Fe5O7混物质的量为(0.1-y)mol,Fe5O7可以看作Fe2O3和Fe3O4的混合物,Fe3O4的可以看做Fe2O3和FeO组成,则Fe2O3的物质的量为2(0.1-y)mol,Fe3+物质的量4(0.1-x)mol;
Fe+2Fe3+=3Fe2+;
1 2
(x-0.01)mol 4(0.1-x)mol
计算得到x=0.07mol;
所以Fe、Fe2O3、Fe5O7混合物共0.1mol反应含有铁的物质的量为0.06<n(Fe)<0.07,在此范围的铁的物质的量符合;
故选B.点评:
本题考点: 铁的氧化物和氢氧化物;二价Fe离子和三价Fe离子的检验.
考点点评: 本题考查了铁及其化合物性质的综合应用和计算分析,极值法计算判断是解题关键,题目难度较大.1年前查看全部
- (2013•崇明县一模)在矩形ABCD中,AB=3BC,点E是DC的中点,那么cot∠CEB=[3/2][3/2].
 来一桶面1年前0
来一桶面1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2012•崇明县一模)已知数列{an}的前n项和为Sn,a1=3,且当n≥2,n∈N*时Sn-1是an与-3的等差中项
(2012•崇明县一模)已知数列{an}的前n项和为Sn,a1=3,且当n≥2,n∈N*时Sn-1是an与-3的等差中项,则数列{an}的通项an=______.
 婚前忧郁1年前1
婚前忧郁1年前1 -
 月光公公 共回答了10个问题
月光公公 共回答了10个问题 |采纳率90%解题思路:由当n≥2,n∈N*时Sn-1是an与-3的等差中项,知Sn-1=
,Sn=an−3 2
,两式相减得到an=an+1,由此能求出an.an+1−3 2 ∵当n≥2,n∈N*时Sn-1是an与-3的等差中项,
∴Sn-1=
an−3
2…①
Sn=
an+1−3
2…②
②-①得
3an=an+1,
∵a1=3,
∴数列{an}是首项为3,公比为3的等比数列,
∴an=3n.点评:
本题考点: 数列递推式;等差数列的性质.
考点点评: 本题考查数列的通项公式的应用,解题时要认真审题,仔细解答,注意迭代法的合理运用.1年前查看全部
- (2006•崇明县二模)一个质量为m带有电荷为-q的小物体,可在水平轨道OX上运动,O端有一与轨道垂直的固定墙.轨道处于
 (2006•崇明县二模)一个质量为m带有电荷为-q的小物体,可在水平轨道OX上运动,O端有一与轨道垂直的固定墙.轨道处于匀强电场中,场强大小为E,方向沿OX轴正方向如图所示,小物体以速度V0从图示位置向左运动,运动时受到大小不变的摩擦力f作用,设小物体与墙壁碰撞时不损失机械能,且电量保持不变,求它停止前所通过的总路程S.
(2006•崇明县二模)一个质量为m带有电荷为-q的小物体,可在水平轨道OX上运动,O端有一与轨道垂直的固定墙.轨道处于匀强电场中,场强大小为E,方向沿OX轴正方向如图所示,小物体以速度V0从图示位置向左运动,运动时受到大小不变的摩擦力f作用,设小物体与墙壁碰撞时不损失机械能,且电量保持不变,求它停止前所通过的总路程S.
解:根据动能定理可得:
qEs-fs=0-m
上述解法正确吗?若你认为是正确的话,则解出其结果,若你认为不正确的话,则列式解出你认为正确的结果.v02 2  从不放弃ii1年前1
从不放弃ii1年前1 -
 zhr25 共回答了19个问题
zhr25 共回答了19个问题 |采纳率94.7%解题思路:当电场力大于摩擦力,电荷最终停在墙角处,对全过程运用动能定理求出物体运动的路程.当电场力小于摩擦力,则滑块向左做减速运动,有可能未到墙壁处速度减为0,可能恰好到墙壁处速度为0,可能跟墙壁碰撞后反弹向右减速到0停在.根据这三种情况分别用动能定理求出物块运动的路程.不全面,要根据电场力与摩擦力大小来分情况讨论,
(1)当qE>f时,最终物体停在墙角处qE•x0-f•s=0-[1/2m
v20]
s=
qE•x0+
1
2m
v20
f
(2)讨论:qE<f
①在碰撞前停下,即f>qE+
m
v20
2x0 时 qE•s-f•s=0-[1/2m
v20]
s=
m
v20
2(qE+f)
②在墙壁处停下,即f=qE+
m
v20
2x0 时
s=x0
③在与墙壁碰撞后向右停下,即qE+
m
v20
2x0>f>qE时
qE(2x0-s)-fs=0-[1/2m
v20]
即s=
2qEx0+
1
2m
v20
qE+f.
答:它停止前所通过的总路程S可能为
qE•x0+
1
2m
v20
f、
m
v20
2(qE+f)、x0、
2qEx0+
1
2m
v20
qE+f.点评:
本题考点: 带电粒子在匀强电场中的运动.
考点点评: 本题通过对物块运动的全过程研究,运用动能定理求出物块运动的总路程,注意要讨论电场力与摩擦力的大小关系.1年前查看全部
- (2010•崇明县二模)同学们通过学习化学,可以知道:
(2010•崇明县二模)同学们通过学习化学,可以知道:
(1)石灰水中溶质的名称是氢氧化钙氢氧化钙;
(2)形成“温室效应”的主要气体是CO2CO2(用化学符号表示);
(3)1mol 水中约含1.806×1024(或3×6.02×1023)1.806×1024(或3×6.02×1023)_个原子;
(4)地壳中含量最多的金属元素的符号是AlAl;
(5)鱼类可在水中呼吸,是因为水中溶有一定量的O2O2(用化学符号表示);
(6)量取7.2mL 溶液,需要一种合适的玻璃仪器是10ml量筒10ml量筒. chg381年前1
chg381年前1 -
 dkwt 共回答了15个问题
dkwt 共回答了15个问题 |采纳率86.7%解题思路:(1)石灰水是生石灰或熟石灰溶于水制得的;(2)形成“温室效应”的主要气体是二氧化碳;(3)水是由大量的水分子构成,一个水分子由2个氢原子、1个氧原子构成;(4)地壳中含量前四位的元素名称为:氧、硅、铝、铁;(5)了解供给动物、植物呼吸的气体为氧气;(6)量取液体时,量筒大小应选用合适的规格,所选的量程稍微比所量取的液体大即可.(1)石灰水中溶质为Ca(OH)2,其名称是氢氧化钙;
(2)二氧化碳的化学式,可以根据其读法书写,故化学式为CO2;
(3)已知1个水分子由3个原子构成,1mol水中约含6.02×1023个水分子,故1mol水中约含1.806×1024(或3×6.02×1023)个原子;
(4)地壳中含量最多的金属元素为铝,它的化学符号是Al;
(5)鱼类可在水中呼吸,是因为水中溶有一定量的氧气,其化学式为O2;
(6)量取7.2mL 溶液,需要一种合适的玻璃仪器是10ml量筒.
故答为:(1)氢氧化钙;(2)CO2;(3)1.806×1024(或3×6.02×1023);(4)Al;(5)O2;(6)10ml量筒点评:
本题考点: 化学符号及其周围数字的意义;常用仪器的名称和选用;氧气的用途;二氧化碳对环境的影响.1年前查看全部
- (2013•崇明县二模)已知正方体ABCD-A1B1C1D1的棱长是3,点M、N分别是棱AB、AA1的中点,则异面直线M
(2013•崇明县二模)已知正方体ABCD-A1B1C1D1的棱长是3,点M、N分别是棱AB、AA1的中点,则异面直线MN与BC1所成的角是[π/3][π/3].
 mwl5061年前0
mwl5061年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (b他大他•崇明县一模)现有下列实验装置,请回答下列问题:
(崇明县一模)现有下列实验装置,请回答下列问题:

(大)仪器①名称是酒精灯酒精灯;
(b)实验室用氯酸钾和二氧化锰混合制Ob时该反应的化学方程式为bKClO手
bKCl+手Ob↑bKClO手MbOb . △
bKCl+手Ob↑,反应前后,二氧化锰在固体混合物中质量分数是变大变大(“不变”或“变大”或“变小”),若将生成的气体用向上排空气法收集,验满方法是用带火星的木条放在集气瓶7,木条复燃说明氧气已收集满.用带火星的木条放在集气瓶7,木条复燃说明氧气已收集满.;MbOb . △
(手)实验室用双氧水溶液与二氧化锰混合制Ob时,为了控制产生氧气的反应速率,应选的发生装置是CC(填字母),该反应的化学方程式为b0bOb
b0bO+Ob↑b0bObMbOb .
b0bO+Ob↑,基本反应类型是分解分解反应;MbOb .
(4)若用D装置进行碳还原氧化铜的实验,a处的实验现象为固体粉末由黑色变为红色,固体粉末由黑色变为红色,,发生反应的化学方程式是C+bCuO
bCu+COb↑,C+bCuO高温 .
bCu+COb↑,;要检验反应后的气体中含有COb,多处试剂的名称为澄清石灰水澄清石灰水;高温 .
(5)实验室用大理石和稀盐酸制COb时选用了装置E,实验一段时间后,关闭C处的活塞,观察到的现象是在气体的压力下,盐酸被压入球形漏斗内,大理石和盐酸脱离接触,反应停止在气体的压力下,盐酸被压入球形漏斗内,大理石和盐酸脱离接触,反应停止;若用如图 装置进行“排空气法”收集制取的COb,请把图中的“导气管”补画完整.
装置进行“排空气法”收集制取的COb,请把图中的“导气管”补画完整.  aa都该aa1年前1
aa都该aa1年前1 -
 zst9820 共回答了12个问题
zst9820 共回答了12个问题 |采纳率66.7%(1)仪器名称:酒精灯
(2)氯酸钾在二氧化锰和加热的条件下生成氯化钾和氧气,故化学方程式为:2KClO3
MkO2
.
△2KCl+3O2↑;;二氧化锰在反应前后质量不变,而反应后固体质量减少了,因此二氧化锰的质量分数变大了;检验氧气是否集满的方法是用带火星的木条放在集气瓶口,木条复燃说明氧气已收集满.
(3)要控制产生氧气的反应速率,需通过控制滴加双氧水的速度,因此需选择装置C;化学方程式为:2H2O2
MkO2
.
2H2O+O2↑反应物是一种,生成物是两种,因此是分解反应;
(4)碳还原氧化铜生成铜和二氧化碳,所以看到的现象为固体粉末由黑色变为红色;化学方程式为:C+2C少O
高温
.
2C少+CO2↑,检验二氧化碳用澄清的石灰水;
(5)用大理石和稀盐酸制CO2时选用了装置E,实验一段时间后,关闭C处的活塞时,在气体的压力下,盐酸被压入球形漏斗内,大理石和盐酸脱离接触,反应停止;二氧化碳密度比空气大,因此要用向下排空气法收集,因此需从长管进,将空气从短管排出.
故答案为: (1)酒精灯
(1)酒精灯
(2)2KClO3
MkO2
.
△2KCl+3O2↑变大 用带火星的木条放在集气瓶口,木条复燃说明氧气已收集满.
(3)C2H2O2
MkO2
.
2H2O+O2↑分解
(4)固体粉末由黑色变为红色,C+2C少O
高温
.
2C少+CO2↑,澄清石灰水(或石灰水)
(5)在气体的压力下,盐酸被压入球形漏斗内,大理石和盐酸脱离接触,反应停止;
[如得:导管“长进短出”.若把导气管画成线条不得分]1年前查看全部
- (2011•崇明县二模)在一定温度下,向一个容积不变的容器中,加入2mol N2和8mol H2及固
(2011•崇明县二模)在一定温度下,向一个容积不变的容器中,加入2mol N2和8mol H2及固体催化剂,使之反应,平衡时容器内气体压强为起始时的80%,该反应的热化学方程式为:N2(g)+3H2(g)→2NH3(g)+92kJ.下列叙述中正确的是( )
A.平衡时,NH3的体积分数为20%,放出的热量小于92.2kJ
B.平衡时,NH3的体积分数为25%,放出的热量等于92.2kJ
C.平衡时,NH3的物质的量为2mol,放出的热量大于92.2kJ
D.平衡时,NH3的物质的量为4mol,放出的热量等于184.4kJ 梦见你离开1年前1
梦见你离开1年前1 -
 try004 共回答了25个问题
try004 共回答了25个问题 |采纳率88%解题思路:利用三段式计算:
N2(g)+3H2(g) 2NH3(g)
2NH3(g)
起始:2mol 8mol 0
转化:x 3x 2x
平衡:2-x 8-3x 2x
根据压强之比等于物质的量之比,则有:(2-x+6-3x+2x)÷(2+8)=0.8,解之得x=1,以此计算转化率和反应放出的热量.利用三段式计算:
N2(g)+3H2(g) 2NH3(g)
2NH3(g)
起始:2mol 8mol 0
转化:x 3x 2x
平衡:2-x 8-3x 2x
根据压强之比等于物质的量之比,则有:(2-x+8-3x+2x)÷(2+8)=0.8,解之得x=1,
则NH3的物质的量为2mol,则NH3的体积分数为
2x
(2−x+8−3x+2x)× 100%=
2
8×100%=25%,
由热化学反应方程式可知此时反应的氮气为1mol,所以放出的热量等于92.2kJ,
故选B.点评:
本题考点: 化学平衡的计算;有关反应热的计算.
考点点评: 本题考查化学平衡和反应热的计算,题目难度不大,注意做题时利用三段式法计算,思路清晰、明朗.1年前查看全部
- 闵行区、崇明县初三英语第一学期期末质量抽查试卷
闵行区、崇明县初三英语第一学期期末质量抽查试卷
那位大哥 给个啊....今天晚上一定要...就是那个文化课强化训练里的...领先一步 2009版 今天hh不睡觉1年前1
今天hh不睡觉1年前1 -
 excellentone 共回答了26个问题
excellentone 共回答了26个问题 |采纳率88.5%给你几个建议:
1、英语是一门语言,绝对不能单靠努力背单词和语法来提高自己的成绩,这一点你是一定要先明白的.
2、英语包括听,说,读,写,考试主要是听和写,关于听力的练习,我建议你多听一些英语磁带,多于别人用英语交流(哪怕说的不好).
3、至于写的部分,我不知道你是哪里人,不过英语试卷不外乎就是单项选择,阅读理解,写作这几方面,我建议你多找这几方面的题目来做,我中考前每天狂做几百道单项选择,结果成绩提高了几十分(我们是150分制的).
4、你说“试卷一发下来觉得跟背的毫无联系”,个人认为会不会是你背的东西本身就错了呢?你上课有没有笔记?如果有一定要立足于笔记,如果没有,我建议你去买一些英语的参考书,里面都有归纳重要语法的.
5、实在不行的话,你也可以去请教你的同学或老师,他们应该会告诉你一些有用的方法的.
^o^1年前查看全部
- (2011•崇明县一模)下列各组物质,只用水作溶剂,就能鉴别的是( )
(2011•崇明县一模)下列各组物质,只用水作溶剂,就能鉴别的是( )
A.CCl4、C6H14、CH3CHO三种液体
B.MnO2、CuO、FeS 三种固体
C.NH4NO3、NaOH、NaCl 三种固体
D.BaSO4、NaHCO3、CaCO3 三种固体 五月JJ1年前1
五月JJ1年前1 -
 拿钱压ff你 共回答了20个问题
拿钱压ff你 共回答了20个问题 |采纳率90%解题思路:只用水就能鉴别,可利用物质的水溶性和密度大小的异同,如产生不同的现象,就可鉴别.A.CCl4和C6H14都不溶于水,但CCl4的密度比水大,C6H14的密度比水小,CH3CHO易溶于水,可鉴别,故A正确;
B.MnO2、CuO、FeS 三种固体都不溶于水,不能鉴别,故B错误;
C.NH4NO3溶于水吸热,NaOH溶于水放热,NaCl无明显现象,可鉴别,故C正确;
D.BaSO4、CaCO3可都不溶于水,不能鉴别,故D错误.
故选AC.点评:
本题考点: 物质的检验和鉴别的实验方案设计.
考点点评: 本题考查物质的鉴别,题目难度不大,注意把握物质的性质的异同,用水就能鉴别的物质往往从物质的水溶性和密度的角度考虑.1年前查看全部
- (2011•崇明县一模)如图,MOH和ROH两种一元碱的稀溶液,分别加水稀释时pH变化可近似看作下图,下列说法错误的是(
 (2011•崇明县一模)如图,MOH和ROH两种一元碱的稀溶液,分别加水稀释时pH变化可近似看作下图,下列说法错误的是( )
(2011•崇明县一模)如图,MOH和ROH两种一元碱的稀溶液,分别加水稀释时pH变化可近似看作下图,下列说法错误的是( )
A.ROH是一种强碱
B.在x点,c(M+)=c(R+)
C.在x点,ROH完全电离
D.稀释前,c(ROH)=10c(MOH) 来看就会1年前1
来看就会1年前1 -
 长天02 共回答了24个问题
长天02 共回答了24个问题 |采纳率70.8%解题思路:由图可知,ROH的pH=13时稀释100倍,pH变为11,则ROH为强碱;而MOH的pH=12时稀释100倍,pH变为11,则说明MOH为弱碱,以此来解答.A.由图可知,ROH的pH=13时稀释100倍,pH变为11,则ROH为强碱,故A正确;
B.在X点,pH相同,则c(OH-)相同,由电荷守恒可知,c(M+)=c(R+),故B正确;
C.ROH为强碱,则在x点,ROH完全电离,故C正确;
D.ROH为强碱,稀释前浓度为0.1mol/L,MOH的pH=12时稀释100倍,pH变为11,则说明MOH为弱碱,稀释前MOH的浓度大于0.01mol/L,则稀释前c(ROH)≠10c(MOH),故D错误;
故选D.点评:
本题考点: 弱电解质在水溶液中的电离平衡.
考点点评: 本题考查强碱、弱碱稀释及图象,明确图象中pH的变化是解答本题的关键,并注意利用pH与浓度的关系来解答.1年前查看全部
- (2007•崇明县二模)在使用过程中对环境不造成污染的能源常被称为绿色能源,请你写出二种绿色能源的名称:______、_
(2007•崇明县二模)在使用过程中对环境不造成污染的能源常被称为绿色能源,请你写出二种绿色能源的名称:______、______.
 香草味奶昔1年前1
香草味奶昔1年前1 -
 ruizhaojun 共回答了18个问题
ruizhaojun 共回答了18个问题 |采纳率94.4%解题思路:氢能、风能、太阳能的使用不产生或残留对环境造成污染的物质,属于绿色能源.氢能、风能、太阳能属于绿色能源,不污染环境;
故答案为:风能、太阳能.点评:
本题考点: 常见能源的种类、能源的分类.
考点点评: 解答本题要理解各种能源物质在使用过程中能够产生哪些物质,并且对这些物质的性质进行分析、判断,从而得出正确的结论.1年前查看全部
- (2011•崇明县模拟)据图分析回答有关“人体内环境与自稳态”问题:
(2011•崇明县模拟)据图分析回答有关“人体内环境与自稳态”问题:

Ⅰ、图1中①~⑤表示相应的生理过程,a~d表示相应的物质,A~C表示相应器官.
(1)图中字母B表示______
(2)人体体温恒定是机体代谢产热量与散热量保持动态平衡的结果.寒冷刺激后,图1中过程______的活动较其它过程更早增强,过程③产生的激素c即______会增加,促使人体代谢产热量增加.当体温升高时,通过反馈调节,激素______的分泌活动会受到抑制.
(3)重感冒发热患者通常会在服药后因大量出汗退热而使尿量减少.医生常常会建议患者主动地多饮水.请根据图1中信息以及所学知识加以解释.
①尿量减少的原因:______.
②主动饮水的作用是______.
Ⅱ、图2表示某些信息分子对靶细胞作用的方式.
(4)如果甲表示促甲状腺激素,乙表示该激素作用的靶细胞上相应的受体.那么当甲与乙结合时激酶激活细胞的特殊功能是______.人类有一种疾病是体内产生了大量促甲状
腺激素分子受体的抗体,该抗体可以结合乙而充当促甲状腺激素的作用,从而引起靶器官A(见图1)功能______.
Ⅲ、图3是一种血糖调控模式图.
(5)图3中A表示葡萄糖.当人体处于低血糖状态时,如果机体通过途径①→②→③使血糖水平恢复正常,其主要机理是______.当人体处于高血糖状态时,也可通过途径④→⑤使血糖水平恢复正常.写出此过程中脂肪细胞中的相关物质转化过程______.
Ⅳ、图4是脂蛋白结构示意图.
(6)写出相应字母名称W______Y______.脂蛋白在血脂代谢中起着重要作用.医生常常会通过血检报告中脂蛋白含量来判断血脂代谢紊乱疾病.与单纯性高胆固醇血症有关的脂蛋白异常情况可能是______. 2831507281年前1
2831507281年前1 -
 xuyan2754 共回答了23个问题
xuyan2754 共回答了23个问题 |采纳率87%解题思路:图1中a为促甲状腺激素释放激素,b为促甲状腺激素,c为甲状腺激素;A为甲状腺,B为肾脏;图2中甲为激素,乙为相应的受体;图3是一种血糖调控模式图;图4是脂蛋白结构示意图:X是磷脂,Y是甘油三酯,Z是蛋白质,W是胆固醇.(1)抗利尿激素作用于肾小管和集合管促进对水的重吸收,故B为肾脏.
(2)人体体温恒定是机体代谢产热量与散热量保持动态平衡的结果.寒冷刺激后,图1中过程①即下丘脑通过神经调节的活动较其它过程更早增强,过程③产生的激素c即甲状腺激素会增加,促使人体代谢产热量增加.当体温升高时,通过反馈调节,甲状腺激素会抑制下去脑和垂体分泌相应的激素,所以激素a、b的分泌活动会受到抑制.
(3)重感冒发热患者通常会在服药后因大量出汗退热而使尿量减少.医生常常会建议患者主动地多饮水.①尿量减少的原因:大量出汗导致血浆渗透压上升,引起下丘脑神经内分泌细胞大量合成分泌抗利尿激素;抗利尿激素可通过促进B中肾小管和集合管对水分的重吸收而使血浆渗透压下降,尿量减少.②主动饮水的作用是主动饮水,不仅有利于血浆渗透压下降,同时减少了对下丘脑渗透压感受器的刺激,使抗利尿激素分泌和释放量减少.
(4)促甲状腺激素作用于甲状腺,使甲状腺合成和分泌甲状腺激素;人类有一种疾病是体内产生了大量促甲状腺激素分子受体的抗体,该抗体可以结合乙而充当促甲状腺激素的作用,从而引起靶器官A甲状腺不断地分泌甲状腺激素,引起甲状腺功能亢进.
(5)当人体处于低血糖状态时,胰岛A细胞会分泌胰高血糖素,胰高血糖素分泌增多,促进了肝糖原分解成葡萄糖,使血糖水平升高.当人体处于高血糖状态时,胰岛B细胞会分泌胰岛素,是血糖浓度降低,此过程中脂肪细胞中的相关物质转化过程为葡萄糖→甘油、脂肪酸→甘油三酯.
(6)由图4可知W为胆固醇,Y为甘油三酯;与单纯性高胆固醇血症有关的脂蛋白异常情况可能是低密度脂蛋白过高或高密度脂蛋白过低.
故答案为:
(1)肾脏
(2)①甲状腺激素 a、b
(3)①大量出汗导致血浆渗透压上升,引起下丘脑神经内分泌细胞大量合成分泌抗利尿激素;抗利尿激素可通过促进B中肾小管和集合管对水分的重吸收而使血浆渗透压下降,尿量减少.②主动饮水,不仅有利于血浆渗透压下降,同时减少了对下丘脑渗透压感受器的刺激,使抗利尿激素分泌和释放量减少.
(4)合成和分泌甲状腺素(合成和分泌激素c) 亢进
(5)胰高血糖素分泌增多,促进了肝糖原分解成葡萄糖,使血糖水平升高.
葡萄糖→甘油、脂肪酸→甘油三酯
(6)胆固醇 甘油三酯 低密度脂蛋白过高或高密度脂蛋白过低点评:
本题考点: 神经、体液调节在维持稳态中的作用;体温调节、水盐调节、血糖调节.
考点点评: 本题考查了人体内环境稳态的调节机制中的水盐平衡调节,体温调节和血糖调节,意在考查考生理解所学的要点,把握知识间的内在联系的能力.1年前查看全部
- (2013•崇明县二模)二十世纪初,为了研究物质内部的结构,物理学家做了大量的实验,揭示了原子内部的结构.发现了电子、中
 (2013•崇明县二模)二十世纪初,为了研究物质内部的结构,物理学家做了大量的实验,揭示了原子内部的结构.发现了电子、中子和质子,通过如图的实验装置( )
(2013•崇明县二模)二十世纪初,为了研究物质内部的结构,物理学家做了大量的实验,揭示了原子内部的结构.发现了电子、中子和质子,通过如图的实验装置( )
A.卢瑟福发现质子
B.汤姆逊发现电子
C.查德威克发现中子
D.卢瑟福建立了原子的核式结构模型 youhot1年前1
youhot1年前1 -
 沉默之鹰 共回答了12个问题
沉默之鹰 共回答了12个问题 |采纳率91.7%解题思路:解答本题应抓住:该实验是卢瑟福和他的助手们做的α粒子散射实验,根据这个实验的结果,卢瑟福提出了原子的核式结构模型.本实验是α粒子散射实验,卢瑟福根据极少数α粒子产生大角度偏转,提出了原子的核式结构模型.故D正确.
故选D点评:
本题考点: 物理学史.
考点点评: 本实验是α粒子散射实验装置,是卢瑟福和他的助手们做的,是物理上著名的实验,要加强记忆.1年前查看全部
- (2009•崇明县模拟)用DIS位移传感器研究小车直线运动的实验中,得到了如图所示的一个S-t图象,A、B、C、D是图象
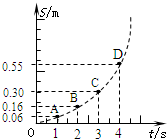 (2009•崇明县模拟)用DIS位移传感器研究小车直线运动的实验中,得到了如图所示的一个S-t图象,A、B、C、D是图象上的四个点,从图象中可以得出小车在AD区域内的位移是______m;在AC区域内平均速度为______m/s;从图象还能推断,小车在运动过程中所受的合外力方向与它的速度方向______(填“相同”、“相反”或“垂直”)
(2009•崇明县模拟)用DIS位移传感器研究小车直线运动的实验中,得到了如图所示的一个S-t图象,A、B、C、D是图象上的四个点,从图象中可以得出小车在AD区域内的位移是______m;在AC区域内平均速度为______m/s;从图象还能推断,小车在运动过程中所受的合外力方向与它的速度方向______(填“相同”、“相反”或“垂直”)  linian20001年前1
linian20001年前1 -
 applehero 共回答了18个问题
applehero 共回答了18个问题 |采纳率88.9%解题思路:根据S-t图象得AD区域内的位移.
根据
=[x/t]可知AC区域内平均速度..v 根据S-t图象得AD区域内的位移是0.49 m.
根据
.
v=[x/t]可知AC区域内平均速度
.
v=[x/t]=0.12 m/s
s-t图象的斜率等于物体的速度,从图象还能推断物体做加速运动,
所以小车在运动过程中所受的合外力方向与它的速度方向相同.
故答案为:0.490.12相同.点评:
本题考点: 探究小车速度随时间变化的规律.
考点点评: 本题是s-t图象的应用题,主要考查图象的斜率等于物体的速度,匀变速运动的x-t图象是抛物线.1年前查看全部
- (2009•崇明县一模)在图所示的电路中,电源电压保持不变.闭合电键S,当滑动变阻器的滑片P向左移动时,电压表V的示数将
 (2009•崇明县一模)在图所示的电路中,电源电压保持不变.闭合电键S,当滑动变阻器的滑片P向左移动时,电压表V的示数将______,电流表A与电流表A1示数的差值将______.(均选填“变大”、“不变”或“变小”)
(2009•崇明县一模)在图所示的电路中,电源电压保持不变.闭合电键S,当滑动变阻器的滑片P向左移动时,电压表V的示数将______,电流表A与电流表A1示数的差值将______.(均选填“变大”、“不变”或“变小”)  dorothyqian1年前1
dorothyqian1年前1 -
 frankyinshen 共回答了14个问题
frankyinshen 共回答了14个问题 |采纳率92.9%解题思路:分析电路知:
电阻R2与滑动变阻器R1并联,电压表测量电源电压.电流表A测量干路电流,电流表A1测量通过滑动变阻器的电流.因为电压表测量电源电压,所以无论滑动变阻器滑片怎样向左滑动,电压表的示数都不变;
在并联电路中干路电流等于支路电流之和,电流表A与A1示数的差值是通过定值电阻R2的电流,因为R2阻值不变,两端电压不变,由公式I=[U/R]知,通过的电流也不变.
故答案为:不变;不变.点评:
本题考点: 欧姆定律的应用;滑动变阻器的使用.
考点点评: 此题给我们的两个启示:①滑动变阻器必须与用电器串联才能起到改变用电器两端电压的作用,并联时对用电器没有影响--甚至造成电源短路;②只要在并联电路中,电压表示数都不变.1年前查看全部
- (2008•崇明县二模)在做“凸透镜成像规律”实验前,应首先观察并记下凸透镜的______.在调试实验装置时,应使凸透镜
(2008•崇明县二模)在做“凸透镜成像规律”实验前,应首先观察并记下凸透镜的______.在调试实验装置时,应使凸透镜和光屏的中心跟______的中心大致在______.
 cqslzhao1年前1
cqslzhao1年前1 -
 y5060921 共回答了22个问题
y5060921 共回答了22个问题 |采纳率100%解题思路:(1)实验前要观察并记录凸透镜的焦距,便于比较物距和焦距的关系,总结成像规律.
(2)探究凸透镜成像的实验时,在桌面上依次放蜡烛、凸透镜、光屏,三者在同一条直线上,三者的中心大致在同一高度,像才能成在光屏的中心.(1)实验前应该首先观察并记下凸透镜的焦距,可以方便描述物距与像距.
(2)在调试实验装置时,蜡烛、凸透镜、光屏,三者在同一条直线上,应使凸透镜和光屏的中心跟烛焰的中心大致在同一高度,像才能成在光屏的中心.
故答案为:焦距;烛焰;同一高度.点评:
本题考点: 凸透镜成像规律及其探究实验.
考点点评: 探究凸透镜成像的规律,要掌握此实验的器材,及实验过程中的实验要求.主要考查了实验中需要注意的一些问题.因此上课时,要一边做实验,一边强调应该注意的问题.1年前查看全部
- (2007•崇明县二模)对人类而言,氧气是一种普通而又极其重要的气体.自然界产生氧气的主要途径是______;工业上常用
(2007•崇明县二模)对人类而言,氧气是一种普通而又极其重要的气体.自然界产生氧气的主要途径是______;工业上常用______ 的方法制得氧气;在化学实验室我们制取氧气的方法是(用化学反应方程式表示)2KClO3
2KCl+3O2↑MnO2 .△ 2KClO3.
2KCl+3O2↑MnO2 .△  yzjordan1年前1
yzjordan1年前1 -
 RealSailer 共回答了12个问题
RealSailer 共回答了12个问题 |采纳率100%解题思路:绿色植物的光合作用能够产生大量的氧气;根据工业上制取氧气的原理上进行分析解答;实验室制氧气的方法有三种:分解过氧化氢溶液、加热氯酸钾、加热高锰酸钾,据此写出反应的化学方程式即可.绿色植物通过光合作用消耗二氧化碳生成氧气;工业上是利用液态氧和液态氮的沸点的不同,采用分离液态空气来制取氧气;
实验室制氧气的方法有:分解过氧化氢溶液、加热氯酸钾、加热高锰酸钾,如采用加热氯酸钾制取氧气,反应的化学方程式为:2KClO3
MnO2
.
△2KCl+3O2↑等.
故答案为:光合作用;分离液态空气;2KClO3
MnO2
.
△2KCl+3O2↑等.点评:
本题考点: 自然界中的氧循环;氧气的工业制法;实验室制取氧气的反应原理;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,掌握光合作用的原理、工业上制取氧气的原理、实验室制氧气的方法等是正确解答本题的关键.1年前查看全部
- (2013•崇明县一模)将抛物线y=(x+1)2向右平移2个单位,得到新抛物线的顶点坐标是______.
 enya04491年前1
enya04491年前1 -
 教主不是uu男 共回答了13个问题
教主不是uu男 共回答了13个问题 |采纳率100%解题思路:先根据顶点式得到y=(x+1)2的顶点坐标为(-1,0),然后把点(-1,0)向右平移2个单位即可得到平移后抛物线的顶点坐标.∵y=(x+1)2的顶点坐标为(-1,0),
∴抛物线y=(x+1)2向右平移2个单位后所得抛物线的顶点坐标为(1,0).
故答案为(1,0).点评:
本题考点: 二次函数图象与几何变换.
考点点评: 本题考查了二次函数的图象与几何变换:先把二次函数y=ax2+bx+c(a≠0)配成顶点式y=a(x-[b/2a])2+4ac−b24a,对称轴为直线x=-[b/2a],顶点坐标为(-[b/2a],4ac−b24a);然后把抛物线的平移问题转化为顶点的平移问题.1年前查看全部
- (2012•崇明县二模)下列对实验现象的描述,错误的是( )
(2012•崇明县二模)下列对实验现象的描述,错误的是( )
A.打开盛有浓盐酸的试剂瓶瓶盖,瓶口上方出现白雾
B.硫在空气中燃烧产生明亮的蓝紫色火焰
C.镁条在空气中剧烈燃烧,发出耀眼白光
D.氢氧化钠溶液滴入氯化铁溶液,出现红褐色沉淀 宁波慈城1年前1
宁波慈城1年前1 -
 lele9463 共回答了18个问题
lele9463 共回答了18个问题 |采纳率88.9%解题思路:A、根据浓盐酸的物理性质进行分析判断.
B、根据硫在空气中燃烧的现象进行分析判断.
C、根据镁条在空气中燃烧的现象进行分析判断.
D、根据碱的化学性质进行分析判断.A、浓盐酸具有挥发性,打开盛有浓盐酸的试剂瓶瓶盖,瓶口上方出现白雾,故选项说法正确.
B、硫在空气中燃烧,产生微弱的淡蓝色火焰,故选项说法错误.
C、镁条在空气中剧烈燃烧,发出耀眼的白光,故选项说法正确.
D、氢氧化钠与氯化铁反应生成氢氧化铁沉淀和氯化钠,则氢氧化钠溶液滴入氯化铁溶液,出现红褐色沉淀,故选项说法正确.
故选B.点评:
本题考点: 氧气与碳、磷、硫、铁等物质的反应现象;酸的物理性质及用途;碱的化学性质;盐的化学性质.
考点点评: 本题难度不大,掌握常见物质燃烧的现象、浓盐酸的物理性质、碱的化学性质即可正确解答.1年前查看全部
- (2013•崇明县一模)如图甲所示,绷紧的水平传送带始终以恒定速率v1运行.初速度大小为v2的小物块从与传送带等高的光滑
 (2013•崇明县一模)如图甲所示,绷紧的水平传送带始终以恒定速率v1运行.初速度大小为v2的小物块从与传送带等高的光滑水平面上的A处滑上传送带.若从小物块滑上传送带开始计时,小物块在传送带上运动的v-t图象(以地面为参考系)如图乙所示.已知v2>v1.则 ( )
(2013•崇明县一模)如图甲所示,绷紧的水平传送带始终以恒定速率v1运行.初速度大小为v2的小物块从与传送带等高的光滑水平面上的A处滑上传送带.若从小物块滑上传送带开始计时,小物块在传送带上运动的v-t图象(以地面为参考系)如图乙所示.已知v2>v1.则 ( )
A.t2时刻,小物块离A处的距离达到最大
B.t1时刻,小物块相对传送带滑动的距离达到最大
C.t2-t3时间内,小物块受到的摩擦力方向向右
D.0-t2时间内,小物块受到摩擦力的大小和方向都不变 siskyhai1年前1
siskyhai1年前1 -
 夕48 共回答了19个问题
夕48 共回答了19个问题 |采纳率94.7%A、由乙图知:物体先向左做匀减速运动,向右做匀加速运动,直到速度与传送带相同,做匀速运动.故t1时刻,小物块离A处的距离达到最大.故A错误.
B、物块先向左运动,后向右运动,而传送带一直向右运动,故速度与传送带相同时小物块相对传送带滑动的距离达到最大.即t2时刻,小物块相对传送带滑动的距离达到最大.故B错误.
C、t2-t3时间内,小物块相对于传送带静止向右做匀速运动,不受摩擦力.故C错误.
D、0-t2时间内,物块相对传送带一直向左运动,受到的滑动摩擦力方向一直向右,大小为f=μmg保持不变.故D正确.
故选D1年前查看全部
- (2005•崇明县一模)20℃时,氯化钠的溶解度为36克/100克水.在20℃时,将20克氯化钠放入50克水中,充分溶解
(2005•崇明县一模)20℃时,氯化钠的溶解度为36克/100克水.在20℃时,将20克氯化钠放入50克水中,充分溶解后所得溶液的质量是______克.
 孤星魂1年前1
孤星魂1年前1 -
 spring226 共回答了22个问题
spring226 共回答了22个问题 |采纳率77.3%解题思路:根据溶解度的含义进行解答.20℃时,氯化钠的溶解度为36g,即20℃时,在100g水中最多溶解36g氯化钠.所以在20℃时,将20克氯化钠放入50克水中,只有18g氯化钠溶解,所得溶液的质量是50g+18g=68g.
故答案为:68.点评:
本题考点: 固体溶解度的概念;溶液、溶质和溶剂的相互关系与判断.
考点点评: 将一定质量物质溶于水中所得溶液质量,要先根据溶解度算出能够溶解多少,不溶解的不能算溶液质量.1年前查看全部
- (2014•崇明县二模)如图所示的是酶、激素、蛋白质、抗体四者关系.下列有关叙述正确的是( )
(2014•崇明县二模)如图所示的是酶、激素、蛋白质、抗体四者关系.下列有关叙述正确的是( )

A.1、2、3分别表示激素、酶、蛋白质
B.能产生4的细胞一定能产生1
C.能产生3的细胞一定能产生4
D.物质1和3都具有专一性,属于高效能物质 水色鱼1年前1
水色鱼1年前1 -
 雨玲儿520 共回答了26个问题
雨玲儿520 共回答了26个问题 |采纳率92.3%解题思路:由题意知,1、2、3、4是激素、蛋白质、酶、抗体,绝大多数酶的本质是蛋白质,抗体属于蛋白质,大多数的激素的本质是蛋白质,蛋白质包括抗体、酶、激素等,因此分析题图可以看出:1是激素,2是蛋白质,3是酶,4是抗体.A、由题图知,1、2、3分别表示激素、蛋白质、酶,A错误;
B、激素是由专门的内分泌器官或细胞产生的,产生抗体的浆细胞不能产生激素,B错误;
C、所有的活细胞均能产生酶,抗体是由浆细胞产生的,产生酶的细胞不一定能产生抗体,C错误;
D、酶和激素的作用都具有专一性,且都是微量、高效的,D正确.
故选:D.点评:
本题考点: 酶的特性;蛋白质在生命活动中的主要功能.
考点点评: 对于酶、激素、蛋白质、抗体概念之间关系的理解、建构合理的概念图的能力是本题考查的重点.1年前查看全部
- (2009•崇明县二模)实验室用氯化钠配制lOOg溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解;②称取氯化钠;
(2009•崇明县二模)实验室用氯化钠配制lOOg溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解;②称取氯化钠;③计算;④量取水;⑤装瓶贴标签.正确的操作顺序是( )
A.①②③④⑤
B.③②④①⑤
C.①③⑤②④
D.③②④⑤① intria1年前1
intria1年前1 -
 startle 共回答了19个问题
startle 共回答了19个问题 |采纳率89.5%解题思路:根据配制溶质质量分数一定的溶液的基本步骤考虑;配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放.
故选B.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 通过回答本题知道了配制溶质质量分数一定的溶液的基本步骤,要熟记它们并能灵活运用.1年前查看全部
大家在问
- 1负隅顽抗是描写敌人狼狈的词语吗?
- 2N4H4(SO4)电离方程式 其含氮质量分数为
- 3课文全文着眼于以情感人,这个情是怎样的情
- 4出师表“以情感人‘中的“情”是什么
- 5鉴别乙酸和乙醇,可用Na2CO3溶液,该反应的离子方程式是什么
- 6乙醇乙酸和笨能用饱和Na2CO3溶液鉴别么 解析下
- 7列方程解应用题:某中学拟组织九年级
- 8一道高中数学题,关于幂函数已知函数∫﹙x﹚=x的[(1-a)/3]次幂的定义域是非零实数,且在(0,﹢∞)上是减函数,在
- 9如图,在等腰梯形ABCD中,AD平行BC,AD=3CM,BC=5CM,∠ABC=45°,求梯形的高
- 10怎样把深夜,整个山庄一片寂静改成拟人句?
- 11英语翻译说的人说是法语,如果不是字面意思还能是什么意思呢~会是和经济有关的的专业术语不?
- 12art,sing,music哪个是不同类的?
- 13填空题 生活中不能没有规则,如果没有规则,___;如果没有规则,___;如果没有规则,_____.
- 14有一个两位数,如果把它的个位数字a和十位数b对偶,那么什么情况下得到的两位数比原来的两位数大?
- 15水溶性维生素对人体有哪些作用

