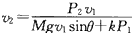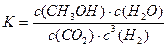动力源期末寒假作业七年级数学答案(蓉城课堂给力A+)
 kaspersky2022-10-04 11:39:541条回答
kaspersky2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 Justin_xu78 共回答了16个问题
Justin_xu78 共回答了16个问题 |采纳率75%- 亲,听说作业帮上有8000本寒假作业答案,应该有你这本。扫描一下就出整本答案。手机搜索作业帮就可以下载试用下啦。有不懂的问题还可以在作业帮单独拍照提问,10万学霸在线帮你解决。
- 1年前
相关推荐
- 2010年上海世博会使用了一种纯电动节能环保车.这种车使用电池作动力源,走起来比燃油车的响声小得多,同时也不会排放气体.
2010年上海世博会使用了一种纯电动节能环保车.这种车使用电池作动力源,走起来比燃油车的响声小得多,同时也不会排放气体.下表是一款纯电动汽车与同型号内燃机汽车对比的测试数据(测试过程认为做匀速直线运动).(汽油的热值4.6×10 7 J/kg).
(1)请计算汽车牵引力做的功及其功率;车型 能源 测试距离 牵引力 速度 百公里总耗能 效率 纯电动汽车 电能 100km 600N 72km/h 7.2×10 7 J 83.3% 内燃机汽车 汽油 100km 600N 3×10 8 J
(2)内燃机汽车每百公里消耗的汽油质量及其效率;
(3)根据题目信息,说出这种纯电动汽车节能与环保主要体现在哪些方面(至少各回答一个)? 大大7041年前1
大大7041年前1 -
 kevin_leee 共回答了15个问题
kevin_leee 共回答了15个问题 |采纳率93.3%根据表中信息可知,汽车受到的牵引力为600N,行驶的距离为100km=10 5 m,行驶的速度为72km/h=20m/s,内燃机汽车每百公里消耗的总能量Q=3×10 8 J;
(1)汽车牵引力做的功:W=FS=600N×10 5 m=6×10 7 J;
汽车的功率:P=Fv=600N×20m/s=1.2×10 4 W;
(2)∵Q=mq
∴内燃机汽车每百公里消耗的汽油质量:m=
Q
q =
3×1 0 8 J
4.6×1 0 7 J/kg =6.52kg;
内燃机汽车的效率:η=
W
Q ×100%=
6×1 0 7 J
3 ×10 8 J ×100%=20%;
(3)节能体现在该电动车的效率高;环保体现在噪音小、无废气排放.
答:(1)汽车牵引力做的功及其功率分别为6×10 7 J和1.2×10 4 W;
(2)内燃机汽车每百公里消耗的汽油质量及其效率分别为6.52kg和20%;
(3)节能体现在该电动车的效率高;环保体现在噪音小、无废气排放.1年前查看全部
- 请问大马力汽车发动机能作为气压盘式制动器的动力源吗?
请问大马力汽车发动机能作为气压盘式制动器的动力源吗?
请列举可以采用什么动力源!
制动器工作状态:制动70m/s,145N.m bulleyes1年前1
bulleyes1年前1 -
 爱的罗曼史 共回答了22个问题
爱的罗曼史 共回答了22个问题 |采纳率100%气压的只有鼓式制动.气压盘式制动器,我还没见过呢.气压式不能装ABS系统.制动器动力源:发动机、电动油泵.气压式:利用发动机带动打气泵,把空气压缩并储在汽罐内备用.液压式:一种,利用发动机进气管内产生的真空,驱动...1年前查看全部
- 航天飞船可用肼(N 2 H 4 )和过氧化氢(H 2 O 2 )为动力源。已知1 g液态肼和足量液态过氧化氢反应生成氮气
航天飞船可用肼(N 2 H 4 )和过氧化氢(H 2 O 2 )为动力源。已知1 g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05 kJ的热量。下列说法中错误的是( )
N 2 H 4 (l)+2H 2 O 2 (l)===N 2 (g)+4H 2 O(g)ΔH=-641.6 kJ·mol - 1A.该反应中肼作还原剂 B.液态肼的燃烧热为20.05 kJ·mol -1 C.该动力源的突出优点之一是生成物对环境污染小 D.肼和过氧化氢反应的热化学方程式为:  土豆囡囡1年前1
土豆囡囡1年前1 -
 fgwqwa 共回答了12个问题
fgwqwa 共回答了12个问题 |采纳率83.3%B
1 g液态肼反应放热20.05 kJ,
则1 mol液态肼反应放热为:20.05 kJ/(1 g /32g·mol - 1 )=641.6 kJ·mol - 1 ,故D正确;
分析元素化合价的变化:H 2 O 2 中-1价的氧反应后降低到H 2 O中的-2价,则肼(N 2 H 4 )中应存在元素化合价的升高,腈被氧化,做还原剂,故A正确;
燃烧热的定义:在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,故B错误;1年前查看全部
- 甲醇燃料电池被认为是21世纪电动汽车的最佳候选动力源,其工作原理如图所示。下列有关叙述正确的是 &
甲醇燃料电池被认为是21世纪电动汽车的最佳候选动力源,其工作原理如图所示。下列有关叙述正确的是 ( )。
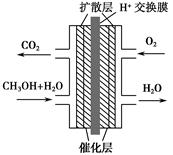
A.通氧气的一极为负极 B.H + 从正极区通过交换膜移向负极区 C.通甲醇的一极的电极反应式为CH 3 OH+H 2 O-6e - =CO 2 ↑+6H + D.甲醇在正极发生反应,电子经过外电路流向负极  猫行者1年前1
猫行者1年前1 -
 纯情的西门庆 共回答了17个问题
纯情的西门庆 共回答了17个问题 |采纳率88.2%C
外电路中电子从负极流向正极,内电路H + 从负极移向正极,B、D错误;O 2 在正极发生还原反应,A错误;甲醇在负极发生氧化反应,负极反应式为CH 3 OH+H 2 O-6e - =CO 2 ↑+6H + 。1年前查看全部
- (2013•广东模拟)2010年上海世博会使用了一种纯电动节能环保车.这种车使用电池作动力源,走起来比燃油车的响声小得多
(2013•广东模拟)2010年上海世博会使用了一种纯电动节能环保车.这种车使用电池作动力源,走起来比燃油车的响声小得多,同时也不会排放气体.下表是一款纯电动汽车与同型号内燃机汽车对比的测试数据(测试过程认为做匀速直线运动).(汽油的热值4.6×107J/kg).
(1)请计算汽车牵引力做的功及其功率;车型 能源 测试距离 牵引力 速度 百公里总耗能 效率 纯电动汽车 电能 100km 600N 72km/h 7.2×107J 83.3% 内燃机汽车 汽油 100km 600N 3×108J
(2)内燃机汽车每百公里消耗的汽油质量及其效率. kitty50951年前1
kitty50951年前1 -
 alric 共回答了18个问题
alric 共回答了18个问题 |采纳率88.9%解题思路:(1)已知汽车的牵引力、行驶的距离以及行驶的速度,根据W=FS和P=Fv即可求出牵引力做的功及其功率;
(2)已知内燃机行驶一百公路消耗的总能量和汽油的热值,根据Q=mq即可求出消耗的汽油质量;利用η=[W/Q]×100%即可求出效率.根据表中信息可知,汽车受到的牵引力为600N,行驶的距离为100km=105m,行驶的速度为72km/h=20m/s,内燃机汽车每百公里消耗的总能量Q=3×108J;
(1)汽车牵引力做的功:W=FS=600N×105m=6×107J;
汽车的功率:P=Fv=600N×20m/s=1.2×104W;
(2)∵Q=mq,
∴内燃机汽车每百公里消耗的汽油质量:m=[Q/q]=
3×108J
4.6×107J/kg=6.52kg;
内燃机汽车的效率:η=[W/Q]×100%=
6×107J
3×108J×100%=20%.
答:(1)汽车牵引力做的功及其功率分别为6×107J和1.2×104W;
(2)内燃机汽车每百公里消耗的汽油质量及其效率分别为6.52kg和20%.点评:
本题考点: 功的计算;功率的计算;热机的效率.
考点点评: 本题考查做功、功率、质量、效率、质量的计算,关键是公式及其变形的灵活运用,重点是从表中所给信息中找到有用的数据.1年前查看全部
- 动力源期末寒假作业物理
 hdxyx1年前2
hdxyx1年前2 -
 从意百货 共回答了20个问题
从意百货 共回答了20个问题 |采纳率85%请下载作业帮吧,有寒假作业答案呢1年前查看全部
- (2012•宁德二模)锌-空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性.在碱性溶液中该电池总反应
(2012•宁德二模)锌-空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性.在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2=2Na2ZnO2+2H2O.下列有关锌-空气电池说法正确的是( )
A.负极反应式为:O2+2H2O+4e-=4OH-
B.碱性或酸性电解质溶液中,该电池正极反应式相同
C.该电池工作时,Na+移向负极
D.每生成1 mol ZnO22-转移电子数为2 NA(NA为阿伏加德罗常数) dong0111年前1
dong0111年前1 -
 咸咸咸 共回答了16个问题
咸咸咸 共回答了16个问题 |采纳率87.5%解题思路:A.负极上锌失去电子,发生氧化反应;
B.正极上氧气得电子,酸性条件生成水,碱性条件生成氢氧根离子;
C.原电池中阳离子向正极移动;
D.根据元素化合价的变化判断转移电子数.A.负极上锌失去电子,发生氧化反应,负极反应式为:2Zn+4OH--4e-=2ZnO22-+2H2O,故A错误;
B.正极上氧气得电子,酸性条件生成水,碱性条件生成氢氧根离子,所以碱性或酸性电解质溶液中,该电池正极反应式不相同,故B错误;
C.原电池中阳离子向正极移动,所以Na+移向正极,故C错误;
D.由2Zn+4OH--4e-=2ZnO22-+2H2O可知,每生成1 mol ZnO22-转移电子数为2NA,故D正确;
故选D.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查了原电池知识,题目难度不大,注意根据电池反应判断原电池的正负极以及电极反应.1年前查看全部
- (2013•大兴区一模)面对能源紧张和环境污染等问题,混合动力汽车应运而生.所谓混合动力汽车,是指拥有两种不同动力源(如
(2013•大兴区一模)面对能源紧张和环境污染等问题,混合动力汽车应运而生.所谓混合动力汽车,是指拥有两种不同动力源(如燃油发动机和电力发动机)的汽车,既省油又环保.车辆在起步或低速行驶时可仅靠电力驱动;快速行驶或者需急加速时燃油发动机启动,功率不足时可由电力补充;在制动、下坡、怠速时能将机械能转化为电能储存在电池中备用.假设汽车质量为M,当它在平直路面行驶时,只采用电力驱动,发动机额定功率为P1,能达到的最大速度为v1;汽车行驶在倾角为θ的斜坡道上时,为获得足够大的驱动力,两种动力同时启动,此时发动机的总额定功率可达P2.已知汽车在斜坡上行驶时所受的摩擦阻力与在平直路面上相等,运动过程阻力不变,重力加速度为g.
求:(1)汽车在平直路面上行驶时受到的阻力
(2)汽车在斜坡道上能达到的最大速度.
(3)若汽车在斜面上以恒定功率P1从静止做加速直线运动,经时间刚好达到最大速度V1,求这段时间的位移. 冷遇寒1年前1
冷遇寒1年前1 -
 爱在洗脸前 共回答了20个问题
爱在洗脸前 共回答了20个问题 |采纳率95%(1)在平直路面行驶,汽车以功率P1匀速行驶时速度最大,设驱动力为F1,阻力为f,则
P1=F1v1①
F1=f ②
解得:f=
P1
v1
(2)设汽车上坡时驱动力为F2,能达到的最大速度为v2,则
P2=F2v2③
F2=Mgsinθ+f ④
由①②③④式解得
v2=
P2v1
Mgv1sinθ+P1 ⑤
(3)由动能定理:
P1t-fs=[1/2]Mv12⑥
解得:s=
2P1v1t-Mv13
2P1
答:(1)汽车在平直路面上行驶时受到的阻力为
P1
v1;
(2)汽车在斜坡道上能达到的最大速度为
P2v1
Mgv1sinθ+P1.
(3)若汽车在斜面上以恒定功率P1从静止做加速直线运动,经时间刚好达到最大速度V1,这段时间的位移为
2P1v1t-Mv13
2P1.1年前查看全部
- 电动自行车以铅蓄电池为动力源,铅蓄电池是一种使用方便、安全、可靠,又可以循环使用的化学电源,铅蓄电池内有溶质质量分数为3
电动自行车以铅蓄电池为动力源,铅蓄电池是一种使用方便、安全、可靠,又可以循环使用的化学电源,铅蓄电池内有溶质质量分数为31%的硫酸溶液,若用98%(密度为1.84克/厘米 3 )的浓硫酸配制上述硫酸溶液,则浓硫酸和水的体积比约是( ) A.1:3 B.3:1 C.1:4 D.4:1  huqin511年前1
huqin511年前1 -
 ghifbsn 共回答了16个问题
ghifbsn 共回答了16个问题 |采纳率75%设配制时使用浓硫酸的体积为x,使用水的体积为y
x×1.84g/ cm 3 ×98%
y×1g/ cm 3 +x×1.84g/ cm 3 ×100%=31%
x:y=1:4
故选C.1年前查看全部
- 我们的动力源自您的舒适与舒心翠峰大酒店热诚欢迎阁下的光临!我们殷切期望酒店的服务和设施令阁下感到满意.为了方便您的旅行,
我们的动力源自您的舒适与舒心
翠峰大酒店热诚欢迎阁下的光临!我们殷切期望酒店的服务和设施令阁下感到满意.为了方便您的旅行,特奉上此《服务指南》,其中详细介绍了本酒店各项设施及其服务项目等,以供参阅.
谨祝阁下在本酒店逗留愉快,并期望您的再次光临! xusen19841年前3
xusen19841年前3 -
 cc 共回答了24个问题
cc 共回答了24个问题 |采纳率87.5%Our dynamic and enjoyable from the comfort of your
Verde Hotel warm welcome you here!We earnestly hope that the hotel services and facilities to make you satisfied.In order to facilitate your travel,special enclose the "Service Guide",which details the various facilities of this hotel and its services,etc.,for reference.
I wish you a pleasant stay in this hotel and look forward to your next visit!1年前查看全部
- (2010•郑州一模)阿波罗宇宙飞船升入太空是以N2H4(联氨)和N2O4为动力源.反应温度高达2700℃,反应式为2N
(2010•郑州一模)阿波罗宇宙飞船升入太空是以N2H4(联氨)和N2O4为动力源.反应温度高达2700℃,反应式为2N2H4+N2O4═3N2+4H2O.对于该反应的说法正确的是( )
A.联氨是氧化剂
B.氧化产物和还原产物的质量比为1:2
C.属于置换反应
D.联氨是还原剂 terrymmmm1年前1
terrymmmm1年前1 -
 44_zlex 共回答了25个问题
44_zlex 共回答了25个问题 |采纳率92%解题思路:反应2N2H4+N2O4=3N2+4H2O中,从化合价的角度分析氧化还原反应的相关概念.N元素的化合价由-2价升高到0,N元素的化合价由+4降低到0,以此来解答.解;A.联氨中N元素的化合价由-2价升高到0,则为还原剂,故A错误;
B.由N元素的化合价由-2价升高到0,N元素的化合价由+4降低到0,则氧化剂和还原剂反应后都生成氮气,氧化产物和还原产物质量之比为4:2=2:1,故B错误;
C.单质与化合物反应生成单质与化合物的反应为置换反应,而该反应的反应物中没有单质,则不属于置换反应,故C错误;
D.联氨中N元素的化合价由-2价升高到0,则为还原剂,故D正确;
故选D.点评:
本题考点: 氧化还原反应;氧化还原反应的计算.
考点点评: 本题考查氧化还原反应,明确化合价的分析是解答本题的关键,熟悉常见物质中元素的化合价及氧化还原反应中的基本概念即可解答,难度不大.1年前查看全部
- 面对能源紧张和环境污染等问题,混合动力汽车应运而生。所谓混合动力汽车,是指拥有两种不同动力源(如燃油发动机和电力发动机)
面对能源紧张和环境污染等问题,混合动力汽车应运而生。所谓混合动力汽车,是指拥有两种不同动力源(如燃油发动机和电力发动机)的汽车,既省油又环保。车辆在起步或低速行驶时可仅靠电力驱动;快速行驶或者需急加速时燃油发动机启动,功率不足时可由电力补充;在制动、下坡、怠速时能将机械能转化为电能储存在电池中备用。假设汽车质量为M,当它在平直路面行驶时,只采用电力驱动,发动机额定功率为P 1 ,能达到的最大速度为v 1 ;汽车行驶在倾角为θ的斜坡道上时,为获得足够大的驱动力,两种动力同时启动,此时发动机的总额定功率可达P 2 。已知汽车在斜坡上行驶时所受的阻力是在平直路面上的k倍,重力加速度为g。求汽车在斜坡道上能达到的最大速度。  重楼081年前1
重楼081年前1 -
 xvdgy 共回答了20个问题
xvdgy 共回答了20个问题 |采纳率100%1年前查看全部
- (12分)甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(12分)甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa时,1 mol CH 3 OH完全燃烧生成稳定的氧化物放出热量726.51 kJ,则甲醇燃烧的热化学方程式为 。
(2)甲醇燃料电池的结构示意图如下左图。甲醇进入 极(填“正”或“负”),正极发生的电极反应为 。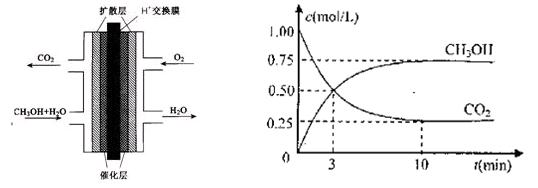
(3)目前工业上有一种方法是用CO 2 来生产燃料甲醇。为探究反应原理,现进行如下实验。在体积为1L的密闭容器中,充入1molCO 2 和3molH 2 ,一定条件下发生反应:
CO 2 (g)+3H 2 (g) CH 3 OH(g)+H 2 O(g)△H =-49.0KJ/mol
CH 3 OH(g)+H 2 O(g)△H =-49.0KJ/mol
测得CO 2 和CH 3 OH(g)的浓度随时间变化如上右图所示。
①从反应开始到平衡,氢气的平均反应速率v(H 2 )=
②该反应的平衡常数表达式为 。
③下列措施中能使n(CH 3 OH)/n(CO 2 )增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H 2 O(g)从体系中分离 D.再充入1molCO 2 和3molH 2 comtx1231年前1
comtx1231年前1 -
 daisy88 共回答了20个问题
daisy88 共回答了20个问题 |采纳率100%1年前查看全部
- (13分)直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(13分)直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa时,1 mol CH 3 OH完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol,则甲醇燃烧的热化学方程式为 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH 3 OH(g)+H 2 O(g)=CO 2 (g)+3H 2 (g) △H 1 ="+49.0" kJ·mol -1
②CH 3 OH(g)+ O 2 (g)= CO 2 (g)+2H 2 (g) △H 2
O 2 (g)= CO 2 (g)+2H 2 (g) △H 2
已知H 2 (g)+ O 2 (g)===H 2 O(g) △H ="-241.8" kJ·mol -1
O 2 (g)===H 2 O(g) △H ="-241.8" kJ·mol -1
则反应②的△H 2 = 。
(3)甲醇燃料电池的结构示意图如右。甲醇进入 极(填“正”或“负”),该极发生的电极反应为 。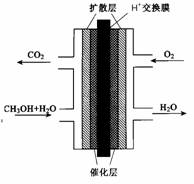
(4)已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:
N 2 ( g ) + 3H 2 ( g ) = 2NH 3 ( g ) ΔH=" —92.4" KJ/mol,则N≡N键的键能是 。 鲸鲸的小梳子1年前1
鲸鲸的小梳子1年前1 -
 ly591405798 共回答了21个问题
ly591405798 共回答了21个问题 |采纳率90.5%(13分)(1)CH 3 OH(l) + 3/2 O 2 (g) = CO 2 (g) + 2H 2 O(l) △H =-726.51 kJ/mol (3分)
(2)-192.8 kJ·mol -1 (3分)
(3)负 (2分) CH 3 OH+ H 2 O-6e - =CO 2 + 6H + (2分) (4)945.6KJ/mol (3分)
1年前查看全部
- 电磁铁应用问题.我想利用电磁铁的技术做推动物体前行的动力源.具体要求是:被推动物品为圆形片状,通道为圆形管状,行程1,5
电磁铁应用问题.
我想利用电磁铁的技术做推动物体前行的动力源.具体要求是:被推动物品为圆形片状,通道为圆形管状,行程1,5米工件依次叠加规则有序前行.请问,采用什么形式电磁铁技术,可以满足需要.
 ydyd11011年前1
ydyd11011年前1 -
 nn的雪碧 共回答了13个问题
nn的雪碧 共回答了13个问题 |采纳率92.3%比例电磁铁.秦能科技1年前查看全部
- 英语翻译目前全球的现代汽车上仍广泛采用内燃机作为动力源,消耗大量的石油资源,排出大量的废气,以至于全球变暖,空气污染,酸
英语翻译
目前全球的现代汽车上仍广泛采用内燃机作为动力源,消耗大量的石油资源,排出大量的废气,以至于全球变暖,空气污染,酸雨,淡水资源危机,资源、能源短缺,噪声污染.电动汽车则是以电力这种可再生资源为能源,既没有有害气体排放也没有温室气体排放,噪音也很小.它是21世纪清洁、高效和可持续的交通工具.
电动汽车的关键部位是动力电源,动力电源系统储存能量的多少是决定电动汽车续驶里程的重要因素.但是目前动力电源技术仍然是发展电动汽车的瓶颈,未能取得突破性进展.电动汽车的续驶里程还不能满足用户的需求,如果将车辆减速时的动能转化为电能,回收入动力电源系统,而不是被摩擦浪费掉,这无疑相当于增加了动力电源系统的容量.在现有的技术条件下,对于提高电动汽车的续驶里程,这无疑是一个最直接有效的措施.文献[1]表明,在城市工况下,制动能量占总驱动能量的50%左右.因此,采用先进的能量回收技术,应用现代车辆设计方法和手段,对汽车的制动能量回收进行深入研究具有十分重要的意义. 原子核心1年前1
原子核心1年前1 -
 巧克力410 共回答了19个问题
巧克力410 共回答了19个问题 |采纳率89.5%Hyundai is currently the world is still widely used in internal combustion engine as a power source, consume large amounts of oil resources, emit large amounts of emissions, that global warming, air pollution, acid rain, freshwater resource crisis, resources, energy shortages, noise pollution. Power electric vehicles is based on renewable resources such as energy, neither of harmful gas emissions and no greenhouse gas emissions, noise is also small. It is the 21st century, clean, efficient and sustainable transport.
The key part is the electric vehicle power supply, power supply system is to determine the amount of stored energy driving range of electric vehicles, an important factor. But the current power supply technology is still the bottleneck of the development of electric cars, not a breakthrough. Driving range of electric vehicles can not meet the needs of users, if the vehicle kinetic energy during deceleration into electrical energy power supply system to income, rather than wasted by friction, which undoubtedly representing an increase of power supply capacity of the system. Under the conditions of the existing technology, for improving the driving range of electric vehicles, this is one of the most direct and effective measures. [1] showed that in urban conditions, the braking energy of the total driving energy of 50%. Therefore, the use of advanced energy recovery technology, application methods and means of modern vehicle design, vehicle braking energy recovery of in-depth study of great significance.1年前查看全部
- 甲醇燃料电池被认为是21世纪电动汽车的最佳候选动力源,其工作原理如图所示.下列有关叙述正确的是( )
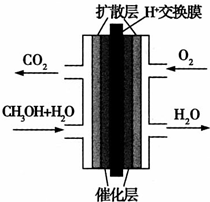 甲醇燃料电池被认为是21世纪电动汽车的最佳候选动力源,其工作原理如图所示.下列有关叙述正确的是( )
甲醇燃料电池被认为是21世纪电动汽车的最佳候选动力源,其工作原理如图所示.下列有关叙述正确的是( )
A.通氧气的一极为负极
B.H+从正极区通过交换膜移向负极区
C.通甲醇的一极的电极反应式为CH3OH+H2O−6e−
CO2↑+6H+..
D.甲醇在正极发生反应,电子经过外电路流向负极 游戏此生1年前1
游戏此生1年前1 -
 songchengfang 共回答了10个问题
songchengfang 共回答了10个问题 |采纳率100%解题思路:根据图片知,电解质溶液是酸性溶液,甲醇燃料电池中,通入甲醇的电极是负极,负极上失电子发生氧化反应,电极反应式为CH3OH(l)+H2O(l)-6e-=CO2(g)↑+6H+,正极反应式为O2+4e-+4H+=2H2O.A.通入氧气的电极是正极,正极上得电子发生还原反应,故A错误;
B.放电时,氢离子向正极移动,故B错误;
C.通入甲醇的电极是负极,负极上电极反应式为CH3OH(l)+H2O(l)-6e-=CO2(g)↑+6H+,故C正确;
D.甲醇易失电子发生氧化反应,所以甲醇在负极发生反应,电子从负极沿导线流向正极,故D错误;
故选C.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查了甲醇燃料电池,题目难度不大,注意把握原电池的工作原理以及电极反应式的书写.1年前查看全部
- 有谁给说一下动力组与一般火车有什么不同,各以什么为动力源
有谁给说一下动力组与一般火车有什么不同,各以什么为动力源
一般火车上面的电线网是给火车供电的吗,动力组是不是现在各大城市都普遍了 哈搭楼神1年前1
哈搭楼神1年前1 -
 琴麻岛的相当左14 共回答了24个问题
琴麻岛的相当左14 共回答了24个问题 |采纳率87.5%lz是说动车组吧?
动车组就是每节车厢上都能为列车提供动力 从而达到提高速度
一般火车光靠火车头 后面的车厢都是无动力的 所以速度没有动车组快
火车上面的电网是给电力机车供电 内燃机车用燃油
动车组还不算太普遍1年前查看全部
- (2004•湖州)电动自行车以铅蓄电池为动力源,铅蓄电池是一种使用方便、安全、可靠,又可以循环使用的化学电源,铅蓄电池内
(2004•湖州)电动自行车以铅蓄电池为动力源,铅蓄电池是一种使用方便、安全、可靠,又可以循环使用的化学电源,铅蓄电池内有溶质质量分数为31%的硫酸溶液,若用98%(密度为1.84克/厘米3)的浓硫酸配制上述硫酸溶液,则浓硫酸和水的体积比约是( )
A.1:3
B.3:1
C.1:4
D.4:1 h6gcogao1年前1
h6gcogao1年前1 -
 MengFanHu 共回答了21个问题
MengFanHu 共回答了21个问题 |采纳率90.5%解题思路:用98%的浓硫酸配制溶质质量分数为31%的硫酸溶液,可采取加水稀释的方法,在加水进行稀释时,所得溶液中溶质质量为浓硫酸中硫酸的质量,利用溶质的质量分数的计算公式,由稀释后所得溶液的溶质质量分数可求得浓硫酸和水的体积比.设配制时使用浓硫酸的体积为x,使用水的体积为y
x×1.84g/cm3×98%
y×1g/cm3+x×1.84g/cm3×100%=31%
x:y=1:4
故选C.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 对浓溶液加水稀释时,溶质质量不变而溶液质量随加水的量增加而使溶液中溶质质量分数减小.1年前查看全部
- 据了解,泸州公交公司最近新投入的电气混合新能源公交车,拥有两种不同的动力源(燃油发动机和电力发动机),具有充电时间短,优
据了解,泸州公交公司最近新投入的电气混合新能源公交车,拥有两种不同的动力源(燃油发动机和电力发动机),具有充电时间短,优先用电,电气混用动力互补,回收储备电能等特点,既省油又环保.假设汽车及车上乘客总质量为M=10×103kg,当它在平直路面上行驶时,只采用电力驱动,发动机额定功率为P1=150kw,能达到的最大速度为v1=54km/h;汽车行驶在倾角为θ=37°的斜坡道上时,为获得足够大的驱动力,两种动力同时启动,此时发动机的总额定功率可达P2=560kw.设汽车在斜坡上行驶时所受的摩擦阻力与在平直路面上的摩擦阻力相等,汽车在运动过程中摩擦阻力不变.(g=10m/s2,sin37°=0.6,cos37°=0.8,不计空气阻力)求:
(1)汽车在平直路面上行驶时受到的摩擦阻力;
(2)汽车在斜坡道上能达到的最大速度v2;
(3)若汽车在斜坡上以恒定功率P2从静止开始做加速直线运动,经过时间t=30s刚好达到最大速度v2,求这段时间内汽车运动的位移. qwwee31年前0
qwwee31年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 锌-空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性.在碱性溶液中该电池总反应可表示为:2Zn+4N
锌-空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性.在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2═2Na2ZnO2+2H2O.下列有关锌-空气电池说法正确的是( )
A.碱性电解质溶液中正极反应式为:4OH--4e-═O2↑+2H2O
B.碱性或酸性电解质溶液中,该电池正极反应式相同
C.该电池工作时,Na+移向负极
D.每生成1mol ZnO22-转移电子数为2NA yiwei_lu1年前1
yiwei_lu1年前1 -
 zazdq 共回答了26个问题
zazdq 共回答了26个问题 |采纳率88.5%解题思路:根据电池反应式知,锌作负极,负极上电极反应式为:Zn+40H--2e-═ZnO22-+2H20,正极上通入空气,其电极反应式为O2+2H2O+4e-=4OH-,原电池放电时,阳离子向正极移动,再结合ZnO22-和转移电子之间关系计算.A.碱性电解质溶液中,正极上电极反应式为O2+2H2O+4e-=4OH-,故A错误;
B.酸性条件下,负极反应式为Zn-2e-=Zn2+、正极反应为O2+4e-+4H+=2H2O,与碱性条件下电极反应式不同,故B错误;
C.放电时,钠离子向正极移动,故C错误;
D.每生成1mol ZnO22-转移电子数=1mol×2×NA/mol=2 NA,故D正确;
故选D.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池原理,知道离子移动方向、各个物理量之间的关系等知识点即可解答,难点是电极反应式书写,电解质溶液影响电极反应式书写,题目难度不大.1年前查看全部
- 能作驱动动力源有哪些?除了电机、内燃机、蒸汽机、液压、气动.
能作驱动动力源有哪些?除了电机、内燃机、蒸汽机、液压、气动.
人力这种不算啦.要比较有发散性的思维~ zhang0150001年前1
zhang0150001年前1 -
 liuhuali8705 共回答了18个问题
liuhuali8705 共回答了18个问题 |采纳率77.8%水能,风能,潮汐能,核反应堆,人力应该叫做生物能1年前查看全部
- 直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。

(1)101 kPa时,1 mol CH 3 OH完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol,则甲醇燃烧的热化学方程式为 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH 3 OH(g)+H 2 O(g)=CO 2 (g)+3H 2 (g) △H 1 ="+49.0" kJ·mol -1
②CH 3 OH(g)+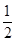 O 2 (g)= CO 2 (g)+2H 2 (g) △H 2
O 2 (g)= CO 2 (g)+2H 2 (g) △H 2
已知H 2 (g)+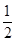 O 2 (g)=H 2 O(g) △H ="-241.8" kJ·mol -1
O 2 (g)=H 2 O(g) △H ="-241.8" kJ·mol -1
则反应②的△H 2 = kJ·mol -1 。
(3)甲醇燃料电池的结构示意图如右。甲醇进入 极(填“正”或“负”),正极发生的电极反应式为 。负极发生的电极反应式为 。 不能三言两语1年前1
不能三言两语1年前1 -
 啊啊72 共回答了23个问题
啊啊72 共回答了23个问题 |采纳率87%(1)CH 3 OH(g)+3/2O 2 (g)=CO 2 (g)+2H 2 O(l) △H=-726.51kJ/mol (2)-192.8
(3)负 O 2 +4H + +4e - =2H 2 O CH 3 OH+H 2 O-6e - =CO 2 ↑+6H +
1年前查看全部
- 电动自行车以铅蓄电池为动力源,铅蓄电池是一种使用方便、安全、可靠,又可以循环使用的化学电源,铅蓄电池内有溶质质量分数为3
电动自行车以铅蓄电池为动力源,铅蓄电池是一种使用方便、安全、可靠,又可以循环使用的化学电源,铅蓄电池内有溶质质量分数为31%的硫酸溶液,若用98%(密度为1.84克/厘米3)的浓硫酸配制上述硫酸溶液,则浓硫酸和水的体积比约是( )
A. 1:3
B. 3:1
C. 1:4
D. 4:1 hia20041年前1
hia20041年前1 -
 再唱空城计 共回答了18个问题
再唱空城计 共回答了18个问题 |采纳率94.4%解题思路:用98%的浓硫酸配制溶质质量分数为31%的硫酸溶液,可采取加水稀释的方法,在加水进行稀释时,所得溶液中溶质质量为浓硫酸中硫酸的质量,利用溶质的质量分数的计算公式,由稀释后所得溶液的溶质质量分数可求得浓硫酸和水的体积比.设配制时使用浓硫酸的体积为x,使用水的体积为y
x×1.84g/cm3×98%
y×1g/cm3+x×1.84g/cm3×100%=31%
x:y=1:4
故选C.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 对浓溶液加水稀释时,溶质质量不变而溶液质量随加水的量增加而使溶液中溶质质量分数减小.1年前查看全部
- 动力源期末暑假作业八年纪语文在哪买
 macnabbs1年前1
macnabbs1年前1 -
 猪然 共回答了23个问题
猪然 共回答了23个问题 |采纳率91.3%新华书店看看 我以前就买到我的暑假作业的1年前查看全部
- 机器如果没有了摩擦力和动力如果一个机器在稳定运行的过程中,突然没有了动力源与消耗能量的东西(比如摩擦力),这个机器的情况
机器如果没有了摩擦力和动力
如果一个机器在稳定运行的过程中,突然没有了动力源与消耗能量的东西(比如摩擦力)
,这个机器的情况是怎样的.
例如,一个曲柄滑块机构稳定运行,如果没有了摩擦力和动力,它的情况是怎样的.会永远运行下去吗?
先谢谢楼下几位的回答。
你们还是把我给提醒了。
我承认我当时有点钻牛角尖糊涂了。
我认为,这个要分情况。在这个封闭系统内,能量总量不变(前提是,只有机械能的循环传递,没有变成其他形式的能。)
但是,机器可能会出现:1.2.机器散架(因为有内部力)。
1的情况是什么? 恶心的rr1年前3
恶心的rr1年前3 -
 nancy112233 共回答了16个问题
nancy112233 共回答了16个问题 |采纳率100%这个问题的条件很理想化,要求没有任何消耗能量的东西
这个其实就是永动机的要求啊.永动机是没有意义的,因为永动机虽然在运动 但是不能对外做功.
可以肯定的回答你,如果没有一切消耗能量的东西,那么不需要动力源,是可以维持机械永远运行下去的.1年前查看全部
- 直接甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
 直接甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
直接甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
(1)101KPa时,1mol气态CH3OH完全燃烧生成CO2气体和液态水时,放出726.51kJ的热量,则甲醇燃烧的热化学方程式是CH3OH(l)+[3/2]O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/molCH3OH(l)+[3/2]O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/mol_.
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O (g)═CO2(g)+3H2(g);△H1═+49.0KJ•mol-1
②CH3OH(g)+[1/2] O2 (g)═CO2(g)+2H2(g);△H2═?
已知H2(g)+[1/2] O2 (g)═H2O (g)△H═-241.8KJ•mol-1,则反应②的△H2=______.
(3)一种甲醇燃料电池是采用铂或碳化钨作电极,稀硫酸作电解液,一极直接加入纯化后的甲醇,同时向另一个电极通人空气.则甲醇进入______极,正极发生的电极反应方程式为______. iszero1年前1
iszero1年前1 -
 微雨嫣火 共回答了24个问题
微雨嫣火 共回答了24个问题 |采纳率100%解题思路:(1)1molCH3OH完全燃烧生成稳定的氧化物为气态二氧化碳和液态水,放出热量726.51kJ/mol,以此书写热化学方程式;
(2)由盖斯定律可知,①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol-1、③H2(g)+[1/2]O2(g)═H2O(g)△H=-241.8kJ•mol-1,①+③得到反应②;
(3)甲醇燃料电池中,甲醇为负极,电解质为酸,甲醇失去电子生成二氧化碳;(1)1molCH3OH完全燃烧生成稳定的氧化物为气态二氧化碳和液态水,放出热量726.51kJ/mol,则燃烧的热化学方程式为CH3OH(l)+[1/2]O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/mol,
故答案为:CH3OH(l)+[3/2]O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/mol;
(2)由盖斯定律可知,①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol-1、③H2(g)+[1/2]O2(g)═H2O(g)△H=-241.8kJ•mol-1,①+③得到反应②,
则△H2=+49.0kJ•mol-1+(-241.8kJ•mol-1)=-192.8kJ•mol-1,故答案为:-192.8kJ•mol-1;
(3)甲醇燃料电池中,甲醇中C元素的化合价升高,则甲醇为负极,电解质为酸,甲醇失去电子生成二氧化碳,正极电极反应为O2+4H++4e-=2H2O,
故答案为:负;O2+4H++4e-=2H2O.点评:
本题考点: 用盖斯定律进行有关反应热的计算;热化学方程式;原电池和电解池的工作原理.
考点点评: 本题为综合题,涉及反应热的计算、热化学反应方程式的书写、燃料电池等知识点,注重高考常考考点的考查,题目难度中等.1年前查看全部
- 动力源期末寒假作业八年级物理
 moonlily8151年前2
moonlily8151年前2 -
 龙海二中 共回答了15个问题
龙海二中 共回答了15个问题 |采纳率80%亲,听说作业帮上有8000本寒假作业答案,应该有你这本。扫描一下就出整本答案。手机搜索作业帮就可以下载试用下啦。有不懂的问题还可以在作业帮单独拍照提问,10万学霸在线帮你解决。1年前查看全部
- 风的动力源是什么?空气中的阻力对风不起作用吗?为什么自然风好像不会受到阻力?和风扇的不同?
 望峰1年前1
望峰1年前1 -
 nekro206 共回答了14个问题
nekro206 共回答了14个问题 |采纳率100%风是因为空气温度差引起气压差造成的空气对流运动,自然风当然也会受到阻力啊,不过你感受不出来罢了,有时候还会有一种错觉以为增强了,风扇也是因为气压差形成,但是没有温度因素,纯粹人为的,不过都会受到空气阻力.1年前查看全部
- 关于磁悬浮列车的一个问题.磁悬浮列车不于轨道相接触,那他的动力源自那里.依靠什么力量前进
 zyplsw1年前1
zyplsw1年前1 -
 真誠一生 共回答了14个问题
真誠一生 共回答了14个问题 |采纳率78.6%不是很明白,不能误导你,你去专业的网站上看看吧.不好意思啦.1年前查看全部
- 地球自转的动力源是什么?公转的动力源是什么?为啥公转速度比自转速度高56倍?
 ll大盗我来也1年前3
ll大盗我来也1年前3 -
 哺乳期的肉弄堂 共回答了20个问题
哺乳期的肉弄堂 共回答了20个问题 |采纳率95%地球靠惯性自转,无动力.由于潮汐、地震、海啸等综合影响,自转速度在变慢,不过变化很小,许多年才会慢1秒.
维持公转的能量来源是太阳对地球的万有引力.公转的速度与自转无关,而与运行轨道(日地距离)有关,因此公转速度比自转速度高56倍这样的比较没有意义.1年前查看全部
- (Ⅰ)甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(Ⅰ)甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)25℃、101 kPa时,1 mol CH 3 OH完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol,则甲醇燃烧的热化学方程式为: 。
(2)甲醇燃料电池的结构示意图如下。甲醇进入 极(填“正”或“负”),写出该极的电极反应式 。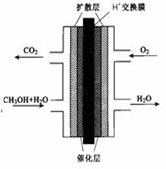
(Ⅱ)铅蓄电池是典型的可充型电池,它的正负极隔板是惰性材料,电池总反应式为:Pb+PbO 2 +4H + +2SO 4 2 - 2PbSO 4 +2H 2 O,请回答下列问题(不考虑氢、氧的氧化还原):
2PbSO 4 +2H 2 O,请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是 电解液中H 2 SO 4 的浓度将变 ;
(2)在完全放电耗尽PbO 2 和Pb时,若按右图连接,电解一段时间后,则在A电极上生成 B电极上生成 。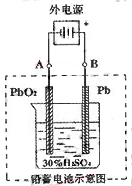
 cyone20061年前1
cyone20061年前1 -
 卜超卜超 共回答了16个问题
卜超卜超 共回答了16个问题 |采纳率81.3%(Ⅰ)(1)CH 3 OH(l) + 3/2 O 2 (g)= CO 2 (g) + 2H 2 O(l) △H ="-726.51" kJ/mol
(2)负 CH 3 OH + H 2 O -6 e - = CO 2 + 6 H +
(Ⅱ)(1)PbO 2 +2e - +4H + +SO 4 2 - =PbSO 4 +2H 2 O 小 (2)Pb PbO 2
1年前查看全部
大家在问
- 1写感怀的作文是一种什么情感
- 2请问有谁知道需要小学六年级上册数学题 四则混合运算及简算题各一道我都迷茫了,
- 3光合作用的原料是怎样到达叶绿体
- 4英语中怎么区分动词后面+s或+es
- 526.5光年和16光年分别等于多少米?合多少天文单位?
- 6Did you find _____ very interesting to play chess?
- 7七言绝句怎么断句?要写出理由!
- 8the children in sichuan look forward with hope_______a chanc
- 9傲慢与偏见英文观后感 50词!..字数40词左右就行了 不要复制版 太长了!
- 10在线求指导:—The pants are very
- 117除以100的余数.
- 12母鸡 阅读题答案先写母鸡的 , , ,后半部分写了母鸡的 , , , ,塑造了一位伟大的母亲形象。作者对母鸡先 ,回来转
- 13牧场有一块草场,牧草每天生长相同,如果有27头牛可吃6天,23头牛吃9天,问25头吃几天
- 14问题一:阅读第一段,你觉得作者为什么会“惊呆”?(请用原文回答) 问题二:请根据2,3,4段的内容,概
- 15请问"新闻媒体"用英语怎么说?