草酸一氢钾与氢氧化钠反应么?
 淡若依涵2022-10-04 11:39:541条回答
淡若依涵2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 距离的树 共回答了16个问题
距离的树 共回答了16个问题 |采纳率100%- 反应,草酸的二个氢,电离常数都不小,
KHC2O4+NaOH----kNaC2O4+H2O - 1年前
相关推荐
- 菠菜中含草酸(乙二酸),其味苦涩,能溶于水,水溶液呈酸性.过量食用菠菜,容易造成人体缺钙.食用菠菜前一般先将菠菜用热水焯
菠菜中含草酸(乙二酸),其味苦涩,能溶于水,水溶液呈酸性.过量食用菠菜,容易造成人体缺钙.食用菠菜前一般先将菠菜用热水焯一焯,以降低草酸含量,除去菠菜的苦涩味.由此判断下列说法中,不正确的是( )
A.草酸是一种酸
B.加热可以降低草酸在水中的溶解度
C.草酸的水溶液pH<7
D.草酸能与人体中的钙结合生成难溶于水的物质 chdy88981年前1
chdy88981年前1 -
 liushabo 共回答了14个问题
liushabo 共回答了14个问题 |采纳率71.4%解题思路:A、根据草酸属于酸解答;
B、根据草酸的溶解度随着温度的升高而增大解答;
C、根据草酸水溶液呈酸性,草酸的水溶液的pH小于7解答;
D、根据对草酸具体性质的描述可以减小相关方面的判断.A、草酸是一种酸.正确;
B、由食用菠菜前一般先将菠菜用热水焯一焯,以降低草酸含量可知,草酸的溶解度随着温度的升高而增大.正确;
C、草酸属于酸,其水溶的液pH<7.错误;
D、由过量食用菠菜,容易造成人体缺钙可以推知,草酸能与人体中的钙结合生成难溶于水的物质.正确.
答案:C.点评:
本题考点: 酸的化学性质;固体溶解度的影响因素;溶液的酸碱性与pH值的关系.
考点点评: 解答本题要充分理解物质的性质方面的内容,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 怎样鉴别草酸,丙二酸,丁二酸请用化学方法鉴别
 内蒙古人在海口1年前2
内蒙古人在海口1年前2 -
 大连小连 共回答了22个问题
大连小连 共回答了22个问题 |采纳率86.4%草酸强还原性,使高锰酸钾退色
丙二酸与尿素反应生成沉淀1年前查看全部
- 草酸及氢氧化钠溶液配制的实验报告?
 siyuanvote091年前1
siyuanvote091年前1 -
 wenxin1687 共回答了17个问题
wenxin1687 共回答了17个问题 |采纳率94.1%100ml以下,10.5mol / L氢氧化钠溶液的制备步骤:
(1)计算:10.5mol / L * 0.1L * 40G /摩尔=42.0克(精确到小数点后一位)
(2)体重:托盘天平称氢氧化钠42.0克(快速重)的
(3)溶固体放入小烧杯中,加少量蒸馏水,用玻璃棒
(4)冷却搅拌:室温
(5)转移:100ml量瓶中,用玻璃棒引流到
(6)洗涤:洗涤烧杯用蒸馏水,2-3次玻璃棒,洗涤液也转移到该烧瓶中
(7)摇:摇瓶允许彻底混合
(8)体积:加蒸馏水至刻度,从1-2cm的距离时,用胶头滴管滴加蒸馏水,用刻度线相切的凹面底重合平面观察时.
(9)摇:震荡瓶(方法略)的
(10)装瓶:干燥的试剂瓶倒入干净,标1年前查看全部
- 草酸盐的溶解性表最好能附上盐酸盐的作比较不用稀土金属,主族和常见的过渡就OK了PS:草酸的水溶液最低pH能达到0吗?(2
草酸盐的溶解性表
最好能附上盐酸盐的作比较
不用稀土金属,主族和常见的过渡就OK了
PS:草酸的水溶液最低pH能达到0吗?(20度) yyykkkppp1年前1
yyykkkppp1年前1 -
 孤独豪杰 共回答了24个问题
孤独豪杰 共回答了24个问题 |采纳率91.7%K+ Na+ NH4+ Ca2+ Ba2+ Mg2+ Al3+ Zn2+ Fe3+ Fe2+ Cu2+ Ag+ Cr3+ Pb2+ Mn2+ Hg2+ Hg22+ Sn2+ Sn4+ Cd2+ As3+
草酸盐 水 水 水 HCl HCl 水 HCl HCl HCl HCl HCl HNO3 HCl HNO3 HCl HCl HNO3 HCl 水 HCl
盐酸盐 水 水 水 水 水 水 水 水 水 水 水 不溶 水 沸水 水 水 HNO3 水解,水解,水 水解 HCl HCl HCl
依次对应1年前查看全部
- 草酸在浓流酸催化作用下热分解的化学方程式
 Islamofascism1年前2
Islamofascism1年前2 -
 hgwii 共回答了20个问题
hgwii 共回答了20个问题 |采纳率75%H2C2O4==浓硫酸==CO2↑+CO↑+H2O1年前查看全部
- 下列物质放在水中形成溶液的pH最大的是 草酸 氧化钠 氯化钠 柠檬汁
 lovesdeep1年前4
lovesdeep1年前4 -
 Bachelor_stock 共回答了20个问题
Bachelor_stock 共回答了20个问题 |采纳率90%草酸,柠檬汁是酸性的,水溶液PH小于7
氯化钠溶液是中性的,PH=7
氧化钠与水反应生成氢氧化钠,Na2O+H2O=2NaOH,显碱性,PH大于7
所以PH最大的是氧化钠1年前查看全部
- 草酸和二氧化锰的反应方程式是什么
草酸和二氧化锰的反应方程式是什么
最好写明出处,不要乱写一气,一小时有效现在是2006-8-22-12:00 大白菜01151年前1
大白菜01151年前1 -
 小橙丸子 共回答了30个问题
小橙丸子 共回答了30个问题 |采纳率96.7%MnO2+2H2C2O4=MnC2O4+2CO2+2H2O
参考:采用10%草酸溶液来洗上述试管,在试管中加入草酸溶液,草酸与二氧化锰反应速度很快,过一会儿,就把污迹清除干净了
关于他们的答案不推荐因为:
试管“锰迹”的快速去除法
初三年级学生实验“高锰酸钾加热分解制取氧气”,实验后的试管有二氧化锰黑色残迹存在,由于学生人数多,要处理的试管多,这就需要选择一种较快的洗涤方法.我经过多次试验,最后选择了用草酸除迹,这种方法污染小,速度快.
方法如下:在有锰迹的试管中,加入适量的用硫酸酸化了的草酸溶液,放置在试管架上,不超过三分钟,二氧化锰残迹全部溶解.其反应的方程式如下:
MnO2++H2C2O4+H2SO4=MnSO4+2CO2+2H2O.
如果用浓盐酸加热的方法除二氧化锰,虽然也很快,但会产生氯气,污染环境.1年前查看全部
- 酸性高猛酸钾会把草酸氧化成二氧化碳和什么物质?
 孤独靓女1年前1
孤独靓女1年前1 -
 不辜负家人 共回答了15个问题
不辜负家人 共回答了15个问题 |采纳率93.3%酸性高猛酸钾有强氧化性,与草酸反应,+7价的Mn离子会被还原成+2价的Mn离子,且随着Mn2+的生成,反应速度会越来越快,因为Mn2+可作为该反应的正催化剂.
反应方程为
5H2C2O4+2KMnO4+6(H+)=2(K+)+2(Mn2+)+10CO2(向上的气体符号)+8H2O1年前查看全部
- 一道初中天原杯竞赛题草酸(H2C2O4)受热分解的产物是(?).
 红月雪光1年前1
红月雪光1年前1 -
 实力是底气 共回答了18个问题
实力是底气 共回答了18个问题 |采纳率88.9%HOOCCOOH(加热,浓H2SO4)=H2O+CO2(g)+CO(g)(实验室制CO)
也可用HCOOH(加热,浓H2SO4)=H2O+CO2(g)1年前查看全部
- 将草酸溶液加入碳酸钠溶液中有CO2放出,能不能验证草酸为弱酸
 bj_yc1年前1
bj_yc1年前1 -
 jilin-123 共回答了16个问题
jilin-123 共回答了16个问题 |采纳率87.5%碳酸为弱酸 草酸能与碳酸钠溶液反应放出CO2 这个是不能确实说明草酸为弱酸 而草酸确实是比硫酸 硝酸 盐酸弱的 而与碳酸反应有CO2放出 不一定要是比它强的.1年前查看全部
- 西红柿的酸味来自那种物质?草酸?VC?苹果酸?琥珀酸?马来酸?还是别的什么什么?
 leslier1年前1
leslier1年前1 -
 wildrsoe 共回答了16个问题
wildrsoe 共回答了16个问题 |采纳率87.5%西红柿含有丰富的胡萝卜素、维生素C和B族维生素.还有苹果酸、柠檬酸、果酸和糖类,维生素C可以控制和提高肌体抗癌能力.番茄内的苹果酸和柠檬酸等有机酸,还有增加胃液酸度,帮助消化,调整胃肠功能的作用.番茄中含有果酸,能降低胆固醇的含量,对高血脂症很有益处.当这些有机酸和维生素C的含量高时就会有酸的味道了.1年前查看全部
- 草酸合铁酸盐合成用双氧水做氧化剂的优点?
 bluezi1年前1
bluezi1年前1 -
 流光映雪 共回答了13个问题
流光映雪 共回答了13个问题 |采纳率100%别的氧化剂容易把草酸氧化.而过氧根离子虽然有很强的氧化性,却似乎对有机物的作用偏弱,所以选择过氧化氢比较好.
并且过氧化氢是纯洁的氧化剂,氧化产物只有H2O,不会引入杂质离子,干扰铁离子的络合反应.1年前查看全部
- 有一瓶已知为草酸三氢钾或草酸之一的纯试剂,如何确定之
 pit99971年前1
pit99971年前1 -
 chris_tom 共回答了15个问题
chris_tom 共回答了15个问题 |采纳率73.3%这二者因为存在共同阴离子,所以要区分的话就区分阳离子,钾离子的话可以用焰色反应实验,也可以滴加高氯酸溶液,没有明显现象就是草酸,有白色沉淀就是草酸三氢钾,高氯酸钾常温下溶解度并不大1年前查看全部
- 共轭酸有哪些?醋酸,草酸,柠檬酸都属于共轭酸吗?
 ruoline1年前2
ruoline1年前2 -
 solarjojo 共回答了19个问题
solarjojo 共回答了19个问题 |采纳率89.5%共轭酸是具有特殊组成形态的一种酸,其结构当中的突出特点为共轭结构,
具有这种结构的酸在化学以及生物学上会有一些特殊的性质.按酸碱质子论,酸和碱并不是彼此孤立的,而统一在对质子的关系上,这种关系可以表示为:酸碱 + 质子即,酸给出质子后就成为碱,碱接受质子后就变成酸.满足上述关系的一对酸和碱称为共轭酸碱对.例如HCN-CN就构成了一个共轭酸碱对.HCN是CN的共轭酸.
根据酸碱质子理论,酸是( 质子供给体),碱是( 质子接受体),醋酸,草酸,柠檬酸都属于共轭酸.1年前查看全部
- 为什么弱酸可以制强酸?草酸和硫酸铜反应为什么可以制得硫酸和草酸铜?
 iqvsc1年前3
iqvsc1年前3 -
 大圣12345 共回答了16个问题
大圣12345 共回答了16个问题 |采纳率81.3%弱酸制强酸有两种情形:
1)非氧化还原反应的复分解反应
诚如,楼上那位所述,酸性较强的酸能够制取酸性较弱的酸,是因为较强酸在水溶液中的电离程度大于较弱酸,电离产生的氢离子可以跟较弱酸的酸根根离子结合,形成较难电离的较弱酸分子从体系中“游离”出去,从而导致化学平衡向着生成较弱酸的方向移动.
事实上,弱酸能制取强酸的道理是相同的,也是使整个反应向总的离子浓度减小的方向进行,只不过是由于生成的盐的溶解度实在是很小.
如:CuSO4 + H2S == CuS(沉淀)+ H2SO4等等.
2)氧化还原反应
这纯粹是与反应物和产物的氧化还原性大小有关.氧化还原反应发生的规律:氧化性强的氧化剂 + 还原性强的还原剂 == 氧化性弱的氧化产物 + 还原性弱的还原产物.
如:Cl2 + H2S == S(沉淀)+ 2HCl
H2SO3 + Cl2 == H2SO4 + HCl(未配平)等等.1年前查看全部
- 有机化学一道题草酸二酯为什么草酸二酯最多能与12molNaOH反应?
 sellia11年前1
sellia11年前1 -
 毛神 共回答了15个问题
毛神 共回答了15个问题 |采纳率93.3%和-COO-断键4mol,然后生成2份苯酚,再反应,用2mol1年前查看全部
- 求草酸,盐酸,醋酸,硝酸,硫酸的化学式.
 我的所罗门1年前3
我的所罗门1年前3 -
 会思考了y 共回答了15个问题
会思考了y 共回答了15个问题 |采纳率86.7%H2C2O4
HCL
CH3COOH
HNO3
H2SO41年前查看全部
- 稀醋酸,双氧水,酒精溶液,草酸溶液,高锰酸钾溶液为什么都能去除色素污渍?有没有应用萃取的原理?
 篮颜知己1年前3
篮颜知己1年前3 -
 lk5258 共回答了14个问题
lk5258 共回答了14个问题 |采纳率100%有的,色素一般都是有机物,有机物和有机物之间可以互溶,所以有机物可以溶解色素,并且将它们除去
此外,色素容易被氧化,因此双氧水、高锰酸钾等物质可以出去色素1年前查看全部
- (2014•杭州一模)二元弱酸是分步电离的,25时碳酸和草酸的Ka如表:
(2014•杭州一模)二元弱酸是分步电离的,25时碳酸和草酸的Ka如表:
(l)设有下列四种溶液:H2CO3 Ka1=4.3×10-7 H2C2O4 Ka1=5.6×10-2 Ka2=5.6×10-11 Ka2=5.42×10-5
A.0.1mol•L-1的Na2C2O4溶液B.0.1mol•L-1的NaHC2O4溶液
C.0.1mol•L-1的Na2CO3溶液D.0.1mol的NaHCO3溶液
其中,c(H+)最大的是______,c(OH-)最大的是______.
(2)某化学实验兴趣小组同学向用大理石和稀盐酸制备CO2后残留液中滴加碳酸钠溶液,在溶液中插人pH传感器,测得pH变化曲线如图所示.
刚开始滴人碳酸钠溶液时发生反应的离子方程式为______,BC段发生反应的离子方程式为______,D点时混合溶液中由水电离产生的c(OH-)=______ mol•L-1. 给不起永远1年前1
给不起永远1年前1 -
 梁朝zz 共回答了24个问题
梁朝zz 共回答了24个问题 |采纳率79.2%解题思路:(1)相同条件下,酸的电离平衡常数越大,则酸的酸性越强,酸根离子的水解程度越小,则溶液的碱性越弱;
(2)溶液pH<7,说明溶液呈酸性,酸和碳酸钠溶液反应生成氯化钠和水、二氧化碳,当pH不变时,碳酸钠和氯化钙发生复分解反应,碳酸钠为强碱弱酸盐,其溶液呈碱性,根据水的离子积常数计算氢氧根离子浓度.(1)相同条件下,酸的电离平衡常数越大,则酸的酸性越强,酸根离子的水解程度越小,则溶液中氢氧根离子浓度越小,氢离子浓度越大,根据电离平衡常数知,酸性强弱顺序是:草酸>草酸氢根离子>碳酸>碳酸氢根离子,离子水解强弱顺序是:碳酸根离子>碳酸氢根离子>草酸根离子>醋酸氢根离子,
根据离子水解程度知,草酸氢根离子水解程度最小,则其溶液碱性最弱,氢离子浓度最大,所以氢离子浓度最大的是B,水解程度最强的是C,则溶液C中碱性最强,氢氧根离子浓度最大,
故答案为:B;C;
(2)溶液pH<7,说明溶液呈酸性,酸和碳酸钠溶液反应生成氯化钠和水、二氧化碳,离子方程式为:2H++CO32-=H2O+CO2↑,当pH不变时,碳酸钠和氯化钙发生复分解反应,离子方程式为Ca2++CO32-=CaCO3↓,碳酸钠为强碱弱酸盐,其溶液呈碱性,D点时混合溶液中由水电离产生的c(OH-)=
10−14
10−10mol/L=10-4 mol/L,
故答案为:2H++CO32-=H2O+CO2↑;Ca2++CO32-=CaCO3↓;10-4.点评:
本题考点: 弱电解质在水溶液中的电离平衡;离子方程式的书写.
考点点评: 本题考查了盐类水解,明确弱酸的电离平衡常数与酸根离子水解程度的关系是解本题关键,难点是(2)题,会根据曲线变化趋势确定发生的反应,结合溶液中溶质的性质来分析解答,难度中等.1年前查看全部
- 稀硝酸呈什么颜色?将无色的饱和草酸溶液和无色的饱和硝酸钙溶液混合在一起后颜色是否改变?
 蚊子的dd二号1年前2
蚊子的dd二号1年前2 -
 fsharp 共回答了18个问题
fsharp 共回答了18个问题 |采纳率88.9%稀硝酸呈无色,浓的就是黄色了.
草酸钙calcium oxalate
化学式CaC2O4 分子量128.10 白色晶体粉末.不溶于水、醋酸,溶于稀盐酸或稀硝酸.灼烧时转变成碳酸钙或氧化钙.由钙盐水溶液与草酸作用制得.用于陶瓷上釉、制草酸等.味道是弱酸的
所以,楼上的是错误的!1年前查看全部
- 草酸和氯化钙的反应是否发生,生成的草酸钙会不会又和盐酸发生强酸制弱酸的反应
草酸和氯化钙的反应是否发生,生成的草酸钙会不会又和盐酸发生强酸制弱酸的反应
如此不断循环下去 葡萄3151年前5
葡萄3151年前5 -
 玻璃心_碎碎 共回答了22个问题
玻璃心_碎碎 共回答了22个问题 |采纳率95.5%CaCl2 + H2C2O4 = CaC2O4 + 2HCl
反应生成的盐酸会使沉淀又溶解,所以在酸性较强时,这个陈淀反应进行的不完全;要想使其沉淀完全,需要加入氨水,中和生成的HCl1年前查看全部
- 草酸 苯甲酸是弱酸吗 草酸根 苯甲酸根与氢离子不共存?
 web791年前1
web791年前1 -
 menglanllffll 共回答了19个问题
menglanllffll 共回答了19个问题 |采纳率89.5%草酸算是中度酸性,苯甲酸是弱酸.这两种酸理论上都可以与氢离子共存(所有的酸都可与氢离子共存,否则不表现为酸性)
但是,由于并不是强酸,所以不能与氢离子大量共存!
其中,草酸的酸性要比苯甲酸的酸性强,苯甲酸可以说有些有机物的性质了~1年前查看全部
- 三草酸合铁酸钾如何测草酸根含量
 rebecca9251年前1
rebecca9251年前1 -
 苍耳刺 共回答了10个问题
苍耳刺 共回答了10个问题 |采纳率90%1.制备三草酸根合铁(III)酸钾
称取6克草酸钾置于100mL烧杯中,注入10mL蒸馏水,加热,使草酸钾全部溶解,继续加热至近沸时,边搅拌边加入4mL三氯化铁溶液(0.40g / mL).将此液置于冰水中冷却至5℃以下,即有大量晶体析出,以布氏漏斗抽滤,得粗产品.
将粗产品溶于10mL热的蒸馏水中,趁热过滤,将滤液在冰水中冷却,待结晶完全后,抽滤,并用少量冰蒸馏水洗涤晶体.取下晶体,用滤纸吸干,并在空气中干燥片刻,称重,计算得率.
2.C2O42– 含量的测定:
精确称取0.18~0.20g K3[Fe(C2O4)3]·3H2O(精确至±0.0002g)于250mL锥形瓶中,加入50mL水溶解,再加12mL 1:5 H2SO4,加热至70~80℃左右,用0.15mol / L KMnO4标准溶液滴定至浅红色,30秒钟不褪色为止.记下读数,计算结果.平行二份.(要求级差≤0.4%)1年前查看全部
- (2010•江苏二模)草酸(H2C2O4)是一种重要的化工原料.已知常温下0.01mol•L-1的H2C2O4、KHC2
(2010•江苏二模)草酸(H2C2O4)是一种重要的化工原料.已知常温下0.01mol•L-1的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示.
(1)在其它条件不变时,下列措施能使KHC2O4溶液中c(K+):c(HC2O4-)接近1:1的是______(填字母).H2C2O4 KHC2O4 K2C2O4 pH 2.0 3.1 8.1
A.加入适量的H2C2O4 B.加入适量的KHC2O4
C.加入适量的Na2C2O4D.升高溶液的温度
(2)取一定质量H2C2O4•2H2O和KHC2O4的混合物,加水溶解,配成250mL溶液,取两份此溶液各25mL,向第一份溶液中先加入几滴酚酞试液,再滴加0.25mol•L-1 NaOH溶液至20.00mL时,溶液由无色变为浅红色;向第二份溶液中滴加适量3mol•L-1 H2SO4溶液酸化后,用0.10mol•L-1 KMnO4溶液滴定,当消耗KMnO4溶液16.00mL时,溶液由无色变为浅紫红色.请回答下列问题:
①完成离子方程式:5C2O42-+2Mn04-+16H+═10______+2Mn2++8H2O.
②原混合物中H2C2O4•2H2O和KHC2O4的物质的量之比为______.
(3)某实验小组用如图所示的装置探究FeC2O4•2H2O在隔绝空气条件下受热分解的产物.当36D0g FeC2O4•2H2O充分反应后,残留固体质量为13.6g,浓硫酸增重7.2g,碱石灰增重11.0g.求残留固体的成分和物质的量.(已知FeC2O4•2H2O的相对分子质量为180;设反应产生的气体被充分吸收) 路_渐行渐远1年前1
路_渐行渐远1年前1 -
 sqhkjy 共回答了16个问题
sqhkjy 共回答了16个问题 |采纳率87.5%解题思路:(1)依据KHC2O4溶液显酸性可知,溶液中电离大于水解,选择抑制电离的试剂;
A、H2C2O4 分步电离显酸性,可以抑制HC2O4-离子的电离;
B、加入KHC2O4仍然离子浓度是大于1:1;
C、加入适量的Na2C2O4,可以抑制 HC2O4-离子的电离;
D、升温促进电离;
(2)①依据电子守恒、电荷守恒和原子守恒配平写出;
②依据原子守恒和化学方程式计算得到;
(3)最后被点燃的为一氧化碳气体,浓硫酸增重7.2g为水,碱石灰增重11.0g为二氧化碳气体.依据反应生成的物质在过程中的质量分别计算得到;(1)图表分析,KHC2O4溶液显酸性可知,溶液中电离大于水解,选择抑制HC2O4-离子电离的试剂;
A、H2C2O4 分步电离显酸性,可以抑制HC2O4-离子的电离,KHC2O4溶液中c(K+):c(HC2O4-)接近1:1;故A符合;
B、加入KHC2O4仍然离子浓度是大于1:1;故B不符合;
C、加入适量的Na2C2O4,可以抑制 HC2O4-离子的电离,KHC2O4溶液中c(K+):c(HC2O4-)接近1:1;故C符合;
D、升温促进电离,KHC2O4溶液中c(K+):c(HC2O4-)大于1:1;故D不符合;
故答案为:AC;
(2)①依据原子守恒得到为CO2;故答案为:CO2;
②25mL中,设xmol H2C2O4•2H2O ymol KHC2O4根据滴定的,可以得出:2x+y=0.25×0.02
根据氧化还原的,可以得出:x+y=0.1×0.016×2.5,x=0.001,y=0.003mol,所以原混合物中H2C2O4•2H2O和KHC2O4的物质的量之比为1:3;故答案为:1:3;
(3)被点燃的气体为CO,质量为m(CO)=36.0 g-13.6 g-7.2 g-11.0 g=4.2 g;
又FeC2O4•2H2O为0.2 mol,n(H2O)=7.2 g÷18 g/mol=0.4 mol,
n(CO2)=11.0 g÷44 g/mol=0.25 mol,n(CO)=4.2 g÷28 g/mol=0.15 mol,
所以,残留固体中所含元素及物质的量为n(Fe)=0.2 mol,n(O)=0.15 mol,
则残留固体为Fe和FeO的混合物,其中Fe为0.05 mol,FeO为0.15 mol;
故答案为:Fe为0.05 mol,FeO为0.15 mol;点评:
本题考点: 影响盐类水解程度的主要因素;氧化还原反应方程式的配平.
考点点评: 本题考查了盐类水解和弱电解质电离的相对大小比较,平衡移动方向的判断,氧化还原反应离子方程式的配平方法,实验过程的计算应用,题目难度中等.1年前查看全部
- 某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如图所示:
某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如图所示: 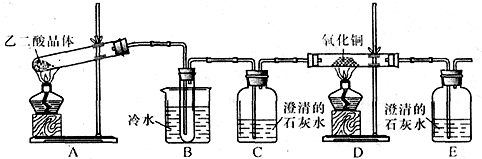
查阅资料可知:乙二酸晶体(H 2 C 2 O 4 •2H 2 O)熔点100.1℃,草酸钙是难溶于水的白色固体;Cu 2 O能溶于稀硫酸,立即发生歧化反应生成Cu 2+ 和Cu.
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:______;
(2)装置B的作用是______;上述装置中有两处需要改进(假设洗气装置每次吸收气体均完全),改进方法是______;______.
(3)实验结束后向装置B的试管中加入NaHCO 3 溶液,产生大量无色气体,由此可以证明两种物质的酸性强弱顺序是______.
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu 2 O的混合物.实验小组进一步探究:①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是______.②取6.8g红色固体与足量的稀硝酸反应,收集到标准状况下的NO气体1.12L.则红色固体中含单质铜的质量分数是______. chenhufen1年前1
chenhufen1年前1 -
 wjhlc 共回答了17个问题
wjhlc 共回答了17个问题 |采纳率82.4%(1)C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,说明乙二酸晶体加热生成一氧化碳、二氧化碳和水,反应的化学方程式:H 2 C 2 O 4 •2H 2 O
△
.
CO↑+CO 2 ↑+3H 2 O;
故答案为:H 2 C 2 O 4 •2H 2 O
△
.
CO↑+CO 2 ↑+3H 2 O;
(2)乙二酸可以和氢氧化钙发生反应,所以防止对检验分解产物CO 2 的干扰,要除去生成物中带出的乙二酸蒸汽,一氧化碳在还原氧化铜之前要将气体干燥,一氧化碳有毒,所以要进行尾气处理,
故答案为:除去生成物中带出的乙二酸蒸汽,防止对检验分解产物CO 2 的干扰;在C与D之间再装配一个盛浓硫酸的洗气瓶(或装有碱石灰的干燥管),将装置E中出来的气体引到酒精灯火焰上让其燃烧(或收集装置E中逸出的尾气);
(3)B的试管中是乙二酸,加入NaHCO 3 溶液,产生大量无色气体应该是二氧化碳,化学反应遵循强酸制弱酸的原理,所以酸性是乙二酸大于碳酸(或H 2 C 2 O 4 >H 2 CO 3 ),故答案为:乙二酸大于碳酸(或H 2 C 2 O 4 >H 2 CO 3 );
(4)①金属铜和硫酸不反应,但是氧化亚铜可以和硫酸反应生成金属铜和硫酸铜,根据实验现象:溶液变为蓝色,则证明红色固体中含有Cu 2 O,故答案为:红色固体中含有Cu 2 O;
②设红色固体中氧化亚铜的物质的量是x,金属铜的物质的量为y,根据质量关系得:144x+64y=6.8,根据电子守恒,得出:2x+2y=
1.12L
22.4L/mol ×(5-2),两式联立解得x=0.025mol,y=0.05mol,所以Cu的质量分数为:
0.05mol×64g/mol
6.8g ×100%=50%,故答案为:50%.1年前查看全部
- 某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如图所示:
某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如图所示:
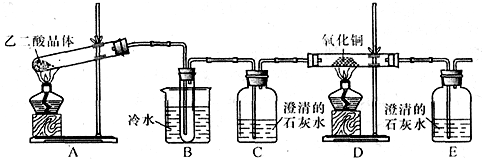
查阅资料可知:乙二酸晶体(H2C2O4•2H2O)熔点100.1℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu.
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:H2C2O4•2H2O
CO↑+CO2↑+3H2OH2C2O4•2H2O△ .
CO↑+CO2↑+3H2O;△ .
(2)装置B的作用是除去生成物中带出的乙二酸蒸汽,防止对检验分解产物CO2的干扰除去生成物中带出的乙二酸蒸汽,防止对检验分解产物CO2的干扰;上述装置中有两处需要改进(假设洗气装置每次吸收气体均完全),改进方法是在C与D之间再装配一个盛浓硫酸的洗气瓶(或装有碱石灰的干燥管)在C与D之间再装配一个盛浓硫酸的洗气瓶(或装有碱石灰的干燥管);将装置E中出来的气体引到酒精灯火焰上让其燃烧(或收集装置E中逸出的尾气)将装置E中出来的气体引到酒精灯火焰上让其燃烧(或收集装置E中逸出的尾气).
(3)实验结束后向装置B的试管中加入NaHCO3溶液,产生大量无色气体,由此可以证明两种物质的酸性强弱顺序是乙二酸大于碳酸(或H2C2O4>H2CO3)乙二酸大于碳酸(或H2C2O4>H2CO3).
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu2O的混合物.实验小组进一步探究:①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是红色固体中含有Cu2O红色固体中含有Cu2O.②取6.8g红色固体与足量的稀硝酸反应,收集到标准状况下的NO气体1.12L.则红色固体中含单质铜的质量分数是50%50%. 为了车票的vv1年前1
为了车票的vv1年前1 -
 tctc022 共回答了23个问题
tctc022 共回答了23个问题 |采纳率95.7%(1)C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,说明乙二酸晶体加热生成一氧化碳、二氧化碳和水,反应的化学方程式:H2C2O4•2H2O
△
.
CO↑+CO2↑+3H2O;
故答案为:H2C2O4•2H2O
△
.
CO↑+CO2↑+3H2O;
(2)乙二酸可以和氢氧化钙发生反应,所以防止对检验分解产物CO2的干扰,要除去生成物中带出的乙二酸蒸汽,一氧化碳在还原氧化铜之前要将气体干燥,一氧化碳有毒,所以要进行尾气处理,
故答案为:除去生成物中带出的乙二酸蒸汽,防止对检验分解产物CO2的干扰;在C与D之间再装配一个盛浓硫酸的洗气瓶(或装有碱石灰的干燥管),将装置E中出来的气体引到酒精灯火焰上让其燃烧(或收集装置E中逸出的尾气);
(3)B的试管中是乙二酸,加入NaHCO3溶液,产生大量无色气体应该是二氧化碳,化学反应遵循强酸制弱酸的原理,所以酸性是乙二酸大于碳酸(或H2C2O4>H2CO3),故答案为:乙二酸大于碳酸(或H2C2O4>H2CO3);
(4)①金属铜和硫酸不反应,但是氧化亚铜可以和硫酸反应生成金属铜和硫酸铜,根据实验现象:溶液变为蓝色,则证明红色固体中含有Cu2O,故答案为:红色固体中含有Cu2O;
②设红色固体中氧化亚铜的物质的量是x,金属铜的物质的量为y,根据质量关系得:144x+64y=6.8,根据电子守恒,得出:2x+2y=
1.12L
22.4L/mol×(5-2),两式联立解得x=0.025mol,y=0.05mol,所以Cu的质量分数为:
0.05mol×64g/mol
6.8g×100%=50%,故答案为:50%.1年前查看全部
- pH=0时草酸在水中主要以什么形态存在?
 summeryhx1年前3
summeryhx1年前3 -
 jinsuicard 共回答了14个问题
jinsuicard 共回答了14个问题 |采纳率85.7%弱酸弱碱在水中电离极少,所谓越稀越水解,能电离2%已经很了不得了,主要存在形态当然是草酸分子了.
另外,正如我所说的,越稀越水解,永远不可能有pH=0的草酸溶液,除非这个溶液里加了其他酸溶液.1年前查看全部
- 大学无机化学中,草酸溶液配制实验的有关问题
大学无机化学中,草酸溶液配制实验的有关问题
大学无机化学实验中,在配制草酸标准溶液时,称量草酸的量一定要称准到浓度为0.05000mol.dm^3的计算量吗?
我想不通的是,连实验时必须要用的仪器容量瓶的精度都达不到小数点后5位,称量量即使真的能够达到计算量又有什么必要呢?计算时对有效数字的选取不是应该以精确度最低的因素为标准么? wacjy1年前1
wacjy1年前1 -
 wx221 共回答了18个问题
wx221 共回答了18个问题 |采纳率94.4%称量草酸的量不一定要称准到计算量,配制草酸标准溶液后需要标定,标定的计算值要保留小数点后4-5位.1年前查看全部
- 草酸氢根电离水解哪个强?
 少年游3331年前1
少年游3331年前1 -
 loveyouverymuch 共回答了11个问题
loveyouverymuch 共回答了11个问题 |采纳率90.9%草酸氢根的电离大于水解.草酸氢根的电离常数:Ka2=5.42*10^-5,而草酸氢根的水解常数为:Kh2=1.79*10^-13,所以草酸氢盐水溶液呈酸性!1年前查看全部
- (2012•邯郸二模)晚会中现场观众手持被称为“魔棒”的荧光棒营造了很好的氛围,“魔棒”发光原理是利用过氧化氢氧化草酸二
(2012•邯郸二模)晚会中现场观众手持被称为“魔棒”的荧光棒营造了很好的氛围,“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式为:

下列说法正确的是( )
A.CPPO属于芳香族化合物
B.CPPO属于高分子化合物
C.1mol CPPO与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4 mol NaOH
D.1mol CPPO与氢气完全反应,需要氢气10mol LOVE简1年前1
LOVE简1年前1 -
 amanda1982334 共回答了17个问题
amanda1982334 共回答了17个问题 |采纳率100%A.含苯环,则CPPO属于芳香族化合物,故A正确;
B.其相对分子质量在10000以下,不属于高分子化合物,故B错误;
C.含-COOC-与NaOH溶液反应,且水解生成的苯酚结构也与NaOH反应,则1mol CPPO与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗6mol NaOH,故C错误;
D.只有苯环与氢气发生加成反应,则1mol CPPO与氢气完全反应,需要氢气6mol,故D错误;
故选A.1年前查看全部
- 水中碳酸氢根离子Hco3主要以CaH2co3的形式存在,那在水中加入草酸H2C2O4后除了形成草酸钙CaC2o4还有?
水中碳酸氢根离子Hco3主要以CaH2co3的形式存在,那在水中加入草酸H2C2O4后除了形成草酸钙CaC2o4还有?
草酸去除水中钙离子后,Hco3缓冲物质是否跟着消失了?草酸与碳酸氢钙CaH2co3的反应的方程式是什么? 我是一只海鸥1年前2
我是一只海鸥1年前2 -
 顺手一枪 共回答了15个问题
顺手一枪 共回答了15个问题 |采纳率100%H2C2O4+Ca(HCO3)2=CaC2O4+2H2O+2CO2;
在这个反应方程中,Hco3缓冲物质反应消失了,但是水中的Hco3缓冲物质是不可能完全 被除去的.1年前查看全部
- 用naoh标准溶液滴定草酸时,为什么使用甲基橙试剂不合适
 wo52082421年前1
wo52082421年前1 -
 黑猫猪脚 共回答了27个问题
黑猫猪脚 共回答了27个问题 |采纳率96.3%终点产物是草酸钠,强大弱酸盐,显碱性,要求在碱性范围内变色,
而甲基橙的变色范围是 3.1----4.4,是酸性的,不合适.1年前查看全部
- 为什么草酸能使酸性高锰酸钾褪色而丁二酸却不行?
 KissMarlboro1年前4
KissMarlboro1年前4 -
 waj99 共回答了17个问题
waj99 共回答了17个问题 |采纳率94.1%因为乙二酸是由两个羧基直接相连而成,
羧基上的羰基氧吸电子能力很强,
所以都向各自的方向拉扯碳碳键,
最终容易被氧化而断键,
HOOC-COOH断裂为两分子CO2.
丁二酸等二元酸没有这种特殊结构,
因而不能!1年前查看全部
- (7分)类比法是化学研究物质的重要方法之一。草酸(C 2 H 2 0 4 )的化学性质与碳酸相似,草酸受热会分解得到三种
(7分)类比法是化学研究物质的重要方法之一。草酸(C 2 H 2 0 4 )的化学性质与碳酸相似,草酸受热会分解得到三种氧化物,某兴趣小组对草酸的有关性质进行了探究,按要求回答相关的问题:
[提出猜想](1)草酸能够使紫色石蕊试液变为 色。
(2)三种氧化物可能是 ,该猜想的依据是 。
[查阅资料]
1.无水硫酸铜是一种白色粉末物质,遇水变成蓝色的硫酸铜晶体。
2.向氯化钯溶液中通入CO,产生黑色沉淀。
[实验探究]兴趣小组为验证猜想,将草酸受热后得到的气体,依次通过了装置A、B、C: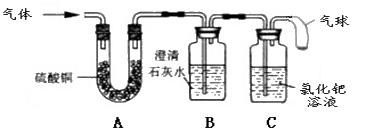
[实验结论](3)当装置A、B、C实验现象是 ,证明猜想是正确的。
[实验反思](4)①实验装置中气球所起的作用是 。
②是否可以将装置A和B对调,其理由是 。 gshengyi1年前1
gshengyi1年前1 -
 阿其郎 共回答了15个问题
阿其郎 共回答了15个问题 |采纳率86.7%[提出猜想](1)红 (2)CO 2 H 2 O CO;元素守恒
[实验结论](3) A种白色固体变为蓝色,B中澄清石灰水变浑浊,C中出现黑色沉淀(2分)
[实验反思](4)①调节C装置容积和收集气体(防CO扩散)
②不可以对调,其理由是气体若先通入B,会将溶液中的水带出,干扰水的检验。
1年前查看全部
- 被称为“魔棒”的荧光棒已成为节日之夜青少年的喜爱之物,其发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物
被称为“魔棒”的荧光棒已成为节日之夜青少年的喜爱之物,其发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光.草酸二酯(cppo)结构简式为:下列有关说法不正确的是( )

a.发光的魔棒不能凑近石油气之类的可燃性气体,否则会导致***
b.草酸二酯的分子式为:c26h24o8cl6
c.如果在发光中途,把它放入冰箱的冷冻室中,发光便会停止或基本停止
d.1molcppo与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4molnaoh lsmgy1年前1
lsmgy1年前1 -
 sldlh40 共回答了23个问题
sldlh40 共回答了23个问题 |采纳率91.3%解题思路:A.荧光不会引爆可燃物;
B.根据结构简式判断分子式;
C.从温度对反应速率的影响判断;
D.能与NaOH反应官能团有酯基,注意水解生成酚羟基.A.这是一种荧光,属冷光,不会引爆可燃性气体,故A错误;
B.由结构简式可知分子中含有26个C、24个H、8个O、6个Cl,则分子式为C26H24O8Cl6,故B正确;
C.它通过化学反应产生荧光,温度过低,化学反应速率慢,故C正确;
D.1 mol该物质可与6 mol NaOH反应(注意酚羟基也和NaOH反应),故D错误.
故选AD.点评:
本题考点: 有机物的结构和性质.
考点点评: 本题考查有机物的结构和性质,题目难度中等,本题注意酯基水解的产物,为该题的易错点.1年前查看全部
- 碘滴定As2O5AgNO3滴定Cl—高锰酸钾滴定草酸EDTA滴定Bi硫氰化铵滴定Ag+
 tomick1年前2
tomick1年前2 -
 夜的风很凉 共回答了14个问题
夜的风很凉 共回答了14个问题 |采纳率85.7%1.你在开玩笑?As是5价,怎么用碘滴定?1若为碘离子的话,理论上pH小于8即可(根据能斯特方程推电位),实际上用氟化铵和氢氟酸的缓冲溶液调节pH,同时还可以掩蔽三价铁.2.无需外加pH调节物,直接用标准AgNO3溶液即可.指示...1年前查看全部
- 如何用实验证明草酸分解式
 白花争妍1年前1
白花争妍1年前1 -
 回忆丢了 共回答了18个问题
回忆丢了 共回答了18个问题 |采纳率88.9%草酸在189.5℃或遇浓硫酸会分解生成二氧化碳、一氧化碳和水.
HOOCCOOH====CO2↑+CO↑+H2O
先将生成气体通入无水硫酸铜,变蓝,证明含有H2O,再通过澄清石灰水证明含有CO2,通入NaOH溶液除尽CO2,将气体点燃,生成气体通入澄清石灰水变浑浊,则含有CO1年前查看全部
- (2014•抚州模拟)乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素的原料之一,可用草酸(HOOCCOOH)电解制
 (2014•抚州模拟)乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素的原料之一,可用草酸(HOOCCOOH)电解制备,装置如图所示.下列说法不正确的是( )
(2014•抚州模拟)乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素的原料之一,可用草酸(HOOCCOOH)电解制备,装置如图所示.下列说法不正确的是( )
A.电解时石墨电极应与直流电源的正极相连
B.阴极反应式为:HOOCCOOH+2H++2e-═OHCCOOH+H2O
C.电解时石墨电极上有O2放出
D.电解一段时间后,硫酸溶液的pH不变化 lemontutu1年前1
lemontutu1年前1 -
 vepje 共回答了20个问题
vepje 共回答了20个问题 |采纳率90%解题思路:草酸(HOOCCOOH)在阴极上得电子生成OHCCOOH,阳极上氢氧根离子失电子生成氧气,电池总反应为2HOOCCOOH═2OHCCOOH+O2↑,根据溶质的变化分析溶液的PH的变化.A、草酸(HOOCCOOH)在阴极上得电子生成OHCCOOH,则复合膜电极为阴极,石墨为阳极与直流电源的正极相连,故A正确;
B、草酸(HOOCCOOH)在阴极上得电子生成OHCCOOH,阴极反应式为:HOOCCOOH+2H++2e-═OHCCOOH+H2O,故B正确;
C、石墨为阳极,阳极上氢氧根离子失电子生成O2,故C正确;
D、电池总反应为2HOOCCOOH═2OHCCOOH+O2↑,溶质由草酸变为乙醛酸,反应后溶液的酸性减弱,则pH变大,故D错误;
故选D.点评:
本题考点: 电解原理.
考点点评: 本题考查了电解池原理的应用,明确阴阳极的判断方法是解题的关键,题目难度中等,注意根据电池总反应判断溶液的PH的变化.1年前查看全部
- 求解几道高中化学反应方程式1.氯气与硫代硫酸钠溶液:2.酸性高锰酸钾溶液与草酸溶液:3.次氯酸钠与尿素反应,生成物除盐外
求解几道高中化学反应方程式
1.氯气与硫代硫酸钠溶液:
2.酸性高锰酸钾溶液与草酸溶液:
3.次氯酸钠与尿素反应,生成物除盐外,都是能参与大气循环的物质: 来生请你爱我1年前5
来生请你爱我1年前5 -
 alva1983 共回答了11个问题
alva1983 共回答了11个问题 |采纳率100%1、Na2S2O3+4Cl2+5H2O=2NaCl+2H2SO4+6HCl
2、2KMnO4+5K2C2O4+8H2SO4=6K2SO4+2MnSO4+10CO2↑+8H2O
3、3NaClO+NH2CONH2+2NaOH==N2↑+3H2O+Na2CO3+3NaCl1年前查看全部
- 固体草酸(H2C2O4)受热分解生成碳的氧化物和水,写出该反应的化学方程式
 q7bt1年前2
q7bt1年前2 -
 晓莜 共回答了21个问题
晓莜 共回答了21个问题 |采纳率90.5%H2C2O4=加热=H2O+CO2↑+CO↑1年前查看全部
- 利用鸡蛋壳与草酸中和制备草酸钙,如何检验生成物是草酸钙
 我要开始行动1年前1
我要开始行动1年前1 -
 他猪 共回答了21个问题
他猪 共回答了21个问题 |采纳率100%检验是否有草酸钙可以向溶液中加入高锰酸钾溶液 看是否褪色
还有一个方法我觉得应该可以
灼烧草酸钙固体后会生成碳酸钙,加入盐酸若有令澄清石灰水变浑浊的气体即CO2产生可验证存在
第一个方法应该可以,草酸根可以被氧化1年前查看全部
- 草酸氢根和氢氧根反应么?如果要反应 那么离子方程式是什么
 pick451年前1
pick451年前1 -
 517098006 共回答了8个问题
517098006 共回答了8个问题 |采纳率87.5%HC2O4(-)+OH(-)=C2O4(2-)+H2O1年前查看全部
- (2008•镇江)草酸晶体(H2C2O4•2H2O)熔点较低,加热会熔化、气化和分解.草酸(H2C2O4)受热会分解,它
(2008•镇江)草酸晶体(H2C2O4•2H2O)熔点较低,加热会熔化、气化和分解.草酸(H2C2O4)受热会分解,它与氢氧化钙的反应为:H2C2O4+Ca(OH)2=CaC2O4↓(白色)+2H2O.
甲、乙两同学对草酸受热分解的产物作如下探究:
(1)猜想与假设:第一种:草酸分解生成CO2和H2;第二种:草酸分解生成CO2、CO和H2O;
第三种:草酸分解:H2C2O4→CO2↑+H2O(未配平);
有同学从理论上就可判断第三种假设不成立,老师也认为这一判断是正确的,该同学判断的理论依据是______.
(2)设计与实验:
甲、乙两同学分别设计了下图所示的A、B两套实验装置(图中铁架台略去).
①甲同学按A装置实验,观察到澄清石灰水变浑浊,认为此现象是由草酸晶体受热分解产生的CO2所导致,此判断______(填“严密”或“不严密”).
②乙同学的B装置图方框内的仪器未画完整,请你帮他画完整(直接画在图上或答题卡上).
乙同学按B装置实验,看到无水硫酸铜由白变蓝,洗气瓶中溶液变浑浊.在尖嘴管口点燃剩余气体,火焰上方罩一个______烧杯,有白色固体生成,证明产物中有______;换一个干、冷烧杯罩在火焰上方,内壁无现象,证明产物中无H2.
(3)结论与思考:
①草酸受热分解的化学方程式为:H2C2O4
CO2↑+CO↑+H2O(2分);加热 ..H2C2O4.
CO2↑+CO↑+H2O(2分);加热 ..
②若省略B装置方框内的仪器,整套装置也能证明产物中有CO2(假设每步都反应完全),方法是:______. ujdf21年前1
ujdf21年前1 -
 zpp402423 共回答了12个问题
zpp402423 共回答了12个问题 |采纳率100%解题思路:猜想生成物首先考虑元素化合价反应前后肯定有升高的也又降低的,再根据图中设计的实验和二氧化碳的性质解决其它题目.(共8分)
(1)酸受热分解若只生成二氧化碳和水,氢氧元素化合价不变,而碳元素化合价升高,所以反应后应有化合价降低的元素,所以(1)答案:(1)无法进行配平、配不平或不符合质量守恒定律或只有化合价的升高,无化合价的降低(1分).
(2)烧杯敞口放置在空气中空气中也有二氧化碳,时间长了烧杯内的澄清石灰水也会变浑浊,故答案:①不严密(1分)注意洗气瓶要长进短出,进气的导管要浸没液体中,出气导管只要刚刚露出橡皮塞.故答案②如右下图(长管不伸入液面下不给分,不作美观要求)(1分)
因为无水硫酸铜由白变蓝,洗气瓶中溶液变浑浊,所以草酸受热分解肯定生成二氧化碳和水,但都被吸收.到最后点燃的是一氧化碳,燃烧生成二氧化碳.故答案:内壁附有澄清石灰水(其它合理答案均给分)(1分)CO(1分)
(3)根据实验现象和前面的分析知草酸受热分解生成二氧化碳、一氧化碳、水.故答案:①H2C2O4
△
.
CO2↑+CO↑+H2O(2分);
二氧化碳能和碱石灰中的氢氧化钠反应,虽没现象但干燥管因吸收它质量增加.故答案:②称量实验前后盛有碱石灰的干燥管的质量(意思相近的表述均给分)(1分)点评:
本题考点: 实验探究物质的性质或变化规律;化学实验方案设计与评价;化学方程式的配平;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题是实验探究题,综合考查到了质量守恒定律、物质的性质、化学用语相关知识.1年前查看全部
- “魔棒”常被用于晚会现场气氛的渲染。其发光原理是利用H 2 O 2 氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出
“魔棒”常被用于晚会现场气氛的渲染。其发光原理是利用H 2 O 2 氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)的结构简式为 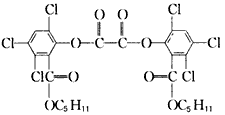
下列有关说法不正确的是 [ ]A.1 mol草酸二酯最多可与6mol氢气发生加成反应
B.草酸二酯的分子式为C 26 H 23 O 8 Cl 6
C.草酸二酯中的C 5 H 11 有8种同分异构体
D.草酸二酯可与NaOH溶液发生取代反应 chen4121年前1
chen4121年前1 -
 舞误_mm 共回答了21个问题
舞误_mm 共回答了21个问题 |采纳率90.5%B1年前查看全部
- PH为4,含有0.1摩尔每升的草酸溶液和0.01摩尔每升的EDTA的溶液中的草酸钙...
PH为4,含有0.1摩尔每升的草酸溶液和0.01摩尔每升的EDTA的溶液中的草酸钙...
PH为4,含有0.1摩尔每升的草酸溶液和0.01摩尔每升的EDTA的溶液中的草酸钙的溶解度 **yy9111年前2
**yy9111年前2 -
 六海光 共回答了15个问题
六海光 共回答了15个问题 |采纳率93.3%此例涉及到的沉淀副反应有:EDTA对钙离子的络合效应,草酸根对钙的同离子效应,酸度对草酸根的酸效应.同时,在计算EDTA对钙的络合效应系数时还要考虑酸度对EDTA的酸效应:
(1)PH=4,EDTA的lgaY(H)=8.44,即[Y]=0.010/10^(8.44)=10^(-10.44)
K(CaY)=10^(10.69)
(2)络合效应系数:aCa(Y)=1+K(CaY)*[Y]=2.78
(3)PH=4.0时,草酸根酸效应分数d(草)=0.392,C(草)=0.10mol/L,[C2O42-]=0.0392mol/L
(4)Ksp=10^(-8.7)
s=C(Ca)=Ksp*aCa(Y) /[C2O42-]=1.41*10^(-7) mol/L1年前查看全部
- 高锰酸钾浓度0.0186mol/L,滴定5mL草酸水用量10.4mL,求草酸根质量浓度?
 三十三不立1年前1
三十三不立1年前1 -
 怡然萱草 共回答了17个问题
怡然萱草 共回答了17个问题 |采纳率88.2%高锰酸钾和草酸反应方程式如下:2MnO4- + 5H2C2O4 +6H +=2Mn2+ + 10CO2↑ +8H2O
n(MnO4-)=0.0186*10.4*10^-3=1.9344*10^-4 mol
因为2/(1.9344*10^-4)=5/n(H2C2O4),所以草酸的物质的量为4.835*10^-4 mol,
所以草酸的浓度为4.835*10^-4 /(5*10^-3)=0.0967mol/L1年前查看全部
- 称取软锰矿试样0.5000g,加入0.7500gH2C2O4·2H2O及稀硫酸,加热至反应完全.过量的草酸用30.00m
称取软锰矿试样0.5000g,加入0.7500gH2C2O4·2H2O及稀硫酸,加热至反应完全.过量的草酸用30.00mL0.02000mol/L的KMnO4溶液滴定至终点,求软锰矿的氧化能力(以已知)(8分)
 c1dt1ybg1年前1
c1dt1ybg1年前1 -
 youbear 共回答了24个问题
youbear 共回答了24个问题 |采纳率91.7%哦,擅长领域还是化学的呢?!
5H2C2O4.2H2O :2KMnO4
5*126.07 2
X 30/1000*0.02 X = 5*126.07*0.02/2/1000 = 0.1891g
MnO2 :H2C2O4.2H2O
86.94 126.07
Y 0.1891 Y = 86.94*0.1891/126.07 = 0.1304g
……1年前查看全部
- 苯环的判断草酸二脂怎么不含苯环?结构间式中不是标有苯环么?如何通过结构间式判断有无苯环.谁能帮帮忙,那草酸二脂为什么不属
苯环的判断
草酸二脂怎么不含苯环?结构间式中不是标有苯环么?如何通过结构间式判断有无苯环.谁能帮帮忙,
那草酸二脂为什么不属于芳香族化合物? 成都第一qq1年前2
成都第一qq1年前2 -
 迪76 共回答了16个问题
迪76 共回答了16个问题 |采纳率93.8%你说的草酸二酯是不是CPPO? 一种荧光原料、?
那东西含有苯环的 三氯水杨酸和草酸 以及异戊醇生成的酯类化合物
水杨酸里面含有苯环
只要你看到结构式中 有一个六角形 里面有三个【双键】 的那种 一定是苯环
有一个六角形 里面是圆圈的 也一定是苯环1年前查看全部
- 我能做什么化学实验,求教我有硫酸铜,氢氧化钠,硼酸,小苏打,柠檬酸,双氧水,草酸,DBP,还有一点电池里抠出来的MnO2
 cn_lzy1年前1
cn_lzy1年前1 -
 记忆无恒 共回答了18个问题
记忆无恒 共回答了18个问题 |采纳率88.9%能做双氧水分解制氧气.将二氧化锰丢进双氧水即可获得氧气.
能用小苏打跟柠檬酸调汽水喝,不过你得保证你的原料是食品级.
你的电池没扔吧?可以用电池皮(锌皮)跟硫酸铜玩置换.没有危险.
DBP是邻苯二甲酸丁二酯.跟氢氧化钠可以玩水解反应,不过条件难控制,要恒温,估计你家的烤蛋糕的箱子不行.
草酸跟小苏打可以制二氧化碳,不过不太好玩,二氧化碳干不了啥.氧气还能助燃啥的,二氧化碳平时玩,确实不好玩啊.
硼酸就用来急救吧,强碱掉身上了,用硼酸溶液3%-5%洗洗.
暂时想到就这么多,不过你还要买点其他的玻璃仪器,或者用洗干净的玻璃罐头瓶冒充一些也可以的.1年前查看全部
大家在问
- 1根据句子意思和首字母完成单词1.The twins are m_____of the club.2.Nancy l___
- 2方程组{x+y+z=50,1500x+2100y+2500z
- 3一般建材不锈钢熔化温度是多少?通过一般的加热能不能使其熔化变成液体?
- 4在环保知识竞赛的预选赛中.在环保知识竞赛的预选赛中,共有20道题,并规定每答对一题得10分,每答错1题或不答扣5分,总分
- 53333*6666的简便算法 ?
- 6如图所示是某一时刻的波形图象,波沿x轴正方向传播,波速是18m/s,则波长和频率分别是( )
- 7仿句:有障碍,才有生活;要是没有的话,水便会毫无生气地立刻流入大洋了,就像不明不白的生...
- 8假期计划(寒假)英语作文80字。谁会啊!帮帮忙吧
- 9给实习老师的诗 作文
- 10英语词根词缀在安卓手机上有什么好的工具?有单词发音吗
- 11化简求值:3x²+(2x²-3x²)—(-4x+5x²),其中x=2010
- 12Do not feel happy having some sweets right away
- 13投资学计算题,两年期国债,面值1000元,票面利率9%,市场利率8%,到期一次还本.如果:(1)每年支付的利息;(2)每
- 14一篇名为Preparing for Tomorrow的英语文章
- 15行列式 计算 .如图.,
