硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下.
 荆棘鸟19752022-10-04 11:39:541条回答
荆棘鸟19752022-10-04 11:39:541条回答 硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下.
硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下.(1)请根据图形判断下列说法正确的是______
A.温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小
B.三个不同温度中,313K时Ksp(SrSO4)最大
C.283K时,图中a点对应的溶液是不饱和溶液
D.283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液
(2)请根据图中b点的数据计算283K时SrSO4的溶度积常数(计算结果用负指数表示).
(3)又知283K时硫酸钡(BaSO4)的溶度积常数Ksp═1.00×10-10mol2•L-2,试判断在该温度下,在SrSO4的饱和溶液中加入BaCl2溶液______(填“有”或“没有”)BaSO4产生,理由是:______.
(4)假定在283K时该反应(SrSO4(s)+Ba2+⇌BaSO4(s)+Sr2+)是一个可逆反应,求此温度下该反应的平衡常数K(计算结果用指数表示).

已提交,审核后显示!提交回复
共1条回复
 沂蒙心 共回答了21个问题
沂蒙心 共回答了21个问题 |采纳率85.7%- 解题思路:(1)沉淀溶解平衡中的溶度积常数只与温度有关,与浓度改变无关;溶解度随温度变化而变化,也随离子浓度改变;硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线,纵轴是锶离子浓度的对数,横轴是硫酸根离子浓度的对数.图象分析采取定一议二的方法进行分析;(2)根据Ksp(SrSO4)=c(Sr2+)×c(SO42-)计算;(3)根据Ksp(SrSO4)与Ksp(BaSO4)的相对大小分析,溶度积大的能转化为溶度积小的;(4)平衡常数K=c(Sr2+)c(Ba2+),根据Ksp(SrSO4)与Ksp(BaSO4)计算.
(1)A、Ksp只与温度有关与浓度无关,故A错误;
B、由图象可知:在相同条件下,温度越低,c(Sr2+)×c(SO42-)越大,Ksp(SrSO4)越大,故B正确;
C、a点在283K的下方,属于不饱和溶液,故C正确;
D、283K下的SrSO4饱和溶液升温到363K后会有晶体析出,还是属于饱和溶液,故D错误.
故答案为:BC;
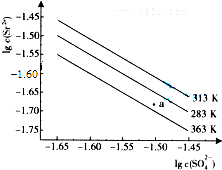
(2)由图可知b点时lgc(Sr2+)=-1.65,lgc(SO42-)=-1.50,则c(Sr2+)=10-1.65mol•L-1,c(SO42-)=10-1.5mol•L-1,
则Ksp(SrSO4)=c(Sr2+)×c(SO42-)=10-1.65mol•L-1×mol•L-1=1.00×10-3.15 mol2•L-2;
答:283K时SrSO4的溶度积常数为:1.00×10-3.15 mol2•L-2;
(3)已知283K时硫酸钡(BaSO4)的溶度积常数Ksp=1.00×10-10mol2•L-2,Ksp(SrSO4)=1.00×10-3.15 mol2•L-2,溶度积大的沉淀转化为溶度积小的沉淀容易实现,Ksp(SrSO4)>sp(BaSO4),所以在SrSO4的饱和溶液中加入BaCl2溶液会有硫酸钡沉淀生成;
故答案为:有;Ksp(SrSO4)=1.00×10-3.15 mol2•L-2>Ksp(BaSO4)=1.00×10-10mol2•L-2,反应向离子浓度减小的方向进行;
(4)已知反应SrSO4(s)+Ba2+⇌BaSO4(s)+Sr2+,则平衡常数K=
c(Sr2+)
c(Ba2+)=
Ksp(SrSO4)
Ksp(BaSO4)=1.00×106.85,
答:此温度下该反应的平衡常数K=1.00×106.85.点评:
本题考点: 难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查了沉淀转化的分析判断,平衡移动原理的应用和方向判断,解答本题的关键是正确分析图象中纵坐标和横坐标的意义,理解曲线的变化趋势,题目难度中等. - 1年前
相关推荐
- 硫酸锶能不能溶解在水里?
 相当地那是1年前1
相当地那是1年前1 -
 衰哥13 共回答了16个问题
衰哥13 共回答了16个问题 |采纳率87.5%任何东西都能溶解在水里,只是溶解多少的问题.
硫酸锶的溶解度很低.是微溶.
但是水中加入其他物质可以增加溶解,比如二亚已基三胺戊醋酸(简称为DTPA混合溶剂),这种化学溶剂就能有效地溶解硫酸钡、硫酸锶.一般随着pH值增加,硫酸钡和硫酸锶的溶解度也随着增加.硫酸钡比硫酸锶溶解困难,在相同的温度下,被溶解的锶的量大约是钡的三倍.1年前查看全部
- 判断正误题1.砹(At)为有色固体 AgAt不溶于水且见光分解2.硫酸锶是难溶于水的白色固体3.将氯气充入H2S溶液中
判断正误题
1.砹(At)为有色固体 AgAt不溶于水且见光分解
2.硫酸锶是难溶于水的白色固体
3.将氯气充入H2S溶液中 会出现淡黄色沉淀
4.气态氢化物稳定性:HF>HCL>H2S 大贝壳蛋糕1年前4
大贝壳蛋糕1年前4 -
 姚川1 共回答了15个问题
姚川1 共回答了15个问题 |采纳率93.3%都是对的
1.At是卤族元素,根据卤族的递变性,又发现从氟气到碘,颜色是变深的,所以At肯定有颜色,而如AgCl等都不溶于水,见光分解,所以AgAt不溶于水且见光分解
2.锶和钡同族,可以根据同族的相似性推断它和硫酸钡一样是难溶于水的白色固体
3.氯气有氧化性,硫化氢有还原性,反应生成硫单质,是淡黄色沉淀
4.元素周期表中,上面比下面的气态氢化物稳定,右边的比左边的稳定,所以HF>HCL>H2S是对的1年前查看全部
- (2009•广东)硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下.下列说法正确的是( )
 (2009•广东)硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下.下列说法正确的是( )
(2009•广东)硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下.下列说法正确的是( )
A.温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小
B.三个不同温度中,313K时Ksp(SrSO4)最大
C.283K时,图中a点对应的溶液是不饱和溶液
D.283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液 今天晚上我有空1年前1
今天晚上我有空1年前1 -
 ljy1111cn 共回答了20个问题
ljy1111cn 共回答了20个问题 |采纳率75%解题思路:沉淀溶解平衡中的溶度积常数只与温度有关,与浓度改变无关;溶解度随温度变化而变化,也随离子浓度改变;
硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线,纵轴是锶离子浓度的对数,横轴是硫酸根离子浓度的对数.图象分析采取定一议二的方法进行分析;A、Ksp只与温度有关与浓度无关,故A错误;
B、由图象可知:在相同条件下,温度越低,c(SO42−)•c(Sr2+)越大,Ksp(SrSO4)越大,B正确;
C、a点在283K的下方,属于不饱和溶液,C正确;
D、283K下的SrSO4饱和溶液升温到363K后会有晶体析出,还是属于饱和溶液,D错误.
故选BC.点评:
本题考点: 难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查沉淀溶解平衡及Ksp的意义和应用,饱和溶液的判断,关键是正确分析图象中纵坐标和横坐标的意义,理解曲线的变化趋势.1年前查看全部
- 硫酸锶能不能溶解在水里?
 hasadream1年前1
hasadream1年前1 -
 qingbuxing 共回答了23个问题
qingbuxing 共回答了23个问题 |采纳率100%硫酸锶的溶解度很低.是微溶.
但是水中加入其他物质可以增加溶解,比如二亚已基三胺戊醋酸(简称为DTPA混合溶剂),这种化学溶剂就能有效地溶解硫酸钡、硫酸锶.一般随着pH值增加,硫酸钡和硫酸锶的溶解度也随着增加.硫酸钡比硫酸锶溶解困难,在相同的温度下,被溶解的锶的量大约是钡的三倍.1年前查看全部
大家在问
- 1利用化学方程式简单计算那三种类型题
- 2根据短文内容,选择正 根据短文内容,选择正确答案. On the bus It's time to go h
- 3在Fe2O3+3CO 高温 . 2Fe+3CO2 的反应中,铁元素由+3价变为0
- 4弹簧测力计的测量范围可以从它的 看出来;弹簧测力计测量时所能达到的准确程度,可以从它的 看出来(填空)
- 5AB,CD,EF相交于O点,EF垂直于AB,OG平分∠COF,OH平分∠DOG,∠AOC:∠DOH=8:29,求∠COH
- 6用度表示78°25′12″ 快
- 7数学题目计算求解1又三分之一减十二分之七加二十分之九减三十分之十一加四十二分之十三减五十六分之十五加七十二分之十七减九十
- 8船为什么会浮在水面上?
- 9实数(综合)1、 1/4的平方是_____,平方根为_____.在3.14,1/3,2π(π是排),—根号8 ,0 ,-
- 10成功路上的反对者(转载) 作文
- 11给定一棵用链表表示的二叉树,其根结点指针为t,编写求二叉树的叶子数目的算法。
- 12suggar on porridge salt on french fries hungry and thirsty
- 131.六(3)班今天实到38人,有2人请假,今天六(3)班的出勤率是()
- 14作为生成的苯酚写离子方程式时能拆吗?需要写沉淀符号吗?反应物呢?
- 15饮酒过量的人表现为语无伦次、走路不稳、呼吸急促,在脑结构中分别与之相对应的是( )
