单线桥法电子转移数怎么算
 爱你会坚持到底2022-10-04 11:39:543条回答
爱你会坚持到底2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 情缘以定 共回答了25个问题
情缘以定 共回答了25个问题 |采纳率96%- 转移的电子数乘以转移物质的物质的量
- 1年前
 dkny110 共回答了3个问题
dkny110 共回答了3个问题 |采纳率- 只算元素化合价差即可
- 1年前
 Tomcool010 共回答了3个问题
Tomcool010 共回答了3个问题 |采纳率- 一共得失电子数除2
- 1年前
相关推荐
- 学了双线桥单线桥法,不清楚,求学霸解释下,
 mhfc1年前2
mhfc1年前2 -
 xxyz604604 共回答了3个问题
xxyz604604 共回答了3个问题 |采纳率双线桥电子得失都要标,而单线桥只用标电子转移。1年前查看全部
- 高一化学的单线桥法具体怎么做?
 木木狼1年前3
木木狼1年前3 -
 深海珊瑚鱼 共回答了27个问题
深海珊瑚鱼 共回答了27个问题 |采纳率96.3%单线桥是指在一个化学方程式里电子的转移 相对于双线桥更难 如过氧化钠与水反应产生氧气 过氧化钠是自我转移电子 可用单线桥 一般教学中不会考到的 只要掌握电子的转移搞清楚就行了1年前查看全部
- 单线桥法转移的电子数怎么算!拿这个示范吧
 透光的玻璃窗1年前3
透光的玻璃窗1年前3 -
 吃饭睡觉Miss豆 共回答了26个问题
吃饭睡觉Miss豆 共回答了26个问题 |采纳率92.3%2个正2价铁离子------2个正3价铁离子,化合价升高,失去了2e,被氧化
4个负1价溴离子------4个0价的溴原子,化合价升高,失去了4e,被氧化
6个0价氯原子------6个负1价氯离子,化合价降低,得到6e,被还原,也就是氧化剂
一个化学式里,得到的电子数=失去的电子数=化合价变化数×原子个数×系数1年前查看全部
- 高一化学的单线桥法具体怎么做?
 白公子1年前1
白公子1年前1 -
 善地 共回答了15个问题
善地 共回答了15个问题 |采纳率100%单线桥是指在一个化学方程式里电子的转移 相对于双线桥更难 如过氧化钠与水反应产生氧气 过氧化钠是自我转移电子 可用单线桥 一般教学中不会考到的 只要掌握电子的转移搞清楚就行了1年前查看全部
- KCLO3+6HCl=KCL+3H2O+3Cl2 用双线桥法和单线桥法表示时如何算得失电子数?
KCLO3+6HCl=KCL+3H2O+3Cl2 用双线桥法和单线桥法表示时如何算得失电子数?
请写出具体步骤。 中山光光1年前1
中山光光1年前1 -
 a_ba123 共回答了21个问题
a_ba123 共回答了21个问题 |采纳率90.5%KCLO3中CL价态为+5得4e-被还原为CL2,HCL中Cl为-1失5e-被氧化为CL2.单线桥从HCL的Cl到KCLO3的Cl标5e-.1年前查看全部
- 用单线桥法表示电子转移,急,
用单线桥法表示电子转移,急,

 liguangshengong1年前0
liguangshengong1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 用单线桥法表示出铁与水蒸气反应3Fe + 4H2O (g) == Fe3O4 + 4H2 中电子转移的数目
 詹瑞庭1年前1
詹瑞庭1年前1 -
 大润 共回答了15个问题
大润 共回答了15个问题 |采纳率86.7%F e 失8e 给H1年前查看全部
- 关于单线桥法的问题-[ ]—| ↓Cu+2FeCl3=CuCl2+2FeCl2括号内要填什么?单线桥法是所有的都填xe-
关于单线桥法的问题
-[ ]—
| ↓
Cu+2FeCl3=CuCl2+2FeCl2
括号内要填什么?
单线桥法是所有的都填xe-吗?有没有要填x*e-的? ranxiaoyan1年前2
ranxiaoyan1年前2 -
 巧笑游云 共回答了20个问题
巧笑游云 共回答了20个问题 |采纳率90%填2e-,xe-和x*e-一样,一般都写成xe-.1年前查看全部
- 分析反应MnO 2 +4HCl(浓) MnCl 2 +2H 2 O+Cl 2 ↑,用单线桥法标出电子转移的方向和数目,指
分析反应MnO 2 +4HCl(浓)  MnCl 2 +2H 2 O+Cl 2 ↑,用单线桥法标出电子转移的方向和数目,指出氧化剂和还原剂。
MnCl 2 +2H 2 O+Cl 2 ↑,用单线桥法标出电子转移的方向和数目,指出氧化剂和还原剂。
___________________________________ 真爱英雄1年前1
真爱英雄1年前1 -
 陌上蝴蝶飞 共回答了26个问题
陌上蝴蝶飞 共回答了26个问题 |采纳率80.8%1年前查看全部
- 只要是初三到高一的方程式都行,不用写文字,只要式子,是离子反应的,另写上离子方程式,有电子转移的,用单线桥法标出.
 newyhs1年前1
newyhs1年前1 -
 海汇中 共回答了18个问题
海汇中 共回答了18个问题 |采纳率94.4%中化学方程式汇总
一、 氧气的性质:
(1)单质与氧气的反应:(化合反应)
1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO
2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O4
3. 铜在空气中受热:2Cu + O2 加热 2CuO
4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O3
5. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O
6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 点燃 2P2O5
7. 硫粉在空气中燃烧: S + O2 点燃 SO2
8. 碳在氧气中充分燃烧:C + O2 点燃 CO2
9. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO
(2)化合物与氧气的反应:
10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO2
11. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O
12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O
(3)氧气的来源:
13.玻义耳研究空气的成分实验 2HgO 加热 Hg+ O2 ↑
14.加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)
15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 MnO22H2O+ O2 ↑(实验室制氧气原理2)
二、自然界中的水:
16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+ O2 ↑
17.生石灰溶于水:CaO + H2O == Ca(OH)2
18.二氧化碳可溶于水: H2O + CO2==H2CO3
三、质量守恒定律:
19.镁在空气中燃烧:2Mg + O2 点燃 2MgO
20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu
21.氢气还原氧化铜:H2 + CuO 加热 Cu + H2O
22. 镁还原氧化铜:Mg + CuO 加热 Cu + MgO
四、碳和碳的氧化物:
(1)碳的化学性质
23. 碳在氧气中充分燃烧:C + O2 点燃 CO2
24.木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑
25. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe + 3CO2↑
(2)煤炉中发生的三个反应:(几个化合反应)
26.煤炉的底层:C + O2 点燃 CO2
27.煤炉的中层:CO2 + C 高温 2CO
28.煤炉的上部蓝色火焰的产生:2CO + O2 点燃 2CO2
(3)二氧化碳的制法与性质:
29.大理石与稀盐酸反应(实验室制二氧化碳):
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
30.碳酸不稳定而分H2CO3 == H2O + CO2↑
31.二氧化碳可溶于水: H2O + CO2== H2CO3
32.高温煅烧石灰石(工业制二氧化碳):CaCO3 高温 CaO + CO2↑
33.石灰水与二氧化碳反应(鉴别二氧化碳):
Ca(OH)2 + CO2 === CaCO3 ↓+ H2O
(4)一氧化碳的性质:
34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO2
35.一氧化碳的可燃性:2CO + O2 点燃 2CO2
其它反应:
36.碳酸钠与稀盐酸反应(灭火器的原理):
Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
五、燃料及其利用:
37.甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O
38.酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O
39. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O
六、金属
(1)金属与氧气反应:
40. 镁在空气中燃烧:2Mg + O2 点燃 2MgO
41. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O4
42. 铜在空气中受热:2Cu + O2 加热 2CuO
43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3
(2)金属单质 + 酸 -------- 盐 + 氢气 (置换反应)
44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑
45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑
46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑
47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑
48. 锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑
49. 铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑
50. 镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑
51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑
(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐
52. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu
53. 锌和硫酸铜溶液反应:Zn + CuSO4 ==ZnSO4 + Cu
54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 == Cu(NO3)2 + Hg
(3)金属铁的治炼原理:
55.3CO+ 2Fe2O3 高温 4Fe + 3CO2↑
七、酸、碱、盐
1、酸的化学性质
(1)酸 + 金属 -------- 盐 + 氢气(见上)
(2)酸 + 金属氧化物-------- 盐 + 水
56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl ==2FeCl3 + 3H2O
57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O
58. 氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl2 + H2O
59. 氧化铜和稀硫酸反应:CuO + H2SO4 == CuSO4 + H2O
(3)酸 + 碱 -------- 盐 + 水(中和反应)
60.盐酸和烧碱起反应:HCl + NaOH == NaCl +H2O
61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 == CaCl2 + 2H2O
62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 == AlCl3 + 3H2O
63. 硫酸和烧碱反应:H2SO4 + 2NaOH == Na2SO4 + 2H2O
(4)酸 + 盐 -------- 另一种酸 + 另一种盐
64.大理石与稀盐酸反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑
67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl
2、碱的化学性质
(1) 碱 + 非金属氧化物 -------- 盐 + 水
68.苛性钠暴露在空气中变质:2NaOH + CO2 == Na2CO3 + H2O
69.苛性钠吸收二氧化硫气体:2NaOH + SO2 == Na2SO3 + H2O
70.苛性钠吸收三氧化硫气体:2NaOH + SO3 == Na2SO4 + H2O
71.消石灰放在空气中变质:Ca(OH)2 + CO2 == CaCO3 ↓+ H2O
72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 == CaSO3 ↓+ H2O
(2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)
(3)碱 + 盐 -------- 另一种碱 + 另一种盐
73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH
3、盐的化学性质
(1)盐(溶液) + 金属单质------- 另一种金属 + 另一种盐
74. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu
(2)盐 + 酸-------- 另一种酸 + 另一种盐
75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑
(3)盐 + 碱 -------- 另一种碱 + 另一种盐
76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH
(4)盐 + 盐 ----- 两种新盐
77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 == AgCl↓ + NaNO高中所有化学方程式(不一定全呀)
非金属单质(F2 ,Cl2 , O2 , S, N2 , P , C , Si)
1, 氧化性:
F2 + H2 === 2HF
F2 +Xe(过量)===XeF2
2F2(过量)+Xe===XeF4
nF2 +2M===2MFn (表示大部分金属)
2F2 +2H2O===4HF+O2
2F2 +2NaOH===2NaF+OF2 +H2O
F2 +2NaCl===2NaF+Cl2
F2 +2NaBr===2NaF+Br2
F2+2NaI ===2NaF+I2
F2 +Cl2 (等体积)===2ClF
3F2 (过量)+Cl2===2ClF3
7F2(过量)+I2 ===2IF7
Cl2 +H2 ===2HCl
3Cl2 +2P===2PCl3
Cl2 +PCl3 ===PCl5
Cl2 +2Na===2NaCl
3Cl2 +2Fe===2FeCl3
Cl2 +2FeCl2 ===2FeCl3
Cl2+Cu===CuCl2
2Cl2+2NaBr===2NaCl+Br2
Cl2 +2NaI ===2NaCl+I2
5Cl2+I2+6H2O===2HIO3+10HCl
Cl2 +Na2S===2NaCl+S
Cl2 +H2S===2HCl+S
Cl2+SO2 +2H2O===H2SO4 +2HCl
Cl2 +H2O2 ===2HCl+O2
2O2 +3Fe===Fe3O4
O2+K===KO2
S+H2===H2S
2S+C===CS2
S+Fe===FeS
S+2Cu===Cu2S
3S+2Al===Al2S3
S+Zn===ZnS
N2+3H2===2NH3
N2+3Mg===Mg3N2
N2+3Ca===Ca3N2
N2+3Ba===Ba3N2
N2+6Na===2Na3N
N2+6K===2K3N
N2+6Rb===2Rb3N
P2+6H2===4PH3
P+3Na===Na3P
2P+3Zn===Zn3P2
2.还原性
S+O2===SO2
S+O2===SO2
S+6HNO3(浓)===H2SO4+6NO2+2H2O
3S+4 HNO3(稀)===3SO2+4NO+2H2O
N2+O2===2NO
4P+5O2===P4O10(常写成P2O5)
2P+3X2===2PX3 (X表示F2,Cl2,Br2)
PX3+X2===PX5
P4+20HNO3(浓)===4H3PO4+20NO2+4H2O
C+2F2===CF4
C+2Cl2===CCl4
2C+O2(少量)===2CO
C+O2(足量)===CO2
C+CO2===2CO
C+H2O===CO+H2(生成水煤气)
2C+SiO2===Si+2CO(制得粗硅)
Si(粗)+2Cl===SiCl4
(SiCl4+2H2===Si(纯)+4HCl)
Si(粉)+O2===SiO2
Si+C===SiC(金刚砂)
Si+2NaOH+H2O===Na2SiO3+2H2
3,(碱中)歧化
Cl2+H2O===HCl+HClO
(加酸抑制歧化,加碱或光照促进歧化)
Cl2+2NaOH===NaCl+NaClO+H2O
2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
3Cl2+6KOH(热,浓)===5KCl+KClO3+3H2O
3S+6NaOH===2Na2S+Na2SO3+3H2O
4P+3KOH(浓)+3H2O===PH3+3KH2PO2
11P+15CuSO4+24H2O===5Cu3P+6H3PO4+15H2SO4
3C+CaO===CaC2+CO
3C+SiO2===SiC+2CO
二,金属单质(Na,Mg,Al,Fe)的还原性
2Na+H2===2NaH
4Na+O2===2Na2O
2Na2O+O2===2Na2O2
2Na+O2===Na2O2
2Na+S===Na2S(爆炸)
2Na+2H2O===2NaOH+H2
2Na+2NH3===2NaNH2+H2
4Na+TiCl4(熔融)===4NaCl+Ti
Mg+Cl2===MgCl2
Mg+Br2===MgBr2
2Mg+O2===2MgO
Mg+S===MgS
Mg+2H2O===Mg(OH)2+H2
2Mg+TiCl4(熔融)===Ti+2MgCl2
Mg+2RbCl===MgCl2+2Rb
2Mg+CO2===2MgO+C
2Mg+SiO2===2MgO+Si
Mg+H2S===MgS+H2
Mg+H2SO4===MgSO4+H2
2Al+3Cl2===2AlCl3
4Al+3O2===2Al2O3(钝化)
4Al(Hg)+3O2+2xH2O===2(Al2O3.xH2O)+4Hg
4Al+3MnO2===2Al2O3+3Mn
2Al+Cr2O3===Al2O3+2Cr
2Al+Fe2O3===Al2O3+2Fe
2Al+3FeO===Al2O3+3Fe
2Al+6HCl===2AlCl3+3H2
2Al+3H2SO4===Al2(SO4)3+3H2
2Al+6H2SO4(浓)===Al2(SO4)3+3SO2+6H2O
(Al,Fe在冷,浓的H2SO4,HNO3中钝化)
Al+4HNO(稀)===Al(NO3)3+NO+2H2O
2Al+2NaOH+2H2O===2NaAlO2+3H2
2Fe+3Br2===2FeBr3
Fe+I2===FeI2
Fe+S===FeS
3Fe+4H2O(g)===Fe3O4+4H2
Fe+2HCl===FeCl2+H2
Fe+CuCl2===FeCl2+Cu
Fe+SnCl4===FeCl2+SnCl2
(铁在酸性环境下,不能把四氯化锡完全
还原为单质锡 Fe+SnCl2==FeCl2+Sn)
三, 非金属氢化物(HF,HCl,H2O,H2S,NH3)
1,还原性:
4HCl(浓)+MnO2===MnCl2+Cl2+2H2O
4HCl(g)+O2===2Cl2+2H2O
16HCl+2KMnO4===2KCl+2MnCl2+5Cl2+8H2O
14HCl+K2Cr2O7===2KCl+2CrCl3+3Cl2+7H2O
2H2O+2F2===4HF+O2
2H2S+3O2(足量)===2SO2+2H2O
2H2S+O2(少量)===2S+2H2O
2H2S+SO2===3S+2H2O
H2S+H2SO4(浓)===S+SO2+2H2O
3H2S+2HNO(稀)===3S+2NO+4H2O
5H2S+2KMnO4+3H2SO4===2MnSO4+K2SO4+5S+8H2O
3H2S+K2Cr2O7+4H2SO4===Cr2(SO4)3+K2SO4+3S+7H2O
H2S+4Na2O2+2H2O===Na2SO4+6NaOH
2NH3+3CuO===3Cu+N2+3H2O
2NH3+3Cl2===N2+6HCl
8NH3+3Cl2===N2+6NH4Cl
4NH3+3O2(纯氧)===2N2+6H2O
4NH3+5O2===4NO+6H2O
4NH3+6NO===5N2+6HO(用氨清除NO)
NaH+H2O===NaOH+H2
4NaH+TiCl4===Ti+4NaCl+2H2
CaH2+2H2O===Ca(OH)2+2H2
2,酸性:
4HF+SiO2===SiF4+2H2O
(此反应广泛应用于测定矿样或钢样中SiO2的含量)
2HF+CaCl2===CaF2+2HCl
H2S+Fe===FeS+H2
H2S+CuCl2===CuS+2HCl
H2S+2AgNO3===Ag2S+2HNO3
H2S+HgCl2===HgS+2HCl
H2S+Pb(NO3)2===PbS+2HNO3
H2S+FeCl2===
2NH3+2Na==2NaNH2+H2
(NaNH2+H2O===NaOH+NH3)
3,碱性:
NH3+HCl===NH4Cl
NH3+HNO3===NH4NO3
2NH3+H2SO4===(NH4)2SO4
NH3+NaCl+H2O+CO2===NaHCO3+NH4Cl
(此反应用于工业制备小苏打,苏打)
4,不稳定性:
2HF===H2+F2
2HCl===H2+Cl2
2H2O===2H2+O2
2H2O2===2H2O+O2
H2S===H2+S
2NH3===N2+3H2
四,非金属氧化物
低价态的还原性:
2SO2+O2===2SO3
2SO2+O2+2H2O===2H2SO4
(这是SO2在大气中缓慢发生的环境化学反应)
SO2+Cl2+2H2O===H2SO4+2HCl
SO2+Br2+2H2O===H2SO4+2HBr
SO2+I2+2H2O===H2SO4+2HI
SO2+NO2===SO3+NO
2NO+O2===2NO2
NO+NO2+2NaOH===2NaNO2
(用于制硝酸工业中吸收尾气中的NO和NO2)
2CO+O2===2CO2
CO+CuO===Cu+CO2
3CO+Fe2O3===2Fe+3CO2
CO+H2O===CO2+H2
氧化性:
SO2+2H2S===3S+2H2O
SO3+2KI===K2SO3+I2
NO2+2KI+H2O===NO+I2+2KOH
(不能用淀粉KI溶液鉴别溴蒸气和NO2)
4NO2+H2S===4NO+SO3+H2O
2NO2+Cu===4CuO+N2
CO2+2Mg===2MgO+C
(CO2不能用于扑灭由Mg,Ca,Ba,Na,K等燃烧的火灾)
SiO2+2H2===Si+2H2O
SiO2+2Mg===2MgO+Si
3,与水的作用:
SO2+H2O===H2SO3
SO3+H2O===H2SO4
3NO2+H2O===2HNO3+NO
N2O5+H2O===2HNO3
P2O5+H2O===2HPO3
P2O5+3H2O===2H3PO4
(P2O5极易吸水,可作气体干燥剂)
P2O5+3H2SO4(浓)===2H3PO4+3SO3
CO2+H2O===H2CO3
与碱性物质的作用:
SO2+2NH3+H2O===(NH4)2SO3
SO2+(NH4)2SO3+H2O===2NH4HSO3
(这是硫酸厂回收SO2的反应.先用氨水吸收SO2,
再用H2SO4处理: 2NH4HSO3+H2SO4===(NH4)2SO4+2H2O+2SO2
生成的硫酸铵作化肥,SO2循环作原料气)
SO2+Ca(OH)2===CaSO3+H2O
(不能用澄清石灰水鉴别SO2和CO2.可用品红鉴别)
SO3+MgO===MgSO4
SO3+Ca(OH)2===CaSO4+H2O
CO2+2NaOH(过量)===Na2CO3+H2O
CO2(过量)+NaOH===NaHCO3
CO2+Ca(OH)2(过量)===CaCO3+H2O
2CO2(过量)+Ca(OH)2===Ca(HCO3)2
CO2+2NaAlO2+3H2O===2Al(OH)3+Na2CO3
CO2+C6H5ONa+H2O===C6H5OH+NaHCO3
SiO2+CaO===CaSiO3
SiO2+2NaOH===Na2SiO3+H2O
(常温下强碱缓慢腐蚀玻璃)
SiO2+Na2CO3===Na2SiO3+CO2
SiO2+CaCO3===CaSiO3+CO2
五,金属氧化物
1,低价态的还原性:
6FeO+O2===2Fe3O4
FeO+4HNO3===Fe(NO3)3+NO2+2H2O
2,氧化性:
Na2O2+2Na===2Na2O
(此反应用于制备Na2O)
MgO,Al2O3几乎没有氧化性,很难被还原为Mg,Al.
一般通过电解制Mg和Al.
Fe2O3+3H2===2Fe+3H2O (制还原铁粉)
Fe3O4+4H2===3Fe+4H2O
3,与水的作用:
Na2O+H2O===2NaOH
2Na2O2+2H2O===4NaOH+O2
(此反应分两步:Na2O2+2H2O===2NaOH+H2O2 ;
2H2O2===2H2O+O2. H2O2的制备可利用类似的反应:
BaO2+H2SO4(稀)===BaSO4+H2O2)
MgO+H2O===Mg(OH)2 (缓慢反应)
4,与酸性物质的作用:
Na2O+SO3===Na2SO4
Na2O+CO2===Na2CO3
Na2O+2HCl===2NaCl+H2O
2Na2O2+2CO2===2Na2CO3+O2
Na2O2+H2SO4(冷,稀)===Na2SO4+H2O2
MgO+SO3===MgSO4
MgO+H2SO4===MgSO4+H2O
Al2O3+3H2SO4===Al2(SO4)3+3H2O
(Al2O3是两性氧化物:
Al2O3+2NaOH===2NaAlO2+H2O)
FeO+2HCl===FeCl2+3H2O
Fe2O3+6HCl===2FeCl3+3H2O
Fe2O3+3H2S(g)===Fe2S3+3H2O
Fe3O4+8HCl===FeCl2+2FeCl3+4H2O
六,含氧酸
1,氧化性:
4HClO3+3H2S===3H2SO4+4HCl
HClO3+HI===HIO3+HCl
3HClO+HI===HIO3+3HCl
HClO+H2SO3===H2SO4+HCl
HClO+H2O2===HCl+H2O+O2
(氧化性:HClO>HClO2>HClO3>HClO4,
但浓,热的HClO4氧化性很强)
2H2SO4(浓)+C===CO2+2SO2+2H2O
2H2SO4(浓)+S===3SO2+2H2O
H2SO4+Fe(Al) 室温下钝化
6H2SO4(浓)+2Fe===Fe2(SO4)3+3SO2+6H2O
2H2SO4(浓)+Cu===CuSO4+SO2+2H2O
H2SO4(浓)+2HBr===SO2+Br2+2H2O
H2SO4(浓)+2HI===SO2+I2+2H2O
H2SO4(稀)+Fe===FeSO4+H2
2H2SO3+2H2S===3S+2H2O
4HNO3(浓)+C===CO2+4NO2+2H2O
6HNO3(浓)+S===H2SO4+6NO2+2H2O
5HNO3(浓)+P===H3PO4+5NO2+H2O
6HNO3+Fe===Fe(NO3)3+3NO2+3H2O
4HNO3+Fe===Fe(NO3)3+NO+2H2O
30HNO3+8Fe===8Fe(NO3)3+3N2O+15H2O
36HNO3+10Fe===10Fe(NO3)3+3N2+18H2O
30HNO3+8Fe===8Fe(NO3)3+3NH4NO3+9H2O
2,还原性:
H2SO3+X2+H2O===H2SO4+2HX
(X表示Cl2,Br2,I2)
2H2SO3+O2===2H2SO4
H2SO3+H2O2===H2SO4+H2O
5H2SO3+2KMnO4===2MnSO4+K2SO4+2H2SO4+3H2O
H2SO3+2FeCl3+H2O===H2SO4+2FeCl2+2HCl
3,酸性:
H2SO4(浓) +CaF2===CaSO4+2HF
H2SO4(浓)+NaCl===NaHSO4+HCl
H2SO4(浓) +2NaCl===Na2SO4+2HCl
H2SO4(浓)+NaNO3===NaHSO4+HNO3
3H2SO4(浓)+Ca3(PO4)2===3CaSO4+2H3PO4
2H2SO4(浓)+Ca3(PO4)2===2CaSO4+Ca(H2PO4)2
3HNO3+Ag3PO4===H3PO4+3AgNO3
2HNO3+CaCO3===Ca(NO3)2+H2O+CO2
(用HNO3和浓H2SO4不能制备H2S,HI,HBr,(SO2)
等还原性气体)
4H3PO4+Ca3(PO4)2===3Ca(H2PO4)2(重钙)
H3PO4(浓)+NaBr===NaH2PO4+HBr
H3PO4(浓)+NaI===NaH2PO4+HI
4,不稳定性:
2HClO===2HCl+O2
4HNO3===4NO2+O2+2H2O
H2SO3===H2O+SO2
H2CO3===H2O+CO2
H4SiO4===H2SiO3+H2O
七,碱
低价态的还原性:
4Fe(OH)2+O2+2H2O===4Fe(OH)3
与酸性物质的作用:
2NaOH+SO2(少量)===Na2SO3+H2O
NaOH+SO2(足量)===NaHSO3
2NaOH+SiO2===NaSiO3+H2O
2NaOH+Al2O3===2NaAlO2+H2O
2NaOH+Cl2===NaCl+NaClO+H2O
NaOH+HCl===NaCl+H2O
NaOH+H2S(足量)===NaHS+H2O
2NaOH+H2S(少量)===Na2S+2H2O
3NaOH+AlCl3===Al(OH)3+3NaCl
NaOH+Al(OH)3===NaAlO2+2H2O
(AlCl3和Al(OH)3哪个酸性强?)
NaOH+NH4Cl===NaCl+NH3+H2O
Mg(OH)2+2NH4Cl===MgCl2+2NH3.H2O
Al(OH)3+NH4Cl 不溶解
3,不稳定性:
Mg(OH)2===MgO+H2O
2Al(OH)3===Al2O3+3H2O
2Fe(OH)3===Fe2O3+3H2O
Cu(OH)2===CuO+H2O
八,盐
1,氧化性:
2FeCl3+Fe===3FeCl2
2FeCl3+Cu===2FeCl2+CuCl2
(用于雕刻铜线路版)
2FeCl3+Zn===2FeCl2+ZnCl2
FeCl3+Ag===FeCl2+AgC
Fe2(SO4)3+2Ag===FeSO4+Ag2SO4(较难反应)
Fe(NO3)3+Ag 不反应
2FeCl3+H2S===2FeCl2+2HCl+S
2FeCl3+2KI===2FeCl2+2KCl+I2
FeCl2+Mg===Fe+MgCl2
2,还原性:
2FeCl2+Cl2===2FeCl3
3Na2S+8HNO3(稀)===6NaNO3+2NO+3S+4H2O
3Na2SO3+2HNO3(稀)===3Na2SO4+2NO+H2O
2Na2SO3+O2===2Na2SO4
3,与碱性物质的作用:
MgCl2+2NH3.H2O===Mg(OH)2+NH4Cl
AlCl3+3NH3.H2O===Al(OH)3+3NH4Cl
FeCl3+3NH3.H2O===Fe(OH)3+3NH4Cl
4,与酸性物质的作用:
Na3PO4+HCl===Na2HPO4+NaCl
Na2HPO4+HCl===NaH2PO4+NaCl
NaH2PO4+HCl===H3PO4+NaCl
Na2CO3+HCl===NaHCO3+NaCl
NaHCO3+HCl===NaCl+H2O+CO2
3Na2CO3+2AlCl3+3H2O===2Al(OH)3+3CO2+6NaCl
3Na2CO3+2FeCl3+3H2O===2Fe(OH)3+3CO2+6NaCl
3NaHCO3+AlCl3===Al(OH)3+3CO2
3NaHCO3+FeCl3===Fe(OH)3+3CO2
3Na2S+Al2(SO4)3+6H2O===2Al(OH)3+3H2S
3NaAlO2+AlCl3+6H2O===4Al(OH)3
5,不稳定性:
Na2S2O3+H2SO4===Na2SO4+S+SO2+H2O
NH4Cl===NH3+HCl
NH4HCO3===NH3+H2O+CO2
2KNO3===2KNO2+O2
2Cu(NO3)3===2CuO+4NO2+O2
2KMnO4===K2MnO4+MnO2+O2
2KClO3===2KCl+3O2
2NaHCO3===Na2CO3+H2O+CO2
Ca(HCO3)2===CaCO3+H2O+CO2
CaCO3===CaO+CO2
MgCO3===MgO+CO21年前查看全部
- 详细的解释一下双线桥法和单线桥法
详细的解释一下双线桥法和单线桥法
急!谢谢~ wait20081年前1
wait20081年前1 -
 behao 共回答了14个问题
behao 共回答了14个问题 |采纳率21.4%单线桥法---不跨越等号。 从反应物中找出还原剂,计算出失电子数或化合价...(2)双线桥法---跨越等号。 从反应物中找出还原剂,从产物中找出氧化产物,1年前查看全部
- 写出下列反应的离子方程式,并用单线桥法标明电子转移的方向和数目.
写出下列反应的离子方程式,并用单线桥法标明电子转移的方向和数目.
(1)Cu和AgNO3溶液反应______
(2)向FeCl3 溶液中加入铁粉 生成FeCl2______. 无天刀剑舞1年前1
无天刀剑舞1年前1 -
 hmilyrose125 共回答了11个问题
hmilyrose125 共回答了11个问题 |采纳率81.8%解题思路:(1)Cu和AgNO3溶液反应生成硝酸铜和金属银的反应中,Cu元素的化合价升高,Ag元素的化合价降低,该反应中转移2e-,以此来解答;
(2)FeCl3溶液中加入铁粉生成FeCl2的反应中,铁元素的化合价升高也降低,该反应中转移2e-,以此来解答.(1)Cu和AgNO3溶液反应生成硝酸铜和金属银,离子反应为:Cu+2Ag+═Cu2++2Ag,化合价升高值=化合价降低值=转移电子数=2,电子转移表示为:
 ,故答案为:
,故答案为: ;
;
(2)向FeCl3溶液中加入铁粉生成FeCl2,离子反应为:Fe+2Fe3+═3Fe2+,Fe元素化合价升高值=铁元素化合价降低值=转移电子数=2, ,
,
故答案为: .
.点评:
本题考点: 离子方程式的书写.
考点点评: 本题考查学生离子方程式的书写以及氧化还原反应中的电子转移知识,属于基本知识的考查题,难度不大.1年前查看全部
- 为什么双线桥法或单线桥法的箭头都不会指向氧,难道氧化还原反应都与氧无关?
 cssq1年前2
cssq1年前2 -
 applefish12 共回答了16个问题
applefish12 共回答了16个问题 |采纳率93.8%氧化还原 反应的特征 是在反应前后元素的化合价具有相应的升降变化的化学反应. 氧化还原反应的实质 是电子的得失或偏移. 任何元素都可以,不一定非得是氧元素元素1年前查看全部
- 用单线桥法表示下列化学方程式中的电子转移指出氧化剂还原剂,氧化产物和还原产物.
用单线桥法表示下列化学方程式中的电子转移指出氧化剂还原剂,氧化产物和还原产物.
1.2Fecl2+cl2=2Fecl3 2.Zn+H2SO4=ZnSO4+H2↑
3.H2SO4(浓)+H2S=S↓+SO4↑+2H2O
4.NH4NO3=N2O+2H2O vtkd11201年前1
vtkd11201年前1 -
 jkok_1818 共回答了23个问题
jkok_1818 共回答了23个问题 |采纳率100%1、
FeCl2 → 2e- → Cl2
氧化剂Cl2,还原剂FeCl2
氧化产物FeCl3,还原产物FeCl3
2、
Zn → 2e- → H2SO4
氧化剂H2SO4,还原剂Zn
氧化产物ZnSO4,还原产物H2
3、
NH4 → 4e- → NO3
氧化剂NH4NO3,还原剂NH4NO3
氧化产物N2O,还原产物N2O1年前查看全部
- 高一化学物质的量我理解不是很透彻,怎么理解可以快速记忆,还有双线桥和单线桥法怎么用?
 子虎19741年前1
子虎19741年前1 -
 那里有鱼 共回答了15个问题
那里有鱼 共回答了15个问题 |采纳率93.3%物质的量是国际单位制中的基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量),它和“长度”,“质量”,“时间”等概念一样,是一个物理量的整体名词.其符号为n,单位为摩尔(mol),简称摩.物质的量是表示物质所含微粒数(N)(如:分子,原子等)与阿伏加德罗常数(NA)之比,即n=N/NA.它是把微观粒子与宏观可称量物质联系起来的一种物理量.其表示物质所含粒子数目的多少.
1摩尔物质的量的物质的分子数为阿伏加德罗常数,即6.02*10^23.1年前查看全部
- 在氧化还原反应中,电子转移的表示方法通常用单线桥法和双线桥法。试分析这两种表示方法的特征,并填空。
在氧化还原反应中,电子转移的表示方法通常用单线桥法和双线桥法。试分析这两种表示方法的特征,并填空。
(1)标单线桥(4分)
KIO 3 +6HI=KI+3I 2 +3H 2 O氧化产物与还原产物物质的量之比= 。
(2)配平化学方程式及标双线桥(5分)
Fe + HNO 3 (稀)= Fe(NO 3 ) 2 + NO↑+ H 2 O反应中,氧化剂与还原剂的物质的量之比 。 有没被用过的名吗1年前1
有没被用过的名吗1年前1 -
 yy_卜风 共回答了19个问题
yy_卜风 共回答了19个问题 |采纳率89.5%1年前查看全部
- 怎么用单线桥法表示3Fe + 2O2 =点燃= Fe3O4
 owall1年前1
owall1年前1 -
 assedo 共回答了14个问题
assedo 共回答了14个问题 |采纳率85.7%O转移到Fe4*2e1年前查看全部
- 我的参考书上这样写双线桥法 表明同一元素原子得失电子情况单线桥法 表明不同种元素原子间失电子情况
我的参考书上这样写双线桥法 表明同一元素原子得失电子情况单线桥法 表明不同种元素原子间失电子情况
这样的说法对吗?还有在写离子反应的时候,氧化物为什么不可以拆 s8833-331年前1
s8833-331年前1 -
 black-ice 共回答了15个问题
black-ice 共回答了15个问题 |采纳率86.7%一般同种元素的价位变化,用的是双向桥法 ,直观, 就比如氯气和水反应,这就是个歧化反应,用单线桥法不是很直观. 氧化物就两种元素组成,成键类型不同,还要考虑实际的状状态,溶度等1年前查看全部
- 氧化还原反应的“双线桥法”和“单线桥法”是怎么一回事?
 xingyunderen1年前3
xingyunderen1年前3 -
 杀毒的虫 共回答了13个问题
杀毒的虫 共回答了13个问题 |采纳率92.3%(1)单线桥法---不跨越等号.
从反应物中找出还原剂,计算出失电子数或化合价升高数;
从反应物中找出氧化剂,计算出得电子数或化合价降低数;
找出公倍数,得失相等,或升降相等!
(2)双线桥法---跨越等号.
从反应物中找出还原剂,从产物中找出氧化产物,计算出失电子数或化合价升高数;
从反应物中找出氧化剂,从产物中找出还原产物,计算出得电子数或化合价降低数;
找出公倍数,得失相等,或升降相等!1年前查看全部
- 什么是双线桥法,什么是单线桥法,有什么通俗易懂的方法,最好举几个例子,
 猫猫的猫猫11年前0
猫猫的猫猫11年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 单线桥法标出电子转移的数目怎么算的? 例如:
单线桥法标出电子转移的数目怎么算的? 例如:
6KMnO4+5KI+9H2SO4===6MnSO4+5KIO3+3k2so4+9H2O
怎么算?求解! winar1年前1
winar1年前1 -
 明灯黑夜 共回答了18个问题
明灯黑夜 共回答了18个问题 |采纳率88.9%箭头由KI中的I指向KMNO4中的Mn有60e1年前查看全部
- 只要式子,不要文字,是离子反应,写出离子反应方程式,有电子转移的,用单线桥法标出.请不要在网上随便搜索、复制一些来敷衍我
只要式子,不要文字,是离子反应,写出离子反应方程式,有电子转移的,用单线桥法标出.请不要在网上随便搜索、复制一些来敷衍我,不符合要求的不给分
请仔细看看我的要求! 流禾1年前1
流禾1年前1 -
 dongtianxueren 共回答了15个问题
dongtianxueren 共回答了15个问题 |采纳率93.3%1、向碳酸氢钙溶液中加入过量的氢氧化钠:
2HCO3-+Ca2++2OH–=CaCO3↓+2H2O+CO32–
2、向碳酸氢钙溶液中加入少量的氢氧化钠:Ca2++HCO3-+OH–=CaCO3↓+H2O
3、澄清石灰水与少量小苏打溶液混合:Ca2++OH–+HCO3-=CaCO3↓+H2O
4、澄清石灰水通入少量CO2:Ca2++2OH–+CO3=CaCO3↓+H2O
5、澄清石灰水通入过量CO2:OH–+CO2=HCO3-
6、碳酸氢钠溶液与少量石灰水反应:Ca2++2OH–+2HCO3-=CaCO3↓+CO32–+2H2O
7、碳酸氢钠溶液与过量石灰水反应:HCO3-+OH–+Ca2+=CaCO3↓+H2O
8、等物质的量氢氧化钡溶液与碳酸氢铵溶液混合:
Ba2++2OH–+NH4++HCO3-=BaCO3↓+H2O+NH3•H2O
9、碳酸钠溶液与盐酸反应:CO32–+H+=HCO3- 或CO32–+2H+=CO2↑+H2O
10、向氢氧化钠溶液中通入少量的CO2¬:CO2+2OH–=CO32–+H2O
11、过量的CO2通入氢氧化钠溶液中:CO2+OH–=HCO3-
12、磷酸溶液与少量澄清石灰水:H3PO4+OH–=H2O+H2PO4–
13、磷酸溶液与过量澄清石灰水:2H3PO4+3Ca2++6OH–=Ca3(PO4)2↓+6H2O
14、向硫酸铁的酸性溶液中通入足量的H2S:2Fe3++H2S=2Fe2++S↓+2H+
15、氯化铁溶液中滴加少量硫化钠溶液:2Fe3++S2–=S↓+2Fe2+
16、硫化钠溶液中滴加少量氯化铁溶液:2Fe3++3S2–=S↓+2FeS↓
17、氯化铁溶液中滴加少量碘化钾溶液:2Fe3++2I–=2Fe2++I2
18、氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH–=Fe(OH)3↓
19、氯化铁溶液跟过量氨水反应: Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+
20、氯化铁溶液与硫氰化钾溶液: Fe3++3SCN–=Fe(SCN)3
21、氯化铁溶液跟过量锌粉反应: 2Fe3++3Zn=2Fe+3Zn2+1年前查看全部
- 用双线桥法和单线桥法表示下列氧化还原反应的电子转移.2NaBr+Cl2=2NaCl+Br2
 最近挺郁闷1年前1
最近挺郁闷1年前1 -
 longwu9t 共回答了14个问题
longwu9t 共回答了14个问题 |采纳率92.9%双线桥是有电子的得失同种元素指向同种元素,一般是氧化剂指向还原产物、还原剂指向氧化产物,但也有特殊:例如分解反应、歧化反应、归中反应等要根据具体反应具体画.而单线桥是还原剂指向氧化剂,箭头由还原剂失去电子的元素指向氧化剂中得电子的元素.
具体情况如下:
双线桥
化合价升高失去2e^-电子,被氧化
-1 0 -1 0
2NaBr+Cl2 = 2NaCl+Br2
化合价降低得到2e^-电子,被还原
单线桥
-1 0
2NaBr + Cl2 = 2NaCl+Br2
今天不知为什么?图片上传不上去,只能给讲一下你自己画了.
此题的双线桥在化学方程式的上面画的箭头由反应物的溴元素指向生成物的溴元素,化合价升高失去2e^-电子,被氧化 , 方程式的下面画的箭头由反应物的氯元素指向生成的氯元素,化合价降低得到2e^-,被还原;
单线桥在方程式的上面画的箭头由反应物的溴元素指向反应物的氯元素.箭头的上面标上2e^-
希望我的回答能对你的学习有帮助!1年前查看全部
- 分析下列氧化还原反应中化合价的变化,指出氧化剂和还原剂,并用单线桥法表示电子转移的方向和数目.
 空空酒瓶1年前3
空空酒瓶1年前3 -
 sammizhou 共回答了10个问题
sammizhou 共回答了10个问题 |采纳率90%得到电子的为还原剂,失去电子的为氧化剂
1、氧化剂:CL2 还原剂:Fe
2、氧化剂:cuo 还原剂:co
3、氧化剂:Al 还原剂:H2So4
4、氧化剂:cl+ 还原剂:o- 4为歧化反应,问题有误吧1年前查看全部
- 双线桥法和单线桥法的区别
 xdkx1年前1
xdkx1年前1 -
 littlemhy 共回答了17个问题
littlemhy 共回答了17个问题 |采纳率100%表示氧化还原反应的双线桥法与单线桥法的区别是:连接的对象不同,
1、单线桥是一条线从还原剂出发箭头指向氧化剂,并在线的上方表示出转移电子的个数,只简单表示电子转移的个数和方向.
2、双线桥法,是两条线一条由氧化剂指向还原产物,线的上方表示得失电子的个数,及化合价升降.
另一条线由还原剂指向氧化产物,线的上方表示得失电子的个数,及化合价升降.
单线桥法简单,双线桥法表示的更全面.两者都表示了氧化还原的本质.1年前查看全部
- 怎样用单线桥法表示氧化还原反应
 zhjgenius1年前1
zhjgenius1年前1 -
 7759171 共回答了17个问题
7759171 共回答了17个问题 |采纳率88.2%从升价元素(还原剂)指向将价元素(氧化剂) 在线桥上写“转移xe-” 这个转移电子数和双线桥中任何一支上的得到电子数或失去电子数是一样的.1年前查看全部
- 单线桥法我只有一个地方不知道,就是不知道怎么在线上标出电子转移总数,电子转移总数怎么计算的呢?举个例子算算电子转移总数好
单线桥法我只有一个地方不知道,就是不知道怎么在线上标出电子转移总数,电子转移总数怎么计算的呢?举个例子算算电子转移总数好吗?
比如Cl2+2NaOH=NaCl+NaClO+H2O,用单线桥法标出反应的电子转移方向与数目 wxfx12151年前2
wxfx12151年前2 -
 哗啦1162 共回答了25个问题
哗啦1162 共回答了25个问题 |采纳率92%电子转移总数是根据化合价得来的
例子中的cl由0变到+1和-1,所以是一个cl得了另一个cl的电子,总共转移了一个电子1年前查看全部
- 在化学方程式配平中怎么使用单线桥法
在化学方程式配平中怎么使用单线桥法
一直都不会使用单线桥法,麻烦哪位仁兄可以教我一下, dtwxs19861年前1
dtwxs19861年前1 -
 蜜语柔情 共回答了16个问题
蜜语柔情 共回答了16个问题 |采纳率87.5%常用的配平化学方程式的方法有:
(1)最小公倍数法:
在配平化学方程式时,观察反应前后出现”个数”较复杂的元素,先进行配平.先计算出反应前后该元素原子的最小公倍数,用填化学式前面化学计量数的方法,对该原子进行配平,然后观察配平其他元素的原子个数,致使化学反应中反应物与生成物的元素种类与原子个数都相等.
例如:在P+O2――P2O5反应中先配氧:最小公倍数为10,得化学计量数为5与2,P+5O2――2P2O5;再配平磷原子,4P+5O2==2P2O5.
(2)观察法:
通过对某物质的化学式分析来判断配平时化学计量数的方法.
例如:配平Fe2O3+CO――Fe+CO2.在反应中,每一个CO结合一个氧原子生成CO2分子,而Fe2O3则一次性提供三个氧原子,因而必须由三个CO分子来接受这三个氧原子,生成三个CO2分子即Fe2O3+3CO――Fe+3CO2,最后配平方程式Fe2O3+3CO==2Fe+3CO2,这种配平方法是通过观察分析Fe2O3化学式中的氧原子个数来决定CO的化学计量数的,故称为观察法.
(3)奇数变偶数法:
选择反应前后化学式中原子个数为一奇一偶的元素作配平起点,将奇数变成偶数,然后再配平其他元素原子的方法称为奇数变偶数法.
例如:甲烷(CH4)燃烧方程式的配平,就可以采用奇数变偶数法:CH4+O2――H2O+CO2,反应前O2中氧原子为偶数,而反应后H2O中氧原子个数为奇数,先将H2O前配以2将氧原子个数由奇数变为偶数:CH4+O2――2H2O+CO2,再配平其他元素的原子:CH4+2O2==2H2O+CO2.
(4)归一法:
找到化学方程式中关键的化学式,定其化学式前计量数为1,然后根据关键化学式去配平其他化学式前的化学计量数.若出现计量数为分数,再将各计量数同乘以同一整数,化分数为整数,这种先定关键化学式计量数为1的配平方法,称为归一法.
例如:甲醇(CH3OH)燃烧化学方程式配平可采用此法:CH3OH+O2――H2O+CO2,显然决定生成H2O与CO2的多少的关键是甲醇的组成,因而定其计量数为1,这样可得其燃烧后生成H2O与CO2的分子个数:CH3OH+O2――2H2O+CO2.然后配平氧原子:CH3OH+3/2O2===2H2O+CO2,将各计量数同乘以2化分为整数:2CH3OH+3O2==4H2O+2CO2.
需要注意的是,不论用何种方法配平化学方程式,只能改动化学式前面的化学计量数,而决不能改动化学式中元素右下角的数字.因为改动元素符号右下角的数字即意味着改动反应物与生成物的组成,就可能出现根本不存在的物质或改变了原有化学变化的反应物或生成物,出现根本不存在的化学变化.
最常见的就这几种1年前查看全部
- 氯气与氢氧化钠反应的单线桥法为什么是1个电子不是两个?
 junjun20065101年前3
junjun20065101年前3 -
 什么最搞笑 共回答了23个问题
什么最搞笑 共回答了23个问题 |采纳率91.3%Cl2 + 2 NaOH = NaCl + NaClO + H2O
此反应中,Cl2中氯的化合价为0,降低为NaCl 中的-1价Cl ,Cl2作氧化剂.
Cl2中氯的化合价为0,升高为NaClO 中的+1价Cl ,Cl2作还原剂.
所以Cl2既是氧化剂又是还原剂.
从后面的生成1 NaCl来看,每1个 Cl2反应(虽有两个原子)却只有一个Cl原子化合价降低为NaCl 中的-1价Cl 得到1个电子,另一个Cl原子化合价升高为NaClO 中的+1价Cl 失去1个电子,所以单线桥法桥上标出的当然是1个电子了.1年前查看全部
- 单线桥法电子转移数目怎么算?请童鞋们说的具体点哈,
 suda51971年前3
suda51971年前3 -
 yeguohua7713980 共回答了24个问题
yeguohua7713980 共回答了24个问题 |采纳率91.7%找到被氧化或被还原的那个原子,然后找到被氧化或被还原后的那个原子,算出一个原子的电子转移数目,最后乘以被氧化或被还原的原子数目就行了.希望我的解释够清楚1年前查看全部
- 关于氧化还原方程式氯化铁(FeCl3) 和 铁(Fe) 生成氯化亚铁(FeCl2)若用单线桥法该怎么画
 莉莎551年前4
莉莎551年前4 -
 对面儿 共回答了23个问题
对面儿 共回答了23个问题 |采纳率91.3%你的问题比较深.而且这个反应比较特殊 我们从浅入深,先举个其他例子
首先 一般氧化还原反应满足如下条件 化合价不交叉 举个例子 一个反应中 反应物的硫元素有+4+6 生成物有0,-2 将这个化合价写成下图
+4 -2
+6 0 化合价小的写在上(只要按顺序从大到小就行),然后画箭头从左指向右,表示由该化合价的反应物生成生成物.
在此条件中 +4到0 +6到-2 是不可以的,因为箭头交叉 ,这就是只靠拢 不交叉原则
而在你的反应中,反应的实质不是这样的.它的第一步反应是2Al+6H2O===2Al(OH)3+3H2 H2O全部作为氧化剂
然后是NaOH和氢氧化铝反应,NaOH不做氧化剂 这是高考易错点
如有不清楚请追问 我表述可能不大好1年前查看全部
- 人教版高一必修一化学方程式化学方程式、离子方程式、单线桥法表示都要.纳、铝、铁、铜、硅、氯、氮、硫的.
 阴阳rr1年前2
阴阳rr1年前2 -
 yoyo9142003 共回答了20个问题
yoyo9142003 共回答了20个问题 |采纳率85%1、硫酸根离子的检验: BaCl2 + Na2SO4 = BaSO4↓+ 2NaCl
2、碳酸根离子的检验: CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
5、铁片与硫酸铜溶液反应: Fe + CuSO4 = FeSO4 + Cu
6、氯化钙与碳酸钠溶液反应:CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl
7、钠在空气中燃烧:2Na + O2 △ Na2O2
钠与氧气反应:4Na + O2 = 2Na2O
8、过氧化钠与水反应:2Na2O2 + 2H2O = 4NaOH + O2↑
9、过氧化钠与二氧化碳反应:2Na2O2 + 2CO2 = 2Na2CO3 + O2
10、钠与水反应:2Na + 2H2O = 2NaOH + H2↑
11、铁与水蒸气反应:3Fe + 4H2O(g) = F3O4 + 4H2↑
12、铝与氢氧化钠溶液反应:2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑
13、氧化钙与水反应:CaO + H2O = Ca(OH)2
14、氧化铁与盐酸反应:Fe2O3 + 6HCl = 2FeCl3 + 3H2O
15、氧化铝与盐酸反应:Al2O3 + 6HCl = 2AlCl3 + 3H2O
16、氧化铝与氢氧化钠溶液反应:Al2O3 + 2NaOH = 2NaAlO2 + H2O
17、氯化铁与氢氧化钠溶液反应:FeCl3 + 3NaOH = Fe(OH)3↓+ 3NaCl
18、硫酸亚铁与氢氧化钠溶液反应:FeSO4 + 2NaOH = Fe(OH)2↓+ Na2SO4
19、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3
20、氢氧化铁加热分2Fe(OH)3 △ Fe2O3 + 3H2O↑
21、实验室制取氢氧化铝:Al2(SO4)3 + 6NH3?H2O = 2Al(OH)3↓ + 3(NH3)2SO4
22、氢氧化铝与盐酸反应:Al(OH)3 + 3HCl = AlCl3 + 3H2O
23、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 + NaOH = NaAlO2 + 2H2O
24、氢氧化铝加热分2Al(OH)3 △ Al2O3 + 3H2O
25、三氯化铁溶液与铁粉反应:2FeCl3 + Fe = 3FeCl2
26、氯化亚铁中通入氯气:2FeCl2 + Cl2 = 2FeCl3
27、二氧化硅与氢氟酸反应:SiO2 + 4HF = SiF4 + 2H2O
硅单质与氢氟酸反应:Si + 4HF = SiF4 + 2H2↑
28、二氧化硅与氧化钙高温反应:SiO2 + CaO 高温 CaSiO3
29、二氧化硅与氢氧化钠溶液反应:SiO2 + 2NaOH = Na2SiO3 + H2O
30、往硅酸钠溶液中通入二氧化碳:Na2SiO3 + CO2 + H2O = Na2CO3 + H2SiO3↓
31、硅酸钠与盐酸反应:Na2SiO3 + 2HCl = 2NaCl + H2SiO3↓
32、氯气与金属铁反应:2Fe + 3Cl2 点燃 2FeCl3
33、氯气与金属铜反应:Cu + Cl2 点燃 CuCl2
34、氯气与金属钠反应:2Na + Cl2 点燃 2NaCl
35、氯气与水反应:Cl2 + H2O = HCl + HClO
36、次氯酸光照分2HClO 光照2HCl + O2↑
37、氯气与氢氧化钠溶液反应:Cl2 + 2NaOH = NaCl + NaClO + H2O
38、氯气与消石灰反应:2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O
39、盐酸与硝酸银溶液反应:HCl + AgNO3 = AgCl↓ + HNO3
40、漂白粉长期置露在空气中:Ca(ClO)2 + H2O + CO2 = CaCO3↓ + 2HClO
41、二氧化硫与水反应:SO2 + H2O ≈ H2SO3
42、氮气与氧气在放电下反应:N2 + O2 放电 2NO
43、一氧化氮与氧气反应:2NO + O2 = 2NO2
44、二氧化氮与水反应:3NO2 + H2O = 2HNO3 + NO
45、二氧化硫与氧气在催化剂的作用下反应:2SO2 + O2 催化剂 2SO3
46、三氧化硫与水反应:SO3 + H2O = H2SO4
47、浓硫酸与铜反应:Cu + 2H2SO4(浓) △ CuSO4 + 2H2O + SO2↑
48、浓硫酸与木炭反应:C + 2H2SO4(浓) △ CO2 ↑+ 2SO2↑ + 2H2O
49、浓硝酸与铜反应:Cu + 4HNO3(浓) = Cu(NO3)2 + 2H2O + 2NO2↑
50、稀硝酸与铜反应:3Cu + 8HNO3(稀) △ 3Cu(NO3)2 + 4H2O + 2NO↑
51、氨水受热分NH3?H2O △ NH3↑ + H2O
52、氨气与氯化氢反应:NH3 + HCl = NH4Cl
53、氯化铵受热分NH4Cl △ NH3↑ + HCl↑
54、碳酸氢氨受热分NH4HCO3 △ NH3↑ + H2O↑ + CO2↑
55、硝酸铵与氢氧化钠反应:NH4NO3 + NaOH △ NH3↑ + NaNO3 + H2O
56、氨气的实验室制取:2NH4Cl + Ca(OH)2 △ CaCl2 + 2H2O + 2NH3↑
57、氯气与氢气反应:Cl2 + H2 点燃 2HCl
58、硫酸铵与氢氧化钠反应:(NH4)2SO4 + 2NaOH △ 2NH3↑ + Na2SO4 + 2H2O
59、SO2 + CaO = CaSO3
60、SO2 + 2NaOH = Na2SO3 + H2O
61、SO2 + Ca(OH)2 = CaSO3↓ + H2O
62、SO2 + Cl2 + 2H2O = 2HCl + H2SO4
63、SO2 + 2H2S = 3S + 2H2O
64、NO、NO2的回收:NO2 + NO + 2NaOH = 2NaNO2 + H2O
65、Si + 2F 2 = SiF4
66、Si + 2NaOH + H2O = Na2SiO3 +2H2↑
67、硅单质的实验室制法:粗硅的制取:SiO2 + 2C 高温电炉 Si + 2CO
(石英沙)(焦碳) (粗硅)
粗硅转变为纯硅:Si(粗) + 2Cl2 △ SiCl4
SiCl4 + 2H2 高温 Si(纯)+ 4HCl
金属非金属
1、 Na与H2O反应:
2Na+2H2O=2NaOH+H2↑
2、 Na2O2与H2O反应(标出电子转移):
2Na2O2+2H2O=4NaOH+O2↑
3、 Na2O2与CO2反应:
2Na2O2+2CO2=2Na2CO3+O2↑
4、 NaHCO3受热分
2NaHCO3=Na2CO3+CO2↑+H2O
5、 Na2CO3中通入过量CO2:
Na2CO3+CO2+H2O=2NaHCO3
6、 足量NaOH与CO2反应:
2NaOH+CO2=Na2CO3+H2O
7、 NaOH与过量CO2反应:
2NaOH+CO2=Na2CO3+H2O
Na2CO3+CO2+H2O=2NaHCO3
8、 氯与H2O反应:
Cl2+H2O=HCl+HClO
9、 氯气与NaOH溶液(标出电子转移):
Cl2+NaOH=NaCl+NaClO+H2O
10、工业制漂白粉:
2Cl2+Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
11、漂白粉漂白原理:
Ca(ClO)2+H2O=2HClO+CaCO3↓
12、实验室制Cl2(标出电子转移):
4HCl+MnO2=Cl2↑+MnCl2+2H2O
13、NaI溶液中滴加氯水:
2NaI+Cl2=I2+2NaCl
14、Mg与热水反应:
Mg+2H2O=Mg(OH)2+H2↑
15、AlCl3中滴入NaOH:
AlCl3+3NaOH=Al(OH)3↓+3NaCl
继续滴入NaOH,沉淀溶
NaOH+Al(OH)3=NaAlO2+2H2O
16、Al2O3与NaOH反应:
Al2O3+2NaOH=2NaAlO2+H2O
17、实验室制H2S
FeS+H2SO4=FeSO4+H2S↑
18、H2O2中加少量MnO2:(标出电子转移)
2H2O2=2H2O+O2↑
19、H2S长期放置变浑浊或H2S不完全燃烧:
2H2S+O2=2H2O+2S↓
20、H2S充分燃烧:
2H2S+3O2=2H2O+2SO2
21、H2S与SO2反应:(标出电子转移)
2H2S+SO2=3S↓+2H2O
22、SO2通入氯水中褪色:
SO2+Cl2+H2O=2HCl+H2SO4
23、Cu与浓H2SO4,加热:(标出电子转移)
Cu+2H2SO4=CuSO4+SO2↑+2H2O
24、木炭与浓H2SO4共热:(标出电子转移)
C+2H2SO4=2H2O+CO2↑+2SO2↑
25、工业上制粗硅:
SiO2+2C=Si+2CO↑ 条件:电炉内
26、石英与NaOH反应:
SiO2+2NaOH=Na2SiO3+H2O
27、玻璃工业上两个反应:
Na2CO3+SiO2=Na2SiO3+CO2↑
CaCO3+SiO2=CaSiO3+CO2↑
28、水玻璃中加CO-2-产生沉淀:
2H2O+Na2SiO3+CO2=Na2CO3+H4SiO41年前查看全部
- 电子转移的单线桥法怎么弄氯气与氢氧化钠的反应怎么标
 七慕侠1年前1
七慕侠1年前1 -
 kg21tm1 共回答了20个问题
kg21tm1 共回答了20个问题 |采纳率90%首先这条箭头是标在反应物之间的
只要从失去电子的元素开始划线,箭头指向得电子的元素上,再在线中间标出具体几个转移几个电子即可1年前查看全部
- 如图单线桥法中,为什么Na会向Cl2转移电子?
 誰为谁心痛1年前1
誰为谁心痛1年前1 -
 KAMECHAN 共回答了12个问题
KAMECHAN 共回答了12个问题 |采纳率91.7%因为钠最外层为一个电子'而氯最外层为七个电子.为了形成稳定结构.
故钠失去一个电子,氯得到一个电子.
或者说钠的金属性强,易失电子,氯非金属性强,易得电子1年前查看全部
- 化学中高一必修一中电子转移使用的单线桥法和双线桥法杂回事?麻烦介绍的详细些!
 苦涩季节1年前1
苦涩季节1年前1 -
 高松婴 共回答了18个问题
高松婴 共回答了18个问题 |采纳率100%化学反应是有得失电子的 反应是在反应物中发生 生成生成物 单线桥法就是 将电子在反应过程中 真正的电子转移去向标出来了 例如 氢气和氧气反应 是氢原子失去电子 氧原子得到电子 那么单线桥就是氢原子指向氧原子 同...1年前查看全部
- 考试时,单线桥法方程式右边的元素化合价没标,只标了左边的化合价,给不给对?
 willtalk1年前1
willtalk1年前1 -
 dawei6575868 共回答了22个问题
dawei6575868 共回答了22个问题 |采纳率100%本来就是只标左边的1年前查看全部
- 在氧化还原反应中,电子转移的表示方法通常用单线桥法和双线桥法.试分析这两种表示方法的特征,并填空.
在氧化还原反应中,电子转移的表示方法通常用单线桥法和双线桥法.试分析这两种表示方法的特征,并填空.
(1)标单线桥:KIO3+6HI═KI+3I2↑+3H2O______ 氧化产物与还原产物物质的量之比=______
(2)配平化学方程式及标双线桥
______Fe+______HNO3(稀)=______Fe(NO3)2+______NO↑+______H2O反应中______,氧化剂与还原剂的物质的量之比______. 受伤的羊羊1年前1
受伤的羊羊1年前1 -
 谭博文 共回答了18个问题
谭博文 共回答了18个问题 |采纳率94.4%解题思路:(1)I元素的化合价由+5价降低为0,I元素的化合价由-1价升高为0,转移5e-;(2)Fe元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,结合电子守恒、原子守恒分析.(1)KIO3+6HI═KI+3I2↑+3H2O中,I元素的化合价由+5价降低为0,I元素的化合价由-1价升高为0,转移5e-,单线桥表示电子转移的方向和数目为
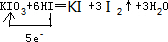 ,氧化产物与还原产物均为碘,物质的量之比为5:1,
,氧化产物与还原产物均为碘,物质的量之比为5:1,
故答案为: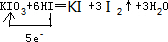 ;5:1;
;5:1;
(2)Fe元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,结合电子守恒、原子守恒可知,反应为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,
还原剂为Fe,氧化剂为HNO3,由电子守恒可知氧化剂与还原剂的物质的量之比为2:3,双线桥表示为 ,
,
故答案为:3;8;3;2;4; ;2:3.
;2:3.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子表示方法的考查,题目难度不大.1年前查看全部
大家在问
- 1怎么判断物质的氧化还原性?根据化合价撒?
- 2已知1,8,17,28,41,.组成数列{bn}.试证不存在正整数K和M【1
- 3等比数列bn=aq^n(a.q为常数,且aq不等于0)对任意m存在k,有bm×bm+1=bk,求a、q满足的条件(见下)
- 4一个三角形的三条边长都是整厘米数,第一条边长3厘米,第二条边长8厘米第三条边可能是多少厘米
- 5气旋(低压)过境时,气压先由高变低,再由低变高的过程.为什么
- 6某固体仅由一种元素组成,其密度为5g/cm^3,用X射线研究该固体的结构表明,在棱长为1×10^-7cm
- 7将Mg离子中的铝离子全部除去用什么溶液
- 8形容文雅又礼貌的成语是什么
- 9计算:(50分之1—1)(49分之1—1)(48分之1—1)…(4分之1—1)(3分之1—1)(2分之1—1)
- 10已知点P(x,y)是圆x^2+y^2=2y上的动点,若x+y+a≥0恒成立,求实数a的取值范围.
- 11CaCl2是既含有离子键又含有非极性键的化合物吗?为什么?
- 12两阻值相同的灯泡串联在某电路中,消耗总功率为10W,若把它们并联在同一电路上,消耗的总功率为_______.
- 13小学六年级上册寒假作业上的英语答案(凤凰出版社)
- 14冰的比热容和水的比热容各是多少?
- 15空气的比热容是多少





