离子的还原性强弱与什么有关
 applefish122022-10-04 11:39:543条回答
applefish122022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 法拉利拖拉机 共回答了24个问题
法拉利拖拉机 共回答了24个问题 |采纳率95.8%- 单质的氧化性强,则其离子的还原性就弱
- 1年前
 付辛博的娘 共回答了350个问题
付辛博的娘 共回答了350个问题 |采纳率- 简单的离子的还原性,可以参照该离子单质的氧化性,如果单质氧化性强的话,那么离子的还原性就很弱了。比如
氧化性 CL2>Br2>I2
还原性I->Br->CL-
要是复杂的离子还原性就要根据主要元素可升降化合价具体问题具体分析了。 - 1年前
 尚良 共回答了31个问题
尚良 共回答了31个问题 |采纳率- 与元素的核外电子排布有关,一般情况氧化性强的单质,离子的还原性就弱。容易得到电子既不容易失去电子,氧化性还原性就是得是电子能力。
- 1年前
相关推荐
- 氢离子和钠离子在细胞内外的交换机制?
 candyfu19831年前1
candyfu19831年前1 -
 一米阳光的飘 共回答了20个问题
一米阳光的飘 共回答了20个问题 |采纳率90%氢离子与钠离子的交换发生在肾近曲小管上皮细胞泌氢重吸收碳酸氢根离子的过程当中.
近曲小管中从肾小囊中滤过的NaHCO3解离为钠离子和碳酸氢根离子,钠离子顺浓度梯度被重吸收入近曲小管上皮细胞中.在近曲小管上皮细胞内含有很多的碳酸酐酶,CO2和水反应生成碳酸,碳酸在碳酸酐酶的作用下分解为氢离子和碳酸氢根离子.氢离子借钠离子氢离子交换体在小管上皮细胞处出细胞,发生钠离子和氢离子的交换.
这种交换是一种继发式主动转运,能量来自于上皮细胞的基底膜上钠钾ATP酶.1年前查看全部
- 氢离子二价铁离子硫酸根离子能共存么?
氢离子二价铁离子硫酸根离子能共存么?
如题
那么氢离子 氯离子 碳酸氢离子能共存么 简单爱你1年前2
简单爱你1年前2 -
 一位村rr 共回答了20个问题
一位村rr 共回答了20个问题 |采纳率80%可以共存.
Fe2+和H+,SO4^2-之间不会发生任何反应,能共存.
但如果把SO4^2-换成NO3-就不能共存了,因为Fe2+能被HNO3氧化为Fe3+
氢离子 氯离子 碳酸氢离子 不能共存,氢离子和碳酸氢离子会反应生成CO2气体1年前查看全部
- 溶液的导电性与离子的种类、阴阳等有什么关系
溶液的导电性与离子的种类、阴阳等有什么关系
给了几种离子,要判断溶液的导电性好差 nb101001年前4
nb101001年前4 -
 zootty 共回答了18个问题
zootty 共回答了18个问题 |采纳率94.4%离子带电或正或负,溶液导电性与离子浓度有关,给出的几个离子要是能够大量共存,溶液的导电性就强;
要是不能大量共存,容易产生沉淀或气体等,溶液导电性就弱.1年前查看全部
- 由水电离出的氢氧根离子浓度=1*10^-13mol/L的无色溶液中,一定能大量共存的离子组是
由水电离出的氢氧根离子浓度=1*10^-13mol/L的无色溶液中,一定能大量共存的离子组是
答案是NO3-、Ba2+、K+、CL-
怎样思考? jifengyu1年前1
jifengyu1年前1 -
 来自银杏之乡 共回答了21个问题
来自银杏之乡 共回答了21个问题 |采纳率95.2%由水电离出的氢氧根离子浓度=1*10^-13mol/L的无色溶液中.
两个条件:1.无色溶液,要排除有色离子,如Fe2+、Fe3+、Cu2+、MnO4-等.
2.由水电离出的氢氧根离子浓度=1*10^-13mol/L,表明水的电离被抑制,溶液是酸性或者是碱性的,要求离子在酸性和碱性条件下都可以共存.
还有就是要求选项中的离子间不能发生反应.1年前查看全部
- 纸层析法分离铁铜离子时,哪一种离子溶解度大,向上移动得快?
纸层析法分离铁铜离子时,哪一种离子溶解度大,向上移动得快?
还有,在***中,是亲脂性强的离子溶解度大,移动得快么? hu_0081年前1
hu_0081年前1 -
 vincent1982 共回答了18个问题
vincent1982 共回答了18个问题 |采纳率88.9%Fe3+移动的快在上面,Cu2+在下面.用氨熏后可以看到下面是蓝色上面是红棕色.
层析时,水是固定相,有机溶剂是移动相,一般来说,亲脂性强的物质在移动相中分配得多,就是移动得快;亲水性的在固定相分配得多,移动得慢1年前查看全部
- 写出下列离子鼓号的化学式1.氧离子 2.+2价的钙 3.两个氢离子 4.氦气 5.氢氧化钙6.硝酸铜 7.碳酸钾 8.硫
写出下列离子鼓号的化学式
1.氧离子 2.+2价的钙 3.两个氢离子 4.氦气 5.氢氧化钙
6.硝酸铜 7.碳酸钾 8.硫酸铵 9.磷酸铵 10.氧化钾
11.氯化铝 12.磷酸 13.碳酸 14.硝酸 15.硫酸 16.氧化镁 倩颖红妆1年前1
倩颖红妆1年前1 -
 vcbc 共回答了12个问题
vcbc 共回答了12个问题 |采纳率91.7%1.O2-
2.Ca2+
3.2H+
4.He
5.Ca(OH)2
6.Cu(NO3)2
7.K2CO3
8.(NH4)2SO4
9.(NH4)3PO4
10.K2O
11.AlCl3
12.H3PO4
13.H2CO3
14.HNO3
15.H2SO4
16.MgO1年前查看全部
- 铜离子与次氯酸根双水解吗?能大量共存吗?铵根离子与碳酸根离子呢?
铜离子与次氯酸根双水解吗?能大量共存吗?铵根离子与碳酸根离子呢?
讲明理由. 风也有ff1年前1
风也有ff1年前1 -
 yetfat 共回答了19个问题
yetfat 共回答了19个问题 |采纳率100%铵根离子与碳酸根离子可以水解 但只是不完全水解 是可以大量共存的 但要注意的是写化学方程式的时候要用可逆符号 不能用沉淀和气体符号 还有像铵根和醋酸根、碳酸氢根这些都是不完全水解 是可以共存的
至于铜离子与次氯酸根 是不可以水解的1年前查看全部
- 氯离子能跟次氯酸根离子大量共存吗?
 随便大佬1年前1
随便大佬1年前1 -
 bingxueyu 共回答了15个问题
bingxueyu 共回答了15个问题 |采纳率93.3%氯离子与次氯酸根离子在中性、碱性溶液中可大量共存,酸性条件下会发生归中反应生成Cl2,所以酸性不能共存.
Cl-+ ClO- + 2H+ =Cl2 + H2O1年前查看全部
- 含硝酸跟离子的溶液中,有氨根离子、钡离子、亚铁离子、溴离子.在这溶液中,为什么能大量共存?亚铁不是会水解吗?
 谷熙1年前2
谷熙1年前2 -
 clematis 共回答了18个问题
clematis 共回答了18个问题 |采纳率88.9%NH4+ + H2O ==可逆== NH3 H2O + H+
Fe2+ + 2H2O ==可逆== Fe(OH)2 + 2H+
NH4+ 和 Fe2+ 在溶液中都会发生小程度的水解,它们产生的H+会互相抑制对方的水解,减弱水解的程度,此时可以认为NH4+和Fe2+可以大量共存
若是将其中一种离子换成弱酸银离子如HCO3-
HCO3- + H2O ==可逆== H2CO3 + OH-
这个时候产生的OH-会和阳离子水解产生的H+反应,使得阴阳离子双方的水解程度增大,此时不能共存1年前查看全部
- 离子方程式有系数的根离子用画括号吗
 buwm1年前1
buwm1年前1 -
 Zww浪子 共回答了9个问题
Zww浪子 共回答了9个问题 |采纳率88.9%一般不需要
如
2Fe + 6H+ = 2 Fe3+ + 3H2↑
2H+ + SO4 2- + Ba2+ + 2OH- = BaSO4↓ + 2H2O1年前查看全部
- (1)0.5mol/L的Fe2(SO4)3溶液中,Fe离子的物质的量浓度为().
(1)0.5mol/L的Fe2(SO4)3溶液中,Fe离子的物质的量浓度为().
(2)V升Fe2(SO4)3溶液中含有a克SO4根离子,SO4根离子的物质的量浓度为();取此溶液0.5V升,Fe离子的物质的量浓度为();用水稀释至2V升,稀释后溶液中Fe离子的物质的量浓度为(). 苍浪影月1年前1
苍浪影月1年前1 -
 阿鹏阿鹏 共回答了17个问题
阿鹏阿鹏 共回答了17个问题 |采纳率94.1%(1)1mol/L
你可以设溶液体积为1L,则Fe2(SO4)3的物质的量为0.5mol
则Fe离子的物质的量为2*0.5mol=1mol
Fe离子的物质的量浓度为1mol/1L=1mol/L
你如果熟练地话 直接用比例 会更快
(2)a/(96V)mol/L a/(144V)mol/L a/(576V)mol/L
含有a克SO4根离子,则SO4根离子的物质的量为a/96mol
SO4根离子的物质的量浓度为a/96mol /1L=a/(96V)mol/L
则Fe离子的物质的量为a/96mol *2/3=a/144mol
Fe离子的物质的量浓度为a/(144V)mol/L
取此溶液0.5V升,Fe离子的物质的量浓度不变
则Fe离子的物质的量浓度为a/(144V)mol/L
0.5V升中Fe离子的物质的量为a/288mol
用水稀释至2V升,
稀释后溶液中Fe离子的物质的量浓度为n(Fe3+)/2V= a/(576V)mol/L1年前查看全部
- 氯水中含有的分子有什么?离子有什么?硝酸银溶液滴入氯水的化学方程式?硝酸银溶液滴入食盐溶液的化学方程式?硝酸银溶液滴入溴
氯水中含有的分子有什么?离子有什么?硝酸银溶液滴入氯水的化学方程式?硝酸银溶液滴入食盐溶液的化学方程式?硝酸银溶液滴入溴化钠溶液的化学方程式?
 ddwiner1年前3
ddwiner1年前3 -
 xiefeng6 共回答了18个问题
xiefeng6 共回答了18个问题 |采纳率94.4%Cl2 HClO H2O
H+ Cl- ClO- OH-
AgNO3+HCl==AgCl↓+HNO3
AgNO3+NaCl==AgCl↓+NaNO3
AgNO3+NaBr==AgBr↓+NaNO31年前查看全部
- 氯水中存在的离子和分子
 伤心愉快的宇1年前3
伤心愉快的宇1年前3 -
 yyllcy 共回答了20个问题
yyllcy 共回答了20个问题 |采纳率85%水分子 氯离子 氢离子 没有氯化氢分子 氯化氢在水中是完全电离的1年前查看全部
- 叶绿素中主要含有的金属离子是什么
 jiaofu_no1年前2
jiaofu_no1年前2 -
 koyori0946 共回答了20个问题
koyori0946 共回答了20个问题 |采纳率100%镁离子1年前查看全部
- 我们老师说氢离子不可以和碳酸根离子、氢氧离子、碳酸氢根离子共存 但为什么检验氢离子的时候可以加碳酸钙
 红楼阁1年前1
红楼阁1年前1 -
 guanai 共回答了17个问题
guanai 共回答了17个问题 |采纳率82.4%氢离子不可以和碳酸根离子、氢氧离子、碳酸氢根离子共存是因为氢离子和它们都会发生反应,分别生成水和二氧化碳、水、水和二氧化碳(此处生成物与碳酸根生成数量不一样).
而检验氢离子,一般情况下就是检验溶液是否是酸性,除了弱酸和某些中强酸,浓度足够的情况下其他酸都可以与碳酸钙发生反应,并生成二氧化碳(有明显现象——气泡)、水以及相应的盐.所以,可以用碳酸钙检验氢离子的存在与否.
另外,检验就是需要发生肉眼可观的化学变化现象,以证明这种东西的存在,这就要考虑到什么不能共存,选择不能共存又会发生明显化学反应现象的药品进行混合,才能证明啊1年前查看全部
- 碳酸氢钠与过量二氧化碳反应的离子化学式怎么写?
 Teddylong1年前1
Teddylong1年前1 -
 桃之妖精 共回答了14个问题
桃之妖精 共回答了14个问题 |采纳率92.9%搞笑啊,碳酸氢钠和二氧化碳没反应的
应该是碳酸钠吧
离子方程式就是OH- + CO2 == HCO3-1年前查看全部
- 离子共存问题:物质的氧化性和还原性是怎样影响离子的共存的?
 战二十1年前3
战二十1年前3 -
 davenxie 共回答了21个问题
davenxie 共回答了21个问题 |采纳率95.2%总的来说就是具有强氧化性的离子和强还原性的离子不能在一起,否则就反应而不能共存.
那么那些是具有强氧化性的离子呢?MnO4(-)
Cr2O7(2-)
CrO4(2-)
Fe(3+)
O2(2-)过氧根
NO3(-)需配合H+
ClO-不体现氧化性,HClO是强氧化剂,这个记住,配合H+
MnO4- 酸性越强 氧化性越高.
具还原性的离子,
S2- 、Fe2+、I-、SO32- 等这些处于低价态的离子1年前查看全部
- 某盐的溶液中含有Na+、Mg2+、Cl-、SO42-四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl-为0
某盐的溶液中含有Na+、Mg2+、Cl-、SO42-四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl-为0.4mol,则SO42-物质的量为( )
A. 0.1mol
B. 0.3mol
C. 0.5mol
D. 0.15mol 我爱柳红花绿1年前1
我爱柳红花绿1年前1 -
 问斑猪 共回答了24个问题
问斑猪 共回答了24个问题 |采纳率87.5%解题思路:溶液中的离子遵循电荷守恒,即溶液中的阳离子带电的电荷量与阴离子所带电电荷量相等.设SO42-物质的量为n,则根据电荷守恒:
0.2mol×1+0.4mol×2=0.4mol×1+2n,
解得n=0.3mol.
故选B.点评:
本题考点: 电解质在水溶液中的电离.
考点点评: 本题考查溶液中的电荷守恒知识,可以根据所学知识进行回答,难度不大.1年前查看全部
- 已知短周期的离子.原子序数为a的A显正二价,原子序数为b的B显正一价,原子序数为c的C显负三价,原子序数为d的D显负一价
已知短周期的离子.原子序数为a的A显正二价,原子序数为b的B显正一价,原子序数为c的C显负三价,原子序数为d的D显负一价.都具有相同的电子结构,则下列叙述正确的是
原子半径A>B>D>C
原子序数d>c>b>a
离子半径C>D>B>A
单质的还原性A>B>D>C Ellenie1年前1
Ellenie1年前1 -
 北极狐888 共回答了13个问题
北极狐888 共回答了13个问题 |采纳率92.3%他们的离子具有相同的电子结构(这一点很重要),不妨设该电子结构有x个电子.
A显+2价,所以是失去两个电子,所以a=x+2,
B显+1价,所以是失去一个电子,所以b=x+1,
C显-3价,所以是得到三个电子,所以c=x-3,
D显-1价,所以是得到一个电子,所以d=x-1,
原子序数为:a>b>d>c.
另外,还可以推出,AB比CD的周期数大1.
所以,原子半径:B>A>C>D.
还原性:B>A>C>D
离子半径:由于核外电子排列相同,所以,原子序数越大(核电荷数越多),则半径越小,所以:C>D>B>A1年前查看全部
- 分别在强酸溶液,强碱溶液中什么离子不能共存
 a4480757031年前2
a4480757031年前2 -
 eamison 共回答了16个问题
eamison 共回答了16个问题 |采纳率81.3%强酸:
氢氧根,偏铝酸根,碳酸根,碳酸氢根,醋酸根,亚硫酸根,亚硫酸氢根,氟离子,硫离子,硫氢根,亚铜离子,次氯酸根,硅酸根等
强碱:
氢离子,铝离子,镁离子,铜离子,亚铁离子,铁离子,铵根离子,碳酸氢根,亚硫酸氢根,硫氢根,汞离子,银离子,亚铜离子等1年前查看全部
- 温室下,在强酸强碱 溶液中为什么以下离子组不能大量共存
温室下,在强酸强碱 溶液中为什么以下离子组不能大量共存
BA2+ FE2+ NO3- BR- moththe1年前2
moththe1年前2 -
 葡桃RAP 共回答了22个问题
葡桃RAP 共回答了22个问题 |采纳率86.4%强碱性条件下就是含有大量的氢氧根离子
亚铁离子遇到氢氧根会变成氢氧化亚铁沉淀..
所以不能大量共存...1年前查看全部
- 如果溶液中含有氢离子,硝酸根离子,钠离子,氯离子则将铁放入溶液中生成三价铁离子还是二价铁离子?
 sizhi41年前4
sizhi41年前4 -
 什么么都有 共回答了12个问题
什么么都有 共回答了12个问题 |采纳率91.7%生成Fe3+
因为溶液中有H+和NO3-,即HNO3,硝酸具有强氧化性,会将Fe氧化到Fe3+.1年前查看全部
- 拉曼能检测水中有哪些离子吗
 sunnylinj1年前1
sunnylinj1年前1 -
 llghh 共回答了16个问题
llghh 共回答了16个问题 |采纳率87.5%单原子离子如钾钠氯离子等--不能,离子本身没有信号,离子和水的络合物信号波数很低,强度很弱,观察不到.
铵根、硫酸根、硝酸根等离子---可以,且信号很强1年前查看全部
- 利用表面增强拉曼检测重金属离子的一种方法是这样的,首先利用巯乙磺酸钠修饰银纳米颗粒,巯乙磺酸钠
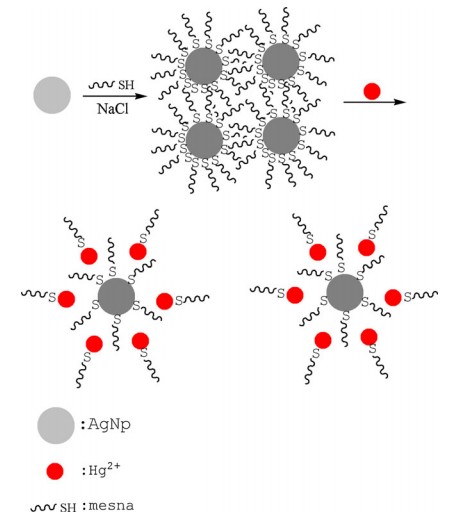
利用表面增强拉曼检测重金属离子的一种方法是这样的,首先利用巯乙磺酸钠修饰银纳米颗粒,巯乙磺酸钠有很强的拉曼信号,银纳米颗粒与巯乙磺酸钠形成的Ag-S共价键.然后在其中加入Hg2+,因为Hg2+与巯乙磺酸钠形成的Hg-S比Ag-S强,这样巯乙磺酸钠就会从银纳米颗粒上脱落,所以就可以通过检测巯乙磺酸钠拉曼信号的变化来判断Hg2+的存在.
我的问题就是,只有Hg2+这一种重金属离子和巯乙磺酸钠形成符合条件的共价键吗?在实际运用中有没有可能别的重金属离子对它有干扰.原理图如下图.请给出详细解答.谢谢.
 让你丫删我贴1年前1
让你丫删我贴1年前1 -
 fay103 共回答了17个问题
fay103 共回答了17个问题 |采纳率82.4%这个主要是利用了Hg和Ag对S(巯基)的亲和性.Hg差不多是最亲S的元素,其他金属争不过他,所以一般来说不会有其他金属干扰了.1年前查看全部
- 下列离子组在所给条件下能够大量共存的是
下列离子组在所给条件下能够大量共存的是
A 甲基橙呈黄色的溶液中 I- Cl- No3- Na+
D 含大量OH-的溶液中 CO32- Cl- F- K+
为什么 SinoPlato1年前1
SinoPlato1年前1 -
 桃树下的木篱笆 共回答了21个问题
桃树下的木篱笆 共回答了21个问题 |采纳率100%D.因为氢氧根不予碳酸根,氯离子,氟离子,钾离子反应.而A中甲基橙呈黄色则表示溶液中有氢离子,而氢离子与硝酸根一起会具有强氧化性会氧化碘离子1年前查看全部
- 就是物质的量,和离子大量共存的问题的解题方法.最好有例题
 laihuajin1年前1
laihuajin1年前1 -
 tianian01 共回答了13个问题
tianian01 共回答了13个问题 |采纳率84.6%n=m/M
n=v/22.4(标况下的气体)
n=c*v
n=N/NA
离子共存首先看颜色排除有色离子,另外看是酸性还是碱性环境,最后看相互间是否会形成沉淀、气体或者弱电解质1年前查看全部
- 用化学符号怎么表示下列内容?钾离子 钠离子 银离子 钙离子 镁离子 钡离子 锌离子 铝离子 铜离子 亚铁离子 铁离子 氢
用化学符号怎么表示下列内容?
钾离子 钠离子 银离子 钙离子 镁离子 钡离子 锌离子 铝离子 铜离子 亚铁离子 铁离子 氢离子 硫离子 氯离子 氧离子 氟离子
铵根离子 氢氧根离子 硫酸根离子 氯酸根离子 碳酸根离子
硫酸根离子
盐酸 硫酸 硝酸 碳酸 氯酸
氢氧化钠 氢氧化钾 氢氧化钙 氢氧化镁 氢氧化钡 氢氧化锌
氢氧化铝 氢氧化铜 氢氧化铁 氢氧化亚铁
氯化钠 氯化镁 氯化铝 氯化铜 氯化钡 氯化钙 氯化亚铁
氯化铁 氯化锌 氯化银
硫酸铜 硫酸钠 硫酸钾 硫酸铝 硫酸钡 硫酸钙 硫酸亚铁
碳酸钠 碳酸钙 碳酸铵 碳酸钡 碳酸铝
硝酸根 硝酸铵 硝酸钠 硝酸镁 硝酸铝
拜托拉…………
帮帮忙!我才刚刚学呀~!…………
帮帮你们的学妹拉 张无忌俺小弟1年前1
张无忌俺小弟1年前1 -
 chenglu2007 共回答了19个问题
chenglu2007 共回答了19个问题 |采纳率94.7%钾离子K+ 钠离子Na+ 银离子Ag+ 钙离子Ca2+ 镁离子Mg2+ 钡离子Ba2+ 锌离子Zn2+ 铝离子Al3+ 铜离子Cn2+ 亚铁离子Fe2+ 铁离子Fe3+ 氢离子H+ 硫离子S2- 氯离子Cl- 氧离子O2- 氟离子F-
铵根离子NH4+ 氢氧根离子OH- 硫酸根离子SO4 2- 氯酸根离子ClO3- 碳酸根离子 CO3 2-
硫酸根离子 SO4 2-
盐酸HCl 硫酸H2SO4 硝酸HNO3 碳酸H2CO3 氯酸HClO3
氢氧化钠NaOH 氢氧化钾KOH 氢氧化钙Ca(OH)2 氢氧化镁Mg(OH)2 氢氧化钡Ba(OH)2 氢氧化锌 Zn(OH)2
氢氧化铝Al(OH)3 氢氧化铜Cu(OH)2 氢氧化铁Fe(OH)3 氢氧化亚铁Fe(OH)2
氯化钠NaCl 氯化镁MgCl2 氯化铝AlCl3 氯化铜CuCl2 氯化钡BaCl2 氯化钙CaCl2 氯化亚铁FeCl2 氯化铁FeCl3 氯化锌ZnCl2 氯化银AgCl
硫酸铜CuSO4 硫酸钠Na2SO4 硫酸钾K2SO4 硫酸铝Al2(S04)3 硫酸钡BaSO4 硫酸钙CaSO4 硫酸亚铁 FeSO4
碳酸钠Na2CO3 碳酸钙CaCO3 碳酸铵(NH4)2CO3 碳酸钡BaCO3 碳酸铝Al2(CO3)3
硝酸根NO3- 硝酸铵NH4NO3 硝酸钠NaNO3 硝酸镁Mg(NO3)2 硝酸铝Al(NO3)31年前查看全部
- 关于溴,碘离子的检验..望高手回答
关于溴,碘离子的检验..望高手回答
检验溴,碘离子,大家都知道是通入氯气后加入有机溶液,显紫红色说明是碘,显棕红色说明是溴.但原因是什么?生成了什么? 七星票票1年前4
七星票票1年前4 -
 笑忘书0218 共回答了25个问题
笑忘书0218 共回答了25个问题 |采纳率100%溴,碘离子分别被氯氧化成溴,碘单质
其在有机溶液中溶解度较大,能按显色来判别
碘单质为紫色,溴单质为棕红色1年前查看全部
- 因发生氧化还原反应在水溶液中不能大量共存的离子组是A.Ca2+,Cl-,Fe3+ ,CO32-,B.Na+,SO32-,
因发生氧化还原反应在水溶液中不能大量共存的离子组是A.Ca2+,Cl-,Fe3+ ,CO32-,B.Na+,SO32-,NO3-,H+ ,C.Fe3+,Mg2+,Cl-,SO42-,D.Na+,Al3+,SO42-,HCO3-
 jcsea1231年前1
jcsea1231年前1 -
 水光浮动 共回答了21个问题
水光浮动 共回答了21个问题 |采纳率95.2%选择B.
A、Ca2+与CO32-沉淀,Fe3+与CO32-双水解.
B、酸性条件下,NO3-能氧化SO32-,属于氧化还原反应.
C、可以共存.
D、Al3+与HCO3-双水解.1年前查看全部
- 为何不能用加热溶液除去易水解的离子.如加热除去氯化钾中的三价铁离子,不是因为铁离子水解吸热吗.加热不就会促进水解析出沉淀
为何不能用加热溶液除去易水解的离子.如加热除去氯化钾中的三价铁离子,不是因为铁离子水解吸热吗.加热不就会促进水解析出沉淀吗.但为何一定要用双水解原理.
 zhongchuang1231年前1
zhongchuang1231年前1 -
 suantianhuizi 共回答了21个问题
suantianhuizi 共回答了21个问题 |采纳率90.5%水解可逆,除不干净的.除非你把溶液蒸干再加强热,然后溶解,过滤.这样想太麻烦,不如直接加氢氧化钾调ph至沉淀完全.1年前查看全部
- 钾离子 钙离子 钡离子现有 钾离子 钙离子 钡离子 氢氧根离子 醋酸根离子 碳酸根离子 要求组成三种化合物(当然都是碱性
钾离子 钙离子 钡离子
现有 钾离子 钙离子 钡离子 氢氧根离子 醋酸根离子 碳酸根离子 要求组成三种化合物(当然都是碱性)A B C
且碱性A>C>B 求A B C分别是什么 安然20071年前2
安然20071年前2 -
 happy游柚 共回答了21个问题
happy游柚 共回答了21个问题 |采纳率95.2%因为酸性 H2O< H2CO3< CH3COOH,
所以碱性 OH-> CO32-> CH3COO-,
所以碱性 Ba(OH)2 > K2CO3>(CH3COO)2Ca.
即 A 是Ba(OH)2、B是(CH3COO)2Ca、C是K2CO3.
因为BaCO3、CaCO3难溶,所以与CO32-配对的只能是K+.
因为Ca(OH)2微溶,不是最佳组合.所以Ba(OH)2.
则只能是 (CH3COO)2Ca1年前查看全部
- 化学离子共存问题中怎么看离子发生了氧化还原反应?
化学离子共存问题中怎么看离子发生了氧化还原反应?
比如说CLO-离子能氧化S离子 是怎么看出来的? asdsad0uio001年前5
asdsad0uio001年前5 -
 涵玉 共回答了12个问题
涵玉 共回答了12个问题 |采纳率100%要记住一些的
NO3-/H+ 与 Fe2+ S2- I-
MnO4-/H+ 与 Fe2+ S2- I-
ClO- H+ 与S2- I- Fe2+
Fe3+ 与 S2- I-
或者说要记住高中常见的氧化性的离子和还原性的离子
ClO-有强氧化性 S2-还原性1年前查看全部
- 离子共存问题中的氧化还原反应能发生氧化还原反应的离子是不能共存的,『但我不知道怎么判断是否会发生氧化还原反应,怎么判断』
离子共存问题中的氧化还原反应
能发生氧化还原反应的离子是不能共存的,『但我不知道怎么判断是否会发生氧化还原反应,怎么判断』还有是怎么看离子是具有还原性还是氧化性的?求详细解答离子共存中氧化还原反应这一块.(求列出高中化学中会发生氧化还原反应的离子,要详细) sr8k1年前2
sr8k1年前2 -
 男画皮 共回答了22个问题
男画皮 共回答了22个问题 |采纳率90.9%常见的判断氧化性/还原性强弱的方法有:
1.从元素的价态考虑
最高价态——只有氧化性,如Fe3+ H2SO4 KMnO4
最低价态——只有还原性,如金属单质 Cl- S2-
中间价态——既有氧化性有有还原性,如Fe2+ S等
同种元素的价态高,其氧化性较强;价态低,其还原性较强.
2.根据金属活动顺序表判断
金属越活泼,金属单质的还原性越强,其对应离子的氧化性越弱.
单质还原性:按金属活动顺序表的顺序依次减弱.
金属离子氧化性:按金属活动顺序表的顺序依次减弱.(铁指Fe2+)
如氧化性:Ag+ > Hg2+ > Fe3+ > Cu2+ > H+ > Fe2+
3.根据非金属的活泼型判断
非金属性越强,单质的氧化性越强,其对应离子的还原性越弱.
单质氧化性:F2 > Cl2 > Br2 > I2 > S
离子还原性:S2- > I- > Br- > Cl- > F-
4.通过化学反应比较
氧化剂 + 还原剂 → 氧化产物 + 还原产物
氧化性:氧化剂 > 氧化产物
还原剂:还原剂 > 还原产物
5.通过与同一物质反应的产物比较
如:2Fe + 3Cl2 =(点燃) 2FeCl3
3Fe + 2O2 =(点燃) Fe3O4
可得出氧化性Cl2 > O2.
高锰酸根离子、次氯酸根离子、过氧根离子、高铁酸根离子都是强氧化性
硫离子,卤素离子都是青还原性
至于反应的判断,具有氧化性的和具有还原性的一起都会反应
如果一种离子价态还能更高,说明具有还原性,反之亦然1年前查看全部
- 二氧化碳溶于水后也会产生氢离子,二氧化碳是酸吗?下列各组离子属于酸电离产生的是( ) A.H+、NO3-、SO42-
二氧化碳溶于水后也会产生氢离子,二氧化碳是酸吗?下列各组离子属于酸电离产生的是( ) A.H+、NO3-、SO42-
麻烦详细一点.
下列各组离子属于酸电离产生的是( )
A.H+、NO3-、SO42- B.OH-、Ba2+
C.H+、Na+、SO42- D.Na+ 、Ba2+、 Cl- 强飞1年前3
强飞1年前3 -
 妯娌仨人体 共回答了25个问题
妯娌仨人体 共回答了25个问题 |采纳率88%答案选A
二氧化碳溶于水会产生氢离子,CO2+H2O===H2CO3 ,碳酸(H2CO3)是一种二元弱酸,电离常数都很小.氢离子是碳酸产生的.
根据酸的定义--酸:化学上是指在溶液中电离时阳离子完全是氢离子且能使紫色石蕊试液变红的化合物.狭义上也可分为无机酸、有机酸.酸碱质子理论认为:酸是能释放出质子的物质总称为酸.
由此认定二氧化碳不是酸.1年前查看全部
- 1.某研究性学习小组调查发现,甲、乙两工厂排放的污水各含下列离子:H、Cu、K、NO3、OH中的三种离子(两厂有一种相同
1.某研究性学习小组调查发现,甲、乙两工厂排放的污水各含下列离子:H、Cu、K、NO3、OH中的三种离子(两厂有一种相同离子).若将两厂的污水按一定比例混合,沉淀后污水会变成无色澄清中性溶液.下列说法正确的是:
A.OH和Cu来自同一工厂 B.H和OH来自同一工厂
C.Cu和K来自同一工厂 D.H和Cu来自同一工厂
(两厂排放的污水中所含的离子分别是什么?为什么共同含有的离子是NO3-不是K+啊
2.下列离子能在PH=2的无色溶液中大量共存的是()
A .SO4 Fe Na OH
B.K SO4 Cu NO3
C.Cl K SO4 Na
D.Ca Cl CO3 Na
3.下列各组物质,只需用组内溶液相互混合就能鉴别出来的是
A K2SO4 BaCL2 NaNO3 NaCL
B HCL Na2CO3 BaCL2 Na2SO4
C KOH Na2SO4 CuSO4 HCL
D KCL AgNO3 KNO3 NaCL
这个答案是多选的 为什么选B C 白色海浪1年前1
白色海浪1年前1 -
 简单最靠得住 共回答了15个问题
简单最靠得住 共回答了15个问题 |采纳率100%1.甲:H+ Cu2+ NO3- 乙:K+ OH- NO3-
思路:H+与OH-,Cu2+与OH-不共存,可以肯定H+与Cu2+来自同一工厂
污水中的离子一定有阴离子有阳离子(溶液显电中性),阴离子必是NO3-
可确定甲为:H+,Cu2+,NO3-
乙肯定有OH-,K+,排除可知剩下的一种是NO3-
2.pH=2,代表溶液呈酸性,有H+
A中OH-不行,而且Fe离子与OH-反应
D中CO3 2- 不行,且Ca2+与CO3 2-反应
3.B都是无色透明溶液,先用小试管取样,任取一种,分别加入其它试管中,4种情况:
(1)一个有气泡,其他两个无现象.取的是HCl,有气泡的是Na2CO3,.再取Na2CO3分别加入剩余两种试剂的样品,有白色沉淀的是BaCl2,无现象的是Na2SO4.
(2)一个有气泡,一个有沉淀,一个无现象.取的是Na2CO3,有气泡的是HCl,有沉淀的是BaCl2,无现象的是Na2SO4.
(3)一个有沉淀,其他两个无现象.取的是BaCl2,有沉淀的是Na2CO3.再取Na2CO3分别加入剩余两种试剂,有气泡的是HCl,无现象的是Na2SO4.
(4)均无现象.取的是Na2SO4.在剩下的三种中任取一种,加入其它两种,情况有三:
1.一个有气泡,一个无现象.取的是HCl,有气泡的是Na2CO3,无现象的是BaCl2.
2.一个有气泡,一个有沉淀.取的是Na2CO3,有气泡的是HCl,有沉淀的是BaCl2.
3.一个无现象,一个有沉淀.取的是BaCl2,无现象的是HCl,有沉淀的是Na2CO3.
C CuSO4,是蓝色溶液,其他均为无色,可直接判断出CuSO4.
将CuSO4加入剩余三种溶液中,有蓝色沉淀生成的是KOH.之后将剩下的两种先后加入有沉淀的试液中,蓝色沉淀消失的是HCl,无现象的是Na2SO4.
好累---1年前查看全部
- 求离子的ph值室温下,两种ph不同的氢氧化钠溶液,其ph值分别为8和10 ,将这两种溶液等体混合后溶液的氢离子物质的量浓
求离子的ph值
室温下,两种ph不同的氢氧化钠溶液,其ph值分别为8和10 ,将这两种溶液等体混合后溶液的氢离子物质的量浓度最接近 0.02摩尔每升.为什么? 麻辣仙子1年前1
麻辣仙子1年前1 -
 mmddbhu 共回答了13个问题
mmddbhu 共回答了13个问题 |采纳率92.3%碱等体积混合PH=PH大的-0.3
所以PH=8 和PH=10的氢氧化钠混合PH=9.7≈0.02mol/L1年前查看全部
- 若某溶液中有 亚铁离子 和 碘离子 共存,要氧化碘离子 而又不氧化 亚铁离子,可以加入的试剂是 1 氯气 2 高锰酸钾
若某溶液中有 亚铁离子 和 碘离子 共存,要氧化碘离子 而又不氧化 亚铁离子,可以加入的试剂是 1 氯气 2 高锰酸钾 3氯化铁 4氯化氢
选哪个?为什么? 锦色华年谁与共1年前2
锦色华年谁与共1年前2 -
 smartegg 共回答了20个问题
smartegg 共回答了20个问题 |采纳率100%选第3个氯化铁.
氯气和高锰酸钾同属于强氧化剂,能把碘和亚铁离子都氧化.
而FeCL3中的Fe3+能与I-发生反应:2Fe3++2I-=2Fe2+ + I2
使得碘离子被氧化,你看方程式,Fe3+自身被还原为Fe2+,那Fe3+肯定不能氧化亚铁离子了.
至于氯化氢,它没有氧化性,加进去没用,
还有什么不会的可以继续Hi我1年前查看全部
- 溶液中有五种离子,其中各离子个数比为Cl-:(SO4)2-:Fe3+:K+:M=2:3:1:3:1
溶液中有五种离子,其中各离子个数比为Cl-:(SO4)2-:Fe3+:K+:M=2:3:1:3:1
则M为 A;(CO3)2-
B;Mg2+
C;Na+
D;Ba2+ 桐子1年前4
桐子1年前4 -
 云雨雾烟 共回答了11个问题
云雨雾烟 共回答了11个问题 |采纳率100%根据题意知
阴离子有Cl-,SO4(2-),分别是2个,3个.于是负电荷是2*1+3*2=8个
阳离子有Fe(3+)与K+,分别是1个,3个,于是正电荷一共是1*3+3*1=6个
由于溶液中正负电荷相等,所以,剩下的一定是1个带有两个正电荷的离子
选项为Mg(2+)与Ba(2+),然而,Ba(2+)与SO4(2-)不能够共存,所以选择
B,Mg(2+)1年前查看全部
- 亚铁氰化钾检验三价铁离子?有蓝色普鲁士蓝沉淀,化学式是KFe[Fe(CN)6]·6H2O.可以提供下吗?(方程要配平呀!
亚铁氰化钾检验三价铁离子?
有蓝色普鲁士蓝沉淀,化学式是KFe[Fe(CN)6]·6H2O.
可以提供下吗?(方程要配平呀!) gzh_lee1年前1
gzh_lee1年前1 -
 快乐星球 共回答了17个问题
快乐星球 共回答了17个问题 |采纳率94.1%普鲁士蓝沉淀的化学式应该是Fe4[Fe(CN)6]3
3[Fe(CN)6](2-)+4Fe3+ KFe[Fe(CN)6]·6H2O1年前查看全部
- 从500ml0.5mol/L的NaOH溶液中取出50ml,溶液物质的量为?Na离子的个数为?(为什么提取的50ml与原本
从500ml0.5mol/L的NaOH溶液中取出50ml,溶液物质的量为?Na离子的个数为?(为什么提取的50ml与原本溶液的
为什么提取的50ml与原本溶液的物质的量不一样呢? 西虹霞1年前1
西虹霞1年前1 -
 bianyuanno1 共回答了19个问题
bianyuanno1 共回答了19个问题 |采纳率94.7%物质的量为0.5*0.05=0.025mol Na离子个数为0.025mol 前面说的是溶度~后面要你求的是物质的量~这是两个完全不同的概念~1年前查看全部
- 分别为一价和两价的静止铜离子,经过同一电场加速后,在垂直经过同一偏转电场,然后落到一光屏上.图略,离子重力不计.A 离子
分别为一价和两价的静止铜离子,经过同一电场加速后,在垂直经过同一偏转电场,然后落到一光屏上.图略,离子重力不计.A 离子经加速电场时,二价铜离子受到电场力的冲量大.B 在偏转电场中电场力对两种离子做功一样多.C 两种铜离子打在屏上速度一样大.D 两种铜离子打在屏上的两个不同点.选择?理由?
 oqbydxm1年前1
oqbydxm1年前1 -
 88212853 共回答了15个问题
88212853 共回答了15个问题 |采纳率93.3%A对 .二价离子受力大,距离相同,FS大,做功大,动能大,速度大,MV大,由冲量定理,冲量大
D要看情况.可以计算(字数限制不能细说)电场中偏转距离相同.所以,如屏紧挨偏转电场边沿,D不对,否则对
楼上想当然1年前查看全部
- 电解池的离子放电请解释一下什么是离子放电?怎么放 谁放电 举个例子
 西夏的梦1年前3
西夏的梦1年前3 -
 csodifupaosufd 共回答了20个问题
csodifupaosufd 共回答了20个问题 |采纳率95%离子得失电子:阴离子失电子、阳离子得电子,使离子所带电荷数降低.1年前查看全部
- 晶体(包括离子,原子,分子,金属)发生物理变化(比如固体液化)是不是只克服分子间作用力?
 liaops-1021年前1
liaops-1021年前1 -
 guoting501 共回答了13个问题
guoting501 共回答了13个问题 |采纳率100%只有共价晶体分子才要克服分子间作用力
其他不存在分子结构,离子晶体克服离子键,金属克服金属键,原子晶体克服共价键1年前查看全部
- H2C2O4是一种二元弱酸,NaHC2O4溶液显酸性.现测得某溶液中存在的离子有C2O42-、
H2C2O4是一种二元弱酸,NaHC2O4溶液显酸性.现测得某溶液中存在的离子有C2O42-、
HC2O4-、OH-、Na+、H+.下列判断正确的是
A.该溶液的溶质只能是Na2C2O4或NaHC2O4或两者的混合物
B.该溶液可能显酸性、碱性或中性
C.溶液中一定存在c(Na+) >c(HC2O4-)
D.溶液中一定存在c(H+) -c(OH-) >c(HC2O4- ) - c(Na+) 路人孤寂1年前1
路人孤寂1年前1 -
 血雨降尘 共回答了20个问题
血雨降尘 共回答了20个问题 |采纳率90%A,错,可以是H2C2O4和Na2C2O4或H2C2O4和NaHC2O4的混合物
B,对,这几种物质,单独或按不同的比例组合,就能使溶液显酸性、碱性或中性
C,错,若是H2C2O4和Na2C2O4或H2C2O4和NaHC2O4的混合物,此式就不成立
D,对,按电荷守恒: c(H+) +c(Na+)= c(OH-) +c(HC2O4- )+2c(C2O42-)
所以:c(H+) -c(OH-) = c(HC2O4- )+2c(C2O42-)-c(Na+)
等式的右边减去2c(C2O42-),等号就可以换成的>
即:c(H+) -c(OH-) >c(HC2O4- ) - c(Na+)1年前查看全部
- 氢离子和锰酸根离子共存吗
 3433721601年前1
3433721601年前1 -
 TT3916197 共回答了28个问题
TT3916197 共回答了28个问题 |采纳率85.7%不能共存
锰酸根在酸性条件下立即歧化
生成高锰酸和二氧化锰
3MnO4( 2-)+4H(+)=2MnO4(-)+MnO2+2H2O
其中锰酸根中锰为正6价
高锰酸根中锰为正7价
二氧化锰中锰为正4价1年前查看全部
- K+.NH4+.硫酸根离子,锰酸根离子在酸性溶液中为什么不能共存
K+.NH4+.硫酸根离子,锰酸根离子在酸性溶液中为什么不能共存
MnO4- jaysun1年前1
jaysun1年前1 -
 想念你的日子 共回答了25个问题
想念你的日子 共回答了25个问题 |采纳率92%酸性条件下高锰酸根离子具有很强的氧化性(你所提供的题目不是锰酸根离子而是高锰酸根离子)
而NH4+具有强还原性!相互作用可以得到硝酸根离子!1年前查看全部
- 在不确定液体中检验硫酸根离子为什么要先加盐酸?
 爱驹的卫1年前2
爱驹的卫1年前2 -
 xxxatb 共回答了20个问题
xxxatb 共回答了20个问题 |采纳率95%加盐酸可排除Ag+、SO32-、CO32-离子的干扰
而加硝酸会把SO32-氧化成SO42-
所以只能加盐酸1年前查看全部
- 1.常温下,在含有氢离子、氯离子和三价铁离子的溶液中加入下列离子后,溶液中各种离子仍能大量共存的是
1.常温下,在含有氢离子、氯离子和三价铁离子的溶液中加入下列离子后,溶液中各种离子仍能大量共存的是
A.硝酸根离子 B.CLO离子 C.碳酸氢根离子 D.碘离子
2.在下列化合物中,只有在水溶液中才能导电的电解质是
A.氯化钠 B.酒精 C.硫酸 D.硫酸钾
麻烦给出正确答案和解释. 别封啦prhlt0id1年前4
别封啦prhlt0id1年前4 -
 mrdawei0 共回答了16个问题
mrdawei0 共回答了16个问题 |采纳率93.8%1:
a.正确
b会和cl-发生氧化还原反应、
c会和h+反应生成co2
d会和fe3+发生氧化还原反应到I和fe2+
2:
a熔融状态下也行.
b是非电解质,水溶液中肯定不导电
c正确
d与a一样.
加油咯!1年前查看全部
- 1、离子是否一定能溶解在水中2、不是离子是否一定不能溶解在水中3、2H2O2==催化剂==2H2O+O2↑是不是氧化还原
1、离子是否一定能溶解在水中
2、不是离子是否一定不能溶解在水中
3、2H2O2==催化剂==2H2O+O2↑是不是氧化还原反应,若是,那什么是还原剂?什么是氧化剂?
要原因 萧亚轩1年前4
萧亚轩1年前4 -
 A_nan 共回答了19个问题
A_nan 共回答了19个问题 |采纳率78.9%1.离子不一定能溶解在水中.比如氧离子,过氧离子就不能在水中存在.
2.不是离子也可以溶解在水中,比如乙醇,甲醛,氯气(溶于水后,发生反应,生成HCl,HCLO,也有一部分氯气分子溶于水,使溶液显出黄绿色).
3.过氧化氢发生了歧化反应,氧化剂还原剂都是它本身.1年前查看全部
大家在问
- 1阿房宫赋原文和一句一句翻译,还要有讲解,
- 2表达友情的诗句
- 3光速快还是音速快?
- 4读书时的感受作文400字
- 5高山气候区什么季节降水?
- 6班级趣事,600字的作文,急呀,
- 7读书的好处作文400字左右特急.
- 8基因表达载体中含有启动子和内含子,错在哪?
- 9英语作文上学方式
- 10在尝试中成长作文600字 不要抄的,常见的
- 11班级趣事作文600字不要复制其他的答案
- 12在尝试中成长作文600字,自己写的!速度啊!
- 13关于成长作文600字只要是关于成长的,都可以
- 14圆的最小旋转角为几度
- 15两道题目①【(x+y)(x-y)-(x-y)的平方】÷2y ②【(a+b)的平方-b(2a+b)-8a】÷2
