精制氯化钠是纯净物吗?
 千家驹2022-10-04 11:39:543条回答
千家驹2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 虚拟与现实之间 共回答了16个问题
虚拟与现实之间 共回答了16个问题 |采纳率81.3%- 没有绝对的纯净物,所谓的纯净物仅仅是相对而言的.
所以精制氯化钠在一定的程度上来讲,是纯净物 - 1年前
 祝君好运 共回答了6个问题
祝君好运 共回答了6个问题 |采纳率- 不是,还含有氯化镁,氯化钙 ,氯化钠应该是占百分之70多吧
- 1年前
 愚愚乐 共回答了42个问题
愚愚乐 共回答了42个问题 |采纳率- 额,一开始看错了,当成精致食盐了,精制氯化钠是提纯过的氯化钠,一定程度上来说是纯净物吧
- 1年前
相关推荐
- 加碘食盐 配料表:精制盐、碘酸钾
加碘食盐 配料表:精制盐、碘酸钾
主要成分:氯化钠
碘含量(以I计):35㎎/㎏
一袋500g规格的加碘食盐中含碘酸钾(KIO3)的质量是____㎎. miss_weed1年前5
miss_weed1年前5 -
 guotuanghua 共回答了16个问题
guotuanghua 共回答了16个问题 |采纳率100%碘酸钾(KIO3) 分子量:214 碘分子量:127
碘含量(以I计)35mg/kg ,所以500g规格碘含量17.5mg
碘酸钾的质量:214÷127×17.5=29.5mg1年前查看全部
- 在工业电解食盐水制烧碱时为什么要用精制饱和的食盐水溶液?
在工业电解食盐水制烧碱时为什么要用精制饱和的食盐水溶液?
既然是溶液,为什么没有电离出氢氧根离子和氢离子?
为什么有些电解质溶液的电离,水也会跟着电离,出现氢离子和氢氧根离子?
我没学好.
 柳生静云紫霞光1年前1
柳生静云紫霞光1年前1 -
 变色仙人球 共回答了20个问题
变色仙人球 共回答了20个问题 |采纳率90%因为食盐水中混有Ca2+、Mg2+、SO42-等杂质,一要使产品纯度不高,二是电解产生的OH-会与Ca2+、Mg2+结合生成难溶物质,堵塞阳离子交换膜.
在电解质溶液中,水也会电离生成氢离子和氢氧根离子,氢离子和氢氧根离子也会参与放电.1年前查看全部
- 氯碱工业中,食盐水的精制除杂顺序
 风之凋1年前1
风之凋1年前1 -
 eelemon 共回答了25个问题
eelemon 共回答了25个问题 |采纳率96%通常用BaCl2除去SO42-,Na2CO3除去Ca2+,NaOH除去Mg2+.基本步骤为:
①粗盐溶解、沉降除去泥沙;②加入过量的氯化钡除去硫酸根离子;③再加入过量氢氧化钠溶液除去镁离子;④加入过量碳酸钠溶液除去钙离子;⑤过滤所有沉淀;⑥然后加入适量盐酸除去过量的碳酸根离子和氢氧根离子;⑦将溶液通过阳离子交换塔以进一步除去少量的钙离子和镁离子,得到精制的食盐水.1年前查看全部
- 小亮妈妈下岗后开了一家糕点店,现有10.2千克面粉,10.2千克鸡蛋,计划加工一般糕点和精制糕点两种产品共50盒.已知加
小亮妈妈下岗后开了一家糕点店,现有10.2千克面粉,10.2千克鸡蛋,计划加工一般糕点和精制糕点两种产品共50盒.已知加工一盒一般糕点需0.3千克面粉和0.1千克鸡蛋;加工一盒精制糕点需0.1千克面粉和0.3千克鸡蛋.
(1)有哪几种符合题意的加工方案?请你帮忙设计出来;
(2)若销售一盒一般糕点和一盒精制糕点的利润分别为1.5元和2元,那么按哪一个方案加工,小亮妈妈可获得最大利润,最大利润是多少? hellmoney1年前3
hellmoney1年前3 -
 xiangyue2006 共回答了30个问题
xiangyue2006 共回答了30个问题 |采纳率90%解题思路:(1)本题可根据“加工一般糕点用的面粉的量+加工精制糕点用的面粉的量≤10.2”来列出不等式组,求出自变量的取值范围,判断出符合条件的方案;
(2)根据一盒一般糕点和精制糕点的利润,我们可看出,制作的精制糕点越多,利润越大,因此找出(1)中精制糕点最多的方案,计算出这个方案的利润即可.(1)设加工一般糕点x盒,则加工精制糕点(50-x)盒,根据题意得
0.3x+0.1(50−x)≤10.2
0.1x+0.3(50−x)≤10.2
解这个不等式组,得24≤x≤26
因为x为整数,所以x=24,25,26.
因此,加工方案有三种:
①加工一般糕点24盒、精制糕点26盒;
②加工一般糕点25盒、精制糕点25盒;
③加工一般糕点26盒、精制糕点24盒.
(2)由题意知,显然精制糕点数越多利润越大,故当加工一般糕点24盒、精制糕点26盒时,可获得最大利润.
最大利润为24×1.5+26×2=88(元).
答:加工一般糕点24盒、精制糕点26盒时,可获得最大利润.最大利润为=88元.点评:
本题考点: 一元一次不等式组的应用.
考点点评: 本题考查一元一次不等式组的应用,将现实生活中的事件与数学思想联系起来,读懂题列出不等式关系式即可求解.1年前查看全部
- 英语翻译特选西峡香菇、西班牙进口特级初榨橄榄油精制.加倍健康,自然食尚
 50213051年前4
50213051年前4 -
 adodoa 共回答了15个问题
adodoa 共回答了15个问题 |采纳率86.7%Preferential West Canyon Mushroom,refined by Spain imported extra virgin olive oil
More health,natural food fashion
仅供参考1年前查看全部
- (2013•衢州)从自然界中获得的粗盐,含有较多的杂质,需要精制.为了除去粗盐中泥沙等不溶性杂质设计了如图A、B、C三个
(2013•衢州)从自然界中获得的粗盐,含有较多的杂质,需要精制.为了除去粗盐中泥沙等不溶性杂质设计了如图A、B、C三个步骤.

(1)B步骤称为______.
(2)C步骤中,当蒸发皿内出现较多固体时,应该______(填字母).
A、移去酒精灯,停止搅拌
B、移去酒精灯,用玻璃棒继续搅拌
C、继续加热蒸干水分,再移去酒精灯. tuoge1年前1
tuoge1年前1 -
 有人吧 共回答了15个问题
有人吧 共回答了15个问题 |采纳率100%解题思路:(1)B操作是将不溶于液体的固体与液体分离的操作.
(2)根据蒸发操作停止加热的时机进行分析解答.(1)B步骤为过滤操作,是将不溶于液体的泥沙与食盐水分离的操作.
(2)在蒸发操作中,当蒸发皿内出现较多固体时,应移去酒精灯停止加热,用玻璃棒继续搅拌,利用余热把剩余滤液蒸干.
故答案为:(1)过滤;(2)B.点评:
本题考点: 氯化钠与粗盐提纯;过滤的原理、方法及其应用;蒸发与蒸馏操作.
考点点评: 本题难度不大,掌握粗盐提纯的原理、一般步骤、注意事项等即可正确解答本题.1年前查看全部
- 某食盐溶液中含有钙离子镁离子等杂质离子,现设计实验,采用常见的试剂,精制食盐溶液.回答下列问题:
某食盐溶液中含有钙离子镁离子等杂质离子,现设计实验,采用常见的试剂,精制食盐溶液.回答下列问题:
(1)操作:依次向溶液中加入足量的( )溶液和足量的( )溶液,过滤,向滤液中加入适量的( ) jjlaopo1年前3
jjlaopo1年前3 -
 lyn800 共回答了11个问题
lyn800 共回答了11个问题 |采纳率72.7%(1)操作:依次向溶液中加入足量的( 氢氧化钠 )溶液和足量的( 碳酸钠 )溶液,过滤,向滤液中加入适量的( 稀盐酸 )1年前查看全部
- 精制石油时,用氢氧化钠中和石油终残留的硫酸.80克含量为10%的氢氧化钠溶液,能中和多少克硫酸
 newsky21001年前1
newsky21001年前1 -
 日子325 共回答了17个问题
日子325 共回答了17个问题 |采纳率100%2NaOH+H2SO4=Na2SO4+2H20
80.98
80*10%.x
80/8=98/x
x=9.81年前查看全部
- 下列分离或提纯物质的方法错误的是 A.用渗析的方法精制氢氧化铁胶体 B.用加热的方法提纯含有少量碳酸氢钠的碳酸钠 C.用
下列分离或提纯物质的方法错误的是
A.用渗析的方法精制氢氧化铁胶体 B.用加热的方法提纯含有少量碳酸氢钠的碳酸钠 C.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡 D.用盐析的方法分离、提纯蛋白质  凤栖梧1年前1
凤栖梧1年前1 -
 dum2000 共回答了17个问题
dum2000 共回答了17个问题 |采纳率76.5%C
考查物质分离和提纯
硫酸钡和碳酸钡都是难溶性物质,C不正确,其余都是正确的,答案选C。1年前查看全部
- 电解饱和食盐水时,电解之前食盐水需要精制,目的是除去精盐中含有的钙离子、镁离子、硫酸根离子等杂质离子,使用的试剂有:a.
电解饱和食盐水时,电解之前食盐水需要精制,目的是除去精盐中含有的钙离子、镁离子、硫酸根离子等杂质离子,使用的试剂有:a.Na2CO3溶液 b.Ba(OH)2溶液 c.稀盐酸,其合理的加入顺序为______
答案是bac请问为什么不能abc? 莞儿99021年前3
莞儿99021年前3 -
 晴晴666 共回答了20个问题
晴晴666 共回答了20个问题 |采纳率90%加入Ba(OH)2溶液使硫酸根以硫酸钡沉淀形式除去,但又引入新的杂质钡离子.再加入过量Na2CO3溶液可以让钡离子也除去1年前查看全部
- 什么是石油的精制?
 wuzi20081年前1
wuzi20081年前1 -
 瘾姓埋铭 共回答了20个问题
瘾姓埋铭 共回答了20个问题 |采纳率70%各装置生产的油品一般还不能直接作为商品,为满足商品要求,除需进行调合、添加添加剂外,往往还需要进一步精制,除去杂质,改善性能以满足实际要求.常见的杂质有含硫、氮、氧的化合物,以及混在油中的蜡和胶质等不理想成分.它们可使油品有臭味,色泽深,腐蚀机械设备,不易保存.除去杂质常用的方法有酸碱精制、脱臭、加氢、溶剂精制、白土精制、脱蜡等.酸精制是用硫酸处理油品,可除去某些含硫化合物、含氮化合物和胶质.碱精制是用烧碱水溶液处理油品,如汽油、柴油、润滑油,可除去含氧化合物和硫化物,并可除去酸精制时残留的 硫酸.酸精制与碱精制常联合应用,故称酸碱精制.脱臭是针对含硫高的 原油制成的汽、煤、柴油,因含硫醇而产生恶臭.硫醇含量高时会引起油品生胶质,不易保存.可采用催化剂存在下,先用碱液处理,再用空气氧化.加氢是在催化剂存在下,于300~425℃,1.5兆帕压力下加氢,可除去含硫、氮、氧的化合物和金属杂质,改进油品的 储存性能和腐蚀性、燃烧性,可用于各种油品.脱蜡主要用于精制航空煤油、柴油等.油中含蜡,在低温下形成蜡的结晶,影响流动性能,并易于堵塞管道.脱蜡对航空用油十分重要.脱蜡可用分子筛吸附.润滑油的精制常采用溶剂精制脱除不理想成分,以改善组成和颜色.有时需要脱蜡.白土精制一般放在精制工序的 最后,用白土(主要由二氧化硅和三氧化二铝组成)吸附有害的物质.石油精致一般采取以下几种方法 酸精制法 碱精制法 脱蜡法 加痒法 脱臭法 白土精致法 溶剂精致法1年前查看全部
- 为了消除碘缺乏病,我国政府规定居民的食用盐必须是加碘盐.如图是一种市售碘盐包装袋上的部分说明.试回答: XX牌精制碘盐
为了消除碘缺乏病,我国政府规定居民的食用盐必须是加碘盐.如图是一种市售碘盐包装袋上的部分说明.试回答:
(1)碘酸钾中碘的化合价为______;XX牌精制碘盐
配料:氯化钠、碘酸钾(KIO3)
含碘:30mg/kg
食用方法:勿长时间炖炒
贮藏方法:避光、避热、密封、防潮
(2)“含碘量”中的碘是指(填序号)______:
A.碘酸钾B.碘元素C.碘分子D.碘离子
(3)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是______.
(4)根据你的生活经验写出碘酸钾的一点物理性质______. 天来客1年前1
天来客1年前1 -
 ahong134513 共回答了21个问题
ahong134513 共回答了21个问题 |采纳率95.2%解题思路:(1)根据在化合物中正负化合价代数和为零,进行解答.
(2)“含碘量”中的“碘”不是以单质、氧化物、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
(3)根据加碘盐图中标签信息(食用方法和贮藏指南)进行分析解答.
(4)根据食盐的物理性质进行分析推测碘酸钾的物理性质即可.(1)根据在化合物中正负化合价代数和为零,钾元素显+1,氧元素显-2,设碘酸钾(KIO3)中碘元素的化合价为x,则 (+1)+x+(-2)×3=0,x=+5.
(2)“含碘量”中的碘不是以单质、分子、原子、离子等形式存在,这里所指的“碘”是强调存在的元素,与具体形态无关;故选B.
(3)根据加碘盐图中标签信息,勿长时间炖炒、避热等,可得碘酸钾的一种化学性质是:受热易分解或受热不稳定.
(4)从食盐我外观可以推知碘酸钾也是白色固体,食盐能在水中溶解可以知道碘酸钾也能溶于水.
故答案为:(1)+5;(2)B;(3)受热易分解或受热不稳定;(4)白色固体或可溶于水.点评:
本题考点: 有关元素化合价的计算;物质的元素组成.
考点点评: 本题难度不大,考查同学们灵活运用所学知识(化合价、元素、物理性质与化学性质等)进行解题的能力.1年前查看全部
- 粗硫酸铜的提纯为什么用双氧水而不用高锰酸钾或者重铬酸钾氧化Fe2+?精制后的硫酸铜溶液为什么要滴几滴稀硫酸调节PH至1-
粗硫酸铜的提纯
为什么用双氧水而不用高锰酸钾或者重铬酸钾氧化Fe2+?
精制后的硫酸铜溶液为什么要滴几滴稀硫酸调节PH至1-2,然后再加热蒸发? liu730961年前1
liu730961年前1 -
 披着uuuu 共回答了17个问题
披着uuuu 共回答了17个问题 |采纳率100%因为双氧水氧化掉杂质后被还原的产物是水,不增加新的杂质,其他的氧化剂不能做到这一点.
精制后的硫酸铜溶液要滴几滴稀硫酸调节PH至1-2,可以除去硫酸铜里其他的一些杂质1年前查看全部
- 【急】高一化学选择题(溴苯精制有关的)
【急】高一化学选择题(溴苯精制有关的)
实验室里用溴和苯反应制取溴苯.得到粗溴苯后,要用如下操作精制:①蒸馏②水洗③用干燥剂干燥④10%氢氧化钠溶液洗.正确操作顺序是()
A①②③④② B②④②③①
C④②③①② D②④①②③
还有③中干燥剂可以用哪些 ruyi0011年前5
ruyi0011年前5 -
 leosdjn 共回答了17个问题
leosdjn 共回答了17个问题 |采纳率82.4%1、水洗洗去溴与苯反应生成的氢溴酸.(HBr易溶于水而其它不易溶于水)
2、用氢氧化钠洗去溴单质(溴和氢氧化钠反应)
3、用水洗去多余的氢氧化钠
4、干燥剂除去多余的水
5、蒸馏分离溴苯与苯(两者沸点不同,苯的沸点小,被蒸馏出,溴苯留在母液中)
干燥剂可以用无水CaCl2、MgSO4、硅胶等1年前查看全部
- (2014•房山区一模)氢溴酸在医药和石化工业上有广泛用途.下图是模拟工业制备氢溴酸粗品及精制的流程:
(2014•房山区一模)氢溴酸在医药和石化工业上有广泛用途.下图是模拟工业制备氢溴酸粗品及精制的流程:

已知:Br2是易挥发、深红棕色的液体;氢溴酸是易挥发、无色液体.
根据上述流程回答下列问题:
(1)反应室①中发生反应的化学方程式为______.
(2)反应室①使用冰水的目的______.
(3)操作I的名称______,操作Ⅱ用到的玻璃仪器有______.
(4)反应室②中加入Na2SO3的目的是______.
(5)工业生产中制得的氢溴酸带有淡淡的黄色.于是甲乙两同学设计了实验加以探究:
①甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为______,若假设成立可观察到的现象为______.
②乙同学假设工业氢溴酸呈淡黄色是因为______,其用于证明该假设成立的方法为______. 紫血清霜1年前1
紫血清霜1年前1 -
 我迷糊 共回答了14个问题
我迷糊 共回答了14个问题 |采纳率92.9%解题思路:流程反应室①中发生反应 SO2+Br2+2H2O=H2SO4+2HBr,经操作Ⅰ蒸馏得硫酸和氢溴酸的粗品(含溴),反应室②中加入Na2SO3还原粗品中的Br2,但会反应生成SO42- 加入氢氧化钡后过滤得硫酸钡沉淀和无色溶液,再蒸馏得到精致的氢溴酸.
(1)Br2具有强氧化性,在溶液中将SO2氧化为H2SO4,自身被还原为HBr;
(2)Br2氧化SO2放出很多热量,Br2和HBr挥发;
(3)由工艺流程可知,操作Ⅰ为互溶的溶液组分的分离,应是蒸馏,操作Ⅱ分离固体与液体,应是过滤;
(4)粗品中可能含有为反应的Br2,应除去Br2;
(5)用KSCN溶液检验Fe3+,滴加KSCN溶液,溶液变成血红色;
由工艺流程可知,溶液中可能含有Br2,可以用CCl4萃取方法检验;流程分析:反应室①中发生反应 SO2+Br2+2H2O=H2SO4+2HBr,经操作Ⅰ蒸馏得硫酸和氢溴酸的粗品(含溴),反应室②中加入Na2SO3还原粗品中的Br2,但会反应生成SO42- 加入氢氧化钡后过滤得硫酸钡沉淀和无色溶液,再蒸馏得到精致的氢溴酸.
(1)Br2具有强氧化性,在溶液中将SO2氧化为H2SO4,自身被还原为HBr,反应方程式为SO2+Br2+2H2O=2HBr+H2SO4,
故答案为:SO2+Br2+2H2O=2HBr+H2SO4;
(2)Br2氧化SO2放出很多热量,Br2和HBr易挥发,使用冰水,降低体系温度,防止Br2和HBr挥发,使反应完全,故答案为:Br2和HBr挥发;
(3)由工艺流程可知,操作Ⅰ为互溶的溶液组分的分离,应是蒸馏,操作Ⅱ分离固体与液体,应是过滤,用到的玻璃仪器有漏斗、玻璃棒、烧杯;故答案为:蒸馏,漏斗、玻璃棒、烧杯;
(4)粗品中可能含有为反应的Br2,加入Na2SO3,除去粗品中未反应完的溴,故答案为:除去粗品中未反应完的溴;
(5)①用KSCN溶液检验Fe3+,取少许溶液滴加KSCN溶液,溶液变成血红色,说明氢溴酸呈淡黄色是因为含Fe3+.故答案为:KSCN溶液;溶液变成血红色;
②由工艺流程可知,溶液中可能含有Br2,证明该假设成立的方法:用玻璃棒蘸取制得的氢溴酸,点在湿润淀粉KI试纸上变蓝(或用胶头滴管取制得的氢溴酸于试管中,滴加CCl4、振荡、静止,下层呈橙红色),证明因含Br2而显黄色;故答案为:含有Br2;用玻璃棒蘸取制得的氢溴酸,点在湿润淀粉KI试纸上变蓝(或用胶头滴管取制得的氢溴酸于试管中,滴加CCl4、振荡、静止,下层呈橙红色),证明因含Br2而显黄色.点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用;制备实验方案的设计.
考点点评: 本题以制备氢溴酸为载体,考查学生对工艺流程的理解、物质的分离提纯等基本操作、离子检验、物质性质等,难度中等,是对知识的综合运用,需学生具有扎实的基础知识与灵活运用知识解决问题的能力.1年前查看全部
- 粗盐的精制实验中,必须要用到的一组仪器是
粗盐的精制实验中,必须要用到的一组仪器是
A.量筒、酒精灯、漏斗、玻璃棒
B.烧杯、漏斗、坩埚、玻璃棒
C.烧杯、酒精灯、玻璃棒、漏斗、蒸发皿
D.铁架台、烧杯、胶头滴管、酒精灯 无梦无心1年前4
无梦无心1年前4 -
 jbnh 共回答了21个问题
jbnh 共回答了21个问题 |采纳率71.4%A的量筒B的坩埚D的胶头滴管不用
选C1年前查看全部
- 方糖是一种用细砂糖精制成的长方体糖块.为了测定出它的密度,除了一些这种糖块外还有下列器材:天平、量筒、毫米刻度尺、水、白
方糖是一种用细砂糖精制成的长方体糖块.为了测定出它的密度,除了一些这种糖块外还有下列器材:天平、量筒、毫米刻度尺、水、白砂糖、小勺、镊子、玻璃棒.利用上述器材可有多种测量方法,请你答出两种测量方法,要求写出:
(1)测量的主要步骤及所测的物理量;
(2)用测得的物理量表示密度的式子. coolpy1年前1
coolpy1年前1 -
 小周二娃 共回答了17个问题
小周二娃 共回答了17个问题 |采纳率88.2%解题思路:这是一道设计实验的题目,首先要根据实验的目的确定实验的原理依据,这里我们依然要靠密度的公式来进行测量.设计步骤时要根据所提供的器材想出测量方糖的质量与体积的方法,尤其是测体积的方法,因为方糖是溶于水的,所以它的体积测量是本题中的难点.方糖的质量较小,实际操作中为了减小误差,我们可同时取多块同样的糖进行测量.方法一:
(1)主要实验步骤:
①用天平测出3块方糖的质量m;
②用毫米刻度尺测出其中一块的长a、宽b、高c.
(2)方糖密度表达式:ρ=[m/V]=[m/3abc];
方法二:
(1)主要实验步骤:
①用天平测出3块方糖的质量m;
②向量筒里倒入适量的水,记下水的体积V1;
③将方糖放入量筒内的水中,马上读出这时水和方糖的总体积V2.
(2)方糖密度表达式:ρ=
m
V2−V1.
方法三:
(1)主要实验步骤:
①用天平测出3块方糖的质量m;
②向量筒里倒入适量的水并放入白砂糖,用玻璃棒搅动制成白砂糖的饱和溶液,记下饱和溶液的体积V1;
③把3块方糖放入量筒内的饱和溶液中,记下饱和溶液和方糖的总体积V2.
(2)方糖密度表达式:ρ=
m
V2−V1.点评:
本题考点: 设计实验测密度.
考点点评: 设计这一实验,重点在于突破方糖体积测量这一难点,并根据实际想出不同的测量方法.方糖的特点是溶于水,但当水成为饱和溶液时则不再溶解.白砂糖呈粉末状,必要时可用量筒测它的体积,这些都是我们可利用的特点.1年前查看全部
- 用什么方法精制Fe(OH)3胶体?
用什么方法精制Fe(OH)3胶体?
注意不是向蒸馏水中加入Fecl3那种方法 是精制
 45fdsa561年前1
45fdsa561年前1 -
 mingh0505 共回答了19个问题
mingh0505 共回答了19个问题 |采纳率100%渗析的方法.即用半透膜“过滤”将Fe(OH)3胶体置于半透膜内,然后将半透膜置于蒸馏水中,再更换蒸馏水多次,即可1年前查看全部
- 实验室制浓硫酸、浓硝酸的混合物与苯反应制取硝基苯.得到粗产品后,要选用如下几步操作对粗产品进行精制:
实验室制浓硫酸、浓硝酸的混合物与苯反应制取硝基苯.得到粗产品后,要选用如下几步操作对粗产品进行精制:
①蒸馏
②水洗
③用干燥剂进行干燥
④用10%的NaOH溶液洗涤.
正确的操作步骤是( )
A. ①②@④②
B. ②④②③①
C. ④②③①②
D. ③④①②③ xmz13131年前1
xmz13131年前1 -
 patpat21 共回答了18个问题
patpat21 共回答了18个问题 |采纳率88.9%解题思路:根据硝基苯中混有酸,酸能与碱反应以及硝基苯不溶于水来分析;要除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤,最后用无水CaCl2干燥、蒸馏得到纯硝基苯,故选:B;
点评:
本题考点: 苯的性质.
考点点评: 本题主要考查了有机物的性质与物质的分离,难度不大,抓住有机物的性质与物质的分离方法是解题的关键.1年前查看全部
- 高中范围内,下列反应方程式侯式制碱法炼钢的脱碳脱硫反应热还原法制镁精制饱和食盐水:钙镁铁硫酸根离子煤的液化泡沫灭火器反应
高中范围内,下列反应方程式
侯式制碱法
炼钢的脱碳脱硫反应
热还原法制镁
精制饱和食盐水:钙镁铁硫酸根离子
煤的液化
泡沫灭火器反应
混凝法净水
钢铁生锈 iom_xd3b_ve688f1年前4
iom_xd3b_ve688f1年前4 -
 进士 共回答了19个问题
进士 共回答了19个问题 |采纳率94.7%1第一步:CO2 + NH3 + NaCl + H2O = NaHCO3 + NH4Cl
第二部:NaHCO3 (加热)=Na2CO3 + CO2↑+ H2O
2炼钢主要是用氧化剂把生铁里过多的碳和其它杂质氧化而除去,常用的氧化剂:空气、氧气或氧化铁,降低碳量:C+FeO==CO+Fe-热量;
脱硫:炉渣脱硫
气化去硫:3(Fe2O3)+CaS=CaO+6(FeO)+SO2↑
3碳热还原:MgO+C=Mg+CO
4加入足量NaCO3,去沉淀,之后加入BaCl2,去沉淀,之后蒸馏使其饱和(这个不一定对)
5直接液化
间接液化:高温液化、低温液化
6、Al2(SO4)3+6NaHCO3==3Na2SO4+2Al(OH)3↓+6CO2↑
7混凝法:在混凝剂的作用下,使废水中的胶体和细微悬浮物凝聚成絮凝体,然后予以分离除去的水处理法.
8在潮湿的空气中:4Fe + 3O2 + XH2O ==== 2Fe2O3·XH2O
铁的缓慢氧化:4Fe+3O2=2Fe2O31年前查看全部
- 【高一化学】精制食盐水去除杂质的基础问题
【高一化学】精制食盐水去除杂质的基础问题
食盐水除去各种杂质成为精制食盐水,而最后一步要加HCL就能把氢氧根和碳酸跟除掉,变成了精制食盐水.但为什么他不说加稀HCL,而是加HCL? LY-wangxiao1年前5
LY-wangxiao1年前5 -
 林零四 共回答了23个问题
林零四 共回答了23个问题 |采纳率91.3%主要考虑稀HCL加入会带入大量的水,会大量稀释精制食盐水,降低的盐水的浓度,这样盐水的浓度和质量指标又不会达标了.另外,稀释后的溶液也下降了酸碱中和反应速度.1年前查看全部
- 精制粗盐第三步:蒸发如果蒸发皿中有液滴飞溅,原因是-----,应该采取的措施是---当蒸发皿出现大量固体时,应-----
精制粗盐
第三步:蒸发
如果蒸发皿中有液滴飞溅,原因是-----,应该采取的措施是---
当蒸发皿出现大量固体时,应--------蒸干 lylcl1年前2
lylcl1年前2 -
 丫头不拽 共回答了17个问题
丫头不拽 共回答了17个问题 |采纳率94.1%1 蒸发样品时受热不均匀导致暴沸 应用玻璃棒搅拌
2 应停止加热,利用余热把样品蒸干(节省能源)1年前查看全部
- 关于氯化钠的电解计算已知氯化钠在60摄氏度的溶解度是37.1度.现电解60摄氏度的精制饱和食盐水1371克.经分析,电解
关于氯化钠的电解计算
已知氯化钠在60摄氏度的溶解度是37.1度.现电解60摄氏度的精制饱和食盐水1371克.经分析,电解后的溶液密度为1.37克每毫升,其中含有氯化钠20克,试计算电解后所得溶液中氢氧化钠的物质的量浓度;电解过程中得到的氢气的体积. jingjiren11年前1
jingjiren11年前1 -
 闪光糖果 共回答了17个问题
闪光糖果 共回答了17个问题 |采纳率100%60摄氏度是氯化钠溶解度37.1g
说明100g水中溶解37.1g氯化钠达到饱和
则1371g氯化钠饱和溶液中含有氯化钠371g,水1000g
371g NaCl电解后剩余 20g,说明有 351g NaCl被电解消耗
2NaCl + 2H2O --(通电)→ H2↑ + Cl2↑ + 2NaOH
117-------36----------------2-------71-------80
351g-------x----------------y--------z--------a
解得:
x = 108g(物质的量6mol)
y = 6g(物质的量3mol)
z = 213g(物质的量3mol)
a = 240g(物质的量6mol)
反应后剩余水质量=1000g - 108g = 892g
生成NaOH物质的量6mol(240g)
反应后溶液体积 = (240g + 892g)/ 1.37g/ml = 826.28 ml
则NaOH物质的量浓度 = 6mol / 0.82628L = 7.26 mol/L
氢气物质的量 = 3mol
换算成标准状况下体积 = 22.4L/mol * 3mol = 67.2L1年前查看全部
- 关于纯净物与混合物1.下列物质中,属于纯净物的是A.蔗糖水 B.精制的食盐水 C.无水酒精 D.蜡烛燃烧后的生成物有必要
关于纯净物与混合物
1.下列物质中,属于纯净物的是
A.蔗糖水 B.精制的食盐水 C.无水酒精 D.蜡烛燃烧后的生成物
有必要加简洁理由 jackghl1年前4
jackghl1年前4 -
 maskyh 共回答了19个问题
maskyh 共回答了19个问题 |采纳率89.5%C
A 蔗糖和水 当然不是纯净了
B 食盐水 和A一样,并且食盐里面还含有碘
D 蜡烛燃烧后的生成物为二氧化碳和水 也不是纯净物1年前查看全部
- 将粗盐提纯,精制盐质量分数偏小的原因
 楼主你好坏1年前1
楼主你好坏1年前1 -
 feiyang0329 共回答了13个问题
feiyang0329 共回答了13个问题 |采纳率100%粗盐未完全溶解、滤液的损失1年前查看全部
- 粗盐的精制步骤中过滤装置要注意什么
 iuhxq1年前1
iuhxq1年前1 -
 play4ever 共回答了23个问题
play4ever 共回答了23个问题 |采纳率91.3%1滤纸边缘低于漏斗边缘2也面低于滤纸边缘3漏斗管紧靠烧杯壁4玻璃棒抵住三层滤纸侧
应该讲全了~希望对你有帮助.1年前查看全部
- 实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:1蒸馏2 水洗 3用干燥剂干燥 4用0.1的氢氧化钠溶液润洗
实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:1蒸馏2 水洗 3用干燥剂干燥 4用0.1的氢氧化钠溶液润洗 5水洗
正确的顺序是?
答案是24531 每一步的目的都是什么? 老曼娥1年前1
老曼娥1年前1 -
 lmlily020 共回答了21个问题
lmlily020 共回答了21个问题 |采纳率81%2 为了洗掉大量为反应的溴
4 进一步洗掉溴
5 洗掉氢氧化钠
3 去水
1 提取溴苯,1年前查看全部
- 实验室常用溴和苯反应制取溴苯,得到溴苯后,精制的操作顺序是什么,为什么?
实验室常用溴和苯反应制取溴苯,得到溴苯后,精制的操作顺序是什么,为什么?
有溴有苯 qqtxt1年前1
qqtxt1年前1 -
 浪子无坏心 共回答了16个问题
浪子无坏心 共回答了16个问题 |采纳率93.8%制取溴苯一般是溴过量,所以溴苯不会混有苯,而是混有溴.
分离方法:将反应后液体倒入水中,加NaOH溶液,生成NaBr溶于水,在上层,溴苯在下层,用分液漏斗分离,就可以获得纯净的溴苯了.
没看明白吗?一般不可能混有苯,如果有,我可以多加些溴与苯反应生成溴苯,然后才分离溴苯和溴.1年前查看全部
- 食盐的精制实验中如何判断加入的试剂已经过量?
食盐的精制实验中如何判断加入的试剂已经过量?
快 急 醴陵121年前1
醴陵121年前1 -
 NewEinstein 共回答了15个问题
NewEinstein 共回答了15个问题 |采纳率93.3%继续加入同样试剂,不见沉淀即可1年前查看全部
- 电解质量分数为23.4%的精制食盐水1000 g,电解后残液的密度为1.20 g/mL.
电解质量分数为23.4%的精制食盐水1000 g,电解后残液的密度为1.20 g/mL.
电解质量分数为23.4%的精制食盐水1000 g,电解后残液的密度为1.20 g/mL.将产生的H2、Cl2在一定条件下反应制成质量分数为36.5%的盐酸180 g,已知H2、Cl2的利用率均为90%
计算:
(1)制得氯化氢__________mol;
(2)残液中氯化钠的质量
(3)残液中氢氧化钠的质量分数 Ason0071年前1
Ason0071年前1 -
 星的流浪 共回答了21个问题
星的流浪 共回答了21个问题 |采纳率90.5%(1)盐酸溶液中含氯化氢的质量=180g*36.5%=65.7g
则实际生成氯化氢的质量=65.7g/90%=73g
制得氯化氢的物质的量=73g/36.5g/mol=2mol
(2)设反应的氯化钠的物质的量为X
根据氯原子守恒得到如下关系式:
2NaCl~Cl2~2HCl
2 2
X 2mol
X=2mol
残液中氯化钠的质量=1000g*23.4%-2mol*58.5g/mol=117g
(3)根据钠离子守恒得:生成氢氧化钠的物质的量n(NaOH)=消耗氯化钠的物质的量n(NaCl)=2mol
生成氢氧化钠的质量=2mol*40g/mol=80g
所得溶液的质量=1000g-73g=927g
残液中氢氧化钠的质量分数=80g/927g*100%=8.63%
答:1)制得氯化氢___2_______mol;
(2)残液中氯化钠的质量117克
(3)残液中氢氧化钠的质量分数8.63%1年前查看全部
- 将1mol/l Fecl3饱和溶液滴入沸水中,得到红褐色液体,精制该液体的方法是----;向其中滴入过量的稀硫酸,
将1mol/l Fecl3饱和溶液滴入沸水中,得到红褐色液体,精制该液体的方法是----;向其中滴入过量的稀硫酸,
现象是-------;反映的化学方程式、离子方程式------ Hynoo1年前1
Hynoo1年前1 -
 鸟鸟_妖 共回答了11个问题
鸟鸟_妖 共回答了11个问题 |采纳率81.8%精制该液体的方法是渗析
向其中滴入过量的稀硫酸,现象是:红褐色逐渐变浅,最终得到黄色溶液.
化学方程式:2Fe(OH)3 + 3H2SO4 = Fe2(SO4)3 + 6H2O
离子方程式:Fe(OH)3 + 3H^+ = Fe^3+ + 3H2O1年前查看全部
- 为什么用氯化钠饱和溶液反复冲洗食盐能得到精制食盐
 小羊爱吃草141年前3
小羊爱吃草141年前3 -
 coffee8156 共回答了10个问题
coffee8156 共回答了10个问题 |采纳率90%饱和的氯化钠溶液中不能再溶解氯化钠了,但能溶解食盐中的可溶性杂质,1年前查看全部
- 超容易的物理题我们现在吃的都是加了碘的精制盐.一般要求炒菜在出锅前加盐,你知道为什么吗?能根据你所学的知识试着解释一下吗
超容易的物理题
我们现在吃的都是加了碘的精制盐.一般要求炒菜在出锅前加盐,你知道为什么吗?能根据你所学的知识试着解释一下吗? via694x1年前2
via694x1年前2 -
 huangwb168 共回答了21个问题
huangwb168 共回答了21个问题 |采纳率100%我们现在吃的都是加了碘的精制盐.一般要求炒菜在出锅前加盐,你知道为什么吗?能根据你所学的知识试着解释一下吗?
防止碘受热升华.1年前查看全部
- 精制粗溴苯为什么要水洗,碱洗,再水洗,然后干燥蒸馏
 tonycycu1年前1
tonycycu1年前1 -
 blue_sky99 共回答了17个问题
blue_sky99 共回答了17个问题 |采纳率76.5%水洗:除去HBr
碱洗:除去Br2
水洗:除去NaB1年前查看全部
- 胆矾精制五水硫酸铜时边上的绿色物质是什么?
胆矾精制五水硫酸铜时边上的绿色物质是什么?
做胆矾精制五水硫酸铜实验,在第一次结晶时发现蒸发皿边边上有绿色的晶体,而且皿壁上方的溶液干后也变绿色,为什么?是氯化铜吗? 胡说八道之葱花1年前3
胡说八道之葱花1年前3 -
 309515898 共回答了15个问题
309515898 共回答了15个问题 |采纳率93.3%不太可能是氯化铜,除非你的胆矾也太不纯了
应该是因为铜离子浓度高
产生了水合铜离子1年前查看全部
- 实验室用溴和苯反应自取实验室里用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制水洗、用10%的NaOH溶液洗、水洗、
实验室用溴和苯反应自取
实验室里用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制
水洗、用10%的NaOH溶液洗、水洗、用干燥剂干燥、蒸馏,求这每一步的目的
1、水洗洗去溴与苯反应生成的氢溴酸.(HBr易溶于水而其它不易溶于水)
2、用氢氧化钠洗去溴单质(溴和氢氧化钠反应)
3、用水洗去多余的氢氧化钠(理由如1)
4、干燥剂除去多余的水
5、蒸馏分离溴苯与苯,(两者沸点不同,笨的沸点小,被蒸馏出,溴苯留在母液中)
请问第三不怎么理解呀 carefreeman1年前1
carefreeman1年前1 -
 兰色微风 共回答了28个问题
兰色微风 共回答了28个问题 |采纳率89.3%第三部用水洗去多余的氢氧化钠,即加入蒸馏水后,溶液就变成溴苯(下层)和HB的水溶液(上层)的混合液,如果多次水洗上层液体就是极稀HB的水溶液,而下层仍是溴苯,然后用分液漏斗从上口倒出极稀HB的水溶液,下口分离出溴苯(含少量极稀HB的水溶液),再接着第四部干燥操作等.这样说你能意会吗?1年前查看全部
- 关于精制食盐水为什么碳酸钠在精制时顺序要放在氯化钡后面
 周公说梦1年前1
周公说梦1年前1 -
 fww416 共回答了19个问题
fww416 共回答了19个问题 |采纳率89.5%最后溶液中剩下的离子只能有钠离子和氯离子,也就是说钡离子和碳酸根离子是杂质,要祛除的.最后用盐酸中和时,碳酸根离子可以很好的除去,而钡离子则不然.所以碳酸钠在精制时顺序一定要放在氯化钡后面1年前查看全部
- 纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域.工业上以食
纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域.工业上以食盐、氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱.其流程如下:
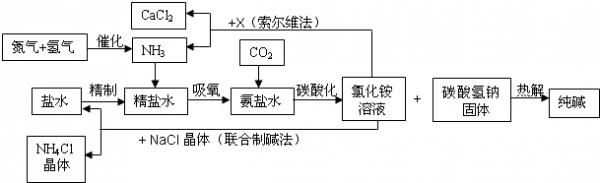
已知有关物质重要反应的化学方程式如下:
①NaCl+NH3+H2O+CO2
NaHCO3↓+NH4Cl△ .
②2NaHCO3
Na2CO3+H2O+CO2↑△ .
③2NH4Cl+X
2NH3↑+CaCl2+2H2O△ .
④NH4Cl═NH3↑+HCl↑
根据以上信息回答下列问题.
(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+、Mg2+等沉积,可以向其一和加入过量纯碱.此时将混合液中不溶物除去的方法是______;溶液中多余的纯碱可以加______试剂来除去.
(2)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通人二氧化碳气体,溶液中会有碳酸氢钠晶体析出.试分析该流程需要加压条件的原因是:______.
(3)在氨碱工业的历史上.如何处理流程中剩余的氯化铵溶液,出现了两种工艺:一是“索尔维法”.即在氯化铵溶液中加入物质X______(填化学式),产生了可循环使用的氨气,和大量固体废弃物氯化钙;二是我国化学家侯德榜发明的“联合制碱法”,即在氯化铵溶液中加入适量氯化钠晶体.降低了氯化氨的______,使氯化铵晶体单独析出得到另一种产品--氮肥.氯化钠溶液则可以循环利用.
(4)在氨碱工业处理剩余的氯化铵溶液时.为何不直接蒸发结晶析出氯化铵固体?答:______. gxb0031年前1
gxb0031年前1 -
 雾海碧竹 共回答了21个问题
雾海碧竹 共回答了21个问题 |采纳率81%解题思路:(1)根据过滤的原理回答前一空;根据碳酸钠的化学性质和除杂的原理回答后一空.
(2)根据气体的溶解度随压强的增大而增大回答.
(3)根据铵盐与碱性物质反应生成氨气的性质回答前一空;根据氯化钠溶液和氯化铵溶液中都含氯离子,氯化钠是制纯碱的原料回答.
(4)根据氯化铵的化学性质回答.(1)过滤是把不溶于液体的固体与液体分开的操作,所以除去液体混合物中的不溶性杂质用过滤的方法;碳酸钠能和盐酸反应生成氯化钠、水、二氧化碳,用盐酸除去多余的碳酸钠不会产生新杂质.
(2)二氧化碳能溶于水,但溶解性较差,气体的溶解度随压强的增大而增大,为了促进更多二氧化碳溶解,使反应更充分,所以需加压条件.
(3)铵盐与碱性物质反应生成氨气,在氯化铵溶液中加入物质X产生了可循环使用的氨气,定是加入的碱性物质,最廉价的碱是熟石灰,所以加入的物质是熟石灰;氯化钠溶液和氯化铵溶液中都含氯离子,在氯化铵溶液中加入适量氯化钠晶体可降低氯化铵的溶解度,使氯化铵晶体单独析出.
(4)不直接蒸发结晶析出氯化铵固体,是因氯化铵受热易分解.
故答案为:(1)过滤;盐酸;
(2)促进更多二氧化碳溶解,使反应更充分;
(3)Ca(OH)2;溶解度;
(4)因氯化铵受热易分解.点评:
本题考点: 过滤的原理、方法及其应用;物质除杂或净化的探究;纯碱的制取.
考点点评: 化学来源于生产、生活,又服务于生产、生活,氨碱工业是初中化学重要的应用之一,是考查重点,常涉及化学方程式的书写,二氧化碳和氨气通入的顺序及原因,反应时析出碳酸氢钠的原因与物质溶解度的关系.1年前查看全部
- 芦丁的精制过程中,为什么要将溶解的芦丁的溶剂从200ML浓缩到50ML?
 血煞手1年前1
血煞手1年前1 -
 快乐就是那么简单 共回答了19个问题
快乐就是那么简单 共回答了19个问题 |采纳率94.7%因为在200ML的稀溶液中,芦丁很难析出来,那就不能得到芦丁的结晶,而溶剂浓缩到50ML时,溶液达到饱和溶液,这样芦丁在乙醇的溶解度降低,就能从乙醇中析出结晶.1年前查看全部
- 著名画家韩美林城市雕塑,先用石膏,精制一小精品,高为30厘米质量为8.1千克,石膏密度为3g/立方厘米
著名画家韩美林城市雕塑,先用石膏,精制一小精品,高为30厘米质量为8.1千克,石膏密度为3g/立方厘米
(1)石膏小像体积多大?
(2)再用青铜制成该雕塑,但高为3米,青铜密度为8.8克/立方厘米,雕塑体积有多大? 提早一小时休息1年前1
提早一小时休息1年前1 -
 厕所里的大象 共回答了22个问题
厕所里的大象 共回答了22个问题 |采纳率95.5%1、石膏小样体积:8100g除以3g/立方厘米 =2700立方厘米
2、青铜雕像体积:300厘米除以30厘米=10 既等比例放大长宽高10倍,体积放大10*10*10=1000倍 2700立方厘米*1000=2700000立方厘米=2.7立方米
重量自己算吧1年前查看全部
- 小亮妈妈下岗后开了一家糕点店,现有10.2千克面粉,10.2千克鸡蛋,计划加工一般糕点和精制糕点两种产品共50盒.已知加
小亮妈妈下岗后开了一家糕点店,现有10.2千克面粉,10.2千克鸡蛋,计划加工一般糕点和精制糕点两种产品共50盒.已知加工一盒一般糕点需0.3千克面粉和0.1千克鸡蛋;加工一盒精制糕点需0.1千克面粉和0.3千克鸡蛋.
(1)有哪几种符合题意的加工方案?请你帮忙设计出来;
(2)若销售一盒一般糕点和一盒精制糕点的利润分别为1.5元和2元,那么按哪一个方案加工,小亮妈妈可获得最大利润,最大利润是多少? had20051年前4
had20051年前4 -
 华赛zz帐号 共回答了11个问题
华赛zz帐号 共回答了11个问题 |采纳率81.8%解题思路:(1)本题可根据“加工一般糕点用的面粉的量+加工精制糕点用的面粉的量≤10.2”来列出不等式组,求出自变量的取值范围,判断出符合条件的方案;
(2)根据一盒一般糕点和精制糕点的利润,我们可看出,制作的精制糕点越多,利润越大,因此找出(1)中精制糕点最多的方案,计算出这个方案的利润即可.(1)设加工一般糕点x盒,则加工精制糕点(50-x)盒,根据题意得
0.3x+0.1(50−x)≤10.2
0.1x+0.3(50−x)≤10.2
解这个不等式组,得24≤x≤26
因为x为整数,所以x=24,25,26.
因此,加工方案有三种:
①加工一般糕点24盒、精制糕点26盒;
②加工一般糕点25盒、精制糕点25盒;
③加工一般糕点26盒、精制糕点24盒.
(2)由题意知,显然精制糕点数越多利润越大,故当加工一般糕点24盒、精制糕点26盒时,可获得最大利润.
最大利润为24×1.5+26×2=88(元).
答:加工一般糕点24盒、精制糕点26盒时,可获得最大利润.最大利润为=88元.点评:
本题考点: 一元一次不等式组的应用.
考点点评: 本题考查一元一次不等式组的应用,将现实生活中的事件与数学思想联系起来,读懂题列出不等式关系式即可求解.1年前查看全部
- 下列选项中哪一项是不能通过石油精制得到的() A、机油 B、黄油 C、柴油 D、色拉油
 介仔高手1年前2
介仔高手1年前2 -
 ajh915 共回答了20个问题
ajh915 共回答了20个问题 |采纳率75%选D,色拉油是由植物得到的,ABC都可以由石油得到.1年前查看全部
- 在除杂精制盐水过程中,为什么BaCl2必须在碳酸钠之前,为什么加入盐酸一定要在过滤之后
 魏格1年前2
魏格1年前2 -
 sthyuuo 共回答了20个问题
sthyuuo 共回答了20个问题 |采纳率95%加入BeCl2后,溶液中引入了新离子Be+
再加碳酸钠,能除去钡离子;过滤前,溶液中的碳酸盐与盐酸反应使其中又出现钡离子,过滤后再加盐酸,就能有效除去所有杂质1年前查看全部
- 久置的苯胺红棕色,用什么方法可以精制.过滤、活性炭脱色、蒸馏、水蒸气蒸馏
 keke221年前1
keke221年前1 -
 onedaysure 共回答了16个问题
onedaysure 共回答了16个问题 |采纳率93.8%蒸馏.1年前查看全部
- 小亮妈妈下岗后开了一家糕点店,现有10.2千克面粉,10.2千克鸡蛋,计划加工一般糕点和精制糕点两种产品共50盒.已知加
小亮妈妈下岗后开了一家糕点店,现有10.2千克面粉,10.2千克鸡蛋,计划加工一般糕点和精制糕点两种产品共50盒.已知加工一盒一般糕点需0.3千克面粉和0.1千克鸡蛋;加工一盒精制糕点需0.1千克面粉和0.3千克鸡蛋.
(1)有哪几种符合题意的加工方案?请你帮忙设计出来;
(2)若销售一盒一般糕点和一盒精制糕点的利润分别为1.5元和2元,那么按哪一个方案加工,小亮妈妈可获得最大利润,最大利润是多少? 66851年前1
66851年前1 -
 siwaki 共回答了13个问题
siwaki 共回答了13个问题 |采纳率92.3%解题思路:(1)本题可根据“加工一般糕点用的面粉的量+加工精制糕点用的面粉的量≤10.2”来列出不等式组,求出自变量的取值范围,判断出符合条件的方案;
(2)根据一盒一般糕点和精制糕点的利润,我们可看出,制作的精制糕点越多,利润越大,因此找出(1)中精制糕点最多的方案,计算出这个方案的利润即可.(1)设加工一般糕点x盒,则加工精制糕点(50-x)盒,根据题意得
0.3x+0.1(50−x)≤10.2
0.1x+0.3(50−x)≤10.2
解这个不等式组,得24≤x≤26
因为x为整数,所以x=24,25,26.
因此,加工方案有三种:
①加工一般糕点24盒、精制糕点26盒;
②加工一般糕点25盒、精制糕点25盒;
③加工一般糕点26盒、精制糕点24盒.
(2)由题意知,显然精制糕点数越多利润越大,故当加工一般糕点24盒、精制糕点26盒时,可获得最大利润.
最大利润为24×1.5+26×2=88(元).
答:加工一般糕点24盒、精制糕点26盒时,可获得最大利润.最大利润为=88元.点评:
本题考点: 一元一次不等式组的应用.
考点点评: 本题考查一元一次不等式组的应用,将现实生活中的事件与数学思想联系起来,读懂题列出不等式关系式即可求解.1年前查看全部
- (轻浮)的柳絮,精制的杨花,(滥造)的榆钱,随着风,飘来飘去,自由地堆成垛 括号内词语的表达作用
 tracy猫猫1年前2
tracy猫猫1年前2 -
 xu_ing1981 共回答了17个问题
xu_ing1981 共回答了17个问题 |采纳率88.2%拟人的修辞手法,把本来没有生命的植物用了更形象的富有生命力的表现特征1年前查看全部
- 我是说精制食盐中·,加入氢氧化钠,氯化钡,碳酸钠之后,再过滤,为什么还要加盐酸呢?
 泡饭MM1年前2
泡饭MM1年前2 -
 MobileSupply 共回答了20个问题
MobileSupply 共回答了20个问题 |采纳率90%先前你加的氢氧化钠,碳酸钠过量的,因为要充分保证除去杂质,加盐酸一方面为了调节pH至7,另一方面使氢氧化钠碳酸钠转变成NaCl.1年前查看全部
- 食盐涨价了吗?颗粒盐(也就是粗盐)能长期食用吗?能代替精制盐吗?
食盐涨价了吗?颗粒盐(也就是粗盐)能长期食用吗?能代替精制盐吗?
昨天去买盐的时候,发现以前买1元钱/包的中盐,现在要1元4角了,怎么涨了这么多? wang92081年前2
wang92081年前2 -
 九雁 共回答了26个问题
九雁 共回答了26个问题 |采纳率88.5%盐一般不会轻易涨价的,粗盐不能长期食用,里面不含有碘,不能代替精盐,如果该地区不缺碘的话,可以交替食用.1年前查看全部
大家在问
- 1(2014•大港区二模)如图所示,是某手机用的锂电池铭牌,观察可知该电池的输出电压是______V,它充满电后所储存的电
- 2某年级参加课外小组,占12/25,后来又有四人参加,这时课外小组人数占年级人数的13/25,
- 3属于共生关系的一组()A人与其肠道正常菌落B噬菌体与细菌C牛与其胃中的微生物D捕虫真菌与线菌
- 4地球上的生命丰富多彩,人类是自然界的一部分,我们对待地球上的其他生命的正确态度是 [
- 5初二的数学 因式分解 是怎麼一回事 它的概念和其他的方法有哪些?
- 6题,为什么?
- 7英语翻译《豫》:利建侯行师.《彖》曰:《豫》,刚应而志行,顺以动,《豫》.《豫》顺以动,故天地如之,而况“建侯行师”乎.
- 8填写词语,_天_地,四条
- 9阅读下面这首诗歌,然后回答问题(10分)
- 101.集合{x/x的平方-2x+m=0}含有2个元素,则实属m满足的条件是________
- 11已知公差不为零的等差数列{an}中,a1=1,且a1,a3,a13成等比数列.
- 12冬者岁之余,夜者日之余,阴雨者时之余也 文言文翻译
- 13标准跑道的全长是400米,跑道的弯道是半圆形,而且最内圈半径是36米,每条跑道宽1.2米,现有6个跑道.
- 14要生产一种容积为500升的球形容器,这种球形窗口的半径是多少分米(结果保留小数点后两位)?(球的体积公式是V=43πR3
- 15(2010•江苏)某棉纺厂为了了解一批棉花的质量,从中随机抽取了100根棉花纤维的长度(棉花纤维的长度是棉花质量的重要指
