邻苯二甲酸氢钾也氢氧化钾的反应式
 啦啦歌舞2022-10-04 11:39:541条回答
啦啦歌舞2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 乌鸦少帅 共回答了24个问题
乌鸦少帅 共回答了24个问题 |采纳率87.5%- 解析:
O ― H
|
HC ― C ―C = O
/
HC O C ― C = O + KOH →
/ |
HC ― CH O ― K
O ― K
|
HC ― C ―C = O
/
HC O C ― C = O + H2O (环形中间的O表示大π键)
/ |
HC ― CH O ― K - 1年前
相关推荐
- 精密称取基准物质邻苯二甲酸氢钾0.6225g,标定NaOH溶液,终点时用去NaOH溶液21.50ml,求NaOH溶液的浓
精密称取基准物质邻苯二甲酸氢钾0.6225g,标定NaOH溶液,终点时用去NaOH溶液21.50ml,求NaOH溶液的浓度.
邻苯二甲酸氢钾的式量为:204.22 慌原孤爱1年前2
慌原孤爱1年前2 -
 iamrain6666 共回答了24个问题
iamrain6666 共回答了24个问题 |采纳率95.8%邻苯二甲酸氢钾中两个羧基一个是钾盐一个是羧酸,可以与NaOH反应的只有一个羧酸
0.6225/204.22/0.02150 = 0.1418 mol/L1年前查看全部
- 稍加解释下:“硼砂、小苏打、氢氧化钠、邻苯二甲酸氢钾”中,最适宜标定HCl标准溶液的基准物是哪个?
 wth_1101年前1
wth_1101年前1 -
 万马军中一tt 共回答了24个问题
万马军中一tt 共回答了24个问题 |采纳率87.5%都不适宜.
硼砂、小苏打、氢氧化钠在空气中都容易发生变化,不能作为基准物.邻苯二甲酸氢钾是基准物,但是只能标定碱溶液.
标定HCl标准溶液一般用无水碳酸钠.
只有这几种物质的话,可以先配置NaOH标准溶液,用邻苯二甲酸氢钾标定.然后再用已知浓度的NaOH标准溶液标定HCl标准溶液.1年前查看全部
- 比较下列化合物的酸性.1、2、(A)邻苯二甲酸 (B)苯甲酸(C)对苯二甲酸 (D)邻苯二甲酸氢钾 (E)对苯二甲酸氢钾
比较下列化合物的酸性.
1、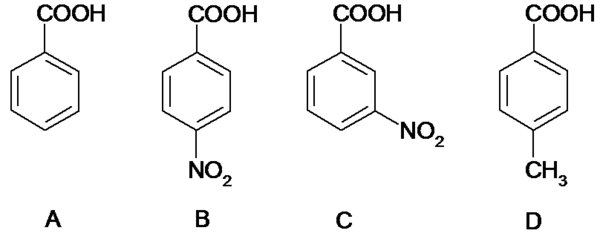
2、(A)邻苯二甲酸 (B)苯甲酸(C)对苯二甲酸 (D)邻苯二甲酸氢钾 (E)对苯二甲酸氢钾
3、(A) 氨 (B) N-甲基乙酰胺 (C) 甲胺 (D)二甲胺 (E) N-甲基苯甲酰胺 (F) 丁二酰亚胺 (G) 邻苯二甲酰亚胺 (H) N-苯基苯甲酰胺 王小灵1年前3
王小灵1年前3 -
 zgrc 共回答了17个问题
zgrc 共回答了17个问题 |采纳率100%1、B>C>A>D
首先总的原则是苯环上吸电子基团增大酸性,供电子基团减弱酸性,所以BC>A>D.
然后比较B和C.
间位与对位的主要区别在于共轭效应.
间位碳原子的电子云密度较高,对羧基上电子的吸引力较小,羧酸解离变弱.所以间位酸性最弱.
2、A>C>B>E>D
首先需要说明,对苯二甲酸氢钾实际上是比较对苯二甲酸的pK2.
所以分为2组:ABC>DE.
ABC三种物质,—COOH是吸电子基团,类似于上题中—NO2的作用.所以AC>B.
A和C的比较,A邻苯二甲酸的-1价酸根能形成分子内氢键,特别稳定.
所以A一个羧基上H电离变得容易,所以A>C.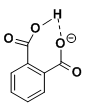
D和E的比较,D实际上就是上图的结构式.
由于H被禁锢在氢键里面了,所以电离难.因此E>D.
3、胺的碱性跟溶剂有关.不好说.1年前查看全部
- 标定NaOH溶液浓度时所用基准物质邻苯二甲酸氢钾的质量范围是如何确定的
 guzhiqiu1年前3
guzhiqiu1年前3 -
 nntt 共回答了18个问题
nntt 共回答了18个问题 |采纳率88.9%1、滴定误差控制在0.1%.2、分析天平称量时有0.0002mg的误差.称量质量大于0.2g相对误差小于0.1%.3、移液管、滴定管有0.02mL的读数误差.试液体积大于20mL相对误差小于0.1%.4、若,NaOH浓度为0.10mol/L,消耗体积为20mL到...1年前查看全部
- 分析化学实验中邻苯二甲酸氢钾标定氢氧化钠,邻苯二甲酸氢钾或多或少对标定会有啥影响?
 米儿是我的1年前3
米儿是我的1年前3 -
 日月更相锁 共回答了19个问题
日月更相锁 共回答了19个问题 |采纳率100%在氢氧化钠溶液浓度一定时,邻苯二甲酸氢钾或多或少将决定消耗的氢氧化钠溶液的体积,而滴定体积一般在20-40mL,超出这个范围,会增大某些误差.1年前查看全部
- 为什么基准邻苯二甲酸氢钾COD为500mg/L测量出来只有60mg左右
为什么基准邻苯二甲酸氢钾COD为500mg/L测量出来只有60mg左右
用直接加热法做,吸取5ml标样,加5ml 0.25mol/L的重铬酸钾,加15ml的催化剂,用0.1mol/L的硫酸亚铁滴定,为什么基准邻本二甲酸氢钾COD为500mg/L,测量出来只有60mg左右,怎么一直都偏低呢?
还请问1g的邻苯二甲的氢钾耗氧1.1768g/g是什么意思?(因为刚刚做这个实验,有点迷糊) jj5517021年前1
jj5517021年前1 -
 shenkaiyun719 共回答了23个问题
shenkaiyun719 共回答了23个问题 |采纳率78.3%1.1768g/g是指1g的邻苯二甲的氢钾所耗费的氧是1.1768g1年前查看全部
- 邻苯二甲酸氢钾和苯二甲酸氢钾是不是同一物质,不同的名称啊?急
 都市潜艇1年前4
都市潜艇1年前4 -
 solo898 共回答了16个问题
solo898 共回答了16个问题 |采纳率93.8%不是,严格地讲苯二甲酸氢甲不能准确地表示任何一种物质,它可包括邻苯二甲酸氢甲,间苯二甲酸氢甲,和对苯二甲酸氢甲.1年前查看全部
- 邻苯二甲酸氢钾了为什么作为PH标准缓冲溶液
 我已麻木麻木1年前3
我已麻木麻木1年前3 -
 newmoonone 共回答了12个问题
newmoonone 共回答了12个问题 |采纳率100%邻苯二甲酸氢钾(KHP)是酸碱滴定的“第一类标准物”.它的水溶液本身并不能作为pH标准缓冲溶液!但是,与盐酸,或氢氧化钠溶液混合可以配制成为缓冲溶液.1年前查看全部
- 为什么用无水碳酸钠标定盐酸溶液通常用移液管法而用邻苯二甲酸氢钾标定氢氧化钠熔液直接用称量法?
 地球村℡1年前3
地球村℡1年前3 -
 bonniecoming 共回答了15个问题
bonniecoming 共回答了15个问题 |采纳率100%因为Na2CO3摩尔质量太小,且与盐酸反应是1:2的计量关系,直接称量量太小,称量误差大,所以先配在容量瓶中,再用移液管法标定;相反,邻苯二甲酸氢钾摩尔质量太大,且与盐酸反应是1:1的计量关系,称量量大,可以直接用称量法.1年前查看全部
- ph计校正液配制以前一直都是在用磷酸氢二钠,磷酸二氢钾,邻苯二甲酸氢钾,和四硼酸钠来配校正液的,但是最近发现磷酸氢二钠在
ph计校正液配制
以前一直都是在用磷酸氢二钠,磷酸二氢钾,邻苯二甲酸氢钾,和四硼酸钠来配校正液的,但是最近发现磷酸氢二钠在空气中易风化失水,配制会有阻碍,就使用了干燥方法.但是又发现四硼酸钠也是会风化,要在几百度的温度下才变成无水的.实在有点瞎搞,请问谁有办法解决呢?不能测pH 哈福1年前1
哈福1年前1 -
 膀胱镜 共回答了21个问题
膀胱镜 共回答了21个问题 |采纳率95.2%不可以……你用了6.86~pH计会自动认为那个是7.00的,因为pH计自动取最当然可以.pH=6.86就是中性的,我们都是用这种标液校正的. 不能1年前查看全部
- 用邻苯二甲酸氢钾标准溶液做COD的校准.请问“邻苯二甲酸氢钾标准溶液”有效期是多久?
用邻苯二甲酸氢钾标准溶液做COD的校准.请问“邻苯二甲酸氢钾标准溶液”有效期是多久?
我们的溶液都是放在冰柜里,就想知道,大概保存多久,这个标准溶液还是可以拿来校准的. yymeilin1年前2
yymeilin1年前2 -
 hillview 共回答了19个问题
hillview 共回答了19个问题 |采纳率89.5%在调试COD设备的时候经常要用到邻苯二甲酸氢钾标准溶液,以前我们配制的试剂都是高浓度的母液,存放在冰箱,需要用的时候就稀释成低浓度的标液.
为了保证试剂的准确性,一般试剂保存在冰箱时间为三个月,当然,有放置半年的试剂也还是有效的,但不建议使用.1年前查看全部
- 标定NaOH溶液的基准物质常用的有,草酸.苯甲酸.邻苯二甲酸氢钾.;基准物质烘干时分解要完全,但不吸收空气中的CO2.这
标定NaOH溶液的基准物质常用的有,草酸.苯甲酸.邻苯二甲酸氢钾.;基准物质烘干时分解要完全,但不吸收空气中的CO2.这句话哪里错了?
 小粉肠1年前1
小粉肠1年前1 -
 scjinmingwei 共回答了20个问题
scjinmingwei 共回答了20个问题 |采纳率90%烘干不能分解需要把水分烘干.1年前查看全部
- 邻苯二甲酸氢钾标定NaOH理论上邻苯二甲酸氢钾要称0.4-0.6克,但我们做实验时放大十倍称4-5克.这样的话求出的氢氧
邻苯二甲酸氢钾标定NaOH
理论上邻苯二甲酸氢钾要称0.4-0.6克,但我们做实验时放大十倍称4-5克.
这样的话求出的氢氧化钠浓度不是也放大了吗?但是对于给定的样品,浓度不是一定的吗?不明白呀. wei9193941年前2
wei9193941年前2 -
 江湖不杀生 共回答了14个问题
江湖不杀生 共回答了14个问题 |采纳率92.9%放大称,是为了称的过程相对误差小.配成溶液以后,可以再稀释,最终NaOH浓度不会放大的.1年前查看全部
- 精密称取基准物质邻苯二甲酸氢钾(KHP)0.5225g,标定NaOH溶液,终点时用去NaOH溶液22.50ml,求NaO
精密称取基准物质邻苯二甲酸氢钾(KHP)0.5225g,标定NaOH溶液,终点时用去NaOH溶液22.50ml,求NaOH溶液的浓度.
(MKHP=204.44g/mol) slumpliang1年前1
slumpliang1年前1 -
 zhang7221 共回答了18个问题
zhang7221 共回答了18个问题 |采纳率83.3%邻苯二甲酸氢钾属有机酸式盐,是由邻苯二甲酸与少量的氢氧化钾反应得到(如果氢氧化钾过量的话会把邻苯二甲酸中的两个氢都中和掉变成邻苯二甲酸钾就属于有机正盐.其实可以类比于碳酸和氢氧化钾反应,如果氢氧化钾少量就只能生成碳酸氢钾,过量则生成碳酸钾,邻苯二甲酸氢钾也可类比为碳酸氢钾,只含有一个氢离子显酸性).用邻苯二甲酸氢钾标定氢氧化钠实质上是邻苯二甲酸中的氢离子和氢氧化钠中的氢氧根离子中和.
n(NaOH) = n(邻苯二甲酸氢钾)
先计算出0.5225g的邻苯二甲酸氢钾的物质的量(即酸性氢离子的物质的量)n = m|M = 0.5225g | 204.44g|mol
假设氢氧化钠溶液的浓度为c(NaOH),则:
c(NaOH) * 22.50ml = 0.5225g | 204.44g|mol
解出 c(NaOH) = 1.136 * 10^-4 mol|ml1年前查看全部
- KOH大概浓度是0.140mol/L,邻苯二甲酸氢钾应该称取多少克.用来标定氢氧化钾溶液.
 rxxing1年前2
rxxing1年前2 -
 breezewin 共回答了17个问题
breezewin 共回答了17个问题 |采纳率94.1%KOH是0.140mol,一般滴定时将滴定量控制在20~30ml,按25.00ml算,那么就是25.00×0.140=3.50mmol,
邻苯二甲酸氢钾的摩尔质量是204g/mol,
所以m=204×3.5×10^-3=0.714g
所以应该称取0.714±0.143g
希望对你有所帮助!1年前查看全部
- 邻苯二甲酸氢钾是强酸还是弱酸,难道不是弱酸吗?
 情为何物_xx1年前2
情为何物_xx1年前2 -
 小魔女陈小乐 共回答了19个问题
小魔女陈小乐 共回答了19个问题 |采纳率100%不是
是盐,水解呈酸性,Ph和它的浓度有很大关系,0.1mol/L的溶液大约Ph=3左右1年前查看全部
- 标定碱标准溶液时,邻苯二甲酸氢钾( KHC8H4O4 , M=204.32g*mol)和二水草酸( H2C2O4'H2O
标定碱标准溶液时,邻苯二甲酸氢钾( KHC8H4O4 , M=204.32g*mol)和二水草酸( H2C2O4'H2O , M=126.07g*mol
都可以作为基准物质,你认为选择哪一种好,为什么?
可以再具体点 可以加方程式吗 那样我比较容易理解 萧萧52013141年前2
萧萧52013141年前2 -
 bossji55 共回答了20个问题
bossji55 共回答了20个问题 |采纳率65%邻苯二甲酸氢钾
基准物质的标准中有一条,就是在其他条件一样的情况下,分子量越大越好,这样称量的相对误差较小.1年前查看全部
- 12.在标定NaOH溶液的基准物质邻苯二甲酸氢钾中含有少量邻苯二甲酸,则用此基准物质标定NaOH溶液的浓度时,
12.在标定NaOH溶液的基准物质邻苯二甲酸氢钾中含有少量邻苯二甲酸,则用此基准物质标定NaOH溶液的浓度时,
其测定结果引进了( )
A.负误差 B.正误差
C.无影响 D.不一定 凌云乐1年前1
凌云乐1年前1 -
 wenlijsw 共回答了15个问题
wenlijsw 共回答了15个问题 |采纳率100%负偏差,用的酸多了,消耗掉的碱也变多,结果得出碱的浓度变小了1年前查看全部
- 用0.1mol/l的邻苯二甲酸氢钾和0.1mol/l的盐酸怎么配成pH=3.3的缓冲液?分别需要两种溶液多少体积?
 ccedison1年前1
ccedison1年前1 -
 zhijunwin 共回答了24个问题
zhijunwin 共回答了24个问题 |采纳率87.5%邻苯二甲酸的PKa1=2.95
邻苯二甲酸氢钾和盐酸反应会生成邻苯二甲酸,所以缓冲液是由邻苯二甲酸与邻苯二甲酸氢钾(这是酸及其共轭碱)组成的(盐酸的量小于邻苯二甲酸氢钾,否则无邻苯二甲酸氢钾剩余),其PH的计算如下:
PH=PKa1+lg([邻苯二甲酸氢钾]/[邻苯二甲酸]),
代入数值 3.3=2.95+lg([邻苯二甲酸氢钾]/[邻苯二甲酸]),得二者浓度比
[邻苯二甲酸氢钾]/[邻苯二甲酸]=2.24
假设配制1L缓冲液,设取0.1mol/l的邻苯二甲酸氢钾xmL(邻苯二甲酸氢钾的量为0.1x/1000=0.0001x),则取0.1mol/l盐酸(1000-x)mL(HCl的量为0.1*(1000-x)/1000=0.1-0.0001x)
由于邻苯二甲酸氢钾过量,所以0.0001x>0.1-0.0001x)(x>500),反应按盐酸的量进行.
C8H5O4K + HCl = C8H6O4 + KCl
0.1-0.0001x 0.1-0.0001x 0.1-0.0001x
则生成邻苯二甲酸的量:0.1-0.0001x,剩余邻苯二甲酸氢钾的量:0.1-(0.1-0.0001x)=0.0001x
由于在同一溶液中,体积相同,所以二者浓度比
[邻苯二甲酸氢钾]/[邻苯二甲酸]=0.0001x/(0.1-0.0001x)=2.24,解得x=690mL,即需加入邻苯二甲酸氢钾溶液690mL,而需加入的盐酸为1000-690=310mL
当然若需配制溶液的体积不是1L,按照二者比例(69:31)配制即可.1年前查看全部
- 邻苯二甲酸氢钾为什么要干燥用邻苯二甲酸氢钾标定氢氧化钠时,为什么要把邻苯二甲酸氢钾放在100℃烘箱里干燥呢?把全部的邻苯
邻苯二甲酸氢钾为什么要干燥
用邻苯二甲酸氢钾标定氢氧化钠时,为什么要把邻苯二甲酸氢钾放在100℃烘箱里干燥呢?把全部的邻苯二甲酸氢钾放在烘箱里吗? 吉祥的生鱼片1年前1
吉祥的生鱼片1年前1 -
 pxh123 共回答了27个问题
pxh123 共回答了27个问题 |采纳率88.9%作为标定的标准物,必须有稳定的性质,并且其化学式能够代表其组成,才能得到比较精确地标定结果.邻苯二甲酸氢纳干燥就是为了出去其中含有的水分,以使化学式能够代表其组成.
当然是将全部的都干燥后再进行称量1年前查看全部
- 用邻苯二甲酸氢钾作基准物质标定氢氧化钠溶液,在分析天平上准确称量出0.5251克邻苯二甲酸氢钾,用氢氧化钠溶液滴定之,用
用邻苯二甲酸氢钾作基准物质标定氢氧化钠溶液,在分析天平上准确称量出0.5251克邻苯二甲酸氢钾,用氢氧化钠溶液滴定之,用去25.00毫升,求氢氧化钠溶液的物质的量浓度.(邻苯二甲酸氢钾的式量为:204.22)
 caocaocao211年前2
caocaocao211年前2 -
 xyliuguohui 共回答了14个问题
xyliuguohui 共回答了14个问题 |采纳率100%邻苯二甲酸氢钾中两个羧基一个是钾盐一个是羧酸,可以与NaOH反应的只有一个羧酸
0.5251/204.22/0.02500 = 0.1028 mol/L1年前查看全部
- 在标定NaOH标准溶液的实验中,为什么要求称取0.3到0.4g基准邻苯二甲酸氢钾,不是0.4至0.6(⊙o⊙)哦
 暗香花影1年前2
暗香花影1年前2 -
 欢乐NANHAI 共回答了20个问题
欢乐NANHAI 共回答了20个问题 |采纳率85%邻苯二甲酸氢钾摩尔质量204.22g/mol,0.0.4g相当于0.15~0.2mmol
用来标定NaOH的话,如果NaOH浓度在0.1mol/L附近(这是一般标准溶液的大致浓度),那么所用的NaOH的体积就大约是15~20mL,这是中和滴定比较恰当的用量(灌满的滴定管可以保证完成2次滴定).
如果邻苯二甲酸氢钾称取量太多或太少,则相应NaOH体积也太多或太少,前者需要频繁添加NaOH很不方便,后者相对误差会较大,都不太适合.1年前查看全部
- 用邻苯二甲酸氢钾标定氢氧化钠溶液时为什么用酚酞做试剂
 天源东方1年前1
天源东方1年前1 -
 sqllovesql 共回答了20个问题
sqllovesql 共回答了20个问题 |采纳率100%邻苯二甲酸氢钾显酸性.用已知浓度的邻苯二甲酸溶液滴定未知浓度的氢氧化钠时,用酚酞作指示剂,酚酞的变色范围8~10 ,对应无色~浅红色~红色,用邻苯二甲酸测定,氢氧化钠溶液由红色变为无色,且颜色半分钟红色不复原,表明达到滴定终点.1年前查看全部
- 标定氢氧化钠标准滴定溶液时使用了分析纯的邻苯二甲酸氢钾,会产生什么性质的误差,如何处理.
 dshlyq1年前1
dshlyq1年前1 -
 41493348 共回答了18个问题
41493348 共回答了18个问题 |采纳率88.9%因为分析纯邻苯二甲酸氢钾浓度比不上基准试剂或优级纯邻苯二甲酸氢钾,标定时会导致NaOH标准溶液浓度值变大,改用基准试剂或优级纯邻苯二甲酸氢钾进行标定即可.1年前查看全部
- PH缓冲液配制需要的邻苯二甲酸氢钾需要基准试剂吗?一般试剂行吗?
 单身贵族_吻1年前1
单身贵族_吻1年前1 -
 寻找晚风 共回答了17个问题
寻找晚风 共回答了17个问题 |采纳率76.5%邻苯二甲酸氢钾本身就是基准试剂,比如标定NaOH溶液就是使用邻苯二酸氢钾.
去试剂商店一般就能够买到基准试剂.
还有,购买酸度计的时候一般都附带有缓冲溶液,用完了接着买就行.1年前查看全部
- 在含有邻苯二甲酸氢钾和酚酞指示液的溶液中滴入氢氧化钠饱和溶液,为什么溶液没有变色
 shdx1年前2
shdx1年前2 -
 曦少 共回答了19个问题
曦少 共回答了19个问题 |采纳率89.5%原先就是碱性溶液呀1年前查看全部
- 氢氧化钠和酚酞指示剂都发生反应,有邻苯二甲酸氢钾搀和就没有发生反应,是不是邻苯二甲酸氢钾有问题?
 轻轻走过不留痕迹1年前1
轻轻走过不留痕迹1年前1 -
 紫竹零星雨 共回答了18个问题
紫竹零星雨 共回答了18个问题 |采纳率88.9%邻苯二甲酸氢钾的水溶液呈酸性,会与氢氧化钠发生中和反应,使酚酞的红色褪去
NaOH + HOOC-(o-C6H4)-COOK —— NaOOC-(o-C6H4)-COOK + H2O1年前查看全部
- 称取0.4克邻苯二甲酸氢钾溶于50毫升水中,问此时溶液pH值多少?
 jacky1120cn1年前1
jacky1120cn1年前1 -
 graycosmos 共回答了17个问题
graycosmos 共回答了17个问题 |采纳率94.1%线性分子式:HOOCC6H4COOK 分子量为 204 ,0.4g邻苯二甲酸氢钾的物质的量为 n1=0.4/204=0.00196mol , 一个分子中只电离一个H+, 所以nH+=0.00196mol ,
则CH+=0.00196mol /0.05L=0.04mol.L-1 PH=1.41年前查看全部
- 思考题 :怎样溶解邻苯二甲酸氢钾?
 ufxa1年前1
ufxa1年前1 -
 jialaowu 共回答了21个问题
jialaowu 共回答了21个问题 |采纳率90.5%邻苯二甲酸氢钾溶解速度比较慢,还会浮在水面上,尤其是接近液面的杯壁处.因此称好试样回到实验室后,分别在四个烧杯中,洗杯壁后加50mL纯水,放入玻棒,搅拌后,盖好表面皿,然后准备滴定管,使样品有足够的溶解时间.在滴定前,先检查一号烧杯内试样溶解情况,特别注意接近液面的烧杯壁处,如还有未溶解的试样,则搅拌直至完全溶解,当滴定完第一份试样后,再检查二号烧杯内试样的溶解情况,搅拌全溶后滴定.依次重复至全部滴定好.1年前查看全部
- 邻苯二甲酸钾和邻苯二甲酸氢钾我感觉应该不一样,邻苯二甲酸钾应该比邻苯二甲酸氢钾多一个钾,但是网上没有邻苯二甲酸钾的信息,
邻苯二甲酸钾和邻苯二甲酸氢钾
我感觉应该不一样,邻苯二甲酸钾应该比邻苯二甲酸氢钾多一个钾,但是网上没有邻苯二甲酸钾的信息,疑惑中……
还有,哪个厂家的邻苯二甲酸钾质量比较好点,正在准备采购中 湖心塔影1年前1
湖心塔影1年前1 -
 狗尾巴草也有春天 共回答了17个问题
狗尾巴草也有春天 共回答了17个问题 |采纳率94.1%邻苯二甲酸氢钾的是代替水中的还原性污染物,它和强氧化剂重铬酸钾的反应就是氧化还原反应,由邻苯二甲酸氢钾的结构式可以推测,完全氧化的最终产物可能是1年前查看全部
- 已知邻苯二甲酸氢钾的摩尔质量是 204.2g/mol,用它来标定0.1mol/L NaOH 溶液,宜称取邻苯二甲酸氢钾为
已知邻苯二甲酸氢钾的摩尔质量是 204.2g/mol,用它来标定0.1mol/L NaOH 溶液,宜称取邻苯二甲酸氢钾为:() A.0.25g左右; B.1g左右; C.0.1g左右; D.0.05g左右; E.0.5g左右.
为什么 jacques271年前1
jacques271年前1 -
 小迪迪 共回答了22个问题
小迪迪 共回答了22个问题 |采纳率90.9%A1年前查看全部
- 若标定0.5mol/L氢氧化钠溶液,应称取邻苯二甲酸氢钾多少克?怎么算质量和最后的浓度,求公式
 selinatang1年前1
selinatang1年前1 -
 落雁韵舞 共回答了11个问题
落雁韵舞 共回答了11个问题 |采纳率90.9%标准溶液的配制与标定
4.1 氢氧化钠标准溶液
C(NaOH)=1mol/L(1N)
C(NaOH)=0.5mol/L(0.5N)
C(NaOH)=0.1mol/L(0.1N)
4.1.1 配制
称取100gNaOH,溶于100ml水中,摇匀,注入聚乙烯容器中,静置直到溶液清亮.用塑料管虹吸下述规定体积的上层清液,注入1000ml无CO2的水中,摇匀.
C(NaOH),mol/L 氢氧化钠饱和溶液,ml
1 52
0.5 26
0.1 5
4.1.2 标定
a.标定方法:称取规定量基准邻苯二甲酸氢钾于105-1100C烘干至恒重,称准至0.0001g,溶于下述规定体积的无CO2的水中,加2滴酚 指示液(10g/L),用配制好的NaOH溶液滴至溶液呈粉红色,同时作空白试验.
C(NaOH),mol/L 基准邻苯二甲酸氢钾,g 无CO2的水,ml
1 6 80
0.5 3 80
0.1 0.6 50
b.计算:NaOH标准溶液浓度按下式计算
C(NaOH)= m/(V1-V2)x0.2042
式中:
C(NaOH)-NaOH标准溶液的物质的量浓度,mol/L;
m-邻苯二甲酸氢钾之质量,g;
V1-NaOH溶液之用量,ml;
V2-空白试验NaOH溶液之用量,ml;
0.2042-与1.00mlNaOH标准溶液[C(NaOH)=1.000mol/L]相当的以克表示的邻苯二甲酸氢钾的质量;1年前查看全部
- 用邻苯二甲酸氢钾标定NaOH时,滴定管中有气泡,但在滴定过程中消失结果偏高还是偏低
 qqv0071年前1
qqv0071年前1 -
 linda487 共回答了23个问题
linda487 共回答了23个问题 |采纳率95.7%偏高,假设你的气泡有1ml,则你用于标定的实际体积要比你的读数体积小1ml,这样造成的结果必然是计算NaOH比实际值高.1年前查看全部
- 计算0.05Mol/L的邻苯二甲酸氢钾的PH
 我就是soso1年前1
我就是soso1年前1 -
 呼拉拉再 共回答了21个问题
呼拉拉再 共回答了21个问题 |采纳率90.5%邻苯二甲酸氢钾在质子论中当两性物质
PH=(PKa1+PKa2)/2 查表计算1年前查看全部
- 思考题 :怎样溶解邻苯二甲酸氢钾?
 苦乐cc1年前1
苦乐cc1年前1 -
 果仁张 共回答了14个问题
果仁张 共回答了14个问题 |采纳率78.6%邻苯二甲酸氢钾溶解速度比较慢,还会浮在水面上,尤其是接近液面的杯壁处.因此称好试样回到实验室后,分别在四个烧杯中,洗杯壁后加50mL纯水,放入玻棒,搅拌后,盖好表面皿,然后准备滴定管,使样品有足够的溶解时间.在滴定前,先检查一号烧杯内试样溶解情况,特别注意接近液面的烧杯壁处,如还有未溶解的试样,则搅拌直至完全溶解,当滴定完第一份试样后,再检查二号烧杯内试样的溶解情况,搅拌全溶后滴定.依次重复至全部滴定好.1年前查看全部
- COD 标液配制1、我看说明书上还需要硫酸95-98%分析纯(0.5ml硫酸+1.700g邻苯二甲酸氢钾).到底需不需要
cod 标液配制
1、我看说明书上还需要硫酸95-98%分析纯(0.5ml硫酸+1.700g邻苯二甲酸氢钾).到底需不需要这个呢?
2、配制2000mg/l标液 应该***. uhrfbm1年前1
uhrfbm1年前1 -
 2d4540d0bf062db1 共回答了21个问题
2d4540d0bf062db1 共回答了21个问题 |采纳率85.7%1、加硫酸的目的是为了给氧化反应造成酸性环境,以利于氧化还原反应的进行.
2、用邻苯二甲酸氢钾标准溶液配置,由于每克邻苯二甲酸氢钾的理论CODcr值为 1.176g,所以,溶解1.7004邻苯二甲酸氢钾于重蒸馏水中,转入1000mL容量瓶,用重蒸馏水稀释至标线,使之成为2000mg/L的CODcr标准溶液.
邻苯二甲酸氢钾:基准试剂级
用前需在105度烘至恒重.1年前查看全部
- 过量邻苯二甲酸氢钾与醋酸反应后,用氢氧化钠滴定改用什么指示剂?
 我的名字叫后羿1年前1
我的名字叫后羿1年前1 -
 captureit 共回答了19个问题
captureit 共回答了19个问题 |采纳率89.5%反应后生成强碱弱酸盐,所以用酚酞.1年前查看全部
- 用邻苯二甲酸氢钾滴定NaOH有什么显著的优点?
 yangsky3211年前4
yangsky3211年前4 -
 冬天的不板砖 共回答了22个问题
冬天的不板砖 共回答了22个问题 |采纳率77.3%除了较大的摩尔质量以外,还有3个:有足够的纯度;组成和化学式完全符合;稳定.这3个条件也是直接配置标准溶液的条件.NaOH标准溶液不能直接配置,需要间接法来标定.1年前查看全部
- 滴定消耗0.2mol/LNaOH25~30ml,应取多少邻苯二甲酸氢钾
 刚刚注册了1年前1
刚刚注册了1年前1 -
 nihaba 共回答了20个问题
nihaba 共回答了20个问题 |采纳率90%氢氧化钠与邻苯二甲酸氢钾是1:1反应,所以需要邻苯二甲酸氢钾的量=5~6mmol
邻苯二甲酸氢钾的摩尔质量=204
所以需要邻苯二甲酸氢钾的量=1.02~1.224克1年前查看全部
- 求邻苯二甲酸氢钾与氢氧化钠反应离子方程式
 huangjc19811年前1
huangjc19811年前1 -
 孤独不孤 共回答了18个问题
孤独不孤 共回答了18个问题 |采纳率100%Ph—COOH + OH- → Ph—COO- + H2O
│ │
COO- COO-1年前查看全部
- 邻苯二甲酸氢钾与氢氧化钠反应
 lovermy1年前1
lovermy1年前1 -
 gzzyxdp 共回答了16个问题
gzzyxdp 共回答了16个问题 |采纳率100%HOOCC6H4COOK+NaOH=NaOOCC6H4COOK+H2O1年前查看全部
- 邻苯二甲酸氢钾是否有毒
 黄雪丽1年前2
黄雪丽1年前2 -
 wswzp 共回答了13个问题
wswzp 共回答了13个问题 |采纳率76.9%一般带苯环的都有一定的毒性.而且它的水溶液呈酸性,有一定的腐蚀性.化学试剂大多都对身体一定的危害,操作小心点吧.1年前查看全部
- 如果用未烘干的基准物质邻苯二甲酸氢钾标定标准溶液浓度,对标定结果有何影响
 sevwolfthree1年前4
sevwolfthree1年前4 -
 laike922 共回答了16个问题
laike922 共回答了16个问题 |采纳率93.8%有影响,是KHP和NaOH反应,含水时KHP肯定不足量使C(KHP)偏小,消耗V(NaOH)变小,待测C(NaOH)增大1年前查看全部
- 为什么用分析化学实验中邻苯二甲酸氢钾标定氢氧化钠用0.4到0.6克?
为什么用分析化学实验中邻苯二甲酸氢钾标定氢氧化钠用0.4到0.6克?
这是大二分析化学里的实验思考题
或多或少会有什么影响呢? 有话好好说_1年前1
有话好好说_1年前1 -
 victorben 共回答了15个问题
victorben 共回答了15个问题 |采纳率86.7%一般滴定时,滴定溶液的浓度是0.1 mol/L左右,设消耗25mL氢氧化钠,则需要称邻苯二甲酸氢钾为0.5g,为了控制滴定溶液的体积在20-30mL时(以前这样,现在可以更多),则需要邻苯二甲酸氢钾0.4到0.6克.
计算:m=nM=cVM=0.1*0.025*204=0.5g1年前查看全部
- 称取邻苯二甲酸氢钾于烧杯中,加水50ml溶解,此时用量筒取还是用移液管吸取?为什么?
 比利_HB1年前2
比利_HB1年前2 -
 maxsimon25 共回答了15个问题
maxsimon25 共回答了15个问题 |采纳率80%邻苯二甲酸氢钾是作什么用?如果是用来标定氢氧化钠溶液,加水50ml溶解,使用量筒即可.因为所称的邻苯二甲酸氢钾是用万分之一天平称量,称取的质量是准确的(小数点后四位),无论用多少水溶解,溶液中所含邻苯二甲酸氢钾的量是不会发生变化的,邻苯二甲酸氢钾与氢氧化钠1:1反应,所以只要邻苯二甲酸氢钾质量一定,其物质的量就一定,那么消耗的氢氧化钠的量就不会受影响,所以邻苯二甲酸氢钾体积无所谓准不准,也就用不着移液管.
如果是配制邻苯二甲酸氢钾标准溶液,那么要先在烧杯中溶解,然后转移到容量瓶中,并在容量瓶中定容,所以在烧杯中溶解时,所加水量用量筒即可,也用不着移液管,因为最终溶液的体积是整个容量瓶的容积,只要定容操作正确就行.1年前查看全部
- 称取0.4511g邻苯二甲酸氢钾的固体,加入50ml蒸馏水溶解,用新配制的氢氧化钠溶液标定,滴定管的初始读书为0,10m
称取0.4511g邻苯二甲酸氢钾的固体,加入50ml蒸馏水溶解,用新配制的氢氧化钠溶液标定,滴定管的初始读书为0,10ml,终点读数为21,05ml,求新配制的氢氧化钠的浓度.
 心灵呼唤31年前2
心灵呼唤31年前2 -
 流水有情GBS 共回答了16个问题
流水有情GBS 共回答了16个问题 |采纳率87.5%邻苯二甲酸氢钾与氢氧化钠1:1反应.设氢氧化钠的浓度为c则有
0.4511/204=cX(21.05-0.1)X10^-3
解得c=0.1056mol/L1年前查看全部
- 标定0.1mol/L NaOH溶液的准确浓度,问应称取基准邻苯二甲酸氢钾多少克
 san_nn1年前4
san_nn1年前4 -
 赫内斯 共回答了19个问题
赫内斯 共回答了19个问题 |采纳率89.5%0.1mol/LNOH标准溶液称取0.4-0.6克于105-110℃烘至恒重的邻苯二甲酸氢钾,称准至0.0002克,分别溶于80ml不含二氧化碳水中,加2滴10g/L酚酞指示剂,用配好的待标定溶液至溶液呈粉红色与标准色相同.同时作空白试验.1年前查看全部
- 标定标准碱为什么用邻苯二甲酸氢钾吗
 深篮淡篮1年前3
深篮淡篮1年前3 -
 丐帮首席执行tt 共回答了21个问题
丐帮首席执行tt 共回答了21个问题 |采纳率90.5%邻苯二甲酸氢钾易得到纯制品,在空气中不吸水,容易保存,它与NaOH或OH离子 起反应时化学计量数为1∶1,其摩尔质量较大,因此它是标定碱标准溶液较好的基准物质.1年前查看全部
- 氢氧化钠溶液标定的计算0.1mol/L氢氧化钠标定时,称取基准物邻苯二甲酸氢钾6g左右,消耗氢氧化钠滴定液30ml左右,
氢氧化钠溶液标定的计算
0.1mol/L氢氧化钠标定时,称取基准物邻苯二甲酸氢钾6g左右,消耗氢氧化钠滴定液30ml左右,计算氢氧化钠的浓度,求答案.
要详细的计算过程 幸福的小猪子1年前1
幸福的小猪子1年前1 -
 braveandlove 共回答了21个问题
braveandlove 共回答了21个问题 |采纳率100%那基准的邻苯二甲酸氢钾试剂标明的分子量是多少呢?纯度又是多少呢?1年前查看全部
大家在问
- 1按要求作图,图甲是远处物体通过某人眼睛成像的示意图,请在图乙中的虚线框内画上适当的透镜,使远处物体能成像在视网膜上.
- 2抗生素溶解细胞壁还是抑制细胞壁的合成
- 3有一张5元,2张2元,一张1元,一张5角,3张2角,一张1角,如何拿出7.6元
- 4下面是一段介绍王羲之书法的文字,请用比较工整的语句(如排比)概括王羲之在书法史上的主要贡献。要求:符合原意;不超过3
- 5Give up or never give up?
- 6如题,地球是太阳的卫星吗?
- 7怎样和同学相处文章
- 8一个玻璃管的一端用手按住,并且下方有一段水柱,倒置后(水柱在上方),水为什么不会流下来?
- 9英语翻译它们分别是:种花、节约水、打扫街道
- 10I gave Susie the wrong direction to get to my house!
- 11在反应中,如何表示某一物质体现酸性
- 12水果店运来一批红富士苹果,每箱15千克,卖出12箱后,还剩150千克.水果店运进红富士苹果多少千克?
- 13如图,D是等边三角形ABC中AC边的中点,E在BC的延长线上,DE=DB,若△ABC的周长为6,则△BDE的周长
- 14写出同义短语
- 15(3+2i)/(2-3i)如何计算
