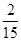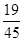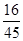含铜废料在空气中中灼烧产生黑色固体及残留物 加入足量的稀盐酸加热 产生蓝色溶液和不容物 求两次方程式
 红炉雪2022-10-04 11:39:541条回答
红炉雪2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 青鸟98 共回答了17个问题
青鸟98 共回答了17个问题 |采纳率88.2%- 2Cu+O2=△=2CuO
CuO+2HCl=CuCl2+H2O - 1年前
相关推荐
- (2013•莘县一模)2012年4月15日,央视《每周质量报告》报道:一些企业用皮革废料熬制工业明胶,在加工过程中添加重
(2013•莘县一模)2012年4月15日,央视《每周质量报告》报道:一些企业用皮革废料熬制工业明胶,在加工过程中添加重铭酸钾.在加热条件下重铬酸钾分解,反应的化学方程式为:4K2Cr2O7═4K2CrO4+2X+3O2↑,工业明胶制造药用胶囊,导致胶囊重金属铬超标.铬是一种重金属元素,能对肝、肾等内脏器官和DNA造成损伤.在通常情况下,铬单质是银白色金属光泽的固体,有较高的熔点,是最硬的金属;在加热时,能与浓硫酸反应生成硫酸铬(其中铬元素化合价为+3价),同时还生成一种大气污染物和一种常见的液体.
回答下列问题:
(1)请写出K2Cr2O7分解生成X的化学式为______;
(2)归纳铬单质的物理性质______;
(3)铬单质与浓硫酸反应的化学方程式为2Cr+6H2SO4(浓)
Cr2(SO4)3+3SO2↑+6H2O△ .2Cr+6H2SO4(浓).
Cr2(SO4)3+3SO2↑+6H2O△ . 为了爱远走xx1年前1
为了爱远走xx1年前1 -
 我是新月 共回答了15个问题
我是新月 共回答了15个问题 |采纳率80%解题思路:在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.
不需要通过化学变化表现出来的性质属于物质的物理性质.(1)由反应的化学方程式可知,反应物中的4个铬原子和6个氧原子转化到了X中,因为X的化学计量数是2,所以每个X中含有2个铬原子和3个氧原子,X是三氧化二铬.
故填:Cr2O3.
(2)铬的颜色、金属光泽、状态、熔点、硬度等不需要通过化学变化表现出来,属于物理性质.
故填:银白色、有金属光泽的固体,熔点较高、最硬的金属.
(3)由叙述可知,铬和浓硫酸反应生成硫酸铬、二氧化硫和水,反应的化学方程式为:2Cr+6H2SO4(浓)
△
.
Cr2(SO4)3+3SO2↑+6H2O.
故填:2Cr+6H2SO4(浓)
△
.
Cr2(SO4)3+3SO2↑+6H2O.点评:
本题考点: 质量守恒定律及其应用;化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查质量守恒定律,重点是化学方程式的书写,书写化学方程式时要遵循四个步骤:一是反应物和生成物要正确;二是要遵循质量守恒定律,即配平;三是要写上必要的反应条件;四是要判断是否有“↑”或“↓”.1年前查看全部
- 多功能榨油机能榨黄豆和花生吗?一吨花生能榨出多少油?榨出的废料有什么用处啊?
 很爱很爱YOU1年前2
很爱很爱YOU1年前2 -
 采菊东南下13 共回答了15个问题
采菊东南下13 共回答了15个问题 |采纳率93.3%最好买专用的机器,不同的机器出油率有很大区别,就算是多功能的一般也内有那么神奇,废料就是豆饼之类的,一般都卖给养殖户了,给动物做饲料1年前查看全部
- 求老师解答.一张大板切小板能切几张?有多少废料,要求写出公式是多少?怎么算的?
求老师解答.一张大板切小板能切几张?有多少废料,要求写出公式是多少?怎么算的?
例如:一张大板的长2440mm宽1220mm厚3mm
一张小板420*260*3,请问怎么算出一张大板能切几个小板,还剩多少废料,要求有公式!解释出怎么算的? 兔兔数星星1年前1
兔兔数星星1年前1 -
 爱的就是这粒米 共回答了19个问题
爱的就是这粒米 共回答了19个问题 |采纳率94.7%﹙2440÷420﹚×﹙1220÷260﹚×﹙3÷3﹚
=5×4×1
=20﹙张﹚
剩余:2440×1220×3-420×260×3×20
=8930400-6552000
=2378400﹙mm³﹚1年前查看全部
- (2012•湘潭)去年4月央视曝光了“毒胶囊”事件,某些不良企业利用皮革废料加工制成药用胶囊.但合格的药用胶囊主要成分是
(2012•湘潭)去年4月央视曝光了“毒胶囊”事件,某些不良企业利用皮革废料加工制成药用胶囊.但合格的药用胶囊主要成分是淀粉,不经咀嚼直接吞服,这主要是保护哪个器官免受药物的刺激( )
A.口腔
B.胃
C.小肠
D.大肠 ntuli1年前1
ntuli1年前1 -
 hhqyson 共回答了18个问题
hhqyson 共回答了18个问题 |采纳率100%解题思路:食物中含有的维生素、水和无机盐等小分子的营养物质人体可以直接吸收利用,而蛋白质、糖类、脂肪这些大分子的营养物质是不溶于水的,必须在消化道内变成小分子的能溶于水的物质后,才能被消化道壁吸收.人体各段消化道对食物中含有的各种营养物质的消化能力是不同的.食物中含有的淀粉的消化从口腔开始,口腔中的唾液淀粉酶能够将部分淀粉分解为麦芽糖,当淀粉和麦芽糖进入小肠后,由于小肠中的胰液和肠液中含有消化糖类、脂肪和蛋白质的酶,因此,淀粉等糖类物质在小肠内被彻底消化为葡萄糖;可见胃对淀粉没有消化作用,人们利用这个特性,把对胃有刺激作用的药物放在由淀粉制成的胶囊里直接吞服,这样就可以避免药物对胃的刺激.
故选:B点评:
本题考点: 食物的消化和营养物质的吸收过程.
考点点评: 该题考查了各段消化道的消化特点和对食物的消化能力.1年前查看全部
- (2012•道外区二模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=6米.用这块废料剪出一个矩形CDEF,
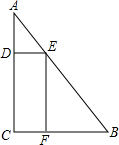 (2012•道外区二模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=6米.用这块废料剪出一个矩形CDEF,其中点D、E、F分别在AC、AB、BC上、设边AE的长为x米,矩形CDEF的面积为S平方米.
(2012•道外区二模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=6米.用这块废料剪出一个矩形CDEF,其中点D、E、F分别在AC、AB、BC上、设边AE的长为x米,矩形CDEF的面积为S平方米.
(1)请直接写出S与x之间的函数关系式(不要求写出自变量x的取值范围);
(2)根据(1)中的函数关系式,计算当x为何值时S最大,并求出最大值.
参考公式:二次函数y=ax2+bx+c(a≠0),当x=−
时,y最大(小)值=b 2a
.4ac−b2 4a  我想吃榴莲1年前1
我想吃榴莲1年前1 -
 古不灵精不怪 共回答了20个问题
古不灵精不怪 共回答了20个问题 |采纳率90%解题思路:(1)在直角三角形ADE中,利用直角三角形中30°的锐角所对的直角边是斜边的一半可求出DE的长,进而求出AD,同理在直角三角形ACB中可求出AC,所以就可以求出DC的长,即矩形DEFC的长,再利用矩形的面积公式即可得到S和x的函数关系式;
(2)利用求二次函数最值公式即可求出当x为何值时S最大,以及最大值.(1)
 ∵四边形DEFC是矩形,
∵四边形DEFC是矩形,
∴∠ADE=90°,
∵∠A=30°,
∴DE=[1/2]AE,
∵AE=x,
∴DE=[1/2]x,
∴AD=
3
2x,
同理在直角三角形ACB中,AC=
AB2−CB2 =3
3米,
∴DC=AC-AD=3
3-
3
2x,
∴S矩形DECF=DE•CD=[1/2]x(3
3-点评:
本题考点: 二次函数的应用;相似三角形的判定与性质.
考点点评: 本题考查的是直角三角形的性质:在直角三角形ADE中,利用直角三角形中30°的锐角所对的直角边是斜边的一半以及勾股定理的运用,利用矩形的面积公式得到关于x的二次函数,根据二次函数的性质,确定x,y的取值和面积的最大值是解题的关键.1年前查看全部
- △ABC是一块等腰三角形的废料,已知∠BAC是锐角,量得底边BC长为60cm,BC边长的高为40cm,用它截一块边长为3
△ABC是一块等腰三角形的废料,已知∠BAC是锐角,量得底边BC长为60cm,BC边长的高为40cm,用它截一块边长为30cm的矩形(要求:使矩形的一边与△ABC的一边重合,而矩形的另外两个顶点分别在△ABC的另两边上),问共有几种不同的截法,画图并求得的矩形的面积.
 library1年前1
library1年前1 -
 376415519 共回答了16个问题
376415519 共回答了16个问题 |采纳率93.8%有6种不同的解法:
1.连AB中点E和AC中点F,并作EG⊥BC于G,FH⊥BC于H,EFHG即所求,面积=20*30=600
2.作EF∥BC,且相距30cm,交AB于E,交AC于F,并作EG⊥BC于G,FH⊥BC于H,EFHG即所求,面积=450
对另外两边可仿此进行.
1年前查看全部
- 某中学化学兴趣小组用含有铁铝合金的工业废料,制备FeSO 4 ·7H 2 O和硫酸铝晶体。具体实验操作步骤如下:
某中学化学兴趣小组用含有铁铝合金的工业废料,制备FeSO 4 ·7H 2 O和硫酸铝晶体。具体实验操作步骤如下:
① 将5%Na 2 CO 3 溶液加入到盛有一定量废合金的烧杯中,加热数分钟,用倾析法除去Na 2 CO 3 溶液,然后将废合金用蒸馏水洗涤2至3遍;
② 取洗涤后废合金,加入足量的NaOH溶液中,反应完全后过滤;
③ 向滤液中边搅拌边滴加稀硫酸至溶液的pH为8—9,静置,过滤,洗涤;
④ 将③中固体溶于足量的稀硫酸,将得到的溶液蒸发浓缩,冷却,结晶,过滤,干燥,得到硫酸铝晶体;
⑤ 将②得到的固体洗涤后加入过量的稀硫酸,至铁溶解完全;
⑥ 将得到的溶液转入密闭容器中,静置,冷却结晶;
⑦ 待结晶完毕后,滤出晶体,用少量冰水洗涤2至3次,再用滤纸将晶体吸干,得到FeSO 4 ·7H 2 O晶体。 (1)实验步骤①的目的是_____________ 。
(2)步骤②发生的离子反应方程式为___________ 。
(3)步骤③中,溶液中pH难控制,可改用_____________ 。
(4) 步骤⑤明显不合理,理由是 _________________。
(5)用少量冰水洗晶体,其目的是 __________________。
(6)FeSO 4 ·7H 2 O晶体在高温下可以分解生成Fe 2 O 3 ,SO 2 和H 2 SO 4 ,写出该反应的化学方程式_____________ 。 小疼_20991年前1
小疼_20991年前1 -
 wenkeshanew 共回答了19个问题
wenkeshanew 共回答了19个问题 |采纳率100%(1)除去油污
(2)2Al + 2OH - +6H 2 O = 2[Al(OH) 4 ] - + 3H 2 ↑
(3)通入CO 2 气体
(4)应该Fe过量,否则溶液中可能有Fe 3+
(5)洗涤除去晶体表面附着的硫酸等杂质
(6)2FeSO 4 ·7H 2 O == Fe 2 O 3 +SO 2 ↑+ H 2 SO 4 +13H 2 O1年前查看全部
- (2009•深圳一模)硬铝废料(含90%铝、2.5%镁、7.5%铜)可以制取明矾KAl(SO4)2•12H2O,某探究小
(2009•深圳一模)硬铝废料(含90%铝、2.5%镁、7.5%铜)可以制取明矾KAl(SO4)2•12H2O,某探究小组设计了下列实验.
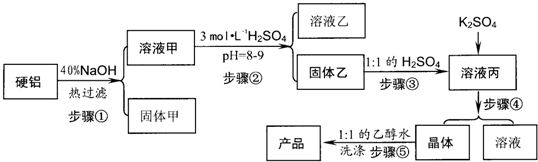
请回答以下问题:
(1)写出步骤②的离子方程式______;简述用pH试纸的过程:______.
(2)步骤④包括三个环节,分别是______、______、______.
(3)步骤⑤不直接用水洗的原因是______,洗涤的操作是______.
(4)有人建议:直接将硬铝溶于稀硫酸中,过滤;滤液中加入硫酸钾得到溶液丙,在进行后续实验.请你评价此建议的可行性______. joanchen1年前1
joanchen1年前1 -
 ¤霜枫¤ 共回答了17个问题
¤霜枫¤ 共回答了17个问题 |采纳率94.1%解题思路:依据流程图分析可知,硬铝中铝与氢氧化钠反应生成偏铝酸钠,故溶液甲含有偏铝酸钠,向溶液甲中加入硫酸,偏铝酸根与氢离子反应,生成氢氧化铝沉淀,所以固体乙为氢氧化铝,向固体乙加入硫酸,氢氧化铝与硫酸反应生成硫酸铝和水,加入硫酸钾减小物质溶解度析出硫酸铝钾晶体,过滤得到明矾KAl(SO4)2•12H2O;
(1)步骤②是偏铝酸钠和硫酸反应,调节溶液PH为8-9生成氢氧化铝沉淀;依据PH试纸使用方法叙述回答操作步骤;
(2)丙溶液含有硫酸铝,向其中加入硫酸钾,得混合溶液,通过蒸发、结晶、过滤制得明矾;
(3)明矾在酒精中的溶解度小,用酒精洗涤减少产品的损失,洗涤晶体的操作为在过滤装置中加入洗涤剂浸没晶体后使洗涤剂自然流出,洗涤2-3次;
(4)硬铝废料含90%铝、2.5%镁、7.5%铜,直接加入稀硫酸其中铝和镁都可以溶解,通过后续实验操作得当的晶体中会含有杂质硫酸镁;(1)步骤②是偏铝酸钠和硫酸反应,调节溶液PH为8-9生成氢氧化铝沉淀,离子方程式为AlO2-+H++H2O=Al(OH)3↓,
故答案为:AlO2-+H++H2O=Al(OH)3↓;
(2)向硫酸铝溶液中加入硫酸钾,得混合溶液,通过蒸发浓缩、冷却结晶、过滤洗涤制得明矾;
故答案为:蒸发浓缩;冷却结晶,过滤;
(3)明矾在酒精中的溶解度小,用酒精洗涤,明矾在酒精中的溶解度小,减少产品的损失,洗涤晶体的操作步骤为:在过滤装置中加入洗涤剂浸没晶体后使洗涤剂自然流出,重复洗涤2-3次;
故答案为:减少产品的损失;往漏斗中加入洗涤剂至浸没固体,自然流出,重复2~3次;
(4)硬铝废料含90%铝、2.5%镁、7.5%铜,直接加入稀硫酸其中铝和镁都可以溶解,按此方法获得的溶液中还含有Mg2+,最后得到的产品不纯;
故答案为:不可行,因为按此方法获得的溶液中还含有Mg2+,最后得到的产品不纯.点评:
本题考点: 制备实验方案的设计;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题考查了物质制备实验过程分析和分离方法,知识涉及元素化合物、实验原理等,侧重考查学生对实验方案理解、元素化合物的知识应用、实验基本操作的步骤叙述,难度中等.1年前查看全部
- (2012•常德)2012年4月,媒体曝光某不法企业用皮革废料熬制成工业明胶,再制成药用胶囊流向市场.皮革废料中重金属铬
(2012•常德)2012年4月,媒体曝光某不法企业用皮革废料熬制成工业明胶,再制成药用胶囊流向市场.皮革废料中重金属铬超标,危害人体健康.铬(Cr)原子的核电荷数为24,相对原子质量为52,铬原子的核外电子数为( )
A.24
B.28
C.52
D.76 风中云12161年前1
风中云12161年前1 -
 阿瑞8 共回答了16个问题
阿瑞8 共回答了16个问题 |采纳率87.5%解题思路:根据相对原子质量与质子数和中子数之间的关系来分析本题,并要结合核内质子数等于核外电子数,对这些关系要灵活运用.由在原子中质子数=电子数=核电荷数,可知铬原子的核外电子数等于元素的核电荷数为24,所以:
A、铬原子的核外电子数为24,故A正确;
B、铬原子的核外电子数不是28,故B错误;
C、铬原子的核外电子数不是52,故C错误;
D、铬原子的核外电子数不是76,故D错误.
故选A.点评:
本题考点: 原子的定义与构成;亚硝酸钠、甲醛等化学品的性质与人体健康.
考点点评: 通过回答本题要知道在原子里:质子数=电子数=核电荷数;相对原子质量=质子数+中子数.1年前查看全部
- (2012•南通)某科研小组利用工业废酸(10%H2S04)来浸泡含有氧化铜、氧化锌的废料,实现废物的综合利用.流程如下
(2012•南通)某科研小组利用工业废酸(10%H2S04)来浸泡含有氧化铜、氧化锌的废料,实现废物的综合利用.流程如下图所示:
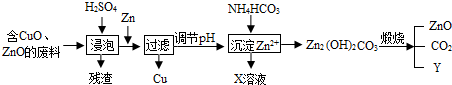
(1)写出氧化锌与硫酸反应的化学方程式:______,Zn→Cu的化学方程式为______.
(2)物质X可用作氮肥,化学式为______;该化肥不能与______混合使用.
(3)请推出物质Y的化学式:______. wangziyilong11年前1
wangziyilong11年前1 -
 ljk2008 共回答了20个问题
ljk2008 共回答了20个问题 |采纳率85%解题思路:(1)根据氧化锌与硫酸反应生成了硫酸锌和水分析,根据Zn、Cu的活泼性分析;
(2)根据废物的综合利用流程图和物质间的反应分析推断物质X的化学式,根据X的性质分析;
(3)根据质量守恒定律推断Y的化学式.(1)氧化锌与硫酸反应生成了硫酸锌和水,反应的化学方程式:ZnO+H2S04═ZnS04+H20;由于锌的活泼性大于铜,可以将锌与硫酸铜反应来实现
Zn→Cu的转变,反应的化学方程式是:Zn+CuSO4═Cu+ZnS04;
(2)由废物的综合利用流程图和物质间的反应可知,物质X是硫酸铵,可用作氮肥,化学式是:(NH4)2S04,由于铵盐与碱性物质反应放出氨气降低肥效,所以,该化肥不能与碱性物质 混合使用;
(3)由元素守恒可知,煅烧碱式碳酸锌碳酸锌生成氧化锌、二氧化碳和水,水的化学式是:H2O.
故答为:(1)ZnO+H2S04═ZnS04+H20Zn+CuSO4═Cu+ZnS04(2)(NH4)2S04,碱性物质(3)H2O.点评:
本题考点: 金属活动性顺序及其应用;常见化肥的种类和作用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题看上去是一道分析推断图框题,但题目考查的知识点全是课本基础知识,熟练掌握酸碱盐的化学性质即可解答本题.1年前查看全部
- 2013年4月15日,央视《每周质量报告》报道:一些不法企业用皮革废料熬制的工业明胶生产药用胶囊.在熬制过程中添加重铬酸
2013年4月15日,央视《每周质量报告》报道:一些不法企业用皮革废料熬制的工业明胶生产药用胶囊.在熬制过程中添加重铬酸钾(K2Cr2O7),导致生产的药用胶囊重金属铬超标.根据化学式计算:
(1)钾、铬、氧三种元素的质量比______(要求填最简整比).
(2)29.4g该物质中含有钾元素的质量为______ g. liuxia1231年前1
liuxia1231年前1 -
 dg风中百合 共回答了22个问题
dg风中百合 共回答了22个问题 |采纳率90.9%解题思路:(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
(2)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行解答.(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得重铬酸钾中钾、铬、氧元素的质量比为:(39×2):(52×2):(16×7)=39:52:56;
(2)29.4g重铬酸钾中含有钾元素的质量为29.4g×([39×2/39×2+52×2+16×7]×100%)=7.8g.
故答案为:
(1)39:52:56;(2)7.8.点评:
本题考点: 元素质量比的计算;化合物中某元素的质量计算.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.1年前查看全部
- 某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用.其实验方案如下:
某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用.其实验方案如下:

请回答下列问题:
(1)由滤液A制得AlCl3溶液有途径Ⅰ和Ⅱ两条,你认为合理的是______,理由是:______.
(2)从滤液E中得到绿矾晶体的实验操作是______.
(3)请用一个总反应式表示由滤渣F制备胆矾晶体过程中发生的变化:2Cu+O2+2H2SO4+8H2O
2CuSO4•5H2O△ .2Cu+O2+2H2SO4+8H2O.
2CuSO4•5H2O△ .
(4).有同学提出可将方案中最初溶解合金的烧碱改用盐酸,重新设计方案,也能制得三种物质,你认为后者的方案是否更合理______,理由是______. 大雪飘飞1年前1
大雪飘飞1年前1 -
 AINGAING 共回答了14个问题
AINGAING 共回答了14个问题 |采纳率92.9%解题思路:铝、铁、铜的合金中加入足量烧碱溶液,只有铝与其反应而溶解,过滤后得滤渣B的成分为铁和铜,滤液A为偏铝酸钠溶液;滤液A生成氯化铝溶液的途径Ⅰ发生反应:NaAlO2+4HCl=AlCl3↓+NaCl+2H2O;而途径Ⅱ通入足量的二氧化碳反应后过滤能得到纯净的氢氧化铝,氢氧化铝与盐酸反应能制得AlCl3溶液;滤渣B中只有铁和稀硫酸反应,反应后经过滤得滤渣为铜,再由铜制取胆矾,滤液为硫酸亚铁溶液,然后由溶液制取晶体.
(1)途径Ⅰ会引入氯化钠杂质;而途径Ⅱ能制得纯净的AlCl3溶液;
(2)由溶液制取晶体,需经过加热浓缩,冷却结晶、过滤洗涤、干燥;
(3)铜和氧气和酸反应生成硫酸铜和水;
(4)将方案中最初溶解合金的烧碱改为盐酸,后者操作步骤多,消耗的试剂量更多,时间长.铝、铁、铜的合金中加入足量烧碱溶液,只有铝与其反应而溶解,过滤后得滤渣B的成分为铁和铜,滤液A为偏铝酸钠溶液;滤液A生成氯化铝溶液的途径Ⅰ发生反应:NaAlO2+4HCl=AlCl3↓+NaCl+2H2O;而途径Ⅱ通入足量的二氧化...
点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用;制备实验方案的设计.
考点点评: 本题主要考查了从工业废料中制取纯净物,注意从框图转化中找出有用信息,利用有关的化学反应进行解答,难度中等.1年前查看全部
- (2009•潍坊一模)某化工厂为了综合利用废料 CaSO4,与相邻的合成氨厂设计了以下制备(NH4)2SO4&
(2009•潍坊一模)某化工厂为了综合利用废料 CaSO4,与相邻的合成氨厂设计了以下制备(NH4)2SO4 的工艺流程

请回答以下问题:
(1)沉淀池中发生的主要反应是(用化学方程式表示)CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4.
(2)从滤液中获取((NH4)2SO4晶体,必须的操作步骤是BCDBCD(填写序号)
A.加热蒸干 B.蒸发浓缩C.冷却结晶 D.过滤 E.萃取F分液
(3)该生产过程中可以循环使用的X是CO2CO2.
(4)在生产中,要检查输送氨气的管道是否漏气,可选用AEAE(填写序号)
A.浓盐酸B.湿润的蓝色石蕊试纸C.湿润的淀粉碘化钾试纸D.稀硫酸E.湿润的红色石蕊试纸. indiasinoaa1年前1
indiasinoaa1年前1 -
 飞跃的轩辕 共回答了16个问题
飞跃的轩辕 共回答了16个问题 |采纳率93.8%(1)将NH3和CO2通入沉淀池中并加入CaSO4,生成(NH4)2SO4和CaCO3,发生CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4,
故答案为:CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4.
(2)从溶液中获取晶体应采取蒸发浓缩、冷却结晶、过滤等操作,所以必须操作步骤是BCD.
故答案为:BCD.
(3)由工艺流程可知,CaCO3在煅烧炉中分解生成CO2和CaO,CO2循环使用.
故答案为:CO2.
(4)A、浓盐酸挥发出的氯化氢与氨气生成氯化铵,有白烟产生,可以检验氨气,故A正确;
B、氨气遇湿润的蓝色石蕊试纸,无明显现象,不能检验氨气,故B错误;
C、氨气遇湿润的淀粉碘化钾试纸,无明显现象,不能检验氨气,故C错误;
D、氨气遇稀硫酸,无明显现象,不能检验氨气,故D错误;
E、氨气是碱性气体,能使湿润的红色石蕊试纸变蓝,可以检验氨气,故E正确.
故选:AE.1年前查看全部
- 两张正方形硬纸板,一张剪去1个圆,一张剪去4个圆(如图).哪一张剩下的废料多一些?( )
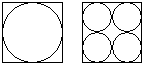 两张正方形硬纸板,一张剪去1个圆,一张剪去4个圆(如图).哪一张剩下的废料多一些?( )
两张正方形硬纸板,一张剪去1个圆,一张剪去4个圆(如图).哪一张剩下的废料多一些?( )
A.剪1个圆剩下的多
B.剪4个圆剩下的多
C.剩下的一样多 15rt15rt36yu1年前1
15rt15rt36yu1年前1 -
 15oil 共回答了19个问题
15oil 共回答了19个问题 |采纳率84.2%解题思路:设正方形的边长为a,一张减去一个最大的圆,它的直径是正方形的边长,一张减去四个小圆,它的直径是正方形边长的一半既是[a/2],再算一算它们的面积谁大,剩下的就少.大圆的面积=[a/2]×[a/2]π=
a2
4π=
a2π
4,
四个小圆的面积=[a/4]×[a/4]×π×4=
a2π
4,
由此可知大圆的面积和4个小圆的面积的和相等.
所以剩的一样多.
故选:C.点评:
本题考点: 面积及面积的大小比较.
考点点评: 此题是考查在正方形里剪圆,半径与边长的关系的灵活应用.1年前查看全部
- (2012•株洲模拟)2012年4月15日,央视《每周质量报告》播出节目《胶囊里的秘密》,曝光河北一些企业用皮革废料熬制
(2012•株洲模拟)2012年4月15日,央视《每周质量报告》播出节目《胶囊里的秘密》,曝光河北一些企业用皮革废料熬制成工业明胶,卖给一些企业制成药用胶囊.皮革是由生皮鞣制而成,在生皮鞣制过程中需要添加重铬酸钾,其化学式为K2Cr2O7,试计算:
(1)重铬酸钾中钾、铬、氧元素的质量比是______;
(2)重铬酸钾中铬元素的质量分数是______.(结果保留一位小数) 有风吹过31年前1
有风吹过31年前1 -
 id36053 共回答了22个问题
id36053 共回答了22个问题 |采纳率77.3%解题思路:(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
(2)根据物质中某元素的质量分数=[该元素的相对原子质量×原子个数/该物质相对分子质量]×100%,进行解答.(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得重铬酸钾中钾、铬、氧元素的质量比为:(39×2):(52×2):(16×7)=39:52:56;
(2)根据物质中某元素的质量分数=[该元素的相对原子质量×原子个数/该物质相对分子质量]×100%,可得重铬酸钾中铬元素的质量分数为:[52×2/39×2+52×2+16×7]×100%=35.4%;
故答案为:(1)39:52:56; (2)35.4%.点评:
本题考点: 化学式的书写及意义;元素质量比的计算;元素的质量分数计算.
考点点评: 本题考查学生硅根据化学式计算物质中某元素的质量分数、元素质量比计算方法的掌握与应用.1年前查看全部
- 含铜废料在空气中灼烧会有污染吗
 sunrain_y1年前2
sunrain_y1年前2 -
 qq认证 共回答了11个问题
qq认证 共回答了11个问题 |采纳率100%如果是铜的话不会,在空气中灼烧生成氧化铜,温度再高,氧化铜分解成氧化亚铜和氧气.但废料中的其他成分可能会有污染空气的物质1年前查看全部
- 为探索工业废料的再利用,某化学兴趣小组设计了如图1实验方案,用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO4•7H
为探索工业废料的再利用,某化学兴趣小组设计了如图1实验方案,用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO4•7H2O)和胆矾晶体.

请回答:
(1)步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是______,该操作中除用到烧杯和玻璃棒外,还必须用到的玻璃仪器有______.
(2)试剂X是______.
(3)步骤Ⅱ中发生反应的离子方程式是:______.
(4)进行步骤Ⅱ时,该小组用如图2所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,为了避免固体C减少,改进的措施是在装置Ⅰ、Ⅱ之间增加一个______.
(5)溶液D中各离子的浓度由大到小的顺序为:______.
(6)工业上由X和F制得CuSO4,还必须使用的最恰当的试剂可以是______或______.
A.浓H2SO4B.Fe2O3C.HNO3D.O2E.H2O2. fangzhuzi21年前1
fangzhuzi21年前1 -
 大漠孤独子 共回答了16个问题
大漠孤独子 共回答了16个问题 |采纳率93.8%解题思路:铝、铁和铜的合金中只有金属铝可以和氢氧化钠之间反应生成溶液A偏铝酸钠,固体B是金属铁和金属铜,A中通入过量的二氧化碳可以得到氢氧化铝沉淀C和碳酸氢钠溶液D,金属铁可以和硫酸之间发生反应生成硫酸亚铁和氢气,但是金属铜和稀硫酸之间不反应,硫酸亚铁溶液蒸发浓缩、冷却结晶可以获得绿矾晶体,金属铜可以获得胆矾晶体.
(1)固体和液体的分离用过滤法,过滤用到的仪器:烧杯、玻璃棒、漏斗等;
(2)根据步骤Ⅰ加过量的氢氧化钠发生的反应以及金属铁、铜的性质区别进行解答;
(3)过量CO2与偏铝酸钠溶液反应;
(4)制得的CO2气体中混有氯化氢气体,用饱和的碳酸氢钠除去;
(5)是饱和的碳酸氢钠溶液,溶液呈碱性,水解程度大于电离程度;
(6)根据铜、稀硫酸的性质来判断反应的发生,并结合产物一会原子的利用率来回答其优点.铝、铁和铜的合金中只有金属铝可以和氢氧化钠之间反应生成溶液A偏铝酸钠,固体B是金属铁和金属铜,A中通入过量的二氧化碳可以得到氢氧化铝沉淀C和碳酸氢钠溶液D,金属铁可以和硫酸之间发生反应生成硫酸亚铁和氢气,但是金属铜和稀硫酸之间不反应,硫酸亚铁溶液蒸发浓缩、冷却结晶可以获得绿矾晶体,金属铜可以获得胆矾晶体.
(1)步骤Ⅰ加过量的氢氧化钠,金属铝和氢氧化钠反应,金属铝溶解其中生成偏铝酸钠溶液,金属铁和金属铜不与氢氧化钠反应,将它们分离用过滤;步骤Ⅰ过滤得到的滤液成分为偏铝酸钠,步骤Ⅱ中向偏铝酸钠中通入足量的二氧化碳,会得到纯净的氢氧化铝沉淀,溶液中的溶质为碳酸氢钠,将它们分离用过滤;步骤Ⅲ中金属铁和金属铜不与氢氧化钠反应,铁和硫酸反应而金属铜不反应将它们分离用过滤,过滤用到的玻璃仪器:烧杯、玻璃棒、漏斗等.
故答案为:过滤;漏斗;
(2)步骤Ⅰ加过量的氢氧化钠,因铝与碱反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,金属铁和金属铜不与氢氧化钠反应,所以溶液A中的离子主要有AlO2-、Na+、OH-;本实验的目的是用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO4•7H2O)和胆矾晶体,金属铁和金属铜不与氢氧化钠反应,铁和硫酸反应生成硫酸亚铁而金属铜不反应,可以实现三种金属的分离,所以试剂X是稀硫酸,
故答案为:稀硫酸;
(3)过量CO2与偏铝酸钠溶液反应,离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)进行步骤Ⅱ时,该小组用如图2所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是二氧化碳气体中含有从盐酸中挥发出的氯化氢气体,氯化氢在水中溶解了部分沉淀氢氧化铝,发生的反应为Al(OH)3+3H+=Al3++3H2O,为了避免固体C减少,可在制取二氧化碳的收集装置中增加一个洗去氯化氢的装置,二氧化碳在饱和碳酸氢钠中不溶,氯化氢和碳酸氢钠反应生成二氧化碳气体,所以可在装置I和Ⅱ之间增加一个盛有饱和碳酸氢钠溶液的洗气瓶,除去二氧化碳中的氯化氢,
故答案为:盛有饱和碳酸氢钠溶液的洗气瓶;
(5)是饱和的碳酸氢钠溶液,溶液呈碱性,水解程度大于电离程度,所以离子浓度大小顺序为:c(Na+)>c(HCO3-)>c(OH)>c(H+)>c(CO32-),故答案为:c(Na+)>c(HCO3-)>c(OH)>c(H+)>c(CO32-);
(6)铜不能和稀硫酸反应,但是当加热并通入空气之后,铜和氧气反应生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,即2Cu+O2+2H2SO4=2CuSO4+2H2O,或者加入过氧化氢氧化不产生新的杂质,故答案为:DE.点评:
本题考点: 常见金属元素的单质及其化合物的综合应用;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题是对物质的分离和提纯知识点的考查,注意掌握铝、铁和铜及其化合物的性质是解答本题的关键,题目难度不大.1年前查看全部
- 小明想用一块三角形废料截取一个正方形,如图所示,操作如下:过AB上点D作DE⊥BC,以DE为边作正方形DEFG,随后他又
小明想用一块三角形废料截取一个正方形,如图所示,操作如下:过AB上点D作DE⊥BC,以DE为边作正方形DEFG,随后他又改变了主意,想尽可能的利用废料,在△ABC内部截一个正方形,使一边在BC上,另外两点位于AB、AC上,利用你
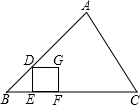 所学知识,帮他画出来.
所学知识,帮他画出来.
(1)在小明作图的基础上作出正方形,简述作法;
(2)证明你所作的四边形是正方形;
(3)若BC=120cm,BC边上的高为80cm,求所作正方形的边长. 蛐蛐宝宝1年前1
蛐蛐宝宝1年前1 -
 恶有报 共回答了18个问题
恶有报 共回答了18个问题 |采纳率94.4%解题思路:(1)根据在△ABC内部截一个正方形,由原正方形与所画正方形位置关系可以判断出,需要做原正方形的位似图形,
(2)证明所画图形是正方形可以证明它们是位似图形,
(3)利用相似三角形对应高的比也等于相似比,可以求出,注意所画图形是正方形,用同一未知数表示未知边,即可求出.(1)位似画法,
连接BG并延长到△ABC的边AC上一点N,过点N做MN∥BC,交边AB于一点M,过点M做MT⊥BC于点T,过点N做NK⊥BC于一点K,所得图形就是所要正方形.
(2)证明:点D与M;点E与T;点G与N;点F与K;相交于一点,
而且MN∥DG,NK∥GF;DE∥MT;FE与TK在一条直线上,
所以正方形DEFG与四边形MTKN是位似图形,
所以四边形MTKN是正方形.
(3)假设正方形边长为x厘米,过点A,做AS⊥BC,交MN于点P,交BC于点S,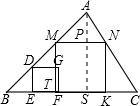 在△ABC中可得:
在△ABC中可得:
[AP/AS=
MN
BC]
∵BC=120cm,BC边上的高为80cm,
∴AS=80cm,MN=x cm,AP=(80-x)cm代入上式得:
[80−x/80=
x
120]
解得:x=48cm
答:正方形的边长是48cm.点评:
本题考点: 相似三角形的应用.
考点点评: 此题主要考查了位似图形的画法,以及位似图形的判定方法,以及相似三角形中对应高与相似比的关系,题目比较新颖.1年前查看全部
- 如何计算每个铜件的重量?现 每公斤黄铜能加工950件产品 利用率是44 % 废料每公斤加4元加工费加工成铜
 gis-susie1年前1
gis-susie1年前1 -
 wzking111 共回答了28个问题
wzking111 共回答了28个问题 |采纳率92.9%1000克*44%/950=0.46克/件
因为废料可以再加工成铜,所以按铜重量的44%计算产品的重量.1年前查看全部
- 草酸废料 一种黑色块状物 有酸味 能当燃料烧吗 今看见有人把草酸厂的废料 拉回家当煤烧
草酸废料 一种黑色块状物 有酸味 能当燃料烧吗 今看见有人把草酸厂的废料 拉回家当煤烧
请问是否有危险.
什么时候的废料就不知道了,颜色是黑色有光泽,和海绵一样有空,不是很沉。
在远处看就和炭灰一样。 拍卖ii11年前2
拍卖ii11年前2 -
 实话实说真人 共回答了18个问题
实话实说真人 共回答了18个问题 |采纳率100%可能是树脂吧..离子交换或者做其他用的树脂1年前查看全部
- 用Mg,AL合金废料,稀硫酸和氢氧化钠溶液,制取MgSO4和AL2(SO4)3,限用4个化学方程式
用Mg,AL合金废料,稀硫酸和氢氧化钠溶液,制取MgSO4和AL2(SO4)3,限用4个化学方程式
答案是先用铝和氢氧化钠反应,再写Mg,为什么不能先用Mg先和硫酸反应? fangzhi10101年前1
fangzhi10101年前1 -
 mezzomin 共回答了16个问题
mezzomin 共回答了16个问题 |采纳率87.5%铝可以和氢氧化钠反应,镁不反应,因此先加入NaOH反应取得Al(OH)3沉淀,然后过滤,在溶液和沉淀中再加入稀硫酸反应制取MgSO4和AL2(SO4)3.不先加入硫酸的原因是硫酸和Mg Al 都反应 无法分离Mg和Al 公式如下
Al + 3NaOH = Al(OH)3 + 3Na+
Mg +H2SO4 = MgSO4 + H2
2Al(OH)3 + 3H2SO4 = AL2(SO4)3 + 6H2O1年前查看全部
- 关于数学问题,一张大板可以切多少个小板,废料多不多,请提供计算公式,长方形 正方形
关于数学问题,一张大板可以切多少个小板,废料多不多,请提供计算公式,长方形 正方形
打个比方把,一张宽1220mm*长2440mm*厚3mm的铝板 要切成长230宽125厚3mm请问怎么计算一张大板能切几个这个小板?剩下的废料多不多? 请写出公式,方便以后计算
或者加Q教我下非常感谢1093353851 雪狼ff1年前2
雪狼ff1年前2 -
 风岩残缺 共回答了11个问题
风岩残缺 共回答了11个问题 |采纳率100%计算裁成块数:大板面积(长*宽)/小板面积(长*宽)
注意:为了裁出最多块数,大板的长(或宽)尽量等于小板所有块数长的和(或宽的和),以减少废料多.1年前查看全部
- 在一块直径是2分米的圆形铁片中间,剪下一个最大的正方形.这个正方形的面积是多少平方分米?四周的废料占圆形面积的百分之几?
在一块直径是2分米的圆形铁片中间,剪下一个最大的正方形.这个正方形的面积是多少平方分米?四周的废料占圆形面积的百分之几?(百分号前保留一位小数)
 哈北龙1年前1
哈北龙1年前1 -
 kk城 共回答了7个问题
kk城 共回答了7个问题 |采纳率71.4%解题思路:在一块直径是2分米的圆形铁片中间,剪下一个最大的正方形,这个正方形的对角线的长是这个圆的直径,即2分米,根据正方形特点,正方形对角线互相垂直平分,在圆内作两条互相垂直的直径,连接两条直径的端点所得到的正方形;计算正方形的面积,不知边长,可把它分成两个三角形来计算,每个三角形的底是圆的直径2分米,高是圆的半径1分米;用圆的面积减去正方形的面积就是废料的面积,用废料的面积除以圆的面积即可求出废料占圆形面积的百分之几.正方形的面积:2×1÷2×2=2(平方分米);
圆的面积:3.14×([2/2])2=3.14×1=3.14(平方分米),
四周废料面积:3.14-2=1.14(平方分米),
1.14÷3.14≈0.363=36.3%;
答:正方形的面积是2平方分米,四周废料占圆面积的约36.3%.
故答案为:2平方分米,36.3%.点评:
本题考点: 图形的拆拼(切拼).
考点点评: 本题是考查图形的切拼问题、正方形面积的计算,圆面积的计算、百分数应用题等.注意,要想剪下一个最大的正方形,这个正方形的对角线的长是这个圆的直径.1年前查看全部
- (2007•天河区一模)在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).下面是某化学兴趣小组处理回收
(2007•天河区一模)在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).下面是某化学兴趣小组处理回收含铜废料的主要步骤.
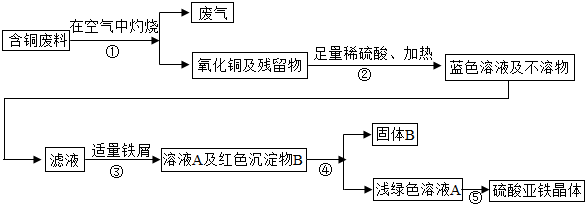
回答下列问题:
(1)溶液A中溶质的化学式是______.
(2)步骤②中发生的化学方程式为______.
(3)步骤④的操作方法是______.
(4)某同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸发生反应(方程式为:2Cu+2H2SO4+O2
2CuSO4+2H2O),该方案明显优于原方案,你认为优点是______.现有160kg含铜80%的废料,完全与硫酸、氧气发生反应,最多生成CuSO4______kg.△ .
(5)方案最后一步所得浅绿色滤液结晶后,会得到硫酸亚铁晶体,可增加经济效益.请写出使“绿矾”结晶的两种可能方法:______、______(“绿矾”溶解度随温度升高而增大). 阿弥陀佛555691年前1
阿弥陀佛555691年前1 -
 zhgg9588 共回答了17个问题
zhgg9588 共回答了17个问题 |采纳率100%解题思路:(1)由蓝色溶液与铁反应考虑所得溶液中的溶质;
(2)由图示知稀硫酸与氧化铜反应,可写其反应的化学方程式;
(3)步骤④是分离固液混合物的操作,根据要求可选择适当的分离方法;
(4)对比分析原实验方案,即可知道该方案的明显优点;根据题给的化学方程式和相关数据即可计算出所求数据,这是一道根据化学方程式的计算题;
(5)根据题意确定“绿矾”结晶的两种方法.(1)铜在空气中灼烧生成黑色固体氧化铜,氧化铜与硫酸反应生成蓝色硫酸铜,与铁屑反应置换出铜,反应方程式为:CuO+H2SO4═CuSO4+H2O; Fe+CuSO4═FeSO4+Cu;故溶液A中溶质的化学式是FeSO4;
(2)步骤②中发生的化学方程式为:CuO+H2SO4═CuSO4+H2O;
(3)加入适量的铁屑,是将硫酸铜中的铜全部置换出来,用过滤法即可分离溶液A和红色固体B;
(4)从环保角度对两套方案的不同部分进行比较,开始方案第一步灼烧会产生污染空气的气体,粉尘,烟雾,由此可知第二个方案更合理,根据方程式2Cu+2H2SO4+O2
△
.
2CuSO4+2H2O,计算160kg含铜80%的废料,完全与硫酸、氧气发生反应,最多生成CuSO4 320kg.
(5)结晶的方法有:冷却热饱和溶液和蒸发溶剂法,即蒸发结晶和降温结晶.
故答案为:1)FeSO4;(2)CuO+H2SO4═CuSO4+H2O;(3)过滤;(4)没有废气产生,不污染环境,320;(5)蒸发水分、降温.点评:
本题考点: 酸的化学性质;化学实验方案设计与评价;晶体和结晶的概念与现象;金属的化学性质.
考点点评: 本题考查通过实验现象,培养学生综合利用所学知识进行分析解题的能力.题型涉及知识面广泛,是一道锻炼能力的好题.1年前查看全部
- (本小题满分12分) 2012年4月15日,央视《每周质量报告》曝光某省一些厂商用生石灰处理皮革废料,熬制成工业明胶,卖
(本小题满分12分)
2012年4月15日,央视《每周质量报告》曝光某省一些厂商用生石灰处理皮革废料,熬制成工业明胶,卖给一些药用胶囊生产企业,由于皮革在工业加工时,要使用含铬的鞣制剂,因此这样制成的胶囊,往往重金属铬超标,严重危害服用者的身体健康。该事件报道后,某市 药监局立即成立调查组,要求所有的药用 胶囊在进入市场前必须进行两轮检测,只有两轮都合格才能进行销售,否则不能销售,两轮检测是否合格相互没有影响。
(1)某 药用 胶囊共生产3个不同批次,经检测发现有2个批次为合格,另1个批次为不合格,现随机抽取该 药用 胶囊5件,求恰有2件不能销售的概率;
(2)若对某药用 胶囊 的3个不同批次分别进行两轮检测,药品合格的概率如下表:
记该药用 胶囊 能通过检测进行销售的批次数为第1批次 第2批次 第3批次 第一轮检测 


第二轮检测 


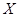 ,求
,求 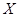 的分布列及数学期望
的分布列及数学期望 
 独自莫凭阑p1年前1
独自莫凭阑p1年前1 -
 deniswong 共回答了9个问题
deniswong 共回答了9个问题 |采纳率66.7%1年前查看全部
- 将一个长、宽、高分别为15厘米、12厘米、9厘米长方体木块,六个面涂上红色,现将它切成正方体,没有废料,至少可切____
将一个长、宽、高分别为15厘米、12厘米、9厘米长方体木块,六个面涂上红色,现将它切成正方体,没有废料,至少可切______块,其中六个面都没有涂上颜色的有______块.
 bennetivan1年前1
bennetivan1年前1 -
 中豪花园 共回答了14个问题
中豪花园 共回答了14个问题 |采纳率78.6%解题思路:(1)要求至少切出多少块,且没有废料,所以切割出的正方体的棱长应是长宽高的最大公因数:15、12、9的最大公因数是3,所以小正方体的棱长是3厘米,所以长宽高上分别可以切出5、4、3个小正方体,再利用长方体的体积公式即可解答切出的小正方体的总个数;
(2)六个面都没涂色的在这个长方体的内部,分别把长宽高边长上切割出的小正方体的个数-2,再利用长方体的体积公式即可计算出内部的小正方体的个数.(1)15、12、9的最大公因数是3,所以小正方体的棱长是3厘米,
则长、宽、高上分别可以切出5、4、3个小正方体,
所以至少可以切出小正方体:5×4×3=60(个);
(2)(5-2)×(4-2)×(3-2),
=3×2×1,
=6(个),
答:至少可切60个小正方体,六个面都没涂色的有6个.
故答案为:60,6.点评:
本题考点: 简单的立方体切拼问题.
考点点评: (1)根据长宽高的最大公因数求出切割的小正方体的边长最大值,是解决此类问题的关键;
(2)要抓住长方体切割成正方体后表面积涂色的规律进行解答.1年前查看全部
- 英语翻译四氯化硅是生产多晶硅的废料,对环境有很大的破坏作用,对四氯化硅的利用不仅能够变废为宝,还能够促进新产业的发展.本
英语翻译
四氯化硅是生产多晶硅的废料,对环境有很大的破坏作用,对四氯化硅的利用不仅能够变废为宝,还能够促进新产业的发展.本文根据四氯化硅与氢氧化钙的水解反应原理,设计出四氯化硅与氢氧化钙的反应制备出硅酸钙的工艺,全面分析工艺组成中的四氯化硅水解系统、原硅酸脱水系统、硅酸钙生成系统的特点,研究工艺过程的影响因素,通过试验,制备出的硅酸钙符合国家标准;在此基础上探讨了工艺副产物的利用.本文的研究有助于解决多晶硅生产废物的严重污染问题,又可大幅度降低多晶硅生产成本,极大提高产业经济效益,对发展***多晶硅和太阳能产业具有十分重要的作用. ss2010081年前1
ss2010081年前1 -
 ysy_f 共回答了20个问题
ysy_f 共回答了20个问题 |采纳率90%The silicon tetrachloride is produces the polycrystalline silicon the waste material, has the very big destructive effect to the environment, not only can recycle waste to the silicon tetrachloride use, but also can promote the new industrial development.This article according to the silicon tetrachloride and the calcium hydroxide hydrolitic reaction principle, designs the silicon tetrachloride and the calcium hydroxide response prepares the calcium silicate the craft, analyzes in the craft composition comprehensively the silicon tetrachloride hydrolysis system, the ortho-silicic acid dehydration system, the calcium silicate production system characteristic, the research technological process influence factor, through the experiment, the calcium silicate which prepares conforms to the national standards; Has discussed the craft by-product use in this foundation.This article research is helpful to the solution polycrystalline silicon production waste serious contamination concern, also may reduce the polycrystalline silicon production cost large scale, enhances the industrial economic efficiency enormously, to develops our country polycrystalline silicon and the solar energy industry has the extremely vital role.1年前查看全部
- 水解法怎样从废水废料中提银
 七月未央12061年前1
七月未央12061年前1 -
 skuirong 共回答了13个问题
skuirong 共回答了13个问题 |采纳率92.3%用3份浓硝酸,1份浓盐酸,混合成王水.然后把废的镀金料放进去.等全部金属溶化后,分离溶液.用石墨电极,通入直流电,进行点解.注意电压别太高,电极别离得太近.接正极的石墨棒上面会凝结金银铜等金属粉末.1年前查看全部
- 在一块面积为888平方厘米的矩形材料的四角,各剪掉一个大小相同的正方形(剪掉的正方形作废料处理,不...
在一块面积为888平方厘米的矩形材料的四角,各剪掉一个大小相同的正方形(剪掉的正方形作废料处理,不...
在一块面积为888平方厘米的矩形材料的四角,各剪掉一个大小相同的正方形(剪掉的正方形作废料处理,不再使用),做成一个无盖的长方体盒子,要求盒子的长为25厘米,宽为高的2倍,盒子的宽和高应为多少? qiyqiy1年前1
qiyqiy1年前1 -
 liushuxin777 共回答了24个问题
liushuxin777 共回答了24个问题 |采纳率91.7%设高为x,则宽为2x,剪拼前材料的宽为4x,长为25+2x.
(25+2x)×4x=888
(2x+37)(x-6)=0
解得 x=6才有意义.
答:高为6厘米,宽为12厘米.1年前查看全部
- 核燃料和裂变后的核废料都具有放射性因而会产生---------污染(填空)
 wzs55371年前2
wzs55371年前2 -
 dthusp 共回答了14个问题
dthusp 共回答了14个问题 |采纳率92.9%环境1年前查看全部
- 本是用来治病救人的药用胶囊,原料竟然是用工业皮革废料制成的工业明胶 翻译成英语怎么翻
 海燕96011年前1
海燕96011年前1 -
 hh大ll 共回答了20个问题
hh大ll 共回答了20个问题 |采纳率95%Medicinal capsule ,which is used to save persons ,is actually made of industrial waste leather industrial gelatin.
虽然没有“原料”——“raw material”,但是意思在,应该没问题.1年前查看全部
- “毒胶囊”泛指利用由工业皮革废料为原料生产的含重金属铬(Cr)超标的胶囊,其中含有可能引起人体肾伤害的+6价的铬.下列铬
“毒胶囊”泛指利用由工业皮革废料为原料生产的含重金属铬(Cr)超标的胶囊,其中含有可能引起人体肾伤害的+6价的铬.下列铬的化合物中铬呈+6价的是( )
A. Cr 2 (SO 4 ) 3 B.Cr 2 O 3 C.K 2 CrO 4 D.CrCl 2  jackyzym1年前1
jackyzym1年前1 -
 一看就知道我懒 共回答了16个问题
一看就知道我懒 共回答了16个问题 |采纳率100%C
根据化合物中正负价代数和为0可知,A~D中Cr元素的化合价分别是+3价、+3价、+6价、+2价,答案选C。1年前查看全部
- 在一块直径是4分米的圆形铁片中间,剪下一个最大的正方形.这个正方形的面积是多少平方分米?四周的废料占圆形面积的几分之几?
 dyg1031年前2
dyg1031年前2 -
 冰千 共回答了22个问题
冰千 共回答了22个问题 |采纳率95.5%正方形对角线即为圆直径,正方形变长为2√2分米
正方形面积=(2√2)^2=4^2/2=8平方分米
原圆面积=π(4/2)^2=4π平方分米=12.56平方分米(π取3.14)
废料占圆形面积=(4π-8)/(4π)=(π-2)/π
π取3.14时废料占圆形面积约为9/251年前查看全部
- 某化学兴趣小组提出可以用含铜废料制备蓝色胆矾(CuSO4•XH2O).查阅资料:
某化学兴趣小组提出可以用含铜废料制备蓝色胆矾(CuSO4•XH2O).查阅资料:
Ⅰ.过氧化氢常温下会缓慢分解为氧气和水.对其水溶液加热、光照或加催化剂(如MnO2)都促进其分解.
Ⅱ.CuSO4•XH2O易溶于水难溶于酒精,加热时会逐步失去结晶水,最终生成CuSO4.
Ⅲ.白色粉末CuSO4易与水化合生成CuSO4•XH2O
I.酸铜晶体的制备
方案1:毛毛同学根据已学知识,提出了制备硫酸铜方案: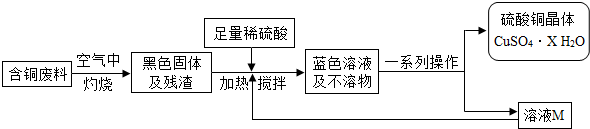
方案2:方舟同学查阅资料归纳了一种工业制备硫酸铜的流程:
(1)上述方案1中加热搅拌的作用是______,形成蓝色溶液的化学反应方程式是:______.
(2)方案2中,加入H2O2后要求温度控制在50℃到60℃是为了防止______.
(3)从环保角度对两套方案的不同部分进行比较,你认为方案______(填1或2)更合理.理由是______.
(4)方案中“一系列操作”依次为:过滤、______、冷却结晶、______(填序号).
A.蒸发浓缩B.加水稀释C.加水溶解D.过滤
(5)溶液M、N都是CuSO4的______(选填a“饱和”、b“不饱和”或c“不一定饱和”)溶液.
(6)所得硫酸铜晶体需要洗涤后晾干,最合适的洗涤试剂是______.
A.冷蒸馏水 B.95%的酒精 C.热蒸馏水
Ⅱ.酸铜晶体(CuSO4•xH2O)中结晶水(xH2O)含量测定学习小组取12.5g硫酸铜晶体(CuSO4•xH2O)进行加热分解,获得相关数据,并绘制成固体质量与温度的关系图.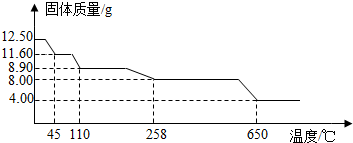
(7)258℃时,固体完全变成白色粉末.根据图中数据,计算CuSO4•xH2O中x的值为______.
加热过程中,硫酸铜晶体分步失去结晶水.请写出45℃到110℃时反应方程式:CuSO4•3H2O
CuSO4•H2O+2H2O↑△ .CuSO4•3H2O.
CuSO4•H2O+2H2O↑△ .
(8)580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为2CuSO4
2CuO+2SO2↑+O2↑△ .2CuSO4.
2CuO+2SO2↑+O2↑△ . liuliudada1年前1
liuliudada1年前1 -
 sssaaa00125 共回答了16个问题
sssaaa00125 共回答了16个问题 |采纳率100%解题思路:(1)根据方案1中加热搅拌的作用是加快反应速率,同时使反应进行更彻底以及氧化铜和硫酸反应生成硫酸铜和水进行解答;
(2)根据方案2中,加入H2O2后要求温度控制在50℃到60℃是为了防止H2O2受热分解进行解答;
(3)根据两个方案的比较,看是否有污染或考虑产量问题;
(4)根据得到硫酸铜晶体需要的步骤进行解答;
(5)根据有晶体析出,说明该溶液是饱和溶液进行解答;
(6)根据用水洗涤可以溶解硫酸铜晶体,使硫酸铜晶体有损失进行解答;
(7)根据由图示数据和“到t1℃时该固体完全失去结晶水”可知,结晶水的质量为:12.50g-8.0g=4.5g,根据结晶水的质量计算出硫酸铜晶体中结晶水的个数;根据加热过程中,硫酸铜晶体分步失去结晶水.所以45℃到110℃时是三水硫酸铜受热分解生成一水硫酸铜和水进行解答;
(8)根据580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物氧化铜、二氧化硫及氧气进行解答.(1)方案1中加热搅拌的作用是加快反应速率,同时使反应进行更彻底;铜灼烧后变成氧化铜,氧化铜与硫酸反应生成硫酸铜和水,所以方程式是:CuO+H2SO4═CuSO4+H2O;
(2)H2O2受热易分解,温度应该控制在50℃到60℃之间,防止H2O2受热分解;
(3)从环保角度对两套方案的不同部分进行比较,甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾,由此可知方案2更合理;
(4)方案中“一系列操作”依次为:过滤、蒸发浓缩、冷却结晶、过滤得到硫酸铜晶体;
(5)有晶体析出,说明该溶液是饱和溶液,所以溶液M、N都是CuSO4的饱和溶液;
(6)用水洗涤可以溶解硫酸铜晶体,使硫酸铜晶体有损失,所以所得硫酸铜晶体需要洗涤后晾干,最合适的洗涤试剂是95%的酒精;
(7)由图示数据和“到t1℃时该固体完全失去结晶水”可知,结晶水的质量为:12.50g-8.0g=4.5g
CuSO4•xH2O
△
.
CuSO4+xH2O↑.
160+18x 18x
12.50g 4.5g
[160+18x/12.50g]=[18g/4.5g]
160+18x=50x
x=5;
(8)加热过程中,硫酸铜晶体分步失去结晶水.所以45℃到110℃时是三水硫酸铜受热分解生成一水硫酸铜和水,反应方程式为:CuSO4•3H2O
△
.
CuSO4•H2O+2H2O↑;
(9)580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物氧化铜、二氧化硫及氧气,反应方程式为:2CuSO4
△
.
2CuO+2SO2↑+O2↑.
故答案为:(1)加快反应速率,同时使反应进行更彻底; CuO+H2SO4═CuSO4+H2O;
(2)H2O2受热分解;
(3)2;避免灼烧废料产生的污染;
(4)A;D;
(5)饱和;
(6)B;
(7)5;
(8)CuSO4•3H2O
△
.
CuSO4•H2O+2H2O↑;
(9)2CuSO4
△
.
2CuO+2SO2↑+O2↑.点评:
本题考点: 物质的相互转化和制备;饱和溶液和不饱和溶液;金属的化学性质;酸的化学性质;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 该题为硫酸铜的知识为线索,考查了多方面的知识,综合性很强,难度较大.1年前查看全部
- 英语翻译1.用焚烧法,废料溶于易燃剂后再焚烧 2.使用过程中外壳,地方排气通风,或其他工程控制,控制空气水平以下建议接触
英语翻译
1.用焚烧法,废料溶于易燃剂后再焚烧
2.使用过程中外壳,地方排气通风,或其他工程控制,控制空气水平以下建议接触限制,设施存储或使用这种材料应配备胡话设施和安全淋浴. shangwenjie_0031年前3
shangwenjie_0031年前3 -
 幻声 共回答了22个问题
幻声 共回答了22个问题 |采纳率95.5%中文都不太通顺,姑且看看吧
1 incineration by pyrolysis.incinerate waste after solved in combustion improver
2 ventilate shells and surroundings under processing or other controls; suggest contact restriction and facility storing on air control,otherwise use of this material requires the equipments of radio communication and security showe1年前查看全部
- (2012•淮安模拟)从一个正方形铁皮上分别剪下不同规格的圆片,剩下的废料( )
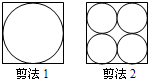 (2012•淮安模拟)从一个正方形铁皮上分别剪下不同规格的圆片,剩下的废料( )
(2012•淮安模拟)从一个正方形铁皮上分别剪下不同规格的圆片,剩下的废料( )
A.剪法1多
B.剪法2多
C.同样多 lijiafang1年前1
lijiafang1年前1 -
 短笛大魔王 共回答了23个问题
短笛大魔王 共回答了23个问题 |采纳率100%解题思路:由题意可知:剪法1:剩下的废料的面积=正方形的面积-一个大圆的面积,剪法2:剩下的废料的面积=正方形的面积-4个小圆的面积;假设正方形的边长是4厘米,则能求出正方形的面积和圆的面积,从而求得剩下的废料的面积.设正方形的边长是4厘米,
则正方形的面积是:4×4=16(平方厘米);
剪法1:圆的半径是4÷2=2(厘米);
剩下的废料的面积是16-3.14×22=16-12.56=3.44(平方厘米);
剪法2:圆的半径是4÷2÷2=1(厘米);
剩下的废料的面积是16-3.14×12×4=16-12.56=3.44(平方厘米);
3.44=3.44,
剩下的废料同样多;
故选:C.点评:
本题考点: 面积及面积的大小比较;长方形、正方形的面积;圆、圆环的面积.
考点点评: 解答此题的关键是明白:剩下的废料的面积=正方形的面积-圆的面积,只要补充上直径的长度,即可求解.1年前查看全部
- (2012•和平区一模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=12.用这块废料剪出一个矩形CDEF,
(2012•和平区一模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=12.用这块废料剪出一个矩形CDEF,其中,点D、E、F分别在AC、AB、BC上.要使剪出的矩形CDEF面积最大,点E应选在何处?

 蚺後弦1年前1
蚺後弦1年前1 -
 zorro521 共回答了20个问题
zorro521 共回答了20个问题 |采纳率80%解题思路:首先在Rt△ABC中利用∠A=30°、AB=12,求得BC=6、AC的长,然后根据四边形CDEF是矩形得到EF∥AC从而得到△BEF∽△BAC,设AE=x,则BE=12-x.利用相似三角形成比例表示出EF、DE,然后表示出有关x的二次函数,然后求二次函数的最值即可.在Rt△ABC中,∠A=30°,AB=12,
∴BC=6,AC=AB•cos30°=12×
3
2=6
3.
∵四边形CDEF是矩形,
∴EF∥AC.
∴△BEF∽△BAC.
∴[EF/AC=
BE
BA].
设AE=x,则BE=12-x.
EF=
6
3(12−x)
12=
3
2(12−x).
在Rt△ADE中,DE=
1
2AE=
1
2x.
矩形CDEF的面积S=DE•EF=
1
2x•
3
2(12−x)=−
3
4x2+3点评:
本题考点: 相似三角形的应用;二次函数的最值.
考点点评: 本题考查了相似三角形的应用及二次函数的应用,解题的关键是从几何问题中整理出二次函数模型,并利用二次函数的知识求最值.1年前查看全部
- )答得好有分给!1.在一块直径是2分米的圆形铁片中间,剪下一个最大的正方形.这个正方形的面积是多少平方分米?四周的废料占
)答得好有分给!
1.在一块直径是2分米的圆形铁片中间,剪下一个最大的正方形.这个正方形的面积是多少平方分米?四周的废料占圆形面积的几分之几?2.一个圆形养鱼池的直径是32米,正中间有一个圆形小岛,直径是6米,这个养鱼池的水面面积是多少平方米?(得数保留整数) 星火20081年前4
星火20081年前4 -
 lanyonqq 共回答了26个问题
lanyonqq 共回答了26个问题 |采纳率96.2%1.正方形面积=对角线平方除以2
所以S正方形为:2*2/2=2(平方分米)
废料的几分之几自己算
2.用养鱼池面积(16*16*π)减去圆形小岛面积(3*3*π)=(256-9)*3=741(平方米)
水玲珑的博客你错了:
[(32/2)-(6/2)]的平方不等于16*16-3*3{初中会提及平方差公式}
还有地地在老大哥:
775不是3的倍数,所以不可能是中间池塘的面积{因为π取3,所以答案应是3的倍数}1年前查看全部
- (7分)(2012•南通)某科研小组利用工业废酸(10%H 2 S0 4 )来浸泡含有氧化铜、氧化锌的废料,实现废物的综
(7分)(2012•南通)某科研小组利用工业废酸(10%H 2 S0 4 )来浸泡含有氧化铜、氧化锌的废料,实现废物的综合利用.流程如下图所示:

(1)写出氧化锌与硫酸反应的化学方程式: _________ ,Zn→Cu的化学方程式为 _________ .
(2)物质X可用作氮肥,化学式为 _________ ;该化肥不能与 _________ 混合使用.
(3)请推出物质Y的化学式: _________ . 3860426891年前1
3860426891年前1 -
 totowc 共回答了18个问题
totowc 共回答了18个问题 |采纳率94.4%(1)ZnO+H 2 S0 4 ═ZnS0 4 +H 2 0 Zn+CuSO 4 ═Cu+ZnS0 4 (2)(NH 4 ) 2 S0 4 ,碱性物质(3)H 2 O
(1)氧化锌与硫酸反应生成了硫酸锌和水,反应的化学方程式:ZnO+H 2 S0 4 ═ZnS0 4 +H 2 0;由于锌的活泼性大于铜,可以将锌与硫酸铜反应来实现Zn→Cu的转变,反应的化学方程式是:Zn+CuSO 4 ═Cu+ZnS0 4 ;
(2)由废物的综合利用流程图和物质间的反应可知,物质X是硫酸铵,可用作氮肥,化学式是:(NH 4 ) 2 S0 4 ,由于铵盐与碱性物质反应放出氨气降低肥效,所以,该化肥不能与碱性物质混合使用;
(3)由元素守恒可知,煅烧碱式碳酸锌碳酸锌生成氧化锌、二氧化碳和水,水的化学式是:H 2 O。1年前查看全部
- 将腰长为6cm,底边长为5cm的等腰三角形废料加工成菱形工件,菱形的一个内角恰好是这个三角形的一个角,菱形的其它顶点均在
将腰长为6cm,底边长为5cm的等腰三角形废料加工成菱形工件,菱形的一个内角恰好是这个三角形的一个角,菱形的其它顶点均在三角形的边上,则这个菱形的边长是______cm.
 hai-run1年前0
hai-run1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2012•株洲模拟)2012年4月15日,央视《每周质量报告》播出节目《胶囊里的秘密》,曝光河北一些企业用皮革废料熬制
(2012•株洲模拟)2012年4月15日,央视《每周质量报告》播出节目《胶囊里的秘密》,曝光河北一些企业用皮革废料熬制成工业明胶,卖给一些企业制成药用胶囊.皮革是由生皮鞣制而成,在生皮鞣制过程中需要添加重铬酸钾,其化学式为K2Cr2O7,试计算:
(1)重铬酸钾中钾、铬、氧元素的质量比是______;
(2)重铬酸钾中铬元素的质量分数是______.(结果保留一位小数) vandean1年前1
vandean1年前1 -
 我没有错123 共回答了22个问题
我没有错123 共回答了22个问题 |采纳率90.9%解题思路:(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
(2)根据物质中某元素的质量分数=[该元素的相对原子质量×原子个数/该物质相对分子质量]×100%,进行解答.(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得重铬酸钾中钾、铬、氧元素的质量比为:(39×2):(52×2):(16×7)=39:52:56;
(2)根据物质中某元素的质量分数=[该元素的相对原子质量×原子个数/该物质相对分子质量]×100%,可得重铬酸钾中铬元素的质量分数为:[52×2/39×2+52×2+16×7]×100%=35.4%;
故答案为:(1)39:52:56; (2)35.4%.点评:
本题考点: 化学式的书写及意义;元素质量比的计算;元素的质量分数计算.
考点点评: 本题考查学生硅根据化学式计算物质中某元素的质量分数、元素质量比计算方法的掌握与应用.1年前查看全部
- (2012•丰泽区质检)已知一种工业废料混合物A是由三种常见金属单质粉末组成,根据该工厂生产用料,可以明确A中不含K、C
(2012•丰泽区质检)已知一种工业废料混合物A是由三种常见金属单质粉末组成,根据该工厂生产用料,可以明确A中不含K、Ca、Na、Sn和Pb五种金属.取少量样品用磁铁检测出含有铁屑,为分离出混合物A中的铁,进行以如图实验操作:

请根据上述实验过程回答以下问题:
(1)金属B属于金属活动顺序表中排在“氢”______(填“前”或“后”)的金属.
(2)操作a的名称是______,该操作需用到的玻璃仪器有______.
(3)金属混合物C中不可能含有以下金属中的______(填化学式).
①Mg②Al③Zn④Fe
(4)写出实验步骤①或③所涉及的一个化学方程式______. 萘萘1年前1
萘萘1年前1 -
 zheg007007 共回答了27个问题
zheg007007 共回答了27个问题 |采纳率92.6%解题思路:本题可根据金属活动性顺序表,利用金属与酸、盐的反应规律来分析,以及分离混合物的常用方法加以解答,从而得出正确的结论.1、加入足量的稀硫酸金属B不能溶解,说明金属B在金属活动顺序表中排在氢后.
2、根据常用混合物的分离方法,操作a后溶液1和固体B分离,符合固体和液体分离,说明操作方法是过滤;用到的玻璃仪器有:玻璃棒、烧杯、漏斗;
3、在金属活动性顺序表中,后面的金属不会把前面的金属从其盐溶液中置换出来,金属镁的活泼性大于铝的活泼性,故不可能含有Mg.
4、根据金属活动性顺序表,利用金属与酸、盐的反应规律,正确写出涉及的一个化学方程式Fe+H2SO4=FeSO4+H2↑,属于置换反应.
答案为:1、后;
2、过滤,玻璃棒、烧杯、漏斗;
3、Mg;
4、Fe+H2SO4=FeSO4+H2↑.点评:
本题考点: 金属的化学性质;过滤的原理、方法及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题可根据金属活动性顺序表及其意义进行考虑,并且考查了化学方程式的写法,及其正确分析实验方面的内容,只要认真思考,按要求作答,一般会到正确答案.1年前查看全部
- 在一个长18厘米,宽16厘米的长方形硬纸板上剪下一个圆,为了使剪掉的废料最少,圆的面积应是多少平方厘米?
 最後的武士1年前3
最後的武士1年前3 -
 命运之匙 共回答了20个问题
命运之匙 共回答了20个问题 |采纳率100%64派1年前查看全部
- 初三试验题,关于铁和氧化铁,32.(6分)同学们在用某硫酸溶液处理金属废料(主要是生铁)时,观察到溶液发烫并闻到刺激性气
初三试验题,关于铁和氧化铁,
32.(6分)同学们在用某硫酸溶液处理金属废料(主要是生铁)时,观察到溶液发烫并闻到刺激性气味,这种反常现象引起同学们的思考.从元素组成的角度分析,他们猜测气体可能是SO2、CO、CO2、H2中的一种或几种.
资料:①SO2与澄清石灰水反应生成亚硫酸钙沉淀;②SO2能与酸性高锰酸钾溶液反应,使之褪色,上述其他气体均不能;③氢气具有还原性.
(1)甲同学认为废气中一定有SO2,原因是 .
(2)为了确定该气体的成分,同学们设计了一套合理的实验装置,如下图所示(铁架台已略去).请你从下列试剂中选择药品并结合实验装置完成实验.
药品:澄清石灰水,酸性高锰酸钾溶液,无水硫酸铜(遇水变蓝),碱石灰(吸收水和CO2).【药品可重复选用,每一步均反应充分】
(Ⅲ)D中反应前有样品10g(样品中可能混有铁),完全反应后剩余固体7.6g,则原样品的成分为:.(写出物质及其对应的质量)
除了8g的氧化铁,还有2g的Fe,为什么啊/?


 shlh181年前1
shlh181年前1 -
 luckpotato 共回答了20个问题
luckpotato 共回答了20个问题 |采纳率85%A→KMnO4,B-是石灰水,c是碱石灰,E是CuSO4,F是石灰水.
原理是先检验二氧化硫(高锰酸钾褪色),高锰酸钾氧化性暴强,基本可以把二氧化硫吸光,接下来检验二氧化碳(排除了二氧化硫的干扰),再用碱石灰确保把把酸性氧化物除尽,用co和H2还原氧化铁(还原氧化铜类似),再检验还原反应产物水的存在,最后检验由co生成的CO2.(不能颠倒,否则石灰水带出水)
结论是"某"硫酸是浓硫酸,会氧化生铁中的碳,铁,生成co,co2,硫酸亚铁,硫酸铁,自己生成二氧化硫,知道变为稀硫酸.
计算用差量法,列出方程3co Fe2O3=3CO2 2Fe求出反应生成的铁是5.6克,拿7.6减掉,是原来混的铁(设氧化铁完全反应,否则没法做),刚好是2克1年前查看全部
- 将一个长、宽、高分别为15厘米、12厘米、9厘米长方体木块,六个面涂上红色,现将它切成正方体,没有废料,至少可切____
将一个长、宽、高分别为15厘米、12厘米、9厘米长方体木块,六个面涂上红色,现将它切成正方体,没有废料,至少可切______块,其中六个面都没有涂上颜色的有______块.
 周至人1年前2
周至人1年前2 -
 蚊蚊77 共回答了12个问题
蚊蚊77 共回答了12个问题 |采纳率100%解题思路:(1)要求至少切出多少块,且没有废料,所以切割出的正方体的棱长应是长宽高的最大公因数:15、12、9的最大公因数是3,所以小正方体的棱长是3厘米,所以长宽高上分别可以切出5、4、3个小正方体,再利用长方体的体积公式即可解答切出的小正方体的总个数;
(2)六个面都没涂色的在这个长方体的内部,分别把长宽高边长上切割出的小正方体的个数-2,再利用长方体的体积公式即可计算出内部的小正方体的个数.(1)15、12、9的最大公因数是3,所以小正方体的棱长是3厘米,
则长、宽、高上分别可以切出5、4、3个小正方体,
所以至少可以切出小正方体:5×4×3=60(个);
(2)(5-2)×(4-2)×(3-2),
=3×2×1,
=6(个),
答:至少可切60个小正方体,六个面都没涂色的有6个.
故答案为:60,6.点评:
本题考点: 简单的立方体切拼问题.
考点点评: (1)根据长宽高的最大公因数求出切割的小正方体的边长最大值,是解决此类问题的关键;
(2)要抓住长方体切割成正方体后表面积涂色的规律进行解答.1年前查看全部
- 将一个长、宽、高分别为15厘米、12厘米、9厘米长方体木块,六个面涂上红色,现将它切成正方体,没有废料,至少可切____
将一个长、宽、高分别为15厘米、12厘米、9厘米长方体木块,六个面涂上红色,现将它切成正方体,没有废料,至少可切______块,其中六个面都没有涂上颜色的有______块.
 又是一个hh呀1年前1
又是一个hh呀1年前1 -
 乐虫虫 共回答了20个问题
乐虫虫 共回答了20个问题 |采纳率100%解题思路:(1)要求至少切出多少块,且没有废料,所以切割出的正方体的棱长应是长宽高的最大公因数:15、12、9的最大公因数是3,所以小正方体的棱长是3厘米,所以长宽高上分别可以切出5、4、3个小正方体,再利用长方体的体积公式即可解答切出的小正方体的总个数;
(2)六个面都没涂色的在这个长方体的内部,分别把长宽高边长上切割出的小正方体的个数-2,再利用长方体的体积公式即可计算出内部的小正方体的个数.(1)15、12、9的最大公因数是3,所以小正方体的棱长是3厘米,
则长、宽、高上分别可以切出5、4、3个小正方体,
所以至少可以切出小正方体:5×4×3=60(个);
(2)(5-2)×(4-2)×(3-2),
=3×2×1,
=6(个),
答:至少可切60个小正方体,六个面都没涂色的有6个.
故答案为:60,6.点评:
本题考点: 简单的立方体切拼问题.
考点点评: (1)根据长宽高的最大公因数求出切割的小正方体的边长最大值,是解决此类问题的关键;
(2)要抓住长方体切割成正方体后表面积涂色的规律进行解答.1年前查看全部
- 在一块直径是8dm的圆形铁片中间,裁下一个最大的正方形.这个正方形的面积是多少平方分米?四周的废料占圆形面积的几分之几?
 从前有座庙1年前1
从前有座庙1年前1 -
 yangchao32 共回答了12个问题
yangchao32 共回答了12个问题 |采纳率83.3%以圆的直径为对角线做一个正方形 面积为 32 圆的面积是16*3.14 废料面积16*3.14-321年前查看全部
- 三张边长都是16cm的正方形铁皮,分别按下图所是剪圆片.哪张铁皮剩下的废料最多?
 c122955331年前0
c122955331年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2012•和平区一模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=12.用这块废料剪出一个矩形CDEF,
(2012•和平区一模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=12.用这块废料剪出一个矩形CDEF,其中,点D、E、F分别在AC、AB、BC上.要使剪出的矩形CDEF面积最大,点E应选在何处?

 恐龙太太1年前3
恐龙太太1年前3 -
 ff5077 共回答了20个问题
ff5077 共回答了20个问题 |采纳率95%解题思路:首先在Rt△ABC中利用∠A=30°、AB=12,求得BC=6、AC的长,然后根据四边形CDEF是矩形得到EF∥AC从而得到△BEF∽△BAC,设AE=x,则BE=12-x.利用相似三角形成比例表示出EF、DE,然后表示出有关x的二次函数,然后求二次函数的最值即可.在Rt△ABC中,∠A=30°,AB=12,
∴BC=6,AC=AB•cos30°=12×
3
2=6
3.
∵四边形CDEF是矩形,
∴EF∥AC.
∴△BEF∽△BAC.
∴[EF/AC=
BE
BA].
设AE=x,则BE=12-x.
EF=
6
3(12−x)
12=
3
2(12−x).
在Rt△ADE中,DE=
1
2AE=
1
2x.
矩形CDEF的面积S=DE•EF=
1
2x•
3
2(12−x)=−
3
4x2+3点评:
本题考点: 相似三角形的应用;二次函数的最值.
考点点评: 本题考查了相似三角形的应用及二次函数的应用,解题的关键是从几何问题中整理出二次函数模型,并利用二次函数的知识求最值.1年前查看全部
大家在问
- 1原始生命诞生的摇篮是什么?
- 2以欲望为话题的高一议论文本次作文题目:印度哲人奥修说:“我无欲无求,我就是皇帝;你有欲有求,你就是奴隶.”请以“欲望”为
- 3下列说法:① ∵ ,∴-0.6是0.36的平方根;② ∵0.8 =0.64,∴0.64的平方根是0.8;③ ∵ ,∴ ;
- 4chicken or fish in it
- 5已知椭圆X^2/a^2+Y^2/b^2=1(a>b>0),圆O:X^2+Y^2=b^2,点A,F分别是椭圆的C的左顶点和
- 6我的英语作文
- 7英语翻译The 'List of Approved Chemicals with Corresponding Brand
- 8(2014•嘉兴二模)在生长素的发现史上,1913年丹麦植物学家波森.詹森进行了如图的实验,以检验达尔文的化学物质假说.
- 9初三英语C篇阅读技巧C篇阅读有很多生词,有时候成片连大体讲的什么事都看不懂.所以C篇阅读每次都会扣两三分.有什么办法能有
- 10The house Mr.Smith _______ has a small grden.
- 11一滴水的旅程 作文
- 12如图所示,有一块直角三角形纸片,两直角边AB=6,BC=8,将直角边AB折叠使它落在斜边AC上,折痕为AD,则BD=__
- 13关于水泵配套电机运行功率计算的问题!
- 14修一条水渠,已修的和未修的长度比是2:5,再修150米正好修了全长的一半,全长是多少米?
- 15一玻璃三棱镜,其截面为等腰三角形,顶角θ为锐角,折射率为 。现在横截面内有一光线从其左侧面上半部射入棱镜。不考虑棱镜内部