在氨的喷泉实验中 若没有胶头滴管 怎么开始试验?
 真的很乱2022-10-04 11:39:541条回答
真的很乱2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 CX_863 共回答了23个问题
CX_863 共回答了23个问题 |采纳率82.6%- 用热毛巾包住烧瓶,使瓶中气体膨胀,向外逸出,接触烧杯中的水,即迅速溶解,导致瓶中气体压强减小,产生倒吸,形成喷泉.
- 1年前
相关推荐
- (10分)下图是做过氨气溶于水的喷泉实验装置,实验完成后烧瓶里的空间被分为两个部分:A和B ,请根据实验内容按要求填空:
(10分)下图是做过氨气溶于水的喷泉实验装置,实验完成后烧瓶里的空间被分为两个部分:A和B
 ,请根据实验内容按要求填空:
,请根据实验内容按要求填空: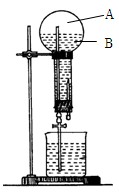
(1)A中的主要成分是 ;
(2)B中溶液即为氨水,把酚酞滴入氨水中,溶液显 色,是因为 (用离子方程式表示);
(3)试剂的滴加顺序不同,有时会产生不同的现象。
①把氨水滴入Al 2 (SO 4 ) 3 溶液中,②把Al 2 (SO 4 ) 3 溶液滴入氨水中, ①、②的实验现象是否相同 (填“相同”或“不同”),写出反应①的化学方程式 ;
反应②的离子方程式 ;
(4)把氨水滴加到FeSO 4 溶液中的现象为
。 放飞心灵sky1年前1
放飞心灵sky1年前1 -
 老蜡 共回答了13个问题
老蜡 共回答了13个问题 |采纳率84.6%1年前查看全部
- 化学氨气喷泉实验甲、乙两组同学用干燥的圆底烧瓶各收集一瓶氨气,根据图B喷泉实验的装置进行实验,都观察到美丽的红色喷泉.甲
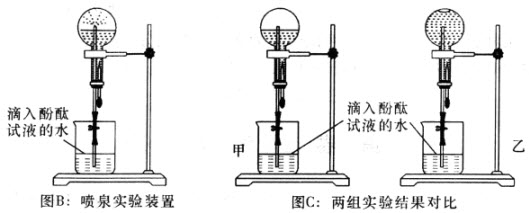
化学氨气喷泉实验
甲、乙两组同学用干燥的圆底烧瓶各收集一瓶氨气,根据图B喷泉实验的装置进行实验,都观察到美丽的红色喷泉.甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图C所示.请通过分析确认:甲组同学所得氨水的物质的量浓度_______(填“大于”、“小于”或“等于”)乙组同学所得氨水的物质的量浓度.
为什么.
 反美hh1191年前3
反美hh1191年前3 -
 轻轻留痕 共回答了22个问题
轻轻留痕 共回答了22个问题 |采纳率95.5%等于
甲进的水少,说明甲收集的氨气少;乙进的水多,说明乙收集的氨气多.但二者进入的水都是因为氨气溶于水而产生内外气压差而被压入的.既然都是氨气自己溶进去的,所以物质的量浓度应该一样.1年前查看全部
- 氨的喷泉实验用氨做的喷泉实验时 烧杯中的水为什么能进入烧瓶中?知道的告诉下 滴有酚酞的水进入烧瓶中为什么会显红色,氨水中
氨的喷泉实验
用氨做的喷泉实验时 烧杯中的水为什么能进入烧瓶中?知道的告诉下
滴有酚酞的水进入烧瓶中为什么会显红色,
氨水中含有哪些粒子
知道的告诉下 我是个zz啊1年前4
我是个zz啊1年前4 -
 泡泡草 共回答了14个问题
泡泡草 共回答了14个问题 |采纳率92.9%氨气在水中溶解度很大,在短时间内产生足够的压强差(负压),则打开活塞后,大气压将烧杯内的水压入烧瓶中,在尖嘴导管口形成喷泉.
滴有酚酞的水进入烧瓶中为什么会显红色,请用化学方程式解释
NH3·H2O=(可逆)NH4+ + OH-
氨水中含有哪些粒子:NH4+,H2O,H+,OH-,NH3·H2O1年前查看全部
- 在同温同压下,用提及不同的烧瓶分别充满氨气和氯化氢气体,做喷泉实验后,水都充满烧瓶
在同温同压下,用提及不同的烧瓶分别充满氨气和氯化氢气体,做喷泉实验后,水都充满烧瓶
烧瓶中物质的量浓度之比是( ) jayappli36961年前2
jayappli36961年前2 -
 lvbinhome 共回答了19个问题
lvbinhome 共回答了19个问题 |采纳率100%设充满氨气和氯化氢气体的体积分别为V1和V2
则n(NH3) = V1/22.4 mol,n(HCl) = V2/22.4 mol
V(氨水) = V1 L,V(盐酸) = V2 L
所以c(NH3.H2O) = (V1/22.4)/V1 = 1/22.4 mol/L,c(HCl) = (V2/22.4)/V2 = 1/22.4 mol/L
所以烧瓶中物质的量浓度之比是1:1
可见容器的体积与物质的量浓度无关.1年前查看全部
- 制取氨气并完成喷泉实验:已知图中:a:氨气; b:水;
制取氨气并完成喷泉实验:
已知图中:a:氨气;b:水;f:止水夹.
(1)写出实验室制取氨气的化学方程式:______
(2)收集氨气应使用______法,要得到干燥的氨气可选用______做干燥剂.
(3)用如图装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是______,该实验的原理是______.
 stretcher1年前1
stretcher1年前1 -
 xiatiandecheng 共回答了13个问题
xiatiandecheng 共回答了13个问题 |采纳率92.3%(1)氯化铵和氢氧化钙发生复分解反应,生成氯化钙、氨气和水,反应方程式为:2NH 4 Cl+Ca(OH) 2
△
.
CaCl 2 +2NH 3 ↑+2H 2 O,
故答案为:2NH 4 Cl+Ca(OH) 2
△
.
CaCl 2 +2NH 3 ↑+2H 2 O;
(2)由于氨气密度比空气小、易溶于水的性质.所以不能采用排水法收集,只能用向下排空气法的收集;反应过程中会产生水,使氨气中混有水蒸气,可用碱石灰吸收水蒸气,但不能用氯化钙和无水硫酸铜,因为它们均与氨气反应,
故答案为:向下排空气;碱石灰;
(3)氨气极易溶于水,如果打开止水夹,氨气溶于水后烧瓶内压强迅速减小,而形成喷泉,
故答案为:打开止水夹,挤出胶头滴管中的水;氨极易溶解于水,致使烧瓶内气体压强迅速减小;1年前查看全部
- 氨:喷泉实验的原理是什么?现象?证明了什么问题?
氨:喷泉实验的原理是什么?现象?证明了什么问题?
急 jyjandwd1年前1
jyjandwd1年前1 -
 wxq8345 共回答了15个问题
wxq8345 共回答了15个问题 |采纳率93.3%氨气易溶于水,生成氨水,成碱性.
现象是水喷到倒置的圆底烧瓶中,成红色.
就是利用大气压,把加酚酞的水压入充满氯气的圆底烧瓶中,氯气迅速溶于水后,遇酚酞变红.1年前查看全部
- (1)同温同压下,两个等体积的干燥烧瓶中分别用排空气法收集①NH3、②HCl,然后分别进行喷泉实验.充分反应后水进入①烧
(1)同温同压下,两个等体积的干燥烧瓶中分别用排空气法收集①NH3、②HCl,然后分别进行喷泉实验.充分反应后水进入①烧瓶3/4,进入②烧瓶2/3.假设溶质全部在烧瓶中,则两个烧瓶中溶质的物质的量浓度为()?
 sepwind1年前1
sepwind1年前1 -
 tangwh 共回答了21个问题
tangwh 共回答了21个问题 |采纳率95.2%设气体的体积是V1,那么气体溶解后进入的溶液的体积也是V1
设该条件下的气体摩尔体积是Vm,则物质的量的浓度c=(V1/Vm)/V1=1/Vm
所以最后的物质的量的浓度都是:1/Vm
比方说,烧瓶内有V L气体溶解了,那么进入的水占的体积就应该是V L,即最后溶液体积是V L.那么溶质就是这V L气体,现在就要算一下气体溶质的物质的量n,有了溶质的物质的量n,和溶液的体积V,可以算物质的量的浓度c=n/V.如果在此时的温度和压强下,1mol气体的体积是Vm L,那么此时的气体摩尔体积就是Vm (L/mol),算出这V L气体的物质的量是V/Vm (mol)
代入公式c=n/V=(V/Vm )mol/V L=1/Vm(mol/L)
可知,在标准状况下,倒吸入烧瓶内的液体浓度就是1/22.4(mol/L)
此公式的条件是,溶于水的气体是单一气体,溶于水后溶质的物质的量不发生改变,适用于SO2,HCL NH3的气体
再比如NO2与O2的混合气体溶于水生成硝酸,就要具体考虑进入液体的体积和溶质硝酸(不再是NO2与O2)的物质的量,再算浓度.1年前查看全部
- 喷泉实验中为什么挤压胶头滴管会有水浸进入烧瓶
 幻望1年前2
幻望1年前2 -
 whong75 共回答了17个问题
whong75 共回答了17个问题 |采纳率94.1%因为挤压滴管,滴管的水进入烧瓶,气体马上溶解在这些水裏面,那麼气压就要减小,小於外界大气压了所以大气压把水压入烧瓶形成喷泉.1年前查看全部
- 有位同学只用了一个圆底烧瓶、带玻璃管的橡胶塞、橡胶管、酒精灯、少量的浓氨水、大烧杯及水,即做成了喷泉实验.如何操作?运用
有位同学只用了一个圆底烧瓶、带玻璃管的橡胶塞、橡胶管、酒精灯、少量的浓氨水、大烧杯及水,即做成了喷泉实验.如何操作?运用了什么原理?若用稀氨水是否也能做成该喷泉实验?
 flyingsqc1年前1
flyingsqc1年前1 -
 赤战云霄 共回答了17个问题
赤战云霄 共回答了17个问题 |采纳率94.1%1年前查看全部
- 城市中常见的人造喷泉及火山爆发的原理与喷泉实验的原理相似吗?
 jedynet1年前2
jedynet1年前2 -
 guzhuowen 共回答了13个问题
guzhuowen 共回答了13个问题 |采纳率84.6%人造喷泉基本原理:控制系统—水泵—喷头,水泵分为两种,潜水泵和离心泵,潜水泵直接放水池里,连接管道和喷头,循环用水.离心泵放泵房里,一般有过滤的水池才用.还有,喷泉的水的确是很脏的,99%是没有过滤的循环水,只补水...1年前查看全部
- 标准状态下,用一充满氨气的圆底烧瓶做喷泉实验,实验完毕后,圆底烧瓶中充入水的体积为其容积的4/5
标准状态下,用一充满氨气的圆底烧瓶做喷泉实验,实验完毕后,圆底烧瓶中充入水的体积为其容积的4/5
1)求原地烧瓶中NH3的体积分数
(2)求所得氨水的物质的量浓度
(3)若测得上述氨水的密度为0.95g/cm3,求此氨水中溶质的质量分数。 叹猪海茫茫1年前1
叹猪海茫茫1年前1 -
 mask1980 共回答了17个问题
mask1980 共回答了17个问题 |采纳率94.1%你想问什么 唔,添加问题啦,这样啊.你看,圆底烧瓶中的NH3的体积分数一定等于浸入的水的体积分数,即就是80%;所得的氨水,设原先的烧瓶为v升,则有氨气0.8v升,氨气的物质的量为0.8v/22.4mol,而溶液的体积现在是0.8v,所以...1年前查看全部
- 做氯化氢的喷泉实验后,烧瓶内的液体只占烧瓶容积的1/3,其原因可能是
做氯化氢的喷泉实验后,烧瓶内的液体只占烧瓶容积的1/3,其原因可能是
A HCl气体没有完全溶解
B 装置漏气,进入空气
C 集气时有空气混入
D 胶头滴管挤入的水太少 zxfbg1年前3
zxfbg1年前3 -
 孤烟刀客 共回答了16个问题
孤烟刀客 共回答了16个问题 |采纳率93.8%HCL溶于水,做那个实验的时候,是Hcl于水接触…HCL能完全溶于水,所以排除AD,然后BC意思是一样的1年前查看全部
- 制取氨气并完成喷泉实验(图中夹持装置均已略去).(1)写出实验室制取氨气化学方程式2NH4Cl+Ca(OH)2
制取氨气并完成喷泉实验(图中夹持装置均已略去).(1)写出实验室制取氨气化学方程式2NH4Cl+Ca(OH)2
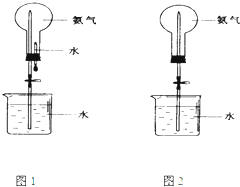 制取氨气并完成喷泉实验(图中夹持装置均已略去).
制取氨气并完成喷泉实验(图中夹持装置均已略去).
(1)写出实验室制取氨气化学方程式2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O△ .2NH4Cl+Ca(OH)2;氨气分子的空间构型为______,该分子由______(填“极性”或“非极性”)键构成的______(填“极性”或“非极性”)分子;氨气的水溶液叫氨水,氨水显弱碱性的原因可用方程式表示为______.
CaCl2+2NH3↑+2H2O△ .
(2)收集氨气应使用______法,要得到干燥的氨气可选用______做干燥剂;用______方法检验氨气是否已收集满.
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是______;该实验的原理是______;
(4)如果只提供如图2的装置,______(填“能”或“不能”)引发喷泉,如果能,请说明引发喷______.
 冷若馨1年前1
冷若馨1年前1 -
 flyeer 共回答了22个问题
flyeer 共回答了22个问题 |采纳率95.5%(1)氯化铵与氢氧化钙反应生成氯化钙、氨气和水,化学方程式为:2NH4Cl+Ca(OH)2
△
.
CaCl2+2NH3↑+2H2O,氨气分子是N与H形成的极性共价键形成的分子,正负电荷重心不重合,是极性分子,氨水中的一水合氨为弱电解质存在电离:NH3?H2O NH4++OH-,所有氨水显碱性;
故答案为:2NH4Cl+Ca(OH)2
△
.
CaCl2+2NH3↑+2H2O;极性;极性;NH3?H2O NH4++OH-;
(2)氨气是一种密度小于空气密度,极易溶于水的气体,应选择向下排空气法收集;氨气为碱性气体,应选择碱石灰等碱性干燥剂;氨气为碱性气体遇到湿润的红色石蕊试纸能够使其变蓝;
故答案为:向下排空气法;碱石灰;湿润的红色石蕊试纸靠近集气瓶口看是否变蓝;
(3)氨气是一种极易溶于水的气体,将胶头滴管中的水挤入烧瓶中,瓶内压强减小,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:打开止水夹,挤出胶头滴管中的水;氨气极易溶解于水,致使烧瓶内气体压强迅速减小;
(4)氨气是一种极易溶于水的气体,打开夹子,用手(或热毛巾等)将烧瓶捂热,部分氨气溶于水形成压强差,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:能;打开夹子,用手(或热毛巾等)将烧瓶捂热.1年前查看全部
- 下列有关实验或操作的叙述正确的是 [ ] A.如图1,做喷泉实验时观察到
下列有关实验或操作的叙述正确的是 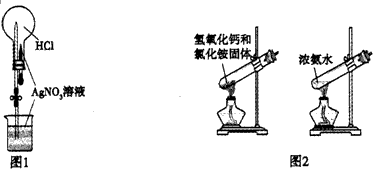 [ ]
[ ]A.如图1,做喷泉实验时观察到产生白色喷泉
B.如图2,两套装置均可用来制备NH 3 (不考虑净化和收集)
C.称取2.5 g CuSO 4 ·5H 2 O,放入100 mL容量瓶中,配制0.10 mol·L -1 的CuSO 4 溶液
D.除去NaHCO 3 溶液中的Na 2 CO 3 ,可加入Ca(OH) 2 溶液后过滤 可爱的猫咪大人1年前1
可爱的猫咪大人1年前1 -
 shadow3000 共回答了14个问题
shadow3000 共回答了14个问题 |采纳率78.6%A1年前查看全部
- 为什么碳酸氢铵和氢氧化钠不会产生喷泉实验
 静如初1年前3
静如初1年前3 -
 78858138a 共回答了12个问题
78858138a 共回答了12个问题 |采纳率83.3%二者反应:NH4HCO3 + 2NaOH = Na2CO3 +NH3•H2O + H2O
在氢氧化钠较浓且过量,加热时,氨气方能逸出,其中仍含有一定量的水蒸气.不具备氨气急速溶解而导致内外压差较大,形成喷泉条件,
如果欲通过此法做喷泉实验,可先将生成的氨气通过碱石灰干燥后再进行收集.1年前查看全部
- HCl气体可以进行喷泉实验,若烧瓶中收集到的HCl气体中混有空气,且占烧瓶体积的一半,则烧瓶中气体的平均式量是_____
HCl气体可以进行喷泉实验,若烧瓶中收集到的HCl气体中混有空气,且占烧瓶体积的一半,则烧瓶中气体的平均式量是_____ ,理论上水将充满烧瓶体积的__________.
 终点是起点1年前1
终点是起点1年前1 -
 浩号 共回答了22个问题
浩号 共回答了22个问题 |采纳率77.3%空气是29 氯化氢气体是36.5吧 平均一下就行
HCl气体和水的溶解度貌似是1:500 反正很高 就当全部可溶 那么空气中大部分的N2和O2气几乎不溶 当时内部气压小于外部气压 剩下的空气又不溶 那就二分之一咯1年前查看全部
- 喷泉是一种常见的自然现象,其产生原因是存在压强差.如图为化学教学中用的喷泉实验装置.在烧瓶中充满干燥气体,胶头滴管及烧杯
喷泉是一种常见的自然现象,其产生原因是存在压强差.如图为化学教学中用的喷泉实验装置.在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体,下列组合中不可能形成喷泉的是( ) A.HCl和H 2 O B.O 2 和H 2 O C.NH 3 和H 2 O D.CO 2 和NaOH溶液 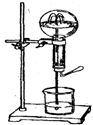
 取舍压田1年前1
取舍压田1年前1 -
 borymeng 共回答了21个问题
borymeng 共回答了21个问题 |采纳率85.7%A、氯化氢易溶于水,烧瓶中的气体压强就会减小,故能形成喷泉.
B、氧气不易溶于水,烧瓶中的气体压强不会有明显的变化,故不能形成喷泉.
C、氨气极易溶于水,烧瓶中的气体压强就会减小,故能形成喷泉.
D、二氧化碳能和氢氧化钠溶液反应,烧瓶中的气体压强就会减小,故能形成喷泉.
故答案选:B1年前查看全部
- 可以进行喷泉实验的物质有什么?如题
 雨滴子恋1年前2
雨滴子恋1年前2 -
 lee_ann 共回答了25个问题
lee_ann 共回答了25个问题 |采纳率84%(1)NH3、HCl、SO2、NO2 与水组合能形成喷泉.
(2)酸性气体与NaOH(aq)组合能形成喷泉.
(3)有机气体与有机溶剂组合也能形成喷泉.
(4)O2、N2、H2 等不溶于水的气体,设计一定实验条件将其反应掉,也能形成喷泉.1年前查看全部
- 用一充满氨气的烧瓶做喷泉实验,当水充满整个烧瓶后,烧瓶内的氨气的物质的量浓度是(按标准状况下计算)
用一充满氨气的烧瓶做喷泉实验,当水充满整个烧瓶后,烧瓶内的氨气的物质的量浓度是(按标准状况下计算)
为什么 晨曦6191年前1
晨曦6191年前1 -
 xg_861020 共回答了28个问题
xg_861020 共回答了28个问题 |采纳率92.9%1/22.4升每摩尔1年前查看全部
- 若用NO和O2(比例为4:3)的混合气进行喷泉实验,
若用NO和O2(比例为4:3)的混合气进行喷泉实验,
则所得溶液中溶质的物质的量浓度为 mol/L; chensanchu_19831年前2
chensanchu_19831年前2 -
 sky19830810 共回答了21个问题
sky19830810 共回答了21个问题 |采纳率95.2%0.0255mol/L1年前查看全部
- 用充满NH3的烧瓶做喷泉实验,当水充满整个烧瓶后,所得溶液物质的量浓度为(非标况下)是不是无法计算呢
 gwcrystal1年前3
gwcrystal1年前3 -
 beastfriend 共回答了24个问题
beastfriend 共回答了24个问题 |采纳率83.3%非标况的情况下计算稍微困难一点.如果是假设标况下,那么知道体积V之后就知道了氨气的摩尔质量n,于是可以得到浓度.
非标况下,需要利用理想气体状态方程,利用PV=nRT,在保证室温和大气压,体积不变情况下,n摩尔质量保持不变,R=8.314为常数,只改变温度以及改变温度引起n的变化,可以得到等式T1/n1=T2/n2,就可以把室温实验条件下的摩尔质量换算成标况下的摩尔质量,从而得到浓度.这个理想气体状态方程高中不要求,所以要计算的话一般只会假设标况的.1年前查看全部
- 用NO2气体和O2按4比1体积比混合,做喷泉实验,喷泉结束后水充满烧瓶,则溶液物质的量浓度是多少?
用NO2气体和O2按4比1体积比混合,做喷泉实验,喷泉结束后水充满烧瓶,则溶液物质的量浓度是多少?
用氯化氢气体做喷泉实验喷泉结束后,水充满烧瓶,则溶液的物质的量浓度为?
用NH3气体做喷泉实验喷泉结束后,水充满烧瓶,则溶液的物质的量浓度为? leaf1621年前2
leaf1621年前2 -
 guyoubao 共回答了14个问题
guyoubao 共回答了14个问题 |采纳率78.6%曼妥思糖含有一种叫做阿拉伯胶的化学物质,这种化学物质遇到含有碳酸盐成分的可乐后,让水分子的表面张力更易被突破,以惊人的速度释放更多的二氧化碳,由于反应剧烈,产生的气体让可乐喷出很高.1年前查看全部
- 二氧化氮和二氧化硫溶解度比氯化氢 氨气小多了,怎么还能做喷泉实验?
 雪后的春天1年前2
雪后的春天1年前2 -
 a_bong16 共回答了21个问题
a_bong16 共回答了21个问题 |采纳率95.2%做喷泉实验的最关键一点是,形成气压差,并且小也是相对的,而不是溶解度问题,因为二氧化氮和水反应生成硝酸和一氧化氮而且反应相当迅速剧烈,二氧化氮和一氧化氮气体比例是3:1,有2的差,形成了气压差,将水压上去,所以可以做喷泉实验,二氧化硫也是同样的道理,形成亚硫酸,气体被吸收.1年前查看全部
- 氯化氢氨气二氧化氮进行喷泉实验
 Google测试员3131年前1
Google测试员3131年前1 -
 mxq2004 共回答了18个问题
mxq2004 共回答了18个问题 |采纳率94.4%HCL与NH3反应使压强变小,从而使容器中的水或者其他液体向上喷,从而形成喷泉.1年前查看全部
- 能做喷泉实验的条件是什么
 2003年5月1年前4
2003年5月1年前4 -
 云灵飞狐 共回答了19个问题
云灵飞狐 共回答了19个问题 |采纳率94.7%条件:气体极易溶于液体.密封性好.形成喷泉的根本原因是压力差.此外,还可以通过温度的改变等情况形成压力差,这样同样可以形成喷泉.氨气溶于与水.还可是气体与液体反应导致压强变小.1年前查看全部
- 相同状况下,在容积相同的三个烧瓶内分别充满干燥的氨气,氯化氢,二氧化氮气体做喷泉实验,实验后烧瓶内溶液液面的高度关系为
 篮叶子1年前1
篮叶子1年前1 -
 ywp2003123 共回答了19个问题
ywp2003123 共回答了19个问题 |采纳率89.5%氨气>氯化氢>二氧化氮原因是相同条件下三种气体的溶解度氨气>氯化氢>二氧化氮.1年前查看全部
- 没有交投滴管氨溶于水的喷泉实验怎么引发
 liuhuangshu1年前1
liuhuangshu1年前1 -
 紫竹_晓 共回答了18个问题
紫竹_晓 共回答了18个问题 |采纳率100%打开止水夹,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃管内的空气,氨气与水接触后迅速溶解,使烧瓶内压强减小.就能发生喷泉.1年前查看全部
- 喷泉实验的原理?
 szyx9881年前1
szyx9881年前1 -
 bdo8e 共回答了20个问题
bdo8e 共回答了20个问题 |采纳率85%实验的基本原理是使瓶内外在短时间内产生较大的气压差,利用大气压将瓶下面烧杯中的液体压入瓶内,在尖嘴导管口处形成喷泉.1体积水可溶解700体积的氨气(0摄氏度,1标准大气压下),当滴管内的水进入烧瓶内时,氨气大量溶于水,外界大气压将水压入瓶中,剩余氨气又溶于进入瓶中的水,最终水充满烧瓶.x0d这类实验的要求是:1.装置气密性好x0d2.所用气体能大量溶于所用液体或气体与液体快速反应x0d推荐几组气体和液体: 1.氯化氢气体和水( HCl溶解度为1:400)x0d2.二氧化碳和氢氧化钠溶液(效果不明显)1年前查看全部
- 化学氨气溶于水的喷泉实验请问该实验器材中双孔塞有什么用
 竖琴手WL1年前1
竖琴手WL1年前1 -
 缘织梦 共回答了26个问题
缘织梦 共回答了26个问题 |采纳率92.3%塞子插倒置的烧瓶(喷泉发生的地方)一个孔插胶头滴管(引发喷泉的关键)另一个插长导管,连接苯酚溶液1年前查看全部
- 用CCL4萃取碘水中的碘为什么不需要玻璃棒呢?用充满氨气的烧瓶做喷泉实验为什么不需要玻璃棒呢?而用蔗糖浓硫酸和水在小烧杯
用CCL4萃取碘水中的碘为什么不需要玻璃棒呢?用充满氨气的烧瓶做喷泉实验为什么不需要玻璃棒呢?而用蔗糖浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验又为什么要用玻璃棒呢
 babyface静静1年前1
babyface静静1年前1 -
 蓉生 共回答了17个问题
蓉生 共回答了17个问题 |采纳率88.2%蔗糖和浓硫酸在小烧杯中进行浓硫酸的脱水性实验时候放出大量的热,要用玻璃棒不断搅拌以使热量扩散,否则会喷出造成事故.其他那2个实验没有这个必要.1年前查看全部
- 在圆底烧瓶里收满氯化氢气体后,借助于水就可以做美丽的喷泉实验,如果实验后烧瓶内未能充满液体
在圆底烧瓶里收满氯化氢气体后,借助于水就可以做美丽的喷泉实验,如果实验后烧瓶内未能充满液体
在圆底烧瓶里收满氯化氢气体后,借助于水就可以做美丽的喷泉实验,如果实验后烧瓶内未能充满液体,可能的原因有_____和______.你还能列举出能形成喷泉实验的气体与液体吗?如______和______. 常忘用户名1年前2
常忘用户名1年前2 -
 mslieo13 共回答了19个问题
mslieo13 共回答了19个问题 |采纳率89.5%气体没充满烧瓶; 烧瓶可能漏气
氨气和水1年前查看全部
- 关于喷泉实验的化学计算题装置烧瓶中NH3的质量是相同状况下相同体积氢气质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧
关于喷泉实验的化学计算题
装置烧瓶中NH3的质量是相同状况下相同体积氢气质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧瓶容积的几分之几? 岁月书签1年前1
岁月书签1年前1 -
 泡泡黑鱼 共回答了29个问题
泡泡黑鱼 共回答了29个问题 |采纳率89.7%17.9
.20
29.3
3/41年前查看全部
- 关于NO2的喷泉实验有做过喷泉实验的亲应该知道的,就是烧瓶里的气体用NO2,滴管里,烧杯里的液体是NaOH溶液.为什么这
关于NO2的喷泉实验
有做过喷泉实验的亲应该知道的,就是烧瓶里的气体用NO2,滴管里,烧杯里的液体是NaOH溶液.为什么这样也能成喷泉?原理是什么呀? 阳澍MX1年前3
阳澍MX1年前3 -
 fqxie 共回答了21个问题
fqxie 共回答了21个问题 |采纳率95.2%喷泉实验的基本原理都一样 存在压差
NO2和NaOH反应 2NO2 + 2NaOH==NaNO3 + NaNO2 + H2O 瓶内压强明显减小,因此能形成喷泉1年前查看全部
- 在喷泉实验的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷
在喷泉实验的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是 ( )
---a(干燥气体)-b(液体)
A---NO2----水
B---Cl2---饱和的NaCl溶液
C---NH3----1mol·L-1HCl
为什么A不可以选而是选C? happy834271年前4
happy834271年前4 -
 yyyyppoo 共回答了19个问题
yyyyppoo 共回答了19个问题 |采纳率89.5%二氧化氮和水反应生成一氧化氮,一氧化氮不融于水,所以无法充满烧瓶,所以不能选择A,氨气完全融于水1年前查看全部
- NO2气体和O2按4比1体积比混合或氨气或一半空气一半氯化氢做喷泉实验 所得的溶液量浓度之比为多少
 繁华如梦1年前3
繁华如梦1年前3 -
 uuuiiiddd 共回答了18个问题
uuuiiiddd 共回答了18个问题 |采纳率94.4%4NO2+O2+2H2O=4HNO3
4+1 4
5mol气体产生4molHNO3
比如1升气体可得到1/22.4× 4/5mol=0.035714285714286mol
那么水溶液浓度≈0.0357mol/L
一半空气一半氯化氢同理1/22.4× 0.5mol= 0.0223mol/L1年前查看全部
- 喷泉实验中装氨气的圆底烧瓶一定要干燥吗?
 笑逗号1年前1
笑逗号1年前1 -
 南京时间 共回答了15个问题
南京时间 共回答了15个问题 |采纳率100%尽量干燥效果最好,因为氨气的溶解度很大,大概1:700,潮湿的烧瓶会影响实验结果.所以干燥的烧瓶喷泉的效果会好很多...1年前查看全部
- 一同学 用排空气发收集了一瓶铵气,测其密度,他对H2的相对密度为10,如果用该瓶子气体做喷泉实验,则水上升的体积约占容器
一同学 用排空气发收集了一瓶铵气,测其密度,他对H2的相对密度为10,如果用该瓶子气体做喷泉实验,则水上升的体积约占容器体积的多少?
 chedi1年前2
chedi1年前2 -
 敢笑柬之不懂书 共回答了19个问题
敢笑柬之不懂书 共回答了19个问题 |采纳率94.7%设氨气占瓶子体积的a% ,空气占瓶子体积的b%.由于空气平均摩尔质量为29,氨气为17,而瓶子里面的气体只可能是氨气和空气的混合气体,很和气体的密度是氢气的10倍,则其相对式量为2x10=20.
17xa%+29xb%=20
a%+b%=1
解得a%=3/4
又因为氨气完全溶于水,所以水上升的体积就是氨气的体积,占容器体积的3/41年前查看全部
- A是一种酸式盐,它与NaOH共热,放出无色气体B,B可以做喷泉实验!请问A,B各是什么?
 020sj1年前3
020sj1年前3 -
 heyalin88 共回答了17个问题
heyalin88 共回答了17个问题 |采纳率88.2%A:碳酸氢铵:NH4HCO3
B:氨气:NH31年前查看全部
- 如图是课外活动小组的同学设计的4个喷泉实验方案.下列有关操作不可能引发喷
如图是课外活动小组的同学设计的4个喷泉实验方案.下列有关操作不可能引发喷
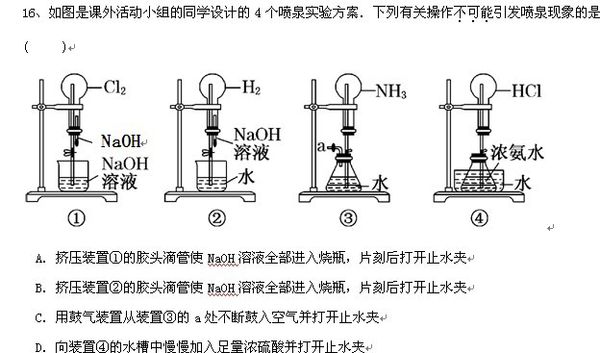
重点分析A, l_jq1年前2
l_jq1年前2 -
 ujjlkss 共回答了34个问题
ujjlkss 共回答了34个问题 |采纳率91.2%A,可以,因为氯气可以与氢氧化钠反应,使烧瓶中形成负压,打开止水夹,氢氧化钠溶液进入到烧瓶中,而氯气可以继续与氢氧化钠溶液反应,形成喷泉.
B,不可以,氢气不与氢氧化钠溶液反应.
C,可以,形成正压,水进入烧瓶,氨气极易溶于水,
D,可以,浓硫酸溶于水放出大量的热,浓氨水分解,生成氨气与氯化氢反应生成氯化铵,形成负压,1年前查看全部
- 下列与氯化氢喷泉实验无关的是A烧瓶内氯化氢气体的体积分数B烧瓶容积的大小C烧瓶内外气体压强D连接烧瓶和烧杯的玻璃管长度答
下列与氯化氢喷泉实验无关的是
A烧瓶内氯化氢气体的体积分数
B烧瓶容积的大小
C烧瓶内外气体压强
D连接烧瓶和烧杯的玻璃管长度
答案B请把其他选项解释一下不选的原因 Lancer111年前1
Lancer111年前1 -
 2185326 共回答了15个问题
2185326 共回答了15个问题 |采纳率100%A,氯化氢多了,更容易形成喷泉,因为它溶解于水后,导致里面气体变小,压强变小.
C.是因为内外压强不同,才被压上去的啊.
D.如果玻璃管太长,喷泉就不一定形成了啊,因为可能内外压强差,只能把液体不能完全压到玻璃管上面啊,这样就没有喷泉了啊.1年前查看全部
- 化学老师说用氨气的融水性可以做一个喷泉实验,具体步骤是什么,现象怎么样啊?
 xiasunny1年前1
xiasunny1年前1 -
 Evilfool 共回答了11个问题
Evilfool 共回答了11个问题 |采纳率81.8%喷泉实验的基本原理是: 气体在液体中溶解度很大,在短时间内产生足够的压强差(负压),则打开活塞后,大气压将烧杯内的液体压入烧瓶中,在尖嘴导管口形成喷泉.为了解决这个问题,我们想起影响气压的几个因素.
请参考百度文库中喷泉实验内容.
在水中滴加几滴酚酞试剂,水溶液进入时会变成红色.1年前查看全部
- 喷泉实验中挤压胶头滴管的作用是什么
 可不可以别这样1年前1
可不可以别这样1年前1 -
 浮躁的鱼 共回答了25个问题
浮躁的鱼 共回答了25个问题 |采纳率96%在胶头滴管中事先吸入少量水,做实验的时候,先挤压胶头滴管,使水释放出来,吸收气体后,烧瓶中的气压降低,这样,烧杯中的水就会压入烧瓶,形成喷泉了.
喷泉形成的原理就是:想办法造成烧瓶内外气压差.1年前查看全部
- 氨气可以做喷泉实验,是因为?1、氨气极易溶于水2、氨气与水反应这是个选择题中的两个选项,选1?还是双选?
 ziyue8001年前2
ziyue8001年前2 -
 akos123 共回答了27个问题
akos123 共回答了27个问题 |采纳率92.6%喷泉实验的基本原理是:气体在液体中溶解度很大,在短时间内产生足够的压强差(负压),则打开活塞后,大气压将烧杯内的液体压入烧瓶中,在尖嘴导管口形成喷泉.
氨气在水中的溶解度极大,所以1正确.虽然氨气和水也发生反应但不是决定因素.1年前查看全部
- 在体积为VL的干燥烧瓶中,用排空气法充入HCl气体后,测得瓶中气体对O2的相对密度为1.082,此气体进行喷泉实验,喷泉
在体积为vl的干燥烧瓶中,用排空气法充入hcl气体后,测得瓶中气体对o2的相对密度为1.082,此气体进行喷泉实验,喷泉停止后,进入***体积是( )
a. 0.25vl
b. 0.5vl
c. 0.75vl
d. vl 曾经的酷爱1年前4
曾经的酷爱1年前4 -
 0625panpan 共回答了9个问题
0625panpan 共回答了9个问题 |采纳率100%解题思路:根据瓶中气体对O2的相对密度为1.082计算混合气体的平均相对分子质量,根据相对分子质量计算混合气体中氯化氢的体积,进入水的体积即为氯化氢的体积.由n=[m/M=
V
Vm]可知,ρ=
m
V=
M
Vm,在相同条件下气体的相对分子质量之比等于密度之比,
瓶中气体对O2的相对密度为1.082,则混合气体的平均相对分子质量为1.082×32=34.624,
设混合气体中含有xmol空气,ymol氯化氢,
则有:[29x+36.5y/x+y]=34.624,
x:y≈1:3,
根据阿伏加德罗定律可知,在相同条件下气体的物质的量之比等于气体的体积之比,
混合气体中氯化氢的体积为
3
1+3×VL=0.75VL,
故选C.点评:
本题考点: 阿伏加德罗定律及推论.
考点点评: 本题考查阿伏加德罗定律定律及其推论,题目难度中等,解答本题的关键是在相同条件下气体的相对分子质量之比等于密度之比,根据相对密度计算混合气体的平均相对分子质量,进而计算混合气体的体积比.1年前查看全部
- 哪些气体与液体能做喷泉实验,最好要有颜色?
哪些气体与液体能做喷泉实验,最好要有颜色?
最好要有颜色,要越多越好,答的最多的有加分,前面说过的别重复,尽快啊, 猪猪呦1年前3
猪猪呦1年前3 -
 gcm0202 共回答了16个问题
gcm0202 共回答了16个问题 |采纳率93.8%1.氨气和酚酞溶液 红色
2.H2S和CuSO4 黑色
3.HCl和AgNO3 白色
4.H2S和H2SO3 黄色
5.HBr和AgNO3 淡黄色
6.HI和AgNO3 黄色1年前查看全部
- 同温同压下,两个等体积的干燥烧瓶中分别用排空气法收集①NH3、②NO2,然后分别进行喷泉实验.充分反应后水进入烧瓶.假设
同温同压下,两个等体积的干燥烧瓶中分别用排空气法收集①NH3、②NO2,然后分别进行喷泉实验.充分反应后水进入烧瓶.假设溶质全部在烧瓶中,则两个烧瓶中溶质的物质的量浓度为()?
答案是①=②
原瓶中充满气体,所以应该没有气体啊!那二氧化氮会和水反应生成一氧化氮啊!一氧化氮不溶于水,那么进入瓶中的水就要少一点啊,那么NO2的不应该大一点吗? 飞双鱼1年前1
飞双鱼1年前1 -
 wangqi9940 共回答了15个问题
wangqi9940 共回答了15个问题 |采纳率93.3%设体积为V,则NH3物质的量为V/22.4,最后充满溶液体积为V,所以溶质的物质的量浓度=1/22.4 mol/L;而NO2体积为V,物质的量=V/22.4 mol,反应为:
3NO2+H2O= 2HNO3 + NO
3 2
V/22.4 2V/3*22.4 所得溶液体积为2V/3
生成溶液溶质的物质的量浓度=2V/3*22.4÷ 2V/3=1/22.4 mol/L
所以①=②1年前查看全部
- (详见补充)向体积为1L的干燥容器中充入氯化氢气体,测出容器里的气体对氧气的相对密度为1.082,若用此气体进行喷泉实验
(详见补充)
向体积为1L的干燥容器中充入氯化氢气体,测出容器里的气体对氧气的相对密度为1.082,若用此气体进行喷泉实验,当喷泉停止后,吸进容器的液体体积为
A)0.25L B)0.5L C)0.75L D)1L 12345asd77551年前1
12345asd77551年前1 -
 zhouruihua 共回答了24个问题
zhouruihua 共回答了24个问题 |采纳率83.3%容器里的气体对氧气的相对密度为1.082,由于密度之比等于相对分子质量之比,则容器里的气体的相对分子质量为1.082*32=34.624,说明容器里的气体是空气与氯化氢的混合气体,设容器中的气体的总物质的量为1mol,氯化氢的物质的量为a,空气的物质的量为b,则a+b=1mol,36.5a+29b=34.625,则解出a=0.75mol,b=0.25mol,由于相同条件下体积之比等于物质的量之比,氯化氢极易溶于水,所以容器的液体的体积就是氯化氢的体积为0.75L1年前查看全部
- 喷泉实验的反应原理是什么?(烧杯里放的是NAOH)为什么H2不能做喷泉实验?
喷泉实验的反应原理是什么?(烧杯里放的是NAOH)为什么H2不能做喷泉实验?
为什么所放的气体一定是要能与烧杯内的液体反应的? liushuai10001年前2
liushuai10001年前2 -
 七月流火lee 共回答了29个问题
七月流火lee 共回答了29个问题 |采纳率79.3%不一定要“能反应”,只要能被大量“吸收”就行.
“吸收”后内部压强减小,液体就被大气压压上去了1年前查看全部
- 都能用右图装置进行喷泉实验的一组气体是 A HCl和CO2 B NH3和CO C SO2和O2 D N2和CO2
都能用右图装置进行喷泉实验的一组气体是 A HCl和CO2 B NH3和CO C SO2和O2 D N2和CO2
装置是 烧杯中是NAOH crazybayb1年前1
crazybayb1年前1 -
 今晚喝了点 共回答了19个问题
今晚喝了点 共回答了19个问题 |采纳率89.5%A1年前查看全部
大家在问
- 1醋酸与纯碱在铝制容器中反应可能会生成什么物质
- 2求很多初中英语阅读文章译文带译文 篇数越多 分越多
- 3下列有关受精作用的叙述中,错误的一项是( )
- 4当现实遇到梦想翻译英语
- 5减数分裂和受精作用过程对于人的重要意义是 其原因是
- 6某超市将进货单价为l8元的商品按每件20元销售时,每日可销售100件,如果每件提价1元,日销售就要减少10件,那么把商品
- 7在正方形除以8等于三角形余数中,余数最大是多少?
- 8把它们混合在一起会是什么运动?英语翻译
- 9用硝酸钙和碳酸钾制取一种复合肥,若使用硝酸钙样品500g,生成200g沉淀,求反应后硝酸钾溶液的溶质质量分
- 10蝉有6只脚,蜘蛛有8只脚,现有蝉和蜘蛛共20只,蝉共比蜘蛛多50只脚,问蝉和蜘蛛各有多少只?
- 11怎样制备氟化钾利用硫酸\氯化钾\氢氧化钙为原料制备
- 12洋葱根尖细胞肯定没有的细胞器是
- 131、妈妈有一张周长是48厘米的正方形彩纸,想给小红剪成半径是1.5厘米的圆形纸片,最多可以剪几个?
- 14要么做恋人,要么做陌生人!英文翻译,
- 15请为下面句子断句,应读出什么语气?


