下表中与各粒子名称对应的各项内容均正确的是( ) 选项 内容
 jvfh2022-10-04 11:39:541条回答
jvfh2022-10-04 11:39:541条回答| 选项 | 内容 粒子名称 | 符号 | 结构示意图 | 电性 | 化学性质 |
| A | 钠原子 | Na | 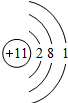 | 中性 | 活泼易得电子 |
| B | 铝离子 | Al3+ |  | 带三个单位正电荷 | 活泼 |
| C | 氧原子 | O | 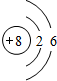 | 中性 | 稳定 |
| D | 氯离子 | Cl- |  | 带一个单位负电荷 | 稳定 |
A.钠原子
B.铝原子
C.氧原子
D.氯原子

已提交,审核后显示!提交回复
共1条回复
 alive119 共回答了19个问题
alive119 共回答了19个问题 |采纳率84.2%- 解题思路:因为物质参加化学反应时发生作用(得失电子)的一般只是最外层电子,所以说与元素化学性质最密切的是最外层电子数.一般以4个外层电子为界(氢,氦除外).其外层电子少于4个较为容易失去电子,外层电子电子数越少,其越容易失去电子,其外层电子多于4个的较为容易得到电子,其外层电子数越多(少于8),其得到电子的能力越强,而外层电子电子数为8刚刚好,因为其电子结构最为稳定,所以化学性质也最为稳定.
A、最外层电子数是1,活泼易失掉电子,故此选项错误.
B、铝离子最外层有8个电子,是稳定结构,故此选项错误.
C、氧原子最外层有6个电子,易得电子,不稳定,故此选项错误.
D、氯离子带一个单位的负电荷,最外层是八个电子稳定结构,故此选项正确.
故选D点评:
本题考点: 核外电子在化学反应中的作用;原子结构示意图与离子结构示意图;化学符号及其周围数字的意义.
考点点评: 此题是对元素原子相关知识的考查,解题的关键是对原子的最外层电子数与性质的关系,以及相关符号书写的掌握. - 1年前
相关推荐
- (2011•武汉模拟)一带电粒子水平射人如图所示电场中(上下极板带异种电荷),射人时的速度V0,两极板的长度为L,相距为
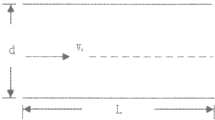 (2011•武汉模拟)一带电粒子水平射人如图所示电场中(上下极板带异种电荷),射人时的速度V0,两极板的长度为L,相距为d,两极板间电压为U,粒子带电量为q,质量为m,求带电粒子射出电场时的竖直偏移的距离y和速度方向的偏转角度∅(不计重力)
(2011•武汉模拟)一带电粒子水平射人如图所示电场中(上下极板带异种电荷),射人时的速度V0,两极板的长度为L,相距为d,两极板间电压为U,粒子带电量为q,质量为m,求带电粒子射出电场时的竖直偏移的距离y和速度方向的偏转角度∅(不计重力)  cvkasdfoiuasdpio1年前1
cvkasdfoiuasdpio1年前1 -
 dabing7216 共回答了18个问题
dabing7216 共回答了18个问题 |采纳率100%解题思路:粒子在电场中做类平抛运动,在垂直于板面方向的分运动为匀加速运动,沿电场方向做匀速运动,根据平抛运动的相关公式即可解题,结合几何关系求解.粒子在电场中做类平抛运动,垂直于板面方向上受电场力作用做匀加速运动,平行于板面的方向不受力,做匀速运动.
粒子在电场中运动的时间:t=[L
v0
粒子在电场中运动时竖直方向的加速度:a=
qU/md]
竖直方向偏移的距离:y=[1/2at2=
qUL2
2dmv02]
又:tanθ=
vy
v0,vy=at=
qUL
mdv0,
所以可得:tanθ=
qUL
mdv02
答:带电粒子射出电场时的竖直偏移的距离为
qUL2
2dmv02,粒子射出时速度偏转角的正切值为
qUL
mdv02.点评:
本题考点: 带电粒子在匀强电场中的运动;匀变速直线运动的位移与时间的关系.
考点点评: 该题考查了带电粒子在电场中偏转的问题,要知道此时粒子做类平抛运动,根据平抛运动的基本公式解题,难度不大,属于中档题.1年前查看全部
- 14.如图所示 ,平行金属板长为L,一个带电为+q,质量为m的粒子以初速度v0紧贴上板垂直射入电场,刚好从下板边缘射出,
14.如图所示 ,平行金属板长为L,一个带电为+q,质量为m的粒子以初速度v0紧贴上板垂直射入电场,刚好从下板边缘射出,末速度恰与下板成30O角,粒子重力不计.求:
(1)粒子未速度大小.
(2)电场强度.
(3)两极间距离d.
图在这里 20题 孤独里的空气1年前4
孤独里的空气1年前4 -
 becky12 共回答了17个问题
becky12 共回答了17个问题 |采纳率100%1)
初速Vo/未速度V=cos30=(根号3)/2
V=Vo/[(根号3)/2]=2Vo/(根号3)=[2(根号3)/3]Vo
2)
V沿场强方向的分量V'=Vsin60=[(根号3)/3]Vo
V'=at
t=L/Vo
V'=aL/Vo=(F/m)L/Vo=qEL/(mVo)
故 qEL/(mVo)=[(根号3)/3]Vo
电场强度为
E=[(根号3)/3]m*(Vo^2)/(qL)
3)
d=(1/2)at^2=0.5*(qE/m)*(L/Vo)^2
代入E=[(根号3)/3]m*(Vo^2)/(qL) 可求出d1年前查看全部
- 粒子在电场中的偏转公式可不可以直接用
粒子在电场中的偏转公式可不可以直接用
如Y=UQL2/2DMV2
还有X=L/2,TAN=.等,
还是要再推一遍? 中南山1年前2
中南山1年前2 -
 天狼111222 共回答了20个问题
天狼111222 共回答了20个问题 |采纳率95%一般都要重新推导一遍
因为偏转公式的推导会有附加条件 不同的条件推导出的结果是不同的
建议每次重新推导吧!
直接用的话——即使用对了,物理老师可能也会给你扣分!
再说推导也不复杂困难~1年前查看全部
- 某粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
 某粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
某粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
A.原子核内有12个质子
B.该粒子是原子
C.在化学反应中易得电子
D.该粒子属于金属元素 wypjfy1年前1
wypjfy1年前1 -
 xtf2008 共回答了11个问题
xtf2008 共回答了11个问题 |采纳率100%解题思路:因为粒子种类与粒子结构间的关系是:阳离子的核内质子数>核外电子数;阴离子的核内质子数<核外电子数;原子的核内质子数=核外电子数,所以可知该粒子为原子;金属元素的原子的最外层电子一般少于4个,在化学变化中容易失去电子,达到8电子(或2电子)稳定结构;A、从图示可以看出,该元素核内质子数为12,故说法正确;
B、该粒子核内质子数等于核外电子数,都为12,为镁原子,故说法正确;
C、该元素的原子最外层上有2个电子,在化学反应中易失去2个电子达到稳定结构,故说法错误.
D、该元素的核内存在12个质子,属于镁元素,镁元素属于金属元素,故说法正确;
故选C点评:
本题考点: 原子结构示意图与离子结构示意图.
考点点评: 本题主要考查原子结构示意图的意义、掌握核内质子数和核外电子数的关系,学会区别阳离子、阴离子、原子的微粒的电子层排布特点是解题的关键.1年前查看全部
- 下列说法正确的是( )A.1897年汤姆逊发现了原子核B.1919年卢瑟福用α粒子从氮原子核中打出了电子C.1932年
下列说法正确的是( )
A.1897年汤姆逊发现了原子核
B.1919年卢瑟福用α粒子从氮原子核中打出了电子
C.1932年查德威克发现了中子
D.1961年盖尔曼提出了层子的设想 岚惜1年前1
岚惜1年前1 -
 lusd1314 共回答了22个问题
lusd1314 共回答了22个问题 |采纳率77.3%解题思路:根据卢瑟福、汤姆逊、查德威克、盖尔曼在物理上的主要贡献进行分析.A、1879年,英国物理学家汤姆逊首先发现了电子,从而揭开了人们对原子内部的认识.故A错误;
B、1919年,卢瑟福从氮原子中打出了质子,故B错误.
C、1932年,查德威克发现了中子,故C正确;
D、1961年,盖尔曼提出质子和中子是由层子组成的设想.故D正确.
故选CD.点评:
本题考点: 人类探究微观世界的历程.
考点点评: 了解物理的发展史和重大成就,有利于激发学生学习物理的兴趣,培养社会责任感,符合新课程标准三维目标的要求.1年前查看全部
- 0.1mol/L的CH3COOH加水稀释,溶液中氢氧根粒子浓度变大.
0.1mol/L的CH3COOH加水稀释,溶液中氢氧根粒子浓度变大.
我知道正确的思路是 稀释促进水解 氢离子量变多 但浓度却因加水而变低,所以……
但我始终还有个想法 没绕过湾 觉得因为加水所以氢氧根粒子也应浓度降低 ,能不能帮我消除下误区 潇湘醉影1年前2
潇湘醉影1年前2 -
 f6bsn 共回答了19个问题
f6bsn 共回答了19个问题 |采纳率94.7%加水稀释,虽然电离总量增加,但氢离子浓度减小,氢氧根粒子浓度变大
氢氧根粒子来源于水的电离,水的电离虽氢离子浓度减小而增大,要保持平衡常数不变,浓度也要变大,因为平衡常数是以浓度计算的1年前查看全部
- 王华同学相了解和探究他生活的周围的空气质量,采用了实验“采集和测算空气中的尘埃粒子”的方法,下面是他在五处各抽测一平方厘
王华同学相了解和探究他生活的周围的空气质量,采用了实验“采集和测算空气中的尘埃粒子”的方法,下面是他在五处各抽测一平方厘米的粒子数,请根据实验结果分析回答下列问题:

(1)如图1,根据上述实验结果推测,他生活的周围的空气中每平方米所含的尘埃粒子数为______.
(2)他采用的取样方法是______.
(3)如图2,第1格中的尘埃粒子数为______.第2格中的尘埃粒子数为______. xcfmh1年前1
xcfmh1年前1 -
 wcgwcg 共回答了17个问题
wcgwcg 共回答了17个问题 |采纳率94.1%解题思路:五点取样法,是在测量范围内选取五个有代表性的点.例如首先选取教室对角线的交点,为中心点,然后从中心点到四个角连线的中点作为四个点,共五个点,观察每个点的尘埃粒子数,算出平均值,这就代表了平均尘埃粒子数.(1)通过计算,他生活的周围的空气中每平方米所含的尘埃粒子数为70000;
(2)采集的粒子太小,计数需要在显微镜下观察进行,在显微镜计数时,通常采取五点取样法进行抽样检测.五点取样法,是在测量范围内选取五个有代表性的点.例如首先选取教室对角线的交点,为中心点,然后从中心点到四个角连线的中点作为四个点,共五个点,观察每个点的尘埃粒子数,算出平均值,这就代表了生活的周围的空气质量.
(3)调查过程中有时因为调查的范围很大,就要选取一部分调查对象作为样本.对于一个种群分布较均匀具良好的代表性的调查对象,可以采用五点取样法:先确定对角线的中点作为中心抽样点,再在对角线上选择四个与中心样点距离相等的点作为样点.如果正好在边线上的遵循计上不计下,计左不计右的原则.如图2,第1格中的尘埃粒子数为3.第2格中的尘埃粒子数为2.
故答案为:(1)70000;
(2)五点取样法;
(3)3;2点评:
本题考点: 采集和测算空气中的尘埃粒子.
考点点评: 解答此类题目的关键是会测算不同环境中空气的尘埃粒子数以及探究实验的要求.1年前查看全部
- 物质是由大量______组成的;在探索微小粒子的历程中人们首先发现______.
 zhuhongliang71年前1
zhuhongliang71年前1 -
 辣之ss 共回答了24个问题
辣之ss 共回答了24个问题 |采纳率95.8%物质是由大量分子组成的;在探索微小粒子的历程中人们首先发现电子.
故答案为:分子;电子.1年前查看全部
- 下列说法中正确的是( )A.分子是化学变化中的最小粒子B.液态和气态物质分子有间隔,固态物资分子间则没有C.不同温度下
下列说法中正确的是( )
A.分子是化学变化中的最小粒子
B.液态和气态物质分子有间隔,固态物资分子间则没有
C.不同温度下的水,其水分子运动速率相同
D.水蒸发后,化学性质没有改变 vv原子核1年前1
vv原子核1年前1 -
 kirchies 共回答了20个问题
kirchies 共回答了20个问题 |采纳率95%解题思路:根据分子的定义及特征进行分析.分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;分子是保持物质化学性质的一种粒子,分子在化学变化中可以再分.A、分子在化学变化中可以再分,分子不是化学变化中的最小粒子.故A错误;
B、分子之间有间隔,液态、气态、固态物质的分子间都有有间隔,只是物质状态不同,分子的间隔不同.故B错误;
C、分子是运动的,运动的速率与温度有关,温度越高,运动的速率越快.所以,不同温度下的水,其水分子运动速率不同.故C错误;
D、水蒸发成水蒸气是物理变化,液态水的水分子和水蒸气的水分子属于同种物质的分子,化学性质相同.故D正确.
故选D.点评:
本题考点: 利用分子与原子的性质分析和解决问题.
考点点评: 水蒸发是物理变化,物理变化中分子不改变,改变的是分子之间的间隔或分子的排列方式;在化学变化中,分子才能分解成原子.1年前查看全部
- 分子是保持物质______的最小粒子;原子是______中最小粒子.分子和原子的本质区别是______.同种物质的分子性
分子是保持物质______的最小粒子;原子是______中最小粒子.分子和原子的本质区别是______.同种物质的分子性质______,不同种物质的分子性质______.
 井宝的背包1年前2
井宝的背包1年前2 -
 qzqs 共回答了19个问题
qzqs 共回答了19个问题 |采纳率89.5%解题思路:根据分子原子的定义你本质区别分析回答.分子是保持化学性质的最小微粒,同种物质的分子,性质相同,不同种物质的分子性质不同;在化学变化中,分子变为原子,原子再重新结合,原子是化学变化中最小微粒.由此可以得出,分子和原子的本质区别是在化学变化中能否再分.分子是保持物质化学性质的最小粒子;同种物质的分子,性质相同,不同种物质的分子性质不同;
原子是化学变化中最小的粒子;与分子的本质区别:在化学变化中分子能再分而原子不能再分.
故答案为:化学性质;
化学变化中;
在化学变化中,分子可分,原子不可分;
相同,不同.点评:
本题考点: 分子的定义与分子的特性;原子的定义与构成.
考点点评: 本题主要考查学生对分子、原子的含义以及区别.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- (2005•宣武区二模)下列粒子示意图中,表示+3价阳离子的是( )
(2005•宣武区二模)下列粒子示意图中,表示+3价阳离子的是( )
A.
B.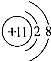
C.
D.
 世事难两全1年前1
世事难两全1年前1 -
 琉璃佛 共回答了24个问题
琉璃佛 共回答了24个问题 |采纳率95.8%解题思路:根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;+3价阳离子带有3的单位的正电荷;据此进行分析解答.+3价阳离子带有3的单位的正电荷.
A、质子数=核外电子数=10,为原子,故选项错误.
B、质子数=11,核外电子数=10,质子数>核外电子数,为阳离子;但该离子带有1个单位的正电荷,故选项错误.
C、质子数=12,核外电子数=10,质子数>核外电子数,为阳离子;但该离子带有2个单位的正电荷,故选项错误.
D、质子数=13,核外电子数=10,质子数>核外电子数,为阳离子;且该离子带有3个单位的正电荷,故选项正确.
故选D.点评:
本题考点: 原子结构示意图与离子结构示意图.
考点点评: 本题考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.1年前查看全部
- 原子中带电的粒子有?
 硬粗糙的茧1年前1
硬粗糙的茧1年前1 -
 ee数码技术 共回答了23个问题
ee数码技术 共回答了23个问题 |采纳率91.3%原子中带电的粒子有原子核内的质子 质子带正电
原子核外的电子 电子带负电1年前查看全部
- 共价键、离子键、配位键和范德华力是粒子之间的四种作用力.现有下列晶体:①Na2O2②SiO2③[Cu(NH3
共价键、离子键、配位键和范德华力是粒子之间的四种作用力.现有下列晶体:①Na2O2②SiO2③[Cu(NH3 )4]Cl2④NH4Cl ⑤NaCl ⑥AlCl3,其中含有三种作用力的是( )
A.只有①②③
B.只有①②③⑥
C.只有③④⑥
D.只有③④ 大丈夫_hh1年前1
大丈夫_hh1年前1 -
 耒姒 共回答了23个问题
耒姒 共回答了23个问题 |采纳率91.3%解题思路:一般来说,活泼金属与非金属形成离子键,非金属元素之间形成共价键,单方提供空轨道和单方提供孤对电子可形成配位键,分子之间存在分子间作用力(范德华力),以此来解答.①Na2O2存在离子键和共价键;
②SiO2中只存在共价键;
③[Cu(NH3)4]Cl2中存在氯离子与四氨合铜离子之间的离子键、N-H之间的共价键及铜离子提供空轨道和N原子孤对电子形成的配位键;
④NH4Cl中含氯离子与铵根离子之间的离子键、N-H之间的共价键及氢离子提供空轨道和N原子孤对电子形成的配位键;
⑤NaCl中只含离子键;
⑥AlCl3中含共价键、配位键和范德华力,
则含有三种作用力的是③④⑥,
故选C.点评:
本题考点: 化学键;配合物的成键情况.
考点点评: 本题考查化学键,为高频考点,把握化学键形成的一般规律为解答的关键,注意特殊物质中的化学键(铵盐、氯化铝)即可解答,氯化铝中含配位键为解答的难点,一般不涉及氯化铝中的配位键,题目难度不大.1年前查看全部
- 如图(a)所示,两平行正对的金属板A、B间加有如图(b)所示的交变电压,一重力可忽略不计的带正电粒子被固定在两板的正中间
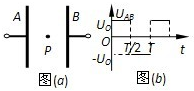 如图(a)所示,两平行正对的金属板A、B间加有如图(b)所示的交变电压,一重力可忽略不计的带正电粒子被固定在两板的正中间P处.若在[5/8T
如图(a)所示,两平行正对的金属板A、B间加有如图(b)所示的交变电压,一重力可忽略不计的带正电粒子被固定在两板的正中间P处.若在[5/8T  whooperok1年前1
whooperok1年前1 -
 johnson_zengjj 共回答了21个问题
johnson_zengjj 共回答了21个问题 |采纳率85.7%解题思路:根据带电粒子的受力,判断出加速度的大小和方向,通过加速度方向与速度方向关系结合运动学公式分析物体的运动情况.在
5
8T释放该粒子,在
5
8T~T这段时间内,正电荷所受电场力方向向左,粒子向左做匀加速直线运动,设加速度为a,T时刻的速度为v=a
3
8T,方向向左;
在T~
11
8]T内,所受的电场力方向向右,加速度方向向右,大小为a,带电粒子向左做匀减速直线运动,[11/8T时刻,速度为零;
在
11
8T~
12
8T内向右做匀加速直线运动,
12
8T时刻的速度为a
1
8T;
在
12
8T~
13
8T内,粒子向右做匀减速直线运动,
13
8]T时刻速度为零;
在整个一个周期内,粒子的位移向左,以后重复做前一个周期内的运动,所以粒子会时而向A板运动,时而向B板运动,并最终打在A板上.故A正确,B、C、D错误.
故选A.点评:
本题考点: 带电粒子在匀强电场中的运动.
考点点评: 解决本题的关键会根据物体的受力判断物体的运动,通过加速度的方向与速度方向的关系得出物体的运动规律.本题也可以通过速度时间图象进行分析.1年前查看全部
- 非相对论的量子力学 薛定谔方程里面的能量E=hv 这是非相对论的 对自由粒子就是动能?
非相对论的量子力学 薛定谔方程里面的能量E=hv 这是非相对论的 对自由粒子就是动能?
非相对论中E=hv为哈密顿量 相对论量子力学中E=hv=mc^2 怎么统一 能量都能用hv来表示吗? lzyamazaki1年前2
lzyamazaki1年前2 -
 csxiejd 共回答了16个问题
csxiejd 共回答了16个问题 |采纳率100%你说的都没错.我认为都用hv表示就行了.(我没学过高量,你最好还是参考别人的)
在自由粒子波函数上,这两种表示只是差一个相位罢了e^(im0c^2).在狄拉克归一化之后就是一样的了.1年前查看全部
- 下面是五种粒子的结构示意图,下列说法不正确的是 [
下面是五种粒子的结构示意图,下列说法不正确的是  [ ]
[ ]A.图中粒子共能表示四种元素
B.a所表示的元素位于元素周期表的第三周期
C.b、c、e都是稳定结构
D.b所表示的元素的原子易得电子 空明的灵动1年前1
空明的灵动1年前1 -
 lazystone83 共回答了32个问题
lazystone83 共回答了32个问题 |采纳率87.5%D1年前查看全部
- 下图是两种元素在元素周期表中的信息和4种粒子的结构示意图。请回答下问题: (1)C、D、E、F中,属于同种元素的是___
下图是两种元素在元素周期表中的信息和4种粒子的结构示意图。请回答下问题: 
(1)C、D、E、F中,属于同种元素的是________(填字母序号,下同),最容易得到电子的是_______。
(2)A和B形成的化合物的化学式是_________。
(3)写出一条从图A中获得的信息_____________。 apai731年前1
apai731年前1 -
 赤血盐 共回答了24个问题
赤血盐 共回答了24个问题 |采纳率91.7%(1)D、E;F
(2)MgCl 2
(3)镁原子序数为12(合理答案均可)1年前查看全部
- (2011•道里区一模)下列现象用粒子的观点解释正确的是( )
(2011•道里区一模)下列现象用粒子的观点解释正确的是( )
选项 现象 解释 A 100毫升酒精和100毫升水混合柱一起,体积小于200毫升 分子间有间隔 B 金刚石坚硬而石墨质软 构成它们的碳原子不同 C 水通电分解成氢气和氧气 分子不断的运动 D 架在高处的电线夏天变得比冬季长 分子的体积热胀冷缩
A.选项A
B.选项B
C.选项C
D.选项D guohairu1年前1
guohairu1年前1 -
 260034092 共回答了25个问题
260034092 共回答了25个问题 |采纳率92%解题思路:A、“100毫升水和100毫升酒精混合后的体积小于200毫升”,说明各种分子之间有间隔;
B、碳的单质多种,但性质不同,原因是它们的碳原子排列不同;
C、水通电后生成氢气和氧气:说明在化学变化中分子可以再分.
D、热胀冷缩:分子体积大小随温度改变而改变,这是解释错误,分子大小是不变的;A、“100毫升水和100毫升酒精混合后的体积小于200毫升”,解释因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,故A正确;
B、金刚石坚硬而石墨质地很软,是碳原子的排列不同;故B不正确;
C、水通电后生成氢气和氧气,在化学变化中水分子分成氢原子和氧原子,氢原子构成氢分子,氧原子构成氧分子,说明在化学变化中分子可以再分,分子的不断运动解释欠缺;故C不正确;
D、有关热胀冷缩的现象解释错误,分子大小是不变的,改变的是分子的间隔,故D不正确;
故选A.点评:
本题考点: 物质的微粒性.
考点点评: 掌握利用分子和原子的性质分析和解决问题的方法;熟练记忆分子和原子的性质;了解分子的定义和分子的特性.此题属基础性题型,需学生熟练掌握.1年前查看全部
- 下列有关溶液中粒子浓度的关系式正确的是( ) A.25℃时,0.1 mol•L -1 pH=4.5的NaHC 2 O
下列有关溶液中粒子浓度的关系式正确的是( ) A.25℃时,0.1 mol•L -1 pH=4.5的NaHC 2 O 4 溶液:c(HC 2 O 4 - )>c(H 2 C 2 O 4 )>c(C 2 O 4 2- ) B.向0.2 mol•L -1 NaHCO 3 溶液中加入等体积的0.1 mol•L -1 NaOH溶液:c(H + )+c(Na + )=c(OH - )+c(CO 3 2- )+-c(HCO 3 - ) C.常温下,NH 4 Cl和NH 3 •H 2 O的混合溶液[pH=7,c(C1 - )=0.l mol/L]中:c(Cl - )>c(NH 4 + )>c(OH - )=c(H + ) D.浓度均为0.1 mol•L -1 的CH 3 COONa和CH 3 COOH的混合溶液中:c(CH 3 COO - )-c(CH 3 COOH)=2[c(H + )-c(OH - )]  rr的呼吸1年前1
rr的呼吸1年前1 -
 scarlett199 共回答了19个问题
scarlett199 共回答了19个问题 |采纳率100%A.NaHC 2 O 4 溶液呈酸性说的HC 2 O 4 - 的电离程度大于水解程度,所以c(C 2 O 4 2- )>c(H 2 C 2 O 4 ),故A错误;
B.等物质的量的碳酸钠和碳酸氢钠溶液中存在电荷守恒,即c(H + )+c(Na + )=c(OH - )+2c(CO 3 2- )+c(HCO 3 - ),故B错误;
C.溶液呈中性,即c(OH - )=c(H + ),溶液中存在电荷守恒c(Cl - )+c(OH - )=c(NH 4 + )+c(H + ),所以c(Cl - )=c(NH 4 + ),故C错误;
D.根据电荷守恒得c(H + )+c(Na + )=c(CH 3 COO - )+c(OH - ),根据物料守恒得c(CH 3 COO - )+c(CH 3 COOH)=2c(Na + ),所以得c(CH 3 COO - )-c(CH 3 COOH)=2[c(H + )-c(OH - )],故D正确;
故选D.1年前查看全部
- 粒子半径:Br->K+>S2->S 还原性:Na+>S2->Br—>Cl—
粒子半径:Br->K+>S2->S 还原性:Na+>S2->Br—>Cl—
粒子半径:Br->K+>S2->S
还原性:Na+>S2->Br—>Cl—
分别应该怎么判断呢? 恨水惊秋1年前1
恨水惊秋1年前1 -
 sanjing888666 共回答了15个问题
sanjing888666 共回答了15个问题 |采纳率93.3%1.Br-在有四个电子层,Br-的半径一定最大.第一个排列有问题啊.应该是Br->S2->S>K+.排列规律是:离子或原子的结构相同的,你看右上角的数字,数字越小,半径越大.
2.这个排列也有问题啊.Na+哪来的还原性啊?规律是:非金属单质氧化性(F>O>N>Cl>Br>I>S>H>C)越强的,其阴离子的还原性就越弱.所以应该是:S2->Br->Cl->Na+1年前查看全部
- 离子 原子的有关知识不懂的地方 1.为什么说分子是保持物质化学性质的最小粒子?什么叫保持物质的化学性质?原子能不能保持物
离子 原子的有关知识不懂的地方
1.为什么说分子是保持物质化学性质的最小粒子?什么叫保持物质的化学性质?原子能不能保持物质的化学性质?
2.元素的定义是:具有相同质子数的一类原子的总称,我想问其中离子,分子是不是元素,如果离子不是元素,又为什么说元素只与质子数有关,与电子数无关?如果离子是元素,定义中的一类原子又怎么解释?
3.分子、原子、离子都是构成物质的一种基本粒子,也就是说分子原子离子都能直接构成物质,为什么说化合物是由分子或离子构成?单质是由原子或分子构成?既然离子能直接构成物质,为什么不说单质是由分子原子或离子构成? hardy8381年前6
hardy8381年前6 -
 花鼻猫 共回答了28个问题
花鼻猫 共回答了28个问题 |采纳率85.7%1、分子是保持物质化学性质的最小粒子,如果分子不变,物质的化学性质不变.如氧气变成液态氧.尽管氧气的状态发生改变,但氧分子没变,所以化学性质不变.所以说分子是保持物质化学性质的最小粒子.由原子构成的物质,当然是原子保持该物质的化学性质.如铁就是由铁原子构成的,当然铁原子保持铁的化学性质.
2、元素是具有相同质子数的一类原子的总称.
定义中的“一类”是将原子按照质子数是否相同进行归类的,与原子里的电子数、中子数都无关.如氢原子里,有的有1个中子,有的还没有中子.但他们质子数相同,所以都统称为氢元素.
,又如:Na和Na+他们的一个是原子一个带电的离子,电子数肯定不同,但他们的质子数相同,所以肯定是一种元素都是钠元素,但他们是钠元素的不同原子.元素是原子的总称,与分子无关.元素只与原子(包括带电的原子)有关.
3、分子、原子、离子都是构成物质的一种基本粒子.
离子化合物是由离子构成的.共价化合物都是由分子构成的.单质:气体都是由分子构成的,金刚石、石墨、金属、稀有气体等都是由原子构成的.离子分为阳离子、阴离子两种,它们带有相反的电荷,所以他们在一起形成的是化合物.一种离子不会形成物质的,也就不会形成单质.否则自然界的物质不就带电了吗?自然界的物质都是电中性的.1年前查看全部
- 下列物质各多少克?含粒子数多少?①100mol 水 ②0.1mol 氢氧根离子 ③2mol 钠离子
 青木原树海1年前2
青木原树海1年前2 -
 wangshisuifen 共回答了23个问题
wangshisuifen 共回答了23个问题 |采纳率91.3%①100mol 水 1800克 6.02×1025个水分子
②0.1mol 氢氧根离子 1.7克 6.02×1022个氢氧根离子
③2mol 钠离子 46克 1.204×1024个钠离子1年前查看全部
- 某元素a的粒子,原子质量为x,第一层电子数为2,第二层电子数为y.若a为阳离子时,x与y的关系,y等于多少
某元素a的粒子,原子质量为x,第一层电子数为2,第二层电子数为y.若a为阳离子时,x与y的关系,y等于多少
当a为中性原子时,x等于10+y. 法律要执行1年前3
法律要执行1年前3 -
 dreamfang 共回答了18个问题
dreamfang 共回答了18个问题 |采纳率88.9%x>10+y,具体数值有多种,不过我还是认为中性时y=6.1年前查看全部
- 一元弱酸稀释后两粒子浓度之比不变?那二元弱酸呢?
 冷静的芋头1年前1
冷静的芋头1年前1 -
 tongyh 共回答了17个问题
tongyh 共回答了17个问题 |采纳率88.2%首先一元弱酸一般是不变的
除非你无限稀释那就要考虑水电离产生的氢离子
二元单纯稀释也不变1年前查看全部
- 以氧原子为例,说明构成原子的粒子有哪几种,它们是怎样构成原子的?为什么整个原子不显电性?
 薰衣的紫1年前3
薰衣的紫1年前3 -
 天堂即望 共回答了13个问题
天堂即望 共回答了13个问题 |采纳率84.6%解题思路:根据原子是由原子核和核外电子组成,原子核由质子和中子组成(质子带正电,中子不带电),相对原子质量=质子数+中子数;在原子中,质子数=核电荷数;进行分析解答本题根据原子的构成:原子是由原子核和核外电子组成,原子核由质子和中子组成(质子带正电,中子不带电).原子核带正电,电子带负电,两者的带电量相同,一正一负,所以整个原子显示的是电中性.
故答案为:
构成原子的粒子有质子、中子和电子;
氧原子有8个质子和8个中子构成原子核,8个电子在原子核外高速运动;
原子核中8个质子带8个单位的正电荷,8个电子带8个单位的负电荷,中子不带电,质子带的电量与核外电子带的电量相等,电性相反,因此整个原子不显电性.点评:
本题考点: 原子的定义与构成;原子的有关数量计算.
考点点评: 通过回答本题知道原子的构成,原子内各量所带电荷情况,整个原子不显电性的原因.1年前查看全部
- R元素的氧化物相对分子质量 142,其中氧原子相对原子质量和 80,R原子核16粒子不带电,儿核电荷数为15 求
R元素的氧化物相对分子质量 142,其中氧原子相对原子质量和 80,R原子核16粒子不带电,儿核电荷数为15 求
2.R元素化合价 babylady111年前3
babylady111年前3 -
 贫血的蚂蚁 共回答了19个问题
贫血的蚂蚁 共回答了19个问题 |采纳率94.7%P2O5
化合价为-3,+5 ,在P2O5中显示+5价1年前查看全部
- 有A、B、C、D四种粒子,A整体不带电,原子核内只有一个质子;B带有两个单位正电荷的离子核外有两个电子层,其原子的第二层
有A、B、C、D四种粒子,A整体不带电,原子核内只有一个质子;B带有两个单位正电荷的离子核外有两个电子层,其原子的第二层电子数为第一层电子数的四倍;C带有一个负电荷的离子比B的离子多8个电子;D∧-离子具有与氩原子相同的核外电子排布.
(1)A、B、C、D的名称;
(2)A的原子中有一个中子,它的相对原子质量为______;
(3)B的相对原子质量为24,其中子数为______. kkvvcccc1年前0
kkvvcccc1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 温度高,平均动能大是动能大的粒子多,动能小的少吗?
 luoxc8881年前1
luoxc8881年前1 -
 过往的人 共回答了13个问题
过往的人 共回答了13个问题 |采纳率92.3%温度不论高低粒子动能分布都是正态分布,温度高时正态分布的峰会右移,所以平均动能比较大1年前查看全部
- (1/2)关于粒子和宇宙,下列说法正确的是()A分子是不可再分的最小粒子B用鼻子臭气味能鉴别醋和酱油,...
(1/2)关于粒子和宇宙,下列说法正确的是()A分子是不可再分的最小粒子B用鼻子臭气味能鉴别醋和酱油,...
(1/2)关于粒子和宇宙,下列说法正确的是()A分子是不可再分的最小粒子B用鼻子臭气味能鉴别醋和酱油,表明分子在运动C磁铁能吸引大头针,说明分子 20065060311年前8
20065060311年前8 -
 uuuuhao 共回答了18个问题
uuuuhao 共回答了18个问题 |采纳率77.8%B1年前查看全部
- 真空中有一匀强电场,方向沿Ox正方向,若一带电粒子质量为m.
真空中有一匀强电场,方向沿Ox正方向,若一带电粒子质量为m.
1 分钟前fly冰风谷v | 分类:| 浏览1次
真空中有一匀强电场,方向沿Ox正方向,若一带电粒子质量为m,电荷量为q从O点以初速度V0沿Oy轴正方向进入电场,经一段时间后到达A点,此时速度大小为V0,方向沿Ox正方向,如图所示,已知重力加速度为g,试求:
【1】从O点到A点的时间t及OA连线与Ox轴的夹角.
【2】该匀强电场的电场强度E.
【3】若设O点电势为0,则A点电势为? 孤独的摆摆1年前0
孤独的摆摆1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 腐殖酸包覆的Fe3O4磁性纳米粒子可以高效去除水中的重金属离子,可是这种材料能否再生循环使用?
腐殖酸包覆的Fe3O4磁性纳米粒子可以高效去除水中的重金属离子,可是这种材料能否再生循环使用?
怎么再生呢? 恭喜首版1年前2
恭喜首版1年前2 -
 jinshiyu 共回答了10个问题
jinshiyu 共回答了10个问题 |采纳率90%可以循环再生使用,但再生后肯定会产生一定数量的重金属废液,应设法妥善处理,避免二次污染.1年前查看全部
- 初中化学题:H3是什么东西?①H3,(3是脚码)是什么粒子,电子式怎么表达?②H3+ (3是脚码,+在右上角)是什么粒子
初中化学题:H3是什么东西?
①H3,(3是脚码)是什么粒子,电子式怎么表达?
②H3+ (3是脚码,+在右上角)是什么粒子?电子式怎么表达?
请附上图,谢谢. shine03251年前2
shine03251年前2 -
 无尾树熊 共回答了15个问题
无尾树熊 共回答了15个问题 |采纳率93.3%H3是在2008年之前找到的新分子 存在于宇宙中 是通过宇宙望远镜观测到的光谱分析得到的
具体的结构为 氢原子1s轨道上的电子受激发 跃迁到2p轨道上(很高的能量 所以极不稳定)三个激发原子 互相共用电子 形成π-3-3共轭大π键(键不稳定 所以不稳定)
H3+是典型的三中心二电子键的代表 和H3的结构不同 在氢分子的电子云中嵌入一个质子 电子则变为在三个中心的电场中运动 具体键型我也不知道 反正那个不是单纯的σ键1年前查看全部
- 粒子代入公式带不带正负符号计算库仑力的时候Q是不把正负符号代进去的,那么洛伦滋力和安培力的Q代不代正负符号进去计算呢?
 21天ss中1年前1
21天ss中1年前1 -
 安徒生妹妹 共回答了20个问题
安徒生妹妹 共回答了20个问题 |采纳率100%洛伦滋力 F=Bqv
安培力 F=Blv
不带正负号,若要判断力的方向,要根据左手定则1年前查看全部
- 粒子在电场中运动都会受到静电力和电场力的作用吗
粒子在电场中运动都会受到静电力和电场力的作用吗
静电力是不是只有存在两个带电粒子的时候才会存在 如夏风筝1年前1
如夏风筝1年前1 -
 癫之颠 共回答了17个问题
癫之颠 共回答了17个问题 |采纳率82.4%带电粒子在电场中受力为电场力,两个带电粒子之间的相互作用力为静电力,但是电场力就是静电力1年前查看全部
- 如何计算粒子对撞后产生的能量比如说 2H+3H-----4He+n+17.6Mev这个17.6Mev是怎样算出的
 wtxi9991年前1
wtxi9991年前1 -
 kk骷髅XP 共回答了18个问题
kk骷髅XP 共回答了18个问题 |采纳率88.9%E=m1c2-m2c21年前查看全部
- 磁场中带电粒子受到的磁场力是什么力
 孤狐莹1年前3
孤狐莹1年前3 -
 snow2099 共回答了17个问题
snow2099 共回答了17个问题 |采纳率88.2%1.如果带电粒子参考磁场是做切割磁感线运动,则带电粒子受到的是洛伦兹力和重力的叠加,重力较小,可以忽略不计.合力方向,大小,均和磁场磁感线方向,带电粒子所带电荷极性有关,运动电荷在磁场受力叫洛伦兹力.f=qvbcosα ;如果带电粒子运动方向与磁感线平行,则带电粒子只受到重力.
2.如果带电粒子参考磁场是处于静止状态,带电粒子受到的是重力.1年前查看全部
- 卢瑟福实验中,a粒子难道不会撞到电子吗?撞到了又会怎样?
卢瑟福实验中,a粒子难道不会撞到电子吗?撞到了又会怎样?
氦原子核外有2个电子,你能建立一个氦原子的模型吗?
怎么画? aiilion1年前2
aiilion1年前2 -
 清桑 共回答了14个问题
清桑 共回答了14个问题 |采纳率85.7%当然会撞到,但是由于电子的质量仅是a粒子的2000分之一,完全无法影响其运动轨迹和方向.a粒子仅是在撞到原子核时运动方向才会发生改变.1年前查看全部
- 溶液中 离子浓度 排序碳酸钠 碳酸氢钠 溶液中的各离子浓度大小排序是什么?是粒子浓度,thanks
 恋土_love20061年前3
恋土_love20061年前3 -
 蓪仔 共回答了13个问题
蓪仔 共回答了13个问题 |采纳率100%碳酸钠 [Na+]>[co32-]>[OH-]>[HCO3-]>[H2CO3]
碳酸氢钠 [Na+]>[HCO3-]>[OH-]>[H2CO3]>[H+]>[CO32-]1年前查看全部
- 分子,原子,粒子,质子,量子...还有什么"...子"?并按体积从大到小的顺序排列.
 龙城小一1年前2
龙城小一1年前2 -
 byebyebirdie 共回答了11个问题
byebyebirdie 共回答了11个问题 |采纳率100%分子是由两个或多个原子构成;原子含有原子核,核内有质子与中子,质子带正电位,中子不带电,中子与质子大小相同,中子与质子数目相等或略有差异,核外有电子围绕原子核做不规则圆周运动的微粒,带负电位,数目与质子数相等.
离子:当一个原子得到或失去电子时称为离子,得到电子的原子称为负离子,失去电子的为正离子.
量子:在微观领域中,某些物理量的变化是以最小的单位跳跃式进行的,而不是连续的,这个最小的单位叫做量子 也是对对原子、电子、光子等物质基本单元的统称.
分子、原子、质子、中子、电子、量子、离子都是粒子.
排序:分子>原子>负离子>正离子>质子=中子>电子1年前查看全部
- 胶体(电荷)---沉聚?已知土壤胶体粒子带负电荷,使用含氮量相等的下列氮肥,当中肥效最差的是( )A.(NH4)2SO4
胶体(电荷)---沉聚?
已知土壤胶体粒子带负电荷,使用含氮量相等的下列氮肥,当中肥效最差的是( )
A.(NH4)2SO4 B.NH4NO3 C.NH4Cl DNH4HCO3 guolubberland1年前2
guolubberland1年前2 -
 of5lzo 共回答了19个问题
of5lzo 共回答了19个问题 |采纳率94.7%肥效流失是指胶体聚沉,土壤胶体带负电荷,所以化肥中氮带正电荷的就会聚沉,降低肥效,求出选项中氮的正负电荷即可.1年前查看全部
- 各种粒子与质子的关系例如,氚核的质量是质子的三倍,电荷量为一个元电荷.a粒子即氦原子核,质量约为质子的四倍,带正电荷,电
各种粒子与质子的关系
例如,氚核的质量是质子的三倍,电荷量为一个元电荷.a粒子即氦原子核,质量约为质子的四倍,带正电荷,电荷量是元电荷的两倍.那么氕,氘,氚,电子,氢核的类似关系是什么呢? fdgsht1年前1
fdgsht1年前1 -
 xujiake 共回答了17个问题
xujiake 共回答了17个问题 |采纳率94.1%氕核就是质子,带一个元电荷;
氘核是由一个质子加一个中子组成,由于只含有一个质子,而中子又是不带电的,所以氘核也是带一个元电荷;
氚核是由一个质子加两个中子组成,带一个元电荷,氚核具有贝塔衰变性.1年前查看全部
- 汤姆生发现原子中存在带负电的粒子,该粒子称为( )
汤姆生发现原子中存在带负电的粒子,该粒子称为( )
A. 电子
B. 质子
C. 中子
D. 核子 茉美眉1年前1
茉美眉1年前1 -
 如风走过 共回答了20个问题
如风走过 共回答了20个问题 |采纳率85%解题思路:原子由位于中心的原子核和核外电子组成.其中,原子核带正电,电子带负电.汤姆生发现了原子中存在一种带负电荷的粒子,这种粒子就是电子.
故选A.点评:
本题考点: 原子结构、元电荷与带电情况.
考点点评: 本题考查了发现电子的历史,是一道基础题.1年前查看全部
- 判断粒子是不是做正功根据带电粒子的正负情况,电场线的方向,从而得出带电粒子受到的电场力方向,若运动轨迹与电场力方向相同,
判断粒子是不是做正功
根据带电粒子的正负情况,电场线的方向,从而得出带电粒子受到的电场力方向,若运动轨迹与电场力方向相同,就作正功,方向不同,作负功.粒子带正电的情况下,顺着箭头走,电场就做正功,逆方向就负功,带负电的就相反(也就是说顺着箭头走电场做负功对吧?那不正好与上一句矛盾?). pgnwm1年前2
pgnwm1年前2 -
 bestpingan 共回答了19个问题
bestpingan 共回答了19个问题 |采纳率94.7%带电粒子受到的电场力方向,若运动轨迹与电场力方向相同,就作正功,方向不同,作负功.粒子带正电的情况下,顺着箭头走,电场就做正功,逆方向就负功,带负电的就相反((也就是说顺着箭头走电场做负功 .这时电场力是逆着箭头的.也就是轨迹与电场力方向相反.那正好与上一句不矛盾1年前查看全部
- 铁和盐酸反应后溶液中主要含有什么粒子
 cupid3181年前6
cupid3181年前6 -
 雨吼 共回答了14个问题
雨吼 共回答了14个问题 |采纳率100%主要有Fe2+ H+ CL- 还有一些OH- Fe3+1年前查看全部
- 氘核和α粒子,从静止开始经相同电场加速后,垂直进入同一匀强磁场作圆周运动.则这两个粒子的动能之比为?
 tdm9977121年前2
tdm9977121年前2 -
 witerman 共回答了20个问题
witerman 共回答了20个问题 |采纳率80%氘核由一个质子和一个中子组成,α粒子由两个质子和两个中子组成.
所以:质量比为 1:2 电荷量比 1:2
从静止开始经相同电场加速后,粒子获得的动能就等于静电力做的功
Ek=qU
所以加速后 两粒子动能之比等于电荷量之比 为1:2
垂直进入同一匀强磁场作圆周运动,洛伦兹力不做功,粒子做匀速圆周运动,动能是不变的.
这两个粒子的动能之比还是1:21年前查看全部
- 我们知道电流的方向是闭合回路中电子受到电场作用而定向移动的反方向,那在这个“反方向”上有没有带正电的粒子定向移动呢?
 aiwobieshangwo1年前2
aiwobieshangwo1年前2 -
 波波bo 共回答了26个问题
波波bo 共回答了26个问题 |采纳率88.5%闭合电路通常是金属导体的,没有带正电的粒子移动;电镀等利用电解液导电的有带正电的粒子(正离子)移动.1年前查看全部
- 带电量为q的粒子以一定的v垂直进入匀强磁场,形成环形电流,当v增大,环形电流的大小为什么不变
 ngpowerse1年前1
ngpowerse1年前1 -
 不得不这样说 共回答了18个问题
不得不这样说 共回答了18个问题 |采纳率77.8%利用电流的定义式 i=q/t
本题中 求这个周期内的情况
速度变大后,周期没有发生变化 电流大小不变1年前查看全部
大家在问
- 1急求雅思water pollution 和 land pollution的大作文 3Q
- 2岁寒,然后知松柏之后凋也 告诉我们什么道理
- 3怎么样利用化学方程式做简单运算?
- 4英语阅读测试When children learn a language,they learn the grammar
- 5鉴别CCl4和蒸馏水分别只用一种试剂;不用任何试剂.
- 6含有乐字的成语写四个
- 7欧阳修上疏说:“京城近有雕印文集二十卷,名为《宋文》者,多是当今议论时政之言‘……详其语言,不可流布,而雕印之人,不知事
- 8我现在有点担心翻译成英语
- 9两道英语选择题Do you know who your teacher would like to have ___ p
- 10英语翻译其义自见的“见”1令洁净端正的“端正”2须整顿几案的“整顿”3却只浪漫诵读的“浪漫”4“详缓看字,字细分明读之”
- 11静摩擦力与什么因素有关,“静摩擦力除了最大值外,与压力无关”这句话对不对?
- 12实变函数里刚讲到勒贝格积分时,提到一个特征函数,f(x)=求和(ci*Xei(x))那个Xei(x)说是特征函数,那特征
- 13生物界千姿百态,生 物种类极其繁多,个体差异很大.除______外,绝大多数生物体结构和功能的基本单位是______.
- 14修改病句。通过老师的教育,同学们改掉了不吃零食的坏习惯。
- 15下列说法正确的是( )A. 数据3,4,4,7,3的众数是4B. 数据0,1,2,5,a的中位数是2C. 一组数据的众
