亚硫酸氢铵和过量氢氧化钠反应方程式和离子方程式
 dirfj2022-10-04 11:39:541条回答
dirfj2022-10-04 11:39:541条回答2OH- + NH4+ + HSO3 - = 2H2O + NH3 + SO32-
还是
2OH- + NH4+ + HSO3 - = H2O + NH3.H2O + SO32-

已提交,审核后显示!提交回复
共1条回复
 foxlu1013 共回答了15个问题
foxlu1013 共回答了15个问题 |采纳率86.7%- 这个问题很纠结.
一般说要共热才产生氨气的.
但是一般考试又不会考生成物有氨水的方程式
应该两个都对.但是应对高考建议写第一个. - 1年前
相关推荐
- 这个离子方程式错在哪了?在溶液中亚硫酸氢铵与等物质的量的氢氧化钠混合 NH4+ + HSO3- +2OH- =SO3 2
这个离子方程式错在哪了?
在溶液中亚硫酸氢铵与等物质的量的氢氧化钠混合 NH4+ + HSO3- +2OH- =SO3 2- + NH3↑ + 2H2O
哪里错了? 葬誮1年前1
葬誮1年前1 -
 天子村 共回答了15个问题
天子村 共回答了15个问题 |采纳率93.3%电荷守恒
HSO3-不能制SO3 2-
这个式子不符合客观现实1年前查看全部
- 问几个离子方程式 二氧化碳通入少量硅酸钠溶液 亚硫酸氢铵溶液中滴加少量氢氧化钠二氧化硫通入亚硫酸钠溶液中 亚硫酸氢铵溶液
问几个离子方程式
二氧化碳通入少量硅酸钠溶液 亚硫酸氢铵溶液中滴加少量氢氧化钠
二氧化硫通入亚硫酸钠溶液中 亚硫酸氢铵溶液中滴加足量氢氧化钠
少量二氧化碳通入碳酸钠溶液
足量二氧化硫通入碳酸钠溶液中
硫酸氢钠溶液中滴加碳酸氢钠
碳酸氢钠溶液中滴加少量氢氧化钙
碳酸氢钠溶液中滴加足量氢氧化钙
硫酸氢钠溶液中滴加少量碳酸氢钡溶液
硫酸氢钠溶液中滴加足量碳酸氢钡溶液
写掉了一个:少量二氧化硫通入碳酸钠溶液 芳251年前2
芳251年前2 -
 mao5650 共回答了12个问题
mao5650 共回答了12个问题 |采纳率100%CO2+SiO32-+H2O=H2SiO3↓+CO32-
SO2+SO32-+H2O=2HSO3-
CO2+CO32-+H20=2HCO3-
2SO2+H2O+CO32-=2HSO3-+CO2
HCO3-+H+=H2O+CO2↑
Ca2++OH2-+2HCO3-=2H2O+CO32-+CaCO3↓
Ca2++OH-+HCO3-=H2O+CaCO3↓
2HSO4-+Ba2++2HCO3-=BaSO4↓+SO42-+2H2O+2CO2↑
HSO4-+Ba2++HCO3-=BaSO4↓+H2O+HCO3-+CO2↑
NH4++HSO3-+OH-=HSO3-+NH3↑+H2O
NH4++HSO3-+2OH-=SO32-+NH3↑+2H2O1年前查看全部
- 求化学的电离方程式H2OHCLOCU(OH)2硝酸铵氯化铝磷酸氢氧化钙KH2SO4亚硫酸氢铵碳酸氢钡
 刺老芽1年前4
刺老芽1年前4 -
 云儿2008 共回答了13个问题
云儿2008 共回答了13个问题 |采纳率76.9%1.H2O=H++OH-
2.次氯酸是弱酸,一般不写电离方程式,一定要写可以写成
HClO=H++ClO-
3.Cu(OH)2=Cu2++2OH-
4.NH4NO3=NH4++NO3-
5.AlCl3=Al3++3Cl-
6.H3PO4=H++H2PO4-
H2PO4-=H++HPO42-
HPO42-=H++PO43-
7.Ca(OH)2=Ca2++2OH-
8.KH2SO4化学式错误
KHSO4=K++HSO4-
HSO4-=H++SO42-
9.NH4HSO3=NH4++HSO3-
HSO3-=H++SO32-
10.Ba(HCO3)2=Ba2++2HCO3-
HCO3-=H++CO32-1年前查看全部
- 亚硫酸铵与二氧化硫反应生成亚硫酸氢铵化学方程式
 youfar1年前1
youfar1年前1 -
 大大uu 共回答了16个问题
大大uu 共回答了16个问题 |采纳率87.5%(NH4)2SO3 +SO2+H2O=2NH4HSO31年前查看全部
- 为了节能减排,提高综合经济效益,某工厂采用焦炉气--含硫烟道气联合生产硫酸铵和亚硫酸氢铵两种产品,其工艺流程图如下:
为了节能减排,提高综合经济效益,某工厂采用焦炉气--含硫烟道气联合生产硫酸铵和亚硫酸氢铵两种产品,其工艺流程图如下:
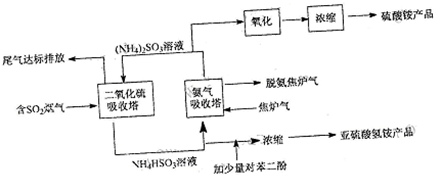
(1)下列有关说法正确的是______.
a.含SO2烟气直接排放易引起酸雨
b.焦炉气若用河水洗涤后直接排放,易引起水体的富营养化
c.脱氨焦炉气可作燃料发电
d.检验硫酸铵产品中是否混有较多的亚硫酸铵杂质,可用溴水作试剂
(2)生产亚硫酸氢铵时,加入少量对苯二酚的作用是______.
(3)氨气吸收塔中发生反应的离子方程式为:______.
(4)已知烟气含SO22%,焦炉气中含NH34.8%,若只生产硫酸铵一种产品,吸收后的尾气中所含的SO2或NH3可忽略.则含SO2烟气与焦炉气的流量(每分钟流过的体积)比为______. yu2003321年前1
yu2003321年前1 -
 zmp13807679760 共回答了19个问题
zmp13807679760 共回答了19个问题 |采纳率94.7%解题思路:(1)a.SO2是引起酸雨的主要气体;
b.含氮物质易引起水体的富营养化;
c.脱氨焦炉气含有甲烷、CO等可燃性气体,可作燃料发电;
d.亚硫酸铵具有还原性,可与溴水发生氧化还原反应;
(2)生产亚硫酸氢铵时,为防止亚硫酸铵氧化,应加入还原剂;
(3)氨气吸收塔中发生的反应为氨水和亚硫酸铵的反应;
(4)根据质量守恒计算,即需要的NH3与SO2的物质的之比理论上应为2:1.(1)a.SO2是引起酸雨的主要气体,故a正确;
b.焦炉气中含有氨气,易引起水体的富营养化,故b正确;
c.脱氨焦炉气含有甲烷、CO等可燃性气体,可作燃料发电,故c正确;
d.亚硫酸铵具有还原性,可与溴水发生氧化还原反应,故d正确;
故答案为:abcd;
(2)生产亚硫酸氢铵时,为防止亚硫酸铵氧化,应加入还原剂,则生产亚硫酸氢铵时,为防止亚硫酸铵氧化,应加入还原剂,
故答案为:对苯二酚作还原荆,保证亚硫酸氧铵不被氧化;
(3)氨气吸收塔中发生的反应为氨水和亚硫酸铵的反应,反应的方程式为HSO3-+NH3•H2O=SO32-+NH4-+H2O,
故答案为:HSO3-+NH3•H2O=SO32-+NH4-+H2O;
(4)需要的NH3与SO2的物质的之比理论上应为2:1,设含SO2烟气与焦炉气的体积分别为x、y,
则有2%x:4.8%y=1:2,x:y=1.2:1,
故答案为:1.2:1.点评:
本题考点: 制备实验方案的设计;含硫物质的性质及综合应用.
考点点评: 本题考查尾气的处理和实验流程问题,题目难度不大,本题注意把握物质的性质,解答本题一定要认真读题,加强自学能力的培养.1年前查看全部
- 几个化学方程式的书写.通直流电的情况下,二氧化硫与水反应生成硫酸根和氢离子的化学方程式.亚硫酸氢铵[NH4HSO3]与二
几个化学方程式的书写.
通直流电的情况下,二氧化硫与水反应生成硫酸根和氢离子的化学方程式.
亚硫酸氢铵[NH4HSO3]与二氧化氮反应生成氮气和铵盐的化学方程式.
 镜中人19811年前1
镜中人19811年前1 -
 赌坊148号 共回答了22个问题
赌坊148号 共回答了22个问题 |采纳率86.4%so2+H2O+O2=H2SO4 H2SO4=2H+ +SO42-
4NH4HSO3+2NO2==N2+2(NH4)2SO4+2H2SO4 有时间我们可以交流哦1年前查看全部
- 亚硫酸氢铵与稀硫酸化学方程式
 北纬36度41年前5
北纬36度41年前5 -
 有钱的vv 共回答了19个问题
有钱的vv 共回答了19个问题 |采纳率89.5%2NH4HSO3 H2SO4=(NH4)2SO4 2SO2↑ 2H2O1年前查看全部
- 亚硫酸氢铵溶液与足量氢氧化钠溶液混合加热 的化学方程式.
 路向何方41年前1
路向何方41年前1 -
 luting1210 共回答了19个问题
luting1210 共回答了19个问题 |采纳率84.2%亚硫酸氢铵溶液与足量氢氧化钠溶液混合加热 的化学方程式
NH4HSO3 +2 NaOH = 加热= Na2SO3 +NH3 (气体箭头) +2H2O
NH4+ HSO3- 都与OH- 反应!1年前查看全部
- 二氧化硫如何一步生成亚硫酸氢铵?
 lee45131年前1
lee45131年前1 -
 xiemyy7 共回答了26个问题
xiemyy7 共回答了26个问题 |采纳率88.5%将过量的SO2通入氨水中,就能得到NH4HSO3
化学方程式:SO2 + NH3.H2O =NH4HSO31年前查看全部
- 为什么亚硫酸铵和少量硫酸反应生成亚硫酸氢铵
为什么亚硫酸铵和少量硫酸反应生成亚硫酸氢铵
2.为什么硫酸氢钠在水中电离出氢离子和硫酸根离子 在熔融状态下电离出硫酸氢根离子?
3.微容物作产物时打不打沉淀符号? 阿里乐乐1年前4
阿里乐乐1年前4 -
 Leox2000 共回答了21个问题
Leox2000 共回答了21个问题 |采纳率90.5%1、严格说是亚硫酸氢铵和硫酸铵,因为亚硫酸根结合氢离子能力比硫酸大的多,可以看成强酸制弱酸.亚硫酸和硫酸是不会发生氧化还原反应的,因为没有中间价态.
2、硫酸氢根和硫酸一样,是由共价键形成的,所以在熔融状态下不电离.硫酸氢根在水中受水分子的作用而电离出氢离子,常温下电离度约30%.
3、要根据题目中的意思,题目说是沉淀就要写,尤其是推断题.1年前查看全部
- (2012•浦东新区二模)向亚硫酸氢铵溶液中逐滴加入一定量NaOH溶液,以下为实验过程中发生反应的离子方程式,其中错误的
(2012•浦东新区二模)向亚硫酸氢铵溶液中逐滴加入一定量NaOH溶液,以下为实验过程中发生反应的离子方程式,其中错误的是( )
A.NH4++2HSO3-+3OH-→NH3•H2O+2SO32-+2H2O
B.NH4++HSO3-+2OH-→NH3•H2O+SO32-+H2O
C.2NH4++HSO3-+3OH-→2NH3•H2O+SO32-+H2O
D.2NH4++5HSO3-+7OH-→2NH3•H2O+5SO32-+5H2O qijisann1年前1
qijisann1年前1 -
 zaj9088 共回答了25个问题
zaj9088 共回答了25个问题 |采纳率92%解题思路:向亚硫酸氢铵溶液中逐滴加入一定量NaOH溶液,首先发生反应OH-+HSO3-=SO32-+H2O,HSO3-反应完毕,剩余的OH-再与NH4+发生反应NH4++OH-=NH3•H2O,亚硫酸氢铵溶液中n(NH4+)=n(HSO3-)(不考虑水解),故离子方程式中HSO3-的系数大于或等于NH4+的系数,结合选项判断.向亚硫酸氢铵溶液中逐滴加入一定量NaOH溶液,首先发生反应OH-+HSO3-=SO32-+H2O,HSO3-反应完毕,剩余的OH-再与NH4+发生反应NH4++OH-=NH3•H2O,亚硫酸氢铵溶液中n(NH4+)=n(HSO3-)(不考虑水解),故离子方程式中HSO3-的系数大于或等于NH4+的系数,
A、NH4++2HSO3-+3OH-=NH3•H2O+2SO32-+2H2O中发生反应2OH-+2HSO3-=2SO32-+2H2O、NH4++OH-=NH3•H2O,亚硫酸氢铵与氢氧化钠物质的量之比为2:3,铵根离子未完全反应,符合反应,故A正确;
B、NH4++HSO3-+2OH-=NH3•H2O+SO32-+H2O中发生反应OH-+HSO3-=SO32-+H2O、NH4++OH-=NH3•H2O,亚硫酸氢铵与氢氧化钠物质的量之比为1:2,二者恰好完全反应,故B正确;
C、2NH4++HSO3-+3OH-=2NH3•H2O+SO32-+H2O表示首先发生反应NH4++OH-=NH3•H2O,故C错误;
D、2NH4++5HSO3-+7OH-=2NH3•H2O+5SO32-+5H2O中发生反应5OH-+5HSO3-=5SO32-+5H2O、2NH4++2OH-=2NH3•H2O,亚硫酸氢铵与氢氧化钠物质的量之比为5:7,铵根离子未完全反应,符合反应,故D正确;
故选C.点评:
本题考点: 离子方程式的书写.
考点点评: 本题考查离子方程式的书写与判断,难度中等,确定离子反应的先后顺序是关键.1年前查看全部
- 求:亚硫酸氢铵和足量NaOH溶液反应的离子方程式
求:亚硫酸氢铵和足量NaOH溶液反应的离子方程式
RT zww02171年前2
zww02171年前2 -
 staranne 共回答了23个问题
staranne 共回答了23个问题 |采纳率87%离子方程式:
NH4+ + HSO3- + 2OH- == NH3.H2O + SO3^2- + H2O1年前查看全部
- 向亚硫酸氢铵溶液中逐滴加入一定量NaOH溶液,以下为实验过程中发生反应的离子方程式,其中错误的是( ) A.NH 4
向亚硫酸氢铵溶液中逐滴加入一定量NaOH溶液,以下为实验过程中发生反应的离子方程式,其中错误的是( ) A.NH 4 + +2HSO 3 - +3OH - →NH 3 •H 2 O+2SO 3 2- +2H 2 O B.NH 4 + +HSO 3 - +2OH - →NH 3 •H 2 O+SO 3 2- +H 2 O C.2NH 4 + +HSO 3 - +3OH - →2NH 3 •H 2 O+SO 3 2- +H 2 O D.2NH 4 + +5HSO 3 - +7OH - →2NH 3 •H 2 O+5SO 3 2- +5H 2 O  光明和黑夜1年前1
光明和黑夜1年前1 -
 h6769 共回答了22个问题
h6769 共回答了22个问题 |采纳率95.5%向亚硫酸氢铵溶液中逐滴加入一定量NaOH溶液,首先发生反应OH - +HSO 3 - =SO 3 2- +H 2 O,HSO 3 - 反应完毕,剩余的OH - 再与NH 4 + 发生反应NH 4 + +OH - =NH 3 •H 2 O,亚硫酸氢铵溶液中n(NH 4 + )=n(HSO 3 - )(不考虑水解),故离子方程式中HSO 3 - 的系数大于或等于NH 4 + 的系数,
A、NH 4 + +2HSO 3 - +3OH - =NH 3 •H 2 O+2SO 3 2- +2H 2 O中发生反应2OH - +2HSO 3 - =2SO 3 2- +2H 2 O、NH 4 + +OH - =NH 3 •H 2 O,亚硫酸氢铵与氢氧化钠物质的量之比为2:3,铵根离子未完全反应,符合反应,故A正确;
B、NH 4 + +HSO 3 - +2OH - =NH 3 •H 2 O+SO 3 2- +H 2 O中发生反应OH - +HSO 3 - =SO 3 2- +H 2 O、NH 4 + +OH - =NH 3 •H 2 O,亚硫酸氢铵与氢氧化钠物质的量之比为1:2,二者恰好完全反应,故B正确;
C、2NH 4 + +HSO 3 - +3OH - =2NH 3 •H 2 O+SO 3 2- +H 2 O表示首先发生反应NH 4 + +OH - =NH 3 •H 2 O,故C错误;
D、2NH 4 + +5HSO 3 - +7OH - =2NH 3 •H 2 O+5SO 3 2- +5H 2 O中发生反应5OH - +5HSO 3 - =5SO 3 2- +5H 2 O、2NH 4 + +2OH - =2NH 3 •H 2 O,亚硫酸氢铵与氢氧化钠物质的量之比为5:7,铵根离子未完全反应,符合反应,故D正确;
故选C.1年前查看全部
- 将氢氧化钠固体加入热的浓亚硫酸氢铵溶液中:NH4+OH-=NH3+H2O为什么不对
 呆呆的笨笨1年前1
呆呆的笨笨1年前1 -
 great_han 共回答了26个问题
great_han 共回答了26个问题 |采纳率88.5%NH4HSO3 + 2NaOH== Na2SO3 +2H2O+NH3
有两个关系:铵根与氢氧化钠产生氨气和水;氢和氢氧根生成水.1年前查看全部
- 在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合的离子方程式
 VR米1年前2
VR米1年前2 -
 yy匿了 共回答了18个问题
yy匿了 共回答了18个问题 |采纳率83.3%因为是等物质的量所以都是amol的H+ NH4+ OH-,H+优先与强碱OH-反应所以
H+ + OH- =H2O1年前查看全部
- 在亚硫酸氢铵稀溶液中加入足量和少量的氢氧化钠稀溶液的两个化学方程式
 mickey63121年前2
mickey63121年前2 -
 我爱田园MM 共回答了24个问题
我爱田园MM 共回答了24个问题 |采纳率79.2%(1)NaOH过量:
NH4HSO3 + 2NaOH == Na2SO3 + NH3 + 2H2O ---加热!
NH4HSO3 + 2NaOH == Na2SO3 + NH3.H2O + H2O ---不加热!
(2)NaOH不足:
2NH4HSO3 + 2NaOH == Na2SO3 + (NH4)2SO3 + 2H2O1年前查看全部
- 下列离子方程式中正确的是 A.氢氧化钠溶液吸收过量的二氧化碳 OH - +CO 2 = HCO 3 - B.亚硫酸氢铵溶
下列离子方程式中正确的是
A.氢氧化钠溶液吸收过量的二氧化碳 OH - +CO 2 = HCO 3 - B.亚硫酸氢铵溶液与足量氢氧化钠溶液反应 HSO 3 - + OH - = SO 3 2 - + H 2 O C.氯气通入冷水中 Cl 2 +H 2 O = Cl - +ClO - +2H + D.碳酸镁悬浊液中加醋酸 CO 3 2 - +2CH 3 COOH = 2CH 3 COO - +CO 2 ↑+H 2 O  witch_zhou1年前1
witch_zhou1年前1 -
 stock_beginner 共回答了20个问题
stock_beginner 共回答了20个问题 |采纳率85%A 试题解析:A、氢氧化钠溶液吸收过量的二氧化碳生成HCO 3 - ,正确;B、当氢氧化钠溶液足量时NH 4 + 与氢氧化钠反应产生氨气,B选项漏掉了离子反应,错误;C、氯气与水反应生成的次氯酸为弱酸不可...1年前查看全部
- 亚硫酸氢铵如何变成亚硫酸铵
 3647808351年前1
3647808351年前1 -
 linushe 共回答了13个问题
linushe 共回答了13个问题 |采纳率92.3%加一些氨水
NH4HSO4+NH3·H2O=(NH4)2SO4+H2O1年前查看全部
- 亚硫酸氢铵与足量氢氧化钠的化学反应方程式是?离子反应方程呢?
 papa6301年前1
papa6301年前1 -
 yxldyl 共回答了23个问题
yxldyl 共回答了23个问题 |采纳率100%一个亚硫酸铵加两个氢氧化钠生成一个亚硫酸钠和两个氨气,两个水! 离子方程式拆开就行了
铵根离子加氢氧根离子得水和氨气(全部都是一个),别忘记气体符号!1年前查看全部
- 亚硫酸氢铵与氢氧化钡反应方程式 亚硫酸铵与氢氧化钡反应方程式 亚硫酸氢铵与硫酸反应方程式
亚硫酸氢铵与氢氧化钡反应方程式 亚硫酸铵与氢氧化钡反应方程式 亚硫酸氢铵与硫酸反应方程式
亚硫酸铵与硫酸反应方程式 渴望你的保护1年前2
渴望你的保护1年前2 -
 packyzhen 共回答了12个问题
packyzhen 共回答了12个问题 |采纳率91.7%亚硫酸氢铵与氢氧化钡反应方程式:Ba(OH)2+2NH4HSO3=BaSO3↓+4H2O+2NH3↑
亚硫酸铵与氢氧化钡反应方程式:Ba(OH)2+(NH4)2SO3=BaSO3↓+2H2O+2NH3↑
亚硫酸氢铵与硫酸反应方程式:2NH4HSO3+ H2SO4=(NH4)2SO4+2H2O+SO2↑
亚硫酸铵与硫酸反应方程式:(NH4)2SO3+ H2SO4=(NH4)2SO4+H2O+SO2↑1年前查看全部
- 亚硫酸氢铵 亚硫酸铵 反应式为?
 gzhill1年前2
gzhill1年前2 -
 无用鬼 共回答了13个问题
无用鬼 共回答了13个问题 |采纳率92.3%(NH4)2SO3-----NH3+SO2+H2O
亚硫酸氢铵产物也一样,没配平,自己配1年前查看全部
- 亚硫酸氢铵溶液中递加碳酸氢钡溶液
 lovejisub1年前2
lovejisub1年前2 -
 丑丑爱美丽 共回答了24个问题
丑丑爱美丽 共回答了24个问题 |采纳率95.8%4NHSO3+BaHCO3==BaSO4+H2O+CO2+2N21年前查看全部
- 硫酸氢铵和亚硫酸氢铵反应的离子方程式.
 jkhypopo1年前2
jkhypopo1年前2 -
 puphy 共回答了16个问题
puphy 共回答了16个问题 |采纳率87.5%H++HSO3-=H2O+SO21年前查看全部
- 亚硫酸氢铵溶液与等物质的量的烧碱溶液的反应离子方程式是什么?
亚硫酸氢铵溶液与等物质的量的烧碱溶液的反应离子方程式是什么?
如题. xstar19751年前1
xstar19751年前1 -
 zmzm爻 共回答了21个问题
zmzm爻 共回答了21个问题 |采纳率90.5%HSO3 ̄+OH ̄===H2O+SO3(2-)1年前查看全部
- 亚硫酸铵和亚硫酸氢铵化学式
 别总说我帅1年前1
别总说我帅1年前1 -
 风中桃花 共回答了14个问题
风中桃花 共回答了14个问题 |采纳率78.6%亚硫酸铵(NH4)2SO3
亚硫酸氢铵NH4HSO31年前查看全部
- 亚硫酸氢铵和等量氢氧化钠反应方程式和离子方程式
亚硫酸氢铵和等量氢氧化钠反应方程式和离子方程式
是在溶液中的 草莓味的棉花糖1年前5
草莓味的棉花糖1年前5 -
 june3622 共回答了8个问题
june3622 共回答了8个问题 |采纳率62.5%2NH4+ + HSO3- + OH- =(SO3)2- +2NH3+2H2O
HSO3- 为弱酸酸根,不能拆开1年前查看全部
- 亚硫酸氢铵先酸性还是碱性,怎么看的
 liusikao1年前2
liusikao1年前2 -
 yyftsl 共回答了14个问题
yyftsl 共回答了14个问题 |采纳率85.7%酸式盐.中性,水溶液是酸性1年前查看全部
- 设计实验证明亚硫酸氢铵具有还原性
 aa3ffv1年前1
aa3ffv1年前1 -
 avz6 共回答了12个问题
avz6 共回答了12个问题 |采纳率91.7%将NH4HSO3配成溶液,滴入酸性高锰酸钾溶液中,
溶液的紫红色退去,
证明NH4HSO3具有还原性.
方程式 10 NH4HSO3 + 4 KMnO4 + H2SO4 = 2 K2SO4 + 5 (NH4)2SO4 + 4 MnSO4 + 6 H2O1年前查看全部
大家在问
- 1绕太阳做匀速圆周运动的行星,所受重力与向心力之间是什么关系?
- 2用6 7\3 10 3 14\3 中选出4个数组成比值小于1的比例是( ):( )=( ):( ).
- 3—Why are you excited today?
- 4有两桶油,甲桶油重28千克,如果取出甲油桶的七分之二倒入乙桶,则两桶油的重量相等,原来乙油桶的重量是甲油
- 5The method main cannot be declared static; static methods ca
- 6繁衍不息的息是什么意思?只解释息字
- 7已知函数f(x)=x^(-k^2+k+2)(k属于z),且f(2)<f(3),(1)求k的值(2)试判断是否存在正数p,
- 8用一种彩色的硬纸板做某种小礼品的包装盒.每张硬纸板可制作盒身20个,或制盒底30个,1个盒身与2个盒底配成一套.现有28
- 9“物质的特性包括弹性和塑性.请简要说明理由.
- 10请以“New School,New Life”为题,用英语写一篇80词左右的短文,谈一谈你的新学校、新生活、新打算.
- 11童年趣事 作文
- 12等温线 的变化 判断请问 在北半球 ,等温线在陆地向北凸 ,是6月吗在南半球,等温线在陆地向男凸 ,是12月吗 谢绝 粘
- 13方程1:x+y=15 方程2:2x+4y=40 求x,y
- 14新课标同步训练小学英语课堂练习六年级上册答案
- 15电解质溶液通电后会一直导电吗?电解质溶液通电后到底那些离子是什么情况?是带正电离子向负极移动,带负电离子向正极移动吗?那
