一盛有盐水的烧杯中,漂浮着一块冰,等到冰熔化后,水面有什么变化?为什么会这样?
 出来看看2022-10-04 11:39:542条回答
出来看看2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 目光愈拉愈远 共回答了20个问题
目光愈拉愈远 共回答了20个问题 |采纳率100%- 上升
冰融化后盐水浓度降低,体积增大 - 1年前
 花舟 共回答了18个问题
花舟 共回答了18个问题 |采纳率- 应该是下降
质量等于密度乘以体积
同样质量的冰和水(冰化为水后质量一样),因为水的密度更大,所以溶化后的水的体积要小于溶化前的冰的体积,所以水面降低了.
希望你能明白 - 1年前
相关推荐
- 怎么选,为什么一天平的两盘总各放一只烧杯,杯子中盛有适量的水,使天平保持平衡.如果将质量相等的实心铅块和铝块各用一根轻而
怎么选,为什么
一天平的两盘总各放一只烧杯,杯子中盛有适量的水,使天平保持平衡.如果将质量相等的实心铅块和铝块各用一根轻而细的线拴住,然后分别使它们全部浸入水中,水不溢出.下列情况中天平的平衡被破坏的是
A.使它们都沉入杯底
B.把细线挂在天平的钩上,使铅块和铝块都不触底
C.两手分别捏住两根线上,两物块都不触底
D.铝块沉底,把栓铅块的线挂在天平的挂钩上 socong1年前1
socong1年前1 -
 julia_zhu 共回答了20个问题
julia_zhu 共回答了20个问题 |采纳率100%B
B:作为一个整体考虑就可以,在天平左右两边考虑,A:G水+G铜=G水+G铅
C:G水+G铜=G水+G铅
D:G水+G铜=G水+G铅
但是B不同,对于每一个球,G=F手(此项不等)+F浮(此项不等),由于铅铜密度不同,所以在质量相同时,体积不同,浮力不同,球对水的作用力大小等于浮力大小,由于浮力不等,所以天平左右受力不平衡选B.
☆请及时点击【采纳为满意回答】按钮☆1年前查看全部
- 串联电解计算题下图所示装置中,烧杯A中盛有100 g质量分数为11.7 %的氯化钠溶液,烧杯B中盛有100 g质量分数为
串联电解计算题
下图所示装置中,烧杯A中盛有100 g质量分数为11.7 %的氯化钠溶液,烧杯B中盛有100 g质量分数为10.0 %的氢氧化钠溶液,烧杯C中盛有100 g质量分数为12.8 %的硫酸铜溶液.用该装置进行电解实验,一段时间后停止电解,测得烧杯A中NaOH的质量变为8.0 g
电解过程中,电极d、e、f上产生的气体质量分别是多少?
电解结束后,烧杯B中溶液的质量分数是多少?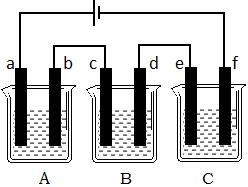
 dreamslink2301年前1
dreamslink2301年前1 -
 彩芸追刖 共回答了16个问题
彩芸追刖 共回答了16个问题 |采纳率87.5%其他同上,只回答你的疑问
确实Cu2+不够,但电解完硫酸铜后,溶液为稀硫酸,还能电解水!
所以O2实际上能达到0.05molO2
但Cu只有0.08 mol!1年前查看全部
- 某烧杯中盛有0.2mol NH 4 Al(SO 4 ) 2 的溶液,向其中缓缓加入4mol•L -1 的NaOH溶液20
某烧杯中盛有0.2mol NH 4 Al(SO 4 ) 2 的溶液,向其中缓缓加入4mol•L -1 的NaOH溶液200mL,使其充分反应,此时烧杯中铝元素的存在形式为( ) A.Al 3+ 和Al(OH) 3 B.AlO - 2 C.AlO - 2 和Al(OH) 3 D.Al(OH) 3  微风四起1年前1
微风四起1年前1 -
 zgq520 共回答了17个问题
zgq520 共回答了17个问题 |采纳率82.4%首先:Al 3+ ~~~3OH -
0.2mol0.6mol
Al 3+ 反应完毕,剩余的OH - 为0.8mol-0.6mol=0.2mol.
然后:NH 4 + ~~~OH -
0.2mol 0.2mol
NH 4 + 与OH - 恰好反应,没有OH - 剩余,Al(OH) 3 不溶解.
故铝元素的存在形式为Al(OH) 3 .
故选D.1年前查看全部
- 如图所示,容器中盛有水,PM为水面,从A点发出一束白光,射到水面上的a点后,折射光发生了色散照到器壁上a、b两点,对应a
 如图所示,容器中盛有水,PM为水面,从A点发出一束白光,射到水面上的a点后,折射光发生了色散照到器壁上a、b两点,对应a、b两种颜色的单色光,则( )
如图所示,容器中盛有水,PM为水面,从A点发出一束白光,射到水面上的a点后,折射光发生了色散照到器壁上a、b两点,对应a、b两种颜色的单色光,则( )
A.由A到O,a光的传播时间等于b光的传播时间
B.若发光点A不变而入射点O向左移,则b光可能发生全反射
C.a光和b光分别通过同一单狭缝,a光在屏上产生的中心亮条纹比b光窄
D.用a光和b光分别在同一套双缝干涉实验装置上做实验,a光的条纹间距较宽 品味生活james1年前1
品味生活james1年前1 -
 三路口 共回答了12个问题
三路口 共回答了12个问题 |采纳率100%解题思路:由光离开水面后的偏折程度,利用折射定律可比较两光的折射率大小,则可求得两光的介质中的光速及波长关系等.再衍射的条件和干涉条纹间距与波长成正比进行分析.A、由图可知,两光在水中的入射角i相同,而a光在真空中的折射角r较小,根据折射定律n=[sinr/sini],故可知a光的折射率要小于b光的折射率; 由v=[c/n]可知,a光在水中的传播速度要大于b光,故A到O,a光的传播时间小于b光的传播时间,故A错误;
B、若发光点A不变而入射点O向左移,则入射角减小,不会发生全反射,故B错误;
C、a光的折射率小,故a光的波长要长,波动性强,a光和b光分别通过同一单狭缝,a光在屏上产生的中心亮条纹比b光宽.故C错误.
D、干涉条纹间距与波长成正比,故a光的干涉条纹间距要宽,故D正确;
故选D点评:
本题考点: 光的折射定律.
考点点评: 本题的解题关键是根据偏折程度确定折射率的大小,再进一步比较波长的大小,分析波动性强弱关系.1年前查看全部
- 如图为某实验小组制取乙酸乙酯的实验装置图,烧瓶中盛有乙醇和浓H2SO4.反应时,将乙酸从分液漏斗滴入烧瓶中即可.
如图为某实验小组制取乙酸乙酯的实验装置图,烧瓶中盛有乙醇和浓H2SO4.反应时,将乙酸从分液漏斗滴入烧瓶中即可.

①为方便研究酯化反应的过程,乙醇中的氧原子用18O进行了标记(即C2H518OH),请用氧的同位素示踪法写出乙酸与乙醇发生酯化反应的化学方程式:______.
②装置A的名称是______,使用时要先从______口(填“a”或“b”)进水.
③实验结束后,锥形瓶中收集到乙酸乙酯、乙醇和乙酸的混合液.为了将这三者进行分离,该小组依如下流程进行了进一步的实验: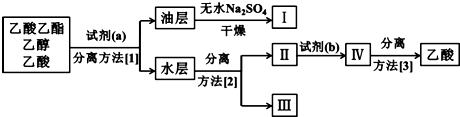
试剂(a)是______,试剂(b)是______,
分离方法(1)是______,分离方法(2)是______,分离方法(3)是______. xy88861年前1
xy88861年前1 -
 czren 共回答了22个问题
czren 共回答了22个问题 |采纳率90.9%解题思路:①根据酯化反应原理酸脱羟基醇脱氢写出反应的化学方程式;
②根据仪器构造可知,A为冷凝管,通水采用逆向通水法;
③试剂a为饱和碳酸钠溶液,试剂b将乙酸钠置换成乙酸,需要加入稳定的、不易挥发的强酸;分离方法(1)分离不相溶的混合液体,方法为分液;方法(2)分离相互溶解的混合液体,采用蒸馏方法;分离方法(3)分离乙酸和硫酸钠溶液,分离方法为蒸馏.①酯化反应中,羧酸脱去羟基,醇脱去氢原子,所以该反应的化学方程式为:CH3COOH+C2H518OH⇌CH3CO18OC2H5+H2O,
故答案为:CH3COOH+C2H518OH⇌CH3CO18OC2H5+H2O;
②仪器A为冷凝管,为了提高冷凝效果,通水方法为逆向,即从b进水,a出水,
故答案为:冷凝管;b;
③乙酸和乙醇能够溶于碳酸钠溶液,而乙酸乙酯不溶于碳酸钠溶液,所以试剂a为饱和碳酸钠溶液;根据流程可知,试剂b将醋酸钠转化成醋酸,由于硝酸和盐酸具有挥发性,试剂b为硫酸;操作方法(1)分离互不相溶的混合液体,操作方法为为分液;操作方法(2)将乙醇与混合液分离,分离方法为蒸馏;操作(3)将乙酸从混合液分离,分离方法为为蒸馏,
故答案为:Na2CO3; H2SO4;分液;蒸馏;蒸馏.点评:
本题考点: 乙酸乙酯的制取;物质的分离、提纯和除杂.
考点点评: 本题考查了乙酸乙酯的制取方法,题目难度不大,注意掌握乙酸乙酯的制取原理,明确在反应过程中浓硫酸、饱和碳酸钠的作用.1年前查看全部
- (2014•长春)甲、乙两个圆柱形容器中盛有两种不同的液体A、B,液面位置如图,液体对两个容器底的压强相等,则ρA___
 (2014•长春)甲、乙两个圆柱形容器中盛有两种不同的液体A、B,液面位置如图,液体对两个容器底的压强相等,则ρA______ρB.现将两个质量相等的物体分别放入两个容器中,静止时一个漂浮,另一个悬浮(液体均无溢出),此时两个容器底受到液压强的大小关系是P甲______P乙.
(2014•长春)甲、乙两个圆柱形容器中盛有两种不同的液体A、B,液面位置如图,液体对两个容器底的压强相等,则ρA______ρB.现将两个质量相等的物体分别放入两个容器中,静止时一个漂浮,另一个悬浮(液体均无溢出),此时两个容器底受到液压强的大小关系是P甲______P乙.  _mfg_c_a6ut0ba_f1年前0
_mfg_c_a6ut0ba_f1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 如图所示,锥形瓶中盛有0℃的水,现用酒精灯加热,使水温升高到10℃,在这一过程中(不考虑水的汽化及锥形瓶的热胀冷缩),则
如图所示,锥形瓶中盛有0℃的水,现用酒精灯加热,使水温升高到10℃,在这一过程中(不考虑水的汽化及锥形瓶的热胀冷缩),则水对锥形瓶底的压强变化是( )
A. 不变
B. 变大
C. 先变小,后变大
D. 先变大,后变小 zhangxiaobo1年前0
zhangxiaobo1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 在一烧杯中盛有100g BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混
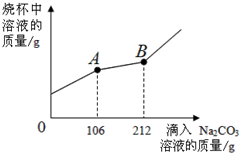 在一烧杯中盛有100g BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入的Na2CO3溶液的质量关系图象如图所示.
在一烧杯中盛有100g BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入的Na2CO3溶液的质量关系图象如图所示.
(1)在实验过程中,有气体放出,还可以看到的明显实验现象是______.
(2)原溶液中HCl的质量分数为______.
(3)当滴入Na2CO3溶液至图中B点时,通过计算求所得不饱和溶液中溶质质量分数为多少?(计算结果精确到0.1%) aaawj1年前1
aaawj1年前1 -
 wuyuying00 共回答了20个问题
wuyuying00 共回答了20个问题 |采纳率95%解题思路:(1)向盛有BaCl2和HCl的混合溶液中滴加Na2CO3溶液时,碳酸钠先与盐酸反应产生二氧化碳,当盐酸反应完后,再与氯化钡反应产生碳酸钡沉淀;
(2)开始时是生成气体的,由于加入的是碳酸钠溶液,而生成的是二氧化碳气体,两者的质量明显是增加多,减少的少,所以曲线明显上扬.当不再生成二氧化碳时,就生成碳酸钡,由于碳酸钡的质量要多于碳酸钠的,所以导致溶液的质量增加减缓.从图中曲线可看出,当滴入碳酸钠106g时,盐酸完全反应,据此可根据滴入碳酸钠质量计算消耗HCl的质量;
(3)从图中曲线可看出,开始滴入106克的碳酸钠与盐酸反应,106克~212克之间滴入碳酸钠与氯化钡反应;即与氯化钡反应的碳酸钠质量为212克-106克;
由化学方程式知,碳酸钠和盐酸、氯化钡反应后溶液中溶质均为氯化钠,可根据化学方程式中参加反应的碳酸钠质量计算生成的氯化钠质量和碳酸钡沉淀质量,再根据质量守恒定律,参加反应的物质总质量等于生成的物质总质量,最后所得不饱和溶液的质量等于l00gBaCl2和HCl的混合溶液,加上滴入的212gNa2CO3溶液,减去生成的气体和沉淀的质量,即可计算所得不饱和溶液中溶质质量分数.(1)碳酸钠和盐酸反应产生二氧化碳,有气体放出,与氯化钡反应产生碳酸钡,即有白色沉淀产生;
(2)设实验过程中放出的气体总质量为x,则
Na2CO3 ~2HCl
106 73
106g×10% x
[106/73=
106g×10%
x],
x=7.3g
原溶液中HCl的质量分数为:[7.3g/100g×100%=7.3%;
(3)设实验过程中产生氯化钠质量为y,产生碳酸钡质量为z,则
本关系是指整个过程的,不考虑是碳酸钠与盐酸还是和氯化钡反应,最终对应的钠都在氯化钠中.
Na2CO3 ~2NaCl
106 117
212g×10% y
106
212g×10%=
117
y],
y=23.4g
后期的碳酸钠中碳酸根转化为碳酸钡沉淀,所以对应的碳酸钠是106g溶液之后的部分.
Na2CO3 ~BaCO3
106 197
(212g-106g)×10% z
=106g×10%
[106/197=
(212g−106g)×10%
z],
z=19.7g
所得NaCl溶液的质量分数为:[23.4g/100g+212g−19.7g−4.4g]×100%=8.1%
答:(1)有白色沉淀生成;
(2)7.3%;
(3)所得不饱和溶液中溶质质量分数是8.1%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题考查根据图象的有关化学方程式的计算,重在考查学生的识图,碳酸钠与两种物质都能发生反应,而首先是与盐酸反应,其次与氯化钡反应.(3)小题结合化学方程式考查溶质质量分数的计算,注意在计算溶液总质量是要灵活运用质量守恒定律,最后所得不饱和溶液的质量等于l00gBaCl2和HCl的混合溶液,加上滴入的212gNa2CO3溶液,减去生成的气体和沉淀的质量,不能多加或少减,此小题较难,学生容易出错,平时要多注意训练.(3)小题在计算氯化钠质量时还可根据钠元素质量守恒,碳酸钠中钠元素全部转移到氯化钠中,据此可求出产生氯化钠质量.1年前查看全部
- (2012•西城区)一个水槽中盛有足够深的水.将一个木块甲放入水中时,木块恰好有一半体积露出水面;当在木块上面放一个金属
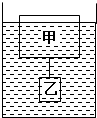 (2012•西城区)一个水槽中盛有足够深的水.将一个木块甲放入水中时,木块恰好有一半体积露出水面;当在木块上面放一个金属块乙时,木块上表面恰好与水面相平;当把金属块乙用细线系在木块下再放入水中时,木块有[1/15]的体积露出水面,如图所示.金属块乙的密度是______g/cm3.
(2012•西城区)一个水槽中盛有足够深的水.将一个木块甲放入水中时,木块恰好有一半体积露出水面;当在木块上面放一个金属块乙时,木块上表面恰好与水面相平;当把金属块乙用细线系在木块下再放入水中时,木块有[1/15]的体积露出水面,如图所示.金属块乙的密度是______g/cm3.  美丽hh女孩1年前1
美丽hh女孩1年前1 -
 luonanxue 共回答了12个问题
luonanxue 共回答了12个问题 |采纳率91.7%解题思路:(1)设木块的体积为V,由于木块漂浮在水面上,根据阿基米德原理和物体的漂浮条件可得ρ水[1/2]Vg=G甲;
(2)金属乙放在甲上,木块上表面恰好与水面相平,根据阿基米德原理和物体的漂浮条件可得F浮′=G甲+G乙,
可求G乙=[1/2]ρ水Vg,进而求出乙的质量;
(3)如图,根据阿基米德原理和物体的漂浮条件可得F浮″=G甲+G乙,而F浮″=ρ水[14/15]Vg+ρ水V乙g,可求乙的体积,再利用密度公式求金属乙的密度.(1)设木块的体积为V,
∵木块漂浮在水面上,
∴F浮=G排=G甲,
∴ρ水[1/2]Vg=G甲;
(2)金属乙放在甲上,木块上表面恰好与水面相平,则:
F浮′=ρ水Vg=G甲+G乙,
∴G乙=ρ水Vg-G甲=ρ水Vg-ρ水[1/2]Vg=ρ水[1/2]Vg
m乙=[1/2]ρ水V;
(3)如图,F浮″=G甲+G乙,
∴ρ水[14/15]Vg+ρ水V乙g=ρ水Vg,
∴V乙=[1/15]V,
ρ乙=
m乙
V乙=
1
2ρ水V
1
15V=7.5ρ水=7.5g/cm3.
故答案为:7.5.点评:
本题考点: 密度的计算;阿基米德原理;物体的浮沉条件及其应用.
考点点评: 本题考查了学生对阿基米德原理和物体漂浮条件的掌握和运用,解题思路:先求金属乙的质量,再求体积,最后利用密度公式求乙的密度.1年前查看全部
- 做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质).某同学处理废液时做了如下
做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质).某同学处理废液时做了如下实验:取废液缸中上层清液于烧杯中,逐滴滴入Na2CO3溶液至过量.记录滴入Na2CO3溶液质量(x)与有关量的变化关系如图所示.下列判断正确的是( )
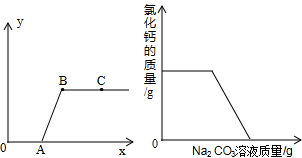
A.图中纵坐标(y)表示生成CO2的质量
B.反应进行到A点时,溶液中的溶质有2种;反应进行到B点时,溶液中的溶质只有1种;反应进行到C点时,溶液中的溶质有2种;
C.OA段溶液的pH增大,AB段溶液的pH不变,BC段溶液的pH增大,
D.纵坐标(y)表示氯化钙的质量,则反应过程可以用右图表示 老区堡垒户1年前1
老区堡垒户1年前1 -
 napolean1 共回答了15个问题
napolean1 共回答了15个问题 |采纳率93.3%解题思路:根据废液中主要含有盐酸与氯化钙,逐滴滴入碳酸钠溶液,碳酸钠应先和盐酸反应,等废液中盐酸被碳酸钠反应消耗完了,碳酸钠开始和氯化钙反应才能产生碳酸钙沉淀,进行分析解答本题.A、根据废液中主要含有盐酸与氯化钙,逐滴滴入碳酸钠溶液,碳酸钠应先和盐酸反应,等废液中盐酸被碳酸钠反应消耗完了,碳酸钠开始和氯化钙反应才能产生碳酸钙沉淀,所以OA段不会有沉淀,发生的反应是碳酸钠应和盐酸的反应.反应当氯化钙被碳酸钠反应完时沉淀达到最大值,反应进行到B点时,碳酸钠和氯化钙恰好完全反应,生成碳酸钙沉淀和氯化钠,因此溶液中所含溶质是NaCl、H2O,继续滴加碳酸钠溶液,沉淀不会增加,溶液中因为有多余的碳酸钠存在而显碱性.因此C点溶液的pH>7,综合分析图中纵坐标(y)轴表示应该是生成碳酸钙沉淀的质量;故A错误;
B、OA段发生的反应是碳酸钠应和盐酸的反应,反应进行到A点时,溶液中的溶质为氯化钠和氯化钙2种;反应进行到B点时,碳酸钠和氯化钙恰好完全反应,生成碳酸钙沉淀和氯化钠,因此溶液中所含溶质是NaCl;反应进行到C点时,溶液中的溶质有2种 NaCl,Na2CO3;故B正确;
C、OA段发生的反应是碳酸钠应和盐酸的反应,随滴入Na2CO3溶液显碱性,OA段溶液的pH增大;因为反应进行到B点时,碳酸钠和氯化钙恰好完全反应,此时溶液显中性;图上B到C点意思是继续滴加碳酸钠,溶液中因为有多余的碳酸钠存在而显碱性.故C点溶液的pH>7.故C正确;
D、根据废液中主要含有盐酸与氯化钙,逐滴滴入碳酸钠溶液,碳酸钠应先和盐酸反应,等废液中盐酸被碳酸钠反应消耗完了,碳酸钠开始和氯化钙反应才能产生碳酸钙沉淀,因此纵坐标(y)表示氯化钙的质量,则反应过程可以用右图表示;故D正确;
故选BCD.点评:
本题考点: 碳酸钠、碳酸氢钠与碳酸钙;溶液、溶质和溶剂的相互关系与判断;酸的化学性质;溶液的酸碱性与pH值的关系;根据化学反应方程式的计算.
考点点评: 学生平时要加强课外实验探究,不断地培养自己的发现问题、分析问题、解决问题的能力.1年前查看全部
- 在相同温度下,在盛有等质量饱和食盐水和不饱和食盐水的两烧杯中,各放一个完全相同的乒乓球,则下列说法不正确的是( )
在相同温度下,在盛有等质量饱和食盐水和不饱和食盐水的两烧杯中,各放一个完全相同的乒乓球,则下列说法不正确的是( )
A. 两烧杯中溶液的溶质质量分数不相同
B. 两乒乓球受到的浮力相同
C. 乒乓球高出液面的部分相同
D. 两烧杯中溶液的导电能力相同 mz2441年前1
mz2441年前1 -
 飞鸟36 共回答了20个问题
飞鸟36 共回答了20个问题 |采纳率90%解题思路:温度相同时,同种物质的饱和溶液比不饱和溶质的质量分数大,密度大,结合物理学知识可以知道,物体在溶液中受到的浮力等于重力,所不同的是,溶液密度不同而使物体浸入液体的体积也不同,可以据此解答本题.A、在相同的温度下,等质量的饱和食盐水所含的食盐比不饱和食盐水所含食盐的质量要大,所以它们的溶质的质量分数也不同,故A对
B、乒乓球所受的浮力跟其重力相等,由于乒乓球完全相同,所它们受到的浮力也相等,故B对
C、虽然它们受到的浮力相等,但是由于溶液的密度不同,根据F浮=ρ液gV排可知他们排开液体的体积不同,所以高出液面的部分不同,故C错
D、溶液的浓度不同,所含的阴阳离子的浓度就不同,所以这两种溶液的导电能力就不同,故D错
故选CD点评:
本题考点: 溶质的质量分数、溶解性和溶解度的关系;浓溶液、稀溶液跟饱和溶液、不饱和溶液的关系.
考点点评: 本题考查的是同一温度下饱和溶液和不饱和溶液与溶质质量分数的关系,要明白在温度相同时,饱和溶液的质量分数最大,同时知道漂浮与液面的物体受到的浮力和重力相等,不同的是由于密度的不同而使排开液体的体积不同.1年前查看全部
- 已知白磷跟氧气可发生如下反应:P4+3O2=P4O6,P4+5O2=P4O10.某密闭容器中盛有31 g白磷和1 mol
已知白磷跟氧气可发生如下反应:P4+3O2=P4O6,P4+5O2=P4O10.某密闭容器中盛有31 g白磷和1 mol氧气,使之恰好完全反应后,所得到的P4O6和P4O10的物质的量之比为
 lihuavv1年前3
lihuavv1年前3 -
 41133018 共回答了25个问题
41133018 共回答了25个问题 |采纳率96%1:1
1molP4需要3mol氧气生成P4O6
1molP4需要1mol氧气生成P4O10
题中31gP4,也就是0.25molP4跟1mol氧气反应,也就是它们的比例是1:4
用十字交叉法,两者物质的量比是1:11年前查看全部
- (2013•泰州)在底面积相等的圆柱体﹑长方体和圆锥体容器中盛有相同高度的水,分别把a克盐(a>0)全部溶解在各容器的水
(2013•泰州)在底面积相等的圆柱体﹑长方体和圆锥体容器中盛有相同高度的水,分别把a克盐(a>0)全部溶解在各容器的水中,圆锥中盐水的含盐率最高.______ (判断对错)
 rzw5881年前1
rzw5881年前1 -
 低级岳母 共回答了15个问题
低级岳母 共回答了15个问题 |采纳率80%解题思路:要比较谁的含盐率高,在盐都是5克的情况下,谁的容器里水少,谁的容器中盐水含盐率就高,因为底面积和水的高度相等,所以圆锥体内水的质量最少,所以圆锥容器中盐水含盐率就最高,据此解答即可.因为盐都是10克,底面积和水的高度相等,所以圆锥体内水的质量最少,
所以圆锥容器中盐水含盐率就最高.
所以题干的说法是正确的.
故答案为:√.点评:
本题考点: 百分率应用题;圆柱的侧面积、表面积和体积;圆锥的体积.
考点点评: 本题考查了立体图形的体积和含盐率的意义的综合应用,关键是明确:溶质一定,浓度与溶液的总质量成反比.1年前查看全部
- 用隔板将一绝热容器隔成A和B两部分,A中盛有一定质量的理想气体,B为真空(如图①),现把隔板抽去,A中的气体自动充满整个
用隔板将一绝热容器隔成A和B两部分,A中盛有一定质量的理想气体,B为真空(如图①),现把隔板抽去,A中的气体自动充满整个容器(如图②),这个过程称为气体的自由膨胀,下列说法正确的是( )
 A. 自由膨胀过程中,气体分子只做定向运动
A. 自由膨胀过程中,气体分子只做定向运动
B. 自由膨胀前后,气体的压强不变
C. 自由膨胀前后,气体的温度不变
D. 容器中的气体在足够长的时间内,还能全部自动回到A部分 偷吃大米的小老鼠1年前1
偷吃大米的小老鼠1年前1 -
 你烦恼暖 共回答了15个问题
你烦恼暖 共回答了15个问题 |采纳率93.3%解题思路:正确解答本题要掌握:气体分子做无规则热运动,不可能只做定向运动;气体自由膨胀过程中不受阻力,因此不做功;自然界中的宏观过程具有方向性,是不可逆的,注意热力学第二定律的应用.A、分子时刻在做无规则的热运动,故A错误;
B、自由膨胀后,温度不变,体积变大,由气态方程可知,压强变小,故B错误;
C、自由膨胀过程中由于不受阻力作用,因此气体不做功,由于容器绝热,因此Q=0,由△U=W+Q可知,气体内能不变,因此温度也不变,故C正确;
D、根据热力学第二定律可知,气体向真空的自由膨胀是不可逆的,故D错误.
故选C.点评:
本题考点: 热力学第二定律;气体的体积、温度、压强之间的关系.
考点点评: 正确利用热力学第二定律解释一些物理现象,在利用热力学第一定律△U=W+Q时注意公式中各个物理量的含义,尤其注意各个物理量的正负问题.1年前查看全部
- 如图所示,玻璃杯中盛有水,现在将杯子放在冰箱里,待温度降低后取出(取出时温度高于4度),那么与放入冰箱前比较,水对杯底的
如图所示,玻璃杯中盛有水,现在将杯子放在冰箱里,待温度降低后取出(取出时温度高于4度),那么与放入冰箱前比较,水对杯底的压强______,水对杯底的压力_____
 zxcj28998afdsjad1年前5
zxcj28998afdsjad1年前5 -
 钱被建行的机给吞 共回答了26个问题
钱被建行的机给吞 共回答了26个问题 |采纳率88.5%在4摄氏度时水的密度最大
取出时温度高于4度温度接近于4摄氏度说明水的密度增加了
质量不变,所以水的体积减小,深度减小
不能用p=pgh计算(密度和深度都变了)
要用 p=F/S S(深度小了加上侧面总S小了而F不变)所以 压强总体都增大.
所以F=PS压力也增大1年前查看全部
- 一个容器中盛有10cm深的水,平放在水平桌面上,容器底部所受水的压强是 Pa如果要使水对杯底压强增大.如果要使水对杯底的
一个容器中盛有10cm深的水,平放在水平桌面上,容器底部所受水的压强是 Pa如果要使水对杯底压强增大.如果要使水对杯底的压强增大,可采取什么方法?
 xdim1121年前1
xdim1121年前1 -
 lanshankafei 共回答了10个问题
lanshankafei 共回答了10个问题 |采纳率90%P=ρ液gh=1000*9.8*0.1(m)=980Pa 可以加水1年前查看全部
- 纸杯中盛有米,米内插有筷子 将米压紧后竖直向上提筷子
纸杯中盛有米,米内插有筷子 将米压紧后竖直向上提筷子
说是米和筷子间的摩擦力大于筷子和杯子的重力 那杯子和米之间的摩擦力也大于杯子的重力吗 -.- 具体的是怎样阿~ wgw12301年前4
wgw12301年前4 -
 娃哈哈0176 共回答了23个问题
娃哈哈0176 共回答了23个问题 |采纳率82.6%米与筷子之间的摩擦力大小等于米和杯子的总重力,杯子与米之间的摩擦力大小等于杯子的重力~作用平衡的知识去想就可以啦~1年前查看全部
- 容器中盛有水,在平底小试管下面挂一小实心铁块,放入水中后浮在水面.现将小铁块取下放入小试管中,将小试管再放入水中后,小试
容器中盛有水,在平底小试管下面挂一小实心铁块,放入水中后浮在水面.现将小铁块取下放入小试管中,将小试管再放入水中后,小试管仍浮在水面.则容器中的液面将 A上升 B下降 C不变 D无法确定
 cockbig1年前1
cockbig1年前1 -
 dfgdfh 共回答了16个问题
dfgdfh 共回答了16个问题 |采纳率100%C正确.把试管和铁块看成一个整体,两种情况中,这个整体都处于漂浮状态,而这个整体的重不变,根据物体漂浮的特点F浮=G物,因此整体受到的浮力不变,由F浮=ρV排g,V排不变,所以水面高度也不变.1年前查看全部
- 下图为某实验小组制取乙酸乙酯的实验装置图,烧瓶中盛有乙醇和浓H 2 SO 4 。反应时,将乙酸从分液漏斗滴入烧瓶中即可。
下图为某实验小组制取乙酸乙酯的实验装置图,烧瓶中盛有乙醇和浓H 2 SO 4 。反应时,将乙酸从分液漏斗滴入烧瓶中即可。

①为方便研究酯化反应的过程,乙醇中的氧原子用 18 O进行了标记(即C 2 H 5 18 OH),请用氧的同位素示踪法写出乙酸与乙醇发生酯化反应的化学方程式: 。
②装置A的名称是 ,使用时要先从 口(填“a”或“b”)进水。
③实验结束后,锥形瓶中收集到乙酸乙酯、乙醇和乙酸的混合液。为了将这三者进行分离,该小组依如下流程进行了进一步的实验:
试剂(a)是 ,试剂(b)是 ,
分离方法(1)是 ,分离方法(2)是 ,分离方法(3)是 。 伤心的路人1年前1
伤心的路人1年前1 -
 无敌的降落伞要员 共回答了17个问题
无敌的降落伞要员 共回答了17个问题 |采纳率100%1年前查看全部
- 已知同温同压下,相同体积的任何气体都含有相同数目的分子在一个密闭容器中盛有H2 O2 CL2组成的混合气体.通过电火花引
已知同温同压下,相同体积的任何气体都含有相同数目的分子在一个密闭容器中盛有H2 O2 CL2组成的混合气体.通过电火花引爆后,三种气体恰好完全反应.经充分冷却后,所得溶液中溶质的质量分数为33.4%,则原混合气体中H2 O2 CL2分子数目简单整数比是?(氢气和氯气点燃生成氯化氢气体,氯化氢气体易容与水)
 emilyxu1年前1
emilyxu1年前1 -
 蟾树烟然 共回答了19个问题
蟾树烟然 共回答了19个问题 |采纳率84.2%假设氧气物质的量为x,氯气物质的量为y
2H2+O2=2H2O H2+Cl2=2HCl
2x x 2x y y 2y 36.5*2y/(36.5*2y+18*2x)=33.4%
解出 H2 O2 CL2之比即(2x+y):x:y=9:4:11年前查看全部
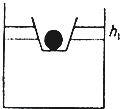
- 在一圆柱形容器中盛有水,水面漂浮着一个小容器.当将一个实心小塑料球放入小容器中后,大容器中的水面上升的高度是h1,如图所
在一圆柱形容器中盛有水,水面漂浮着一个小容器.当将一个实心小塑料球放入小容器中后,大容器中的水面上升的高度是h1,如图所示.若把这个塑料球从小容器中拿出投入大容器的水中,液面又降低了h2,求这个塑料小球的密度.
 muqing1011年前1
muqing1011年前1 -
 弃圣绝智 共回答了17个问题
弃圣绝智 共回答了17个问题 |采纳率76.5%解题思路:根据题意,利用容器的底面积和水上升的高度表示开小球和小容器排开水的体积;根据漂浮的条件,利用体积、密度和表示出小球的重力与浮力的关系;利用容器的底面积和水面上升的高度表示出小球排开水的体积,分别列出关系式,联立解之即可.设大容器的底面积为S,塑料球体积为V塑,密度为ρ塑,当把塑料球放入小容器中时,排开水的体积为V排,则有:
V排=Sh1---①
V塑ρ塑g=V排ρ水g----②
当把塑料球从小容器中拿出放入水中后,塑料球排开水的体积为V塑,则:
△V=V排-V塑=Sh2-----③
[①/②]可得,
V排
V排−V塑=
h1
h2,
化简可得:V排h2=V排h1-V塑h1
V塑h1=(h1-h2)V排----④
[②/④]可得:ρ塑=
h1
h1−h2ρ水.
答:这个塑料小球的密度ρ塑=
h1
h1−h2ρ水.点评:
本题考点: 阿基米德原理.
考点点评: 本题有一定的难度,考查了学生的综合分析能力.解答本题的关键是对实心球质量和体积的求解,质量需要根据物体的浮沉条件和阿基米德原理进行求解,体积需要根据实心球前后V排的变化和物体的浮沉条件去分析.1年前查看全部
- (2005•南京)如图所示,一只烧杯中盛有石蜡油、水和水银三种液体,液体之间并不溶合.将一实心铅块(铅的密度是11.3g
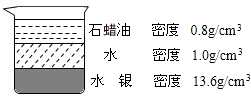 (2005•南京)如图所示,一只烧杯中盛有石蜡油、水和水银三种液体,液体之间并不溶合.将一实心铅块(铅的密度是11.3g/cm3)轻轻该放入烧杯中,图中能正确显示出铅块静止时位置的如图是( )
(2005•南京)如图所示,一只烧杯中盛有石蜡油、水和水银三种液体,液体之间并不溶合.将一实心铅块(铅的密度是11.3g/cm3)轻轻该放入烧杯中,图中能正确显示出铅块静止时位置的如图是( )
A.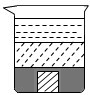
B.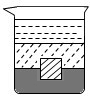
C.
D.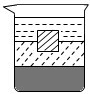
 ewf424we1年前1
ewf424we1年前1 -
 MM16 共回答了22个问题
MM16 共回答了22个问题 |采纳率86.4%解题思路:由物体的浮沉条件可知:
浸没在液体中的某种物体,当物体的密度大于液体的密度时,物体将下沉;
当物体的密度小于液体的密度时,物体将上浮,最后漂浮在液面.
由题中数据知:铅块的密度要大于水和石蜡油的密度,因此在这两种液体中要下沉;
而铅块的密度小于水银的密度,因此最后在水银中漂浮;据此判断.A、铅块在水银中,因为铅块的密度小于水银的密度,铅块将上浮,故A错;
B、铅块在水和水银中,因为铅块的密度大于水、小于水银的密度,受到水和水银的浮力等于铅块重而静止,故B正确;
C、铅块在水中,因为铅块的密度大于水的密度,铅块将下沉,故C错;
D、铅块在水和石蜡油中,因为铅块的密度大于水和石蜡油的密度,铅块将下沉,故D错;
故选B.点评:
本题考点: 物体的浮沉条件及其应用.
考点点评: 本题可以利用“排除法”选择答案,根据浮沉条件(ρ液>ρ物,物体上浮;ρ液<ρ物,物体下沉;ρ液=ρ物,物体悬浮)判断A、C、D是错的,得出B正确.1年前查看全部
- 在一烧杯中盛有100g含CaCl2和HCl两种溶质的溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,生成沉淀
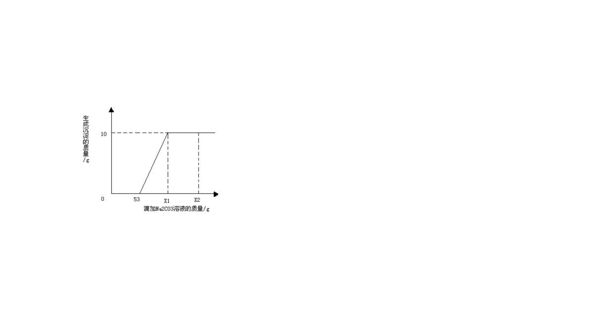
在一烧杯中盛有100g含CaCl2和HCl两种溶质的溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,生成沉淀的总质量与所滴入Na2CO3溶液的质量关系曲线如图所示,根据题意回答问题:
试通过计算求出原烧杯中CaCl2的质量分数.
 mazhou9451年前1
mazhou9451年前1 -
 lihuabing 共回答了18个问题
lihuabing 共回答了18个问题 |采纳率88.9%先根据方程式计算出生成CO2和NaCI的质量,然后根据方程式求出CaCO3和NaCI的质量.NaCI的质量除以100+Na2CO3的质量-CO2和CaCO3的质量
你那图看不清数值.没法给你写过程1年前查看全部
- 将甲、乙两个容器放在水平桌面上,甲容器中盛有密度为0.8g/cm3的酒精,乙容器中盛有密度为13.6g/cm3的水银.现
将甲、乙两个容器放在水平桌面上,甲容器中盛有密度为0.8g/cm3的酒精,乙容器中盛有密度为13.6g/cm3的水银.现有一体积为500cm3的圆柱形金属块.当用竖直向上的拉力F拉浸在酒精中的金属块时,可使金属块的1/4体积露出液面,如图甲所示;当用竖直向下的拉力F拉浸在水银中的金属块时,可使金属块的1/4体积露出液面,如图乙所示.g取10N/kg.则下列判断正确的是( )
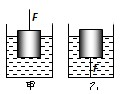 A. 物体在两液体中受的浮力一样大
A. 物体在两液体中受的浮力一样大
B. 物体底部在两液体中所受压强一样大
C. 物体的密度为4.5×103 kg/m3
D. F的大小为24N pearl_19821年前1
pearl_19821年前1 -
 找朋友专用 共回答了23个问题
找朋友专用 共回答了23个问题 |采纳率78.3%解题思路:(1)分别用F浮=ρ液gV排计算出浮力,然后比较即可;
(2)因物体浸没的深度相同,通过P=ρgh比较液体密度即可;
(3)根据金属块在水银河煤油中都是在力F的作用下处于静止状态,合力为零,列出等式即可解得;
(4)根据前面得出的浮力和金属块的重力即可求出拉力F.A、已知金属块体积为V=500cm3=5×10-4m3,则V排=(1-[1/4])V=[3/4]×5×10-4m3=3.75×10-4m3,所以在煤油中受到的浮力为F浮1=ρ煤油gV排=0.8×103kg/m3×10N/kg×3.75×10-4m3=3N,在水银中受到的浮力为F浮2=ρ水银gV排=13.6×103kg/m3×10N/kg×3.75×10-4m3=51N,比较可知,物体在两液体中受的浮力不一样大,故A错;
B、因金属块在甲、乙两个容器里的液体中都是有[1/4]的体积露出液面,所以物体底部在两液体中所处的深度相同,而水银的密度大于煤油的密度,则根据P=ρgh可知,金属块底部在水银中所受压强大,故B错;
C、因金属块在水银河煤油中都是在力F的作用下处于静止状态,
则在煤油中:F浮1+F=G---------①
在水银中:F浮2=G+F---------②
两式相加得:F浮1+F浮2=2G,
所以G=[1/2](F浮1+F浮2)=[1/2]×(3N+51N)=27N.
由G=mg=ρVg得:金属块密度ρ=[G/Vg]=
27N
5×10−4m3×10N/kg=5.4×103kg/m3;
由此可知C选项错;
D、由①式得:F=G-F浮1=27N-3N=24N;故D正确.
故选D.点评:
本题考点: 浮力大小的计算;密度的计算;压强大小比较.
考点点评: 本题考查浮力的计算,知道物体处于平衡状态时合力为零,且能根据两个情况下的平衡列出等式,然后解之,本题难度较大.1年前查看全部
- 在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)⇌2HBr(g);△H<0
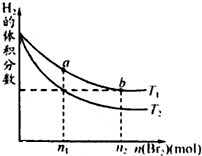 在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)⇌2HBr(g);△H<0.当温度分别为T1、T2达平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法不正确的是( )
在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)⇌2HBr(g);△H<0.当温度分别为T1、T2达平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法不正确的是( )
A.由图可知:T1>T2
B.a、b两点的反应速率:b>a
C.为了提高Br2(g)的转化率,可采取将HBr液化并及时移走的方法
D.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加 feifei6543211年前1
feifei6543211年前1 -
 gfstar 共回答了18个问题
gfstar 共回答了18个问题 |采纳率100%解题思路:A.该反应是正反应为放热的化学反应,升高温度,平衡向逆反应方向移动导致氢气的含量增大,据此判断;
B.对比两个平衡状态,可以看作向a的平衡状态加入(n2-n1)molBr2建立了化学平衡b,利用速率与平衡移动关系分析;
C.根据浓度对化学平衡移动的影响来分析;
D.加入溴平衡向正反应方向移动,HBr的体积分数与加入溴的量及转化率有关.A.根据图象可知,当加入的n(Br2)均为n1建立化学平衡后,H2的体积分数温度T1的大于温度T2,该反应是正反应为放热反应,升高温度,平衡逆反应方向移动导致氢气的体积分数降低,所以T1>T2,故A正确;
B.对a和b来说,温度相同,H2的初始量相同,Br2的初始量是b>a,a、b两个平衡状态,可以认为是向a的平衡状态加入(n2-n1)molBr2建立了化学平衡b,而加入Br2,平衡向正反应方向移动,建立平衡b后,其反应速率要增加,即两点的反应速率a<b,故B正确;
C.将HBr液化并及时移走,HBr的浓度降低,平衡向正反应方向移动,溴的转化率增大,故C正确;
D.当温度均为T1时,加入Br2,平衡会向正反应方向移动,导致HBr的物质的量不断增大,但体积分数不一定逐渐增大,这与加入的溴的量及转化率有关,故D错误,
故选D.点评:
本题考点: 体积百分含量随温度、压强变化曲线.
考点点评: 本题考查了外界条件对化学平衡的影响,易错选项是D,注意反应物的转化率增大,生成物的体积分数不一定增大,这与反应物的量有关.1年前查看全部
- 把1.92克铜投入盛有一定量浓硝酸的试管中
 pictor1年前1
pictor1年前1 -
 chixiangyu 共回答了10个问题
chixiangyu 共回答了10个问题 |采纳率80%铜与浓硝酸反应一部分后,浓硝酸就变稀了,所以其实既有和浓硝酸的反应,也有和稀硝酸的反应,因此放出气体有两种.1年前查看全部
- (2013•枣阳市模拟)在一烧杯中盛有24.3g Na2SO4和NaCl组成的固体混合物,加入100g水使Na
 (2013•枣阳市模拟)在一烧杯中盛有24.3g Na2SO4和NaCl组成的固体混合物,加入100g水使Na2SO4和NaCl全部溶解.向其中逐渐滴加溶质质分数为20%的氯化钡溶液.生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图所示.
(2013•枣阳市模拟)在一烧杯中盛有24.3g Na2SO4和NaCl组成的固体混合物,加入100g水使Na2SO4和NaCl全部溶解.向其中逐渐滴加溶质质分数为20%的氯化钡溶液.生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图所示.
(1)请分析当BaCl2溶液滴加到B点时,溶液中的溶质是BaCl2NaClBaCl2NaCl.
(2)请计算当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数(计算结果保留一位小数). fmd1231年前1
fmd1231年前1 -
 清风幽茗 共回答了17个问题
清风幽茗 共回答了17个问题 |采纳率94.1%(1)当沉淀的质量不再增加时,说明反应已经进行完毕,所以当BaCl2溶液滴加到B点时说明氯化钡溶液滴加过量,当BaCl2溶液滴加到B点时,溶液中的溶质有刚生成的氯化钠和原来的氯化钠以及过量的氯化钡;故填:BaCl2NaCl;
(2)设参加反应的硫酸钠的质量为x,生成的硫酸钡的质量为y,生成的氯化钠的质量为z.
BaCl2+Na2SO4=2NaCl+BaSO4↓
208142117233
104g×20% xzy
208
104g×20%=
142
x
x=14.2g
208
104g×20%=
233
y
y=23.3g
208
104g×20%=
117
z
z=11.7g
当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数=
24.3g-14.2g+11.7g
24.3g+100g+104g-23.3g×100%=10.6%
答:当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数为10.6%.1年前查看全部
- 计算题(第三题需要过程)在一烧杯中盛有100g的FeCl3和HCl的混合溶液,向其中逐渐滴加溶质质量分数为12%的NaO
计算题(第三题需要过程)
在一烧杯中盛有100g的FeCl3和HCl的混合溶液,向其中逐渐滴加溶质质量分数为12%的NaOH溶液,沉淀的质量与所滴入NaOH溶液的质量关系如图所示.请根据题意回答下列问题:
(1)在实验过程中产生沉淀的质量是________;
(2)在实验过程中加入65g的NaOH溶液时所得溶液的pH是_______7(选填大于、小于或等于)
(3)计算原混合溶液中HCl的质量分数.(计算结果精确至0.01%)

 balanacong1年前1
balanacong1年前1 -
 思智 共回答了16个问题
思智 共回答了16个问题 |采纳率87.5%(1)在实验过程中产生沉淀的质量是__4.28g__;
(2)在实验过程中加入65g的NaOH溶液时所得溶液的pH是__大于_7(选填大于、小于或等于)
(3)计算原混合溶液中HCl的质量分数.(计算结果精确至0.01%)
与HCl反应的氢氧化钠溶液的质量为20g(如图)
原混合溶液中HCl的质量 x
HCl + NaOH===NaCl+H2O
36.5 40
y 20g*12%
36.5/Y=40/2.4g
y=2.19g
原混合溶液中HCl的质量分数2.19g/100g*100%=2.19%1年前查看全部
- 一个底面半径是10cm,高14cm的圆柱形容器中盛有一些水,水面高10cm.现在将一个底面半径是5cm
一个底面半径是10cm,高14cm的圆柱形容器中盛有一些水,水面高10cm.现在将一个底面半径是5cm
的圆锥形铁块完全浸没在水中,此时水面高11cm,这个圆锥形铁块的高是多少厘米? 骂我吧1年前2
骂我吧1年前2 -
 syxlm 共回答了17个问题
syxlm 共回答了17个问题 |采纳率88.2%圆锥体积=3.14×10×10×(11-10)=314立方厘米;
高=314×3÷(3.14×5×5)=12厘米
很高兴为您解答,skyhunter002为您答疑解惑
如果本题有什么不明白可以追问,1年前查看全部
- 正在加热的烧杯A中盛有沸水,将装有热水的试管B放入其中,试管B中的水不会沸腾,why?
 zhangqitianjin1年前3
zhangqitianjin1年前3 -
 xxq867 共回答了13个问题
xxq867 共回答了13个问题 |采纳率92.3%沸腾的两个条件是达到沸点和继续吸热.试管里的水虽然达到了沸点,但因为烧杯中的水也是100℃,所以同样为100℃的试管里的水不能从烧杯里的水中吸热,所以不能沸腾.
如果试管里的水换成沸点为78℃的酒精,酒精就可以从烧杯里的100℃的水中吸热,就能沸腾.1年前查看全部
- 使阳光通过棱镜射到容器A中,容器A中盛有葡萄糖溶液,其中生活着大量衣藻,
使阳光通过棱镜射到容器A中,容器A中盛有葡萄糖溶液,其中生活着大量衣藻,
5 - 解决时间:2008-9-6 15:36
请问 衣藻在容器A中是否均匀分布 为什么向容器中放入大量的草履虫,草履虫是否均匀分布 为什么;如果将草履虫换成大量的乳酸菌,则这些乳酸菌如何分布 为什么 wuxiaonline1年前4
wuxiaonline1年前4 -
 Hansxia 共回答了18个问题
Hansxia 共回答了18个问题 |采纳率100%楼上你不要瞎说!我受不了了#¥%#……#¥%……
用棱镜折射是要把阳光散开 应该是七彩光带
光射进衣藻后 会进行光合作用
衣藻有叶绿体 吸收七彩中的蓝紫光 所以散射出的光带中 蓝紫的部分产生的氧气最多
而草履虫会聚集到氧气多的地方 因为他要进行有氧呼吸
乳酸菌厌氧 他会分布在远离氧气的地方
葡萄糖 是用来呼吸分解的 都是单细胞生物 要外界提供养料才行1年前查看全部
- 如图,烧杯中盛有质量相等、质量分数相等的稀盐酸,天平调平后,同时向其中分别加入等质量的锌片和铁片,则从反应开始到金属完全
如图,烧杯中盛有质量相等、质量分数相等的稀盐酸,天平调平后,同时向其中分别加入等质量的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
 A. 始终向左偏
A. 始终向左偏
B. 始终向右偏
C. 先向左偏后向右偏
D. 先向右偏后向左偏 HAOXIANGHAOXIANG1年前1
HAOXIANGHAOXIANG1年前1 -
 dxh0414 共回答了19个问题
dxh0414 共回答了19个问题 |采纳率84.2%解题思路:根据金属与酸反应放出氢气的快慢和金属与酸反应放出氢气的多少,判断变化过程中天平指针会如何变化.天平的指针总是偏向质量大的一方;在两边的金属都没反应完时,由于锌的活动性比铁强,锌与稀盐酸反应放出氢气的速率大于铁,因此,此段时间内,加铁一边因放出氢气的速度慢而质量大,天平指针偏向加铁一边即偏向图中的右边;当金属锌完全反应后,图中天平左边的质量不再减小,而铁继续与稀盐酸反应,最终放出氢气的多少将决定天平指针的偏转,根据金属与酸反应放出氢气的质量=[金属的化合价/金属相对原子质量]×金属质量,可判断两种金属都完全反应后,铁与盐酸放出氢气的质量大于等质量的锌与盐酸反应放出氢气的质量,所以,天平左边加锌的一端因放出氢气质量少而质量大于加铁的右边,天平指针最终将偏向加锌的左边;综上所述,天平指针就先右偏后向左;
故选:D.点评:
本题考点: 金属的化学性质.
考点点评: 金属与酸反应放出氢气的快慢与金属的活动性有关,而放出氢气的多少与金属的相对质量有关.1年前查看全部
- 保温瓶中盛有液态空气,当打开瓶盖将一根燃着的木条,置于瓶口上方时,可观察______,理由______
保温瓶中盛有液态空气,当打开瓶盖将一根燃着的木条,置于瓶口上方时,可观察______,理由______
这个命题是否有不妥,请说明. wiciai1年前1
wiciai1年前1 -
 闲云小语 共回答了21个问题
闲云小语 共回答了21个问题 |采纳率100%根据燃烧需要同时满足三个条件:①可燃物、②氧气或空气、③达到燃烧所需的最低温度即着火点;保温瓶盖打开时,因为氮气的沸点比氧气低,所以氮气先从液态空气中分离出来,氮气没有助燃性,隔绝了氧气,因此将一...1年前查看全部
- 烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如图所示.则符合该变化的一组物质是( )
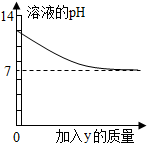 烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如图所示.则符合该变化的一组物质是( )
烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如图所示.则符合该变化的一组物质是( )
x y A NaOH溶液 稀HCl(过量) B 稀H2SO4 BaCl2溶液(少量) C Ca(OH)2 CO2(适量) D 稀H2SO4 H2O
A.A
B.B
C.C
D.D 奇迹会来的1年前1
奇迹会来的1年前1 -
 是故托臣 共回答了19个问题
是故托臣 共回答了19个问题 |采纳率89.5%解题思路:当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性;根据图象,开始时溶液的PH大于7,显碱性,最后溶液的pH接近7,然后根据个选项给出的物质结合物质间的反应进行分析即可.A、氢氧化钠溶液显碱性,pH大于7,当加入过量的稀盐酸时,溶液的pH逐渐减小至小于7,故A错误;
B、稀硫酸显酸性,pH小于7,所以x不是稀硫酸.故B错误;
C、氢氧化钙溶液显碱性,pH大于7,当通入适量二氧化碳时,二氧化碳能和氢氧化钙反应生成碳酸钙沉淀和水,溶液的pH逐渐减小至等于7,故C正确;
D、稀硫酸显酸性,pH小于7,所以x不是稀硫酸.故D错误.
故选C.点评:
本题考点: 溶液的酸碱性与pH值的关系;酸的化学性质;碱的化学性质;中和反应及其应用;酸碱溶液的稀释.
考点点评: 本题结合图象及pH的变化考查了常见物质间的有关反应,掌握溶液的酸碱性和溶液pH大小之间的关系、常见物质间的反应是解题的关键.1年前查看全部
- 一个圆柱形的玻璃杯中盛有水,5cm,玻璃杯内侧的底面积是72cm2,在这个杯中放进棱长6cm的正方体铁块后,水面没有淹没
一个圆柱形的玻璃杯中盛有水,5cm,玻璃杯内侧的底面积是72cm2,在这个杯中放进棱长6cm的正方体铁块后,水面没有淹没铁块,这时水面高多少厘米?
 eyas10221年前1
eyas10221年前1 -
 iloveyuanyuan 共回答了16个问题
iloveyuanyuan 共回答了16个问题 |采纳率100%72×2.5÷(72-6×6)=51年前查看全部
- 冰水混合物的变化将一盛有冰水混合物的敞口玻璃杯在干燥的零摄氏度的环境中放置一段较长的时间,问,杯内冰、水质量比的变化和总
冰水混合物的变化
将一盛有冰水混合物的敞口玻璃杯在干燥的零摄氏度的环境中放置一段较长的时间,问,杯内冰、水质量比的变化和总质量的变化. amwgyyv1年前2
amwgyyv1年前2 -
 缺水544 共回答了15个问题
缺水544 共回答了15个问题 |采纳率100%啊哈哈,忘了,我忘了考虑蒸发了,是杯内冰、水质量比变大,而它的总质量减小.1年前查看全部
- 弹簧测力计下挂一个密度大于水的物块,如图甲所示.水平桌面上的容器中盛有适量的水,将物块浸没在水中,如图乙所示,则物块浸没
弹簧测力计下挂一个密度大于水的物块,如图甲所示.水平桌面上的容器中盛有适量的水,将物块浸没在水中,如图乙所示,则物块浸没在水中后,下列说法错误的是( )
 A. 弹簧测测力计的示数变小
A. 弹簧测测力计的示数变小
B. 水对容器底的压强变大
C. 桌面受到的压强变大
D. 桌面受到的压力不变 不会睡的鱼1年前3
不会睡的鱼1年前3 -
 david5518 共回答了15个问题
david5518 共回答了15个问题 |采纳率93.3%解题思路:(1)将物块浸没在水中,由于物块受到水的浮力,弹簧测力计的示数将变小;(2)物块浸没在水后,排开了一定体积的水,使水的深度增加,根据液体压强公式p=ρgh判断水对容器底部的压强变化;(3)物块浸没在水中,物块受到水的浮力,水受到物块的反作用力,桌面受到的压力等于容器和水的总重加上物块对水的反作用力,据此分析桌面受到的压力变化;而受力面积不变,根据p=FS确定桌面受到的压强变化.A、甲图,F拉=G;乙图,将物块浸没在水中,由于物块受到水的浮力,弹簧测力计的示数F′=G-F浮,所以弹簧测力计的示数将变小,故A正确;
B、物块浸没在水中后,水的深度h增加,由p=ρgh可知水对容器底部的压强变大,故B正确;
CD、物块未浸没在水中时,桌面受到的压力F=G水+G容器;物块浸没在水中后,物块受到水的浮力,水受到物块的反作用力F物,桌面受到的压力F′=G水+G容器+F物,可见桌面受到的压力变大;而受力面积不变,由p=[F/S]可知桌面受到的压强变大,故C正确、D不正确.
故选D.点评:
本题考点: 阿基米德原理;压强的大小及其计算;液体的压强的特点.
考点点评: 本题考查了学生对液体压强公式、压强定义式、浮力的了解与掌握,会对物块进行正确的受力分析是本题的关键.1年前查看全部
- 如图所示,在甲乙丙三个相同的容器中盛有质量相等的不同种类的液体
 gcli324441年前1
gcli324441年前1 -
 sphinx85 共回答了22个问题
sphinx85 共回答了22个问题 |采纳率81.8%选B F甲>F丙>F乙1年前查看全部
- 在一个长50cm,宽40cm,高30cm的玻璃钢中盛有15cm深的水,放入一个棱长是10cm饿正方形,正方形全部
在一个长50cm,宽40cm,高30cm的玻璃钢中盛有15cm深的水,放入一个棱长是10cm饿正方形,正方形全部
没入水中,水面上升多少cm?
 52117561年前1
52117561年前1 -
 迷你NI 共回答了25个问题
迷你NI 共回答了25个问题 |采纳率96%水缸内物质体积增加量就是立方体的体积,
所以ΔV=10×10×10=1000cm³,
水缸底面积为S=50×40=2000cm²,
所以水面上升距离ΔH=ΔV÷S=0.5cm.1年前查看全部
- (2011•西宁)将适量的橡皮泥黏在铅笔的一端(能使铅笔竖直浮在液体中),这就制成了一个很有用的土仪器.将它分别放在盛有
 (2011•西宁)将适量的橡皮泥黏在铅笔的一端(能使铅笔竖直浮在液体中),这就制成了一个很有用的土仪器.将它分别放在盛有不同液体的杯中,静止时的情景如图所示.对于这个土仪器所运用的知识或用途,下列说法不正确的是( )
(2011•西宁)将适量的橡皮泥黏在铅笔的一端(能使铅笔竖直浮在液体中),这就制成了一个很有用的土仪器.将它分别放在盛有不同液体的杯中,静止时的情景如图所示.对于这个土仪器所运用的知识或用途,下列说法不正确的是( )
A.运用了二力平衡的知识
B.运用了物体的漂浮条件
C.用它可以比较不同液体密度的大小
D.用它直接可以测出液体密度的大小 illusion30001年前1
illusion30001年前1 -
 mengxinghun 共回答了6个问题
mengxinghun 共回答了6个问题 |采纳率83.3%解题思路:从图中可以看出,物体在不同液体中,浸入的深度不同,但始终漂浮,所以浮力相等,等于自身的重力,根据公式F浮=ρgV排可以比较液体密度的大小.物体在液体中漂浮,浮力等于重力,故A、B正确,不符合题意;
从图中可以看出,仪器在三种液体中排开液体的体积大小,根据公式F浮=ρgV排可以比较三种液体密度的大小,但无法直接读出液体密度的大小,故C正确,不符合题意;D错误,符合题意.
故选D.点评:
本题考点: 浮力的利用;二力平衡条件的应用;物体的浮沉条件及其应用.
考点点评: 本题考查二力平衡条件的应用和物体的漂浮条件以及浮力公式的应用,关键知道影响浮力大小的因素是液体的密度和物体排开液体的体积,还要知道物体漂浮时浮力等于自身重力.1年前查看全部
- 边长为1dm的正方形木块,密度为0.8×103kg/m3,放在一个底面积很大的平底容器中,容器中盛有深5cm,密度为1.
边长为1dm的正方形木块,密度为0.8×103kg/m3,放在一个底面积很大的平底容器中,容器中盛有深5cm,密度为1.1×103kg/m3的盐水,求木块受到的重力和浮力.
 liuyaozzz1年前1
liuyaozzz1年前1 -
 XUZENG1 共回答了26个问题
XUZENG1 共回答了26个问题 |采纳率88.5%解题思路:(1)知道木块的边长,求出木块的体积,根据密度公式和重力公式求出木块重;
(2)求出了木块重,利用漂浮条件求木块受到的浮力;(1)木块重:
G木=m木g=ρ木v木g=0.8×103kg/m3×(0.1m)3×10N/kg=8N,
(2)∵木块漂浮,
∴木块受到的浮力:
F浮=G木=8N,
答:(1)木块所受的重力为8N;
(2)木块受到的浮力为8N.点评:
本题考点: 重力的计算;浮力大小的计算.
考点点评: 浮力的计算题,往往要利用阿基米德原理与漂浮或悬浮的条件结合,由于木块静止在水面上,所以它所受到的浮力等于自身的重力,这是本题的关键.1年前查看全部
- 请快速回答.在实验课上老师带来了两杯果汁和一个空杯子,老师告诉同学们:“甲乙两个杯中盛有同样重量的果汁,已知甲杯中的果汁
请快速回答.
在实验课上老师带来了两杯果汁和一个空杯子,老师告诉同学们:“甲乙两个杯中盛有同样重量的果汁,已知甲杯中的果汁粉与水的重量比为1:2,乙杯中的果汁粉与水的重量比为1:3,现在我将它们全部倒入丙杯中,那么此时丙杯中的果汁粉与水的重量比为多少呢?”小明回答道:“(1+1):(2+3)=2:5.”你觉得小明的回答正确吗?为什么? 1大于21年前1
1大于21年前1 -
 诗音gg 共回答了15个问题
诗音gg 共回答了15个问题 |采纳率86.7%甲杯中含果汁粉:1÷(1+2)=1/3
乙杯中含果汁粉:1÷(1+3)=1/4
两杯果汁倒在一起放入丙杯中后,果汁粉与水的比是:(1/3+1/4)∶(2/3+3/4)
=7/12∶17/12
=7∶17
因此,小明的回答是错误的.1年前查看全部
- 一个圆柱形容器,底面内直径是30厘米,容器中盛有一些水,把一个铁块浸没在水中,水面上升了1厘米.这个铁块的体积是多少立方
一个圆柱形容器,底面内直径是30厘米,容器中盛有一些水,把一个铁块浸没在水中,水面上升了1厘米.这个铁块的体积是多少立方厘米
 oo变奏曲1年前3
oo变奏曲1年前3 -
 alex2001 共回答了13个问题
alex2001 共回答了13个问题 |采纳率69.2%S底面=3.14*(30/2)^2
=706.5cm^2
V铁块=S底面*h
=706.5*1=706.5cm^31年前查看全部
- 取四支试管,分别加入等量植物油,再分别加入A、B、C、D四组消化液,将试管放置在适宜的温度下,一段时间后再检测,发现盛有
取四支试管,分别加入等量植物油,再分别加入A、B、C、D四组消化液,将试管放置在适宜的温度下,一段时间后再检测,发现盛有下列哪组消化液的试管中植物油的量最少( )
A. 唾液、胃液、胰液
B. 胆汁、胰液、肠液
C. 胰液、肠液、唾液
D. 胃液、肠液、胰液 一灯明1年前3
一灯明1年前3 -
 coco_ing 共回答了21个问题
coco_ing 共回答了21个问题 |采纳率85.7%解题思路:植物油主要成分是脂肪,胆汁中虽不含消化酶,但胆汁能把脂肪乳化成脂肪微粒,促进脂肪的消化,然后根据各种消化液的消化作用分析回答.唾液中只含有唾液淀粉酶;胃液中只含胃蛋白酶;肠液、胰液中含有多种消化酶包括消化脂肪的酶;胆汁不含消化酶,但是胆汁对脂肪有乳化作用,使脂肪变成脂肪微粒,加大了与消化酶的接触面积,促进了脂肪的消化.植物油的主要成分是脂肪,脂肪只能在小肠内才能被消化.首先在小肠中胆汁的作用下,脂肪被变成脂肪微粒,加大了与消化酶的接触面积.而后再在肠液和胰液中酶的作用下,被消化成甘油和脂肪酸.因此选项B即有胆汁的乳化作用,胰液、肠液中还含有消化脂肪的酶,故植物油消化的最快,试管中剩下的植物油最少.
故选:B点评:
本题考点: 各种消化腺的位置和功能.
考点点评: 脂肪只能在小肠中消化,胆汁中不含有消化酶,对脂肪只能进行乳化.1年前查看全部
- 概率论与数理统计 设有两个口袋,甲中盛有1个白球9个黑球,乙中有6个白球 2个黑球.现从甲中任取2个放入乙中,求:(1)
概率论与数理统计
设有两个口袋,甲中盛有1个白球9个黑球,乙中有6个白球 2个黑球.现从甲中任取2个放入乙中,求:(1)从乙中再任取一个为白球的概率;(2)如果从乙中取的是白球,则该白球是来自于甲口袋的概率是多少? 儒之XUAN1年前1
儒之XUAN1年前1 -
 huzhiliang 共回答了11个问题
huzhiliang 共回答了11个问题 |采纳率90.9%1.设“从乙中再任取一个为白球”为事件A 从甲中取出的为1白1黑为事件B,取出的为2黑为事件C B和C是样本空间的一个划分,用全概率公式求P(A)
2.已知结果--从乙中取到的是白球,求原因--白球来自甲口袋,用贝叶斯公式求,照着公式代入即可1年前查看全部
- 一个量杯中盛有300毫升水,放入4个同样大的钢珠后,水面上升到刻度是400毫升的地方,
一个量杯中盛有300毫升水,放入4个同样大的钢珠后,水面上升到刻度是400毫升的地方,
每隔钢珠的体积是多少立方厘米? mnbbnm3491年前1
mnbbnm3491年前1 -
 叶动枝不动 共回答了14个问题
叶动枝不动 共回答了14个问题 |采纳率100%(400-300)/4=100/4=25立方厘米
答:每个钢珠的体积是25立方厘米1年前查看全部
- 30℃时,甲杯中盛有80克食盐饱和溶液,乙杯中盛有40克食盐饱和溶液.若各自蒸发掉20克水后再冷却到30℃时,甲杯中析出
30℃时,甲杯中盛有80克食盐饱和溶液,乙杯中盛有40克食盐饱和溶液.若各自蒸发掉20克水后再冷却到30℃时,甲杯中析出m1克食盐晶体,乙杯中析出m2克食盐晶体,则m1与m2的大小关系是(填大于、小于、相等)__________________.30℃时食盐的溶解度是_____________________(用含有m1或m2的式子表示).
是5m1,我要解题的思路和过程 kjwdszy1年前1
kjwdszy1年前1 -
 鱼翅 共回答了17个问题
鱼翅 共回答了17个问题 |采纳率88.2%1因为都是饱和溶液,质量分数相等,蒸发同样多的水,析出的晶体相同.所以相等.
2.因为20克水溶解m1克盐饱和,而都是饱和溶液,质量分数相等,所以设溶解度为x,
m2/(m2+20)=x/(x+100),解得x=5m1
(问一句,你也是初二的吗)1年前查看全部
- 小明想测一酒杯的密度,将它放入一盛有50毫升的水量筒内,小酒杯浮在水面,水面上升到59毫升,将小酒杯按入水中,小酒杯沉没
小明想测一酒杯的密度,将它放入一盛有50毫升的水量筒内,小酒杯浮在水面,水面上升到59毫升,将小酒杯按入水中,小酒杯沉没到量筒底部,水面下降到55毫升,请帮小明求出酒杯的密度
 a42334811年前1
a42334811年前1 -
 在雨中008 共回答了11个问题
在雨中008 共回答了11个问题 |采纳率100%v酒杯=55ml-50ml=5ml v排=59ml-50ml=9ml
漂浮时:F=G
F=ρ水V排g G=ρ酒杯V物g
ρ水V排g=ρ酒杯V物g
ρ酒杯=ρ水V排g/(V物g)
=1*9/5
=1.8g/cm 31年前查看全部
- 一容器中盛有浓度为45%的硫酸,若再加入16千克水,则浓度变为25%,这个容器内原来含有纯硫酸多少千克?
 北方的河ZY1年前4
北方的河ZY1年前4 -
 登台听雨 共回答了21个问题
登台听雨 共回答了21个问题 |采纳率71.4%解答(一):由于加水前后容器中所含纯硫酸的重量并没有改变,所以我们只需将加水前后容器中所含纯硫酸的量表示出来即可:
设容器中原有溶液x千克:则有
x·45%=(x+16%)·25%
x=20
∴ 容器中所含纯硫酸为20×45%=9(千克)
答:容器中原来含有纯硫酸9千克.
解答(二):设容器内原含有x千克纯硫酸.
依题意有:x÷45%=x÷25%-16
∴ x=9
答:容器内原含有纯硫酸9千克.1年前查看全部
大家在问
- 11.02升等于( )升,0.48平方米等于( )平方分米,7.9吨等于( )千克
- 2下列气候特点为我国东北地区所特有的是( )
- 3他花费一小时修理他的自行车 英文
- 4为什么月球上不能传播声音?因为声音不能在月球上传播.
- 5求雾都孤儿的英语梗概100词左右,求原创
- 6已知F 1 和F 2 分别是双曲线 x 2 a 2 - y 2 b 2 =1(a>0,b>0) 的左、右焦点,P是双曲线
- 7第三个字与第四个字相反的四字词语
- 8有发红光的昆虫吗?好像不是萤火虫
- 9根据米勒及其他学者的实验结果,可以对生命的起源作出怎样的推测
- 10I like to play ____________ my friends after class.
- 11注意,是把文言文翻译成白话文
- 12英译汉My heart will go on!
- 13如果进入超市看到超市里有很多商品你会想到那些成语?
- 14m的绝对值与负5m的大小关系是
- 15(2012•丹东模拟)关于如图所示各装置的叙述中,正确的是( )

