碱式碳酸铜的化学式写法?碱式碳酸铜(铜绿)的化学式是Cu2(OH)2CO3,但我听说也可以写成CuCO3·Cu(OH)2
 禾_本2022-10-04 11:39:541条回答
禾_本2022-10-04 11:39:541条回答碱式碳酸铜(铜绿)的化学式是Cu2(OH)2CO3,但我听说也可以写成CuCO3·Cu(OH)2.这样写对吗?如果对,是不是那些什么酸式盐,碱式盐都可以写出两种化学式?

已提交,审核后显示!提交回复
共1条回复
 panlinbo1982 共回答了26个问题
panlinbo1982 共回答了26个问题 |采纳率88.5%- 对,他不是酸式盐也不是碱式盐,是复式盐,只有复式盐可以这么写
- 1年前
相关推荐
- 碱式碳酸铜与稀硫酸反应得化学式是什么
 泮非涯1年前3
泮非涯1年前3 -
 santadanzig 共回答了19个问题
santadanzig 共回答了19个问题 |采纳率78.9%Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2!(箭头)1年前查看全部
- 碱式碳酸铜是一种绿色粉末,受热易分解为黑色的氧化铜,二氧化碳和水.某同学想验证其分解的产物的确有二氧化碳,于是将碱式碳酸
碱式碳酸铜是一种绿色粉末,受热易分解为黑色的氧化铜,二氧化碳和水.某同学想验证其分解的产物的确有二氧化碳,于是将碱式碳酸铜装入试管,并用带导管的橡皮塞将试管口塞紧后固定在铁架台上,然后将生成的气体通入澄清的石灰水里
①根据上述表述,该实验所用的主要仪器有______,______,______,______
②估计可能产生的现象是:_______,_______,_______.
③试验结束后,发现试管炸裂,可能的原因有(写三条):____________,____________,____________. 异域孤星1年前2
异域孤星1年前2 -
 LOVE雅戈尔 共回答了14个问题
LOVE雅戈尔 共回答了14个问题 |采纳率92.9%1、铁架台、大试管、酒精灯、烧杯.
2、大试管中绿色粉末变黑、澄清石灰水变浑浊、在大试管口部可以看见有液态物质出现.
3、(1)大试管口向上安装的,(2)大试管外部水没有擦干净,(3)加热时没有事先预热等.1年前查看全部
- 碱式碳酸铜是一种绿色粉末,受热易分解为黑色的氧化铜,二氧化碳和.
碱式碳酸铜是一种绿色粉末,受热易分解为黑色的氧化铜,二氧化碳和.
碱式碳酸铜是一种绿色粉末,受热易分解为黑色的氧化铜,二氧化碳和水.某同学想验证其分解的产物的确有二氧化碳,于是将碱式碳酸铜装入试管,并用带导管的橡皮塞将试管口塞紧后固定在铁架台上,然后将生成的气体通入澄清的石灰水里
①根据上述表述,该实验所用的主要仪器有______,______,______,______
②估计可能产生的现象是:_______,_______,_______.
③试验结束后,发现试管炸裂,可能的原因有(写三条):____________,____________,____________. YANFLYING1年前4
YANFLYING1年前4 -
 xiongyong2 共回答了16个问题
xiongyong2 共回答了16个问题 |采纳率87.5%1、铁架台、大试管、酒精灯、烧杯.
2、大试管中绿色粉末变黑、澄清石灰水变浑浊、在大试管口部可以看见有液态物质出现.
3、(1)大试管口向上安装的,(2)大试管外部水没有擦干净,(3)加热时没有事先预热等.1年前查看全部
- 碱式碳酸铜为什么是纯净物啊,它不是由氧化铜,水和二氧化碳组成的吗?
碱式碳酸铜为什么是纯净物啊,它不是由氧化铜,水和二氧化碳组成的吗?
是不是所有有化学公式的物质都是纯净啊?初中有哪些常见的纯净物和混合物 yanyundu1年前2
yanyundu1年前2 -
 爱晶的人 共回答了15个问题
爱晶的人 共回答了15个问题 |采纳率73.3%所有化学式的物质都是纯净物是对的,
纯净物有H2O,O2
混合物有空气等等1年前查看全部
- 碱式碳酸铜放入木炭中灼烧的化学方程式拜托各位大神
 haoliheng1年前1
haoliheng1年前1 -
 De_Novo 共回答了19个问题
De_Novo 共回答了19个问题 |采纳率89.5%Cu2(OH)2CO3=煅烧=2CuO+CO2(气体符号)+H2O CuO+C=加热=Cu+CO(气体符号)1年前查看全部
- 加热碱式碳酸铜生成44g 二氧化碳,则生成水的质量为多少克?
 望雨凝1年前1
望雨凝1年前1 -
 llgui81 共回答了20个问题
llgui81 共回答了20个问题 |采纳率100%Cu2(OH)2CO3,由分子式得,氢原子的物质的量是碳原子的2倍,由由于1mol水有2mol氢原子,所以水的物质的量和二氧化碳一样是1mol,质量也就是18克1年前查看全部
- 水 高锰酸钾 氯酸钾 碱式碳酸铜 这些物质在一定条件下分解 先生成氧化物的是什么
 wangxiaocong1年前1
wangxiaocong1年前1 -
 mathildaleon 共回答了20个问题
mathildaleon 共回答了20个问题 |采纳率95%碱式碳酸铜1年前查看全部
- 为什么碱式碳酸铜分子经过加热变成氧化铜 水 二氧化碳分子,而不是氧化铜 水 二氧化碳原子?
为什么碱式碳酸铜分子经过加热变成氧化铜 水 二氧化碳分子,而不是氧化铜 水 二氧化碳原子?
分子原子有什么区别? aifeidexuan7031年前1
aifeidexuan7031年前1 -
 暮夜炎霜 共回答了23个问题
暮夜炎霜 共回答了23个问题 |采纳率91.3%首先~没有氧化铜 水 二氧化碳原子,只有氧化铜 水 二氧化碳分子.化合物一定是分子.原子是构成元素的最小单元,是物质结构的一个层次,是化学变化中的最小微粒,可以直接构成物质,在化学变化中不可再分.分子是保持物质化学性质的一种微粒,是构成物质的一种微粒,在化学变化中可以再分.原子可以构成分子,分子在化学反应中可以分成原子.1年前查看全部
- 监视碳酸铜加热的化学方程式越快越好!碱式碳酸铜
 mayev1年前2
mayev1年前2 -
 daliangliang 共回答了24个问题
daliangliang 共回答了24个问题 |采纳率100%是碱式碳酸铜,在加热条件下
Cu2(OH)2CO3=2CuO+H2O+CO21年前查看全部
- 碱式碳酸铜受热分解之后 是生成氧化铜还是铜?
 重庆科科1年前1
重庆科科1年前1 -
 一片喜欢秋天叶子 共回答了14个问题
一片喜欢秋天叶子 共回答了14个问题 |采纳率100%生成氧化铜.从生成的化合物是黑色就可以证明这一点.1年前查看全部
- 碱式碳酸铜加热分解生成的氧化铜为什么不加沉淀符号
碱式碳酸铜加热分解生成的氧化铜为什么不加沉淀符号
氧化铜不溶于水,所以市应该沉淀,但为什么不加沉淀符号.
Cu2(OH)2CO3══2CuO+CO2↑+H2O 拉风抱抱牛1年前4
拉风抱抱牛1年前4 -
 goodluckyemin 共回答了23个问题
goodluckyemin 共回答了23个问题 |采纳率95.7%因为对于这个反应来说,反应前是固体,反应后的生成的固体就不用打符号了.同理,对于氢气和氯气生成氯化氢化学方程式中,“↑”和“↓”是我们用来表示生成物和反应物不同聚集状态的符号.但是学生常常不能正确使用.这里通过一些具体例子说明这两个符号的用法.
一、表示气体产物
1.凡是反应物中都是固态或液态,而反应后生成了气态物质,就应该在这种气态物质的化学式后边用“↑”符号标出.如:
2KClO32KCl+3O2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
2.如果反应物中也有气态物质,生成物虽为气体也不用“↑”表示.如:
S+O2SO2 CO+CuOCu+CO2
3.固态或液态反应物,在加热或高温条件下生成物呈气体逸出,也应用“↑”表示,并注明反应条件.如:
NaCl+H2SO4=NaHSO4+HCl↑
如果生成物虽为气体,但溶解在溶液中,没有逸出,则不用“↑”表示.
4.固态或液态反应物,如果生成物中有两种或两种以上气体的,均应分别用“↑”表示.如
2H2O2H2↑+O2↑
5.反应物中的气体物质一律不用“↑”表示.
二、表示不溶性固体生成物
1.反应在溶液中进行,生成不溶性沉淀物,则在这种沉淀物质的化学式后边用“↓”表示.如:
H2SO4+BaCl2=BaSO4↓+2HCl
这里生成的HC1存在于溶液中,不用“↑”表示.
Ca(HCO3)2CaCO3↓+CO2↑+H2O
生成物中的沉淀和气体分别用“↓”和“↑”表示.
2.如果反应物本身是固态,生成物虽是不溶性固体,也不用“↓”表示.
3.在溶液中反应的生成物虽然是可溶的,但在特定的条件下呈晶体析出,也应用“↓”表示.如合成氨联合法生成纯碱有这样的反应:
4.反应物中的不溶性固体,也一律不用“↓”表示. 气体,氯化氢就不用打气体上升符号了.1年前查看全部
- 硫酸铜和碱式碳酸铜均可溶于HCL转化为氧化铜.在高温下这两种化合物均能生成氧化铜.溶解28.4g的上述混合
 corneliusy1年前1
corneliusy1年前1 -
 skycoke219 共回答了17个问题
skycoke219 共回答了17个问题 |采纳率64.7%铜守恒
第一步里所有铜最后都以CuCl2存在 所有Cl都来自于盐酸
根据盐酸的物质的量可以求出Cl的物质的量 即 CL有1*0.5=0.5mol Cu有0.25mol
这个铜便是所以的铜的物质的量
在根据铜的物质的量=氧化铜的物质的量 求出氧化铜的质量
消耗1mol/L盐酸500mL→Cl- 0.5mol→CuCl2 0.25mol→Cu 0.25mol
→CuO 0.25mol→CuO 20g1年前查看全部
- 加热碱式碳酸铜m克一会,过一段时间后冷却,称的固体质量减少了n克,生成二氧化碳的质量是多少?
 hiemails1年前3
hiemails1年前3 -
 赤_橙 共回答了15个问题
赤_橙 共回答了15个问题 |采纳率93.3%碱式碳酸铜加热分解Cu2(OH)2CO3=加热=2CuO+CO2+H2O
碱式碳酸铜物质的量为 m/221 ,由化学方程式可知,二氧化碳物质的量也是吗、221,水也是
44*m/221+18*m/222=n
化简,得31m /111=n
二氧化碳质量为 44m/222=22n/311年前查看全部
- 初中化学加热碱式碳酸铜得到固体的质量比碱式碳酸铜质量小,为什么?
 穿短裤的蚂蚁1年前4
穿短裤的蚂蚁1年前4 -
 pig牟牟 共回答了15个问题
pig牟牟 共回答了15个问题 |采纳率86.7%生成物中有 二氧化碳和水汽挥发,所以质量变小.
化学变化中,若反应前后质量发生变化,则为有沉淀生成或气体溢出.如果反应在很密封的情况下就不会有质量减少的情况了1年前查看全部
- 碱式碳酸铜加热,为什么固体质量减两次?
碱式碳酸铜加热,为什么固体质量减两次?
见到一题:碱式碳酸铜的受热分解的剩余固体的图像,先是碱式碳酸铜2.22g到t1时,固体还剩1.66g,然后过了很长一段时间图像是平的,到t2时减到了1.44g WHY? 11223331年前2
11223331年前2 -
 伤心的蓝天 共回答了24个问题
伤心的蓝天 共回答了24个问题 |采纳率91.7%第一阶段是Cu2(OH)2CO3=2CuO+CO2↑+H2O↑
第二阶段4CuO=2Cu2O+O2↑1年前查看全部
- 氧化镁,红磷,金,氯化钠,二氧化氮,水,空气,澄清石灰水,氧气,碱式碳酸铜
氧化镁,红磷,金,氯化钠,二氧化氮,水,空气,澄清石灰水,氧气,碱式碳酸铜
这十个.属于金属单质的是_____.属于非金属单质的是______.属于化合物的是_____.属于氧化物的是_____.属于混合物的是____.属于纯净物的是_____. gardena1年前3
gardena1年前3 -
 黍子也谈 共回答了17个问题
黍子也谈 共回答了17个问题 |采纳率70.6%第一个空:金;
第二个空:红磷、氧气;
第三个空:氧化镁、氯化钠、二氧化氮、水、碱式碳酸铜;
第四个空:氧化镁、二氧化氮、水;
第五个空:空气、澄清石灰水;
第六个空:氧化镁,红磷,金,氯化钠,二氧化氮,水,氧气,碱式碳酸铜.1年前查看全部
- 将碱式碳酸铜放入火红的木炭中灼烧,出现红色粉末
将碱式碳酸铜放入火红的木炭中灼烧,出现红色粉末
碱式碳酸铜会分解为氧化铜,那么氧化铜为什么会被碳还原,而不是一氧化碳?一氧化碳还原氧化铜应该更容易啊!
c和cuo反应条件的高温是要多少度?木炭燃烧能达到那个温度吗? JDY东东1年前1
JDY东东1年前1 -
 bba60000 共回答了19个问题
bba60000 共回答了19个问题 |采纳率73.7%碱式碳酸铜分解产物有氧化铜,二氧化碳
二氧化碳和碳反应生成一氧化碳
一氧化碳还原氧化铜生成铜
同时生成二氧化碳
一氧化碳是全过程的中间产物
可视为氧化铜和碳反应
不是木炭直接和氧化铜反应,
c+co2=2co总可以达到吧
co+cuo=cu+co2
两式叠加一下c+cuo=cu+co2,我说1molco2相当于催化剂你懂了吧 有催化剂就不用原来那么高的条件了1年前查看全部
- (3)碱式碳酸铜 →氧化铜+水+二氧化碳 是什么反应
 浪子寒云1年前1
浪子寒云1年前1 -
 hotandhot 共回答了18个问题
hotandhot 共回答了18个问题 |采纳率94.4%受热易分解成二氧化碳、水和氧化铜.正二价的铜离子有毒.由于存在氢氧根,所以呈碱性,易与酸反应.1年前查看全部
- 属于纯净物和混合物的是哪些下列物质中①氯酸钾、②海水、③碱式碳酸铜、④冰水混合物、⑤部分分解的氯酸钾粉末⑥澄清石灰水,其
属于纯净物和混合物的是哪些
下列物质中①氯酸钾、②海水、③碱式碳酸铜、④冰水混合物、⑤部分分解的氯酸钾粉末⑥澄清石灰水,其中属于纯净物的是__________;属于混合物的是_______________. 我想爱你1年前1
我想爱你1年前1 -
 lkxjlkj2l3kjlkfa 共回答了20个问题
lkxjlkj2l3kjlkfa 共回答了20个问题 |采纳率95%其中属于纯净物的是_①氯酸钾__、③碱式碳酸铜__、④冰水混合物_____;
属于混合物的是__②海水____、⑤部分分解的氯酸钾粉末⑥澄清石灰水_________.1年前查看全部
- (2013•福建)根据质量守恒定律可知,碱式碳酸铜〔Cu2(OH)2CO3〕受热分解,不可能得到的物质是( )
(2013•福建)根据质量守恒定律可知,碱式碳酸铜〔Cu2(OH)2CO3〕受热分解,不可能得到的物质是( )
A.CuO
B.H2O
C.CO2
D.HCl mdcgmhh1681年前1
mdcgmhh1681年前1 -
 liyang110 共回答了16个问题
liyang110 共回答了16个问题 |采纳率93.8%解题思路:根据质量守恒定律进行分析,化学反应前后元素的种类不变.根据碱式碳酸铜的化学式可以看出,碱式碳酸铜含有铜、氢、碳、氧四种元素,根据质量守恒定律可知生成物中也只含有这四种元素,因此氧化铜、水和二氧化碳可能是生成物,而氯化氢中含有氯元素,不可能是生成物.
故选:D.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 根据题目提供的信息,对问题做出正确的判断,培养学生提取正确有用信息的能力.1年前查看全部
- 碱式碳酸铜和盐酸的反应!..在半小时内1拜托..
碱式碳酸铜和盐酸的反应!..在半小时内1拜托..
碱式碳酸铜和盐酸的反应后有水生成,但如何证明生成的水不是盐酸中的水呢? 游走kk1年前3
游走kk1年前3 -
 晚起的人被鸟吃 共回答了19个问题
晚起的人被鸟吃 共回答了19个问题 |采纳率94.7%碱式碳酸铜与氯化氢气体反应,也会生成使白色的硫酸铜变蓝色的水的1年前查看全部
- 现有①液氮 ②空气 ③碱式碳酸铜 ④高锰酸钾 ⑤二氧化锰 ⑥水银 ⑦冰水混合物 ⑧氯酸钾,其中属于单质的有
现有①液氮 ②空气 ③碱式碳酸铜 ④高锰酸钾 ⑤二氧化锰 ⑥水银 ⑦冰水混合物 ⑧氯酸钾,其中属于单质的有 属于化合物的有 属于含氧化合物的有_________,属于氧化物的有 ,含有氧分子的有 。(以上均填序号)  i415331年前1
i415331年前1 -
 lipansl 共回答了19个问题
lipansl 共回答了19个问题 |采纳率94.7%①⑥;③④⑤⑦⑧;③④⑤⑦⑧;⑤⑦;②1年前查看全部
- 碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2
碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2(OH)2CO3
2CuO+H2O+CO2↑.现将一定量的碱式碳酸铜和铜的粉末放在容器里,在空气中用酒精灯充分加热后冷却,称量,发现加热前后固体的质量相等.据此计算原混合粉末中Cu2(OH)2CO3的质量.△ . 顽固的笑话1年前1
顽固的笑话1年前1 -
 打假派 共回答了23个问题
打假派 共回答了23个问题 |采纳率87%解题思路:根据题意,可知:铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等.铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等;
设原混合物质量为100g,其中碱式碳酸铜的质量为x,则铜的质量为100g-x,生成的水蒸汽和二氧化碳的质量为y;
则根据题意有:
①Cu2(OH)2CO3
△
.
CuO+H2O+CO2↑
222 18+44=62
xy
则[222/x=
62
y],解得y=[62x/222]
②2Cu+O2
△
.
2CuO
12832
100g-xy
[128/100g−x=
32
y],解得y=
32(100g−x)
128
所以得[62x/222]=
32(100g−x)
128,解得x≈47.2g,故
47.2g
100g×100%=47.2%
答:原混合粉末中Cu2(OH)2CO3的质量分数约为47.2%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题是对利用化学方程式计算的考查题,解题的关键是对反应前后质量变化的分析,属于基础性知识考查题.1年前查看全部
- 研究型学习小组欲测定某铜矿中碱式碳酸铜[Cu2(OH)2CO3]的质量分数.现称取15g该铜矿样品放入烧杯中,在逐滴加入
研究型学习小组欲测定某铜矿中碱式碳酸铜[Cu2(OH)2CO3]的质量分数.现称取15g该铜矿样品放入烧杯中,在逐滴加入稀盐酸至恰好完全反应(假如铜矿中的杂质不予稀盐酸反应,也不溶于水),称得烧杯中剩余物质的质量为85.8g.试求:
(1)铜矿中碱式碳酸铜的质量分数
(2)所得溶液中溶质的质量分数.
(反应的化学方程式为:Cu2(OH)2CO3+4HCl=2CuCl2+ CO2↑+3H2O)
这个的答案是:
依题意,生成CO2的质量为:73g+15g-85.8g=2.2g(1分)
设铜矿中碱式碳酸铜的质量为x,生成氯化铜质量为y(0.
Cu2(OH)2CO3+4HCl=2CuCl2+ CO2↑+3H2O
222 270 44
X y 2.2g
= x=11.1g(1分)
= y=13.5g(1分)
(1)铜矿中碱式碳酸铜的质量分数为:×100%=74%(1分)
(2)所得溶液中溶质的质量分数为:×100%=16.5%(1分)
答:铜矿中碱式碳酸铜的质量分数为74%,所得溶液中溶质的质量分数为16.5%(0.
可是原题里面没有告诉你盐酸滴进去的质量啊是不是题目漏了盐酸的质量? 阿ty诺1年前1
阿ty诺1年前1 -
 王丽虎 共回答了19个问题
王丽虎 共回答了19个问题 |采纳率94.7%你说的对,原题里面是漏了盐酸的质量.从答案可以看出,盐酸的质量受73克.
依题意,生成CO2的质量为:73g+15g-85.8g=2.2g1年前查看全部
- 碱式碳酸铜和HCL反应的方程式写下方程式~并说下现象
 窗外的梧桐1年前1
窗外的梧桐1年前1 -
 深圳小民甲 共回答了16个问题
深圳小民甲 共回答了16个问题 |采纳率87.5%2CUCO3+2HCL=2CUCL+2HO2+CO2 固体溶解 放出二氧化碳1年前查看全部
- 硫酸铜和碳酸氢钠反应这两种盐的溶液能相互反应吗?生成物是什么? 难么硫酸铜和碳酸钠能反应生成碳酸铜沉淀吗?那么碱式碳酸铜
硫酸铜和碳酸氢钠反应
这两种盐的溶液能相互反应吗?生成物是什么? 难么硫酸铜和碳酸钠能反应生成碳酸铜沉淀吗?那么碱式碳酸铜是否能通过碳酸铜转化来?
 牛红红啊1年前1
牛红红啊1年前1 -
 weya168 共回答了21个问题
weya168 共回答了21个问题 |采纳率90.5%2CuSO4+Na2CO3+2H2O=Cu2(OH)2CO3 +Na2SO4+H2SO4 只能得到浅蓝色的碱式碳酸酮 一般中学阶段就认为生成CuCO3 CuSO4+Na2CO3 ==CuCO3 +Na2SO41年前查看全部
- 向碱式碳酸铜中加入稀盐酸试验中,实验现象是产生大量气体还是大量气泡
 a22691年前3
a22691年前3 -
 不信邪才怪 共回答了16个问题
不信邪才怪 共回答了16个问题 |采纳率93.8%Cu2(OH)2CO3 + 4HCL=======2CuCL2 + 3H2O +CO2(气体)
溶液变为蓝色,有气泡产生.1年前查看全部
- 铜生锈变成碱式碳酸铜 ,为什么铁生锈不会变成碱式碳酸铁
 自由空间3601年前1
自由空间3601年前1 -
 qdzhb2008 共回答了14个问题
qdzhb2008 共回答了14个问题 |采纳率92.9%分子活性不同1年前查看全部
- 碱式碳酸铜是什么,请具体把其性质,反应等介绍一下,最好详细点.
 南方笨熊1年前3
南方笨熊1年前3 -
 smileboy88 共回答了8个问题
smileboy88 共回答了8个问题 |采纳率75%中文名:碱式碳酸铜,俗称孔雀石、铜绿. 英文名:basic cupric carbonate 化学式:Cu2(OH)2CO3 分子量:221.12 密度:3.85g/cm³ 相对密度:3.8525 折光率:1.655.1.875.1.909 外...1年前查看全部
- 请问一下碱式碳酸铜的受热分解?是不是Cu2(OH)2CO3→CuO+H2O+CO2+O2呢?(我是没有配平的)没有氧气么
请问一下碱式碳酸铜的受热分解?
是不是Cu2(OH)2CO3→CuO+H2O+CO2+O2呢?(我是没有配平的)
没有氧气么,那CO2+O2+H2O+CuO→Cu2(OH)2CO3
又是怎么样的呢?
(不好意思啊,有些想要提前自学一些,为后面打一点基础~) lulu10131年前7
lulu10131年前7 -
 bbhff 共回答了14个问题
bbhff 共回答了14个问题 |采纳率92.9%Cu2(OH)2CO3=2CuO+CO2+H2O
"CO2+O2+H2O+CuO→Cu2(OH)2CO3"这个反应也不对
是氧气与铜先反应,缓慢作用,变成CuO,再变成 Cu2(OH)2CO3的1年前查看全部
- 某学校化学课外活动小组,对铜制品生锈很很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为
某学校化学课外活动小组,对铜制品生锈很很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为
Cu2(OH)2CO3.他们在探究中发现,铜绿受热分解后,除生成二氧化碳和水蒸气外,试管中还有一些黑色粉末状固体.为了更清楚地了解这种黑色粉末,小明和小娜准备通过实验探究,进一步分析黑色固体的组成,并验证产生的气体:
(1)提出问题:黑色固体是什么?
(2)猜想与假设: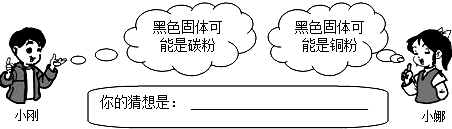
(3)设计实验方案:
向试管中的黑色固体滴加足量的______(填化学式)溶液,充分反应后,观察固体的溶解情况和所得溶液的颜色;
(4)现象与结论:
小刚和小娜经过实验之后,都给自己的猜想做了正确的评价.如果你的猜想是正确的话,实验现象应为:______.
(5)若用如图所示装置验证两种气体生成物(无水硫酸 铜遇水变蓝),应将生成的混合气体先通过______装置,.当将气体通入装置A进行验证,气流应从______口通入.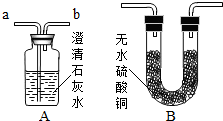
 闷灯儿1年前1
闷灯儿1年前1 -
 总不该又重名了吧 共回答了22个问题
总不该又重名了吧 共回答了22个问题 |采纳率95.5%解题思路:(2)根据质量守恒定律结合小刚和小娜的猜想来进行推测;
(3)根据推测黑色的粉末可以选择酸来进行判断该黑色粉末的组成;
(4)根据自己所作出的猜想来进行判断,得出实验现象;
(5)验证是否产生了水可以用无水硫酸铜,但是要最先进行验证,以防在后续操作中吸收了水分,而干扰了实验现象.(2)碱式碳酸铜中含有碳元素、铜元素、氧元素和氢元素,根据质量守恒定律结合小娜和小刚的推测,可以判断该黑色粉末为氧化铜和碳的混合物;
(3)根据黑色粉末的组成,可以选择稀硫酸、稀盐酸或是稀硝酸来进行鉴别,如果得到蓝色溶液则说明该黑色粉末为氧化铜,若黑色粉末不溶解则说明为碳粉;
(4)若黑色粉末为氧化铜和碳粉,当加入稀硫酸时氧化铜要溶解而生成蓝色溶液,但是碳粉不反应,即如果观察到黑色粉末部分溶解,则说明我们刚才的判断是正确的;
(5)无水硫酸铜吸收水后变为蓝色,所以在验证水时通常用无水硫酸铜,但是为了防止在后续的实验中引入水蒸气而干扰实验,所以要先验证水的存在,然后再来验证二氧化碳的存在,在验证二氧化碳即通过B装置时,要从长管即a管进入.
故答案为:(2)如图
(3)H2SO4(HCl、HNO3也可);
(4)黑色粉末部分溶解,溶液由无色变成蓝色;
(5)B;a;点评:
本题考点: 实验探究物质的组成成分以及含量;猜想与事实验证;常见气体的检验与除杂方法;碳的化学性质.
考点点评: 熟练掌握质量守恒定律的实质,能够根据质量守恒定律来判断反应后生成的物质,记住三种常见的黑色粉末:碳、氧化铜和二氧化锰.1年前查看全部
- 加热碱式碳酸铜会有黑色物质生成么?
加热碱式碳酸铜会有黑色物质生成么?
那加热氯酸钾呢 维嘉思U21年前3
维嘉思U21年前3 -
 好B都让狗ee了 共回答了26个问题
好B都让狗ee了 共回答了26个问题 |采纳率80.8%会,分解生成CuO
Cu2(OH)2CO3==2CuO+H2O+CO2
加热氯酸钾一般无黑色物质生成,除非你用了二氧化锰催化剂,因为二氧化锰是黑色的
直接加热氯酸钾:
4KClO3==(加热)==3KClO4+KCl
有二氧化锰催化:
2KClO3==(MnO2,加热)==2KCl+3O21年前查看全部
- 碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2
碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2(OH)2CO3
2CuO+H2O+CO2↑.现将一定量的碱式碳酸铜和铜的粉末放在容器里,在空气中用酒精灯充分加热后冷却,称量,发现加热前后固体的质量相等.据此计算原混合粉末中Cu2(OH)2CO3的质量.△ . 飘翎叶1年前1
飘翎叶1年前1 -
 潘恬恬 共回答了18个问题
潘恬恬 共回答了18个问题 |采纳率94.4%解题思路:根据题意,可知:铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等.铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等;
设原混合物质量为100g,其中碱式碳酸铜的质量为x,则铜的质量为100g-x,生成的水蒸汽和二氧化碳的质量为y;
则根据题意有:
①Cu2(OH)2CO3
△
.
CuO+H2O+CO2↑
222 18+44=62
xy
则[222/x=
62
y],解得y=[62x/222]
②2Cu+O2
△
.
2CuO
12832
100g-xy
[128/100g−x=
32
y],解得y=
32(100g−x)
128
所以得[62x/222]=
32(100g−x)
128,解得x≈47.2g,故
47.2g
100g×100%=47.2%
答:原混合粉末中Cu2(OH)2CO3的质量分数约为47.2%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题是对利用化学方程式计算的考查题,解题的关键是对反应前后质量变化的分析,属于基础性知识考查题.1年前查看全部
- 研究型学习小组欲测定某铜矿中碱式碳酸铜[Cu2(OH)2CO3]的质量分数.现称取15g该铜矿样品放入烧杯中,在逐滴加入
研究型学习小组欲测定某铜矿中碱式碳酸铜[Cu2(OH)2CO3]的质量分数.现称取15g该铜矿样品放入烧杯中,在逐滴加入稀盐酸至恰好完全反应(假如铜矿中的杂质不予稀盐酸反应,也不溶于水),消耗73g盐酸,称得烧杯中剩余物质的质量为85.8g.
试求:
(1)铜矿中碱式碳酸铜的质量分数
(2)所得溶液中溶质的质量分数.(反应的化学方程式为:Cu2(OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O) 圣斗士-一辉1年前1
圣斗士-一辉1年前1 -
 garylineker 共回答了14个问题
garylineker 共回答了14个问题 |采纳率92.9%解题思路:(1)先算出二氧化碳气体的质量,然后写出化学方程式并代入二氧化碳气体的质量计算出碱式碳酸铜的质量,最后计算铜矿中碱式碳酸铜的质量分数.
(2)根据化学方程式计算出氯化铜的质量,然后计算出反应后溶液的质量,最后计算出溶液中溶质的质量分数.(1)依题意,CO2的质量=73克+15克-85.8克=2.2克.设铜矿中碱式碳酸铜的质量为X,生成氯化铜质量为Y.
Cu2(OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O
222 27044
XY 2.2克
[222/44]═[X/2.2克]
得:X=11.1克
[270/44]═[Y/2.2克]
得:Y=13.5克
∴铜矿中碱式碳酸铜的质量分数为=[11.1g/15g]×100%=74%.
(2)根据(1)的计算可知,反应后溶液的质量=85.8克-(15克-11.1克)=81.9克.
∴所得溶液中溶质的质量分数=[13.5克/81.9克]×100%═16.5%.
答:铜矿中碱式碳酸铜的质量分数为74%;所得溶液中溶质的质量分数为16.5%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 掌握化学方程式的计算格式和规范性,本题的易错点:反应后溶液的质量要减去矿石的杂质.1年前查看全部
- 寻找化学式.有限制的氧气,金刚石.氨气.氯化氢,氧化镁,二氧化硫.碳酸氢铵.碱式碳酸铜.水的化学分式分别是什么麻烦高手辛
寻找化学式.有限制的
氧气,金刚石.氨气.氯化氢,氧化镁,二氧化硫.碳酸氢铵.碱式碳酸铜.水的化学分式分别是什么
麻烦高手辛苦下 已经不存在1年前1
已经不存在1年前1 -
 wangyijun14 共回答了7个问题
wangyijun14 共回答了7个问题 |采纳率85.7%O2 C NH3 HCl MgO SO2 NH4HCO3 CuCO3·Cu(OH)2或Cu2(OH)2CO3 H2O1年前查看全部
- (2014•青岛一模)碱式碳酸铜和氯气都是用途广泛的化工原料.
(2014•青岛一模)碱式碳酸铜和氯气都是用途广泛的化工原料.
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备碱式碳酸铜,其制备过程如下:
已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
①氯酸钠的作用是______;物质 Cu(OH)2 Fe(OH)2 Fe(OH)3 开始沉淀pH 4.2 5.8 1.2 完全沉淀pH 6.7 8.3 3.2
②反应A后调节溶液的pH范围应为______.
③第一次过滤得到的产品洗涤时,如何判断已经洗净?______.
④造成蓝绿色产品中混有CuO杂质的原因是______.
(2)某学习小组在实验室中利用图所示装置制取氯气并探究其性质.
①实验室用二氧化锰和浓盐酸加热制取氯气,所用仪器需要检漏的有______.
②若C中品红溶液褪色,能否证明氯气与水反应的产物有漂白性,说明原因______.
此时B装置中发生反应的离子方程式是______.
③写出A溶液中具有强氧化性微粒的化学式______.若向A溶液中加入NaHCO3粉末,会观察到的现象是______. yy85121年前1
yy85121年前1 -
 panjpalang 共回答了19个问题
panjpalang 共回答了19个问题 |采纳率94.7%解题思路:(1)①工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备碱式碳酸铜,流程分析,加入氯酸钠的作用是氧化剂作用,氧化亚铁离子为铁离子易于除去;
②依据图表数据分析,铁离子全部沉淀,铜离子不沉淀的PH范围为3.2-4.2;
③检验洗涤是否干净,设计实验检验滤液中是否含有氯离子证明是否洗涤干净;
④蓝绿色产品中混有CuO杂质可能的元婴是氢氧化铜咋温度较高会发生分解生成氧化铜;
(2)①实验室用二氧化锰和浓盐酸加热制取氯气的仪器用途和使用方法,需要检漏的仪器是分液漏斗;
②依据氯气、次氯酸都是强氧化剂都可以使品红试液褪色分析;溴化亚铁溶液中通入过量氯气反应生成氯化铁和溴单质;
③A为氯水,溶液中具有氧化性的微粒为氯气、次氯酸、次氯酸根;氯水中 加入碳酸氢钠溶液会和盐酸反应生成二氧化碳气体.(1)①工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备碱式碳酸铜,流程分析,加入氯酸钠的作用是氧化剂作用,氧化亚铁离子为铁离子,调节溶液PH易于把铁离子沉淀除去,
故答案为:将Fe2+氧化成Fe3+并最终除去;
②流程分析可知,分离除杂的方法是通过调节溶液PH大于3.2,小于4.2,使铁离子全部沉淀完全,铜离子不沉淀,达到分离的目的,故答案为:3.2-4.2;
③沉淀表面会含有氯化钠溶液,设计实验检验是否含有氯离子的方法可以检验是否洗涤干净,实验设计为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净,故答案为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净;
④造成蓝绿色产品中混有CuO杂质的原因是B步骤温度过高,生成氢氧化铜会分解生成氧化铜,故答案为:反应B的温度过高;
(2)①根据实验室用二氧化锰和浓盐酸加热制取氯气的仪器用途和使用方法,需要检漏的仪器是带玻璃活塞的分液漏斗,故答案为:分液漏斗;
②若C中品红溶液褪色,可能是氯气本身也具有氧化性,能使品红褪色,也可以是氯气和水反应生成的次氯酸具有氧化性使品红褪色,不能证明氯气与水反应的产物有漂白性,过量氯气通过溴化亚铁溶液发生氧化还原反应,亚铁离子和溴离子全部被氧化生成氯化铁和溴单质,反应的离子方程式为:2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2;
故答案为:不能证明,因为Cl2也有氧化性,此实验无法确定是Cl2还是HClO漂白;2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2;
③A溶液是氯水溶液,存在化学平衡,Cl+H2O=HCl+HClO,溶液中具有强氧化性微粒的化学式Cl2、HClO、ClO-;加入碳酸氢钠溶液和氯水中的盐酸反应生成二氧化碳气体,HCO3-+H+=H2O+CO2↑,现象有无色气体生成,故答案为:Cl2、HClO、ClO-;有无色气体产生.点评:
本题考点: 物质的分离、提纯的基本方法选择与应用;氯、溴、碘的性质实验.
考点点评: 本题考查了实验探究物质分离方法和物质性质的分析判断,实验室制备气体的过程分析和氯气性质的应用判断,掌握物质性质是关键,题目难度中等.1年前查看全部
- 写出下列物质的化学式碳酸碳酸钠碱式碳酸铜碳酸氢钠碳酸钙碳酸氢钙氯化氢氯气氯化钾二氧化锰氯酸氯酸钾二氧化氯氧化二氯硝酸硝酸
写出下列物质的化学式
碳酸
碳酸钠
碱式碳酸铜
碳酸氢钠
碳酸钙
碳酸氢钙
氯化氢
氯气
氯化钾
二氧化锰
氯酸
氯酸钾
二氧化氯
氧化二氯
硝酸
硝酸钾
硝酸钡
硝酸铵
硝酸铜
硝酸汞
硝酸银
硫酸
硫酸铵
硫酸氢铵
硫酸钡
硫酸铝
硫酸铁
硫酸亚铁
磷酸
磷酸钠
磷酸氢钠
磷酸氢二钠
磷酸氢铵
磷酸钙
磷酸二铵
氮气
硫磺
白磷
金刚石
氦气
二氧化硅
氖气
二氧化氮
氩气
氧化铁
氧化铝
氢氧根离子
硫酸根离子
碳酸根离子
硝酸根离子
铵根离子 lcon011年前2
lcon011年前2 -
 lewis_xuxu 共回答了16个问题
lewis_xuxu 共回答了16个问题 |采纳率100%碳酸 H2CO3
碳酸钠 Na2CO3
碱式碳酸铜 Cu2(OH)2CO3
碳酸氢钠 NaHCO3
碳酸钙 CaCO3
碳酸氢钙 Ca(HCO3)2
氯化氢 HCl
氯气 Cl2
氯化钾 KCl
二氧化锰 MnO2
氯酸 HClO3
氯酸钾 KClO3
二氧化氯 ClO2
氧化二氯 Cl2O
硝酸 HNO3
硝酸钾 KNO3
硝酸钡 Ba(NO3)2
硝酸铵 NH4NO3
硝酸铜 Cu(NO3)2
硝酸汞 Hg(NO3)2
硝酸银 AgNO3
硫酸 H2SO4
硫酸铵 (NH4)2SO4
硫酸氢铵 NH4HSO4
硫酸钡 BaSO4
硫酸铝 Al2(SO4)3
硫酸铁 Fe2(SO4)3
硫酸亚铁 FeSO4
磷酸 H3PO4
磷酸钠 Na3PO4
磷酸氢钠 NaH2PO4
磷酸氢二钠 Na2HPO4
磷酸氢铵 NH4H2PO4
磷酸钙 Ca3(PO4)2
磷酸二铵 (NH4)2HPO4
氮气 N2
硫磺 S
白磷 P
金刚石 C
氦气 He
二氧化硅 SiO2
氖气 Ne
二氧化氮 NO2
氩气 Ar
氧化铁 Fe2O3
氧化铝 Al2O3
氢氧根离子 OH^-
硫酸根离子 SO4^2-
碳酸根离子 CO3^2-
硝酸根离子 NO3^-
铵根离子 NH4^+1年前查看全部
- 下列物质中由不同分子构成的是碱式碳酸铜硫酸铜高锰酸钾高锰酸钾水溶液
 庆大1年前3
庆大1年前3 -
 央如 共回答了22个问题
央如 共回答了22个问题 |采纳率100%高锰酸钾水溶液.里面有高锰酸钾分子,还有水分子.是一种混合物.
其他三种各自都是纯净物,只有一种分子组成.1年前查看全部
- 碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2
碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2(OH)2CO3
2CuO+H2O+CO2↑.现将一定量的碱式碳酸铜和铜的粉末放在容器里,在空气中用酒精灯充分加热后冷却,称量,发现加热前后固体的质量相等.据此计算原混合粉末中Cu2(OH)2CO3的质量.△ . dolphin24281年前1
dolphin24281年前1 -
 海底琥珀 共回答了16个问题
海底琥珀 共回答了16个问题 |采纳率93.8%解题思路:根据题意,可知:铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等.铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等;
设原混合物质量为100g,其中碱式碳酸铜的质量为x,则铜的质量为100g-x,生成的水蒸汽和二氧化碳的质量为y;
则根据题意有:
①Cu2(OH)2CO3
△
.
CuO+H2O+CO2↑
222 18+44=62
xy
则[222/x=
62
y],解得y=[62x/222]
②2Cu+O2
△
.
2CuO
12832
100g-xy
[128/100g−x=
32
y],解得y=
32(100g−x)
128
所以得[62x/222]=
32(100g−x)
128,解得x≈47.2g,故
47.2g
100g×100%=47.2%
答:原混合粉末中Cu2(OH)2CO3的质量分数约为47.2%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题是对利用化学方程式计算的考查题,解题的关键是对反应前后质量变化的分析,属于基础性知识考查题.1年前查看全部
- 一道有难度的初中化学题一份因严重锈蚀而部分变成碱式碳酸铜的铜片,将其磨成粉末在空气中灼烧成氧化铜,完全反应后剩余固体质量
一道有难度的初中化学题
一份因严重锈蚀而部分变成碱式碳酸铜的铜片,将其磨成粉末在空气中灼烧成氧化铜,完全反应后剩余固体质量的变化情况( )
A.减少30% B.增加30% C不变 D无法判断 鱼不语1年前1
鱼不语1年前1 -
 bivhc 共回答了22个问题
bivhc 共回答了22个问题 |采纳率90.9%这题是要算出范围的.
Cu2(OH)2CO3===2CuO+H20+CO2
222 160
a x
x=160/222 a
2Cu+O2===2CuO
128 160
b y
y=160/128 b
所以生成物质量x+y约等于0.72a+1.25b
当a=0的时候 x+y的值是a+b的值的1.25倍,也就是增重25%
当b=0的时候 x+y的值是a+b的值的0.72倍,也就是减少28%
结论就是剩余固体的质量比反应之前的减少28%~增重25%
所以AB选项就都不对了.
在这个范围的选项之后不变.
这种竞赛题就是算范围的.1年前查看全部
- 此反应的文字表达式加热碱式碳酸铜,绿色粉末变成黑色,有氧化铜生成,管壁出现水珠,有水生成,能使澄清石灰水变浑浊,有二氧化
此反应的文字表达式
加热碱式碳酸铜,绿色粉末变成黑色,有氧化铜生成,管壁出现水珠,有水生成,能使澄清石灰水变浑浊,有二氧化碳生成. loncinhui1年前2
loncinhui1年前2 -
 琼海溜健哥 共回答了20个问题
琼海溜健哥 共回答了20个问题 |采纳率90%碱式碳酸铜(加热)==氧化铜+水+二氧化碳1年前查看全部
- 孔雀石的主要成分为碱式碳酸铜[Cu2 (OH)2CO3],化学小组的同学利用 Cu2 (OH)2CO3+4HCl=2Cu
孔雀石的主要成分为碱式碳酸铜[Cu2 (OH)2CO3],化学小组的同学利用 Cu2 (OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O,测定某孔雀石中碱式碳酸铜的质量分数.称取该铜矿样品30g于烧杯中,逐滴加入溶质质量分数为10%的稀盐酸至恰好完全反应,共用去稀盐酸146g(假设铜矿中的其他成分不与稀盐酸反应,也不溶于水).则该孔雀石样品中碱式碳酸铜的质量分数是多少?反应后所得溶液中溶质的质量分数是多少?
 不爱理你1年前1
不爱理你1年前1 -
 歪脑袋 共回答了19个问题
歪脑袋 共回答了19个问题 |采纳率100%解题思路:根据碱式碳酸铜与稀酸反应的方程式,由稀盐酸溶液质量和溶质质量分数求出碱式碳酸铜的质量,再除以孔雀石样品的质量即可得出碱式碳酸铜的质量分数,根据碱式碳酸铜与稀盐酸反应的方程式可知,反应后所得溶液中溶质是氯化铜,根据质量守恒定律反应后溶液的质量等于盐酸溶液的质量加上参加反应的碱式碳酸铜的质量减去生成的二氧化碳的质量,根据氯化铜和溶液的质量就可求出反应后所得溶液中溶质的质量分数.设孔雀石样品中碱式碳酸铜的质量为x,生成的二氧化碳的质量为y
Cu2(OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O
222 14627044
X146g×10%y
[222/146=
x
146g×10%] X=22.2g
[146/44=
146g×10%
y] Y=27g
该孔雀石样品中碱式碳酸铜的质量分数是:[22.2/30]×100%=74%
反应后所得溶液中溶质的质量分数是[27/146+22.2−4.4]×100%=16.5%
答:孔雀石样品中碱式碳酸铜的质量分数是74%,反应后所得溶液中溶质的质量分数是16.5%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题主要考查了根据化学方程式的计算,解题的关键是会根据质量守恒定律由参加反应的碱式碳酸铜和稀盐酸的质量以及生成的二氧化碳的质量求出反应后生成的溶液的质量.1年前查看全部
- 急吖一:书写下列化学方程式 1.碱式碳酸铜生成二氧化碳,水和氧化铜 2.高锰酸钾受热分解生成锰酸钾,二氧化锰和氧气 3.
急吖
一:书写下列化学方程式
1.碱式碳酸铜生成二氧化碳,水和氧化铜
2.高锰酸钾受热分解生成锰酸钾,二氧化锰和氧气
3.铁和硫酸反映成硫酸亚铁和氢气
4.铝和盐酸反应生成氯化铝和氧气
5.氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠
6.碳酸钙呵盐酸反应生成氯化钙,二氧化碳和水
7.二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水
8.水在通电条件下生成氢气和氧气
9.二氧化碳呵硫酸反应生成硫酸铁和水 hongzhenfeng1年前1
hongzhenfeng1年前1 -
 pi1215 共回答了18个问题
pi1215 共回答了18个问题 |采纳率83.3%1.Cu2(OH)2CO3=加热=2CuO+CO2+H2O
2.2KMnO4=加热=K2MnO4+MnO2+O2
3.Fe+H2SO4=FeSO4+H2
4.2Al+6HCl=2AlCl3+3H2
5.2NaOH+CuSO4=Cu(OH)2+Na2SO4
6.CaCO3+2HCl=CaCl2+H2O+CO2
7.CO2+Ca(OH)2=CaCO3+H2O
8.2H2O=电解=2H2+O2
9.不反应1年前查看全部
- 教教我吧我是个初中生 要化学竞赛了 可是我不会配平酸式盐与碱式盐.教教我吧比如碱式碳酸铜cu2(oh)2co3 是怎么配
教教我吧
我是个初中生 要化学竞赛了 可是我不会配平酸式盐与碱式盐.教教我吧
比如碱式碳酸铜cu2(oh)2co3 是怎么配平的.那两个2怎么来的
我还是不懂嘞! du7e1年前2
du7e1年前2 -
 达令 共回答了26个问题
达令 共回答了26个问题 |采纳率84.6%这是在写化学式,不是配平
铜是正二价,氢氧根是负一价,碳酸根是负二价
如果直接是碳酸铜的话就是CuCO3,但加上了氢氧根,因为氢氧根和碳酸根的化合价都是负的,所以不会再加上碳酸根,所以铜的数量会增加,一个铜正好对两个氢氧根,所以再加一个铜和两个氢氧根,所以是Cu2(OH)2CO3.就是这么来的.1年前查看全部
- 碱式碳酸铜和碳酸氢纳的化学式化学式看清楚 不要一大堆东西
 爱就让你幸福1年前1
爱就让你幸福1年前1 -
 C风雨飘摇 共回答了17个问题
C风雨飘摇 共回答了17个问题 |采纳率88.2%cu(oh)2co3
nahco31年前查看全部
- 请教下列反应方程式:三氧化硫和水 氧化钠和水 碱式碳酸铜加热 铁和硝酸汞溶液 碳酸氢钙溶液和盐酸
请教下列反应方程式:三氧化硫和水 氧化钠和水 碱式碳酸铜加热 铁和硝酸汞溶液 碳酸氢钙溶液和盐酸
下列物质在水中的电离方程式
碳酸钠 硫酸 硝酸 硝酸铜 碳酸氢钙 硝酸铵 硫酸铝 高锰酸钾 氯酸钾 氢氧化钙 磷酸钠 硝酸钡 氯化铁 氯化铵 口牙1年前2
口牙1年前2 -
 wadeliu 共回答了20个问题
wadeliu 共回答了20个问题 |采纳率100%SO3+H2O=H2SO4
Na2O+H2O=2NaOH
Cu2(OH)2CO3△=2CuO+H2O+CO2↑
Fe+Hg(NO3)2=Hg+Fe(NO3)2
Ca(HCO3)2+2HCl=CaCl2+2H2O+2CO2↑
在水中电离方程式
Na2CO3=Na+ + co32-(钠离子+碳酸根离子)
其余依次写就行(金属离子+酸根离子),注意氯化铵中金属离子是铵根离子1年前查看全部
- 硫酸铜、碱式碳酸铜、氯化铜的颜色区别?
硫酸铜、碱式碳酸铜、氯化铜的颜色区别?
为什么眼镜框上的铜锈是绿色的而硫酸铜溶液时蓝色的?更奇怪的是氯化铜溶液就然是看浓度的?具体的临界浓度值是多少的时候颜色才会发生明显变化 小妖feeling1年前2
小妖feeling1年前2 -
 孩子气给的勇气 共回答了25个问题
孩子气给的勇气 共回答了25个问题 |采纳率92%硫酸铜白色,遇水变蓝、
碱式碳酸铜,就是铜绿(铜生锈后的产物),所以是绿色.
氯化铜不了解.1年前查看全部
- 碱式碳酸铜 孔雀石 铜绿 Cu2(OH)2CO3是混合物?
碱式碳酸铜 孔雀石 铜绿 Cu2(OH)2CO3是混合物?
为什么混合物能用化学式表示?
还有,写出相关化学反应方程式 yimeng13201年前2
yimeng13201年前2 -
 寒星飘零 共回答了15个问题
寒星飘零 共回答了15个问题 |采纳率86.7%1、碱式碳酸铜、Cu2(OH)2CO3为纯净物(单一物质为纯净物),孔雀石、铜绿为混合物.一般来讲,自然界天然有的物质,大多为混合物.少数物质能视为纯净物(如黄金).此处既然碱式碳酸铜可以受热分解,那么在自然环境中,温度较高,同样会分解,铜绿或孔雀石则会含有部分杂质氧化铜.同时,大部分铜器本身就含有其他金属,生锈后其他金属依旧存在,因而不能视为纯净物.
2、混合物如果进行化学反应,其各组分,有参与反应的,有不参与反应的,参与反应的各种物质会有相应的化学式,如果各组分化学反应无相互间的干扰,则是多个化学反应方程式.如只有单一物质参与反应,则只写参与反应物质的化学反应方程式.那么不参与反应的物质则不写入化学反应方程式中.
3、Cu2(OH)2CO3--->2CuO+CO2+H2O1年前查看全部
大家在问
- 1如何证明简谐运动的图像是正弦(余弦)函数图像?
- 2ade,我的蟋蟀们!ade,我的覆盆子们和木莲们
- 3正弦和余弦函数的图像有什么关系
- 4英语中主语,谓语,表语,宾语,宾语补足语,定语,状语等的意思
- 5英语中,主语、谓语、宾语、表语、定语、状语的意义...
- 6I like spring best 同义句
- 71+1=几?答案必须是个文字,不是数字!
- 8写十七题并解释一下为什么这样做不然不给钱.
- 9热力学中什么叫过程量
- 10英语中什么词修饰什么词?太多了,
- 11小奥找规律2.3.7.18.47.( ).( )
- 12He is wearing glasses为什么wear加ing
- 131+1=?只可以回答一个数字!或者你能明白我提问题的目的!
- 14地轴和地球公转轨道面总是保持多少度的夹角?
- 15四字词语 慷()激昂
