称量氢氧化钠固体放纸片上还是放烧杯上.
 要ggID2022-10-04 11:39:541条回答
要ggID2022-10-04 11:39:541条回答如题.

已提交,审核后显示!提交回复
共1条回复
 pingxi 共回答了11个问题
pingxi 共回答了11个问题 |采纳率90.9%- 因氢氧化钠有腐蚀性,所以不能在称盘或称量纸上直接称量,需放在已知质量的小烧杯内或表面皿上称量.
- 1年前
相关推荐
- 31.6克高锰酸钾加热一段时间后冷却,称量剩余固体的质量为30克,根据质量守恒定律判定.反应生成氧气为?
 kik211年前2
kik211年前2 -
 丑的自然 共回答了12个问题
丑的自然 共回答了12个问题 |采纳率91.7%根据质量守恒定律,高锰酸钾的质量等于反应后物质的总质量.反应后的物质是固体和气体组成的.所以气体的质量为1.6g1年前查看全部
- 现在有12个小球,外形和材质无明显区别,但其中一个与另外11个质量不同,不知道是轻还是重.现给你一个天平,允许称量三次,
现在有12个小球,外形和材质无明显区别,但其中一个与另外11个质量不同,不知道是轻还是重.现给你一个天平,允许称量三次,要你判断出是哪一个球,并且要明确判断出这个球与其他球相比是轻还是重?
 阿MO少爷1年前1
阿MO少爷1年前1 -
 假正经kk 共回答了17个问题
假正经kk 共回答了17个问题 |采纳率100%5岁就不玩了
将十二个球编号为1-12.
第一次,先将1-4号放在左边,5-8号放在右边.
1.如果右重则坏球在1-8号.
第二次将2-4号拿掉,将6-8号从右边移到左边,把9-11号放
在右边.就是说,把1,6,7,8放在左边,5,9,10,11放在右边.
1.如果右重则坏球在没有被触动的1,5号.如果是1号,
则它比标准球轻;如果是5号,则它比标准球重.
第三次将1号放在左边,2号放在右边.
1.如果右重则1号是坏球且比标准球轻;
2.如果平衡则5号是坏球且比标准球重;
3.这次不可能左重.
2.如果平衡则坏球在被拿掉的2-4号,且比标准球轻.
第三次将2号放在左边,3号放在右边.
1.如果右重则2号是坏球且比标准球轻;
2.如果平衡则4号是坏球且比标准球轻;
3.如果左重则3号是坏球且比标准球轻.
3.如果左重则坏球在拿到左边的6-8号,且比标准球重.
第三次将6号放在左边,7号放在右边.
1.如果右重则7号是坏球且比标准球重;
2.如果平衡则8号是坏球且比标准球重;
3.如果左重则6号是坏球且比标准球重.
2.如果天平平衡,则坏球在9-12号.
第二次将1-3号放在左边,9-11号放在右边.
1.如果右重则坏球在9-11号且坏球较重.
第三次将9号放在左边,10号放在右边.
1.如果右重则10号是坏球且比标准球重;
2.如果平衡则11号是坏球且比标准球重;
3.如果左重则9号是坏球且比标准球重.
2.如果平衡则坏球为12号.
第三次将1号放在左边,12号放在右边.
1.如果右重则12号是坏球且比标准球重;
2.这次不可能平衡;
3.如果左重则12号是坏球且比标准球轻.
3.如果左重则坏球在9-11号且坏球较轻.
第三次将9号放在左边,10号放在右边.
1.如果右重则9号是坏球且比标准球轻;
2.如果平衡则11号是坏球且比标准球轻;
3.如果左重则10号是坏球且比标准球轻.
3.如果左重则坏球在1-8号.
第二次将2-4号拿掉,将6-8号从右边移到左边,把9-11号放
在右边.就是说,把1,6,7,8放在左边,5,9,10,11放在右边.
1.如果右重则坏球在拿到左边的6-8号,且比标准球轻.
第三次将6号放在左边,7号放在右边.
1.如果右重则6号是坏球且比标准球轻;
2.如果平衡则8号是坏球且比标准球轻;
3.如果左重则7号是坏球且比标准球轻.
2.如果平衡则坏球在被拿掉的2-4号,且比标准球重.
第三次将2号放在左边,3号放在右边.
1.如果右重则3号是坏球且比标准球重;
2.如果平衡则4号是坏球且比标准球重;
3.如果左重则2号是坏球且比标准球重.
3.如果左重则坏球在没有被触动的1,5号.如果是1号,
则它比标准球重;如果是5号,则它比标准球轻.
第三次将1号放在左边,2号放在右边.
1.这次不可能右重.
2.如果平衡则5号是坏球且比标准球轻;
3.如果左重则1号是坏球且比标准球重
幼儿奥数的题目嘛!1年前查看全部
- 说明用托盘天平称量给定药品的质量和称取一定质量的药品的操作过程的区别
 大比阿东1年前1
大比阿东1年前1 -
 _KJJ_ 共回答了20个问题
_KJJ_ 共回答了20个问题 |采纳率75%称量给定药品的质量就是把药品放到左盘,加砝码,移动游标 再读数
称取一定质量的药品就是先放砝码移动游标到需要的质量是加药品知道天平平衡1年前查看全部
- 下列实验操作正确的是( )A.用向上排空气法收集氢气B.称量固体药品时,将称量物放在托盘天平的右盘C.观察液体体积时,
下列实验操作正确的是( )
A.用向上排空气法收集氢气
B.称量固体药品时,将称量物放在托盘天平的右盘
C.观察液体体积时,视线与量筒内液体的凹液面最低处保持水平
D.为加速过滤用玻璃棒搅拌漏斗中的过滤液 7pk30mp51年前1
7pk30mp51年前1 -
 冰若雨 共回答了27个问题
冰若雨 共回答了27个问题 |采纳率92.6%解题思路:A、氢气的密度小于空气的密度,不能用向上排空气法;
B、托盘天平要左物右码;
C、观察液体体积时过高或过低,都会使读数不准确;
D、过滤试验中的玻璃棒是引流,不是搅拌.A、氢气的密度小于空气的密度,应用向下排空气法收集.故A选项不正确;
B、用托盘天平称量药品时要左物右码,将称量物放在托盘天平的右盘是不对的.故B选项不正确;
C、观察液体体积时,视线与量筒内液体的凹液面最低处保持水平,过高过低都会使读数不准确.故选项C正确;
D、过滤试验中的玻璃棒的作用是引流,若过滤用玻璃棒搅拌漏斗中的过滤液,会使固体物质进入滤液内,使过滤效果不好.故D选项不正确;
故选C点评:
本题考点: 过滤的原理、方法及其应用;测量容器-量筒;称量器-托盘天平;常用气体的收集方法.
考点点评: 本题考查试验中的常见错误现象,以此引起同学们对试验中细小问题的重视.1年前查看全部
- 某学生称量12.25g氯酸钾并用少量高锰酸钾代替二氧化锰做催化剂制取氧气,待充分反应后12.25g氯酸钾全部分解制得氧气
某学生称量12.25g氯酸钾并用少量高锰酸钾代替二氧化锰做催化剂制取氧气,待充分反应后12.25g氯酸钾全部分解制得氧气4.96g,则该生所用高锰酸钾多少克?
 禁止cool1年前1
禁止cool1年前1 -
 悠哈苹果 共回答了19个问题
悠哈苹果 共回答了19个问题 |采纳率89.5%解题思路:根据氯酸钾分解的化学方程式和质量守恒定律氯酸钾中的氧元素全部生成了氧气,可以计算出12.25g氯酸钾所生成的氧气的质量;共收集到氧气4.96g减去12.25g氯酸钾所生成的氧气的质量就是高锰酸钾分解所生成的氧气质量;根据高锰酸钾分解所生成的氧气质量可计算出加入高锰酸钾的质量.12.25g氯酸钾分解所生成的氧气的质量为x:2KClO3MnO2.△2KCl+3O2↑245 9612.25g...
点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题主要考查有关化学方程式的计算,要明确发生的反应和各物质间的质量关系是解题的关键.1年前查看全部
- 称量氢氧化钠装在烧杯中能防止吸水吗
 镇镇1年前4
镇镇1年前4 -
 ociq 共回答了10个问题
ociq 共回答了10个问题 |采纳率100%不能用纸装氢氧化钠是因为他吸水后会沾在纸上,当你溶解时就会造成质量减小,用烧杯装氢氧化钠只要迅速就可以减少吸水,最重要的是溶解时不会造成太大的损失1年前查看全部
- 一道关于第一宇宙速度的物理题! 在某个半径为R=10七次方m的行星表面,对于一个质量m=1kg的砝码,用弹簧称量,其重
一道关于第一宇宙速度的物理题!
在某个半径为R=10七次方m的行星表面,对于一个质量m=1kg的砝码,用弹簧称量,其重力的大小G=1.6N.请计算该星球的第一宇宙速度V1是多大!
哥们好像你的算数错了! hq老狼1年前3
hq老狼1年前3 -
 sevenP 共回答了20个问题
sevenP 共回答了20个问题 |采纳率95%v1=(gR)½
mg=mv²÷R
g=G÷m=1.6N/kg
v1=(1.6×10³×10³×10)½
=0.4×10³=400m/s1年前查看全部
- 测量盐水的密度,已知空烧杯的质量是49.5克,在烧杯内装入一定质量的盐水后,放在天平上称量,当天平平衡时,右盘内砝码如图
 测量盐水的密度,已知空烧杯的质量是49.5克,在烧杯内装入一定质量的盐水后,放在天平上称量,当天平平衡时,右盘内砝码如图1所示,则被测盐水的质量是______克.将烧杯内盐水倒入量筒,量筒内液体如图2所示,则被测盐水的体积是______厘米3,盐水的密度是______千克/米3.
测量盐水的密度,已知空烧杯的质量是49.5克,在烧杯内装入一定质量的盐水后,放在天平上称量,当天平平衡时,右盘内砝码如图1所示,则被测盐水的质量是______克.将烧杯内盐水倒入量筒,量筒内液体如图2所示,则被测盐水的体积是______厘米3,盐水的密度是______千克/米3.  oosujun1年前1
oosujun1年前1 -
 tianshi5 共回答了26个问题
tianshi5 共回答了26个问题 |采纳率80.8%解题思路:(1)烧杯和盐水的质量等于砝码的质量加游码对应的刻度值,然后减去空烧杯的质量,即为盐水的质量;
(2)根据量筒的分度值读出盐水的体积,根据密度公式求出盐水的密度.(1)由图示可知,烧杯和剩下的盐水总质量:m=100g+10g=110g,量筒内盐水的质量:m=110g-49.5g=60.5g;(2)量筒的分度值为5ml,盐水的体积:V=55ml=55cm3,盐水的密度:ρ盐水=mV=60.5g55cm3=1.1g/cm3=1.1×103kg/m...
点评:
本题考点: 密度的计算.
考点点评: 本题考查了盐水密度的计算,关键是读出盐水的体积和质量,计算过程要注意单位的换算.1年前查看全部
- 如题.碳酸氢钠和碳酸钠的混合物100克和固体氢氧化钠20克混合加热,充分反应后,冷却·干燥称量剩余固体为95.5克.求原
如题.
碳酸氢钠和碳酸钠的混合物100克和固体氢氧化钠20克混合加热,充分反应后,冷却·干燥称量剩余固体为95.5克.求原混合物中碳酸钠的质量分数 xiangsp1年前1
xiangsp1年前1 -
 tvi54a 共回答了21个问题
tvi54a 共回答了21个问题 |采纳率81%质量守恒,反应后的物质应该全部是碳酸钠,乘上钠的质量分数再除以钠的摩尔质量就是钠的物质的量,再减去氢氧化钠中钠的物质的量,剩下的就是碳酸钠和碳酸氢钠中的钠,设碳酸钠和碳酸氢钠各有Xmol、Ymol,则2X+Y=算出的钠的物质的量,106X+84Y=100,把这个二元一次方程组解出来就行了1年前查看全部
- 一个物体用弹簧秤称物重,弹簧秤实数为4,9N.问能否用称量范围为200g的天平称量?
 panxianting1年前1
panxianting1年前1 -
 图书馆里的女孩 共回答了12个问题
图书馆里的女孩 共回答了12个问题 |采纳率100%200g的物体重力=200÷1000×9.8=1.96N<4.9N
所以:
不可以用称量范围为200g的天平称量.
很高兴为您解答,祝你学习进步!
如果我的回答对你有帮助,请及时选为满意答案,谢谢~~1年前查看全部
- NaHCO3和Na2CO3的混合物100g和NaOH固体20.0g混合加热,充分反应后,冷却、干燥、称量,剩余固体为95
NaHCO3和Na2CO3的混合物100g和NaOH固体20.0g混合加热,充分反应后,冷却、干燥、称量,剩余固体为95.5g,求原混合物中Na2CO3的质量分数.
 龙龙_1年前3
龙龙_1年前3 -
 格子之外 共回答了18个问题
格子之外 共回答了18个问题 |采纳率83.3%解题思路:首先判断NaHCO3反应的情况,根据反应的方程式计算.发生的反应有:NaHCO3+NaOH=Na2CO3+H2O;2NaHCO3
Na2CO3+CO2↑+H2O.△ .发生的反应有:NaHCO3+NaOH=Na2CO3+H2O ①
2NaHCO3
△
.
Na2CO3+CO2↑+H2O ②
若只发生反应①,则固体减重△m≤9g,现固体减重24.5g,故反应①②均发生.
设原固体中有xmolNaHCO3,则反应①固体减重为9g,反应②固体减重为[1/2](x-0.5)×(44+18)g
则有:9+[1/2](x-0.5)×(44+18)=24.5,
解得x=1,
故m(NaHCO3)=84g,m(Na2CO3)=16g,
w(Na2CO3)=16%,
答:原混合物中Na2CO3的质量分数为16%.点评:
本题考点: 有关混合物反应的计算.
考点点评: 本题考查混合物的计算,题目难度中等,注意判断NaHCO3反应的情况为解答该题的关键.1年前查看全部
- 怎样用500克的称量称几千克的大头针的根数
 zyez1年前1
zyez1年前1 -
 lon7687548 共回答了19个问题
lon7687548 共回答了19个问题 |采纳率89.5%称出100根的重量,再分批称出总重量,除以100根的重量,再乘以100就是总根数了1年前查看全部
- 知道了基准物质的称取质量 应该怎样确定称量范围呢?
知道了基准物质的称取质量 应该怎样确定称量范围呢?
比如我算出的理论Na2CO3 质量为2.00g, 那每次标定称取基准物的重量应在什么范围内呢?谢谢高手了啊! Think_Different1年前1
Think_Different1年前1 -
 xxxysjb 共回答了20个问题
xxxysjb 共回答了20个问题 |采纳率90%通常在正负5%吧,也就是称1.9-2.1g1年前查看全部
- 如图是托盘天平上的标尺,尺上分度值是()游码所对的刻度值是()2,称量一枚大头针质量,应先称量()个大头针的总质量m克,

如图是托盘天平上的标尺,尺上分度值是()游码所对的刻度值是()
2,称量一枚大头针质量,应先称量()个大头针的总质量m克,那么一枚大头针质量为() sadghzsergkj1年前2
sadghzsergkj1年前2 -
 zfll_2000 共回答了17个问题
zfll_2000 共回答了17个问题 |采纳率100%分度值0.2g,图示值为2.2g
第二题称量50个或100个(可以更多),一枚那就是m/50g(m/100g)1年前查看全部
- 现有8个形状个体大小都一样铜球,其中一个比那7个轻一些,要求用天枰称量两次找出那个轻的.
 http老头1年前1
http老头1年前1 -
 awpliang 共回答了22个问题
awpliang 共回答了22个问题 |采纳率81.8%先取6个球,一边放三个
如果两边相等,就把剩下两个比较一下就可以了
如果两边不相等,把较轻的一边取两个球比较.相等,则剩下的一个为要找的球,不相等,则较轻的为要找的球.1年前查看全部
- 菌落总数测定时,样品稀释时怎么保证它的无菌称量?需要在超净工作台上称量吗?
 羽灵絮语1年前1
羽灵絮语1年前1 -
 pellw 共回答了16个问题
pellw 共回答了16个问题 |采纳率93.8%在超净工作台或者无菌室内操作,以无菌操作取一定量(一般是25g)到含有无菌稀释液的均质袋中(一般是225ml无菌生理盐水),均质.1年前查看全部
- 物理秤砣上粘了一块泥,用此杆秤称量物体时,秤杆的读数
 bb_ok1年前6
bb_ok1年前6 -
 zc_Zs 共回答了29个问题
zc_Zs 共回答了29个问题 |采纳率96.6%小
秤砣变重了,比如说是十斤的秤砣,现在变成是11斤,你称一个物体正好压着秤砣,你读数是十斤,实际上他是十一斤,所以说读数小1年前查看全部
- 测量一块形状不规则的小石块的密度.在称量其质量前.调节天平,发现指针左偏,放上小石块和砝码后,天平平衡.测量读取小石块浸
测量一块形状不规则的小石块的密度.在称量其质量前.调节天平,发现指针左偏,放上小石块和砝码后,天平平衡.测量读取小石块浸没后水的体积,则测量结果会( )填偏大,偏小,相等
AB两种物质制成的小球,VA=VB=V,已知两球质量MA:MB=3:2,两种物质密度PA=PB=5:3,若两球中只有一个是空心的.则下列结论正确的是( )
A B 球是空心且 V空=1/9V
B B 球是空心且 V空=1/10V
C A 球是空心且 V空=1/9V
D A 球是空心且 V空=1/10V
需要解释.希望大家积极回答. rgwxf1年前3
rgwxf1年前3 -
 丁建勋 共回答了15个问题
丁建勋 共回答了15个问题 |采纳率93.3%1.偏大
天平左偏说明左边偏重,有天平摆放规则左物右砝可知,为求平衡,右边砝码需偏重,故测得石块的质量偏大.
又由密度=质量/体积可知,密度偏大.
2.D
A 球是空心且 V空=1/10V
若两球均为实心,由VA=VB=V PA=PB=5:3可知,MA:MB=5:3
但实际情况是MA:MB=3:2<5:3,
故A球空心.
剩下两个选项就比较好选了,我用的是代入法,因为比较好理解.
设D对,则有V非空=9/10V
由(VA非空*PA)/(VB*PB)=5:3=MA:MB可知,D是对的.
把C选项代入则不成立.
个人意见,供参考.1年前查看全部
- 有一架天平,其最大称量200克能否用他来称一块体积为150立方厘米的铜块质量
有一架天平,其最大称量200克能否用他来称一块体积为150立方厘米的铜块质量
有计算过程,原因 ccf12151年前4
ccf12151年前4 -
 wenli125 共回答了28个问题
wenli125 共回答了28个问题 |采纳率92.9%不行的,如果我没记错铜的密度8.9乘以十的三次千克每立方米
150立方厘米有150×8.9=1335克1年前查看全部
- 将125g由C和CuO组成的混合物充分加热,其中C完全反应,反应结束后将剩余物冷却,称量得固体(Cu和CuO的混合物)质
将125g由C和CuO组成的混合物充分加热,其中C完全反应,反应结束后将剩余物冷却,称量得固体(Cu和CuO的混合物)质量为120.6g.求反应前混合物中CuO的质量分数.
 一块空地1年前1
一块空地1年前1 -
 crclever045 共回答了23个问题
crclever045 共回答了23个问题 |采纳率87%解题思路:因为碳完全反应所以反应前后固体的质量之差即为碳与氧化铜反应生成的二氧化碳质量,利用该值即可依据方程式求出混合物中碳的质量,进而可求氧化铜的质量以及氧化铜的质量分数;C完全反应 所以生成CO2的质量为125g-120.6g=4.4g
设混合物中碳的质量为x
C+2CuO
高温
.
CO2+2Cu
12 44
x 4.4g
[12/x=
44
4.4g]
x=1.2g
所以原混合物中碳的质量为1.2克,氧化铜的质量为125g-1.2g=123.8g,反应前混合物中CuO的质量分数为[123.8g/125g]×100%=99.04%.
答:反应前混合物中CuO的质量分数为99.04%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题是对化学方程式计算的考查题,解题的关键是掌握固体的质量变化即是生成的二氧化碳的质量.1年前查看全部
- 加热10克的高锰酸钾制取氧气,经过一段时间后,称量剩余固体的质量为9.68克.计算生成多少了氧气?
 迷恋花妖1年前3
迷恋花妖1年前3 -
 chaojiaguang 共回答了37个问题
chaojiaguang 共回答了37个问题 |采纳率89.2%根据质量守恒定律,生成氧气的质量是:10g-9.68g==0.32g
物质的量是0.32g/(32g/mol)==0.01mol1年前查看全部
- 有关托盘天平的问题某同学用托盘天平称量物质时,所称的质量比实际质量多0.5克,那么该同学在操作上造成误差的原因可能是(
有关托盘天平的问题
某同学用托盘天平称量物质时,所称的质量比实际质量多0.5克,那么该同学在操作上造成误差的原因可能是( )
A.整个操作中,错放砝码与物质的位置
B.若其他操作正确,只有未称量时,指针静止时偏右
C.若其他操作正确,只有未称量时,指针静止时偏左
D.若其他操作正确,只有天平调零时,游码未回零处
答案说是C,我觉得不对
个人觉得有好几个答案的,请不要像一楼那样就说一句不知道所云的话.请好好看看,再列出答案,如果加上原因当然更好了.
我之所以说C不对,是因为我觉得ACD都是对了. lenovose1年前2
lenovose1年前2 -
 元吉77777 共回答了17个问题
元吉77777 共回答了17个问题 |采纳率88.2%不知道出这道题的人想考什么,这题有什么意义?
若指针不是指中间,还能继续称吗?有这样的人?
就事论事:如果是C,那么未加称量物时,已偏左,当平衡时,砝码已多了.若是称某一样品的质量,则比实际质量多了.
若是称取一定质量的试剂时,实际质量应该是少了.(即砝码质量之和比实际质量多).
所以是C.1年前查看全部
- 天平称量的相对误差为±0.1%,称量:(1)0.5g; (2)1g; (3)2g.试计算绝对误差各为多少
 2632979751年前1
2632979751年前1 -
 记忆大街 共回答了13个问题
记忆大街 共回答了13个问题 |采纳率100%绝对误差 = 测量值 - 真值
相对误差 =( 测量值 - 真值) / 真值 = 绝对误差 /真值
所以绝对误差 = 真值*相对误差 分别为 0.05 .0.1 0.2 +_1年前查看全部
- 某学生在实验室用托盘天平称一质量为4.9g的固体(1g以下用游码),该学生称量的结果却是5.1g其原因可能
某学生在实验室用托盘天平称一质量为4.9g的固体(1g以下用游码),该学生称量的结果却是5.1g其原因可能
A天平没有调平,指针偏右时就开始称量.B.砝码放在左盘,称量物质放在右盘.C计算质量时未将游码计算在内 D不能确定 急速酷客1年前1
急速酷客1年前1 -
 rr零距离 共回答了21个问题
rr零距离 共回答了21个问题 |采纳率95.2%选 D
若天平没有调平,指针偏左时就开始称量.
砝码放在左盘,称量物质放在右盘.1年前查看全部
- 称量几顿甚至十几吨(如汽车)质量的工具是什么,它所能称得最大质量是多少
 米楼1年前1
米楼1年前1 -
 xy82587395 共回答了17个问题
xy82587395 共回答了17个问题 |采纳率82.4%地称,根据力矩平衡来算
具体办法是,先估算出汽车重心的大概位置,然后将前轮压到地秤上,得到一个示数,然后以后轮为转轴,用力矩平衡Fx=Gy来计算(F为示数,x为前轮到后轮距离,G为汽车重力,y为重心到后轮距离),就可以得到G值了
目前看来,地秤没有最大限制1年前查看全部
- 用含有少量氯化钙的氯化钠固体,配制质量分数为 10%的氯化钠溶液,设计如图所示操作方案,根据下图回答: ⑴称量粗盐样品1
用含有少量氯化钙的氯化钠固体,配制质量分数为 10%的氯化钠溶液,设计如图所示操作方案,根据下图回答: 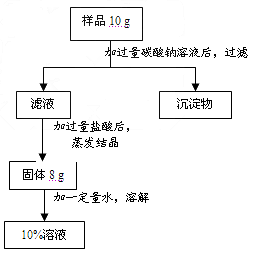
⑴称量粗盐样品10克时,托盘天平右盘放___________ 。
⑵过滤时,过滤器内的液面要低于___________。
⑶蒸发操作应在__________中加热,待出现___________时停止加热。
⑷用化学方程式表示过量盐酸的作用___________
⑸配制10%氯化钠溶液时,加水的量是_________克,配制溶液时应在_________中进行。 铁血亦柔情1年前1
铁血亦柔情1年前1 -
 hole 共回答了18个问题
hole 共回答了18个问题 |采纳率88.9%⑴砝码
⑵滤纸边缘
⑶蒸发皿;较多量固体
⑷Na 2 CO 3 +2HCl==2NaCl +H 2 O +CO 2 ↑
⑸72;烧杯1年前查看全部
- 把H2通入装有50g氧化铜的试管中发生反应,反应一段时间后,称量试管中剩余物质的质量46.8g.
把H2通入装有50g氧化铜的试管中发生反应,反应一段时间后,称量试管中剩余物质的质量46.8g.
求发生反应的氧化铜的质量为多少 showhlx1年前1
showhlx1年前1 -
 fengliguantou 共回答了14个问题
fengliguantou 共回答了14个问题 |采纳率85.7%CuO + H2 ==Cu + H2O △m
80 16
x 50-46.8
x=16g
∴发生反应的氧化铜的质量为16g
❤您的问题已经被解答~(>^ω^1年前查看全部
- 现有氯酸钾和二氧化锰的混合物30g,加热完全反应后,冷却称量剩余物体的质量为20.4g
现有氯酸钾和二氧化锰的混合物30g,加热完全反应后,冷却称量剩余物体的质量为20.4g
求:剩余固体中二氧化锰的质量. 风霜渐起1年前2
风霜渐起1年前2 -
 忘记等于想起 共回答了18个问题
忘记等于想起 共回答了18个问题 |采纳率94.4%设混合物中的质量为x克,MnO2是催化剂,质量不变.反应前KClO3的质量为30-x克,反应后KCl的质量为20.4-x克.
2KClO3 = 2KCl + 3O2 (g)
2*122.5 2*74.5
30 - x 20.4 -x
245 :149 = (30 - x) :(20.4 - x)
x = 5.51年前查看全部
- 将40g高锰酸钾装入大试管中,加热反应一段时间后,冷却称量,得到剩余固体的质量为36.8g 今晚就要,
将40g高锰酸钾装入大试管中,加热反应一段时间后,冷却称量,得到剩余固体的质量为36.8g 今晚就要,
将40g高锰酸钾装入大试管中,加热反应一段时间后,冷却称量,得到剩余固体的质量为36.8g:
(1)加热一段时间后,固体质量为何减少?
(2)生成氧气的质量是多少克?
(3)有多少克高锰酸钾被分解?
(4)反应后的剩余固体中存在哪些物质?
重点解第(3)问 lichee_ase1年前2
lichee_ase1年前2 -
 qqqwwe123 共回答了19个问题
qqqwwe123 共回答了19个问题 |采纳率100%(1)有O2气体产生
(2)40-36.8=3.2克
(3)根据方程式用O2可以求出分解的KMnO4是31.6克
(4)未分解的KMnO4,KMnO4分解出的K2MnO4和MnO2三种1年前查看全部
- (2007•大兴安岭)小娇同学准备配制50g溶质质量分数为16%的氯化钠溶液,应先用天平称量______g氯化钠放在烧杯
(2007•大兴安岭)小娇同学准备配制50g溶质质量分数为16%的氯化钠溶液,应先用天平称量______g氯化钠放在烧杯中,再用规格为______量筒(从1OOmL、5OmL、2OmL申选择)量取______mL水(水的密度为lg/mL),倒入烧杯中搅拌,即可得到所需溶液.
 kuangruipei1年前1
kuangruipei1年前1 -
 361man 共回答了21个问题
361man 共回答了21个问题 |采纳率85.7%解题思路:配制50g溶质质量分数为16%的氯化钠溶液,首先需要计算配制溶液所需的氯化钠和水的量;在量取水时,应选择稍大于所要量取水体积的量筒一次性量取.配制50g溶质质量分数为16%的氯化钠溶液,需要氯化钠的质量=50g×16%=8g;
需要水的质量=50g-8g=42g,合42mL;
量取42mL水应选取稍大于该体积的50mL量筒;
故答:8,50mL,42.点评:
本题考点: 一定溶质质量分数的溶液的配制;有关溶质质量分数的简单计算.
考点点评: 选用量筒时,根据所需液体体积,选取量程稍大于所需液体体积的量筒,一次量取所需液体,减少实验误差.1年前查看全部
- 将一铜片在酒精灯上加热分别插入1醋酸2乙醇3石灰水溶液中,反应完毕,取出铜片洗涤,干燥,称量.为什么醋酸变使铜片质量变轻
将一铜片在酒精灯上加热
分别插入1醋酸2乙醇3石灰水溶液中,反应完毕,取出铜片洗涤,干燥,称量.为什么醋酸变使铜片质量变轻,乙醇使其不变,石灰水溶液使其变重?
卷子的答案就是这样的 海之锋1年前1
海之锋1年前1 -
 gsnacdt 共回答了24个问题
gsnacdt 共回答了24个问题 |采纳率91.7%铜经过加热后表面部分铜会变成氧化铜,放入醋酸中氧化铜会被酸碱反映掉,所以质量会变轻
乙醇把氧化铜还原了,所以质量不变
和石灰水中的水会生成氢氧化铜附着在同表面,所以质量会变重1年前查看全部
- 将6.5g KClO3和MnO2的混合物装入大试管中,加热制氧气.待反应完毕后,冷却试管后称量,剩有4.58g
将6.5g KClO3和MnO2的混合物装入大试管中,加热制氧气.待反应完毕后,冷却试管后称量,剩有4.58g固体物质.
计算:
(1)制得O2多少克?
(2)4.58g固体中含有哪些物质?各多少克? 春天寂静之树1年前1
春天寂静之树1年前1 -
 Sahara-Desert 共回答了15个问题
Sahara-Desert 共回答了15个问题 |采纳率73.3%解题思路:根据题意可以知道题中所发生的反应为氯酸钾的分解反应,该反应分解产生了氯化钾和氧气,二氧化锰是这个反应的催化剂,反应前后不变,因此4.58g固体物质中含有二氧化锰和生成的氯化钾,根据质量守恒定律可以求算出氧气的质量,再根据化学方程式由生成氧气的质量可以计算出氯化钾的质量.进而求出二氧化锰的质量.氯酸钾的分解反应,该反应分解产生了氯化钾和氧气,二氧化锰是这个反应的催化剂,反应前后不变,因此4.58g固体物质中含有二氧化锰和生成的氯化钾
根据质量守恒定律可以知道生成氧气的质量为:6.5g-4.58g=1.92g,
设生成氯化钾的质量为x,反应的氯酸钾的质量为y
2KClO3
MnO2
.
△2KCl+3O2↑
24514996
y x 1.92g
[149/x=
96
1.92g]=[245/y]
解得:x=2.98g,y=4.9g
假设氯酸钾完全反应,则二氧化锰的质量=4.58g-2.98g=1.6g,
然后验证:1.6g+4.9g=6.5g,故氯酸钾完全反应假设正确.
答:制得O21.92g.4.58g固体中含有二氧化锰1.6g和生成的氯化钾2.98g.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 解答本题的关键是要分析出试管内质量的减少量就是生成的氧气质量,再根据氧气质量结合化学方程式进一步计算.1年前查看全部
- 为什么配制蔗糖溶液可用上皿天平称量
 qingqingla1年前3
qingqingla1年前3 -
 三千烦恼随风飘 共回答了16个问题
三千烦恼随风飘 共回答了16个问题 |采纳率81.3%因为配制蔗糖溶液,需要知道质量.1年前查看全部
- 利用如图装置证明质量守恒定律时,先称量小烧杯、试管及其中所有物质的质量m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应发
 利用如图装置证明质量守恒定律时,先称量小烧杯、试管及其中所有物质的质量m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应发生了一段时间后,再称量小烧杯、试管及其中所有物质的总质量为m2,以下判断正确的是( )
利用如图装置证明质量守恒定律时,先称量小烧杯、试管及其中所有物质的质量m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应发生了一段时间后,再称量小烧杯、试管及其中所有物质的总质量为m2,以下判断正确的是( )
A.m1=m2
B.该反应不遵循质量守恒定律
C.该实验因称量的质量中包含了烧杯和试管的质量,所以不能证明质量守恒定律
D.该实验有气体产生,为验证质量守恒定律可以采用密闭容器进行实验 故乡行云似1年前1
故乡行云似1年前1 -
 huicsoft1 共回答了12个问题
huicsoft1 共回答了12个问题 |采纳率100%解题思路:碳酸钠与盐酸反应生成物中有气体二氧化碳,所以放在小烧杯内进行反应时,二氧化碳气体逸散到空气中,而使反应前后烧杯内物质的质量不相等;质量守恒定律适用于所有化学反应;验证质量守恒定律的实验,有气体参加或生成的实验必须在密闭装置中.A、碳酸钠与盐酸混合后,生成氯化钠、水和二氧化碳,由于生成的二氧化碳气体放出,依据质量守恒定律,小烧杯、试管及其中所有物质的质量m1大于反应后小烧杯、试管及其中所有物质的总质量为m2,故错误;
B、该反应属于化学反应,遵守质量守恒定律,故错误;
C、该实验因称量的质量中包含了烧杯和试管的质量,但反应前后称量中都包含,因此若生成的气体不外逸,能证明质量守恒定律,故错误;
D、验证质量守恒定律的实验,有气体参加或生成的实验必须在密闭装置中,故正确.
故选:D.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 在任何与周围隔绝的体系中,不论发生何种变化或过程,其总质量始终保持不变.验证质量守恒定律的实验,有气体参加或生成的实验必须在密闭装置中.1年前查看全部
- 托盘天平能精确称量到多少克?
 xuan19821年前1
xuan19821年前1 -
 FKLDQL 共回答了17个问题
FKLDQL 共回答了17个问题 |采纳率94.1%托盘天平也称台式天平,常用于精密度不高的称量,一般能准确到0.1克1年前查看全部
- 质量为8.02 g的铁片,放入1.0 L 0.9 mol•L-1 CuSO4溶液中,一段时间后取出洗净,干燥后称量,质量
质量为8.02 g的铁片,放入1.0 L 0.9 mol•L-1 CuSO4溶液中,一段时间后取出洗净,干燥后称量,质量为8.66
 真水无香yql1年前1
真水无香yql1年前1 -
 littlelove4u 共回答了16个问题
littlelove4u 共回答了16个问题 |采纳率81.3%这个貌似是91年高考化学题,我先把题目补完,不知对否?将8.02g铁片放入1.0L0.90mol/L硫酸铜溶液中,过一段时间取出清洗,干燥后称量,质量变为8.66g.假设溶液的体积无变化,则铜离子浓度变为多少?设消耗的Cu2+的质量是m克F...1年前查看全部
- 把氧化铜和木炭粉的混合物30g,加热到高温,过一会停止加热,冷却后称量,混合物的质量减轻了4.4g,求有多
把氧化铜和木炭粉的混合物30g,加热到高温,过一会停止加热,冷却后称量,混合物的质量减轻了4.4g,求有多
少克氧化铜参加了反应? wdstar991年前1
wdstar991年前1 -
 lion021 共回答了27个问题
lion021 共回答了27个问题 |采纳率81.5%减少的质量是生成CO2的质量,4.4g.
设参加反应的氧化铜的质量是x.
2CuO+C=高温=2Cu+CO2↑
160 44
x 4.4g
160/x=44/4.4
x=16g
答:16g氧化铜参加了反应.1年前查看全部
- 加热条件下,使足量的CO与Cu和Fe2O3的混合物18.8g充分反应,冷却后,称量剩余物的质量为14g,求剩余物中铜元素
加热条件下,使足量的CO与Cu和Fe2O3的混合物18.8g充分反应,冷却后,称量剩余物的质量为14g,求剩余物中铜元素的质量分数?
 wufei06291年前1
wufei06291年前1 -
 yiqitiaowu 共回答了25个问题
yiqitiaowu 共回答了25个问题 |采纳率92%解题思路:根据质量守恒定律分析固体减少的质量就是氧化铁中氧元素的质量,结合方程式中的比例关系求出参加反应的氧化铁的质量进行分析.根据质量守恒定律分析固体减少的质量就是氧化铁中氧元素的质量,设混合物中氧化铁的质量为x.
Fe2O3+3CO
高温
.
2Fe+3CO2 减少的质量
160 112 48
x 18.8g-14g
[160/x=
48
18.8g−14g]
x=16g
原混合物中铜的质量=18.8g-16g=2.8g
所以剩余物中铜元素的质量分数=
2.8g
14g×100%=20%
答:剩余物中铜元素的质量分数为20%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题主要考查学生根据化学方程式的计算,根据题意找出已知量和待求量的相关数据,根据化学方程式的解题格式进行计算解答.1年前查看全部
- 1.在用托盘天平称量5g粗盐的过程中你认为操作错误的是( )
1.在用托盘天平称量5g粗盐的过程中你认为操作错误的是( )
A称量之前先调节天平平衡
B左边放粗盐,右边放砝码
C称量纸只用在了左盘
D托盘天平平衡时就停止称量
2.某学生做过滤试验后发现,经过过滤的液体仍有浑浊的现象,请你帮他找出造成此现象的两种可能原因
①_____________________________
②______________________________
3,.鉴别三瓶无色气体,分别是空气、二氧化碳、氧气,写出操作步骤、现象和结论
实验目的:_______
实验仪器:________
操作步骤______________
实验现象_______________
实验结论_________________
求写具体 开学考试的内容 只有二十分了…抱歉
补一道题…4.随着绿色奥运的理念逐渐深入人心,空气质量日益受到人们的关注,下列物质中,不计入每日空气质量检测的是( )
A二氧化硫 B二氧化氮 C二氧化碳 D可吸入颗粒 jrtds1年前1
jrtds1年前1 -
 gdfgtf 共回答了16个问题
gdfgtf 共回答了16个问题 |采纳率81.3%1.在用托盘天平称量5g粗盐的过程中你认为操作错误的是( C )
A称量之前先调节天平平衡
B左边放粗盐,右边放砝码
C称量纸只用在了左盘
D托盘天平平衡时就停止称量
称量纸必须两边都放.
2.某学生做过滤试验后发现,经过过滤的液体仍有浑浊的现象,请你帮他找出造成此现象的两种可能原因
①玻璃棒靠在了只有一层滤纸的一端
②滤纸有破损
3,.鉴别三瓶无色气体,分别是空气、二氧化碳、氧气,写出操作步骤、现象和结论
实验目的:鉴别上述气体
实验仪器:集气瓶,带火星的木棒
实验步骤:
操作步骤:将三个带火星的木棒分别插入三瓶气体中,观察现象.
实验现象:在氧气中的木棒发出更亮的光;在空气中的木棒没有变化;在二氧化碳中的木棒熄灭
实验结论:鉴别出了三瓶无色气体
4.随着绿色奥运的理念逐渐深入人心,空气质量日益受到人们的关注,下列物质中,不计入每日空气质量检测的是( C )
A二氧化硫 B二氧化氮 C二氧化碳 D可吸入颗粒1年前查看全部
- 分析天平称量前预称有何意义
 a流沙h1年前2
a流沙h1年前2 -
 qq213 共回答了16个问题
qq213 共回答了16个问题 |采纳率100%现在都是电子天平吧,老式分析天平预称的话可以降低玛瑙刀头的使用时间,保护刀头,同时可以减短称样的时间.这都是只有好处 没有坏处的.1年前查看全部
- 不通过称量,如何判断SO2与NaOH溶液发生了反应呢?丁同学设计了如图所示的装置进行实验,发现试管内液面上升,就得出SO
不通过称量,如何判断SO2与NaOH溶液发生了反应呢?丁同学设计了如图所示的装置进行实验,发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论.其他同学认为这一方案不严谨,理由是
.要得到科学严谨的结论,仍利用该装置,补做的实验是
. assuck1年前2
assuck1年前2 -
 天鸢 共回答了14个问题
天鸢 共回答了14个问题 |采纳率100%建议去菁优网查答案!1年前查看全部
- 天平称量时左码右物会导致什么
 pdszhyy1年前2
pdszhyy1年前2 -
 orientdawn 共回答了19个问题
orientdawn 共回答了19个问题 |采纳率94.7%测未知质量的物体时,如果左码右物:
1、如果移动游码天平才平衡,那读数大于物体质量
2、如果不用移动游码天平就平衡了,那就正确
此时物体的正确质量: m物=砝码质量-游码数1年前查看全部
- 取某铁样品12g加入到盛有50g稀盐酸的烧杯(烧杯质量60g)中,在反应过程中对烧杯进行了四次称量,数据如下
取某铁样品12g加入到盛有50g稀盐酸的烧杯(烧杯质量60g)中,在反应过程中对烧杯进行了四次称量,数据如下
反应时间: T0 T2 T3 T4
烧杯和药品的质量:122 121.8 121.6 121.6
问:1.反应中产生氢气为?
2.列式计算:工业上要冶炼出上述铁24t,需要含氧化铁为百分之80的铁矿石多少吨?
 佳崴1年前1
佳崴1年前1 -
 一个可怜的小nn 共回答了17个问题
一个可怜的小nn 共回答了17个问题 |采纳率100%1、当质量恒定时,说明反应已经完成.
因此氢气质量m=12+50+60-121.6=0.4g
2、由2HCl+Fe==FeCl2+H2得到样品中的铁的质量为m1=0.4/2*56=11.2g
24t样品中含纯铁量为24*11.2/12=22.4t
含氧化铁为百分之80的铁矿石中纯铁的含量为56*2/(56*2+16*3)*80%=56%
所以需要含氧化铁为百分之80的铁矿石22.4/0.56=40t1年前查看全部
- 1.称量是指称物体的重量还是称取一定量的物体?
1.称量是指称物体的重量还是称取一定量的物体?
2.小明用天平称量5.5克的粗盐,一时粗心,称量时把砝码放在左边,粗盐放在右盘.小明是集成的的粗盐的质量为多少?(请说明为什么)
为什么砝码的质量为5克,小明称的时候并不知道是5克啊? 要怎么说1年前4
要怎么说1年前4 -
 诗人 共回答了15个问题
诗人 共回答了15个问题 |采纳率100%1.物体的重量
2.4.5g 因为如果是左物右码的话,物体的质量=砝码的质量+游码的质量.现在是左码右物,当平衡时,砝码的质量=物体的质量+游码的质量,所以物体的质量=砝码的质量-游码的质量=5g-0.5g=4.5g.1年前查看全部
- 智力挑战题!有8个大小、形状、颜色完全一样的乒乓球,其中有一个为次品,次品的重量较轻,现用天平称量,怎样能将次品称出?(
智力挑战题!
有8个大小、形状、颜色完全一样的乒乓球,其中有一个为次品,次品的重量较轻,现用天平称量,怎样能将次品称出?(三次以内 不含三次) woichuangye1年前6
woichuangye1年前6 -
 树啊 共回答了24个问题
树啊 共回答了24个问题 |采纳率87.5%第一次:左边三个,右边三个
若平衡,则次品在剩余两个中,再一左一右称一次便知道哪个是次品
若不平衡,将轻的那一边的三个球,一左一右,一个不称,若平衡,则次品是没称的那个,若不平衡,次品就是轻的那一边的那个.1年前查看全部
- 溶液浓度的配置 有固体物质(CuSO4),可称量.要配置100ml浓度为0.2mol/L的硫酸铜溶液,怎样计算和配置?要
溶液浓度的配置
有固体物质(CuSO4),可称量.要配置100ml浓度为0.2mol/L的硫酸铜溶液,怎样计算和配置?要配置浓度为20%的硫酸铜溶液呢?
3.2g的计算公式是?20%浓度硫酸铜溶液 怎么配置?谁能再解释的清楚点? 快乐小喜12151年前4
快乐小喜12151年前4 -
 yang1219 共回答了24个问题
yang1219 共回答了24个问题 |采纳率87.5%先计算CuSO4的质量
0.1*0.2*160=3.2g
用天平称放在烧杯中,加适量水,用玻璃棒引流导入100ml容量瓶中
再用水清洗烧杯及玻璃棒,将清洗的液体也导入容量瓶中,在距刻度线1-2cm处,改用胶头滴管滴,直至凹液面一刻度线相平,盖住塞子,摇,贴标签.
20%的同理
打字真累.1年前查看全部
- 配置100mL0.1mol/L的NaCl溶液 由于天平会多称量0.05g 氯化钠 那会改变其浓度,这怎么办呢?
 雪里蕻20081年前1
雪里蕻20081年前1 -
 52154sg 共回答了16个问题
52154sg 共回答了16个问题 |采纳率93.8%使用分析天平称量NaCl,分析天平精确到0.0001g.1年前查看全部
- 称量5.8克食盐,具体实验步骤
 nancylzyc06041年前1
nancylzyc06041年前1 -
 醉了梦了就想哭 共回答了12个问题
醉了梦了就想哭 共回答了12个问题 |采纳率91.7%1、把游码放在零处,调节平衡螺母直到天平平衡
2、左右两盘各放一张大小、质量均相等的称量纸
3、把游码移到5.8克的刻度处
4、在左盘添加食盐直到天平再次达到平衡为止.
此时左盘称量纸上的食盐正好是所需要的5.8克.1年前查看全部
大家在问
- 1一个数乘一个比1小的数,积不一定比这个数小.______.(判断对错)
- 2已知向量AB=(5,8),向量BC=(-6,-11),向量CD=(-11,-19),判断四边形ABCD的形状
- 3动物有关的成语万什么更新
- 4督促某人做某事的英文怎么说
- 5大一高数考映射么?
- 6英语作文:假设你想买一顶帽子,营业员给你介绍了各种颜色的帽子,你最喜欢白色的.营业员告诉你白色帽子每顶20元,最后你决定
- 7leave me alone 几种意思
- 8帮我检查一下英语文章my bedroon.
- 9如图,在⊙O中,弦AB‖弦CD,弦AE‖弦CF,求证:BE=DF
- 10拿破仑加冕时说:“我只能做一个加冕的华盛顿”,这句话的意思是 [ ] A
- 11将表面已部分被氧化的金属钠54g样品放入一定量的水中,收集到标准状况下11.2l的H2.若将溶液稀释至500ml,
- 12①已知|2x-4|+|y+3|=0,求x-y的值 ( | | 是绝对值)
- 13英译汉:There are basically to ways to get work done...
- 14ax-7x=-13,a,x都是正整数~
- 15下列现象中,属于用做功的方式改变物体内能的是A打火机点火 B冬天在火炉旁烤火 C冬天用热水袋是身体暖和
