向氯化镁和氯化铝混合物中滴加氢氧化钠,氢氧化钠与氯化镁反应还是先于氯化铝反应,有先后顺序吗?原理...
 把你问青天2022-10-04 11:39:541条回答
把你问青天2022-10-04 11:39:541条回答向氯化镁和氯化铝混合物中滴加氢氧化钠,氢氧化钠与氯化镁反应还是先于氯化铝反应,有先后顺序吗?原理是什么?

已提交,审核后显示!提交回复
共1条回复
 相约33 共回答了20个问题
相约33 共回答了20个问题 |采纳率80%- 理论上,如果非常慢的滴加,氢氧化钠浓度又很低,那氢氧化铝先析出,因为氢氧化镁是微溶,溶解度高于氢氧化铝好几个数量级
一般情况下,滴加的快,局部过浓,没有先后顺序,同时沉淀下来 - 1年前
相关推荐
- 初三化学中如何辨别碳酸钠,氯化钠,硫酸钠和氯化镁
 笔砚斋1年前26
笔砚斋1年前26 -
 voool 共回答了18个问题
voool 共回答了18个问题 |采纳率94.4%1、加入硝酸钡,有白色沉淀的是硫酸钠和碳酸钠.没有沉淀的是氯化钠和氯化镁.
2、再向沉淀中 加入稀硝酸,沉淀溶解的是碳酸钠,不溶解的是硫酸钠.
3、再取没有沉淀的两种溶液,向其中 加入氢氧化钠,有白色沉淀的是氯化镁,没有沉淀的是氯化钠.1年前查看全部
- (12分)利用海水(含氯化钠、氯化镁)处理含二氧化硫废气的方法如下:
(12分)利用海水(含氯化钠、氯化镁)处理含二氧化硫废气的方法如下:
Ⅰ.海水处理流程: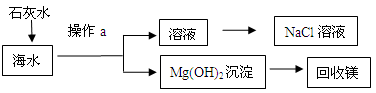
(1)写出生成Mg(OH) 2 沉淀的化学反应方程式 ;
(2)经操作a得到的Mg(OH) 2 沉淀需要洗净,为证明是否洗净,可取洗涤液少量,向其
中加入下列试剂中的 ,即可达到实验目的。
A. Na 2 CO 3 溶液 B.石灰水 C. 硝酸银溶液
Ⅱ.处理二氧化硫流程:
(3)上图中最终得到“NaCl”的过程属于 (填“物理变化”或“化学变化”);
(4)图中反应①、③、④属于化合反应的是 (填序号);
(5)①中反应的化学方程式为 ;
(6)④中反应的化学方程式为 。 hellohsm1年前1
hellohsm1年前1 -
 wujin1126 共回答了21个问题
wujin1126 共回答了21个问题 |采纳率95.2%(1)MgCl 2 +Ca(OH) 2 ="==" Mg(OH) 2 ↓+ CaCl 2 (2)A、C
(3)物理变化 (4)③ (5)2NaCl+2H 2 O 通电 NaOH+2H 2 ↑+Cl 2 ↑
(6)NaHSO 3 +HCl===NaCl+SO 2 +H 2 O
1年前查看全部
- 有一混合溶液是由碳酸钾、氯化镁、稀硫酸、稀硝酸四种物质中的两种混合而成,向该混合液中滴加氢氧化钡溶液,产生沉淀的质量与滴
有一混合溶液是由碳酸钾、氯化镁、稀硫酸、稀硝酸四种物质中的两种混合而成,向该混合液中滴加氢氧化钡溶液,产生沉淀的质量与滴入氢氧化钡溶液的体积的关系如图,则该混合物的可能组成是:(图是一开始一条向上的斜线,然后就变为水平直线)
为什么不是碳酸钾和氯化镁?我选的是这个,但是答案上是氯化镁和稀硫酸.
某物质经过鉴定只含有一种元素,则此物质()
我选的是可能是纯净物,也可能是混合物,但是答案上选的是:一定是一种单质.
为什么? mfdwl1年前3
mfdwl1年前3 -
 cwb94191034 共回答了20个问题
cwb94191034 共回答了20个问题 |采纳率90%1. 这个完全取决于图的细节了.
碳酸钾和氯化镁:图像是不经过原点的斜线+水平线,斜线与纵轴交在原点上方;或者直接是不经过原点的水平线
氯化镁和稀硫酸:图像是经过原点的斜线+另一条斜率不同的斜线+水平线
稀硫酸和稀硝酸:图像是经过原点的斜线+水平线
氯化镁和稀硝酸:图像是不经过原点的斜线+水平线,斜线与横轴交在原点右方;
碳酸钾和稀硫酸:图像是经过原点的斜线+水平线
碳酸钾和稀硝酸:图像是水平线;或是经过原点的斜线+水平线
请对号入座
2. 你正确,答案脑残1年前查看全部
- 有一混合溶液是由碳酸钾、稀硫酸、氯化镁、稀硝酸四种物质中的两种混合而成.
有一混合溶液是由碳酸钾、稀硫酸、氯化镁、稀硝酸四种物质中的两种混合而成.
向该混合溶液中滴加氢氧化钡溶液,则改混合溶液可能是_或_
产生沉淀 plxshmily1年前3
plxshmily1年前3 -
 savage_casper 共回答了15个问题
savage_casper 共回答了15个问题 |采纳率100%出现什么现象?
如果是出现白色沉淀,那么混合溶液可能是稀硫酸和氯化镁的混合溶液,或稀硫酸和稀硝酸的混合溶液.1年前查看全部
- 现有氯化镁和氯化钠的混合物80g 将它们加水完全溶解 然后向其中加入足量的氢氧化钠溶液 生成沉淀8.7g
现有氯化镁和氯化钠的混合物80g 将它们加水完全溶解 然后向其中加入足量的氢氧化钠溶液 生成沉淀8.7g
求原混合物中氯化镁的质量分数 急
对不起 是有20g混合物 刚刚把字打错啦 a13611年前1
a13611年前1 -
 zhangfu31 共回答了9个问题
zhangfu31 共回答了9个问题 |采纳率77.8%设原混合物中氯化镁的质量是x.
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
95 58
x 8.7g
95/x=58/8.7
x=14.25g
原混合物中氯化镁的质量分数是14.25/80*100%=17.8%
答:原混合物中氯化镁的质量分数是17.8%1年前查看全部
- 电催化 电解氯化镁?常规的电解融融氯化镁才能产生金属镁,电解氯化镁溶液产生氢气 如果研究电化学催化剂,能不能在氯化镁溶液
电催化 电解氯化镁?
常规的电解融融氯化镁才能产生金属镁,电解氯化镁溶液产生氢气 如果研究电化学催化剂,能不能在氯化镁溶液中电解出金属镁?很傻的外行问题, liuwenrong1年前1
liuwenrong1年前1 -
 KEN_BAX 共回答了19个问题
KEN_BAX 共回答了19个问题 |采纳率94.7%氯化熔盐电解法包括氯化镁的生产及电解制镁两大过程.该方法又可分为以菱镁矿为原料的无水氯化镁电解法和以海水为原料制取无水氯化镁的电解法.其中后者最大的难点是如何去除MgCl2·6H2O中的结晶水.一般来说:采用普通的加热法可以去除部分结晶水,生成MgCl2·3/2H2O.但MgCl2·3/2H2O在空气中加热时很容易发生水解反应,生成不利于电解过程的杂质,如Mg(OH)2.电解法生产镁的工艺很多,但基本原理相同,其中最有代表性的有DOW工艺、I.G.Farben工艺、Magnola工艺等. 查看原帖1年前查看全部
- 电解氯化镁电解无水氯化镁所得的镁蒸汽在特定环境里冷却后即为固体没下列物质可做镁蒸汽的冷却剂的是A,H2 B.CO2 C.
电解氯化镁
电解无水氯化镁所得的镁蒸汽在特定环境里冷却后即为固体没下列物质可做镁蒸汽的冷却剂的是
A,H2 B.CO2 C.O2 D.水蒸气 小女人mena1年前2
小女人mena1年前2 -
 hqx22 共回答了16个问题
hqx22 共回答了16个问题 |采纳率100%A
本题考查镁的化学性质
欲制备镁单质,所选冷却剂不能和镁反应
1、CO2与Mg反应产生C
2、与O2 氧化镁
3、镁与水再高温下生产氢氧化镁
希望能帮到您.望采纳哟.1年前查看全部
- 简述如何从氯化钠和氯化镁的混合溶液中得到氯化钠和氯化镁固体
 mfktdkj959681年前1
mfktdkj959681年前1 -
 最后的情圣 共回答了23个问题
最后的情圣 共回答了23个问题 |采纳率100%(1)加入足量的NaOH,过滤.
(2)滤液中加入适量稀盐酸,蒸发结晶,得到NaCl
(3)取滤渣,洗涤,加入稀盐酸.小火蒸干,再在干燥的HCl气流,加热,得到MgCl21年前查看全部
- 几道化学题目(FAST)6.下列物质所对应的化学式属于分子式的是……………………………………………( )A、氯化镁 B.
几道化学题目(FAST)
6.下列物质所对应的化学式属于分子式的是……………………………………………( )
A、氯化镁 B.二氧化碳 C.二氧化硅 D.硫化钠
7.下列物质中,属于含有共价键的离子化合物的是………………………………( )
A、HCl B、H2 C、MgCl2 D、NaOH
8.X元素的一个原子失去两个电子,转移到Y元素的两个原子中去,则X、Y两种
元素形成的化合物中含有的化学键类型为…………………………………………( )
A、金属键 B、离子键 C、共价键 D、既有离子键又有共价键
9.下列变化中,只存在放热过程的是………………………………………………( )
A、硫在空气中燃烧 B、NaOH晶体溶于水 C、液氨的挥发 D、水蒸气的液化
10.下列物质在干燥的空气中容易发生风化的是…………………………………( )
A、石碱 B、胆矾 C、食盐 D、烧碱
要详细解释······ lyjking1169261年前5
lyjking1169261年前5 -
 Eleven329 共回答了18个问题
Eleven329 共回答了18个问题 |采纳率88.9%6、选B
MgCl2是由Mg2+和Cl-构成的,属于离子晶体;
CO2是由CO2分子构成的,属于分子晶体
SiO2是由Si原子和O原子构成的,属于原子晶体;
Na2S是由Na+和S2-构成的,属于离子晶体.
7、选D
A和B都是分子晶体,不是离子化合物
MgCl2中只有Mg-Cl构成的离子键,不含共价键.
NaOH中含有O-H共价键,是离子化合物,所以符合要求.
8、选B
发生了电子的转移,即是离子化合物,含有离子键
9、选D
S的燃烧要先吸热生成硫蒸汽;NaOH电离时要吸热;液氨挥发要吸热
10、选B、
胆矾是CuSO4.5H2O,分化生成CuSO4粉末1年前查看全部
- (2003•黑龙江)将10g不纯的氯化镁样品(杂质不溶于水),放入100g水中,充分搅拌,待样品中的氯化镁全部溶解后过滤
(2003•黑龙江)将10g不纯的氯化镁样品(杂质不溶于水),放入100g水中,充分搅拌,待样品中的氯化镁全部溶解后过滤(滤液损失不计),将所得滤液与63.3g氢氧化钠溶液恰好完全反应,生成5.8g白色沉淀.
求:(1)样品中氯化镁的质量.
(2)反应后所得溶液中溶质的质量分数. 玉成千春1年前1
玉成千春1年前1 -
 hengtai2 共回答了14个问题
hengtai2 共回答了14个问题 |采纳率85.7%解题思路:由沉淀质量根据化学方程式可以计算出氯化镁的质量和生成氯化钠的质量,进而计算出所得溶液的溶质质量分数.设样品中氯化镁的质量为x,生成氯化钠的质量为y.
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
9558 117
x5.8g y
(1)[95/58]=[x/5.8g],x=9.5g
(2)[58/117]=[5.8g/y],y=11.7g
所得溶液中溶质的质量分数为
[11.7g/9.5g+100g+63.3g−5.8g]×100%≈7.0%
答:(1)样品中氯化镁的质量为9.5g;
(2)反应后所得溶液的溶质质量分数为7.0%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题考查有关化学方程式的计算和溶质质量分数的计算,难度较大.1年前查看全部
- 有一包白色粉末,可能含有硝酸钡,氯化镁,碳酸钾,氢氧化钠,现做以下实验
有一包白色粉末,可能含有硝酸钡,氯化镁,碳酸钾,氢氧化钠,现做以下实验
1取一定量的粉末加入水中,震荡,有白色沉淀生成
2向1的沉淀物中加入足量稀硝酸,白色沉淀完全消失,没有气泡产生
3向1的上层清液中滴入稀硫酸,有白色沉淀生成
问原白色粉末中一定有什么,一定不含有什么
写出各部变化的离子方程式 傲视群英1年前3
傲视群英1年前3 -
 幻影宝贝 共回答了14个问题
幻影宝贝 共回答了14个问题 |采纳率92.9%解析:
1取一定量的粉末加入水中,震荡,有白色沉淀生成,可以是 BaCO3 Mg(OH)2
2向1的沉淀物中加入足量稀硝酸,白色沉淀完全消失,没有气泡产生.所以没有 BaCO3 ,所以一定有Mg(OH)2 ,故有 氢氧化钠和氯化镁.一定没有碳酸钾
3向1的上层清液中滴入稀硫酸,有白色沉淀生成,所以有硝酸钡.
所以原白色粉末中一定有氢氧化钠,氯化镁,硝酸钡.一定不含有碳酸钾.
离子方程式:Mg2+ + 2OH-=Mg(OH)2(沉淀)
Mg(OH)2+ 2H+= Mg2+ + 2H2O
Ba2+ + SO42-= BaSO4(沉淀)1年前查看全部
- 某氯化镁溶液的密度为1.18g/cm其中镁离子的质量分数为5.1%.300mL该溶液中的氯离子物质的量约为 (1.5mo
某氯化镁溶液的密度为1.18g/cm其中镁离子的质量分数为5.1%.300mL该溶液中的氯离子物质的量约为 (1.5moL)
这是为什么呢? lysx4031年前1
lysx4031年前1 -
 慕容公子119 共回答了20个问题
慕容公子119 共回答了20个问题 |采纳率80%m(aq)=密度*v=300*1.18 m(mg)=m(aq)*5.1%=18.054 n(mg)=m/M=0.75 n(cl-)=2*n(mg)=1.51年前查看全部
- 分子式怎么读,如MgCl2为什么读成氯化镁而不是二氯化镁
 musicbug_z1年前2
musicbug_z1年前2 -
 fdsgfdg135 共回答了26个问题
fdsgfdg135 共回答了26个问题 |采纳率88.5%分子式怎么读,要仔细研究下为什么这么读.一般我们把某元素在自然界中自然存在时的价态加上非金属元素后称为某化某,比如你说的MgCl2,镁在自然界一般是以金属盐的形式存在,如含镁的矿物主要有白云石CaCO3·MgCO3、光卤石KCl·MgCl2·6H2O、菱镁矿MgCO3等,海水中则是以镁的氯化物和硫酸盐为主,所以这些自然存在的镁一般都是正二价的,那么,我们就习惯把自然存在的价态的离子Mg形成盐后称为氯化镁,当然你说成二氯化镁也是对的,但是习惯上不这么说,一提氯化镁自然想到的分子式就是MgCl2,.再如Fe,由于铁单质易氧化成Fe2O3,所以大多是以菱铁矿即Fe2O3存在(当然也有磁铁矿Fe3O4,但相对较少),这样的Fe是正三价的.所以我们把FeCl3称为氯化铁,因为氯化物里的铁也是正三价的,也称三氯化铁.而FeCl2则称为氯化亚铁了.
不知我这么解释能否理解1年前查看全部
- 物质的量浓度相同的氯化钠,氯化镁,氯化铝三种物质的溶液,当溶液的体积比为3:2:1时,它们于同一浓度的硝酸银溶液恰好反应
物质的量浓度相同的氯化钠,氯化镁,氯化铝三种物质的溶液,当溶液的体积比为3:2:1时,它们于同一浓度的硝酸银溶液恰好反应,则消耗的硝酸银溶液的体积比为
A3:4:3 B 1:1:1 C1:2:3 D3:2:1 为什么?
到底谁对? gaolongls1年前3
gaolongls1年前3 -
 moon蝙蝠小侠 共回答了19个问题
moon蝙蝠小侠 共回答了19个问题 |采纳率94.7%A3:4:3
物质的量浓度相同的氯化钠,氯化镁,氯化铝三种物质的溶液,当溶液的体积比为3:2:1时;
他们中的氯离子的物质的量的比为3:4:3
它们于同一浓度的硝酸银溶液恰好反应,则消耗的硝酸银溶液的体积比为
3:4:31年前查看全部
- 4只50ml小烧杯中,分别放入浓度相同的20g稀盐酸,然后向这4分盐酸中分别加入足量的下列物质,经充分反应,都生成氯化镁
4只50ml小烧杯中,分别放入浓度相同的20g稀盐酸,然后向这4分盐酸中分别加入足量的下列物质,经充分反应,都生成氯化镁溶液,其中浓度最大的是()
A.Mg
B.MgO
C.Mg(OH)2
D.MgCO3 镜爷1年前4
镜爷1年前4 -
 wwjzlcw 共回答了16个问题
wwjzlcw 共回答了16个问题 |采纳率75%写出方程式即可得知:
A中没有水生成.
B、C、D中有水生成.
则,BCD中溶剂的质量增加,所以,选A1年前查看全部
- 实验室采用氯化镁、氯化铝的混合溶液与过量氨水反应制备
 katherineyao20061年前1
katherineyao20061年前1 -
 sueky28 共回答了25个问题
sueky28 共回答了25个问题 |采纳率92%(1)如先加入MgCl2、AlCl3的混合溶液,再加氨水,氨水少量,应先生成氢氧化镁沉淀,反之,先加氨水,因氨水足量,则同时生成沉淀,故答案为:B;
(2)过滤时应该将漏斗的尖嘴部分紧贴烧杯的内壁,防止液体溅出,故答案为:漏斗下端尖嘴未紧贴烧杯内壁;
(3)沉淀中应该附着氯离子和铵根离子,若判断是否洗净,可以取少量最后一次洗涤液,加入AgNO3溶液(或硝酸酸性的AgNO3溶液)溶液进行判断,若生成白色沉淀,则说明没有洗涤干净;若没有沉淀生成,则说明已经洗涤干净,高温焙烧固体应在坩埚中进行,
故答案为:AgNO3溶液(或硝酸酸性的AgNO3溶液);坩埚;
(4)B中的饱和食盐水是为了除去混有的HCl气体;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收空气中的CO2,所以可以加入碱石灰来代替F和G的作用,
故答案为:除去HCl;吸收水蒸气;碱石灰.1年前查看全部
- 氯化钠中有氯化镁先加氢氧化钠后为什么要加盐酸
 逍遥追命1年前1
逍遥追命1年前1 -
 一飘香 共回答了16个问题
一飘香 共回答了16个问题 |采纳率93.8%加的氢氧化钠肯定是过量的吧,加盐酸把它全部转化为氯化钠.
然后蒸发的时候盐酸会挥发出去,得到纯净的氯化钠晶体.1年前查看全部
- 让我郁闷了N久的几道化学题.1.某粗盐样品中含有可溶性的氯化镁、氯化钙杂质和不溶性的泥沙.常温下,将140 g该粗盐样品
让我郁闷了N久的几道化学题.
1.某粗盐样品中含有可溶性的氯化镁、氯化钙杂质和不溶性的泥沙.常温下,将140 g该粗盐样品溶解于水中,过滤得到不足3 g泥沙和1000 g溶液.取出500 g溶液进行测定,其中含有镁元素1.2 g,钙元素2 g,氯元素42.6 g.则原粗盐中氯化钠的质量分数约为( )
A.83.6% B.86.3% C.88.1% D.91.6%
2.已知t°C时,氯化钾的溶解度为40g.在该温度下,将20g氯化钾固体加入到50g水中,充分溶解,形成的溶液中溶质的质量分数为( )
A.25% B.28.6% C.33.3% D.50%
我知道答案是什么,
请说明为什么. 拓拔路儿1年前1
拓拔路儿1年前1 -
 爱你很痛 共回答了24个问题
爱你很痛 共回答了24个问题 |采纳率79.2%1.A
500 g溶液中:
镁元素1.2 g来自于 MgCl2.
MgCl2中Mg的质量分数:24/(35.5*2+24) 所以MgCl2质量为4.75g
所以MgCl2中Cl的质量:4.75g-1.2 g=3.55g
钙元素2 g来自于CaCl2
CaCl2中Ca的质量分数:40/(40+35.5*2) 所以 CaCl2质量为5.55g
所以CaCl2中Cl的质量:5.55g-2 g=3.55g
氯元素42.6 g来自于MgCl2,CaCl2,NaCl
NaCl中Cl的质量:42.6 g-3.55g-3.55g=35.5g
所以NaCl的质量为58.5g(方法和前面的一样)
500 g溶液中NaCl的质量为58.5g.1000 g溶液中NaCl的质量为117g
溶液一共140g.质量分数:117/140=83.6%
选A
2.B
氯化钾的溶解度为40g :t°时100g水中可以溶解40gKCl
将20g氯化钾固体加入到50g水中,就恰好可以完全溶解
质量分数:20/(50+20)=28.6%
选B1年前查看全部
- 如果要除去粗盐中含有的可溶性杂质氯化钙,氯化镁及一些硫酸钠,应加入什么试剂?
如果要除去粗盐中含有的可溶性杂质氯化钙,氯化镁及一些硫酸钠,应加入什么试剂?
三种方法
 taxismile1年前1
taxismile1年前1 -
 ll101 共回答了15个问题
ll101 共回答了15个问题 |采纳率86.7%先加过量氯化钡 生成硫酸钡沉淀,除掉硫酸根离子; 再加过量 碳酸钠,生成 钡离子 钙离子 镁离子的硫酸盐沉淀,将它们全都除掉了 ,再加过量盐酸就可以了中和多余的碳酸钠,最后加热 使盐酸挥发掉就可以1年前查看全部
- 什么化学反应可以生成氯化镁,涉及初中和高中的知识,至少三个方程式.
 我真的不是誰的誰1年前4
我真的不是誰的誰1年前4 -
 辣比晓心 共回答了19个问题
辣比晓心 共回答了19个问题 |采纳率100%镁在氯气中燃烧:
Mg + Cl2==MgCl2 (条件是点燃)
镁和稀盐酸反应:
Mg + 2HCl==MgCl2+H2↑
氧化镁和稀盐酸反应:MgO+2HCl==MgCl2+H2O
还有氢氧化镁和稀盐酸:Mg(OH)2+2HCl==MgCl2+H2O
碳酸镁和稀盐酸:
MgCO3+2HCl==MgCl2+H2O+CO2↑1年前查看全部
- 氯化镁与浓氢氧化钠反应为什么现黄色?
 佛也动心1年前2
佛也动心1年前2 -
 桀宿 共回答了23个问题
桀宿 共回答了23个问题 |采纳率95.7%可能是你所用的反应仪器中有较少的Fe3+离子,形成了FeCl3,一般浓度的FeCl3溶液是黄色的.1年前查看全部
- 【问】6水氯化镁配制 42%的氯化镁溶液
【问】6水氯化镁配制 42%的氯化镁溶液
如果配制 42%的氯化镁溶液 250mL ,需要的 6水氯化镁和水分别为多少? lscnc_qin1年前1
lscnc_qin1年前1 -
 ai吃便当的猫 共回答了17个问题
ai吃便当的猫 共回答了17个问题 |采纳率94.1%如果42%氯化镁的密度是ρ,那么
需要六水氯化镁的质量是250ρ×42%×203/95=224.4ρ克
需要水250ρ-224.4ρ=25.6ρ克1年前查看全部
- 实验室里有一包氯化钠和氯化镁的混合固体.请你设计实验把它们分离出来,并将相关的内容填写在下面实验报告的空格内.
实验室里有一包氯化钠和氯化镁的混合固体.请你设计实验把它们分离出来,并将相关的内容填写在下面实验报告的空格内.
实验步骤 实验现象 结论及化学方程式 把混合物加水溶解,向溶液中加______溶液至不再产生沉淀为止.  秋叶泛红1年前1
秋叶泛红1年前1 -
 lilizisu 共回答了16个问题
lilizisu 共回答了16个问题 |采纳率81.3%解题思路:本题要分离的是氯化钠和氯化镁的混合固体,它们均为可溶性盐类,所以不能用物理方法过滤蒸发分离,应思考用化学的方法进行分离,基本思路:加入一种试剂只与其中一种盐反应,将另外一种盐转化为沉淀,那么其中一盐分离;另一种盐转化为新物质沉淀那么在加入另一种试剂再变回原来的盐即可,对于多余的试剂可以通过再加不会产生新杂质的试剂除去.首先将氯化钠和氯化镁的两种可溶性混合固体加水溶解,然后再加入一种试剂使氯化镁变为沉淀,再加一试剂变回氯化镁
实验步骤 实验现象 结论及化学方程式
①把混合物加水溶解,向溶液中加NaOH溶液至不再产生沉淀为止. 产生白色沉淀 MgCl2 +2NaOH=Mg(OH)2↓+2NaCl
氯化镁与氧化钠反应生成氢氧化镁
②将步骤①所得溶液过滤,用蒸馏水洗涤滤渣.把滤渣移入干净烧杯中,加稀盐酸至沉淀刚好溶解.
将所得溶液小心蒸发 白色固体溶解,溶液无色
有白色固体析出 Mg(OH)2+2 HCl=MgCl2+2 H2O
所得溶液为氯化镁溶液.
所得固体是氯化镁.
③往步骤②所得溶液中加适量的稀盐酸
将所得溶液小心蒸发 有白色固体析出 NaOH+HCl=NaCl+H2O
所得溶液为氯化钠溶液.
所得固体是氯化钠.点评:
本题考点: 混合物的分离方法;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题是考查对于两种可溶性固体混合物如何进行分离,两种物质均溶于水时,可考虑用化学方法分离.由此题我们可以联想到其它同类的题型,如BaCl2和NaCl的混合物.可将混合物先溶于水,加入适量Na2CO3溶液,得到BaCO3和NaCl溶液.BaCl2+Na2CO3=BaCO3↓+2NaCl.将沉淀过滤出,洗净后在沉淀中加入适量盐酸溶液,又得到BaCl2溶液,CO2逸出.BaCO3+2HCl=BaCl2+H2O+CO2↑.最后分别将NaCl溶液和BaCl2溶液蒸发,分别得到纯净的NaCl固体和BaCl2固体.另外要注意:用化学方法或用物理方法进行混合物分离时,要区别除杂质与分离物质的不同点是:除杂质时只要求把杂质除掉、保留原物质即可;而混合物分离是几种物质用一定的方法分开,原混合物中各成分都必须保留.1年前查看全部
- 求一些正确的离子方程式‘① 铝与氢氧化钠溶液反映②向碳酸氢钠溶液中加入少量的澄清石灰水③电解氯化镁溶液④向苯酚钠溶液中通
求一些正确的离子方程式‘
① 铝与氢氧化钠溶液反映
②向碳酸氢钠溶液中加入少量的澄清石灰水
③电解氯化镁溶液
④向苯酚钠溶液中通入少量二氧化碳
⑤向溴化亚铁溶液中通入氯气
⑥将氯气通入水中
⑦氧化铁溶于足量氢碘酸中
⑧碳酸钠溶液呈碱性
⑨硫酸与氢氧化钡溶液混合
⑩向稀氨水中通入少量二氧化碳 隆回深圳人1年前1
隆回深圳人1年前1 -
 yagamishen 共回答了14个问题
yagamishen 共回答了14个问题 |采纳率100%al+4oh-=2h2o+alo2-
ca2++2oh-+2hco3-=caco3+2h2o+co32-
2h2o+2cl-=cl2+h2+2oh-
苯o+co3+h2o=hco3-+苯oh
2fe2++4br++3cl2=6cl-+fe3++2br2
cl2+h2o=h++cl-+hclo
fe2o3+6hi=3h2o+2fei3
co32-+h2o=hco3-+oh-
ba2++2oh-+2h++so42-=baso4+2h2o
2nh3h2o+co32-=(nh4)2co3+2oh-1年前查看全部
- 等物质的量浓度氯化钠.氯化镁.氯化铝三种溶液的体积之比为1:1:1,则三种溶液的中氯离子的浓度之比为------
 512051301年前3
512051301年前3 -
 mhenry 共回答了22个问题
mhenry 共回答了22个问题 |采纳率100%设物质的量都为1mol,体积都为1L
那么氯化钠的物质的量浓度=1mol/L 其中氯离子=1mol/L
氯化镁的物质的量浓度=1mol/L 其中氯离子=2mol/L
氯化铝的物质的量浓度=1mol/L 其中氯离子=3mol/L
所以为1:2:31年前查看全部
- 电解氯化镁是否生成沉淀?以石墨棒作为电极
 fkloveqf1年前4
fkloveqf1年前4 -
 又被你雷倒了 共回答了24个问题
又被你雷倒了 共回答了24个问题 |采纳率87.5%看用什么电解棒了
溶液为 MgCl2 + 2H2O === Cl2 + Mg(OH)2 + H21年前查看全部
- 氯化镁为什么不能和碳酸氢钠反应大神们帮帮忙
氯化镁为什么不能和碳酸氢钠反应大神们帮帮忙
RT,一个呈酸性,一个碱性,为什么还不能反应 chrestine1年前1
chrestine1年前1 -
 ai宝de_缃 共回答了16个问题
ai宝de_缃 共回答了16个问题 |采纳率87.5%NaHCO3虽然呈碱性,但是很弱,而Mg(OH)2好歹也是中强碱,不会发生双水解互促到底的.而Mg(HCO3)2是可溶的,而且只要浓度不是很大是可以存在在溶液里的,所以也能不能发生复分解反应.1年前查看全部
- 利用海水淡化后母液中含有的氯化镁和海边盛产的贝壳(主要成分CaCO3),制取金属镁,生产大致流程如图所示:
利用海水淡化后母液中含有的氯化镁和海边盛产的贝壳(主要成分CaCO3),制取金属镁,生产大致流程如图所示:
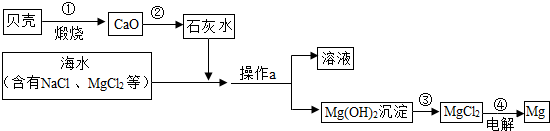
(1)请写出母液中氯化镁转化为氢氧化镁的化学方程式:______.
(2)操作a的名称是______.
(3)工业上常以氯化镁为原料,电解就可以生产金属镁.反应的化学方程式为MgCl2
Mg+X.X的化学式是______.通电 . 五叶虫1年前1
五叶虫1年前1 -
 zo6ht 共回答了13个问题
zo6ht 共回答了13个问题 |采纳率76.9%解题思路:(1)根据氯化镁转化为氢氧化镁的反应,写出反应的化学方程式;
(2)根据实验的操作分析操作的名称;
(3)根据质量守恒定律反应前后原子的种类及数目不变分析X的化学式.(1)由反应的流程可知,氯化镁转化为氢氧化镁的反应是氯化镁与氢氧化钙反应生成了氢氧化镁沉淀和氯化钙,反应的化学方程式是:MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;
(2)由反应的流程可知,操作a是将固液分开,操作的名称是过滤;
(3)在化学方程式为MgCl2
通电
.
Mg+X中,左边有镁原子1个,氯原子两个,右边有镁原子1个,由质量守恒定律反应前后原子的种类及数目不变可知,X的化学式是:Cl2.
故答为:Ⅰ.(1)MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;(2)过滤;(3)Cl2.点评:
本题考点: 物质的相互转化和制备;碳酸钙、生石灰、熟石灰之间的转化;盐的化学性质;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题涉及到镁的生产过程,所考查知识点较多,但都较简单,所以题目本身不难.1年前查看全部
- 完全沉淀相同体积的氯化钠.氯化镁.氯化铝溶液中的Cl离子,消耗相同浓度同体积的硝酸银溶液,则原氯化钠.氯化镁.氯化铝溶液
完全沉淀相同体积的氯化钠.氯化镁.氯化铝溶液中的Cl离子,消耗相同浓度同体积的硝酸银溶液,则原氯化钠.氯化镁.氯化铝溶液的物质的量的浓度之比为
A.1:2:3 B.3:2:1 C.9:3:1 D.6:3:2 西域静子1年前2
西域静子1年前2 -
 flygloom 共回答了21个问题
flygloom 共回答了21个问题 |采纳率90.5%D
三者n(Cl-)相同,所以:
c(Cl-)=c(NaCl)=2c(MgCl2)=3c(AlCl3)
=>c(NaCl):c(MgCl2):c(AlCl3)=6:3:2 (别算错了哦!)1年前查看全部
- 氯化镁是一种盐,请按要求写一个生成氯化镁的化学方程式.
氯化镁是一种盐,请按要求写一个生成氯化镁的化学方程式.
(1)置换反应______;
(2)中和反应______;
(3)碱性氧化物和酸反应______;
(4)盐和酸反应______;
(5)盐和盐反应______. qfwj6661年前1
qfwj6661年前1 -
 星期111 共回答了18个问题
星期111 共回答了18个问题 |采纳率100%(1)镁与稀盐酸反应生成氯化镁和氢气.
该反应由一种单质和一种化合物反应生成另一种单质和另一种化合物,符合置换反应的概念.
该反应的化学方程式为:Mg+2HCl=MgCl 2 +H 2 ↑.
(2)氢氧化镁与稀盐酸反应生成氯化镁和水.
该反应由酸与碱反应生成盐和水,符合中和反应的概念,属于中和反应.
该反应的化学方程式为:Mg(OH) 2 +2HCl=MgCl 2 +2H 2 O.
(3)氧化镁与稀盐酸反应生成氯化镁和水.
氧化镁属于碱性氧化物,稀盐酸是酸,符合碱性氧化物与酸反应的要求.
该反应的化学方程式为:MgO+2HCl=MgCl 2 +H 2 O.
(4)碳酸镁和稀盐酸反应生成氯化镁、水和二氧化碳.
碳酸镁属于盐,稀盐酸是酸,符合盐和酸反应的要求.
该反应的化学方程式为:MgCO 3 +2HCl=MgCl 2 +H 2 O+CO 2 ↑.
(5)碳酸镁和氯化钙反应生成氯化镁和碳酸钙.
碳酸镁和氯化钙都属于盐,符合盐和盐反应的要求.
该反应的化学方程式为:MgCO 3 +CaCl 2 =MgCl 2 +CaCO 3 ↓.
故答案为:
(1)Mg+2HCl=MgCl 2 +H 2 ↑;
(2)Mg(OH) 2 +2HCl=MgCl 2 +2H 2 O;
(3)MgO+2HCl=MgCl 2 +H 2 O;
(4)MgCO 3 +2HCl=MgCl 2 +H 2 O+CO 2 ↑;
(5)MgCO 3 +CaCl 2 =MgCl 2 +CaCO 3 ↓.1年前查看全部
- 硝酸银、氢氧化钾、硫酸、氯化钡、碳酸钠、盐酸、氯化镁、氢氧化钠、硫酸钠、硝酸钡、氯化钙、氯化钾、硝酸镁、
 longhr1年前0
longhr1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 氯化镁的用途有哪些?请问氯化镁有哪些用途,
 liurui5551年前1
liurui5551年前1 -
 vv之花街大少 共回答了22个问题
vv之花街大少 共回答了22个问题 |采纳率90.9%1.冶金行业:用以制造耐火材料和砌炉臂的粘合剂,并是制造二号熔剂和冶炼金属镁的原料.
2.化学工业:主要用于制作各种镁盐,如氧化镁、氢氧化镁,碳酸镁,也用作防冻剂的原料.
3.建筑材料:与菱苦土(MgO)制成坚硬的耐腐蚀的镁氧水泥,可制成人造大理石,苦土瓦,地板,天花板,装饰板,防火板,大棚支架,隔墙板,菱镁井盖,浴缸,门窗框以及活动房屋等.
4.机械工业:生活中,用菱苦土可制成机械包装箱,三角垫棱和家具等,是“以土代料”的好材料.
5.食品行业:用卤水(氯化镁水溶液)点制的豆腐较石点制的豆腐,质嫩味鲜,部分食品的添加剂.
6.交通行业:用作道路化冰融雪剂,化冰速度快,对车辆腐蚀性小,高于氯化钠效果.
7.医药:用氯化镁制成“卤干”可作药用.
8.农业:可用做制镁肥,钾镁肥和棉花脱叶剂.1年前查看全部
- 1g氯化镁中含有 ____个氯离子.
 ashley_10161年前3
ashley_10161年前3 -
 junjunmars 共回答了21个问题
junjunmars 共回答了21个问题 |采纳率90.5%n氯=2n氯化镁=2*95/NA1年前查看全部
- 已知由海水制得的粗盐中含有的主要成分为氯化钠,还有不溶性泥沙,可溶性氯化钙,氯化镁以及硫酸盐,设计实验提纯氯化纳
 yqbtb8131年前1
yqbtb8131年前1 -
 苗玉 共回答了20个问题
苗玉 共回答了20个问题 |采纳率95%这到题目我读书的的时候化学书上有,建议你仔细看看一下书1年前查看全部
- 下列实验方案中合理的是 A.鉴别氯化铝和氯化镁溶液:分别滴加过量的氢氧化钠溶液 B.除去氯化铵溶液中的氯化铁:向溶液中滴
下列实验方案中合理的是
A.鉴别氯化铝和氯化镁溶液:分别滴加过量的氢氧化钠溶液 B.除去氯化铵溶液中的氯化铁:向溶液中滴加适量氢氧化钠溶液,过滤 C.除去苯中的苯酚:向溶液中加入浓溴水,过滤 D.检验溴乙烷中的溴元素:在溴乙烷中滴入氢氧化钾溶液加热后,用稀硝酸酸化再滴加硝酸银溶液  yimuy1年前1
yimuy1年前1 -
 edcrfvtgb1 共回答了20个问题
edcrfvtgb1 共回答了20个问题 |采纳率80%AD
B中除去氯化铵溶液中的氯化铁:向溶液中滴加适量氨水,过滤;C中除去苯中的苯酚:向溶液中加入氢氧化钠溶液,分液。1年前查看全部
- 已知氯化镁、氢氧化镁、碳酸镁、硫酸镁四种物质都能和某些物质反应生成化合物,那是什么?
 baccabac1年前3
baccabac1年前3 -
 andy凯 共回答了11个问题
andy凯 共回答了11个问题 |采纳率90.9%硝酸银
速度给分啊!1年前查看全部
- (2008•塘沽区一模)将氯化镁和氯化钠的固体混合物25g,加入密度为1.2g/cm3、溶质的质量分数为20%的氢氧化钠
(2008•塘沽区一模)将氯化镁和氯化钠的固体混合物25g,加入密度为1.2g/cm3、溶质的质量分数为20%的氢氧化钠溶液50mL,充分反应后,过滤;所得滤液显碱性,在此碱性滤液中加入73g溶质的质量分数为5%的盐酸,恰好完全反应.求恰好完全反应时,滤液的溶质质量分数.
 luo_76611年前1
luo_76611年前1 -
 vcitorwoo520 共回答了19个问题
vcitorwoo520 共回答了19个问题 |采纳率84.2%50mL氢氧化钠溶液中NaOH的质量为:50mL×1.2g/cm3×20%=12g;盐酸中HCl的质量为:73g×5%=3.65g(1分)
设与盐酸反应的NaOH的质量为x,生成的氯化钠质量为m1;与NaOH反应的氯化镁的质量为y,生成的氢氧化镁沉淀质量为z,生成的氯化钠质量为m2.
NaOH+HCl═NaCl+H2O
4036.5 58.5
x 3.65g m1
40:x=36.5:3.65g
解之得x=4g(1分)
58.5:m1=36.5:3.65g
解之得 m1=5.85g
与氯化镁反应的NaOH的质量为:12g-4g=8g
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
95 8058 117
y 8gz m2
95:y=80:8g
解得y=9.5g
58:z=80:8g
解得z=5.8g
117:m2=80:8g
解得 m2=11.7g
则原混合物中氯化钠的质量为25g-9.5g=15.5g
最后得到的溶液中的氯化钠的质量为15.5g+5.85g+11.7g=33.05g
滤液的溶质质量分数为[33.05g/60g+73g+25g−5.8g]×100%≈21.7%
答:恰好完全反应时,滤液的溶质质量分数为:21.7%.1年前查看全部
- 如何除去氯化镁中的氯化铝,求完整的化学方程式,
 灌水就灌纯净水1年前1
灌水就灌纯净水1年前1 -
 你就是那毛毛虫 共回答了13个问题
你就是那毛毛虫 共回答了13个问题 |采纳率92.3%加入过量氢氧化钠 过滤 将沉淀溶于稀盐酸1年前查看全部
- 氯化镁溶液是什么颜色?氯化镁固体呢?
 略带忧郁1年前1
略带忧郁1年前1 -
 闲云自在 共回答了13个问题
闲云自在 共回答了13个问题 |采纳率92.3%无色溶液
高纯的是青白色片状
六水是青色块状1年前查看全部
- 在2008年春节期间,许多遭受雪灾的地区使用氯化钠、氯化镁等融雪盐除雪.下列有关说法正确的是( )
在2008年春节期间,许多遭受雪灾的地区使用氯化钠、氯化镁等融雪盐除雪.下列有关说法正确的是( )
A.撒了融雪盐的积雪融化后对周边的植被及河流没有影响
B.融雪盐能与冰反应生成水
C.应大力推广使用融雪盐去除道路积雪
D.过量使用融雪盐会加速钢铁桥梁的腐蚀 留在唐朝1年前1
留在唐朝1年前1 -
 微笑的真诚 共回答了15个问题
微笑的真诚 共回答了15个问题 |采纳率100%解题思路:A.融雪盐会污染绿地河流;
B.对根据融雪盐的成分来确定其性质;
C.根据融雪盐的使用产生的危害来回答判断;
D.原电池能加快化学反应的速率.A.融雪盐会污染绿地河流,撒了融雪盐的积雪不宜往绿地、河流中倾倒,故A错误.
B.融雪盐氯化钠、氯化镁都不能与冰反应,故B错误;
C.融雪盐会污染绿地河流,不大力推广使用融雪盐去除道路积雪,故C错误;
D.融雪盐作为电解质,与钢铁中的铁和碳构成原电池,原电池能加快化学反应的速率,会加速钢铁桥梁的腐蚀,故D正确;
故选D.点评:
本题考点: 氯、溴、碘及其化合物的综合应用.
考点点评: 本题考查融雪盐及它产生的污染,难度不大,注意目前世界上使用的融雪盐主要有四种,包括氯化钠、氯化钙、氯化镁和氯化钾,统称作“融雪盐”.1年前查看全部
- 如何用酸和碱反应得到氯化镁
 yn8204061年前6
yn8204061年前6 -
 wwwlihua 共回答了21个问题
wwwlihua 共回答了21个问题 |采纳率95.2%2HCl+Mg(OH)2===MgCl2+2H2O1年前查看全部
- 把氢氧化钠 氯化镁 氯化铝 三种固体组成的混合物溶于足量的水中
 lthh24_bcj1ab31年前1
lthh24_bcj1ab31年前1 -
 王老虫 共回答了18个问题
王老虫 共回答了18个问题 |采纳率94.4%110ml.,C点以后的反应是:Al(OH)3+3HCl=AlCl3+3H2O,用HCl60,Mg(OH)2+2HCl=MgCl2+H2O用20,加上前面图片上用的301年前查看全部
- 粗食盐中的硫酸钠.氯化镁等可溶性杂质,应用化学方法使其转化为氯化钠.试剂的加入顺序可以是什么?【两种
 超级Q版yy1年前1
超级Q版yy1年前1 -
 水土流失s 共回答了17个问题
水土流失s 共回答了17个问题 |采纳率82.4%先加入过量氢氧化钡,再加入过量碳酸钠,再加入足量的盐酸1年前查看全部
- 一块镁、铝合金溶于盐酸中,加入足量的苛性钠溶液.此时溶液存在A氯化镁B氯化铝C偏铝酸钠D氢氧化镁
 sunnylj1年前3
sunnylj1年前3 -
 上海-安然 共回答了17个问题
上海-安然 共回答了17个问题 |采纳率82.4%C偏铝酸钠
注意:氢氧化镁 是沉淀1年前查看全部
- 16.为了鉴别氯化镁、硫酸钾、氯化钠三瓶无色溶液,依下表进行实验,试推断加入试剂①,②,③各是什么物质?图在
16.为了鉴别氯化镁、硫酸钾、氯化钠三瓶无色溶液,依下表进行实验,试推断加入试剂①,②,③各是什么物质?图在
①是______,②是______,③是______.
请说明是怎么判断的 苏祁1年前1
苏祁1年前1 -
 lingerwang 共回答了18个问题
lingerwang 共回答了18个问题 |采纳率83.3%1是硝酸银,2是硝酸钡,3是氢氧化钠或者氢氧化钾.
加入1后出现沉淀,沉淀加入2后出现出了钡粒子和硝酸根和氯粒子,那么加入1产生的沉淀应该是氯化银,那么再往下推2肯定就是硝酸钡了.再看加入1后的氯液加入3以后出现氢氧化镁沉淀,那么加入的3肯定是碱.再看下面的阳离子只有钾粒子跟钠粒子,那么应该是氢氧化钾或者氢氧化钾.
再将1、2、3带入去看,发现结果相同,所以应该是他们.1年前查看全部
- 有一个包粉末,可能由氯化钠、硫酸铁、氯化镁、硝酸钠、碳酸钠中的一种或几种组成.
有一个包粉末,可能由氯化钠、硫酸铁、氯化镁、硝酸钠、碳酸钠中的一种或几种组成.
现做下列实验:①取少量粉末,加水溶解得无色透明溶液;②在上述溶液里,加氢氧化钠溶液,无明显变化;③另取少量固体,加稀盐酸,无明显变化.
根据上述实验,试回答:
(1)从实验①推断,不可能存在______(填化学式),原因是_________.
从实验②推断,不可能存在______(填化学式),原因是_________.
从实验③推断,不可能存在______(填化学式),原因是_________.
(2)根据上述实验,可得出初步结论,该粉末中可能含有_________.
(3)若该白色粉末只有一种物质,要证明是什么物质,则需取少量原粉末,装入试管
再加入少量水溶解,然后加入_____试剂,根据____________现象进行判断. 王佳年12041年前3
王佳年12041年前3 -
 小蛋113 共回答了13个问题
小蛋113 共回答了13个问题 |采纳率84.6%①取少量粉末,加水溶解得无色透明溶液;--------没有Fe2(SO4)3,它的溶液是黄色的,另外注意MgCl2与Na2CO3不能共存
②在上述溶液里,加氢氧化钠溶液,无明显变化;-----------没有MgCl2
③另取少量固体,加稀盐酸,无明显变化.----------没有Na2CO3
可能存在NaCl、NaNO3中的1种或2种
(1)从实验①推断,不可能存在___Fe2(SO4)3___(填化学式),原因是____它的溶液显黄色_____.
从实验②推断,不可能存在___MgCl2___(填化学式),原因是_____会与NaOH生成Mg(OH)2白色沉淀____.
从实验③推断,不可能存在___Na2CO3___(填化学式),原因是____会与盐酸反应生成CO2气体_____.
(2)根据上述实验,可得出初步结论,该粉末中可能含有____NaCl和NaNO3中的1种或者2种_____.
(3)若该白色粉末只有一种物质,要证明是什么物质,则需取少量原粉末,装入试管
再加入少量水溶解,然后加入__AgNO3溶液___试剂,根据_____有无白色沉淀_______现象进行判断.1年前查看全部
- 如何不用其它试剂鉴别氢氧化钠,硫酸铜,氯化镁,硫酸钠
 hdjhlp1年前3
hdjhlp1年前3 -
 gunaijin 共回答了16个问题
gunaijin 共回答了16个问题 |采纳率100%1,蓝色的是硫酸铜
2,将硫酸铜加到另三个中,出现蓝色沉淀的是氢氧化钠
3,将氢氧化钠加到另两个中,出现沉淀的是氯化镁
注意,以上操作叙述应是取出少量进行反应,而不是在原瓶中1年前查看全部
- 粗盐提纯中除去可溶性杂质是根据什么除去的?比如氯化镁 硫酸钠..急!
 kean2001cn1年前2
kean2001cn1年前2 -
 五子希 共回答了18个问题
五子希 共回答了18个问题 |采纳率88.9%根据物质溶解性.生成溶解性小的物质而除去.
氯化镁——加氢氧化钠,生成氢氧化镁沉淀
硫酸钠——加氯化钡,生成硫酸钡沉淀1年前查看全部
大家在问
- 1奥数问题,高手请进“如果将一个立方体的六个面分别用红和黄两种颜色着色,那么一共可得到( )种不同着色的立方体(如果着色后
- 2听话听声,锣鼓听音的表面意思和实际意思
- 3下列关于甲烷结构的说法错误的是( ) A.甲烷分子中的化学键都是共价键 B.甲烷分子为正四面体结构 C.甲烷分子为正四
- 4已知三个有理数a,b,c的积为正数,和为负数,当x=|a|/a+|b|/b+|c|/c时,试求代数式x2011次方-20
- 5后追加100分我不懂一个问题:什么:主语+be动词+动词要求(第一、二、三人称)什么时候加s,或者.我就是不懂什么喜欢不
- 6(2010•福建模拟)下列相关实验不能达到预期目的是( )
- 7一块梯形玻璃,上底是14分米,下底是26分米,高是18分米.如果每平方分米的玻璃价钱是0.6元,那么买15块的
- 8有关期待的作文,四百字以上,五百字以下
- 9已知x=1是关于一元一次方程ax-1=2(x-b)的解,y=1是关于y的一元一次方程b(y-3)=2(1-a)的解.在y
- 10WINDOWS 9X是一种( )操作系统(选项在补充中)
- 11英语翻译后一句是:居则至其敬译到“然后能事亲”
- 12英语里of的用法.特别是一串of
- 13一张长方形纸片的周长是18厘米,2张这样的长方形纸片恰好可以拼成一个大正方形纸片.这张大正方形纸片的周长是多少厘米?亲们
- 14关于压强的初中题1.a,b两个由同种材料制成的圆柱体,它们的高度相同,质量之比m1:m2=3:5,把它们竖直放置在水平桌
- 15英语翻译我想知道狗形容人的N种翻译是?而且请高手帮我翻译一下这几个句子,都是用来形容人的!He is a luck do
