CCI4和CIO2的俗称
 NANA唯一2022-10-04 11:39:541条回答
NANA唯一2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 泥巴巴123 共回答了21个问题
泥巴巴123 共回答了21个问题 |采纳率95.2%- CCI4,四氯化碳,俗称:四氯甲烷.
CIO2,二氧化氯,俗称:亚氯酸酐,氯酸酐. - 1年前
相关推荐
- 三养化二铁和四养化三铁的俗称是什么?
三养化二铁和四养化三铁的俗称是什么?
精确点! 8119689091年前1
8119689091年前1 -
 天降丑石 共回答了14个问题
天降丑石 共回答了14个问题 |采纳率100%三氧化二铁的俗称是铁锈.在空气中灼烧亚铁化合物或氢氧化铁等可得三氧化二铁.四氧化三铁 别名 :磁性氧化铁、氧化铁黑、磁铁、磁石、吸铁石、偏铁酸亚铁1年前查看全部
- 管理者代表俗称管代用英文怎么说啊
管理者代表俗称管代用英文怎么说啊
如题 浪迹江南5181年前4
浪迹江南5181年前4 -
 wangwang20061212 共回答了26个问题
wangwang20061212 共回答了26个问题 |采纳率96.2%管理者 = MANAGEMENT ,代表 = REPRESENTATIVE
MANAGEMENT REPRESENTATIVE1年前查看全部
- 用纱布包住面团用清水洗,最后会在纱布上留下俗称“面筋”的物质.说明面筋是________
 zxkml1年前1
zxkml1年前1 -
 这个估计没人用 共回答了13个问题
这个估计没人用 共回答了13个问题 |采纳率84.6%洗出来的1年前查看全部
- 问一到化学题为改良酸性土壤,可施用适量的碱是( )【填俗称】,用化学方程式说明这种碱的溶液放置在空气中变质的原因:( )
问一到化学题
为改良酸性土壤,可施用适量的碱是( )【填俗称】,用化学方程式说明这种碱的溶液放置在空气中变质的原因:( ). 吾言wy1年前1
吾言wy1年前1 -
 无盐301 共回答了19个问题
无盐301 共回答了19个问题 |采纳率94.7%可施用适量的碱是( 熟石灰 ).
用化学方程式说明这种碱的溶液放置在空气中变质的原因:
( Ca(OH)2+CO2==CaCO3+H2O ).1年前查看全部
- 碳酸钠俗称纯碱,因其水溶液显碱性而得名,实验室现有白醋,食盐水和碳酸钠三瓶溶液,请设计实验鉴别它们
碳酸钠俗称纯碱,因其水溶液显碱性而得名,实验室现有白醋,食盐水和碳酸钠三瓶溶液,请设计实验鉴别它们
现在就要,快, fireontina1年前3
fireontina1年前3 -
 zxc8709 共回答了19个问题
zxc8709 共回答了19个问题 |采纳率94.7%将碳酸钠溶于水,滴加无色酚酞,由于其水溶液显碱性,所以酚酞变红;在白醋和食盐水中滴加无色酚酞,不变红.
白醋和食盐水闻气味,或将Zn或Fe放入二者,有气泡产生则为白醋,或向在二者中滴加氯化银溶液,有沉淀生成为食盐水.1年前查看全部
- ⑤为初中化学一些常见物质的相互转化关系(反应条件已略去),其中C的固体俗称“干冰”,
⑤为初中化学一些常见物质的相互转化关系(反应条件已略去),其中C的固体俗称“干冰”,
L分子中各原子个数比为1﹕2﹕2,⑤为置换反应.① A+B→C ② D→B+E ③ C+L→F+D ④ M+K→C+G ⑤ G+H→E+N
⑴B、C、F、L的化学式分别为 、 、 、 .
⑵写出符合反应④的一个化学方程式 .
⑶写出符合反应⑤的一个化学方程式 .
第二小题能否写成Fe3O4+2C=3Fe+2CO2 9benduck1年前1
9benduck1年前1 -
 风月无恒 共回答了22个问题
风月无恒 共回答了22个问题 |采纳率90.9%(1)B、C、F、L的化学式分别为
O2、CO2、CaCO3、Ca(OH)2
(2)写出符合反应④的一个化学方程式
3CO+Fe2O3高温 = 2Fe+3CO2
(3)写出符合反应⑤的一个化学方程式
Fe+2HCl=FeCl2+H2↑(或Fe+H2SO4=FeSO4+H2↑)
.
由C的固体俗称“干冰”,L分子中各原子个数比为1:2:2,我们可以大胆的断定C为二氧化碳;L为氢氧化钙.所以F和D一种为碳酸钙另一种为水.由①A+B→C可得一种为碳一种为氧气,又由②D→B+E和③C+L→F+D可知D为水,B为氧气,E为氢气,A为碳,F为碳酸钙,D为水.由⑤为置换反应和G+H→E+N,所以可推断G和H一种是活泼金属,一种是酸.④是有二氧化碳生成的反应,在初中常见的就是一氧化碳还原金属氧化物.1年前查看全部
- 阅读理解、分析. 阅读理解、分析. 为什么夏天那么热还会下冰雹 ①冰雹,俗称雹子,在春末和夏季最为常见,它小如绿豆、
阅读理解、分析.
阅读理解、分析. 为什么夏天那么热还会下冰雹①冰雹,俗称雹子,在春末和夏季最为常见,它小如绿豆、黄豆,大似栗子、鸡蛋,特大的冰雹比柚子还大.***各地每年都会遭不同程度的雹灾. 2005年6月,一场罕见的大冰雹突袭北京:许多汽车在这次特大冰雹中遭了殃,车窗穿孔,车顶被砸成了麻子脸
②在春末和夏季,有时早晨天气还非常晴朗,可是中午前后突然下起了冰雹.夏天的气温那么高,为什么会下冰雹呢?而冬天天气寒冷却不落冰雹,这是什么原因呢?
③如果你在夏天爬过山的话,一定记得在山顶上早上和晚上还是非常凉快的,还要穿毛衣和棉衣.在海拔4~5千米的山顶上有着终年不化的积雪和冰川.这就说明了,随着高度的升高,气温也在不断下降.在高山顶上如此,那高空应该更是这样吧!事实上,高空中的云,即使在夏季,温度也在o℃以下.
④夏天太阳炙烤大地,在大气层中,有着大量的水汽的热气流,迅速地向高空上升.这时,地面上虽然很热,但是在高空中却依然很冷.当湿热空气进入到高空并冷却下来时,它夹带的一小部分水汽凝结成小水滴;当小水滴继续变冷时,就被冻成小冰晶了.小冰晶从高空降落下来,在降落的同时兼并了很多温度低于o℃的小水滴,在自己身上冻结,就成了冰粒;有时候在下降的过程中,遇到一股由下往上吹的强风,也就是我们通常所说的上升气流,又再一次把它带回到空中去.这些小冰粒在高空中再度受冷,与温度低于o℃的小水滴碰撞在一起,并兼并它们,把小水滴冻结在自已身上,因此它的表面上又包上了一层冰.就是这样,它在空中不停的翻腾,不断与温度低于0℃的小水滴相碰撞,穿上一件又一件冰做的外衣,一直到变成一定的重量时,上升气流无法再把它带到高空时,于是就一落千丈,从高空中降落下来——下冰雹了.拾起冰雹,用刀子破开,你会发现它的纵剖面层次分明,那是在高空中冰雹所穿的几层冰衣与雪服.
⑤冰雹是在积雨云和强烈的空气形成对流运动过程中产生的. 而在冬天,空气比较稳定,上下的“气流差”不像夏天那样大,空气垂直对流运动不像夏天那么强烈,积雨云不容易发生 ,所以冰雹不容易发生.(选自《品味一生的99篇科学美文》,文/张震越,略有删改)
1.第①段中划线的句子运用了_________和打比方这两种说明方法,具体形象地说明了冰雹的____________________________.
第⑤段中画线的句子运用了_________的说明方法,是为了说明____________________________.
2.细读第④段,将下面冰雹形成过程的示意图补充完整.
水汽→()→()→()→冰雹
3.第④段中加粗的词语“一件又一件”,为什么不能改成“一件”?请结会语境,说说你的理解.
________________________________________________ LL9451年前1
LL9451年前1 -
 rr如风3029 共回答了23个问题
rr如风3029 共回答了23个问题 |采纳率91.3%1.举例子危害(破坏性)
作比较冬天不容易下冰雹的原因(夏天容易下冰雹的原因)
2.小水滴(水滴)小冰晶(冰晶)冰粒(小冰粒)
3.“一件”不能准确说明冰粒在空中不停翻腾,与低温小水滴不断碰撞后形成冰雹的过程(“一件又一件”)准确说明冰粒在空中不停翻腾,与低温小水滴不断碰撞后形成冰雹的过程1年前查看全部
- ________色的孔雀石主要成分是________________(俗称_________).
________色的孔雀石主要成分是________________(俗称_________).
________色的孔雀石主要成分是________________(俗称_________)
硫酸铜晶体(俗称_________、__________),无水硫酸铜是________色的.1nm=_____m e819052531年前1
e819052531年前1 -
 遇雨微微 共回答了23个问题
遇雨微微 共回答了23个问题 |采纳率91.3%翠绿色,碱式碳酸铜,铜绿
胆矾、蓝矾,蓝色,10的-9次方1年前查看全部
- 某学校化学课外活动小组,对铜制品生锈很很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为
某学校化学课外活动小组,对铜制品生锈很很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为
Cu2(OH)2CO3.他们在探究中发现,铜绿受热分解后,除生成二氧化碳和水蒸气外,试管中还有一些黑色粉末状固体.为了更清楚地了解这种黑色粉末,小明和小娜准备通过实验探究,进一步分析黑色固体的组成,并验证产生的气体:
(1)提出问题:黑色固体是什么?
(2)猜想与假设:
(3)设计实验方案:
向试管中的黑色固体滴加足量的______(填化学式)溶液,充分反应后,观察固体的溶解情况和所得溶液的颜色;
(4)现象与结论:
小刚和小娜经过实验之后,都给自己的猜想做了正确的评价.如果你的猜想是正确的话,实验现象应为:______.
(5)若用如图所示装置验证两种气体生成物(无水硫酸 铜遇水变蓝),应将生成的混合气体先通过______装置,.当将气体通入装置A进行验证,气流应从______口通入.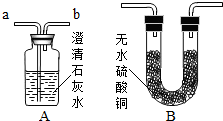
 闷灯儿1年前1
闷灯儿1年前1 -
 总不该又重名了吧 共回答了22个问题
总不该又重名了吧 共回答了22个问题 |采纳率95.5%解题思路:(2)根据质量守恒定律结合小刚和小娜的猜想来进行推测;
(3)根据推测黑色的粉末可以选择酸来进行判断该黑色粉末的组成;
(4)根据自己所作出的猜想来进行判断,得出实验现象;
(5)验证是否产生了水可以用无水硫酸铜,但是要最先进行验证,以防在后续操作中吸收了水分,而干扰了实验现象.(2)碱式碳酸铜中含有碳元素、铜元素、氧元素和氢元素,根据质量守恒定律结合小娜和小刚的推测,可以判断该黑色粉末为氧化铜和碳的混合物;
(3)根据黑色粉末的组成,可以选择稀硫酸、稀盐酸或是稀硝酸来进行鉴别,如果得到蓝色溶液则说明该黑色粉末为氧化铜,若黑色粉末不溶解则说明为碳粉;
(4)若黑色粉末为氧化铜和碳粉,当加入稀硫酸时氧化铜要溶解而生成蓝色溶液,但是碳粉不反应,即如果观察到黑色粉末部分溶解,则说明我们刚才的判断是正确的;
(5)无水硫酸铜吸收水后变为蓝色,所以在验证水时通常用无水硫酸铜,但是为了防止在后续的实验中引入水蒸气而干扰实验,所以要先验证水的存在,然后再来验证二氧化碳的存在,在验证二氧化碳即通过B装置时,要从长管即a管进入.
故答案为:(2)如图
(3)H2SO4(HCl、HNO3也可);
(4)黑色粉末部分溶解,溶液由无色变成蓝色;
(5)B;a;点评:
本题考点: 实验探究物质的组成成分以及含量;猜想与事实验证;常见气体的检验与除杂方法;碳的化学性质.
考点点评: 熟练掌握质量守恒定律的实质,能够根据质量守恒定律来判断反应后生成的物质,记住三种常见的黑色粉末:碳、氧化铜和二氧化锰.1年前查看全部
- 阅读短文,回答问题:一般手电筒都有一个俗称灯窝的东西,灯窝相当于一面凹面镜,它有聚光焦点.当光源在焦点上时,光就会被强烈
阅读短文,回答问题:
一般手电筒都有一个俗称灯窝的东西,灯窝相当于一面凹面镜,它有聚光焦点.当光源在焦点上时,光就会被强烈地反射出来,近似地形成平行光,这样手电筒的光就能照亮较远的地方,避免发散的光照到远处时就很快地变暗.然而,钢笔型电筒、打火机电筒等微型电筒并没有灯窝,它们发出来的光也能近似平行射出,这是什么原因呢?
这要从微型电筒的电珠分析入手,微型电筒使用的电珠和普通的电珠不同,它顶端玻璃很厚,呈半圆形,恰好是一个凸透镜,能起聚光作用,所以不用灯窝也能使电珠发出的光近似于平行地射出.
(1)一般手电筒得到近似的平行光,是把光源放在凹面镜的焦点上,利用凹面镜的“从焦点射向凹面镜的光经凹面镜______后平行射出”这一性质制成的.
(2)微型手电筒得到近似的平行光,是把光源放在凸透镜的______上,利用凸透镜的“从______射向凸透镜的光经凸透镜______后平行射出”这一性质制成的.
(3)请你列举出一种与一般手电筒或微型手电筒非常相似的应用______.
(4)通过阅读以上的一段文章,你还可以知道:同样的一束光线照射到物体的表面,光照面的明亮程度与光照面的面积、光源距光照面的距离有关,光照面的面积越______,光照面上亮度就越小. 雷动九天1年前1
雷动九天1年前1 -
 432713 共回答了21个问题
432713 共回答了21个问题 |采纳率81%解题思路:(1)面镜对光有反射作用;(2)经过凸透镜焦点的光线经凸透镜折射后平行于凸透镜的主光轴.灯泡尖端很厚、呈半圆形的玻璃是凸透镜,灯丝放在凸透镜的焦点上,光线经过凸透镜折射后是平行光线.(3)利用凹面镜或凸透镜可获得平行光,应用还有汽车前灯等.(4)同样的一束光线照射到物体的表面,光源距光照面的距离一定,所照光面越大,物体单位面积上的光线越少,光照面上亮度就越小.(1)面镜对光有反射作用,从焦点射向凹面镜的光经凹面镜反射后平行射出;
(2)灯泡尖端很厚、呈半圆形的玻璃是凸透镜,灯丝放在凸透镜的焦点上,光线经过凸透镜折射后是平行光线.
(3)利用凹面镜或凸透镜可获得平行光.汽车前灯内有一凹面镜,把光源放在凹面镜的焦点处,经凹面镜反射后得到一束平行光.
(4)同样的一束光线照射到物体的表面,光照面的明亮程度与光照面的面积、光源距光照面的距离有关,光照面的面积越大,光照面上亮度就越小.
故答案为:(1)反射;
(2)焦点;焦点;折射;
(3)汽车前灯内有一凹面镜,把光源放在凹面镜的焦点处,经凹面镜反射后得到一束平行光;
(4)大.点评:
本题考点: 凸面镜和凹面镜;凸透镜的会聚作用.
考点点评: 考查了学生获取信息的能力,要求平时多注意生活中的现象,并能利用所学知识解释问题.1年前查看全部
- (2011•平顶山二模)气焊和气割都需要用到乙炔.乙炔俗称电石气(化学式为C2H2),是一种无色无味的气体,密度比空气略
(2011•平顶山二模)气焊和气割都需要用到乙炔.乙炔俗称电石气(化学式为C2H2),是一种无色无味的气体,密度比空气略小,难溶于水.实验室常用块状固体碳化钙与水反应制备乙炔,该反应比二氧化锰催化过氧化氢分解更加剧烈.请回答:

(1)写出乙炔的物理性质.
(2)从下图选择实验室制备乙炔所用仪器的最佳组合是______和______(填序号). 大对头1年前1
大对头1年前1 -
 顺便说说可以吧 共回答了19个问题
顺便说说可以吧 共回答了19个问题 |采纳率89.5%解题思路:本题是根据学生已经学习过氧气和二氧化碳的实验室制备,在此基础上结合题中给出乙炔的物理性质和制取反应信息,让同学们自选最佳的组合,体现对气体制取方法的理解和应用.(1)物理性质是不需要通过化学变化表现出来的性质.根据题给信息可知,乙炔俗称电石气(化学式为C2H2),是一种无色无味的气体,密度比空气略小,难溶于水,都是物理性质.
故答案为:无色无味的气体,或密度比空气略小,难溶于水;
(2)根据题给信息可知,制取乙炔反应为固体和液体不需加热的反应,且生成的气体不易溶于水、密度比空气小,制备与制二氧化碳的反应物状态和条件相同,故制备的最佳组合应用能控制反应速度的装置A,收集可选D与E,但该题要求最佳的收集方法(即最纯净的气体),所以应选E排水法进行收集.
故选A;E.点评:
本题考点: 气体制取装置的探究;化学性质与物理性质的差别及应用.
考点点评: 本题综合考查了学生的基本实验能力,涉及装置选择、连接、实验基本操作.重点考查学生对药品的选择、发生装置的选用等方面的能力,掌握知识的程度、深度和广度.1年前查看全部
- 碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2
碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2(OH)2CO3
2CuO+H2O+CO2↑.现将一定量的碱式碳酸铜和铜的粉末放在容器里,在空气中用酒精灯充分加热后冷却,称量,发现加热前后固体的质量相等.据此计算原混合粉末中Cu2(OH)2CO3的质量.△ . 飘翎叶1年前1
飘翎叶1年前1 -
 潘恬恬 共回答了18个问题
潘恬恬 共回答了18个问题 |采纳率94.4%解题思路:根据题意,可知:铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等.铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等;
设原混合物质量为100g,其中碱式碳酸铜的质量为x,则铜的质量为100g-x,生成的水蒸汽和二氧化碳的质量为y;
则根据题意有:
①Cu2(OH)2CO3
△
.
CuO+H2O+CO2↑
222 18+44=62
xy
则[222/x=
62
y],解得y=[62x/222]
②2Cu+O2
△
.
2CuO
12832
100g-xy
[128/100g−x=
32
y],解得y=
32(100g−x)
128
所以得[62x/222]=
32(100g−x)
128,解得x≈47.2g,故
47.2g
100g×100%=47.2%
答:原混合粉末中Cu2(OH)2CO3的质量分数约为47.2%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题是对利用化学方程式计算的考查题,解题的关键是对反应前后质量变化的分析,属于基础性知识考查题.1年前查看全部
- 硫酸铜的结晶水合物俗称胆矾或蓝矾,化学式CuSO 4 •5H 2 O.
硫酸铜的结晶水合物俗称胆矾或蓝矾,化学式CuSO 4 •5H 2 O.
请计算:
(1)该物质的式量是______;
(2)其组成元素的质量比Cu:S:H:O=______. sjsj1529141年前1
sjsj1529141年前1 -
 a_toad 共回答了20个问题
a_toad 共回答了20个问题 |采纳率90%(1)胆矾的化学式为CuSO 4 •5H 2 O;
则胆矾的相对分子质量=64+32+16×4+5×(1×2+16)=250;则胆矾的式量为250.
(2)胆矾的化学式为CuSO 4 •5H 2 O;
则胆矾中Cu、S、H、O元素的质量比为64:32:(1×10):(9×16)=32:16:5:72.
故答案为:
(1)250;
(2)32:16:5:72.1年前查看全部
- 氯酸钾 高锰酸钾 醋酸 乙醇 蔗糖 葡萄糖的化学式 氧化钙 氢氧化钙 氢氧化钠 碳酸钠 碳酸氢钠 甲烷的俗称
氯酸钾 高锰酸钾 醋酸 乙醇 蔗糖 葡萄糖的化学式 氧化钙 氢氧化钙 氢氧化钠 碳酸钠 碳酸氢钠 甲烷的俗称
粗盐纯化的6个步骤
测定酸碱度的4要点 风中高歌1年前3
风中高歌1年前3 -
 爱的气味 共回答了25个问题
爱的气味 共回答了25个问题 |采纳率84%KCLO3 KMnO4 CH3COOH C2H5OH C6H12O6
氧化钙 生石灰 消石灰
氢氧化钙 熟石灰
氢氧化钠 烧碱 火碱
碳酸钠 苏打、纯碱、洗涤碱
碳酸氢钠 小苏打
甲烷 沼气
粗盐提纯6注意
一贴、二低、三靠
一贴:滤纸要紧贴漏斗壁,二低:1是滤纸的边缘要稍低于漏斗的边缘;2是在整个过滤过程中还要始终注意到滤液的液面要低于滤纸的边缘.
三靠:1是待过滤的液体倒入漏斗中时,盛有待过滤液体的烧杯的烧杯嘴要靠在倾斜的玻璃棒上(玻璃棒引流);2是指玻璃棒下端要靠在三层滤纸一边(三层滤纸一边比一层滤纸那边厚,三层滤纸那边不易被弄破);3是指漏斗的颈部要紧靠接收滤液的接受器的内壁.
就是不能提前润湿试纸,然后不能把试纸浸入溶液,要用玻璃棒蘸取少量溶液,然后在溶液滴到试纸上三秒后立即与标准比色板对照.1年前查看全部
- 下列选项中物质的名称、俗称、化学式一致的是( )
下列选项中物质的名称、俗称、化学式一致的是( )
A.碳酸钠、小苏打、Na2CO3
B.氢氧化钠、纯碱、NaOH
C.氢氧化钙、生石灰、CaO
D.氢氧化钙、消石灰、Ca(OH)2 楚天英雄1年前1
楚天英雄1年前1 -
 btbtt 共回答了26个问题
btbtt 共回答了26个问题 |采纳率88.5%解题思路:熟记常见物质的名称、俗名、化学式,如:氢氧化钠、氢氧化钙、氧化钙、碳酸钠等物质;能根据物质化学式的书写规则正确书写物质的化学式.A、碳酸钠的俗名为苏打,化学式为Na2CO3,而小苏打名称为碳酸氢钠,其化学式为NaHCO3,故A错误;B、氢氧化钠的俗名为烧碱,化学式为NaOH,而纯碱的名称为碳酸钠,其化学式为Na2CO3,故B错误;C、氢氧化钙的俗名为熟...
点评:
本题考点: 化学式的书写及意义;常见元素与常见原子团的化合价.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写;熟记常见元素及原子团的化合价.1年前查看全部
- (2014•江苏模拟)次硫酸氢钠甲醛(xNaHSO2•yHCHO•zH2O)俗称吊白块,在印染、医药以及原子能工业中有广
(2014•江苏模拟)次硫酸氢钠甲醛(xNaHSO2•yHCHO•zH2O)俗称吊白块,在印染、医药以及原子能工业中有广泛应用.它的组成可通过下列实验测定:①准确称取1.540 0g样品,完全溶于水配成100mL溶液;②取25.00mL所配溶液经AHMT分光光度法测得甲醛物质的量浓度为0.10mol•L-1;③另取25.00mL所配溶液,加入过量碘完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体0.582 5g.次硫酸氢钠甲醛和碘反应的方程式如下:
xNaHSO2•yHCHO•zH2O+I2-→NaHSO4+HI+HCHO+H2O(未配平)
(1)生成0.582 5g白色固体时,需要消耗碘的质量为______.
(2)若向吊白块溶液中加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物,写出该反应的离子方程式______.
(3)通过计算确定次硫酸氢钠甲醛的组成(写出计算过程).25.00mL的溶液中,NaHSO2的物质的量和NaHSO4的量是相等的,即为[0.5825/233]=0.0025mol,所以甲醛的物质的量为0.0025mol,在100mL溶液中,
NaHSO2的物质的量为4×0.0025mol=0.01mol,所以甲醛的物质的量为0.01mol,水的物质的量为:[1/18](1.540g-88g/mol-0.01mol-1×0.01mol)=0.02mol,所以x:y:z=1:1:2,次硫酸氢钠甲醛的组成为:NaHSO2•HCHO•2H2O.
答:次硫酸氢钠甲醛的组成为:NaHSO2•HCHO•2H2O.25.00mL的溶液中,NaHSO2的物质的量和NaHSO4的量是相等的,即为[0.5825/233]=0.0025mol,所以甲醛的物质的量为0.0025mol,在100mL溶液中,.
NaHSO2的物质的量为4×0.0025mol=0.01mol,所以甲醛的物质的量为0.01mol,水的物质的量为:[1/18](1.540g-88g/mol-0.01mol-1×0.01mol)=0.02mol,所以x:y:z=1:1:2,次硫酸氢钠甲醛的组成为:NaHSO2•HCHO•2H2O.
答:次硫酸氢钠甲醛的组成为:NaHSO2•HCHO•2H2O. 让错纯粹下去1年前1
让错纯粹下去1年前1 -
 aa的aass 共回答了12个问题
aa的aass 共回答了12个问题 |采纳率91.7%解题思路:(1)根据次硫酸氢钠甲醛和碘单质之间反应的化学反应方程式来计算即可;
(2)甲醛会发生自身氧化还原反应,被氧化为甲酸,被还原为甲醇;
(3)根据元素守恒结合物质之间的反应情况来计算.(1)根据反应:xNaHSO2•yHCHO•zH2O+I2→NaHSO4+HI+HCHO+H2O,据电子守恒,生成1mol的NaHSO4,消耗碘单质1mol,硫酸根守恒,得到白色固体0.5825g,即生成硫酸钡的质量是0.5825g,物质的量是0.5825g233g/mol=0.0025...
点评:
本题考点: 复杂化学式的确定.
考点点评: 本题是一道有关物质的分子式的确定题目,考查学生分析和解决问题的能力,综合性强,难度大.1年前查看全部
- 压强俗称压力,单位之间是怎么换算的
 柳永词1年前1
柳永词1年前1 -
 korla7a 共回答了23个问题
korla7a 共回答了23个问题 |采纳率95.7%压强和压力首先不是一个概念,压强等于压力除以受力面积1年前查看全部
- 某盐矿井采出的食盐(俗称井盐)中含有CaCl2,为测定CaCl2的含量;准确称量上述井盐22.8g,向其中加入87.2克
某盐矿井采出的食盐(俗称井盐)中含有CaCl2,为测定CaCl2的含量;准确称量上述井盐22.8g,向其中加入87.2克水使其完全溶解,然后向其中加入100g质量分数为10.6%的Na2CO3溶液,恰好完全反应,且所得食盐溶液仍为不饱和溶液.
求:
(1)井盐中CaCl2的质量.
(2)检测后的溶液中NaCl的质量分数 (结果保留一位小数). yxj_03291年前1
yxj_03291年前1 -
 kk 共回答了18个问题
kk 共回答了18个问题 |采纳率88.9%解题思路:(1)氯化钙和碳酸钠反应满足复分解反应的条件,所以按照复分解反应的定义把二者反应的方程式写出来,根据化学方程式,用碳酸钠的质量可把氯化钙的质量求出来;
(2)因为题目中没提到井盐中除氯化钙外还有其他杂质,所以可认为井盐中除氯化钙外的其他成分都是氯化钠,然后再加上氯化钙和碳酸钠反应生成的氯化钠,就是检测后溶液中溶质氯化钠的质量,再除以检测后溶液的质量就是检测后的溶液中NaCl的质量分数.(1)碳酸钠溶液中溶质Na2CO3的质量为:100g×10.6%=10.6g
设井盐中CaCl2的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111100 117
10.6g x z y
[106/111=
10.6g
x] x=11.1g
(2)井盐中含NaCl的质量为:22.8g-11.1g=11.7g
设反应生成的NaCl的质量为y,生成的CaCO3的质量为z
[106/117=
10.6g
y] y=11.7g
[106/100=
10.6g
z] z=10g
所以检测后溶液中含NaCl的质量为:11.7g+11.7g=23.4g
检测后溶液的质量为:22.8g+87.2g+100g-10g=200g
故检测后的溶液中NaCl的质量分数为:[23.4g/200g]×100%=11.7%
答:(1)井盐中CaCl2的质量为11.1g;
(2)检测后的溶液中NaCl的质量分数为11.7%.点评:
本题考点: 根据化学反应方程式的计算;实验探究物质的组成成分以及含量.
考点点评: 此题是溶质质量分数和化学方程式相结合的计算题,其中用到了求质量分数的公式及其变形,所以同学们一定要牢记此公式,另外要正确求出反应后溶液的质量.此题总起来说不难,就是计算过程有点长,属于中等难度的题目.1年前查看全部
- 总结氢氧化钠和氢氧化钙的物理性质、化学性质、俗称以及用途
 conpaklisa1年前1
conpaklisa1年前1 -
 气氛太糟糕 共回答了18个问题
气氛太糟糕 共回答了18个问题 |采纳率88.9%NaOH:烧碱,火碱,苛性钠.
Ca(OH)2:熟石灰,消石灰,(石灰水,石灰乳).1年前查看全部
- 初中《盐和化肥》知识点1.定义:能分解出( )(或 )和( )的化合物2.氯化钠()俗称() 白色粉末 水溶液有咸味,溶
初中《盐和化肥》知识点
1.定义:能分解出( )(或 )和( )的化合物
2.氯化钠()俗称() 白色粉末 水溶液有咸味,溶液度受温度影响() 用途1作( )2作( ) 3消除()(消除雪的熔点)4 农业上用NACL溶液来( )5制( )(0.9%氯化钠溶液) bent471年前1
bent471年前1 -
 行者蓝 共回答了17个问题
行者蓝 共回答了17个问题 |采纳率82.4%1水,气体,沉淀
2Nacl 食盐 大1年前查看全部
- 氢氧化钠俗称?氢氧化钙俗称?氢氧化钙水溶液俗称?氢氧化钙的物理性质?
 清水盈草1年前9
清水盈草1年前9 -
 雨飘 共回答了26个问题
雨飘 共回答了26个问题 |采纳率92.3%1烧碱,火碱
2熟石灰
3澄清石灰水
4氢氧化钙 细腻的白色粉末.俗名是熟石灰,又名消石灰.相对密度2.24.加热至580℃脱水成氧化钙,在空气中吸收二氧化碳而成碳酸钙.溶于酸、铵盐、甘油,难溶于水,不溶于醇1年前查看全部
- 〔化学--选修2:化学与技术〕锌锰电池(俗称干电池)在生活中的用量很大.两种锌锰电池的构造如图(a)所示.回答下列问题:
〔化学--选修2:化学与技术〕
锌锰电池(俗称干电池)在生活中的用量很大.两种锌锰电池的构造如图(a)所示.回答下列问题:
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2═Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是______,电解质的主要成分是______,正极发生的主要反应是______.
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是______.
(2)图(b)表示回收利用废旧普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金属).
①图(b)中产物的化学式分别为A______,B______.
②操作a中得到熔块的主要成分是K2MnO4.操作b中,绿色的K2MnO4溶液反应生成紫色溶液和一种黑褐色固体,该反应的离子方程式为______.
③采用惰性电极电解K2MnO4溶液也能得到化合物D,则阴极处得到的主要物质是______(填化学式). Best泪1年前1
Best泪1年前1 -
 legalraymond2007 共回答了13个问题
legalraymond2007 共回答了13个问题 |采纳率92.3%解题思路:(1)①根据电池反应判断正负极和电解质;二氧化锰和铵根离子在正极发生反应;
②根据碱性锌锰电池的特点分析;
(2)①根据电池的材料分析;
②根据已知反应物和产物,再利用元素守恒
③K2MnO4溶液中阴极产物的判断,根据溶液中阳离子得电子能力分析.(1)根据化学方程式Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH,反应中Zn被氧化,为电池负极锌,氯化铵是电解质的主要成分,二氧化锰和铵根离子在正极发生反应,MnO2+NH4++e-=MnOOH+NH3.与普通锌锰电池相比,碱性锌锰电池的优点及其理由是碱性电池不易发生电解质的泄露,因为消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因为金属材料在碱性电解质中比在酸性电解质中的稳定性提高;
故答案为:①锌;NH4Cl;MnO2+NH4++e-=MnOOH+NH3②碱性电池不易发生电解质的泄露,因为消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因为金属材料在碱性电解质中比在酸性电解质中的稳定性提高.
(2)废电池经机械分离后,加水溶解后溶液中的成分是氯化铵,再加稀盐酸Zn溶解生成氯化锌,因此浓缩结晶得到氯化铵和氯化锌.氯化铵不稳定,受热易分解,所以B为氯化铵,A为氯化锌.绿色的K2MnO4溶液发生反应后生成紫色的高锰酸钾溶液和黑褐色的二氧化锰,该反应的离子方程式为3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-.采用惰性电极电解K2MnO4溶液,阴极氢离子得电子生成氢气.故答案为:①ZnCl2 NH4Cl②3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-l③H2点评:
本题考点: 常见化学电源的种类及其工作原理.
考点点评: 本题考查了化学与技术、原电池原理、电极方程式的书写,综合性较强.1年前查看全部
- 科学家发现在特殊条件下,水能表现出许多有趣的结构和性质.一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,
科学家发现在特殊条件下,水能表现出许多有趣的结构和性质.一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,如图为其模拟图.下列说法不正确的是( )

A.利用该性质,人们在常温常压下可建成溜冰场
B.上述变化过程中分子间间隔发生了变化
C.在弱电场下,水分子运动从无序转变为有序
D.水结成“热冰”的过程中原子个数发生变化 jackcc05311年前1
jackcc05311年前1 -
 aileen89 共回答了22个问题
aileen89 共回答了22个问题 |采纳率81.8%解题思路:根据水变成冰的过程考虑,发生物理变化时分子本身不变,所以原子个数也不变.A、根据题干中:一定条件下给水施加一个弱电场,常常压下水结成冰,俗称“热冰”,所以在常温常压下可建成溜冰场.故A说法正确.
B、水变成冰分子之间间隔变大,故B说法正确;
C、水结成冰由液态变为固态,固体是有序排列的,分子运动的范围比较小,液态的水分子运动的范围大呈无序状,故C说法正确;
D、发生物理变化时分子本身不变,变化的是分子之间的间隔,所以原子个数也不变;故D说法错误;
故选D.点评:
本题考点: 微粒观点及模型图的应用;利用分子与原子的性质分析和解决问题.
考点点评: 解答本题的关键是水由液态变为固态,在这一变化过程中分子本身不变,变化的是分子之间的间隔或距离.还需要结合固体、液体分子运动的特点考虑.1年前查看全部
- (2013•吉林二模)CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机
 (2013•吉林二模)CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物.工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
(2013•吉林二模)CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物.工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
(1)已知:CH4、H2和CO的燃烧热分别为890.3kJ/mol、285.8kJ/mol和283.0kJ/mol,且1mol液态水汽化时的能量变化为44.0kJ.写出甲烷与水蒸气在高温下反应制取合成气的热化学方程式______.
(2)在一定条件下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),测得CH4(g)和H2(g)的物质的量浓度随时间变化如下表所示:
①3-4min之间,化学平衡向______反应方向移动(填“正”或“逆”).时间/min
物质
浓度0 1 2 3 4 CH4 0.2mol•L-1 0.13mol•L-1 0.1mol•L-1 0.1mol•L-1 0.09mol•L-1 H2 0mol•L-1 0.2mol•L-1 0.3mol•L-1 0.3mol•L-1 0.33mol•L-1
②3min时改变的反应条件是______(只填一种条件的改变)
(3)已知温度、压强、投料比X〔n(CH4)/n(H2O)〕对该反应的影响如图所示.
①图1中的两条曲线所示投料比的关系X1______X2(填“=”“>”或“<”下同)
②图2中两条曲线所示的压强比的关系:p1______p2
(4)以天然气(设杂质不参与反应)、KOH溶液为原料可设计成燃料电池
①放电时,正极的电极反应式______
②设装置中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下的体积为8.96L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为______. qinglaixia1年前1
qinglaixia1年前1 -
 beyond_chu 共回答了13个问题
beyond_chu 共回答了13个问题 |采纳率92.3%解题思路:(1)根据燃烧热写出热化学方程式,利用盖斯定律计算;(2)反应方程式为CH4(g)+H2O(g)=CO(g)+3H2(g),根据表中数据可知3min时达到平衡,再根据4min时各组分浓度变化量判断改变的条件;(3)①碳水比n(CH4)/n(H2O)值越大,平衡时甲烷的转化率越低,含量越高;②根据压强对平衡移动影响,结合图象分析解答;(4)①甲烷燃料电池工作时,正极发生还原反应,氧气得电子被还原;②计算氧气的物质的量,进而计算生成二氧化碳的物质的量,根据n(NaOH)与n(CO2)比例关系判断反应产物,进而计算溶液中电解质物质的量,结合盐类水解与电离等判断.(1)已知:①H2(g)+[1/2]O2(g)=H2O(l)△H=-285.8kJ•mol-1
②CO(g)+[1/2]O2(g)=CO2(g) )△H=-283.0kJ•mol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(l))△H=-890.3kJ•mol-1,
④H2O(g)=H2O(l)△H=-44.0kJ•mol-1,
利用盖斯定律将④+③-②-3×①可得:CH4(g)+H2O(g)=CO(g)+3H2(g)
△H=(-44.0kJ•mol-1)+(-890.3kJ•mol-1)-(-283.0kJ•mol-1)-3×(-285.8kJ•mol-1)=+206.1 kJ•mol-1,
故答案为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ/mol;
(2)①反应方程式为CH4(g)+H2O(g)=CO(g)+3H2(g),由表中数据可知3-4min之间,CH4浓度减小,H2浓度增大,则反应向生产氢气的方向移动,即向正方向进行,故答案为:正;
②3min时改变的反应条件,反应向正反应方向进行,可能为升高温度或增大H2O的浓度或减小CO的浓度,故答案为:升高温度或增大H2O的浓度或减小CO的浓度;
(3)①碳水比n(CH4)/n(H2O)值越大,平衡时甲烷的转化率越低,含量越高,故x1>x2,故答案为:>;
②该反应正反应是气体体积增大的反应,增大压强平衡向逆反应方向移动,平衡时甲烷的含量增大,故p1>p2,故答案为:>;
(4)①正极发生还原反应,氧气在正极放电生成氢氧根离子,正极电极反应式为:O2+4e-+2H2O=4OH-,故答案为:O2+4e-+2H2O=4OH-;
②参与反应的氧气在标准状况下体积为8960mL,物质的量为[8.96L/22.4L/mol]=0.4mol,根据电子转移守恒可知,生成二氧化碳为[0.4mol×4/8]=0.2mol,n(NaOH)=0.1L×3.0mol•L-1=0.3mol,n(NaOH):n(CO2)=0.3mol:0.2mol=3:2,发生发生2CO2+3NaOH=Na2CO3+NaHCO3+H2O,溶液中碳酸根水解,碳酸氢根的水解大于电离,溶液呈碱性,故c(OH-)>c(H+),碳酸根的水解程度大于碳酸氢根,故c(HCO3-)>c(CO32-),钾离子浓度最大,水解程度不大,碳酸根浓度原大于氢氧根离子,故c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:c(K+)>c (HCO3- )>c (CO32- )>c (OH- )>c( H+).点评:
本题考点: 化学平衡的计算;热化学方程式;化学电源新型电池;化学平衡建立的过程;离子浓度大小的比较.
考点点评: 本题综合性较大,涉及热化学方程式书写、化学平衡图象、化学平衡的影响因素、化学平衡计算、原电池、化学计算、离子浓度比较等,为高考常见题型,难度中等,是对基础知识与学生能力的综合考查,注意把握化学平衡的影响因素以及图象、数据的分析能力的培养.1年前查看全部
- NaNO3 的化学名称及俗称
 tinystone811年前1
tinystone811年前1 -
 ooggg9746 共回答了19个问题
ooggg9746 共回答了19个问题 |采纳率94.7%硝酸钠1年前查看全部
- 过氧化氢是一种常见绿色氧化剂,用途广泛,其水溶液俗称双氧水.
过氧化氢是一种常见绿色氧化剂,用途广泛,其水溶液俗称双氧水.
(1)已知液态过氧化氢与水相似,可微弱电离,得到两种等电子微粒.请写出过氧化氢的电离方程式______.
(2)如图所示:两个盛有等量过氧化氢溶液的容器A和B,向A中加入少量MnO2;向B中加入H2SO4和足量MnO2.充分反应后,B中放出气体的量是A中放出气体的2倍(相同状况),则B中反应的化学方程式是______;原因是______.
(3)火箭推进器中盛有强还原剂肼(N2H4)和强氧化剂液态双氧水(H2O2).当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知:0.4mol液态肼与足量的液态双氧水反应放出256.0kJ的热量.则该反应的热化学方程式是______. bladering9991年前1
bladering9991年前1 -
 jxh__259999 共回答了16个问题
jxh__259999 共回答了16个问题 |采纳率100%解题思路:(1)过氧化氢电离得到的等电子体产物为H3O2+、HO2-;
(2)A中过氧化氢在二氧化锰的催化作用下发生分解反应,B中在酸性条件下,过氧化氢与二氧化锰发生氧化还原反应,B中的MnO2作氧化剂,可将过氧化氢中的-1价氧全部氧化为氧气,而A中的过氧化氢发生歧化反应,只有一半-1价氧被氧化为氧气;
(3)反应方程式为:N2H4+2H2O2=N2+4H2O,根据0.4mol液态肼放出的热量,计算1mol液态肼放出的热量,进而写出热化学方程式.(1)过氧化氢电离得到的等电子体产物为H3O2+、HO2-,其电离方程式为:2H2O2
 H3O2++HO2-,
H3O2++HO2-,
故答案为:2H2O2 H3O2++HO2-;
H3O2++HO2-;
(2)A中过氧化氢在二氧化锰的催化作用下发生分解反应,B中在酸性条件下,过氧化氢与二氧化锰发生氧化还原反应,B中反应方程式为MnO2+H2O2+H2SO4=MnSO4+O2↑+2H2O,B中的MnO2作氧化剂,可将过氧化氢中的-1价氧全部氧化为氧气,而A中的过氧化氢发生歧化反应,只有一半-1价氧被氧化为氧气,故B中放出气体是A中2倍,
故答案为:MnO2+H2O2+H2SO4=MnSO4+O2↑+2H2O;B中的MnO2作氧化剂,可将过氧化氢中的-1价氧全部氧化为氧气,而A中的过氧化氢发生歧化反应,只有一半-1价氧被氧化为氧气,故B中放出气体是A中2倍;
(3)反应方程式为:N2H4+2H2O2═N2+4H2O,0.4mol液态肼放出256.652KJ的热量,则1mol液态肼放出的热量为[256kJ/0.4]=640kJ,
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-640kJ/mol,
故答案为:N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-640kJ/mol.点评:
本题考点: 过氧化氢;热化学方程式;弱电解质在水溶液中的电离平衡.
考点点评: 本题考查等电子体、氧化还原反应、热化学方程式的书写,题目难度一般,注意热化学方程式与化学方程式的区别.1年前查看全部
- 现在,一些大厦都用许 现在,一些大厦都用许多大块的镀膜玻璃做外墙(俗称“玻璃幕墙”).这种外墙既能透射光线也能反射光线.
现在,一些大厦都用许
现在,一些大厦都用许多大块的镀膜玻璃做外墙(俗称“玻璃幕墙”).这种外墙既能透射光线也能反射光线.
(1)外面看玻璃幕墙相当于平面镜,光线照射到光滑的玻璃幕墙上时会发生 反射,物体经玻璃幕墙反射后所成的像是 (填“实”或“虚”)像;
(2)玻璃幕墙不仅会造成光污染,还会给人们带来哪些负面影响?请举一例: .
(3)请就减小玻璃幕墙造成的光污染,提出一条合理化的建议: . 王佳名1年前1
王佳名1年前1 -
 杂役六号 共回答了23个问题
杂役六号 共回答了23个问题 |采纳率91.3%(1)镜面;虚
(2)暴露家居隐私或影响居民工作和休息(答案不唯一,合理即可)
(3)统一规划.减小或不用玻璃幕墙进行居房的外装饰(答案不唯一,合理即可)1年前查看全部
- 俗称“金毛”的狗狗科学上的定义属于哪个犬种?
 ldxwbl61年前1
ldxwbl61年前1 -
 briar 共回答了25个问题
briar 共回答了25个问题 |采纳率76%中文学名:金毛寻回犬
拉丁学名:golden retriever
别称:金毛或者金毛犬
门:脊索动物
亚门:脊椎动物
纲:哺乳
亚纲:哺乳
目:食肉
科:犬
金毛猎犬体格健壮,工作热心,可以用来捕捉水鸟,任何气候下都能在水中游泳.深受猎手的喜爱,现在有的被作为家犬饲养,为中型犬.最初的名字是苏俄追踪犬,后来加入佛乐寻猎物犬种,寻血猎犬种,水猎鹬犬种的基因.1年前查看全部
- 过氧化氢俗称双氧水,可用过氧化钡(BaO 2 )与稀硫酸反应来制备。过氧化氢与过氧化钡都是过氧化物,过氧化物一般可用作氧
过氧化氢俗称双氧水,可用过氧化钡(BaO 2 )与稀硫酸反应来制备。过氧化氢与过氧化钡都是过氧化物,过氧化物一般可用作氧化剂、漂白剂、供氧剂等。阅读下文并回答有关问题:
(1)实验室可用过氧化氢溶液制取氧气,其反应的化学方程式是 。
(2)过氧化钠(Na 2 O 2 )也是一种过氧化物,潜水艇常用过氧化钠作供氧剂,同时维持艇内空气成分的稳定,写出这一反应的化学方程式 。 anniemaymay1年前0
anniemaymay1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2
碱式碳酸铜(Cu2(OH)2CO3)俗称铜绿,受热易分解,生成黑色固体氧化铜、水蒸汽和二氧化碳.反应的化学方程式为Cu2(OH)2CO3
2CuO+H2O+CO2↑.现将一定量的碱式碳酸铜和铜的粉末放在容器里,在空气中用酒精灯充分加热后冷却,称量,发现加热前后固体的质量相等.据此计算原混合粉末中Cu2(OH)2CO3的质量.△ . dolphin24281年前1
dolphin24281年前1 -
 海底琥珀 共回答了16个问题
海底琥珀 共回答了16个问题 |采纳率93.8%解题思路:根据题意,可知:铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等.铜绿受热易分解,生成黑色固体氧化铜,水蒸汽和二氧化碳,水蒸汽和二氧化碳跑到空气中了,铜粉与氧气反应生成CuO,因为加热前后固体的质量相等,所以跑掉的水蒸汽和二氧化碳的质量与铜反应的氧气的质量相等;
设原混合物质量为100g,其中碱式碳酸铜的质量为x,则铜的质量为100g-x,生成的水蒸汽和二氧化碳的质量为y;
则根据题意有:
①Cu2(OH)2CO3
△
.
CuO+H2O+CO2↑
222 18+44=62
xy
则[222/x=
62
y],解得y=[62x/222]
②2Cu+O2
△
.
2CuO
12832
100g-xy
[128/100g−x=
32
y],解得y=
32(100g−x)
128
所以得[62x/222]=
32(100g−x)
128,解得x≈47.2g,故
47.2g
100g×100%=47.2%
答:原混合粉末中Cu2(OH)2CO3的质量分数约为47.2%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题是对利用化学方程式计算的考查题,解题的关键是对反应前后质量变化的分析,属于基础性知识考查题.1年前查看全部
- 氢氧化钙在工农业生产上应用很广,下列关于氢氧化钙的描述错误的是( ) A.其水溶液能使紫色石蕊试液变红 B.俗称熟石灰
氢氧化钙在工农业生产上应用很广,下列关于氢氧化钙的描述错误的是( ) A.其水溶液能使紫色石蕊试液变红 B.俗称熟石灰或消石灰 C.可用于改良酸性土壤 D.对皮肤、衣服等有腐蚀作用  benmaogao1年前1
benmaogao1年前1 -
 xq279 共回答了18个问题
xq279 共回答了18个问题 |采纳率83.3%A、氢氧化钙为碱,其水溶液可以使紫色石蕊变蓝,故A描述错误;
B、氢氧化钙俗称熟石灰或消石灰,故B描述正确;
C、氢氧化钙为碱性物质,常用来改良酸性土壤,故C描述正确;
D、氢氧化钙为碱性物质,对皮肤或衣服有一定的腐蚀能力,故D描述正确.
故选A.1年前查看全部
- (2010•松江区一模)二氧化钛(TiO2)俗称钛白,是世界上最白的物质之一.二氧化钛中钛元素的化合价为( )
(2010•松江区一模)二氧化钛(TiO2)俗称钛白,是世界上最白的物质之一.二氧化钛中钛元素的化合价为( )
A.-2
B.+2
C.-4
D.+4 东东DBL1年前1
东东DBL1年前1 -
 繁星2002 共回答了21个问题
繁星2002 共回答了21个问题 |采纳率85.7%解题思路:根据物质二氧化钛的化学式TiO2,利用化合物中各元素的化合价代数和为0的原则,由化合物中氧为-2价,计算化合物中钛元素的化合价.设化合物TiO2中钛元素化合价为n价,依化合物中各元素化合价代数和为零的原则,有n+(-2)×2=0,解之得n=+4;
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 根据化合物中各元素的化合价代数和为0,利用化合物的化学式可计算其中未知的元素化合价.1年前查看全部
- 88岁有个俗称,请问是什么?1:喜寿.2:白寿.3:米寿.4:仗朝之年
 acc4051469971年前1
acc4051469971年前1 -
 明媚鲜妍 共回答了16个问题
明媚鲜妍 共回答了16个问题 |采纳率93.8%3.米寿
因为“米”字,上面一个倒八,中间一个十,下面一个八,所以是八十八,所以88岁的俗称是米寿.1年前查看全部
- (2012•润州区二模)下列物质的名称、俗称、化学式相符的是( )
(2012•润州区二模)下列物质的名称、俗称、化学式相符的是( )
A.碳酸氢钠苏打NaHCO3
B.氢氧化钠烧碱NaOH
C.水银汞Ag
D.氯化钠食盐NaCl2 pqoig1年前1
pqoig1年前1 -
 着青石顶 共回答了19个问题
着青石顶 共回答了19个问题 |采纳率94.7%解题思路:根据常见化学物质的名称、俗称、化学式进行分析判断即可.A、碳酸氢钠俗称小苏打,其化学式为NaHCO3,其名称、俗称、化学式不相符.
B、氢氧化钠俗称火碱、烧碱、苛性钠,其化学为NaOH,其名称、俗称、化学式相符.
C、水银是金属汞的俗称,其化学式为Hg,其名称、俗称、化学式不相符.
D、氯化钠的俗称是食盐,其化学式为NaCl,其名称、俗称、化学式不相符.
故选B.点评:
本题考点: 化学式的书写及意义.
考点点评: 本题难度不大,熟练掌握常见化学物质的名称、俗称、化学式是正确解答此类题的关键.1年前查看全部
- 氢氧化钙俗称______或______,______溶于水,溶解在水中形成的溶液俗称石灰水.配制好的石灰水若放置很长时间
氢氧化钙俗称______或______,______溶于水,溶解在水中形成的溶液俗称石灰水.配制好的石灰水若放置很长时间.其表面会形成一层白膜,白膜的成分是______,形成的原因用化学方程式表示为______;熟石灰有很多用途,在工业上,用它制漂白粉、制烧碱,制烧碱的反应原理为______;在农业上用它______土壤酸性,配制农药波尔多液;建筑业上,用它建筑材料,则反应原理是______.熟石灰可由生石灰与水反应得到,化学方程式为______.  bnbtt163001年前1
bnbtt163001年前1 -
 lgm0128 共回答了15个问题
lgm0128 共回答了15个问题 |采纳率86.7%氢氧化钙俗称熟石灰或消石灰,微溶于水,能与空气中的二氧化碳反应生成碳酸钙沉淀和水,碳酸钙是白色坚硬的物质,因此利用此反应可以用作建筑材料;氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,可以用于制取烧碱;利用其碱性,可以用于改良酸性土壤,氧化钙与水反应生成氢氧化钙,故填:熟石灰,消石灰,微,碳酸钙,Ca(OH) 2 +CO 2 =CaCO 3 ↓+H 2 O,Ca(OH) 2 +Na 2 CO 3 =CaCO 3 ↓+2NaOH,改良,Ca(OH) 2 +CO 2 =CaCO 3 ↓+H 2 O,CaO+H 2 O═Ca(OH) 2 .1年前查看全部
- 阅读答案 怕痒树——紫薇紫薇属干屈菜科,人们俗称它“怕痒树”,是树木中一种奇特的树种.紫薇为花叶乔木,又名无皮树、满堂红
阅读答案 怕痒树——紫薇
紫薇属干屈菜科,人们俗称它“怕痒树”,是树木中一种奇特的树种.紫薇为花叶乔木,又名无皮树、满堂红、百日红.由于花期特长,7月至10月花开不断,故名百日红.
宋代诗人杨万里诗赞颂:“似痴如醉丽还佳,露压风欺分外斜.谁道花无红百日,紫薇长放半年花.”明代薛蕙也写过:“紫薇花最久,烂熳十旬期,夏日逾秋序,新花续放枝.”
北方人叫紫薇树为“猴刺脱”,是说树身太滑,猴子都爬不上去.它的可贵之处是无树皮.物以稀为贵,世界上千树万木之中有几种是无皮的?年轻的紫薇树干,年年生表皮,年年自行脱落,表皮脱落以后,树干显得新鲜而光滑.老年的紫薇树,树身不复生表皮,筋脉挺露.莹滑光洁.
紫薇树长大以后,树干外皮落下,光滑无皮.如果人们轻轻抚摸一下,立即会枝摇叶动,浑身颤抖,甚至会发出微弱的“咯咯”响动声.这就是它“伯痒”的一种全身反应,实是令人称奇.
紫薇属共有4个种,有赤薇、银薇、翠薇等.以花瓣蓝色的翠薇最佳,为圆锥花序,着生新枝顶端,长达20厘米,每朵花6瓣,瓣多皱襞,似一轮盘.花开满树,艳丽如霞,故又称满堂红.结果为蒴果,状如大豆,内有种子多粒,11月成熟.
紫薇原产***,分布于长江流域,华南、西北、华北也有栽培,它的适应性很强.
紫薇耐旱、怕涝,喜温暖潮润,喜光,喜肥,对二氧化硫、氟化氢及氮气的抗性强,能吸入有害气体.据测定,每千克叶能吸硫10克而生长良好.紫薇又能吸滞粉尘,在水泥厂内距污染源200~250米处,每平方米叶片可吸滞粉尘4042克.因此,它是城市、工矿绿化最理想的树种,也可作盆景.
紫薇还具有药物作用,李时珍在《本草纲目》中论述,其皮、木、花有活血通经、止痛、消肿、解毒作用.种子可制农药,有驱杀害虫的功效.叶治白痢、花治产后血崩不止、小儿烂头***,根治痈肿疮毒,可谓浑身是宝.
 SDboubou1年前1
SDboubou1年前1 -
 afanafan 共回答了18个问题
afanafan 共回答了18个问题 |采纳率94.4%题目呢1年前查看全部
- (2009•宣武区一模)“金银铜铁锡”俗称五金.在这五种金属中,金属活动性最弱的是( )
(2009•宣武区一模)“金银铜铁锡”俗称五金.在这五种金属中,金属活动性最弱的是( )
A.铁
B.金
C.银
D.铜 xiaoheigrr1年前1
xiaoheigrr1年前1 -
 huangshihao001 共回答了15个问题
huangshihao001 共回答了15个问题 |采纳率100%解题思路:根据已有的知识进行分析,在金属活动性顺序中,锡>铁>铜>银>金.锡>铁>铜>银>金,活动性最弱的是金,观察选项,故选B.
点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题考查了金属活动性顺序,完成此题,可以依据已有的知识进行.1年前查看全部
- 为什么碳酸钠俗称“纯碱”?【请说明清楚理由!】
为什么碳酸钠俗称“纯碱”?【请说明清楚理由!】
胡说八道的不给分!一楼请注意!不是胡扯!请注意! legendzhu1年前2
legendzhu1年前2 -
 手刃侬 共回答了17个问题
手刃侬 共回答了17个问题 |采纳率94.1%碳酸钠水溶液呈碱性,所以,在生活中,人们一直认为它是碱,并叫它纯碱.
又因为集散地“张家口”的碱最好,又叫口碱.
还因为面团发酵后用它来中和面团产生的酸,还叫“面碱”1年前查看全部
- 乙醇(C2H5OH)俗称酒精,属于可再生能源,医院可用体积分数为75%酒精(含有体积分数为25%的水)来消毒.某兴趣小组
乙醇(C2H5OH)俗称酒精,属于可再生能源,医院可用体积分数为75%酒精(含有体积分数为25%的水)来消毒.某兴趣小组将大小相同的若干棉布在5份不同体积分数的酒精溶液中浸透后取出点火,做了烧不坏的棉布“试验.其试验结果记录如下:
(1)你推测⑤的实验现象是______.试验序号 ① ② ③ ④ ⑤ 所用酒精的体积分数 95% 65% 55% 15% 5% 实验现象 酒精烧完
棉布烧坏酒精烧完
棉布无损酒精烧完
棉布无损不燃烧
(2)写出酒精燃烧的化学反应方程式______.
(3)实验②③中“酒精烧完,棉布无损”的原因是______.实验室里的酒精灯经常存在灯中有酒精且灯芯正常却点不燃的现象,你认为可能的原因是______. 海后观鹭江1年前1
海后观鹭江1年前1 -
 爱吃红烧牛肉的我 共回答了17个问题
爱吃红烧牛肉的我 共回答了17个问题 |采纳率82.4%解题思路:(1)当酒精的质量分数小到一定程度时不能燃烧,根据实验中数据及对应的现象,判断酒精燃烧与其质量分数的关系并进行推断;
(2)根据酒精的组成,利用燃烧规律,判断酒精的燃烧反应,写出反应的化学方程式;
(3)根据可燃物燃烧所应满足的条件,分析棉布没有燃烧的原因;酒精是一种容易挥发的物质,根据可燃物燃烧所应满足的条件,结合探究所得结果,分析灯内有酒精却点不燃的原因.(1)根据实验可发现,当酒精溶液中酒精含量为15%时,就不能被点燃;因此,当含酒精5%的溶液点燃时,可燃物的浓度太低,所以也不能燃烧;
(2)酒精由C、H、O三种元素组成,完全燃烧时生成二氧化碳和水,反应的化学方程式为C2H5OH+3O2
点燃
.
2CO2+3H2O;
(3)当55%~65%酒精溶液在点燃时,由于有不能燃烧的水存在,一部分热量还要供水的汽化和水蒸气的升温,从而消耗了大量的热量.这样,棉布的温度升得并不高,以致于达不到它的着火点,显然棉布也就不会被烧着了;实验室里常出现酒精灯内有酒精却点不着的原因可能是灯芯上的酒精挥发掉了,留下溶液中酒精浓度达不到燃烧所需要的尝试,因此不能被点燃;
故答案为:
(1)不燃烧.
(2)C2H5OH+3O2═2CO2+3H2O.
(3)实验②③所用酒精中含水量较多,酒精燃烧过程中,水分蒸发会吸收热量,使棉布温度降低,难达到其着火点;酒精挥发,灯芯上水分过多难以点燃.点评:
本题考点: 燃烧与燃烧的条件;常用燃料的使用与其对环境的影响.
考点点评: 学会根据所给信息分析问题,并把相应的结论加以运用,这是本题的目的.1年前查看全部
- 苯酚有酸性,俗称石炭酸,苯酚是酸吗?
苯酚有酸性,俗称石炭酸,苯酚是酸吗?
给个理由好吗? samfine1年前1
samfine1年前1 -
 yuanbandeng 共回答了23个问题
yuanbandeng 共回答了23个问题 |采纳率78.3%苯酚不是酸,它的羟基与苯环相连二者互相影响.使的羟基活性增强,溶于水的苯酚在水溶液中电离出来氢离子1年前查看全部
- “三观”指的是什么?俗称的“三观”除人生观、世界观,还包括什么“观”
 atlanticblue01年前1
atlanticblue01年前1 -
 鄱湖月 共回答了17个问题
鄱湖月 共回答了17个问题 |采纳率94.1%人生观、价值观、世界观1年前查看全部
- 初三所有的化学物质的化学式和俗称
 逮住一只ll耗子1年前5
逮住一只ll耗子1年前5 -
 色非空 共回答了16个问题
色非空 共回答了16个问题 |采纳率93.8%俗名掌握这些物质的就可以:
氢氧化钙Ca(OH)2 (熟石灰 消石灰)
Ca(OH)2水溶液俗名石灰水
氧化钙CaO (生石灰)
乙醇C2H5OH (酒精)
乙酸CH3COOH (醋酸)
氢氧化钠 NaOH(火碱、烧碱、苛性钠)
碳酸钠Na2CO3(纯碱、苏打)
碳酸氢钠NaHCO3 (小苏打)
硫酸铜晶体CuSO4•5H2O (蓝矾、胆矾)1年前查看全部
- 下列各组物质的名称或俗称和化学式表示的是同一种物质的是( ) A.熟石灰、消石灰、CaO B.铁锈、氢氧化铁、Fe(O
下列各组物质的名称或俗称和化学式表示的是同一种物质的是( ) A.熟石灰、消石灰、CaO B.铁锈、氢氧化铁、Fe(OH) 3 C.生石灰、消石灰、Ca(OH) 2 D.烧碱、火碱、NaOH  1mmhl01年前1
1mmhl01年前1 -
 duancht 共回答了20个问题
duancht 共回答了20个问题 |采纳率90%A、熟石灰、消石灰指的是氢氧化钙而不是氧化钙,故A不正确;
B、Fe(OH) 3 的名称是氢氧化铁,但不是铁锈,故B不正确;
C、生石灰是氧化钙,而不是消石灰、Ca(OH) 2 ,故C不正确;
D、烧碱、火碱氢氧化钠的俗名,化学式为NaOH,故D正确.
故选D.1年前查看全部
- 小明家搞装修,为了美观,想把所有电线都埋藏在墙壁里(俗称走暗线).小明在查阅有关资料时了解到:埋藏在墙壁里的电线,要整条
小明家搞装修,为了美观,想把所有电线都埋藏在墙壁里(俗称走暗线).小明在查阅有关资料时了解到:埋藏在墙壁里的电线,要整条铺设,不能在墙壁里中途接驳.请你运用相关知识解释其道理:由于接驳处导线电阻______(填“增大”或“减小”),电流在该处产生的热量较______(填“多”或“少”),存在安全隐患.
 vywsol1年前1
vywsol1年前1 -
 大vv生 共回答了15个问题
大vv生 共回答了15个问题 |采纳率100%解题思路:影响电阻大小的因素:导线的长度、横截面积、材料、温度等,根再据Q=I2Rt作出分析和解答.由于接驳处导线接触不良,横截面积减小,故接驳处的电阻增大;由焦耳定律Q=I2Rt可知,电流一定时,电阻越大,电流在该处的产生的热量较多.
故答案为:增大;多.点评:
本题考点: 焦耳定律的计算公式及其应用.
考点点评: 本题主要考查对焦耳定律及应用的了解和掌握,知道导线和导线接驳处横截面积减小是本题的关键.1年前查看全部
- 气凝胶(如图所示)俗称“冷冻烟雾”,其密度仅为每立方厘米3毫克(每升3克),是普通玻璃的千分之一.它虽属于固体,但99.
气凝胶(如图所示)俗称“冷冻烟雾”,其密度仅为每立方厘米3毫克(每升3克),是普通玻璃的千分之一.它虽属于固体,但99.8%是由气体构成的,这使得它外观看起来像云一样.这种新材料坚固耐用,最高能承受1400℃的高温.***“神州七号”飞船轨道舱采用的多层隔热材料是一种镀铝的聚酯薄膜.镀铝的功能类似于保温瓶中的内胆能对热量进行大量反射.它的密度大约是0.5×103kg/m3,总体积为2m3,如果用气凝胶代替聚酯薄膜,可使飞船的质量减轻多少?

 xuhongmei1年前2
xuhongmei1年前2 -
 blueskygy 共回答了19个问题
blueskygy 共回答了19个问题 |采纳率84.2%解题思路:先根据密度公式求出气凝胶的密度,用气凝胶代替聚酯薄膜时,所需材料的体积相等,再根据密度公式分别求出两种材料的质量,质量之差即为飞船减轻的质量.气凝胶的密度:
ρ气凝胶=
m气凝胶
V气凝胶=
3×10−6kg
10−6m3=3kg/m3,
∵用气凝胶代替聚酯薄膜时,所需材料的体积相等,
∴飞船减轻的质量:
△m=m聚酯薄膜-m气凝胶′
=ρ聚酯薄膜V-ρ气凝胶V
=0.5×103kg/m3×2m3-3kg/m3×2m3
=994kg.
答:如果用气凝胶代替聚酯薄膜,可使飞船的质量减轻994kg.点评:
本题考点: 密度公式的应用.
考点点评: 本题考查了密度公式的应用,关键是根据题意得出气凝胶的密度和知道用气凝胶代替聚酯薄膜时所需材料的体积相等,计算过程要注意单位的换算.1年前查看全部
- 硫代硫酸钠(Na 2 S 2 O 3 )俗称保险粉,可用作定影剂,也可用于纸浆漂白、脱氯剂等。
硫代硫酸钠(Na 2 S 2 O 3 )俗称保险粉,可用作定影剂,也可用于纸浆漂白、脱氯剂等。
Na 2 S 2 O 3 易溶于水,不溶于乙醇,常温下溶液中析出晶体通常为Na 2 S 2 O·5H 2 O。实验室制备保险粉的装置如下图所示。涉及的总化学方程式如下: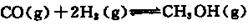

(1)检查虚线框内装置气密性的方法是 。
(2)反应前仪器a中加入的药品为 ,仪器c中加入的药品为 。
(3)仪器b的名称是 。
(4)在制备过程中,持续通人气体时,观察到B装置中先有大量浅黄色沉淀析出,反应一段时间,沉淀逐渐减少;待浅黄色沉淀消失时反应完成,停止加热。反应的离子方程式为 。
(5)反应完成后,为了从混合溶液中获取产品,操作如下:
操作②为 。
(6)为了测产品的纯度,称取8.000 g粗产品,配制成250 mL溶液,用移液管移取25.00 mL于锥形瓶中,再用0.05000 mol·L -l 的碘标准溶液进行滴定(2S 2 O 3 2- +I 2 =S 4 O 6 2- +2I - ),
平行3次实验,平均消耗碘标准溶液的体积为30.00mL。
①测得产品的纯度为 。
②关于上述实验的有关操作,以下表述正确的是 。(填编号)A.用碱式滴定管盛装碘标准溶液 B.用移液管移取25.00mL溶液于锥形瓶中,移液管的尖嘴和锥形瓶内壁要接触 C.如果滴定终点没有控制好,碘标准溶液滴加过量,则必须重新进行滴定 D.滴定过程中若剧烈摇动锥形瓶(溶液不外溅),则所测得的纯度将会偏高  bailinghua1年前1
bailinghua1年前1 -
 新重庆遮阳扇 共回答了20个问题
新重庆遮阳扇 共回答了20个问题 |采纳率95%(1)关闭蒸馏烧瓶右端活塞,往分液漏斗中加水,打开分液漏斗的活塞,水开始下滴,一段时间后,如果水不再下滴,表明气密性良好。反之则气密性不好。
(2)Na 2 SO 3 固体 NaOH溶液(或KMnO 4 溶液等)
(3)三颈烧瓶
(4)S 2 O 3 2- +SO 2 +H 2 O=S↓+2HSO 3 2-
(5)蒸发浓缩、冷却结晶
(6)①93.00% ②B
1年前查看全部
- N2O(俗称笑气)的电子式是怎样的?NO2的电子式又是怎样?中心原子形成几个共价键由 什么来决定?
 jindouzi1年前0
jindouzi1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 马戏团演员运动后躺在一个钉满铁钉的木板上,俗称硬气功.
 juverby1年前1
juverby1年前1 -
 我爱柔然 共回答了24个问题
我爱柔然 共回答了24个问题 |采纳率95.8%其原理在于,所用石头的质量很大,所以其惯性也很大,因此,锤子很快的砸下去,由于惯性,石块的加速度很小,从而对人不会产生巨大的压力.1年前查看全部
大家在问
- 1能帮我写一篇英语作文吗?题目:my school
- 23支钢笔和12是圆珠笔的价钱相等,一支钢笔比一智圆珠笔贵3.6元,两种笔的单价各多少
- 3如果圆锥高为4,底面周长为6π,那么圆锥的侧面积等于
- 4你早上喜欢吃什么用英文怎么说?
- 5某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。
- 6已知f(x)是偶函数.他的定义域为R,在(0.+∞)上递减,那么一定有?A.f(-3/4)〉f(a的平方-a+1)
- 7核糖体合成的物质中含有50个氨基酸,问在该核糖体上最多会有几个水分子生成?(带点解析)
- 8What dod she forget when she left for home?—( ) the book A.T
- 9以学自损 不如无学文言文译文
- 10清明上河园可以用什么词来形容多些好些的
- 11根据语境,依次填入下面空格内最恰当的一组词语是
- 12将4.5g Al 投入1mol/L NaOH 溶液中,Al完全反应,至少需要NaOH溶液的体积和生成氢气的体积(标况)
- 13在标准状况下,二氧化硫和氧气混合气体500ml,通过灼热的催化剂层后,体积换算到标准
- 14黄沙飞舞四个字加一起总共几画
- 15the little girl doesn't like the medicine because it tastes
