ph试纸是怎样测试溶液酸碱度的我想问的是,为什么PH试纸遇上不同酸碱度的溶液会显示不同的颜色
 梦想会实现2022-10-04 11:39:544条回答
梦想会实现2022-10-04 11:39:544条回答
已提交,审核后显示!提交回复
共4条回复
 般若波 共回答了12个问题
般若波 共回答了12个问题 |采纳率100%- PH试纸上有甲基红、溴甲酚绿、百里酚蓝这三种指示剂.甲基红、溴甲酚绿、百里酚蓝和酚酞一样,在不同PH值的溶液中均会按一定规律变色.甲基红的变色范围是PH4.2(红)--6.2(黄),溴甲酚绿的变色范围是PH3.6(黄)--5.4(绿),百里酚蓝的变色范围是PH6.7(黄)--7.5(蓝).用定量甲基红加定量溴甲酚绿加定量百里酚蓝的混合指示剂浸渍中性白色试纸,晾干后制得的PH试纸可用于测定溶液的PH值便不难理解了.
- 1年前
 二鸟 共回答了37个问题
二鸟 共回答了37个问题 |采纳率- 对
- 1年前
 woaiyyoo 共回答了21个问题
woaiyyoo 共回答了21个问题 |采纳率- 化学反应
- 1年前
 bule18 共回答了13个问题
bule18 共回答了13个问题 |采纳率- 化学离不开溶液,溶液有酸碱之分。检验溶液酸碱性的“尺子”是“广泛pH试纸”。这是一种现成的试纸,使用时,撕下一条,滴上一滴溶液,从它的颜色变化就可以知道溶液的酸碱性,十分方便。pH试纸按测量精度上可分0.2级、0.1级、0.01级或更高精度
pH试纸上有甲基红、溴甲酚绿、百里酚蓝这三种指示剂。甲基红、溴甲酚绿、百里酚蓝和酚酞一样,在不同PH值的溶液中均会按一定规律变色。甲基红的变色范围... - 1年前
相关推荐
- 紫色石蕊和红色石蕊试纸有何不同
 yanjie1301年前4
yanjie1301年前4 -
 ee人们ff 共回答了13个问题
ee人们ff 共回答了13个问题 |采纳率84.6%紫色石蕊是溶液,酸性和碱性的东西都可以检验,酸性变红,碱性变蓝
红色石蕊试纸只能检验碱性气体或液体,现象是试纸由红变蓝1年前查看全部
- 白色醋酸铅试纸用于检验什么物质?会有什么现象?
 武日器1年前1
武日器1年前1 -
 北极熊和我 共回答了15个问题
北极熊和我 共回答了15个问题 |采纳率93.3%醋酸铅试纸就是白色的,和白纸的颜色一样.因为醋酸铅是无色的盐.在测试硫化氢气体的时候,先将试纸润湿.有H2S的话试纸会变黑.是因为生成了黑色的PbS .1年前查看全部
- 我的血糖空腹为6.2左右,而我的尿糖用尿糖试纸测每次都有3个加号是什么原因?
 站在金矿上1年前1
站在金矿上1年前1 -
 skyaso 共回答了16个问题
skyaso 共回答了16个问题 |采纳率87.5%血糖和尿糖是不一致的没关系.重要的是血糖.要准确知道情况,必须定期查血糖,6.2还可以.你可以一个月查一次.(标准的是:3.9-6.1)并记录.还有餐后两小时血糖也很重要.建议你和空腹血糖交错查.另外,一定要注意饮食.希望你好好控制血糖哦!1年前查看全部
- 氯气(Cl 2 )是黄绿色气体,其水溶液叫氯水。把品红试纸(染有品红的纸)伸入氯水中,品红褪色。请回答下列各题。
氯气(Cl 2 )是黄绿色气体,其水溶液叫氯水。把品红试纸(染有品红的纸)伸入氯水中,品红褪色。请回答下列各题。
【发现问题】 氯水中的哪些成分能使品红褪色呢?
【查阅资料】 氯气溶于水,部分与水反应,方程式为Cl 2 + H 2 O =" HCl" + HClO。其中,HClO的名称叫次氯酸,是一种弱酸,具有强氧化性。
【猜想】猜想1:是氯水中的水使品红褪色的;
猜想2:是氯水中的氯气使品红褪色的;
猜想3:是氯水中的盐酸使品红褪色的;
猜想4:是氯水中的次氯酸使品红褪色的。
【实验探究】
【结论】实 验 操 作 实验现象 过程分析 ①把品红试纸伸入水中 没有褪色 猜想1不成立 ②把品红试纸伸入干燥的氯气中 没有褪色 猜想2不成立 ③ 没有褪色 猜想3不成立
综合分析:氯水中的 (填化学式)使品红褪色,具有漂白作用(能使品红等有色物质褪色)。
【反思】HClO中氯元素的化合价为 价。 1389617ww71年前1
1389617ww71年前1 -
 哆咧咪 共回答了23个问题
哆咧咪 共回答了23个问题 |采纳率91.3%把品红试纸伸入盐酸中 HClO +1
1年前查看全部
- (2014•西青区模拟)某合作学习小组为探究二氧化碳的化学性质,做了以下实验:他们取一张用石蕊染成紫色的干燥的试纸,放到
(2014•西青区模拟)某合作学习小组为探究二氧化碳的化学性质,做了以下实验:他们取一张用石蕊染成紫色的干燥的试纸,放到已通入二氧化碳的水中,观察到试纸变成红色.由此部分同学判断:二氧化碳能使紫色石蕊试纸变成红色.请你围绕该问题进行探究:
(1)你认为这些同学的判断正确吗?不正确不正确
(2)如果正确,请说明理由;如果不正确,请你设计还需进行的实验,以得出满意的结论.(简要叙述实验步骤、现象和结论,用语言或图示均可) wangyou82001年前1
wangyou82001年前1 -
 zsxwt 共回答了20个问题
zsxwt 共回答了20个问题 |采纳率95%(1)这些同学的判断不正确.故填:不正确.
(2)验证实验如下:
①将一张干燥的紫色石蕊试纸放入盛满二氧化碳的集气瓶中,石蕊试纸不变色,说明二氧化碳不能使石蕊变红.
②将一张干燥的紫色石蕊试纸放入水中,石蕊试纸不变色,说明水不能使石蕊变红.由此证明是二氧化碳和水反应生成的碳酸使紫色石蕊变红色.1年前查看全部
- pH试纸晾干后颜色还准吗?
 huangadkadk1年前1
huangadkadk1年前1 -
 dew3rer3 共回答了20个问题
dew3rer3 共回答了20个问题 |采纳率85%应该是不准了,别说晾干,就是干的,新的也要避免暴晒,阴凉处储存1年前查看全部
- 浸有磷钼酸溶液的氯化钯试纸与一氧化碳的反应原理?
浸有磷钼酸溶液的氯化钯试纸与一氧化碳的反应原理?
"浸有磷钼酸溶液的氯化钯试纸"是在初三一道化学题中出现的,还是"磷钼酸"也可以? 狼语1年前1
狼语1年前1 -
 lingling99 共回答了19个问题
lingling99 共回答了19个问题 |采纳率89.5%首先纠正一下:浸有磷钼酸铵溶液的氯化钯试纸与一氧化碳反应,而不是“磷钼酸”.
氯化钯、一氧化碳和水这三种物质发生反应生成二氧化碳、金属钯(单质)和氢氯酸.
磷钼酸铵可分解出三氧化钼.
一氧化碳在钯单质的催化作用下将三氧化钼还原,生成二氧化钼和二氧化碳.二氧化钼呈蓝色.
实际上,不一定非要用氯化钯,只要是可溶性钯盐就可以,因为反应需要的只是钯离子.
p.s.估计是题目打错了.
况且,初三的学生不需要掌握这么复杂的东西.那道题也不会要求掌握这些原理的.1年前查看全部
- 取某白色固体,分成相等质量的两份.用一份固体与过量的亲氧化钠溶液加热反应,放出能使红色石蕊试纸变蓝的气体,这些气体正好中
取某白色固体,分成相等质量的两份.用一份固体与过量的亲氧化钠溶液加热反应,放出能使红色石蕊试纸变蓝的气体,这些气体正好中和30ml 0.1mol/l的硫酸;用另一份固体与足量的盐酸反应,放出无色无臭气体,这些气体通入过量澄清石灰水产生0.4g沉淀.
问1.计算这种白色固体中所含阴,阳离子的物质的量之比.
2.该白色固体是什么
(第一问答案貌似2:3) 孤独白领Daniel1年前2
孤独白领Daniel1年前2 -
 俟然 共回答了31个问题
俟然 共回答了31个问题 |采纳率93.5%用一份固体与过量的亲氧化钠溶液加热反应,放出能使红色石蕊试纸变蓝的气体,气体为NH3
NH4+ +OH-=加热=NH3(气体)+H2O
这些气体正好中和30ml 0.1mol/l的硫酸;
2NH3+H2SO4=(NH4)2SO4
那么气体的物质的量就是30*0.1/1000*2=0.006mol
用另一份固体与足量的盐酸反应,放出无色无臭气体,这些气体通入过量澄清石灰水产生0.4g沉淀.
是CO2气体
根据CO2+Ca(OH)2=CaCO3(沉淀)+H2O
所以CO2的摩尔数就是0.4/100=0.004mol
可以产生CO2的酸根有
HCO3- +H+=H2O+CO2(气体)
CO32- +2H+ =CO2(气体)+H2O
每1molHCO3-或者1molCO32-得到1molCO2
现在CO2有0.004mol
所以阴离子一共是0.004mol
所以、阴阳离子的物质的量比例为0.004:0.006=2:3
因为是分成等质量的2份,所以原来固体中含有0.012molNH4+,HCO3-和CO32-一共是0.008mol
因为化合物是电中性的.
设HCO3-是xmol,CO32-是ymol
那么有x+2y=0.012
x+y=0.008
所以x=y=0.004
因此原来固体混合物是由0.004molNH4HCO3和0.004mol(NH4)2CO3混合得到的.1年前查看全部
- 1.下列说法正确的是:A.某溶液与NAOH溶液共热,产生是湿润蓝色石蕊试纸变红的气体,则原溶液中存在NH4^+B.某溶液
1.下列说法正确的是:
A.某溶液与NAOH溶液共热,产生是湿润蓝色石蕊试纸变红的气体,则原溶液中存在NH4^+
B.某溶液中加入硝酸银溶液时,产生白色沉淀,说明原溶液中含有Cl-
C.用铂丝蘸取某溶液在酒精灯上灼烧时,火焰呈黄色,说明原溶中含有Na+
D.某溶液中加入BaCl2溶液时,产生白色沉淀,原溶液可能存在Ag+或SO4^2-或CO3^2-或SO3^2-
D,为什么?C中的焰色反应不是只能检验元素的存在吗?怎么能检验离子的存在?
2.现有试剂:1.蒸馏水,2.AgNO3溶液,3.BaCl2溶液,4.稀HNO3,欲检验硝酸银固体中是否有少量可溶性盐酸盐杂质,应选用试剂是()
A.1,4 B.2,4 C.1,2 D.1,2,3
为什么选A?
3.对下列实验过程的评价,正确的是()
A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B.某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有SO4^2-
C.某无色溶液滴入紫色石蕊试液显红色,该溶液一定是酸溶液
D.验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl-
为什么?
4.下列各组物质,只用水不能将它们区分开来的是()
A.氢氧化钠,硝酸铵,氯化钠三种固体
B.硫酸铜,碳酸钠,氧化钙三种白色粉末
C.汽油,乙醇,四氯化碳三瓶无色溶液
D.氯化钠,氯化钾,氯化镁三瓶无色溶液
为什么? 的松100201年前3
的松100201年前3 -
 我在风之翼 共回答了14个问题
我在风之翼 共回答了14个问题 |采纳率92.9%1.钠在水中是以离子的方式存在的
2.先要溶解固体硝酸银,所以需要蒸馏水,在样品中加入AgNO3没有现象,加入BaCl2无论有无杂质都有白色沉淀生成,所以无法判断,故选A
3.因为AgNO3与OH-反应会生成白色沉淀,故先要出去OH-
4.NAOH加水放出热,NH4NO3加水有气体生成,NACL加水没有变化
CUSO4加水变蓝,CAO加水放出大量热,NA2CO3加水没有变化
汽油浮在水上,CCL4沉在水下,乙醇与水互溶1年前查看全部
- 将pH试纸用水湿润后测定某溶液的酸碱度,所测得该溶液的pH与实际情况相比,其结果是( )
将pH试纸用水湿润后测定某溶液的酸碱度,所测得该溶液的pH与实际情况相比,其结果是( )
A. 相等
B. 偏大
C. 偏小
D. 三种结果均有可能 恒睿1年前1
恒睿1年前1 -
 axi858 共回答了25个问题
axi858 共回答了25个问题 |采纳率96%解题思路:用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量溶液置于干燥的PH试纸上,通过与标准比色卡对比来确定PH.此题中PH试纸已经用蒸馏水湿润,稀释了待测溶液,且待测液酸碱性未知,故无法确定.pH试纸用水润湿以后,再将待测液滴到pH试纸上,相当于把待测液给稀释了,如果待测液显酸性,则测出的pH偏大,如果待测液显碱性,则测出的pH偏小,如果待测液显中性,则pH不变.
故选D.点评:
本题考点: 溶液的酸碱度测定.
考点点评: 此题是对PH试纸使用的考查,解题的关键是知道润湿PH试纸会使待测液变稀的知识即可,属基础性知识考查题.1年前查看全部
- 有元素R的氧化物RO,将其与化合物X混合后,再加少量的水,微热后,便能生成一种气体使潮湿石蕊试纸变红
有元素R的氧化物RO,将其与化合物X混合后,再加少量的水,微热后,便能生成一种气体使潮湿石蕊试纸变红
错了 是变蓝 则X和元素R可能是 A.X是纯碱 R是碳元素 B.X是氯化钠 R是硫元素 X是硫酸铵 R是钙元素 D.X是碳酸氢铵 R是钠元素 找个用户名真难阿1年前2
找个用户名真难阿1年前2 -
 bee123 共回答了11个问题
bee123 共回答了11个问题 |采纳率90.9%形成RO,是第二主族元素,可以生成氨气,那么RO肯定是强碱,常见的就是CaO或者氧化钡.
另外一个肯定是铵盐.
所以答案只有C1年前查看全部
- 能使pH试纸呈红色的溶液中能共存NA+、NH4+、I离子、NO3离子吗?
能使pH试纸呈红色的溶液中能共存NA+、NH4+、I离子、NO3离子吗?
能使pH试纸呈红色的溶液中能共存NA+、NH4+、I离子、NO3离子吗? piaomiaoyan1年前1
piaomiaoyan1年前1 -
 穿山甲A 共回答了12个问题
穿山甲A 共回答了12个问题 |采纳率91.7%不能
酸性溶液含有NO3离子会氧化I离子1年前查看全部
- 不能使湿润的碘化钾淀粉试纸变蓝色的物质是 A次氯酸溶液 B 碘化钾溶液
 yangchenc1年前1
yangchenc1年前1 -
 ssjj418 共回答了15个问题
ssjj418 共回答了15个问题 |采纳率80%B.
因为使湿润的碘化钾淀粉试纸变蓝色的物质必须是I2碘单质.
而B无法产生碘单质.1年前查看全部
- 检验氨气可选用( )A. 湿润的蓝色石蕊试纸B. 干燥的红色石蕊试纸C. 干燥的蓝色石蕊试纸D. 湿润的红色石蕊试纸
 猪猪宝宝万岁1年前1
猪猪宝宝万岁1年前1 -
 kgb1050ee 共回答了20个问题
kgb1050ee 共回答了20个问题 |采纳率85%解题思路:根据检验氨气的方法:氨气是碱性气体,氨气能使红色石蕊试纸变蓝或氨气能和浓盐酸反应生成白烟.因氨气能使红色石蕊试纸变蓝或氨气能和浓盐酸反应生成白烟,
故选D.点评:
本题考点: 氨的化学性质.
考点点评: 本题主要考查了氨气的检验,难度不大,需要注意的是氨气是高中阶段唯一的碱性气体.1年前查看全部
- 怎样的条件下存储微生物产品如含培养基的试纸
 clindy1年前1
clindy1年前1 -
 一月Y头 共回答了22个问题
一月Y头 共回答了22个问题 |采纳率86.4%要看什么产品啦!要是你说的微生物试纸的话,要将其放在密闭的容器中,防止蒸发培养基不能用,在把培养基放在冰箱中保存.1年前查看全部
- ph试纸的原理是这种试纸遇到什么不同的溶液会显示不同的颜色
 我是梦做一半1年前3
我是梦做一半1年前3 -
 一笑飞天IV 共回答了23个问题
一笑飞天IV 共回答了23个问题 |采纳率87%ph试纸的原理是这种试纸遇到酸碱度不同的溶液会显示不同的颜色.1年前查看全部
- Cl2使蘸有Naoh的ph试纸退色的主要原因,具因为和NaOH发生了反应还是因为生成的HCLO具有漂白性?为什么?
 谜失的永恒1年前2
谜失的永恒1年前2 -
 kfyu_001 共回答了17个问题
kfyu_001 共回答了17个问题 |采纳率82.4%是漂白的作用,因为是褪色了,不是变色了
如果说是变色了,到可能是反应了NaOH,因为碱性变弱了嘛,但是褪色的话就是显色物质不见了,就是被氧化了1年前查看全部
- Fcl2和淀粉ki试纸能区别cl2和so2吗 ,要过程
Fcl2和淀粉ki试纸能区别cl2和so2吗 ,要过程
这不是体现了氧化性吗,为什么说是还原性 fatboy11111年前1
fatboy11111年前1 -
 叶下青苔 共回答了14个问题
叶下青苔 共回答了14个问题 |采纳率78.6%可以
2FeCl2+Cl2==2FeCl3 溶液颜色发生改变 浅绿色---浅黄色
2KI+Cl2=2KCl+I2 I2遇到试纸变蓝
而SO2没有这样的现象
从而区别开1年前查看全部
- Fcl2和淀粉ki试纸能区别cl2和so2吗
 原来是你09091年前2
原来是你09091年前2 -
 我生活我快乐 共回答了14个问题
我生活我快乐 共回答了14个问题 |采纳率85.7%2FeCl2+Cl2==2FeCl3 溶液颜色发生改变 浅绿色---浅黄色
2KI+Cl2=2KCl+I2 I2遇到试纸变蓝 有因为试纸是湿润的,所以可能会发生褪色1年前查看全部
- 黄绿色气体(氯气)使湿润的碘化钾淀粉试纸变蓝的方程式?
黄绿色气体(氯气)使湿润的碘化钾淀粉试纸变蓝的方程式?
黄绿色气体(氯气)使湿润的碘化钾淀粉试纸变蓝的方程式是什么?
拜托大家告诉我~~~~
 纯蓝GG1年前1
纯蓝GG1年前1 -
 ilucweb2006 共回答了19个问题
ilucweb2006 共回答了19个问题 |采纳率89.5%Cl2 + 2KI = 2KCl +I2
回答完毕,1年前查看全部
- ph试纸使自来水变蓝今天我用ph试纸测自家的自来水,结果水变成了蓝色.请问我家的自来水的ph只是多少?对照表中没有蓝色的
ph试纸使自来水变蓝
今天我用ph试纸测自家的自来水,结果水变成了蓝色.请问我家的自来水的ph只是多少?
对照表中没有蓝色的一项 quite11年前1
quite11年前1 -
 henry84 共回答了12个问题
henry84 共回答了12个问题 |采纳率83.3%不知道具体多少,不过可以肯定的是你家自来水是碱性的.红色是酸性,蓝色是碱性.
卖试纸的地方都会有对照表,根据对照表才知道具体是多少~1年前查看全部
- 下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变
下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。
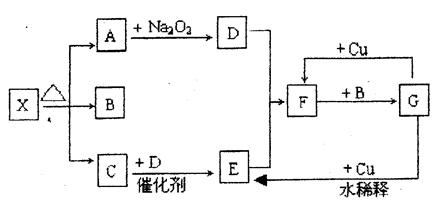
(1)写出下列各物质的化学式:
X: ;B: ;F: ;G: 。
(2)写出下列变化的反应方程式:
A→D: ;
G→E: 。
(3)实验室里,常用加热 的混合物的方法制取气体C,常采用 法来收集。 tarcy5211年前1
tarcy5211年前1 -
 旗木倾城 共回答了25个问题
旗木倾城 共回答了25个问题 |采纳率84%(共10分)(1)X:NH 4 HCO 3 或(NH 4 ) 2 CO 3 ; B:H 2 O; F:NO 2 ; G:HNO 3 (每空1分)。(2)A→D:2CO 2 +2Na 2 O 2 =2Na 2 CO 3 +O 2G→E:3Cu+8HNO 3 (稀)=3Cu(NO 3 ) 2 +2NO↑+4H 2 O(每空2分)(3...1年前查看全部
- 11.在下列三个实验中:①配制一定物质的量浓度的溶液②pH试纸的使用③过滤、蒸发,均用到的仪器%
11.在下列三个实验中:①配制一定物质的量浓度的溶液②pH试纸的使用③过滤、蒸发,均用到的仪器%
A.试管 B.胶头滴管
C.玻璃棒 D.漏斗 miong1年前2
miong1年前2 -
 追忆瞬间 共回答了18个问题
追忆瞬间 共回答了18个问题 |采纳率100%C.玻璃棒1年前查看全部
- pH试纸的读数pH试纸能测出pH等于12.8 7.5么,实验室用的那种
 网上客户信息机1年前1
网上客户信息机1年前1 -
 青秋龙月 共回答了21个问题
青秋龙月 共回答了21个问题 |采纳率90.5%不能,PH试纸只能让你知道你所测的液体大约在哪个范围内.1年前查看全部
- 为啥浓硝酸遇石蕊试纸会变白?给个理由先.
 陇南人1年前1
陇南人1年前1 -
 qwerty6 共回答了21个问题
qwerty6 共回答了21个问题 |采纳率90.5%浓硝酸的氧化性让石蕊试纸的有效成分氧化变质了,把试纸漂白了1年前查看全部
- (2003•武汉)某学习小组的同学,欲在不使用酸碱指示剂或试纸等测酸碱性的条件下,通过添加试剂的方法将含有硝酸的硝酸钙溶
(2003•武汉)某学习小组的同学,欲在不使用酸碱指示剂或试纸等测酸碱性的条件下,通过添加试剂的方法将含有硝酸的硝酸钙溶液变为中性.甲同学提出选用石灰石粉末,乙同学提出选用澄清的石灰水.比较甲、乙两同学所选试剂,你认为______同学的选择不可行;理由是该试剂虽能除去原混合液中的______,但______.
 有朋不亦乐乎1年前1
有朋不亦乐乎1年前1 -
 香山红叶22 共回答了26个问题
香山红叶22 共回答了26个问题 |采纳率96.2%解题思路:可以根据物质的性质方面进行分析、判断,从而得出正确的结论.例如,用石灰水中和硝酸时,因为两者反应时无明显现象,无法判断是否恰好完全反应.石灰石不溶于水,和硝酸充分反应后不再溶解.石灰水和硝酸是否恰好完全反应不容易判断.
故填:乙;H+(或HN03或硝酸);在不用指示剂的情况下,难控制溶液的酸碱性.点评:
本题考点: 物质除杂或净化的探究;化学性质与物理性质的差别及应用;反应现象和本质的联系.
考点点评: 解答本题的关键是要掌握物质的物理性质和化学性质,只有这样才能对问题做出正确的判断.1年前查看全部
- 含碘盐中含的是碘化钾,请设计一种试纸,方便准确的测试碘盐中的碘离子,并写出检验的操作
 冰点爱一回伤一回1年前2
冰点爱一回伤一回1年前2 -
 心随鱼雪 共回答了25个问题
心随鱼雪 共回答了25个问题 |采纳率96%把碘盐溶液 滴加、到氯水带淀粉的试纸1年前查看全部
- 臭氧(O 3 )可以使湿润的淀粉碘化钾试纸变蓝,同时产生O 2 ,则:
臭氧(O 3 )可以使湿润的淀粉碘化钾试纸变蓝,同时产生O 2 ,则:
(1)该反应的化学方程式为:______;
(2)该反应中氧化剂的名称为______,还原产物的化学式为______;
(3)若消耗0.1mol氧化剂,反应中转移电子的物质的量为______. xingrou1年前1
xingrou1年前1 -
 senloveJennifer 共回答了9个问题
senloveJennifer 共回答了9个问题 |采纳率77.8%(1)臭氧(O 3 )可以使湿润的淀粉碘化钾试纸变蓝,说明反应过程中有碘单质生成,反应中碘化钾是还原剂,臭氧作氧化剂得电子发生还原反应,所以是碘化钾和臭氧、水反应生成碘、氧气和氢氧化钾,
反应方程式为:2KI+O 3 +H 2 O=2KOH+I 2 +O 2 .
故答案为:2KI+O 3 +H 2 O=2KOH+I 2 +O 2 ;
(2)该反应中臭氧得电子化合价降低,所以臭氧是氧化剂;氧化剂对应的产物是还原产物,所以氢氧化钾是还原产物.
故答案为:臭氧; KOH;
(3)设转移电子的物质的量是x.
2KI+O 3 +H 2 O=2KOH+I 2 +O 2 转移电子
1mol 2mol
0.1mol x
x=0.2mol
故答案为:0.2 mol.1年前查看全部
- PH试纸与pHS-2C型酸度计测定溶液的PH值的准确度如何
 iefha1年前3
iefha1年前3 -
 chenchu5588 共回答了18个问题
chenchu5588 共回答了18个问题 |采纳率94.4%pHS-2C型酸度计测定溶液的PH值的准确度要高些
pHS-2C型酸度计的基本误差为:±0.02pH
广泛PH试纸只能读取整数值,精密PH试纸通常能精确到±0.2pH1年前查看全部
- 下列各种情况下,可以大量共存的离子组是( ) A.使pH试纸呈红色的溶液中:Fe 3+ 、NO 3 - 、SO 4 2
下列各种情况下,可以大量共存的离子组是( ) A.使pH试纸呈红色的溶液中:Fe 3+ 、NO 3 - 、SO 4 2- 、Na + B.由水电离的c(H + )=1×10 -14 mol/L的溶液中:Ba 2+ 、K + 、Cl - 、HCO 3 - C.与Al反应放出大量氢气的溶液中:NH 4 + 、SO 4 2- 、CO 3 2- 、Na + D.使紫色石蕊变蓝的溶液中:NH 4 + 、Al 3+ 、Ca 2+ 、Cl -  失落的再见萤火虫1年前1
失落的再见萤火虫1年前1 -
 I眼看穿 共回答了18个问题
I眼看穿 共回答了18个问题 |采纳率94.4%A、使pH试纸呈红色的溶液中存在大量的H + ,该条件下该组离子之间不反应,则能够大量共存,故A正确;
B、由水电离的c(H + )=1×10 -14 mol/L的溶液,水的电离受到抑制,溶液可能为酸或碱溶液,酸溶液中H + 、HCO 3 - 结合生成水和二氧化碳气体,碱溶液中OH - 、HCO 3 - 、Ba 2+ 结合生成碳酸钡沉淀和水,则离子一定不能大量共存,故B错误;
C、与Al反应放出大量氢气的溶液可能为酸或碱的溶液,酸溶液中H + 、CO 3 2- 结合生成水和二氧化碳气体,碱溶液中OH - 、NH 4 + 结合生成弱电解质,则不能大量共存,故C错误;
D、使紫色石蕊变蓝的溶液中存在较多的OH - ,NH 4 + 、Al 3+ 都能分别与OH - 反应生成一水和氨、氢氧化铝沉淀,则不能大量共存,故D错误;
故选A.1年前查看全部
- (09衢州)为了鉴定实验室一瓶标签脱落的无色试剂,某同学开展如下实验,步骤1:先用蒸馏水湿润pH试纸,然后用玻璃棒蘸取该
(09衢州)为了鉴定实验室一瓶标签脱落的无色试剂,某同学开展如下实验,步骤1:先用蒸馏水湿润pH试纸,然后用玻璃棒蘸取该溶液滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,测得溶液的pH为2;步骤2:取少量该溶液于试管中,加入氯化钡溶液和稀盐酸,无明显变化;步骤3:另取少量该溶液,加入硝酸银溶液,产生白色沉淀,再加足量的稀硝酸,沉淀不消失。步骤1中错误的操作是 ;根据以上实验可以推断该试剂为 溶液。
 豳风-七月1年前1
豳风-七月1年前1 -
 dychdj 共回答了14个问题
dychdj 共回答了14个问题 |采纳率85.7%先用蒸馏水湿润pH试纸盐酸
① 相关知识点:物质的检验溶液的pH值测定方法
②解析思路:用pH试纸测溶液的pH时,不能用水润湿,否则会对结果造成影响,测酸时结果偏大。通过步骤1可知该溶液显酸性,含有氢离子,步骤2说明溶液中不含硫酸根离子,步骤3说明溶液中含有氯离子。1年前查看全部
- 氯气使淀粉-KI试纸变蓝后会不会再褪色?
 itisnottrue1年前1
itisnottrue1年前1 -
 xingyuanchao 共回答了16个问题
xingyuanchao 共回答了16个问题 |采纳率87.5%该反应生成的是络合物,属络和反应.就好象碘融到了淀粉里,由于范德瓦耳斯力,也就是分子间作用力,产生的的变蓝的结果,除非人为的使两重物质分离.1年前查看全部
- 在实验室中,某学生测定溶液的pH时,将pH试纸先用水润湿或浸在待测液中,请问上述两种操作是否正确?如不正确,指出错误所在
在实验室中,某学生测定溶液的pH时,将pH试纸先用水润湿或浸在待测液中,请问上述两种操作是否正确?如不正确,指出错误所在,如何正确使用pH试纸测溶液的pH.
 箜箜no11年前1
箜箜no11年前1 -
 louiswen 共回答了17个问题
louiswen 共回答了17个问题 |采纳率88.2%解题思路:测定pH最简单的方法是使用pH试纸,测定时,用玻璃棒蘸取待测溶液,滴在试纸上,然后再与标准比色卡对照,便可测出溶液的pH,这是检验溶液PH的正确方法,利用这一方法可进行相关的判断.pH试纸直接浸入待测液,这样操作会污染溶液,pH试纸先用水润湿再浸入待测,这样的操作会使待测溶液变稀,导致测量的数据不准确,故这两种测量溶液pH的方式均不正确.正确的操作应该是:测定时,用玻璃棒蘸取待测溶液,滴在试纸上,然后再与标准比色卡对照,便可测出溶液的pH;
答:上述两种操作均不正确;正确的测量方法是:用玻璃棒蘸取待测溶液,滴在试纸上,然后再与标准比色卡对照,便可测出溶液的pH.点评:
本题考点: 溶液的酸碱度测定.
考点点评: 此题是对PH试纸使用的考查,解题的关键是能正确的解决PH使用的操作要领,属实验基本操作题.1年前查看全部
- 下面框图中B用于改良酸性土壤,J是最常见的金属,G是红棕色粉末,E、F、I为无色气体,I能使湿润的红色石蕊试纸变蓝.
下面框图中B用于改良酸性土壤,J是最常见的金属,G是红棕色粉末,E、F、I为无色气体,I能使湿润的红色石蕊试纸变蓝.

(1)指出反应①的基本类型______.
(2)日常生活中为了阻止反应③发生,通常采取的措施是______(写一条).
(3)利用反应⑤可鉴别______和钾肥.
(4)写出反应②、⑤的化学方程式:
②2H2O
2H2↑+O2↑通电 .2H2O
2H2↑+O2↑通电 .
⑤______. VIP-职业灌水者1年前1
VIP-职业灌水者1年前1 -
 paulapauling 共回答了21个问题
paulapauling 共回答了21个问题 |采纳率95.2%解题思路:根据B可以用于改良酸性土壤,所以B是氢氧化钙,I是无色气体,I能使湿润的红色石蕊试纸变蓝,氢氧化钙和氯化铵会生成氨气,所以I就是氨气,C通电会生成E和F,A和金属反应也会生成E,所以C是水,E是氢气,F就是氧气,氧气、水和J反应会生成红棕色的G,所以G是氧化铁,J是铁,A就是酸,A和氢氧化钙生成的D还得会与碳酸钠反应,所以A可以是盐酸,D就是氯化钙,H是碳酸钙,然后将推出的物质代入转换关系中进行验证即可.B可以用于改良酸性土壤,所以B是氢氧化钙,I是无色气体,I能使湿润的红色石蕊试纸变蓝,氢氧化钙和氯化铵会生成氨气,所以I就是氨气,C通电会生成E和F,A和金属反应也会生成E,所以C是水,E是氢气,F就是氧气,氧气、水和J反应会生成红棕色的G,所以G是氧化铁,J是铁,A就是酸,A和氢氧化钙生成的D还得会与碳酸钠反应,所以A可以是盐酸,D就是氯化钙,H是碳酸钙,通过验证,推出的各种物质均满足题中的转化关系,推导合理,所以
(1)通过推导可知,反应①铁和盐酸反应生成氯化亚铁和氢气,该反应由一种单质与一种化合物反应生成另一种单质和另一种化合物,符合置换反应的条件,属于置换反应;
(2)铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程,只要消除一个条件,就可以阻止③的反应发生,所以通常采取的措施是:刷油漆;
(3)铵态氮肥和氢氧化钙反应会生成氨气,而钾肥不会,所以利用反应⑤可鉴别铵态氮肥和钾肥;
(4)反应②是水在通电的条件下生成氢气和氧气,化学方程式为:2H2O
通电
.
2H2↑+O2↑;
反应⑤是氢氧化钙和氯化铵反应生成氯化钙、水和二氧化碳,化学方程式为:Ca(OH)2+2NH4Cl=CaCl2+2H2O+2NH3↑.
故答案为:(1)置换反应;
(2)刷油漆;
(3)铵态氮肥;
(4)2H2O
通电
.
2H2↑+O2↑;Ca(OH)2+2NH4Cl=CaCl2+2H2O+2NH3↑.点评:
本题考点: 物质的鉴别、推断;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.1年前查看全部
- 用醋酸铅试纸检验硫化氢气体反而看不到硫化铅产生的特征亮黑色
 wldw6101年前1
wldw6101年前1 -
 ligl_520 共回答了14个问题
ligl_520 共回答了14个问题 |采纳率92.9%因为醋酸铅试纸使用之前要润湿1年前查看全部
- 碘化钾能使湿润的淀粉碘化钾试纸变蓝吗
 被你吓大的老鼠1年前1
被你吓大的老鼠1年前1 -
 1个人精彩 共回答了14个问题
1个人精彩 共回答了14个问题 |采纳率78.6%不能,能使之变蓝的是单质I,不是I离子1年前查看全部
- 浓硝酸或稀纸硝酸加到蓝色石蕊试纸上有什么现象?它们有漂白性吗
 爱你的腚1年前1
爱你的腚1年前1 -
 dsfasfasdfsdafsa 共回答了15个问题
dsfasfasdfsdafsa 共回答了15个问题 |采纳率80%浓硝酸加到蓝色石蕊试纸上,试纸先变红后褪色;
稀硝酸加到蓝色石蕊试纸上,试纸变红.
浓硝酸使试纸褪色,靠其强氧化性,也可称为漂白性,因腐蚀性强,不用作漂白剂1年前查看全部
- 能使PH试纸显蓝色的溶液中:Na+ ClO- Fe2+ SO42- 可以共存么?
能使PH试纸显蓝色的溶液中:Na+ ClO- Fe2+ SO42- 可以共存么?
如题.
如果是能使PH试纸显红色的溶液中:Na+ ClO- Fe2+ SO42- ClO-为什么会把Fe2+转化成3价? xx32573551年前3
xx32573551年前3 -
 zhaiqiuhua 共回答了25个问题
zhaiqiuhua 共回答了25个问题 |采纳率92%能使PH试纸显蓝色的溶液为碱性溶液,Fe2+ 与OH-反应生成沉淀,不可以大量共存
能使PH试纸显红色的溶液为酸性溶液,ClO-在酸性条件下具有较强的氧化性,而 Fe2+具有较强的还原性,ClO-把Fe2+转化成3价1年前查看全部
- 浓硫酸 氯水 红颜算滴在蓝色石蕊试纸上的颜色
浓硫酸 氯水 红颜算滴在蓝色石蕊试纸上的颜色
把浓硫酸、氯水、浓盐酸分别地在三张蓝色石蕊试纸上,最终呈现的颜色分别是_______、________、________? 我的天渊1年前3
我的天渊1年前3 -
 鸿玉 共回答了16个问题
鸿玉 共回答了16个问题 |采纳率100%把浓硫酸、氯水、浓盐酸分别滴在三张蓝色石蕊试纸上,最终呈现的颜色分别是黑色、白色、红色 .
浓硫酸显酸性,先会使蓝色石蕊试纸变成红色,因为浓硫酸具有脱水性,会使石蕊试纸炭化,最后显黑色.
氯气遇到水生成盐酸和次氯酸,次氯酸会使蓝色石蕊试纸褪成无色.
浓盐酸显酸性,会使蓝色石蕊试纸变红色.1年前查看全部
- 氯气的酒精溶液为什么不能使干燥的蓝色石蕊试纸变红又褪色?
 my稻草人1年前1
my稻草人1年前1 -
 hehelanyu 共回答了15个问题
hehelanyu 共回答了15个问题 |采纳率86.7%酒精中有水,与氯气反应生成盐酸和次氯酸,都有酸性,试纸变红,次氯酸有漂白性,可使试纸变白.我觉得1年前查看全部
- 取三张蓝色石蕊试纸湿润后贴在玻璃片上,然后按顺序分别滴加65%硝酸溶液、98%的硫酸溶液、新制氯水,三张试纸最终变成(
取三张蓝色石蕊试纸湿润后贴在玻璃片上,然后按顺序分别滴加65%硝酸溶液、98%的硫酸溶液、新制氯水,三张试纸最终变成( ).
 屋檐无语1年前1
屋檐无语1年前1 -
 诗韵梦月 共回答了25个问题
诗韵梦月 共回答了25个问题 |采纳率88%取三张蓝色石蕊试纸湿润后贴在
玻璃片上,然后按顺序分别滴加65%硝酸溶液、98%的硫酸溶液、新制氯水,三张试纸最终变成( ).
(A)白、红、白 (B)红、黑、白
(C)红、红、红 (D)白、黑、白1年前查看全部
- 用冰醋酸,蒸馏水、PH试纸如何证明醋酸(CH3COOH)是弱酸
 ewrwerer1年前1
ewrwerer1年前1 -
 killua111 共回答了16个问题
killua111 共回答了16个问题 |采纳率100%配制约0.1mol/L的醋酸溶液(约1:120稀释),使用pH试纸检测,如果其pH远大于1,则说明醋酸是弱酸.1年前查看全部
- 检验氯气,硫化氢,氨气,溴化氢这四种气体,可选用的试纸有:醋酸铅试纸,碘化钾淀粉试纸,酚酞试纸,蓝色石蕊试纸,红色石蕊试
检验氯气,硫化氢,氨气,溴化氢这四种气体,可选用的试纸有:醋酸铅试纸,碘化钾淀粉试纸,酚酞试纸,蓝色石蕊试纸,红色石蕊试纸,假定每种试纸限用一次.以下选择对应试纸的顺序中,正确的是
2135 5423 5312 2134 秋水11111年前1
秋水11111年前1 -
 janezhu200 共回答了13个问题
janezhu200 共回答了13个问题 |采纳率92.3%氯气是淀粉碘化钾 发生的反应时Cl2+2KI===2KCl+I2
硫化氢是醋酸铅 Pb(CH3COO)2+H2S===PbS+2CH3COOH
氨气是湿润的红色石蕊试纸 因为氨气是碱性的
溴化氢则是湿润的蓝色石蕊试纸 因为溴化氢是酸性的
石蕊试纸可以看做是石蕊溶液1年前查看全部
- 什么能使氯化钯试纸变蓝?是一种气体!
 头牌不举1年前2
头牌不举1年前2 -
 盗夜香者 共回答了13个问题
盗夜香者 共回答了13个问题 |采纳率92.3%是一氧化碳.
CO+PdCl2+H2O=CO2+Pd↓+2HCl1年前查看全部
- 有关化学分子那一部分的题依据下列现象回答问题:1.将颗粒状的碘放在湿淀粉纸上,试纸变成蓝色;2.用玻璃棒蘸取酒精,碘酒分
有关化学分子那一部分的题
依据下列现象回答问题:1.将颗粒状的碘放在湿淀粉纸上,试纸变成蓝色;2.用玻璃棒蘸取酒精,碘酒分别滴在淀粉试纸上,滴酒精的试纸不变蓝,滴碘酒的试纸变蓝;3.把五氧化二碘放在干燥的试管中加热,将湿淀粉纸放在试管口,淀粉纸上,淀粉试纸变蓝色;4.将带火星的木条放在试管口,木条复燃.
1.可能得到关于分子的结论 投影在水中1年前1
投影在水中1年前1 -
 lesliefang 共回答了14个问题
lesliefang 共回答了14个问题 |采纳率92.9%不知道问题是什么
分子式表现物质化学性质的最小单位
能够使淀粉变蓝的是碘分子
在物理变化中分子的结构不会改变,所以碘酒溶液中的碘分子可以使淀粉变蓝
五氧化二碘加热时分解为碘分子和氧气分子所以能使淀粉试纸变蓝,同时带火星的木条复燃1年前查看全部
- “漂白粉溶液可使淀粉碘化钾试纸变蓝”“次氯酸钠可以与亚硫酸钠共存”这2句话对不对?
 xahjp6661年前1
xahjp6661年前1 -
 麻团儿炖蘑菇 共回答了17个问题
麻团儿炖蘑菇 共回答了17个问题 |采纳率94.1%在中学阶段,第一句是对的.漂白粉中有Ca(ClO)2,会与KI发生反应:ClO- + 2I- + H2O = Cl- + I2 + 2OH-,产生I2,使淀粉变蓝.
第二句……如果是固体,那么是正确的;如果是溶液,就是错的,因为会反应:ClO- + SO32- = Cl- + SO42-1年前查看全部
- 1、SO2能使淀粉碘化钾试纸变蓝吗 2、少量SO2通入漂白粉溶液的反应物和生成物,过量SO2呢
1、SO2能使淀粉碘化钾试纸变蓝吗 2、少量SO2通入漂白粉溶液的反应物和生成物,过量SO2呢
有把握再回答 不要误导
用高一的化学知识回答就可以了 不用太深 ColdBloodAnimal11年前1
ColdBloodAnimal11年前1 -
 海东311 共回答了18个问题
海东311 共回答了18个问题 |采纳率94.4%1.不能.SO2与KI不反应,SO2的氧化性很弱,不足以把I-氧化成I2.
但是I2+SO2+2H2O=2HI+H2SO4
2.Ca2+ + CIO- + SO2 +H2O =CI- +CaSO4(沉淀) +2H+,如果SO2过量,再发生SO2+H2O=H2SO31年前查看全部
- 五色试液使红色石蕊试纸变蓝,结论:一定是碱溶液?
五色试液使红色石蕊试纸变蓝,结论:一定是碱溶液?
五色试液使红色石蕊试纸变蓝,结论:一定是碱溶液.答案是不对.不知为什么、、求答、、谢谢~
额…是无色… 鸟天堂sctj1年前1
鸟天堂sctj1年前1 -
 黄抱车夫 共回答了18个问题
黄抱车夫 共回答了18个问题 |采纳率88.9%不是!因为有些盐溶液电离之后也显碱性!常见的有Na2CO3.NaHCO31年前查看全部
- Cl2使湿润蓝色石蕊试纸怎么变化?
Cl2使湿润蓝色石蕊试纸怎么变化?
是先变红再腿色吗?我觉得是这样的,可老师的答案是只变红.难道是老师的答案错了吗? 落尘点点1年前1
落尘点点1年前1 -
 anne** 共回答了23个问题
anne** 共回答了23个问题 |采纳率91.3%先变红,再褪色.
因为Cl2+H2O=HCl+HClO,生成盐酸完全电离为氢离子和氯离子,而氢离子使蓝色石蕊试纸变红(这是离子反应,接触充分,反应快),
褪色是因为Cl2与H2O生成的HClO具有强氧化性,将色素氧化,反应相对要慢一些.1年前查看全部
大家在问
- 1描述一个自己在生活中看到过的科学现象,并简单解释它的形成原因
- 2求这两首诗的题目:1)晴川历历汉阳树,芳草萋萋鹦鹉洲。2)亭亭山上松,瑟瑟谷中风。
- 3已知A-2B=7a²-7ab,B=-4a²+6ab+7 (1)求A (2)若|a+1|=0,(b-
- 4内有关汽油机和柴油机的说法,不正确的是
- 5解不等式ax^2-(a^2+3)x+3a>0(a>0)
- 6现有一杯20摄氏度的饱和氯化钾溶液,其溶质的质量分数是25.4%,请回答以下问题:
- 7二氧化氮和氮气哪个是空气污染物?
- 83(x+2)³-81=0
- 9如图,直线y=2x+4与x轴、y轴分别相交于A、B两点,把△OAB绕点O顺时针旋转得到△OCD.
- 10谁能告诉我在英语中in the first person
- 11分析判断:(1)已知线段AB=10cm,1.点C在线段AB上,点D.E分别是AC和BC的中点,求线段DE的长.2.若点C
- 12(2008•茂名一模)豇豆对多种害虫具有抗性,根本原因是豇豆体内具有胰蛋白酶抑制剂基因(CPTI基因).科学家将其转移到
- 13匆匆 朱自清仿写第二自然段,就是默默里算着,到我不禁头涔涔而泪潸潸了.
- 14Shopping will be ____ cheaper if in holidays.
- 15能否用水蒸气蒸馏分离硝基苯和苯胺的混合物
