span 标签的用法``举例说明下``谢谢``
 tiantian1662022-10-04 11:39:541条回答
tiantian1662022-10-04 11:39:541条回答如何运用span让 层横向排列``请举例说明``谢谢咯~``

已提交,审核后显示!提交回复
共1条回复
 sineal 共回答了24个问题
sineal 共回答了24个问题 |采纳率75%- span标记不能用来控制层
控制层的标签
span标签可以用来控制一行文字的样式
如果想控制层得横向排列,可以这样定义
样式
然后在div标签中调用即可 - 1年前
相关推荐
- 图示是某学校实验室从化学试剂商店买回来的硫酸试剂标签上的部分内容.某实验需要0.5mol•L-1 H2SO4溶液240m
图示是某学校实验室从化学试剂商店买回来的硫酸试剂标签上的部分内容.某实验需要0.5mol•L-1 H2SO4溶液240mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84g•cm-3
质量分数:98%
①所需浓硫酸的体积是______mL,若该硫酸与等体积的水混合后,所得溶液中溶质的质量分数______
49%(填写“<”“=”或“>”).
②配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是______. wh太阳鸟1年前1
wh太阳鸟1年前1 -
 西安兆隆7 共回答了19个问题
西安兆隆7 共回答了19个问题 |采纳率89.5%解题思路:①根据c=[1000ρω/M]计算浓硫酸的物质的量浓度,没有240mL容量瓶,应选择250mL容量瓶,再根据稀释定律计算需要浓硫酸的体积;该硫酸与等体积的水混合后,所得溶液的质量小于原硫酸溶液质量的2倍,而溶质硫酸的质量不变;
②浓硫酸稀释:将浓硫酸沿器壁(或玻璃棒)慢慢注入水中,且边加边搅拌.①浓硫酸的物质的量浓度=[1000×1.84×98%/98]mol/L=18.4mol/L,没有240mL容量瓶,应选择250mL容量瓶,根据稀释定律,需要浓硫酸的体积=[250mL×0.5mol/L/18.4mol/L]=6.8mL;
该硫酸与等体积的水混合后,所得溶液的质量小于原硫酸溶液质量的2倍,而溶质硫酸的质量不变,所得溶液的质量分数>49%,
故答案为:6.8;>;
②浓硫酸稀释:将浓硫酸沿器壁(或玻璃棒)慢慢注入水中,且边加边搅拌,故答案为:将浓硫酸沿器壁(或玻璃棒)慢慢注入水中,且边加边搅拌.点评:
本题考点: 物质的量浓度的相关计算;配制一定物质的量浓度的溶液.
考点点评: 本题考查溶液浓度计算、基本操作,比较基础,注意理解掌握物质的量浓度与质量分数之间的关系.1年前查看全部
- .图6是某省生产的加钙加碘实验包装标签上的部分文字,请仔细阅读后回答下列问题配料表:氯化钠、食用碳
.图6是某省生产的加钙加碘实验包装标签上的部分文字,请仔细阅读后回答下列问题配料表:氯化钠、食用碳
酸钙、碘酸钾净含量:500g钙(以Ca计):0.5%-1.3%碘(以I计):(20-50)mg/kg.每千克这种食盐中至少要加多少克碳酸钙才符合要求?急啊!
 asdfgqeuy1年前1
asdfgqeuy1年前1 -
 matrixbirdy 共回答了17个问题
matrixbirdy 共回答了17个问题 |采纳率100%0.5%*1000g / (40/ 100)=12.5g1年前查看全部
- 探究性学习小组的同学发现化学实验室一瓶白色固体粉末已失去标签.科代表将粉末取少量于试管中,加入足量的稀盐酸,有大量的气泡
探究性学习小组的同学发现化学实验室一瓶白色固体粉末已失去标签.科代表将粉末取少量于试管中,加入足量的稀盐酸,有大量的气泡冒出,用向上排空气法收集到一集气瓶气体.同学们很兴奋,白色固体粉末可能是什么物质?他们设计实验方案,展开探究.
(1)猜想:产生的气体可能是______.
(2)检验气体的实验记录如下:
(3)根据上述实验结果推断,白色固体可能是______.实验操作 实验现象 结论 ______ ______ 产生的气体是______.
(4)白色固体还可能是______,理由是______. hury_011年前1
hury_011年前1 -
 batistuta1 共回答了16个问题
batistuta1 共回答了16个问题 |采纳率93.8%(1)由于该白色粉末加入盐酸后会生成气体,所以可以猜想是碳酸盐的白色固体遇盐酸会产生二氧化碳气体;
(2)检验二氧化碳可采用澄清的石灰水进行验证,如果气体通入到石灰水中时石灰水变浑浊,则说明该气体就是二氧化碳;
(3)由以上的解答可知该碳酸盐的粉末可能是碳酸钠;
(4)碳酸钾同样是能与稀盐酸生成二氧化碳的白色粉末,所以该白色粉末也可能是碳酸钾等;
故答案为:(1)二氧化碳;
(2)
实验操作 实验现象 结论
将收集的气体通入到澄清石灰水中. 石灰水变浑浊. 产生的气体是二氧化碳. (3)碳酸钾(合理即可);碳酸钾同样是能与稀盐酸生成二氧化碳的白色粉末;1年前查看全部
- (09衢州)为了鉴定实验室一瓶标签脱落的无色试剂,某同学开展如下实验,步骤1:先用蒸馏水湿润pH试纸,然后用玻璃棒蘸取该
(09衢州)为了鉴定实验室一瓶标签脱落的无色试剂,某同学开展如下实验,步骤1:先用蒸馏水湿润pH试纸,然后用玻璃棒蘸取该溶液滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,测得溶液的pH为2;步骤2:取少量该溶液于试管中,加入氯化钡溶液和稀盐酸,无明显变化;步骤3:另取少量该溶液,加入硝酸银溶液,产生白色沉淀,再加足量的稀硝酸,沉淀不消失。步骤1中错误的操作是 ;根据以上实验可以推断该试剂为 溶液。
 豳风-七月1年前1
豳风-七月1年前1 -
 dychdj 共回答了14个问题
dychdj 共回答了14个问题 |采纳率85.7%先用蒸馏水湿润pH试纸盐酸
① 相关知识点:物质的检验溶液的pH值测定方法
②解析思路:用pH试纸测溶液的pH时,不能用水润湿,否则会对结果造成影响,测酸时结果偏大。通过步骤1可知该溶液显酸性,含有氢离子,步骤2说明溶液中不含硫酸根离子,步骤3说明溶液中含有氯离子。1年前查看全部
- 下图为某医用葡萄糖注射液标签的一部分,据此下列说法不正确的是( )
下图为某医用葡萄糖注射液标签的一部分,据此下列说法不正确的是()

A.该葡萄糖注射液中溶质的质量分数为5% B.葡萄糖的相对分子质量为180 C.葡萄糖中碳元素、氢元素和氧元素的质量比为1:2:1 D.在人体组织里,葡萄糖在酶的作用下经缓慢氧化转变成二氧化碳  yang00551年前1
yang00551年前1 -
 justinajiang 共回答了16个问题
justinajiang 共回答了16个问题 |采纳率87.5%C
1年前查看全部
- (2008•哈尔滨)某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液.现有一瓶标签已破损的过氧化氢溶液,为测定瓶内
 (2008•哈尔滨)某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液.现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g.请根据要求回答下列问题:
(2008•哈尔滨)某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液.现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g.请根据要求回答下列问题:
(1)加入二氧化锰后发生反应的化学方程式为2H202
2H20+02↑MnO2 .2H202;
2H20+02↑MnO2 .
(2)生成氧气的质量是______;
(3)根据氧气的质量列出求解过氧化氢质量(x)的比例式为[68/32=
=X 3.2g] [68/32X 3.2g];
(4)瓶内过氧化氢溶液中溶质的质量分数是______;
(5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是______.赞
ji28941 幼苗
共回答了18个问题采纳率:94.4% 举报
解题思路:(1)过氧化氢在常温可以发生分解反应生成氧气和水(缓慢分解),在加热或者加入催化剂后能加快反应,通常使用的催化剂为二氧化锰.据此写出化学方程式即可;
(2)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.故生成氧气的质量=反应前各物质的质量总和-反应后生成各物质的质量总和;
(3)根据过氧化氢分解的化学方程式和生成氧气的质量,列出比例式,就可得出求解过氧化氢质量(x)的比例式;
(4)根据溶质质量分数=[溶质质量/溶液质量]×100%计算即可;
(5)根据溶质一定,列出方程式,就可计算出需瓶内溶液的质量,然后100g-需瓶内溶液的质量就是需加入水的质量.(1)加入二氧化锰后发生反应的化学方程式为:2H202 MnO2 . 2H20+02↑;(2)生成氧气的质量为:34g+3g-33.8g=3.2g;(3)设参与反应的过氧化氢的质量为x,2H202 MnO2 . 2H20+02↑68-...
点评:
本题考点: 根据化学反应方程式的计算;实验室制取氧气的反应原理;有关溶质质量分数的简单计算;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查学生运用化学方程式和溶质质量分数和质量守恒定律综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前
1可能相似的问题-
1年前1个回答
-
1年前1个回答
你能帮帮他们吗
Copyright © 2022 YULUCN.COM - 雨露学习互助 - 17 q. 0.019 s. - webmaster@yulucn.com nanayi1年前1
nanayi1年前1 -
 ji28941 共回答了18个问题
ji28941 共回答了18个问题 |采纳率94.4%解题思路:(1)过氧化氢在常温可以发生分解反应生成氧气和水(缓慢分解),在加热或者加入催化剂后能加快反应,通常使用的催化剂为二氧化锰.据此写出化学方程式即可;
(2)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.故生成氧气的质量=反应前各物质的质量总和-反应后生成各物质的质量总和;
(3)根据过氧化氢分解的化学方程式和生成氧气的质量,列出比例式,就可得出求解过氧化氢质量(x)的比例式;
(4)根据溶质质量分数=[溶质质量/溶液质量]×100%计算即可;
(5)根据溶质一定,列出方程式,就可计算出需瓶内溶液的质量,然后100g-需瓶内溶液的质量就是需加入水的质量.(1)加入二氧化锰后发生反应的化学方程式为:2H202 MnO2 . 2H20+02↑;(2)生成氧气的质量为:34g+3g-33.8g=3.2g;(3)设参与反应的过氧化氢的质量为x,2H202 MnO2 . 2H20+02↑68-...
点评:
本题考点: 根据化学反应方程式的计算;实验室制取氧气的反应原理;有关溶质质量分数的简单计算;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查学生运用化学方程式和溶质质量分数和质量守恒定律综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 一句话翻译成英文,“你是需要空白的黑墨标签20张吗?”
 ansilieyo1年前2
ansilieyo1年前2 -
 圣淘沙的红树林 共回答了15个问题
圣淘沙的红树林 共回答了15个问题 |采纳率93.3%Do you need 20 pieces of blank black ink tags?1年前查看全部
- 下表为某品牌燕麦片标签中的一部分: 营养成分 蛋白质 糖类 油脂 钙 铁 钠 锌 维生素C 每100g含有 7.4 g
下表为某品牌燕麦片标签中的一部分:
(1)燕麦片中能为人体提供能量的营养素有______;营养成分 蛋白质 糖类 油脂 钙 铁 钠 锌 维生素C 每100g含有 7.4 g 7.8 g 7.9 g 206 mg 19.2 mg 37.8 mg 10.1 mg 18 mg
(2)燕麦片中含有______种人体所需的微量元素;
(3)人体健康离不开钙元素.下列有关钙元素的叙述中,不正确的是(填序号)______;
①人体中钙元素大部分存在于骨骼和牙齿中
②幼儿及青少年缺钙会得佝偻病和发育不良
③老年人缺钙会发生骨质疏松,容易骨折
④成年人比幼儿和青少年需要摄入更多的钙
(4)钙片的有效成分是碳酸钙,虽然碳酸钙难溶于水,但服用后可转化为可溶性钙盐被人体吸收,其原因是______(用化学方程式表示);为了提高补钙效果,服用钙片时常需配合服用维生素D,据此可推知维生素D的功能是______.
(5)现有下列食物:①大米②豆油③鱼④鸡蛋⑤青菜 ⑥西瓜.其中能提供丰富蛋白质的有______. 白郁金香1年前1
白郁金香1年前1 -
 alexqianqian 共回答了16个问题
alexqianqian 共回答了16个问题 |采纳率93.8%由标签可判断出燕麦片中含有的营养素;六类营养素中能提供能量的营养素有糖类、蛋白质、油脂.服用钙片时常需配合服用维生素D可提高补钙效果,故可推测出它能促进钙片在人体内的吸收.
故答案为:(1)糖类、蛋白质、油脂
(2)2
(3)④
(4)CaCO 3 +2HCl═CaCl 2 +H 2 O+CO 2 ↑促进钙片在人体内的吸收
(5)③④1年前查看全部
- 我们在生活中会接触到许多英文标志,如在公共场所,在食品的包装上,在义务的标签上……请列出你所搜集的英文标志,并写出中文含
我们在生活中会接触到许多英文标志,如在公共场所,在食品的包装上,在义务的标签上……请列出你所搜集的英文标志,并写出中文含义与发现地点.
例:英文标志 中文含义 发现地点
Cotton 棉,棉花 衣服外套上
“义务“应该是“衣物
越多越好!好的有赏! 披云促宴筵1年前1
披云促宴筵1年前1 -
 luxinrun 共回答了21个问题
luxinrun 共回答了21个问题 |采纳率100%wc 厕所 公厕
parking 停车 马路边
capsule 胶囊 药盒
caution 注意 各种包装袋
!你也太自大了吧,孩子.1年前查看全部
- 尿素[CO(NH2)2]是一种化肥,右表为某品牌尿素包装袋上的标签.
 尿素[CO(NH2)2]是一种化肥,右表为某品牌尿素包装袋上的标签.
尿素[CO(NH2)2]是一种化肥,右表为某品牌尿素包装袋上的标签.
求:(本题计算结果保留小数点后一位)
(1)尿素中氮元素的质量分数.
(2)某一片地计划施用氮元素质量30Kg,实际需要施用这种品牌的尿素多少Kg? 我是蛙蛙1年前1
我是蛙蛙1年前1 -
 泉水叮儿 共回答了16个问题
泉水叮儿 共回答了16个问题 |采纳率93.8%解题思路:(1)尿素中氮元素的质量分数=[氮的相对原子质量×氮原子个数/尿素的相对分子质量]×100%;
(2)利用元素的质量分数等于物质的质量乘以该元素的质量分数解决.(1)尿素中氮元素的质量分数=[氮的相对原子质量×氮原子个数/尿素的相对分子质量]×100%=[14×2/60]×100%≈46.7%;
(2)根据某一片元素的质量分数等于物质的质量乘以该元素的质量分数,所以计划施用氮元素质量30Kg,实际需要施用这种品牌的尿素=[30kg/46.7%]=65.2Kg
答:(1)尿素中氮元素的质量分数是46.7%;
(2)某一片地计划施用氮元素质量30Kg,实际需要施用这种品牌的尿素65.2Kg.点评:
本题考点: 元素的质量分数计算;混合物中某元素的质量计算;标签上标示的物质成分及其含量.
考点点评: 主要考查了元素质量分数的求法,这些基本计算要求掌握.元素质量的求法,利用了:①某元素的质量分数=[该元素分子的相对原子质量×原子个数/相对分子质量]×100%;②某元素的质量=物质的质量×某元素的质量分数这两个计算公式.1年前查看全部
- 如图为某加钙食盐包装袋袋上的标签.小明为了探究该食盐中的钙元素的含量:取30.00g该盐样品,测得期中碳元素0.09g
如图为某加钙食盐包装袋袋上的标签.小明为了探究该食盐中的钙元素的含量:取30.00g该盐样品,测得期中碳元素0.09g

(1)30.00g该食盐中含碳酸钙的质量是多少?
(2)此加钙食盐钙含量是否符合标签要求?
(3)一袋该加钙食盐中至少要加入碘酸钾多少克?
(4)若一个成年人每天摄取5.0g碘盐,则至少能从中获取碘元素多少克?
 skill61年前1
skill61年前1 -
 鱼哇哇 共回答了22个问题
鱼哇哇 共回答了22个问题 |采纳率81.8%(1)设该食盐中含碳酸钙的质量为x
CaCO3------------Ca(NO3)2
100 44
x 0.33g
100/44=x/0.33g -----x=0.75g
30.00g食盐中含碳酸钙的质量是0.75g;
(2)加钙食盐钙元素的质量分数为 =(0.75*40/100)/30×100%=1.0%,
根据标签钙判断 此加钙食盐钙含量符合标签要求.
(3) 一袋500g的加碘食盐中碘酸钾的质量:碘含量(以I计)35mg/kg ,所以500g规格碘含量17.5mg
碘酸钾的质量:214÷127×17.5=29.5mg
(4)一个成人每天摄取5g碘盐,则至少能从中获得碘元素0.175毫克.1年前查看全部
- 某药品标签内容如下表所示: 凯凯的妈妈去药店购买了一盒治疗感冒的药,取出说明书看了看,心中很是疑惑,但又不知道错在哪里。
某药品标签内容如下表所示: 
凯凯的妈妈去药店购买了一盒治疗感冒的药,取出说明书看了看,心中很是疑惑,但又不知道错在哪里。请你根据此说明书回答以下问题:
(1)此说明书中没有提供_________信息。
(2)你认为凯凯的妈妈应该怎么做?____________。
(3)你能否判断凯凯妈妈所购买的药是处方药还是非处方药?
(4)在家中服用药品时,应注意什么? tim602021年前1
tim602021年前1 -
 天冷你就回来 共回答了24个问题
天冷你就回来 共回答了24个问题 |采纳率95.8%(1)药品名称(正规)、功能与主治、贮藏、有效期、批准文号、生产企业等
(2)凯凯的妈妈可以向医生咨询之后,在医生指导下服用或者直接将药物退还药店等等(答案只要合理即可)
(3)据提供的信息,凯凯的妈妈买的是感冒药,一般不需要医生的处方,患者可以直接从药房或药店中购买。所以可以断定凯凯的妈妈购买的是非处方药。
(4)分析药品标签,充分考虑药品的不良反应,禁忌及注意事项等,对症下药;孕妇、哺乳期妇女和儿童服用更应严格按标签说明使用;还应分清处方药和非处方药。1年前查看全部
- 次氯酸钠 分析纯 的标签说明杂质含量 游离氯 不少于6% 碱(以NAOH)计 7-8% 最好把说明书发下那个化学纯的次氯
次氯酸钠 分析纯 的标签说明
杂质含量 游离氯 不少于6% 碱(以NAOH)计 7-8% 最好把说明书发下
那个化学纯的次氯酸钠浓度是多少 何小如1年前2
何小如1年前2 -
 肖无盐 共回答了11个问题
肖无盐 共回答了11个问题 |采纳率72.7%文名称:sodium hypochlorite
分子式:NaClO
分子量:74.44
性状:微黄色溶液,有似氯气的气味.熔点(℃):-6 ,沸点(℃):102.2 ,相对密度(水=1):1.10 .
用途:用于水的净化,以及作消毒剂、纸浆漂白等,医药工业中用制氯胺等.
储存:密闭阴凉干燥保存.
项目名称Item
分析纯AR
活性氯Active Chlorine
>=5.5%
游离碱(以NaOH计)Free alkali(as NaOH)
0.1%-1.0%
铁Iron(Fe)1年前查看全部
- 某瓶装保健食品的外包装标签上的部分文字如下图.某同学为了测定该保健食品中CaCO3的质量分数,进行了如下实验:将100片
 某瓶装保健食品的外包装标签上的部分文字如下图.某同学为了测定该保健食品中CaCO3的质量分数,进行了如下实验:将100片该食品放入一烧杯中,再向其中注入120g(足量)的稀盐酸,直到不再产生气泡时,测得烧杯内剩余物质的总质量为150.2g.
某瓶装保健食品的外包装标签上的部分文字如下图.某同学为了测定该保健食品中CaCO3的质量分数,进行了如下实验:将100片该食品放入一烧杯中,再向其中注入120g(足量)的稀盐酸,直到不再产生气泡时,测得烧杯内剩余物质的总质量为150.2g.
请你根据以上数据计算:
(1)反应生成气体(CO2)的质量为多少克?
(2)该保健食品中CaCO3的质量分数为多少?(注:该保健食品中其它成分不与盐酸反应) 看云在奔跑1年前1
看云在奔跑1年前1 -
 dino1314 共回答了18个问题
dino1314 共回答了18个问题 |采纳率94.4%解题思路:(1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,可求得反应生成气体(CO2)的质量
(2)根据反应的化学方程式和二氧化碳的质量可以求100片该食品中所含碳酸钙的质量,进而求出该保健食品中CaCO3的质量分数.(1)根据质量守恒定律反应前烧杯内物质的总质量等于烧杯内剩余物质的总质量与生成的二氧化碳的质量之和,故反应生成气体(CO2)的质量为:100×0.5g+120g-150.2g=19.8g;
(2)设100片该保健食品中CaCO3质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 19.8g
[100/44=
x
19.8g]
x=45g
该保健食品中CaCO3的质量分数:[45g/100×0.5g]=90%
答:(1)反应生成气体(CO2)的质量为19.8g;(2)该保健食品中CaCO3的质量分数为90%;点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题难度不是很大,主要考查了数据地分析及根据化学方程式进行计算,培养学生的分析能力和解决问题的能力.1年前查看全部
- 医生给病人输液时,常用葡萄糖注射液.下图为葡萄糖注射液的部分标签图,据图回答下列问题
医生给病人输液时,常用葡萄糖注射液.下图为葡萄糖注射液的部分标签图,据图回答下列问题
如果从瓶中取出100g,将他变为15%的注射液,需要加入_____g葡萄糖(精确到0.1g)

 easypeper1年前1
easypeper1年前1 -
 shenaxing 共回答了19个问题
shenaxing 共回答了19个问题 |采纳率89.5%设加入Xg,(5+X)/(100+X)=0.151年前查看全部
- (2014•顺德区二模)实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素
(2014•顺德区二模)实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种,为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如下实验(此处箭头表示得出实验结论)

根据上述实验,下列说法不正确的是( )
A.三种化肥中,尿素的含氮量最高
B.B物质为碳酸氢铵
C.常温下如要鉴别B、C两种样品,能能采取闻气味的方法
D.如果实验Ⅱ中B、C两种样品没有另取,则会使检验结果不准确 wlh751年前1
wlh751年前1 -
 eruyhrts 共回答了17个问题
eruyhrts 共回答了17个问题 |采纳率88.2%解题思路:A、根据三种肥料的含氮量考虑;B、根据碳酸氢铵与盐酸反应产生二氧化碳,氯化铵与盐酸不反应分析;C、根据碳酸氢铵易分解产生有刺激性气味气体分析;D、根据碳酸氢根离子与酸反应生成二氧化碳考虑;A、NH4Cl中氮元素的质量分数=[14/58.5]×100%=26.2%;NH4HCO3中氮元素的质量分数=[14/79]×100%=17.7%;CO(NH2)2中氮元素的质量分数=[28/60]×100%=46.7%故A说法正确;
B、因为碳酸氢铵与盐酸反应产生氯化铵、水、二氧化碳,氯化铵与盐酸不反应,所以B物质为碳酸氢铵,故B说法正确;
C、因为碳酸氢铵、氯化铵都是铵态氮肥,但是碳酸氢铵能分解,而氯化铵常温不分解.所以能采取闻气味的方法鉴别,C说法正确;
D、碳酸氢铵与盐酸反应产生氯化铵、水、二氧化碳,氯化铵与盐酸不反应,所以只要含有碳酸氢铵和氯化铵就能通过加入盐酸鉴别开,故D说法错误.
故选D.点评:
本题考点: 铵态氮肥的检验.
考点点评: 本题主要是考查了铵态氮肥的检验和碳酸氢根离子与酸反应产生气体,应熟悉物质之间的化学反应及反应的现象,能利用现象来确定物质.1年前查看全部
- 如图是某保健品标签的部分内容,请仔细阅读后回答下列问题 xxxx(品牌名称)
如图是某保健品标签的部分内容,请仔细阅读后回答下列问题
(1)该保健品的功能是______,其主要成分中,提供钙元素的物质是______;参与钙的代谢,促进其吸收的是______;矿物质中的锌元素属于人体的______元素(选填“微量”或“常量”),锌元素的符号是______.xxxx(品牌名称)
帮助防治骨质疏松
【每片主要成分】
碳酸钙1.5g
维生素D3 200国际单位
(维生素D3能参与钙和磷代谢,
促进其吸收并对骨质形成有重要作用)
镁、锌、锰等矿物质
(2)胃酸过多的病人,服用该保健品后,有时会出现腹胀、打嗝的反应,出现这种反应的原因是______,因此该保健品还可以用于治疗______.
(3)每片中钙元素的质量是______g. yingsu3051年前1
yingsu3051年前1 -
 戈壁狼2008 共回答了22个问题
戈壁狼2008 共回答了22个问题 |采纳率86.4%解题思路:(1)根据图中信息进行;根据常量元素与微量元素的区别和种类进行分析判断即可;根据元素符号的书写方法分析;
(2)根据碳酸盐能与盐酸反应有二氧化碳气体生成分析;
(3)根据化合物中某元素的质量=化合物的质量×元素的质量分数分析.(1)从图可以看出,该保健品的功能是防治骨质疏松症;其主要成分中,提供钙元素的物质是碳酸钙;参与钙的代谢,促进其吸收的是维生素D3;微量元素包括铁、钴、铜、锌、铬、锰、钼、氟、碘、硒,因此矿物质中的锌元素属于人体的微量元素;锌元素的符号是Zn;
(2)该保健品中含有碳酸钙,胃酸中的盐酸与碳酸钙反应产生二氧化碳,因此胃酸过多的病人,服用该保健品后,有时会出现腹胀、打嗝的反应;该保健品还可以用于治疗胃酸过多症;
(3)每片中钙元素的质量是1.5g×([40/100]×100%)=0.6g.
故答案为:(1)防治骨质疏松症;碳酸钙;维生素D3;微量;Zn;
(2)胃酸中的盐酸与碳酸钙反应产生二氧化碳;胃酸过多症;
(3)0.6.点评:
本题考点: 标签上标示的物质成分及其含量;酸的化学性质;化合物中某元素的质量计算;人体的元素组成与元素对人体健康的重要作用;矿物质与微量元素.
考点点评: 本题的难度不大,解题的关键是根据题中信息结合所学的化学知识进行分析、解决问题,能做到具体问题具体分析就可以.1年前查看全部
- 对危险化学品要在包装标签上印上警示性标志.下列化学品名称与警示标志名称对应正确的是( )
对危险化学品要在包装标签上印上警示性标志.下列化学品名称与警示标志名称对应正确的是( )
a. 酒精-剧***
b. 浓硫酸-腐蚀品
c. 氯化钠-易燃品
d. 烧碱-剧*** 昌黎县1年前1
昌黎县1年前1 -
 东心岭 共回答了18个问题
东心岭 共回答了18个问题 |采纳率83.3%解题思路:A.酒精易燃;
B.浓硫酸有强腐蚀性;
C.氯化钠不能燃烧;
D.烧碱有强腐蚀性.A.酒精易燃,是易燃品,故A错误;
B.浓硫酸有强腐蚀性,是腐蚀品,故B正确;
C.氯化钠不能燃烧,不是易燃品,故C错误;
D.烧碱有强腐蚀性,是腐蚀品,故D错误.
故选B.点评:
本题考点: 化学试剂的分类.
考点点评: 本题考查危险化学品的分类,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.1年前查看全部
- 一张A4纸,两个标签纸做承重结构
一张A4纸,两个标签纸做承重结构
使用一张A4纸,两张标签纸做一个承重的结构,要求高度在10到10.5cm间,不能使用其他任何材料,A4纸和标签纸可以剪裁、折叠 qpsoso1年前1
qpsoso1年前1 -
 attact777 共回答了16个问题
attact777 共回答了16个问题 |采纳率81.3%.头脑奥林匹克的试题.
把A4纸才成两半,具体大小要自己设计一下,一半折成瓦楞结构,就是像扇子那样的,另一半一分为二,卷成纸卷,用标签纸黏在瓦楞纸的下方,标签纸也裁一下,这样贴的更牢.
就是这样一个结构,是最佳设计方案,我做个这个试题.1年前查看全部
- 如图是某种加钙食盐包装标签上的部分文字,回答下列问题: 配料表:氯化钠
如图是某种加钙食盐包装标签上的部分文字,回答下列问题:
(1)包装标签上钙含量是指______(填“钙单质”“碳酸钙”或“钙元素”)配料表:氯化钠
食用碳酸钙 碘酸钾
净含量:500g
成分表:氯化钾≥88%
钙(以Ca计):(0.5-1.3%)
(2)为了检验此盐中是否有碳酸钙,在家庭厨房中可选用的物质______. 没正形1年前1
没正形1年前1 -
 正确的是 共回答了20个问题
正确的是 共回答了20个问题 |采纳率90%解题思路:(1)食品、药品、营养品等物质中的“钙”等不是以单质、化合物、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
(2)根据碳酸盐的检验方法进行分析解答.(1)某种加钙食盐包装标签上的钙含量中的“钙”不是以单质、碳酸钙、分子、原子等形式存在,这里所指的“钙”是强调存在的元素,与具体形态无关.
(2)因为碳酸钙中含有碳酸根离子,与酸反应有二氧化碳气体生成,故在家庭厨房里可选用食醋来检验盐中是否含有碳酸钙.
故答案为:(1)钙元素;(2)食醋.点评:
本题考点: 标签上标示的物质成分及其含量;证明碳酸盐.
考点点评: 本题难度不大,以加钙食盐包装标签为载体,考查了同学们新信息获取、处理及灵活运用化学知识进行分析问题、解决实际问题的能力.1年前查看全部
- 下面是一种除草剂瓶上的标签. 施药方法用清水将本剂稀释后,均匀喷洒于杂草叶面上. 作物 施药量(毫升:公顷) 棉花 40
下面是一种除草剂瓶上的标签.
(1)如果要在10公顷玉米地里喷洒这种除草剂,需要除草剂多少毫升?施药方法
用清水将本剂稀释后,均匀喷洒于杂草叶面上.作物 施药量(毫升:公顷) 棉花 40:1 玉米 60:1 水稻 55:1
(2)如果有100毫升这样的除草剂,可以喷洒多少公顷的水稻地? cyb1841年前1
cyb1841年前1 -
 saer74 共回答了22个问题
saer74 共回答了22个问题 |采纳率95.5%解题思路:(1)由题意可知:玉米地中喷洒的除草剂的施药量是:1公顷需要60毫升,现在有10公顷,则需要除草剂10个60毫升,根据整数乘法的意义,用乘法解答即可;
(2)由题意可知:水稻地中喷洒的除草剂的施药量是:1公顷需要55毫升,现在有100毫升这样的除草剂,可以喷洒多少公顷的水稻地,即求100毫升里面含有几个55,根据求一个数里面含有几个另一个数,用除法解答即可.(1)60×10=600(毫升);
答:需要除草剂600毫升;
(2)100÷55≈1.82(公顷);
答:可以喷洒1.82公顷的水稻地.点评:
本题考点: 按比例分配应用题.
考点点评: 解答此题用到的知识点:(1)整数乘法的意义;(2)求一个数里面含有几个另一个数,用除法解答.1年前查看全部
- 问一道初中化学试题某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液.现有一瓶标签已破损的过氧化氢(图见下),为测定
问一道初中化学试题
某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液.现有一瓶标签已破损的过氧化氢(图见下),为测定瓶内溶液中溶质的质量分数,取该溶液34克于烧杯中,加入一定量的二氧化锰.完全反应后,称得烧杯内剩余物质的总质量是33.8克,将杯内剩余物质过滤、洗涤、干燥后得滤渣3克.请回答下列问题:
(图内容:体积,500毫升.溶质化学式,H2O2.密度,1.2克/立方厘米.溶质质量分数,已破损.)
1.加入二氧化锰后发生反应的化学方程式为:______.
2.生成氧气的质量是______.
3.根据氧气的质量列出求解过氧化氢质量(X)的比例式为______.
4.瓶内过氧化氢溶液中溶质的质量分数是______.
5.若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100克,需加入水的质量是______.
我想要的是每个答案的具体计算过程.我实在不会做吖.谢谢.
 znkl5211年前1
znkl5211年前1 -
 xycaocao 共回答了16个问题
xycaocao 共回答了16个问题 |采纳率87.5%1.二氧化锰仅仅作为催化剂催化过氧化氢的分解,本身并不参加反应,所以加入二氧化锰以后的反应是过氧化氢的分解反应,即2H2O2=2H2O+O2↑
2.生成氧气的质量是_3.2g__.(34g+3g-33.8g=3.2g)
3.根据方程式2H2O2=2H2O+O2↑可知
2*34 32
x 3.2
=>x=3.2*2*34/32=6.8g
4.瓶内过氧化氢溶液中溶质的质量分数是_20%__.(100%*6.8g/34g=20%)
5.欲配置质量分数为3%的过氧化氢100g需要过氧化氢的质量为3g
瓶内过氧化氢的质量分数为20%,假设需要瓶内的过氧化氢为xg,则0.2x=3=>x=15g
即需要瓶内过氧化氢15g,需要水的质量为100-15=85g1年前查看全部
- (2006•泉州)下列化学试剂瓶标签上的化学式书写正确的是( )
(2006•泉州)下列化学试剂瓶标签上的化学式书写正确的是( )
A.
B.
C.
D.
 WSK2091年前1
WSK2091年前1 -
 nadia921923 共回答了11个问题
nadia921923 共回答了11个问题 |采纳率81.8%解题思路:在化合物中,元素的化合价代数和为零.A、在氧化铜中,铜元素的化合价是+2,氧元素的化合价是-2,氧化铜的化学式是CuO.正确;
B、硫酸中,氢元素的化合价是+1,氧元素的化合价是-2,硫元素的化合价是+6,硫酸的化学式是H2SO4.错误;
C、碳酸钠中,钠元素的化合价是+1,氧元素的化合价是-2,碳元素的化合价是+4,碳酸钠的化学式是Na2CO3.错误;
D、锌属于金属单质,化学式是Zn.错误.
故选A.点评:
本题考点: 化学式的书写及意义.
考点点评: 解答本题要理解在单质中,元素化合价为零,在化合物中,各种元素的化合价不为零,但是代数和为零.1年前查看全部
- 现有失去标签的A、B二瓶无色溶液,它们有如下性质:
现有失去标签的A、B二瓶无色溶液,它们有如下性质:
则:(1)A可能是______或______,为进一步确定A中的溶质,可向A溶液中滴加______溶试剂 与石蕊试液作用 与稀H 2 SO 4 作用 与Ca(OH) 2 溶液作用 与Fe作用 A 变红 不反应 放热、无浑浊 产生气体 B 变蓝 产生气体 产生白色沉淀 不反应
液,观察是否有白色沉淀,若有白色沉淀,则原A溶液中含有的微粒是______.
(2)经分析知B物质中含有钠元素,则B溶液中溶质的化学式为______. 1119661年前1
1119661年前1 -
 liuhang1971 共回答了21个问题
liuhang1971 共回答了21个问题 |采纳率95.2%(1)根据表中物质的性质,可以看出A能使石蕊变红,与硫酸不反应,与碱反应,与金属反应生成气体,则A为酸,且是盐酸或硝酸,因确定A中溶质观察到白色沉淀,则加硝酸银即可,A中微粒有离子和分子,
故答案为:HCl;HNO 3 ;AgNO 3 ;H + 、Cl - 、H 2 O.
(2)B能使石蕊变蓝,B的溶液显碱性,与酸反应产生气体,与氢氧化钙反应生成沉淀,可知B中含碳酸根或碳酸氢根,又知物质中含有钠元素,则B为Na 2 CO 3 或NaHCO 3 .
故答案为:Na 2 CO 3 或NaHCO 3 .1年前查看全部
- 科学实验课上,老师拿出两瓶无标签的溶液,一瓶是氢氧化钠溶液,一瓶是碳酸钠溶液,要求学生鉴别,并帮助贴上标签.
科学实验课上,老师拿出两瓶无标签的溶液,一瓶是氢氧化钠溶液,一瓶是碳酸钠溶液,要求学生鉴别,并帮助贴上标签.
(1)***同学认为氢氧化钠溶液是碱溶液,碳酸钠溶液是盐溶液,所以用酚酞试液鉴别.你认为***同学想法正确吗?______并简述理由______
(2)苏田同学各取少量未知溶液于两支试管中,分别滴入稀盐酸,若有气体产生的为碳酸钠溶液.她想进一步测知碳酸钠溶液的质量分数,取出20克碳酸钠溶液于烧杯中,往烧杯中滴加10%的稀盐酸至没有气泡产生,共用去稀盐酸73克.求碳酸钠溶液的质量分数. ccsk0071年前1
ccsk0071年前1 -
 疯着的智慧 共回答了16个问题
疯着的智慧 共回答了16个问题 |采纳率93.8%解题思路:(1)碳酸钠溶液与氢氧化钠溶液都能使酚酞变红色;
(2)根据盐酸的质量求出碳酸钠的质量,进而求出碳酸钠溶液的质量分数.(1)碳酸钠溶液和氢氧化钠溶液都呈碱性,都能使酚酞试液变红色,不能用酚酞试液鉴别;
(2)设73g10%的盐酸完全反应消耗碳酸钠的质量是x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
10673
x73g×10%
[106/x]=[73/73g×10%]
x=10.6g
碳酸钠溶液的质量分数=[10.6g/20g]×100%=53%
答:碳酸钠溶液的质量分数为53%
故答案为:(1)碳酸钠溶液和氢氧化钠溶液都呈碱性,都能使酚酞试液变红色;
(2)设73g10%的盐酸完全反应消耗碳酸钠的质量是x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
10673
x73g×10%
[106/x]=[73/73g×10%]
x=10.6g
碳酸钠溶液的质量分数=[10.6g/20g]×100%=53%
答:碳酸钠溶液的质量分数为53%点评:
本题考点: 酸、碱、盐的鉴别;有关溶质质量分数的简单计算;根据化学反应方程式的计算.
考点点评: 本题考查了碳酸钠和氢氧化钠溶液的性质,溶质质量分数的计算;要理解和熟记碳酸钠和氢氧化钠的性质和溶质质量分数的计算方法.1年前查看全部
- 平方差的题平方差公式题[ 标签:平方差,平方差 公式,公式 ] (3x-2y)(9x^2+4y^2)(-2y-3x)=
平方差的题
平方差公式题
[ 标签:平方差,平方差 公式,公式 ]
(3x-2y)(9x^2+4y^2)(-2y-3x)=
(2+1)(2^2+1)(2^4+1)(2^8+1)…(2^64+1)=?
100^2-99^2+98^2-97^2+96^2-95^2+…+2^2-1^2=?
1 1 1 1 1
(1- — )(1- — )(1- — )…(1- — )(1- — )
2^2 3^2 4^2 9^2 10^2
1减 2的平方分之一后面的都一样 gayooo1年前2
gayooo1年前2 -
 比比波拨 共回答了22个问题
比比波拨 共回答了22个问题 |采纳率86.4%1.(3x-2y)(9x^2+4y^2)(-2y-3x)
= (3x-2y)[-(2y+3x)]^2
(9x^2+4y^2)
=(9x^2-4y^2)(9x^2+4y^2)
=81x^4-16y^4
2.(2+1)(2^2+1)(2^4+1)(2^8+1)…(2^64+1)
=(2^2-1)(2^2+1)(2^4+1)(2^8+1)…(2^64+1)
=(2^4-1)(2^4+1)(2^8+1)…(2^64+1)
=(2^64-1)(2^64+1)
=2^128-1
3.100^2-99^2+98^2-97^2+96^2-95^2+…+2^2-1^2
=(100+99)(100-99)+(98+97)(98-97)+(96+95)(96-95)...+(2+1)(2-1)=100+99+98+97.+2+1
=101*50
=5050
4.1 1 1 1 1
(1- — )(1- — )(1- — )…(1- — )(1- — )
2^2 3^2 4^2 9^2 10^2
=(1-1/2)^2(1-1/3)^2(1-1/4)^2.(1-1/9)^2(1-1/10)^2
=(1+1/2)(1-1/2)(1+1/3)(1-1/3).(1+1/9)(1-1/9)(1+1/10)(1-1/10)
=3/2 * 1/2 * 4/3 * 2/3...11/10 * 9/10
=1/2 * 11/10
=11/201年前查看全部
- (2008•常德)某化学实验室有一瓶黑色固体粉末X(X是纯净物),因试剂瓶标签破损无法确定其成分.为此小军进行了以下实验
(2008•常德)某化学实验室有一瓶黑色固体粉末X(X是纯净物),因试剂瓶标签破损无法确定其成分.为此小军进行了以下实验,请你参与他的探究:
(一)探究X的成分
【猜想与假设】物质X可能是______;
【实验设计与实施】取两份等量的X样品,进行实验一、实验二: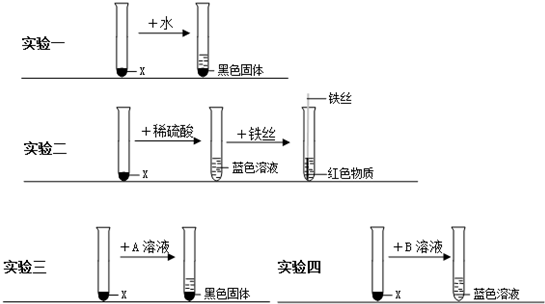
【实验分析与结论】
①从“实验一”小军得出X的物理性质是:______;
②从“实验二”小军推断出X的化学式是______;
③“实验二”中向蓝色溶液插入铁丝发生反应的化学方程式是______.
(二)探究X与稀硫酸的反应
(1)稀硫酸中含有H2O、H+、SO42-等粒子,其中属于分子的有______;属于离子的有______;
(2)小军分析“实验一、二”后认为:可能是稀硫酸中的H+或SO42-使X溶解.
为确定稀硫酸中何种粒子使X溶解,他继续设计了实验三、实验四进行探究:
“实验三”中的A可能是______(填化学式,下同),“实验四”中的B可能是______;
(3)小军通过上述实验证明:稀硫酸中的______(填离子符号)才能使X溶解;
(4)某同学建议小军:要确定稀硫酸中何种粒子使X溶解,只需进行实验一、二、三即可.你是否同意该同学的观点?______(填“同意”或“不同意”) handgun1年前1
handgun1年前1 -
 zfj25 共回答了18个问题
zfj25 共回答了18个问题 |采纳率88.9%(一)【猜想与假设】初中化学实验室常见的黑色粉末有CuO、MnO2、Fe3O4、铁粉、炭粉等,根据以实验知,能和硫酸等物质反应,可猜想为氧化铜,故答案为:CuO【实验分析与结论】①从“实验一”可知,X不溶于水,故答案...1年前查看全部
- 从细口瓶倾倒液体时,为什么要瓶塞倒放在桌上,标签向着手心,瓶口紧靠着试管口?
 战战9111年前9
战战9111年前9 -
 MYMONTAGUT 共回答了13个问题
MYMONTAGUT 共回答了13个问题 |采纳率76.9%瓶塞倒放为了防止桌面上的异物遗留在瓶塞塞子上污染试剂
标签向掌心:由于试剂可能有腐蚀性,防止腐蚀标签
瓶口紧靠:更易倾倒试剂,试剂沿管壁流下,不易溅出试管1年前查看全部
- (1)矿泉水中往往含多种有益于人体健康的成分.如图是某品牌矿泉水中标签上的部分内容,则这瓶矿泉水中含Ca2+的物质的量≥
(1)矿泉水中往往含多种有益于人体健康的成分.如图是某品牌矿泉水中标签上的部分内容,则这瓶矿泉水中含Ca2+的物质的量≥______mol.
(2)现代生活离不开铝,工业上以铝土矿为原料生产铝.现将一定量某铝土矿样品(主要成分Al2O3)溶于过量稀盐酸并制成500mL溶液.取100mL该溶液,测得其中含有H+、Cl-、Mg2+、Al3+、Fe3+五种离子(不考虑其它离子).已知部分离子的物质的量浓度为:净含量:500mL 饮用水矿物质成分(mg.L-1) 钙Ca ≥4.0 镁Mg ≥1.0 钠Na ≥3.0
c(H+)=0.02mol•L-1c(Mg2+)=0.01mol•L-1
c(Fe3+)=0.02mol•L-1c(Cl-)=0.52mol•L-1
①溶液中Al3+物质的量浓度为______mol•L-1
②则该铝土矿样品中Al2O3的质量为______g(精确至0.01g). fangfang9281年前1
fangfang9281年前1 -
 blue文 共回答了18个问题
blue文 共回答了18个问题 |采纳率100%解题思路:(1)计算该瓶矿泉水中Ca2+的质量,根据n=[m/M]计算这瓶矿泉水中含Ca2+的物质的量;
(2)①根据溶液中电荷守恒可知,c(H+)+2c(Mg2+)+3c(Fe3+)+3c(Al3+)=c(Cl-),据此计算;②根据n=cV计算n(Al3+),再根据Al原子守恒计算n(Al2O3),根据m=nM计算Al2O3的质量.(1)由表中数据可知,Ca2+的浓度≥4mg/L,故500mL该矿泉水中m(Ca2+)≥0.5L×4mg/L=2mg,故该瓶矿泉水中含Ca2+的物质的量≥
2×10−3g
40g/mol=5×10-5mol,
故答案为:5×10-5;
(2)①根据溶液中电荷守恒可知,c(H+)+2c(Mg2+)+3c(Fe3+)+3c(Al3+)=c(Cl-),
故0.02mol/L+2×0.01mol/L+3×0.02mol/L+3c(Al3+)=0.52mol/L,
解得c(Al3+)=0.14mol/L,
故答案为:0.14;
②500mL溶液中n(Al3+)=0.14mol/L×0.5L=0.07mol,
据Al原子守恒可知n(Al2O3)=[1/2]n(Al3+)=[1/2]×0.07mol=0.035mol,
故Al2O3的质量为0.035mol×102g/mol=3.57g,
故答案为:3.57.点评:
本题考点: 物质的量浓度的相关计算.
考点点评: 本题考查物质的量浓度的有关计算,难度中等,注意利用电荷守恒、原子守恒进行的计算.1年前查看全部
- 实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液,为确定甲乙两瓶溶液的成分
实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液,为确定甲乙两瓶溶液的成分
及其物质的量浓度,现操作如下:
①量取25.00mL甲溶液,向其中缓慢滴加乙溶液15.00mL,共收集到二氧化碳224mL.
②另取15.00mL乙溶液,向其中缓慢滴加甲溶液25.00mL,共收集到二氧化碳112mL.
求甲的物质的量浓度.
我现在知道了甲是HCl,乙是Na2CO3.物质的量浓度怎么算?关键就是我现在没法判断哪个过量.
这是我在弄白猫杯的题目,要是参加过,分享下经验吧~ 噼里啪啦1年前2
噼里啪啦1年前2 -
 宾沁能 共回答了17个问题
宾沁能 共回答了17个问题 |采纳率94.1%设盐酸溶液中含氯化氢的物质的量为X
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
2 22.4
X 0.224ml
X=0.02mol
盐酸的物质的量浓度=0.02mol/0.025L=0.8mol/L
设碳酸氢钠反应消耗氯化氢的物质的量为Y,碳酸钠的物质的量为Z
NaHCO3 + HCl =NaCl + H2O + CO2↑
1 22.4
Y 0.112ml
Y=0.005mol
则碳酸钠转化为碳酸氢钠消耗氯化氢的物质的量=0.02mol-0.005mol=0.015mol
Na2CO3 + HCl = NaCl +NaHCO3
1 1
Z 0.015mol
Z=0.015mol
碳酸钠溶液的物质的量浓度=0.015mol/0.015L=1mol/L
分析:根据①和② 可知甲为盐酸,乙为碳酸钠,
当把碳酸钠滴入盐酸时,开始盐酸过量,碳酸钠完全反应,直接发生如下反应:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑,随着碳酸钠溶液的滴入,碳酸钠使盐酸完全反应.
当把盐酸滴入碳酸钠时,开始碳酸钠过量,盐酸不足先发生
Na2CO3 + HCl = NaCl +NaHCO3 的反应,
当碳酸钠完全转化为碳酸氢钠后,再滴加盐酸,盐酸又与碳酸氢钠反应,根据②反应生成二氧化碳气体体积小于①反应的体积,说明②中再滴入的盐酸没有使生成碳酸氢钠完全反应.最终盐酸的量不足.反应的化学方程式为:
NaHCO3 + HCl =NaCl + H2O + CO2↑1年前查看全部
- 现有两只没有标签、外观相同的试剂瓶,内盛500ml无色澄清的液体
现有两只没有标签、外观相同的试剂瓶,内盛500ml无色澄清的液体
一瓶是饱和NaCi,一瓶是H20.写出五种鉴别的方法
我只想出来三种:尝一尝、滴入AgNo3、电解
各位帮下忙,还有什么方法,非常感谢!
 不雅笔名1年前1
不雅笔名1年前1 -
 放大镜看世界 共回答了25个问题
放大镜看世界 共回答了25个问题 |采纳率96%还可以放冰箱里冷冻,饱和NaCi在零度不会结冰.
或者根据密度不同,分别放入同一物体,下沉深度较深的是水.
还可以加热蒸发,生成晶体的是氯化钠溶液1年前查看全部
- 实验室中有失去标签的固体和液体试剂各一瓶,小明同学分别取这两种试剂各少量,放入试管中混合,立即产生一种无色无味的气体
实验室中有失去标签的固体和液体试剂各一瓶,小明同学分别取这两种试剂各少量,放入试管中混合,立即产生一种无色无味的气体
(1)【提出问题】产生的气体为何种气体
(2)【猜想】小明猜想该气体可能是氢气,你认为还可能是(列举两种)______
(3)【设计实验方案】选择你猜想的其中一种气体,设计实验方案验证你的猜想,要求答出实验步骤,现象和结论.你猜想的气体 实验步骤 现象 结论  无厘头小贼1年前1
无厘头小贼1年前1 -
 开家我们自己的店 共回答了13个问题
开家我们自己的店 共回答了13个问题 |采纳率84.6%解题思路:首先根据题中信息“固体与液体”反应生成气体进行猜测生成的气体可能有氧气、二氧化碳和氢气.然后根据猜测的结果进行逐一解答以下题目.根据题中信息所生成的气体是通过固体与液体反应制得,回忆课本所学知识可知符合题意的有二氧化碳、氧气和氢气.根据第(2)问要小明猜想是氢气,故还可以猜想是二氧化碳和氧气;若猜想是氧气,则可将带火星的木条伸入集气瓶内,带火星的木条复燃.
若猜想是二氧化碳,则可用收集一集气瓶气体,将燃着的木条放在集气瓶内,观察到木条熄灭.
故答案为:
(2)氧气、二氧化碳;
(3)
你猜想的气体实验步骤现象结论
氧气 收集一集气瓶气体,将带火星的木条放在集气瓶内 木条复燃 是氧气点评:
本题考点: 缺失标签的药品成分的探究;常见气体的检验与除杂方法;实验室制取氧气的反应原理;二氧化碳的实验室制法.
考点点评: 回答开放性试题时,要结合所学知识,对答案进行大胆猜想,然后利用物质的性质等进行验证,从而得出正确答案.1年前查看全部
- 在4个洁净的罐头瓶上分别贴上写有1、2、3、4的标签,然后在4个瓶中各放入两张餐巾纸,并在餐巾纸上均匀的放上10粒种子,
在4个洁净的罐头瓶上分别贴上写有1、2、3、4的标签,然后在4个瓶中各放入两张餐巾纸,并在餐巾纸上均匀的放上10粒种子,然后按照下表中的处理方式操作,请分析回答问题:
(1)能够萌发的只有______号瓶内的种子.1号瓶 2号瓶 3号瓶 4号瓶 处理方式 拧紧瓶盖 洒入少量的清水,使餐巾纸湿润,然后拧紧瓶盖 倒入较多的清水,使种子淹没在清水中,拧紧瓶盖 洒入少量的清水,使餐巾纸湿润,然后拧紧瓶盖 置于室温环境中 置于室温环境中 置于室温环境中 放在低温处(如冰箱内)
(2)其他瓶内的种子不能萌发的原因分别是:
①______;
②______;
③______. 龙之派1年前1
龙之派1年前1 -
 yyyyyy_123 共回答了12个问题
yyyyyy_123 共回答了12个问题 |采纳率91.7%解题思路:本题重点考查影响种子萌发的外界条件:一定的水;适宜的温度;充足的空气和探究实验的步骤、变量等.(1)种子萌发的外界条件为充足的空气,适量的水分,适宜的温度.2号号瓶内的种子具备了种子萌发的外界条件,因此2号瓶内的种子萌发,1、3、4号不萌发.
(2)①、1号瓶子内的种子不能萌发的原因是缺少适量的水,种子不萌发.
②、3号瓶子内的种子不能萌发的原因是种子淹没在清水中,缺少充足的空气,种子不萌发.
③、4号瓶子内的种子不能萌发的原因是缺少适宜的温度,种子不萌发.
故答案为:
(1)2;
(2)
①、1号瓶缺少适量的水,种子不萌发;
②、3号瓶缺少充足的空气,种子不萌发;
③、4号瓶缺少适宜的温度,种子不萌发.点评:
本题考点: 探究种子萌发的条件.
考点点评: 解答的关键是熟知影响种子萌发的外界条件:一定的水;适宜的温度和有关探究实验的步骤等.1年前查看全部
- 初二科学实验题病人输液时用的生理盐水是一种溶质质量分数为0.9%的氯化钠溶液,下面是一瓶生理盐水的标签,请根据标签上给出
初二科学实验题
病人输液时用的生理盐水是一种溶质质量分数为0.9%的氯化钠溶液,下面是一瓶生理盐水的标签,请根据标签上给出的信息,回答下列问题.
标签:氯化钠注射液
【规格】495ml 内含氯化钠4.5g
【注意】如发现溶液有絮状物、瓶身细微破裂等均不可使用
【储存】密封保存
0.9%
该瓶生理盐水如果用溶质的质量分数为20%的氯化钠溶液(密度为1.07g/cm立方)来配制的话,问:需20%的氯化钠溶液___克
急 zhangbo8004291年前1
zhangbo8004291年前1 -
 南京2001 共回答了21个问题
南京2001 共回答了21个问题 |采纳率85.7%4.5===M*20%
M=22.5g1年前查看全部
- 一瓶工业酒精和一瓶食盐水都失去了标签,用物理方法和化学方法各一种分别鉴别它们.
 hebao1721年前1
hebao1721年前1 -
 yylong2 共回答了24个问题
yylong2 共回答了24个问题 |采纳率91.7%解题思路:①工业酒精同乙醇一样,都具有特殊气味,而食盐水没有气味;
②工业酒精可燃,生成二氧化碳气体,食盐水不可燃;食盐水的主要成分是氯化钠,可与硝酸银反应生成不溶于硝酸的白色沉淀氯化银,而工业酒精无明显变化.物理方法:闻气味.工业酒精同乙醇一样,都具有特殊气味;食盐水没有气味;
化学方法:(1)燃烧法.可燃,且生成了使澄清石灰水变浑浊的气体和无色液体的是工业酒精,不燃烧的是食盐水.
(2)加入硝酸银.若生成了白色且不溶于硝酸的沉淀的是食盐水,无明显变化是工业酒精.点评:
本题考点: 物质的鉴别、推断;化学性质与物理性质的差别及应用.
考点点评: 此题主要是考查学生的综合分析能力,不但要求学生具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.1年前查看全部
- 融合蛋白肽指纹图谱分析,该蛋白为带有his标签的多角体融合目的蛋白(his-多角体蛋白-目的蛋白).
融合蛋白肽指纹图谱分析,该蛋白为带有his标签的多角体融合目的蛋白(his-多角体蛋白-目的蛋白).
您说可以用多角体蛋白做个指纹,我现在手上有另一人做的多角体的二级质谱结果,即指纹图谱和肽段氨基酸序列,我的融合蛋白做二级质谱,但不知道结果拿到手后怎么处理得到目的蛋白的结果,您说的差减我不懂什么意思,具体指教.质谱公司是否可以继续帮我做啊!
质谱新手,有很多地方不懂,请您多指教, XXL_S1年前1
XXL_S1年前1 -
 桂花_涵 共回答了21个问题
桂花_涵 共回答了21个问题 |采纳率95.2%差减:你手上有2张指纹图谱,一张是有目的蛋白的,一张没有,2张图叠加,剔除共同拥有剩下来的就是目的蛋白的1年前查看全部
- 求助,英语翻译,在线等衣服上标签有下面内容,麻烦大家帮我翻译一下,着急!POLYESTER 85%COTTON/COTO
求助,英语翻译,在线等
衣服上标签有下面内容,麻烦大家帮我翻译一下,着急!
POLYESTER 85%
COTTON/COTON 15%
LINING/DOUBLURE-NYLON 100%
INTERMEDIAIRE-NYLON 100% ring88771年前2
ring88771年前2 -
 九月传说 共回答了19个问题
九月传说 共回答了19个问题 |采纳率84.2%聚酯85%
棉 15%
内层里面 尼龙100%
中间层 尼龙100%1年前查看全部
- (2007•辽宁)如图是某袋化肥标签的部分说明,下列有关说法错误的是( )
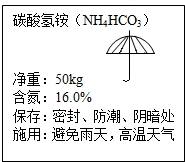 (2007•辽宁)如图是某袋化肥标签的部分说明,下列有关说法错误的是( )
(2007•辽宁)如图是某袋化肥标签的部分说明,下列有关说法错误的是( )
A.该化肥属于氮肥
B.该袋化肥的含氮量为50kg×16.0%
C.碳酸氢铵由四种元素组成
D.该化肥属于复合肥料 hupo121年前1
hupo121年前1 -
 ANNY_LEE 共回答了17个问题
ANNY_LEE 共回答了17个问题 |采纳率82.4%解题思路:含有氮元素的化肥属于氮肥;根据质量和质量分数可以求出某种元素的质量;根据物质的化学式可以判断物质的元素组成.A、碳酸氢铵中含有氮元素,属于氮肥.正确;
B、该袋化肥的含氮量为:50kg×16.0%=8kg.正确;
C、碳酸氢铵由氮元素、氢元素、氧元素和碳元素等四种元素组成.正确;
D、碳酸氢铵中只含有一种营养元素,不属于复合肥.错误.
故选D.点评:
本题考点: 常见化肥的种类和作用;物质的元素组成;混合物中某元素的质量计算.
考点点评: 解答本题要掌握化肥的分类方法和相关方面方面的计算方法,只有这样才能对问题做出正确的判断.1年前查看全部
- 化学科代表小聪与小明同学帮助实验老师整理化学药品室时,发现分别放在两个试剂瓶中的两片用砂纸磨得光亮的银白色金属,未贴标签
化学科代表小聪与小明同学帮助实验老师整理化学药品室时,发现分别放在两个试剂瓶中的两片用砂纸磨得光亮的银白色金属,未贴标签.到底它们是哪种金属?两位同学首先对这两种金属X和Y的金属活动性顺序进行实验探究.
(1)进行猜想:
①科代表小聪猜想:活动性X大于Y.
②小明同学猜想:活动性Y大于X.
(2)设计实验方案、进行实验、获得知识.完成如下实验报告,并回答后续有关问题.
(3)上述实验之前,实验老师只知道X、Y是银铁中的各一种,则根据实验结果说明Y就是______.实验室急需一定量的Y粉末,科代表小聪认为可用现有的X金属粉末和Y的盐溶液、蒸馏水等药品,配以必要的仪器来制得急需的Y粉末,原因是(用反应的化学方程式表示)______.①实验步骤 ②实验现象 ③结论
______金属Y表面无明显变化,金属X的表面有气泡冒出.
将燃着的木条放在装金属X的试管口,气体燃烧
______
科代表小聪的猜想:______
(“正确”或“正确”)
(4)实验老师经实验分析得知制得的Y粉末中含有未反应完的X粉末,若用化学方法将杂质X粉末除去,两个同学经讨论、交流一致认为可选用的除杂质试剂是______. 文兰梦境1年前1
文兰梦境1年前1 -
 CD公主1 共回答了19个问题
CD公主1 共回答了19个问题 |采纳率89.5%解题思路:金属的活动性顺序的应用主要表现在两个方面:一是只有排在氢前面的金属才能与酸发生置换反应,生成盐和氢气;二是只有排在前面的金属才能把后面的金属从它的盐溶液中置换出来;化学方程式的书写主要做好以下几个方面:反应物、生成物、反应条件、化学式的书写、配平、沉淀气体的标注等.(2)根据已完成的实验报告可以看出,验证X与Y的活动性采用的是加酸的方法,可以加入稀盐酸或稀硫酸,X表面冒泡,说明X>H,Y表面无变化,说明H>Y,所以本题答案为:
实验步骤 实验现象 结论
将金属X、Y分别放入试管中,再分别加入稀盐或稀硫酸酸 金属的活动性为X>Y
不正确(3)根据实验现象可知,X>H>Y,而铁>氢>银,所以Y就是银,铁能将银从其盐溶液中置换出来,所以本题答案为:银或Ag,2AgNO3+Fe═2Ag+Fe(NO3)2;
(4)因为铁>氢>银,铁能与酸反应而银不能,所以除去银粉中含有铁粉,可以用酸溶液.
故答案为:(2)
实验步骤 实验现象 结论
将金属X、Y分别放入试管中,再分别加入稀盐或稀硫酸酸 金属的活动性为X>Y
不正确(3)银;2AgNO3+Fe═2Ag+Fe(NO3)2;
(4)盐酸(或稀硫酸).点评:
本题考点: 金属活动性的探究;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.1年前查看全部
- 化学实验室中药品应该按要求存放在容器中,并贴上标签,标签中通常包含物质的名称和化学式.如图,请认真观察图,然后回答下列问
化学实验室中药品应该按要求存放在容器中,并贴上标签,标签中通常包含物质的名称和化学式.如图,请认真观察图,然后回答下列问题:
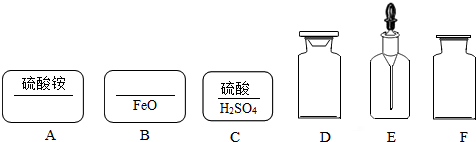
(1)请在A标签填上化学式;在B标签填上物质名称.
(2)D仪器的名称是______;C标签应该贴在______仪器上(填编号)
(3)标签所示三种物质中属于氧化物的是______.
(4)F仪器可以用来存放SO2气体,存放时该仪器应该______放置桌面上(填“正放”或“倒放”);其中化学式SO2中数字“2”的含义为______. 欣子221年前1
欣子221年前1 -
 和地方时嘎 共回答了19个问题
和地方时嘎 共回答了19个问题 |采纳率89.5%解题思路:(1)硫酸铵中铵根显+1价,硫酸根显-2价,写出其化学式即可;化合物化学式的读法:一般是从右向左读,读作“某化某”,有时还要把元素符号右下角的数字读出来,如SO2、P2O5等,据此进行分析解答.
(2)根据常见的化学仪器的名称进行分析解答;硫酸是液体药品,据此进行分析解答..
(3)氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
(4)根据SO2气体的密度比空气大、标在化学式中元素右下角的数字表示一个分子中所含原子的数目,进行分析解答.(1)硫酸铵中铵根显+1价,硫酸根显-2价,其化学式为(NH4)2SO4.FeO中铁元素显+2价,从右向左读,读作氧化亚铁.(2)D仪器的名称是集气瓶;硫酸是液体药品,应盛放在细口瓶或滴瓶中,故C标签应该贴在E上.(3)标...
点评:
本题考点: 化学式的书写及意义;常用仪器的名称和选用;从组成上识别氧化物;化学符号及其周围数字的意义.
考点点评: 本题难度不大,掌握化合物化学式的书写方法与读法、氧化物的特征、常见仪器的名称与用途等是正确解答本题的关键.1年前查看全部
- 通过学习,同学们知道了液体压强的特点。在此基础上,老师提出了这样的问题:有两只杯子,分别盛有清水和盐水,但没有标签,你能
通过学习,同学们知道了液体压强的特点。在此基础上,老师提出了这样的问题:有两只杯子,分别盛有清水和盐水,但没有标签,你能否用压强计将它们区别开?
(1)当压强计的金属盒在空气中时,U形管两边的液面应当相平,而小明同学却观察到如图(a)所示的情景。出现这种情况的原因是:U形管左支管液面上方的气压______大气压(填“大于”、“小于”或“等于”);调节的方法是:________
A.将此时右边支管中高出的液体倒出
B.取下软管重新安装
(2)小明再作图(b)所示的检查。当用手指按压(不论轻压还是重压)橡皮膜时,发现U形管两边液柱的高度几乎不变化。出现这种情况的原因是:__________________________。
(3)压强计调节正常后,小明将金属盒先后浸入到两杯液体中,如图(c)和(d)所示。他发现图(d)中U形管两边的液柱高度差较大,于是认为图(d)杯子中盛的是盐水。
①你认为,小明的结论是 _______(填“可靠的”或“不可靠的”);②简要说明理由:_____________________ 。



 暮hh朝生1年前1
暮hh朝生1年前1 -
 930753 共回答了21个问题
930753 共回答了21个问题 |采纳率90.5%(1)大于; B;
(2)压强计的气密性不好;或压强计金属盒(或“软管”)漏气;或U形管与软管连接不好。
(3)①不可靠的; ②金属盒(或“橡皮膜”)在两种液体中的深度不同;或没有控制金属盒(或“橡皮膜”)在两种液体(或“在液体”)中的深度(或“深度相同”)。1年前查看全部
- (2003•辽宁)某同学发现他菜园中的蔬菜生长缓慢,便使用了一种氮肥,下图是氮肥包装标签的部分文字.这种氮肥的相对分子质
(2003•辽宁)某同学发现他菜园中的蔬菜生长缓慢,便使用了一种氮肥,下图是氮肥包装标签的部分文字.这种氮肥的相对分子质量为______,其纯度(即化肥硝酸铵的质量分数)是______.
______显示解析试题篮.硝酸铵
(NH4NO3)
净重:50kg
含氮量:34.3%
×××工业公司 xuezhixi0303171年前1
xuezhixi0303171年前1 -
 cngy110 共回答了23个问题
cngy110 共回答了23个问题 |采纳率95.7%解题思路:(1)根据标签所示硝酸铵的化学式可得,其相对分子质量为:(氮的相对原子质量×氮原子个数)+(氢的相对原子质量×氢原子个数)+(氧的相对原子质量×氧原子个数);
(2)化肥的含氮量÷硝酸铵中氮元素的质量分数,就是化肥中硝酸铵的质量分数.(1)根据标签所示硝酸铵的化学式可得,其相对分子质量=14×2+1×4+16×3=80;
(2)化肥中硝酸铵的质量分数=34.3%÷[14×2/80]×100%=98%.
故答案为:(1)80;(2)98%.点评:
本题考点: 标签上标示的物质成分及其含量;相对分子质量的概念及其计算.
考点点评: 本题主要考查学生运用化学式,计算物质的相对分子质量和元素的质量分数的能力.注意元素的质量分数公式的格式.1年前查看全部
- 急...数学高手请进1.一种圆柱形罐头的底面直径是20厘米,高50厘米,给500个这样的罐头贴标签纸,需要多少米长的纸?
急...数学高手请进
1.一种圆柱形罐头的底面直径是20厘米,高50厘米,给500个这样的罐头贴标签纸,需要多少米长的纸?这些标签纸的面积有多少平方米?
2.图书馆里故事书的本数比科技书多30本,当故事书借出3/7,科技书借出2/5时。余下的科技书和故事书本数一样多。原有故事书、科技书各多少本?(需要用比例的基本性质来解)
以上的题目请说明为什么要这样做。 zzh869221年前2
zzh869221年前2 -
 jianzhuxin 共回答了23个问题
jianzhuxin 共回答了23个问题 |采纳率87%1.标签怎么贴,有多大的标签没有说明,如果是包住侧面的话,就是底面的周长x高x500/10000=10*3.14=31.4平方米
长度是500x3.14x20/100=15.7米
2.假设科技书有x本,则故事书为x+30本,依题意得:
(1-3/7)*(x+30)=(1-2/5)x
得到x=600
所以科技书有600本,故事书为630本1年前查看全部
- 实验室里有两卷钢丝,甲卷钢丝标签注明直径是0.9毫米;乙卷钢丝比这卷更细,但没有标签.如果没
实验室里有两卷钢丝,甲卷钢丝标签注明直径是0.9毫米;乙卷钢丝比这卷更细,但没有标签.如果没
实验室里有两卷钢丝,甲卷钢丝标签注明直径是0.9毫米;乙卷钢丝比这卷更细,但没有标签.如果没有刻度尺,请你利用简易的物品,设计一下方案测出乙卷钢丝的直径. limengxuan1年前3
limengxuan1年前3 -
 江作青罗带 共回答了14个问题
江作青罗带 共回答了14个问题 |采纳率92.9%1、截取两种钢丝相同的长度(最好长些可减小误差):质量甲、质量乙.
2、因为质量 = 密度 * 体积,体积 = 横截面 * 长度,
所以:质量 = 密度 * 横截面 * 长度
3、又因为:甲乙密度,长度都相等,所以横截面比等于质量比:
横截面甲 :横截面乙 = 质量甲 :质量乙
4、又因为横截面比等于直径比的平方:
横截面甲 :横截面乙 = 直径甲2:直径乙2
5、 所以开方后即可得甲乙的直径比,又知道了甲的直径,当然就可以
算出乙的直径大小了.1年前查看全部
- 某种矿泉水的标签上注明,每升水中含:Na:45.02毫克中的这里的钠指的是什么?元素还是单质?
 奥里工艺1年前1
奥里工艺1年前1 -
 卡布JI诺 共回答了14个问题
卡布JI诺 共回答了14个问题 |采纳率78.6%钠元素,因为单质状态的钠元素是非常活泼的金属,在空气中也会被氧化的.
更不可能在水里存在.1年前查看全部
- 溶液瓶上的标签应包括哪些内容?最好是教材上有的
 mazei27221年前2
mazei27221年前2 -
 anthony165 共回答了22个问题
anthony165 共回答了22个问题 |采纳率86.4%试剂的中文名称、试剂的化学式、试剂的配制日期1年前查看全部
- 今有四瓶失去标签的无色溶液,分别是Na2CO3、NaNO3、NaCl、Na2SiO3,请设计一个实验方案把他们鉴别出来.
今有四瓶失去标签的无色溶液,分别是Na2CO3、NaNO3、NaCl、Na2SiO3,请设计一个实验方案把他们鉴别出来.首先由小组间进行可行性方案设计、讨论,然后再做试验.
 ekindling1年前2
ekindling1年前2 -
 gongchaozj 共回答了14个问题
gongchaozj 共回答了14个问题 |采纳率92.9%1.分别取样,加入盐酸溶液,将会有一种溶液产生气体,则此溶液是Na2CO3,反应方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O;另有一种溶液将产生凝胶状沉淀,则此溶液是Na2SiO3,反应方程式为Na2SiO3+2HCl=2NaCl+H2SiO3;另两个溶液没有现象
2.取第一步中无现象的两种溶液,分别滴加硝酸银,将有一种产生沉淀,是NaCl,反应方程式为AgNO3+NaCl=AgCl↓+NaNO3;另一种无现象,是NaNO31年前查看全部
- 右图为某市售盐酸试剂瓶标签上的部分数据.通过计算回答:(1)求该浓盐酸的物质的量浓度.
右图为某市售盐酸试剂瓶标签上的部分数据.通过计算回答:(1)求该浓盐酸的物质的量浓度.

盐酸的物质的量浓度为c=[1000*0.365*11.8g/cm3]/36.5g/mol 分母上不用换算成dm3吗? 末班车没我的位置1年前1
末班车没我的位置1年前1 -
 grace916 共回答了17个问题
grace916 共回答了17个问题 |采纳率94.1%不用,密度的单位是:g/cm3,1年前查看全部
- 计算化学的题以下是我省生产的某种加钙食盐包装标签上的部分文字,请仔细阅读回答配料表:NaCI 食用caco3 碘酸钾净含
计算化学的题
以下是我省生产的某种加钙食盐包装标签上的部分文字,请仔细阅读回答
配料表:NaCI 食用caco3 碘酸钾
净含量:500g
成分表:NaCI ≥88%
钙(以Ca计) (0.5 - 1.3)%
碘 (以I计) (20 - 50)mg/kg
(1)包装标签上钙含量是指——(指单质钙、碳酸钙、钙元素中的一种)
(2)为了检验此盐中是否含有碳酸钙,在家庭厨房可以选用的物质是——
(3) 为了测定此盐中的钙元素的含量,取10g这种盐溶于水,加入足量的盐酸,生成0.132g二氧化碳,请计算此加钙食盐中钙元素的质量分数. v2bbd1年前1
v2bbd1年前1 -
 小蝴蝶于于 共回答了14个问题
小蝴蝶于于 共回答了14个问题 |采纳率85.7%1,钙元素.
2,醋酸.
3,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 0.132g
列比例,解得
X=0.3g
因为碳酸钙中钙元素的质量分数为40%
所以钙元素的质量为:0.3*40%=0.12克
此加钙食盐中钙元素的质量分数=0.12克/10克=1.2%1年前查看全部
大家在问
- 1y=x²/(2x+1)²求导(要步骤)
- 2怎样读寓言故事
- 3friend wanted作文三十词
- 4古代的文人很有责任感,他们始终奉行孟子说过的一句话是什么?
- 5急用一篇 网络利与弊的英语作文 文章要 深刻 生动点的.
- 6nsql="select * from gonggao where passed=1 order by id desc
- 7We were surprised that the little girl could draw so well=——
- 8心情糟透了, 用英语怎么说
- 9已知两个正方形的周长之和等于48cm 它们的面积之差为72平方厘米 求这两个正方形的边长
- 10—It's dark (黑的) n
- 11中学生提高自身生存能力、竞争能力和自我发展能力的基础是 A.良好的习惯 B.优良的意志品质 C.高雅的生活情趣 D.学会
- 12红红的太阳像()圆圆的月亮像()
- 13求一份抄作业的保证书,给同学的,要在班上念的那种.
- 14培优小学六年级二班45个同学和一名老师去春游,来到公园门口准备买票,他们怎样买票最划算?每人10元20人(含20人)九折
- 15进入未知用英语怎么说?



