NaCO3与NO、NO2的反应式是怎样的?
 calmch2022-10-04 11:39:541条回答
calmch2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 美人鱼亲亲 共回答了24个问题
美人鱼亲亲 共回答了24个问题 |采纳率95.8%- 水溶液中反应
Na2CO3+NO2+NO=2NaNO2+CO2
Na2CO3+2NO2=NaNO2+NaNO3+CO2 - 1年前
相关推荐
- 光合作用的反应式补充完整:
 我来自尘世1年前0
我来自尘世1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 电解池如何判断正负,与原电池的区别 ,如何写反应式
 bx23971年前1
bx23971年前1 -
 jieli_72 共回答了16个问题
jieli_72 共回答了16个问题 |采纳率93.8%解析:
★原电池中,较活泼的一般是负极,较不活泼的一般是正极,但这里的活泼和不活泼是相对于电解质溶液而言的.比如:铁的金属性比铜活泼,但是如果电解溶液是浓硫酸的话,铁会钝化,这时候铜就是负极了.负极放电,通过外路流入正极.这里的“放电”是指电子流出,与电流的方向相反(这你肯定知道的吧,虽然很简单的原理,但是至关重要!).失电子发生氧化反应,得电子发生还原反应(这你也是很清楚的吧~)
★原电池的书写技巧:⑴先确定正负极
⑵若负极反应生成的阳离子与电解质溶液中的阴离子不共存,则电解质溶液中的阴离子应写入负极反应式.
这里氢氧燃料电池的反应式尤其重要.
若正极反应物是氧气,电解质溶液为中性或碱性,H2O必须写入正极的反应式中,O2生成OH-(吸氧腐蚀);若电解质溶液为酸性,则H+必须写入正极反应式中,O2生成H2O(析氢腐蚀).
★电解池的正负判断简单,与正极相连的为阳极,与负极相连的为阴极.
★电解池反应式书写技巧;这个很容易的,只要记得阴阳离子的放电顺序即可.
好累啊~~
这些都是我高考的法宝,我老师很关注电化学的,我也学的很用心的,所以高考考到这些我一点都不怕的.
看在我一个字一个字打出来的份上,把分给我吧!~~Т Т
-1年前查看全部
- 亚硝酸根和氢碘酸的反应式
 yicai07581年前1
yicai07581年前1 -
 mapleH 共回答了13个问题
mapleH 共回答了13个问题 |采纳率100%NO2—+ 2I― + 4H+ == 2NO + I2 + 2H2O
您好,很高兴为您解答,OutsiderL夕为您答疑解惑
如果本题有什么不明白可以追问,如果满意记得采纳,手机客户端右上角评价点满意即可.
如果有其他问题请采纳本题后另发点击向我求助,答题不易,请谅解,谢谢.
祝学习进步1年前查看全部
- 正极锌,负极铜硫酸铜原电池反应式,【注意是正极是锌】
 sonicjacky1年前1
sonicjacky1年前1 -
 海稻税 共回答了19个问题
海稻税 共回答了19个问题 |采纳率94.7%如果是原电池,肯定是错误1年前查看全部
- 铝为负级,铂网做正级,空气做氧化剂,海水做电解质溶液,正极反应式:总反应式:
 qiumao1年前1
qiumao1年前1 -
 alvinailey 共回答了22个问题
alvinailey 共回答了22个问题 |采纳率90.9%正极反应式:O2+2H2O+4e-=4OH-
负极反应式:Al-3e- +3OH-=Al(OH)3↓
总反应式:4Al+3O2+6H2O=4Al(OH)31年前查看全部
- 邻苯二甲酸氢钾也氢氧化钾的反应式
 啦啦歌舞1年前1
啦啦歌舞1年前1 -
 乌鸦少帅 共回答了24个问题
乌鸦少帅 共回答了24个问题 |采纳率87.5%解析:
O ― H
|
HC ― C ―C = O
/
HC O C ― C = O + KOH →
/ |
HC ― CH O ― K
O ― K
|
HC ― C ―C = O
/
HC O C ― C = O + H2O (环形中间的O表示大π键)
/ |
HC ― CH O ― K1年前查看全部
- 正负极反应式在Fecl3溶液中插入两根电极(铜和石墨),然后用导线连接请问负极和正极的反应式分别是什么那Cl呢?
 zsdydy1年前1
zsdydy1年前1 -
 ivan0905 共回答了16个问题
ivan0905 共回答了16个问题 |采纳率81.3%首先铜失电子变成铜离子证明这边是负极
Cu-2e-=Cu2+
就是说石墨是正极
2Fe3+ +2e- =2Fe2+1年前查看全部
- 1Cr2O7 2- +6Fe2+ + 14H+=2Cr3+ +6Fe3+ +7H2O 请分别列出反应式中氧化、还原反应,
1Cr2O7 2- +6Fe2+ + 14H+=2Cr3+ +6Fe3+ +7H2O 请分别列出反应式中氧化、还原反应,
1Cr2O7 2- +6Fe2+ + 14H+=2Cr3+ +6Fe3+ +7H2O
请分别列出反应式中氧化、还原反应, 几经风霜情自真1年前2
几经风霜情自真1年前2 -
 csjxx 共回答了22个问题
csjxx 共回答了22个问题 |采纳率86.4%楼上的有点小错,第一个应该是-e-.
写氧化、还原反应时先判断氧化剂、还原剂是什么.
对于Cr2O7 2- +6Fe2+ + 14H+=2Cr3+ +6Fe3+ +7H2O
Cr反应后由+6价转化为+3价,化合价下降,是氧化剂,发生还原反应;
Fe反应后由+2价转化为+3价,化合价上升,是还原剂,发生氧化反应.
所以氧化反应是:Fe2+ - e- == Fe3+
还原反应是:Cr2O7^2- + 6e- + 14H+ == 2Cr3+ + 7H2O1年前查看全部
- 硫酸钠溶液与氯化钡溶液反应:SO42-+Ba2+ = BaSO4 ↓ 这是它的离子反应式 我老师说是错的...
 拉一人1年前1
拉一人1年前1 -
 dgfertew 共回答了24个问题
dgfertew 共回答了24个问题 |采纳率87.5%如果你是初中生或者是高中生,那么这个离子方程式是没错的,是你们老师在找茬.
麻烦采纳,谢谢!1年前查看全部
- 氢化硫在空气中燃烧的完全反应式氢化硫与氢氧化硫(浓)的反应时,生成物中X的化学式
 己JA221年前2
己JA221年前2 -
 guest2000 共回答了20个问题
guest2000 共回答了20个问题 |采纳率90%2H2S+02=2H2O+S 氧气不足
2H2S+302=2H2O+2SO2 氧气充足
你说的那个X可能是S或者SO2
没有氢氧化硫
你是不是想说硫酸?1年前查看全部
- 由Mg、Al、NaOH溶液组成的原电池、其负极反应式为:Al - 3e- +4OH-====AlO2-+2H2O 相对于
由Mg、Al、NaOH溶液组成的原电池、其负极反应式为:Al - 3e- +4OH-====AlO2-+2H2O 相对于NaOH溶液而言、Al比Mg更活泼、铝为负极.
我想问”相对于NaOH溶液而言、Al比Mg更活泼“这是为什么啊、还有这个规律吗、详细是怎样的?
还有就是有碱参与的原电池中、我见好多都是负极生成碱而这个是AlO2-+2H2O、能类比吗? 西北风七八级1年前6
西北风七八级1年前6 -
 mandylucy 共回答了18个问题
mandylucy 共回答了18个问题 |采纳率100%因为铝具有两性,就是铝可以和酸或者碱反应,如果和碱反应的话就是生成偏铝酸根也就是你说的ALO2-铝是特殊的例子,这个要记的,这是两性定义 .两性元素:既有金属性又有非金属性,在周期表中金属元素与非金属元素交界处(阶梯线附近)的元素.
两性物质:既能跟酸反应,又能跟碱反应,如Al,Al2O3,
ZnO等(望丢分)下面是我去搜的两性物质,太多了,不愿打= =对了、、、你看下我的再结合下楼上的377680504他的也比较全面1年前查看全部
- (7分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
(7分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO 3 — +4H + +3e — →NO+2H 2 O KMnO 4 、Na 2 CO 3 、Cu 2 O、Fe 2 (SO 4 ) 3 四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出该氧化还原反应的离子方程式:________________________________。
(2)反应中硝酸体现的性质有_________、__________。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是________________mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: _______________________________________________________________________。 angelboy091年前1
angelboy091年前1 -
 Lic-ZKW 共回答了16个问题
Lic-ZKW 共回答了16个问题 |采纳率87.5%(1)14H + +2NO 3 — +3Cu 2 O = 6Cu 2+ +2NO↑+7H 2 O
(2)酸性 氧化性
(3)0.6mol
(4)使用了较浓的硝酸,产物中有部分二氧化氮生成
(注原试题下载后无题文部分)
考查氧化还原反应的基本知识,重点考查浓稀硝酸在氧化还原反应中的应用。
(1)还原剂只有Cu 2 O,14H + +2NO 3 — +3Cu 2 O = 6Cu 2+ +2NO↑+7H 2 O
(2)硝酸根离子部分变价,显氧化性,不有部分化合价不变,显酸性。
(3)每生成1molNO转移3mol电子,生成0.2mol气体转移0.6mol电子。
(4)使用了较浓的硝酸,产物中有部分二氧化氮生成1年前查看全部
- 电解硫酸铜溶液电极阴、阳极的反应式
 李文吉1年前1
李文吉1年前1 -
 七色板 共回答了11个问题
七色板 共回答了11个问题 |采纳率100%如果是惰性电极
阴极:2Cu2+ + 4e- == 2Cu
阳极:2H2O - 4e- == 4H+ + O2(溶液呈酸性,最好不要写氢氧根)
总方程式:2Cu2+ + 2H2O =通电= 2Cu + O2 + 4H+
或 2CuSO4 + 2H2O =通电= 2Cu + O2 + 2H2SO41年前查看全部
- (2008•枣庄一模)如图是一个化学反应过程的示意图.已知甲池的总反应式为:
 (2008•枣庄一模)如图是一个化学反应过程的示意图.已知甲池的总反应式为:
(2008•枣庄一模)如图是一个化学反应过程的示意图.已知甲池的总反应式为:
2CH3OH+3O2+4KOH=2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称.甲电池是______装置,乙池是______装置.
(2)请回答下列电极的名称:通入CH3OH的电极名称是______,B(石墨)电极的名称是______.
(3)写出电极反应式:通入O2的电极的电极反应式是______.A(Fe)电极的电极反应式为______,
(4)乙池中反应的化学方程式为4AgNO3+2H2O
4Ag+O2↑+4HNO3通电 .4AgNO3+2H2O.
4Ag+O2↑+4HNO3通电 .
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2______mL(标准状况下) yqlcbs1年前1
yqlcbs1年前1 -
 潇洒一行 共回答了22个问题
潇洒一行 共回答了22个问题 |采纳率100%解题思路:(1)根据方程式及燃料电池的特点判断甲装置;根据甲装置判断乙装置;
(2)根据反应方程式得失电子判断电极名称;根据外加电源名称确定乙装置石墨电极名称;
(3)先判断原电池、电解池的电极名称,再写出相应的电极反应式;
(4)根据离子放电顺序写出相应的电解反应方程式;
(5)先根据得失电子数相等找出银与氧气的关系式,然后计算.(1)根据反应方程式知,甲装置是一个燃料电池,所以甲是把化学能转变为电能的装置,是原电池;乙有外加电源,所以是电解池.
故答案为:原电池(化学能转变为电能);电解池(电能转变为化学能)
(2)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极是阳极.
故答案为:负极;阳极
(3)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 得电子和水反应生成氢氧根离子,发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极是阳极该电极上发生氧化反应;铁电极是阴极,该电极上银离子得电子发生还原反应.
故答案为:O2+2H2O+4e-=4OH-4Ag++4e-=4Ag
(4)乙池中离子放电顺序为:阳离子 Ag+>H+,阴离子OH->NO3 -,
故答案为:4AgNO3+2H2O
通电
.
4Ag+O2↑+4HNO3
(5)根据得失电子数相等,氧气与银的关系式为:
O2--------4Ag
22.4L( 4×108 )g
280mL 5.40g
故答案为 280点评:
本题考点: 原电池和电解池的工作原理;电极反应和电池反应方程式.
考点点评: 原电池、电解池的判断方法:
1、若无外加电源,可能是原电池,然后再根据原电池的形成条件判定.
2、若有外接电源,两电极插入电解质溶液中,可能是电解池或电镀池,当阳极金属与电解质溶液中的金属阳离子相同时,则为电镀池.
3、若无明显外接电源的串联电路,则利用题中信息找出能自发进行氧化还原反应的装置为原电池.1年前查看全部
- 【高中化学】这个反应式的反应原理是什么?
【高中化学】这个反应式的反应原理是什么?
这个反应式的反应原理是什么?==红色框中的,
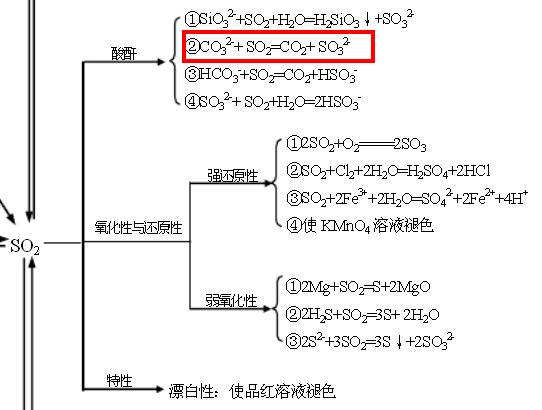
=====红色框下面一个反应式的原理呢, 低调的奢华1年前3
低调的奢华1年前3 -
 vqpfe2_cvx2362 共回答了17个问题
vqpfe2_cvx2362 共回答了17个问题 |采纳率88.2%二氧化硫溶于水生成亚硫酸,亚硫酸与碳酸根反应生成二氧化碳.CO32-+SO2+H2O=H2CO3+SO32- (SO2+H2O相当于亚硫酸)
H2CO3=CO2+H2O
两个化学式合并有:CO32-+SO2+H2O=CO2+H2O+SO32- 两边把水消去得到:CO32-+SO2=CO2+SO32-
这是复分解反应,但必须要满足我们高中学的强酸制弱酸的规律.这个反应说明:酸性:亚硫酸大于碳酸.反过来则不行.1年前查看全部
- 如何判断电解质有没参与反应有一道题是甲烷燃料电池的,电解质溶液是NaOH 我当时想总反应式是CH4+2O2=CO2+2H
如何判断电解质有没参与反应
有一道题是甲烷燃料电池的,电解质溶液是NaOH 我当时想总反应式是CH4+2O2=CO2+2H2O 但是答案是CH4+2O2+2NaOH=Na2CO3+3H2O 我不懂为什么电解质参与了反应.
上网问了下怎么判断电解质何时参与反应.但网友们说看总方程式.问题是多数情况下总方程式我都要自己凑自己想.结果就错了.
我想请各位先帮我分析一下上面这道题.再结合我的情况教下我怎么判断? 我首席牛人被封了1年前3
我首席牛人被封了1年前3 -
 luhuiluhui 共回答了17个问题
luhuiluhui 共回答了17个问题 |采纳率100%最主要的方法就是看反应产物能不能和电解质反应,比如本题中显然CO2是溶解于碱的
欢迎追问1年前查看全部
- 用重铬酸钾法测定褐铁矿中铁含量,整个反应过程如何?定出测定过程中各反应的反应式
 等你忘了我是谁1年前1
等你忘了我是谁1年前1 -
 颓废的种子 共回答了22个问题
颓废的种子 共回答了22个问题 |采纳率81.8%(1)加入盐酸 氧化铁和盐酸的反应
(2)过量SnCl2 还原三价铁 Sn2++Fe3+---Fe2++Sn3+(没配平)
(3)多出来的SnCl2用Hgcl2氧化 这是个两部反应先是 HgCl2+SnCl2----Hg2Cl2(白色)+SnCl4 然后Hg2Cl2(白色)+SnCl2----Hg(黑色)+SnCl4 即出现黑色停止滴定
(4)指示剂:二苯磺酸钠和硫酸磷酸配在一起 然后就是重铬酸钾滴定二价铁的反应了.
差不多就这些了吧.呼呼.1年前查看全部
- 铝和氢氧化钠反应生成沉淀方程式就是先生成NaAlO2,再生成沉淀的总反应式
 xihaworm1年前1
xihaworm1年前1 -
 等峰的人 共回答了21个问题
等峰的人 共回答了21个问题 |采纳率100%2Al+2NaOH+6H2O=2Na(Al(OH)4)+3H2
Al+3(Al(OH)4)=4Al(OH)3
第一个是个方程式 氢气是气体 你说的东西其实就是四羟基合铝酸钠 现在是这样写 第二个是个离子是 有时可以直接就写完这个式子的 两个式子可以合成一个的1年前查看全部
- 9 alcl3反应式如何将1升 0.2mol/l的alcl3溶液与300ml 2.5mol/l的naoh溶液混合,混合后
9 alcl3反应式如何
将1升 0.2mol/l的alcl3溶液与300ml 2.5mol/l的naoh溶液混合,混合后最后可以得到白色沉淀多少克? 021411年前1
021411年前1 -
 pkwen 共回答了18个问题
pkwen 共回答了18个问题 |采纳率94.4%AlCl3+3NaOH=3NaCl+Al(OH)3(沉淀)
0.2mol-0.6mol---0.2mol
氢氧化钠过量了0.15mol,会继续和Al(OH)3反应
Al(OH)3+NaOH=NaAlO2+2H2O
0.15--0.15
最后得到的白色沉淀只有0.2-0.15=0.05mol
沉淀质量=0.05*78=3.9g1年前查看全部
- 电解溶液的阴 阳极的反应式怎么写,书写规则
 czhhgg19811年前3
czhhgg19811年前3 -
 lnn0625 共回答了28个问题
lnn0625 共回答了28个问题 |采纳率85.7%首先,阴极和阳极是针对电解池的,阴极得电子,阳极失去电子;原电池是正极和负极,负极失去电子,正极得电子,原电池中的负极相当于电解池中的阳极,正极相当于电解池中的阴极,这是就电子而言的,对于电极反应式的书写,首先要知道离子的放电顺序,阴离子有氟离子1年前查看全部
- 人们往往喜欢将许多观赏植物放在卧室内过夜,这是否科学?______,其理由是______.写出呼吸作用反应式:_____
人们往往喜欢将许多观赏植物放在卧室内过夜,这是否科学?______,其理由是______.写出呼吸作用反应式:______.
 七-色-阳-光1年前4
七-色-阳-光1年前4 -
 厌倦cc2 共回答了17个问题
厌倦cc2 共回答了17个问题 |采纳率100%解题思路:由我们所学的知识可以知道:(1)植物在白天能进行光合作用、呼吸作用和蒸腾作用,但是到了晚上只进行呼吸作用,消耗氧释放出二氧化碳.(2)人同样也要进行呼吸作用,消耗氧释放出二氧化碳.(3)呼吸作用的表达式是:有机物+氧气→水+二氧化+能量,据此可以解答本题.呼吸作用是细胞内的有机物在氧气的参与下被分解成二氧化碳和水,同时释放出能量的过程.呼吸作用的原料是:有机物(能量)和氧气,产物是:二氧化碳和水同时释放能量.晚上无光植物和人都要进行呼吸作用,消耗氧而释放出二氧化碳,所以植物和人都争夺氧.呼吸作用反应式:有机物+氧气→水+二氧化+能量.
故答案为:有机物+氧气→水+二氧化+能量故答案为:不科学(或错误);植物夜晚只进行呼吸作用,与人争夺氧气;有机物+氧气→水+二氧化+能量点评:
本题考点: 植物的呼吸与人类生产生活的关系.
考点点评: 关键是晚上植物和人都进行呼吸作用,而植物不进行光合作用.1年前查看全部
- 电解池中如果是活性阳极,阴阳两极的点解反应式怎么写
 ok6111年前1
ok6111年前1 -
 xiaozhu841017 共回答了9个问题
xiaozhu841017 共回答了9个问题 |采纳率100%阴极原来怎么写就怎么写,阳极就只写活泼金属失去电子价态升高.
例如铜电解精炼的原理如下:
阳极反应:Cu — 2e = Cu2+阴极反应:Cu2+ + 2e = Cu1年前查看全部
- 人体无氧呼吸会产生二氧化碳吗?反应式是什么
 摩登爱情大爱1年前2
摩登爱情大爱1年前2 -
 hhbiue 共回答了22个问题
hhbiue 共回答了22个问题 |采纳率95.5%无氧呼吸不会产生二氧化碳,产生乳酸.反应式可以上网查一下.1年前查看全部
- ADP+Pi+能量→ATP当反应式由左向右进行时,左边的能量用于______,此过程称为_____反应.
 肚宝1年前1
肚宝1年前1 -
 枯荷 共回答了15个问题
枯荷 共回答了15个问题 |采纳率93.3%合成ATP
合成反应1年前查看全部
- NaCl溶液只能与什么溶液反应,反应式为
 kk额会更好1年前1
kk额会更好1年前1 -
 天堂雪莲 共回答了18个问题
天堂雪莲 共回答了18个问题 |采纳率88.9%硝酸银溶液反应
NaCl + AgNO3=AgCl(沉淀符号) + NaNO31年前查看全部
- A、B、C三种金属,根据下列反应式中的关系:
A、B、C三种金属,根据下列反应式中的关系:
①A+B(NO3)2→A(NO3)2+B ②C+B(NO3)2→C(NO3)2+B;
③A+H2SO4(稀)→ASO4+H2↑; ④C与H2SO4(稀)不反应;
试判断三种金属的活动顺序( )
A.A>C>B
B.A>B>C
C.C>A>B
D.B>C>A 185468621年前1
185468621年前1 -
 15只手 共回答了19个问题
15只手 共回答了19个问题 |采纳率89.5%解题思路:在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.活动性强的金属能把活动性弱的从它的盐溶液中置换出来,①A+B(NO3)2→A(NO3)2+B,说明A的金属活动性比B强,即A>B;②C+B(NO3)2→C(NO3)2+B,说明C的金属活动性比B强,即C>B;
位于氢前面的金属能置换出酸中的氢,③A+H2SO4(稀)→ASO4+H2↑,说明A的金属活动性比氢强,即A>H;④C与H2SO4(稀)不反应,说明C的金属活动性比氢弱,即H>C.
则三种金属的活动顺序A>C>B.
故选:A.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.1年前查看全部
- 氯水中通入so2反应式
 梦里花落不知道1年前3
梦里花落不知道1年前3 -
 开始北漂 共回答了31个问题
开始北漂 共回答了31个问题 |采纳率93.5%氧化还原反应:cl2+2H2O+SO2=2HCL+H2SO4,如有不懂可以继续问的,亲1年前查看全部
- (2005•白山一模)用铝制饭盒盛放醋,一段时间后饭盒被腐蚀,该腐蚀属______腐蚀,相应的化学反应式为______;
(2005•白山一模)用铝制饭盒盛放醋,一段时间后饭盒被腐蚀,该腐蚀属______腐蚀,相应的化学反应式为______;
如盛放纯碱溶液而被腐蚀,有关离子反应式为______;
如盛放食盐(含少量MgCl2杂质)一段时间后变潮湿原因的是______,而且饭盒也会被腐蚀,发生______腐蚀,有关电极反应式______,______. nlink1年前1
nlink1年前1 -
 xinyi 共回答了22个问题
xinyi 共回答了22个问题 |采纳率100%解题思路:金属铝能和酸之间发生反应生成可溶性的铝盐和氢气,纯碱碳酸钠溶液水解显碱性,金属铝可以和碱之间发生反应生成偏铝酸盐和氢气,在中性环境下,金属铝发生吸氧腐蚀,在酸性环境下,金属铝发生析氢腐蚀,据此来回答.用铝制饭盒盛放醋,一段时间后饭盒被腐蚀,因为金属铝和醋酸之间发生2Al+6CH3COOH═2(CH3COOH)3Al+3H2↑,该腐蚀属于金属的化学腐蚀,
如果盛放纯碱溶液,由于碳酸钠水解而显碱性,金属铝可以和碱之间反应生成偏铝酸钠和氢气而被腐蚀,CO32-+H2O⇌HCO3-+OH-,2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑,氯化镁易吸水,导致氯化钠潮解,在中性环境下,金属铝会发生吸氧腐蚀,负极上是金属铝发生失电子的氧化反应,Al-3e-═Al3+,正极上是氧气发生得电子的还原反应,O2+2H2O+4e-═4OH-,
故答案为:化学;2Al+6CH3COOH═2(CH3COOH)3Al+3H2↑;CO32-+H2O⇌HCO3-+OH-,2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑;氯化镁具有较强的吸水性;吸氧;Al-3e-═Al3+;O2+2H2O+4e-═4OH-.点评:
本题考点: 金属的电化学腐蚀与防护.
考点点评: 本题考查学生金属铝的腐蚀情况知识,在中性环境下,金属发生析氢腐蚀,在碱性环境下,金属发生吸氧腐蚀.1年前查看全部
- O3+NH3=?(臭氧与氨的反应式?)
 kerry_8202121年前4
kerry_8202121年前4 -
 素婉 共回答了21个问题
素婉 共回答了21个问题 |采纳率95.2%7O3+6NH3=6NO2+9H2O1年前查看全部
- 按题目要求要求写一个电池反应式的半反应,把箭头左面和右面的倒过来写一不一样
 zjclon1年前1
zjclon1年前1 -
 oorin 共回答了26个问题
oorin 共回答了26个问题 |采纳率88.5%不一样,化学方程式表现的是物质反应的过程,若倒过来,反应就是倒过来进行的了1年前查看全部
- Cu片碳棒共同组成原电池Cu片碳棒同时进入到稀硫酸中,并连接好闭合回路会形成原电池,阴极和阳极的反应式是什么?总反应方程
Cu片碳棒共同组成原电池
Cu片碳棒同时进入到稀硫酸中,并连接好闭合回路会形成原电池,阴极和阳极的反应式是什么?总反应方程式?
实验证明会发生原电池反应 zljlily1年前1
zljlily1年前1 -
 南kk木棉jewel 共回答了15个问题
南kk木棉jewel 共回答了15个问题 |采纳率80%...
不能发生原电池反应.铜的电极电势比氢高.1年前查看全部
- 亚硫酸氢纳会和纳反应吗如果反应.求反应式.
 balige661年前1
balige661年前1 -
 joinshen 共回答了18个问题
joinshen 共回答了18个问题 |采纳率94.4%能反应,2Na+2NaHSO3=2Na2SO3+H21年前查看全部
- 氯的最高价氧化物生成酸的反应式
 财迷意乱1年前3
财迷意乱1年前3 -
 李大为 共回答了15个问题
李大为 共回答了15个问题 |采纳率100%CL2O7+H2O=2HCLO41年前查看全部
- 锂电池的总反应式为Li+MnO2==》LiMnO2,那么其中的LiMnO2怎么读?
锂电池的总反应式为Li+MnO2==》LiMnO2,那么其中的LiMnO2怎么读?
锰酸钾:LiMn2O4
所以LiMnO2不是锰酸钾
那么他读什么呢?
我再说一遍!锰酸钾是LiMn2O4!不是LiMnO2! rzwqy1年前3
rzwqy1年前3 -
 向往净土18607 共回答了20个问题
向往净土18607 共回答了20个问题 |采纳率95%二氧锰化锂1年前查看全部
- 光合作用的反应式补充完整:
 rongshu2191年前0
rongshu2191年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 是不是化学反应式前面的系数就是它的摩尔质?量
 平平鱼ppy1年前2
平平鱼ppy1年前2 -
 sf6hgoj 共回答了16个问题
sf6hgoj 共回答了16个问题 |采纳率87.5%摩尔质量是一摩尔物质的质量,单位是g/mol.数值上等于该物质的式量.
化学方程式前面的系数为参加反应的各物质的分子个数之比,也是物质的量之比.用它们列式计算,可以求物质的量.要求质量,还要通过物质的量来求.用物质的量乘以摩尔质量,就得到质量了1年前查看全部
- 有关电化学原理的推断正确的是 A.金属腐蚀就是金属原子失去电子被还原的过程 B.钢铁吸氧腐蚀时,负极反应式为:2H 2
有关电化学原理的推断正确的是
A.金属腐蚀就是金属原子失去电子被还原的过程 B.钢铁吸氧腐蚀时,负极反应式为:2H 2 O+O 2 +4e→4OH - C.氯碱工业中,阳极发生的反应为:2Cl - –2e→Cl 2 ↑ D.镀锌铁皮的镀层损坏后,铁更容易腐蚀  jimoivy1年前1
jimoivy1年前1 -
 明天就是艳阳天 共回答了30个问题
明天就是艳阳天 共回答了30个问题 |采纳率76.7%C
1年前查看全部
- 用惰性电极点解下列电解质溶液,求阳极反应式,阴极反应式,总反应方程式,溶液复原所需物质,Na2So4,H2SO4。
用惰性电极点解下列电解质溶液,求阳极反应式,阴极反应式,总反应方程式,溶液复原所需物质,Na2So4,H2SO4。
若没有阳离子交换膜的存在,则电解饱和食盐水的化学方程式是? huxinan1231年前3
huxinan1231年前3 -
 6517556 共回答了17个问题
6517556 共回答了17个问题 |采纳率94.1%1、楼上说的不错,电解Na2SO4和H2SO4事实上就是【电解水】
不过楼上写的反应式有点问题,应该是:
阳极:4OH- - 4e- ==== 2H2O + O2
阴极:2H+ + 2e- ==== H2
总反应:2H2O ==== 2H2 + O2
【要复原溶液,需要补充被电解掉的水即可】
2、若没有阳离子交换膜的存在,则电解饱和食盐水的化学方程式是?
【这个题楼上答错了】
阳离子交换膜的作用是【使阴阳离子隔绝,避免其相互反应】.
2NaCl + 2H2O ==== 2NaOH + H2 + Cl2而这样的产物极易反应.所以如果没有阳离子交换膜,这些产物就会继续反应.
具体如下:2NaCl + 2H2O ==== 2NaOH + H2(气体) + Cl2(气体)
2NaOH + Cl2 ==== NaCl + NaClO + H2O
【所以最终的结果是:NaCl + H2O ==(通电)== NaClO + H2(气体)】1年前查看全部
- 分别写出FeO、 Fe2O3、 Fe3O4的颜色状态和与盐酸的反应式
 njkel1年前2
njkel1年前2 -
 令狐冲12 共回答了15个问题
令狐冲12 共回答了15个问题 |采纳率93.3%FeO 黑色固体
Fe2O3 红褐色固体
Fe3O4 黑色固体
FeO+2HCl=FeCl2+H2O
Fe2O3+6HCl=2FeCl3+3H2O
Fe3O4+8HCl=FeCl2+2FeCl3+4H2O1年前查看全部
- 有机物知识有机物燃烧的反应式的通式是什麽?
 zouge1391年前3
zouge1391年前3 -
 mn_27 共回答了20个问题
mn_27 共回答了20个问题 |采纳率100%CxHy + (X+Y/4) O2—-XCO2+Y/2H2O1年前查看全部
- 如何鉴别碳酸钠,碳酸钾,氯化钠,硫酸钾?写出有关反应的化学方程式和离子反应式.
 海曼与人鱼1年前2
海曼与人鱼1年前2 -
 ylindi 共回答了12个问题
ylindi 共回答了12个问题 |采纳率91.7%先加AgNO3溶液碳酸钠:2AgNO3+Na2CO3=Ag2CO3↓+2NaNO32Ag+ +CO3-=Ag2CO3↓碳酸钾:2AgNO3+K2CO3=Ag2CO3↓+2KNO32Ag+ +CO3-=Ag2CO3↓氯化钠:AgNO3+NaCl=AgCl↓+NaNO3Ag+ +Cl-=AgCl↓硫酸钾无明显反应接着加HNO3碳酸钠和...1年前查看全部
- 化学电极反应中得注意负极生成的阳离子能否和电解质中的阴离子共存,不能共存则写入反应式中,为什么呢
化学电极反应中得注意负极生成的阳离子能否和电解质中的阴离子共存,不能共存则写入反应式中,为什么呢
Zn Cu Hcl原电池中Zn离子不能和Cl离子共存,可以生成Zncl,Cl离子怎么不写到电极反应式中呢? 窗子的aa1年前1
窗子的aa1年前1 -
 niunai80_hh 共回答了15个问题
niunai80_hh 共回答了15个问题 |采纳率100%Zn离子和Cl离子可以共存啊,ZnCl2在溶液中是以离子存在的 ,ZnCl2在熔融态也是有着很好的导电性能,虽然Zn和Al一样都是两性金属,但是氯化铝是共价化合物,熔融态不导电,但是氯化锌是可以的,这一点你可以搜百科:http://baike.baidu.com/view/525735.htm1年前查看全部
- 燃料电池上,若用C2H4来做燃料,负极反应式是什么
燃料电池上,若用C2H4来做燃料,负极反应式是什么
能知道正极反应式吗 庄梦鱼1年前4
庄梦鱼1年前4 -
 秋意已浓YOYO 共回答了20个问题
秋意已浓YOYO 共回答了20个问题 |采纳率100%打错了 O2+2H2O+4e- =4OH- 是正极的反应 负极的是C2H4+3O2-4e-=2CO2+2H2O1年前查看全部
- 为什么考离子反应式题中有时物质会写物质的量或体积,有什么目的
 Tony7231年前3
Tony7231年前3 -
 二农戏猪看电视 共回答了26个问题
二农戏猪看电视 共回答了26个问题 |采纳率96.2%考虑少量反应还是过量反应
如:
少量Ca(OH)2与NaHCO3反应:Ca+2OH-+2HCO3-==CaCO3+ CO32- +2H2O
过量Ca(OH)2与NaHCO3反应:Ca+ OH- + HCO3-==CaCO3+ + H2O1年前查看全部
- 义乌科学中考中的物理问题酵母菌的呼吸作用方式可以用以下两个反应式来表示:有氧呼吸:C6H12O6+6O2→6CO2+6H
义乌科学中考中的物理问题
酵母菌的呼吸作用方式可以用以下两个反应式来表示:
有氧呼吸:C6H12O6+6O2→6CO2+6H2O+能量
无氧呼吸:C6H12O6 →2C2H5OH+2CO2 +能量
某兴趣小组成员为了探究酵母菌在呼吸作用过程中气体体积的变化(已知相同条件下,分子数相同的任何气体,体积相同),进行了实验.在装有酵母菌和足量葡萄糖溶液的气球中通入O2和CO2直到饱和,再注入一定量的氧气,扎紧后放入装有温水的量筒中(如图所示),记下液面的读数,以后每隔一段时间进行观察并记录量筒中液面的读数.
若不考虑温度变化对气体体积的影响,则实验过程中量筒内的液面如何变化?▲ .
这道题的答案是液面先不变后升高,那么产生的CO2不会和H2O反应吗? CU20031年前1
CU20031年前1 -
 ngi7 共回答了13个问题
ngi7 共回答了13个问题 |采纳率100%二氧化碳能微溶于水形成碳酸: CO2+ H2O ==== H2CO3
但H2CO3 很不稳定,极易分解,因此不用考虑CO2和H2O反应1年前查看全部
- 镁在空气中燃烧为什么反应式为 镁与二氧化碳反应 而不是镁与氧气反应
 kihvf1年前1
kihvf1年前1 -
 魅力春春 共回答了19个问题
魅力春春 共回答了19个问题 |采纳率94.7%镁在空气中燃烧,和空气中的氮气、氧气、二氧化碳都能反应
2Mg + O2 ==点燃== 2MgO
3Mg + N2 ==点燃== Mg3N2
2Mg + CO2 ==点燃== 2MgO + C1年前查看全部
- 23g钠在氧气中完全燃烧失去电子数为 请写出反应式和解题思路.
 汤林红1年前3
汤林红1年前3 -
 斯言_ 共回答了26个问题
斯言_ 共回答了26个问题 |采纳率92.3%写出方程式并表化合价升降:
0 0 +1 -2
2Na + O2 = Na2O2 2e- (转移电子数)
46g 2NA
23g x x=NA
失去电子数为NA1年前查看全部
- CH4碱性燃料电池 的总反应式怎么写?为什么?
 lunyongliang1年前1
lunyongliang1年前1 -
 不吃鸟的小虫 共回答了13个问题
不吃鸟的小虫 共回答了13个问题 |采纳率100%亲爱的楼主:
CH4+2OH-+2O2=CO32-+3H2O.
【相关】
负极:CH4+10OH - - 8e-===CO32- +7H2O 正极:2O2+8e-+4H2O===8OH- 离子方程式为:CH4+2O2+2OH-===CO32-+3H2O 总反应方程式为:CH4+2O2+2KOH===K2CO3+3H2O
祝您步步高升1年前查看全部
- 已知一混合物由1—戊炔和2—戊烯组成,设计一个方案分离各自纯品,写出相关的反应式
 zhangjiaqi_ivan1年前1
zhangjiaqi_ivan1年前1 -
 737085970 共回答了9个问题
737085970 共回答了9个问题 |采纳率100%利用端基炔氢的酸性,将1-戊炔生成CuCCHCH2CH2CH3与2-戊烯分离1年前查看全部
大家在问
- 1英语翻译如题
- 2已知三棱锥O-ABC,侧棱OA,OB,OC 两两垂直,且OA=OB=OC=2,则以O为圆心且半径为1的球与三棱锥重叠部分
- 3种树者必培其根,种德着必养其心.意思
- 4思念一眉颦,念恩爱厚深,杨柳多情绪,娜息耳应心 .这句话具体是什么意思,前男友在他空间写的、
- 5激动( )跳起来括号里怎么填?填的、得、地中哪一个?
- 6粟粥荠菜文言文的朗读停顿
- 7质量相等的两种液体,密度分别为p1,p2,混合后的密度为多少?体积相等呢?
- 820℃时,某物质不饱和溶液的质量分数为10%,若将此溶液恒温蒸发30g水;或者往此溶液中再溶解5g该物质,
- 9下列各项属于生物的是( )A. 弹钢琴的机器人B. 慢慢长大的钟乳石C. 小溪中的流水D. 天空中飞翔的老鹰
- 10地热能、潮汐能是来自于太阳能?
- 11已知函数的定义域为(-∞,0)∪(0,+∞) 且满足2f(x)+f(1/x)=x ,
- 12出自木兰诗的一个成语是什么啊?它在汉语中的意思是?帮一下忙啊,求啊!
- 13____ Kate have missed the early bus ! A. may B. can C.must D
- 14There is a big clothing s______near my home.The n______ of t
- 15书写平衡常数表达式 如果方程式中有水 默认为1吗?为何?
