由黄铜矿(主要成分是CuFeS 2 )可以冶炼得到粗铜,再经过电解精炼得到纯铜.
 我看着你微笑2022-10-04 11:39:541条回答
我看着你微笑2022-10-04 11:39:541条回答| 由黄铜矿(主要成分是CuFeS 2 )可以冶炼得到粗铜,再经过电解精炼得到纯铜. (1)黄铜矿冶炼得到粗铜的一步反应为:8CuFeS 2 +21O 2
根据原电池原理,稀硫酸做电解质溶液,使用惰性电极,一极通入SO 2 ,另一极通入O 2 ,治理SO 2 污染,负极反应的离子方程式为______ (2)粗铜的电解精炼如图所示.在粗铜的电解过程中,纯铜板应是图中电极______(填图中的字母);在电极d上发生的电极反应式为______;若粗铜中还含有金、银、铁,它们在电解槽中的存在形式位置为______. (3)生物炼铜近几年来逐渐被重视,其原理是:在细菌的帮助下,氧气氧化硫化铜矿石为可溶解性硫酸铜,再进行简单的后续生产.生物炼铜与高温火炼铜相比,优点有______(回答两点)硫酸铜可以配制波尔多液,杀灭果树上的某些细菌,其杀菌原理是______.  |

已提交,审核后显示!提交回复
共1条回复
 yiranzhi 共回答了25个问题
yiranzhi 共回答了25个问题 |采纳率88%- (1)黄铜矿冶炼得到粗铜的一步反应为:8CuFeS 2 +21O 2
高温
.
8Cu+4FeO+2Fe 2 O 3 +16SO 2 若CuFeS 2 中的Fe的化合价为+2价,铜的化合价为+2价,硫的化合价为-1价,氧气中氧元素的化合价为0价,产物中铜的化合价为0价,氧化亚铁中铁的化合价为+2价,氧元素为-2价,三氧化二铁中铁的元素化合价为+3价,氧元素为-2价,二氧化硫中硫元素的化合价为+4价,氧元素为-2价,根据氧化还原规律,化合价降低的发生还原反应,所以反应中被还原的元素是Cu、O;根据原电池原理,稀硫酸做电解质溶液,使用惰性电极,一极通入SO 2 ,另一极通入O 2 ,治理SO 2 污染,负极反应是化合价升高的反应,所以负极离子反应是SO 2 -2e - +2H 2 O=SO 4 2+ +4H + ,
故答案为:Cu、O;SO 2 -2e - +2H 2 O=SO 4 2+ +4H + ;
(2)该装置中a为原电池的正极,b为原电池的负极,所以c为电解池的阳极,d为电解池的阴极,电解时,以硫酸铜-硫酸溶液为电解液,溶液中的Cu 2+ 得到电子沉积在阴极上,发生还原反应,即Cu 2+ +2e - =Cu,作阳极的粗铜中的铜以及比铜活泼的金属失去电子进入溶液,如Fe以Fe 2+ 的形式进入溶液中;比铜不活泼的金属Au、Ag不会失去电子,以单质的形成沉入电解槽形成“阳极泥”,
故答案为:d;Cu 2+ +2e - =Cu;Au、Ag以单质的形成沉积在c(阳极)下方,Fe以Fe 2+ 的形式进入溶液中;
(3)生物炼铜技术是一种利用微生物开矿的湿式制铜技术,生物炼铜的成本远远低于其他冶炼法,具有污染小、反应条件简单、即使含量(品味)很低的矿石也可以被利用等优点;硫酸铜可以配制波尔多液,杀灭果树上的某些细菌,其杀菌原理是铜离子与蛋白质作用使蛋白质变性而丧失其生理功能杀菌,
故答案为:污染小、能量消耗少、反应条件简单等;Cu 2+ 可以使蛋白质变性. - 1年前
相关推荐
- 因为颜色与黄金相似,被称为愚人金的矿石是 (单选 2.0分) A、 雄黄 B、 黄铜矿 C、 黄铁矿 D、
 鸟谈禅1年前1
鸟谈禅1年前1 -
 zhushujie 共回答了13个问题
zhushujie 共回答了13个问题 |采纳率92.3%黄铁矿
常有完好的晶形,呈立方体、八面体、五角十二面体及其聚形,浅黄(铜黄)色,条痕绿黑色,强金属光泽,不透明,无解理,参差状断口,外观和金矿非常相似.1年前查看全部
- (2014•山东一模)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一.其中炉渣的主要成分是Fe0、Fe203、S
(2014•山东一模)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一.其中炉渣的主要成分是Fe0、Fe203、Si02、Al203.各物质有如下转化关系,

请回答:
(1)写出能证明SO2具有氧化性且现象明显的化学方程式______.
(2)用NaOH溶液吸收SO2,所得NaHSO3溶液pH<7,则该溶液中存在离子的物质的量 浓度由大到小的顺序是______.
(3)写出Cu2S熔炼制取粗铜的化学方程式Cu2S+O2
2Cu+SO2高温 .Cu2S+O2
2Cu+SO2高温 .
(4)废电解液中常含有Pb2+、Zn2+,向废电解液中加入Na2S溶液,当有PbS和ZnS沉淀时,C(Zn2+):C(Pb2+)=______.已知:Ksp(PbS)=3.4×10-28mol•L-2,Ksp(Zns)=1.6×10-24mol•L-2.
(5)写出证明溶液I中含有Fe2+的实验过程______o
(6)Na2FeO4能杀菌净水的原因是______
(7)Na2FeO4和Zn可以组成碱性电池,其反应式为:3Zn+2FeO42-+8H20═3Zn(OH)2+2Fe(0H)3+40H-.请写出放电时正极电极反应式______. shallphone1年前1
shallphone1年前1 -
 包包195 共回答了16个问题
包包195 共回答了16个问题 |采纳率93.8%解题思路:(1)根据二氧化硫与硫化氢的水溶液发生反应生成单质硫沉淀;
(2)NaHSO3溶液呈酸性,说明亚硫酸氢根离子水解程度小于电离程度,然后根据电离平衡和水解平衡分析解答.
(3)工业上可用Cu2S和O2反应制取粗铜,说明亚铜被还原,硫元素被氧化,依据氧化还原反应的化合价升降守恒分析书写判断;
(4)根据C(Zn2+):C(Pb2+)=
;Ksp(Zns) Ksp(Pbs)
(5)根据酸性KMnO4溶液能氧化Fe2+,溶液颜色褪去;
(6)根据Na2FeO4是可溶于水的强氧化剂,在水中有杀菌消毒的作用.,其还原产物主要是Fe3+,会水解形成Fe(OH)3胶体,Fe(OH)3胶体,能吸附水中的悬浮的固体颗粒;
(7)依据原电池反应,3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-,正极上FeO42-发生还原反应;(1)二氧化硫与硫化氢的水溶液发生反应生成单质硫沉淀:SO2+2H2S=3S↓+2H2O,SO2体现了氧化性且现象明显,故答案为:SO2+2H2S=3S↓+2H2O;
(3)NaHSO3溶液中亚硫酸氢根离子无论电离还是水解都是较微弱的,NaHSO3溶液呈酸性,说明亚硫酸氢根离子水解程度小于电离程度,所以c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-),故答案为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);
(2)工业上可用Cu2S和O2反应制取粗铜,元素化合价铜元素化合价降低,硫XYZ元素化合价升高,氧气中氧元素化合价降低,说明亚铜被还原,硫元素被氧化,发生的氧化还原反应为Cu2S+O2
高温
.
2Cu+SO2,故答案为:Cu2S+O2
高温
.
2Cu+SO2;
(4)C(Zn2+):C(Pb2+)=
Ksp(Zns)
Ksp(Pbs)=
1.6×10 −24
3.4×10 −28=4.7×10-3;
(5)酸性KMnO4溶液能氧化Fe2+,溶液颜色褪去,故答案为:取少量溶液于试管中,然后滴加少量酸性KMnO4溶液,紫色褪去,证明有Fe2+;
(6)Na2FeO4是可溶于水的强氧化剂,在水中有杀菌消毒的作用,其还原产物主要是Fe3+,会水解形成Fe(OH)3胶体,Fe(OH)3胶体,能吸附水中的悬浮的固体颗粒;故答案为:Na2FeO4是可溶于水的强氧化剂,在水中有杀菌消毒的作用,其还原产物主要是Fe3+,会水解形成Fe(OH)3胶体,Fe(OH)3胶体,能吸附水中的悬浮的固体颗粒;
(7)反应原理为:3Zn+2FeO42-+8H20═3Zn(OH)2+2Fe(0H)3+40H-,正极电极反应式为:FeO42-+3e-+4H2O═Fe(OH)3+5OHˉ,故答案为:FeO42-+3e-+4H2O═Fe(OH)3+5OH-.点评:
本题考点: 二氧化硫的化学性质;难溶电解质的溶解平衡及沉淀转化的本质;二价Fe离子和三价Fe离子的检验.
考点点评: 本题考查学生阅读题目获取信息的能力、氧化还原反应、原电池的工作原理的应用,电极反应,电极产物的判断等,难度中等,要求学生要有扎实的基础知识和灵活运用知识解决问题的能力.注意基础知识的全面掌握.1年前查看全部
- 辨别石头,如何辨别(1)黄铁矿和黄铜矿;(2)石英、方解石和斜长石;(3)辉石和角闪石从外观,手感,质地等,直观的方面.
 janlove1年前1
janlove1年前1 -
 xbxofacq 共回答了25个问题
xbxofacq 共回答了25个问题 |采纳率80%黄铜比黄铁矿颜色更“黄”更深,手感稍重,硬度低(找块石头划一下);斜长石有两组解理,石英没有,透明度低;石英常单晶,长石有多晶;方解石解理好,解理面为菱面体,加点盐酸强烈起泡,因为它就是碳酸钙;辉石单晶体短柱状,横切面近正八边形,角闪石是菱形;辉石颜色比角闪石更深;有平行柱状的两组解理,交角为56,角闪石交角124.1年前查看全部
- [三选一-选修化学与技术]近年来,以黄铜矿(主要成分是CuFeS 2 ,含少量杂质SiO 2 )为原料炼铜有了新进展,科
[三选一-选修化学与技术]
近年来,以黄铜矿(主要成分是CuFeS 2 ,含少量杂质SiO 2 )为原料炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐:
4CuFeS 2 +2H 2 SO 4 +17O 2 =4CuSO 4 +2Fe 2 (SO 4 ) 3 +2H 2 O
某工厂运用该原理生产铜和绿矾的工艺如下:
回答下列问题:
(1)固体A的成分为 ___________(写化学式);
(2)写出反应Ⅲ的化学方程式___________ ;
(3)试剂a为__________,试剂b为_____________;
(4)欲从溶液中获得绿矾晶体,分离操作Ⅰ应为_______、____________、___________。 二仙桥东二路1年前1
二仙桥东二路1年前1 -
 cyr0223 共回答了18个问题
cyr0223 共回答了18个问题 |采纳率94.4%(1)Fe(OH) 3 、CuO
(2)CuSO 4 + Fe= Cu + FeSO 4
(3)稀H 2 SO 4 ;铁粉
(4)蒸发浓缩 ;冷却结晶 ;过滤1年前查看全部
- 黄铜矿(CuFeS2)是制取铜的主要原料,还可制备硫及铁的化合物.
黄铜矿(CuFeS2)是制取铜的主要原料,还可制备硫及铁的化合物.
(1)冶炼铜的反应为:
8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2高温 .
若CuFeS2中Cu、Fe的化合价均为+2,反应中被氧化的元素有______(填元素符号).
(2)上述冶炼过程中产生大量的SO2,下列关于SO2的说法中正确的是______(填字母).
a.可处理后用于消毒杀菌
b.可排放到空气中消灭害虫
c.可处理后用于漂白织物
d.可用KMnO4溶液吸收制浓硫酸
(3)过二硫酸钾(K2S2O8)具有强氧化性,经少量K2S2O8处理过的KI溶液遇淀粉变蓝色,写出K2S2O与KI溶液反应的离子方程式:______.
(4)用冶炼铜反应的固体产物配制FeCl2溶液,首先用______处理,然后过滤,再向溶液中加入过量的______.FeCl2溶液长期放置会变质,溶液变成棕黄色.检验FeCl2溶液已变质加入______,溶液中立即出现______现象.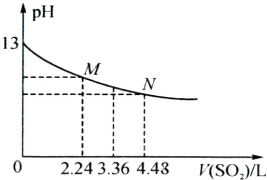
(5)将足量的SO2慢慢通入一定体积某浓度的NaOH溶液中,溶液的pH随SO2体积(已换算成标准状况,不考虑溶液体积变化)的变化曲线如图所示:
①NaOH溶液的物质的量浓度为______mol•L-1;
②n(SO2):n(NaOH)=1:2,反应对应M点的纵坐标______7(填“<”、“=”或“>”);
③N点溶液中含有的阴离子除OH-外,还有______(填化学式). 心情使者1年前1
心情使者1年前1 -
 陈可心 共回答了10个问题
陈可心 共回答了10个问题 |采纳率80%解题思路:(1)在氧化还原反应中,化合价升高的元素被氧化;
(2)根据二氧化硫的性质和作用来回答;
(3)过二硫酸钾(K2S2O8)具有强氧化性,碘离子具有还原性,根据氧化还原反应知识来回答;
(4)FeO和Fe2O3都能和盐酸反应生成对应的盐,三价铁可以和金属铁反应生成亚铁离子,三价铁离子遇到硫氰酸钾显示红色;
(5)①根据氢氧化钠溶液的pH计算溶液的浓度;
②当n(SO2):n(NaOH)=1:2时,二者发生反应生成亚硫酸钠和水,亚硫酸钠会发生水解反应;
③根据二氧化硫的量以及氢氧化钠的量之间的关系来判断化学反应后的产物.(1)在氧化还原反应中,化合价升高的元素Fe、S,被氧化,故答案为:Fe、S;(2)a.二氧化硫处理后用于消毒杀菌,故a正确;b.二氧化硫有毒,不可排放到空气中,故b错误;c.二氧化硫具有漂白性,可处理后用于漂白...
点评:
本题考点: 含硫物质的性质及综合应用;氧化还原反应;二氧化硫的化学性质.
考点点评: 本题综合考查学生氧化还原反应知识以及元素及化合物知识,属于综合知识的考查,难度大.1年前查看全部
- 黄铜矿,其中含硫的质量分数是32.16%求其中的铁元素的质量分数
黄铜矿,其中含硫的质量分数是32.16%求其中的铁元素的质量分数
要过程
 莹雪1年前1
莹雪1年前1 -
 八级mm 共回答了19个问题
八级mm 共回答了19个问题 |采纳率100%设 铁元素的质量分数是X
黄铜矿 分子式 CuFeS2
Fe/S:56/(32×2)=X/32.16%
X=28.14%1年前查看全部
- (12分)(2012•山东)工业上由黄铜矿(主要成分CuFeS 2 )冶炼铜的主要流程如下:
(12分)(2012•山东)工业上由黄铜矿(主要成分CuFeS 2 )冶炼铜的主要流程如下:

(1)气体A中的大气污染物可选用下列试剂中的 吸收.
a.浓H 2 SO 4 b.稀HNO 3
c.NaOH溶液 d.氨水
(2)用稀H 2 SO 4 浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在 (填离子符号),检验溶液中还存在Fe 2+ 的方法是 (注明试剂、现象).
(3)由泡铜冶炼粗铜的化学反应方程式为 .
(4)以CuSO 4 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是 .
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu 2+ 向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应2Cu+O 2 +2H 2 SO 4 ═2CuSO 4 +2H 2 O可制备CuSO 4 ,若将该反应设计为原电池,其正极电极反应式为 . 冻梨1年前1
冻梨1年前1 -
 风月无边住持 共回答了18个问题
风月无边住持 共回答了18个问题 |采纳率88.9%(1)cd(2)Fe 3+ ;取少量溶液,滴加KMnO 4 溶液,KMnO 4 溶液紫色褪去(3)3Cu 2 O+2Al Al 2 O 3 +6Cu(4)bd(5)4H + +O 2 +4e ﹣ =2H 2 O
Al 2 O 3 +6Cu(4)bd(5)4H + +O 2 +4e ﹣ =2H 2 O
(1)由流程图转化可知,气体A中的大气污染物主要是二氧化硫,选择试剂吸收二氧化硫,不能产生新的污染气体,二氧化硫是酸性氧化物,结合选项中各物质的性质判断;
(2)用稀H 2 SO 4 浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe 3+ ;
Fe 2+ 具有还原性,可以利用KMnO 4 溶液检验;
(3)由流程图转化可知,Cu 2 O与Al反应置换反应生成Al 2 O 3 与Cu;
(4)a、反应中有热能产生;
b、精炼铜时,粗铜做阳极;
c、溶液中Cu 2+ 向阴极移动;
d、Ag、Pt、Au不如铜活泼,铜放电后Ag、Pt、Au从粗铜脱落;
(5)利用原电池原理,负极失电子发生氧化反应,正极上得到电子发生还原反应.
(1)由流程图转化可知,气体A中的大气污染物主要是二氧化硫,选择试剂吸收二氧化硫,不能产生新的污染气体,
a、浓H 2 SO 4 不能吸收二氧化硫,故a错误;
b、稀HNO 3 可以吸收二氧化硫,但生成NO污染大气,故b错误;
c、NaOH溶液与二氧化硫反应生成亚硫酸钠,故c正确;
d、氨水与二氧化硫反应生成亚硫酸铵,故d正确;
故选cd;
(2)用稀H 2 SO 4 浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe 3+ ;
Fe 2+ 具有还原性,可以利用KMnO 4 溶液检验,取少量溶液,滴加KMnO 4 溶液,KMnO 4 溶液紫色褪去,
故答案为:Fe 3+ ;取少量溶液,滴加KMnO 4 溶液,KMnO 4 溶液紫色褪去;
(3)由流程图转化可知,Cu 2 O与Al反应置换反应生成Al 2 O 3 与Cu,反应方程式为3Cu 2 O+2Al Al 2 O 3 +6Cu,
Al 2 O 3 +6Cu,
故答案为:3Cu 2 O+2Al Al 2 O 3 +6Cu;
Al 2 O 3 +6Cu;
(4)a、反应中有热能产生,故a错误;
b、精炼铜时,粗铜做阳极,连接电源正极,发生氧化反应,故b正确;
c、溶液中Cu 2+ 向阴极移动,故c错误;
d、Ag、Pt、Au不如铜活泼,铜放电后Ag、Pt、Au从粗铜脱落,利用阳极泥可回收Ag、Pt、Au等金属,故d正确;
故选bd;
(5)利用反应2Cu+O 2 +2H 2 SO 4 ═2CuSO 4 +2H 2 O可制备CuSO 4 ,若将该反应设计为原电池,正极上是氧气得到电子发生还原反应,酸性溶液中生成的氢氧根离子以水的形式存在,其正极电极反应式为:4H + +O 2 +4e ﹣ =2H 2 O,故答案为:4H + +O 2 +4e ﹣ =2H 2 O.
<>1年前查看全部
- (16分). 铜是人类最早知道的金属之一,实验室可用C、H 2 还原CuO制取少量的Cu,工业上主要用火法从黄铜矿中提炼
(16分). 铜是人类最早知道的金属之一,实验室可用C、H 2 还原CuO制取少量的Cu,工业上主要用火法从黄铜矿中提炼Cu。
Ⅰ. 实验证明,C还原CuO时既可能生成Cu,也可能生成Cu 2 O,即使在C过量时,实验中CuO也可能部分未被还原。为了测定某次实验产物的组成,取1.2 g C跟8.0 g CuO混合加热,将反应生成的气体通过足量的澄清石灰水并集气。一段时间后停止加热,共收集到560 mL气体(已经折算成标准状况),测得沉淀的质量为2.5 g。则:
(1)上述实验中C (填“完全”或“不完全”)参加反应,实验中收集到的气
体是 (填写化学式),产生这种气体的化学方程式为: 。
(2)反应后得到的固体混合物总质量为 ,其中含氧化合物的物质的量为 mol。
Ⅱ. 黄铜矿的主要成分X是由Cu、Fe、S三种元素组成的复盐,其中Cu、Fe两种元素的质量比为8∶7;将 m g X粉末全部溶于200 mL的浓HNO 3 ,反应后的溶液加水稀释至 2.12 L时测得其pH为0;将稀释后的溶液分为两等份,向其中一份溶液中滴加6.05mol/L的NaOH溶液,向另一份溶液中滴加0.600mol/L Ba(NO 3 ) 2 溶液,两溶液中均生成沉淀,且沉淀的质量随所加溶液的体积变化如下图所示:
(1) 请通过计算确定 m 的值;
(2) X的摩尔质量为368 g/mol,请确定X的化学式。 lxh_丢丢1年前1
lxh_丢丢1年前1 -
 七月花吼 共回答了19个问题
七月花吼 共回答了19个问题 |采纳率78.9%Ⅰ⑴不完全(1分);CO(1分);CO 2 +C 高温 2CO 或 CuO+C 高温 Cu+CO↑ (1分);
⑵ 7.4g,(1分); 0.025 mol(1分)
Ⅱ、⑴ 依题意, m g X中: n (Cu)∶ n (Fe)=1∶1
2 n (Cu 2 + ) +3 n (Fe 3 + ) =6.05mol·L - 1 ×0.2L×2-1 mol·L - 1 ×2.12L
故: n (Cu) = n (Fe) = 0.06mol
又, n (S) = 0.6mol·L - 1 ×0.1L×2 = 0.12mol
因此, m g = m (Cu) + m (Fe) + m (S)
= 0.06mol×64g·mol - 1 +0.06mol×56g·mol - 1 +0.12mol×32g·mol - 1 = 11.04g
即 m 的值为11.04(3分)
⑵ 设X的化学式为(CuFeS 2 ) n ,则
(64+56+32×2)×n = 368 n = 2故X的化学式为Cu 2 Fe 2 S 4 (3分)
Ⅰ(1)560ml气体是CO,物质的量是0.025mol。生成CO的方程式是CO 2 +C 高温 2CO 或 CuO+C 高温 Cu+CO↑。沉淀是碳酸钙,物质的量是0.025mol,则生成的CO 2 也是0.025mol。由于碳的物质的量是0.1mol,所以实验中碳没有完全参加反应。
(2)与碳原子结合的氧原子的物质的量是0.025mol+0.025mol×2=0.075mol,质量是12.g,所以最终固体的质量是8g-1.2g+1.2g-0.6g=7.4g。原氧化铜中氧原子的物质的量是0.1mol,所以剩余氧原子的物质的量是0.1mol-0.075mol=0.025mol,因此含氧化合物的物质的量是0.025mol。
Ⅱ、考查根据方程式及有关图像进行的有关计算。1年前查看全部
- 以黄铜矿(CuFeS 2 )为原料冶炼铜的反应为:
以黄铜矿(CuFeS 2 )为原料冶炼铜的反应为:
8CuFeS 2 +21O 2 8Cu +4FeO+2Fe 2 O 3 + 16SO 2
8Cu +4FeO+2Fe 2 O 3 + 16SO 2
(1)若Cu为+2价,则反应中每生成1 mol Cu需要转移____________ mol 电子。
(2)为综合利用炉气中的大量SO 2 ,下列方案合理的是____________。
a.用浓硫酸吸收
b.用于制备硫酸
c.高空排放
d.用纯碱溶液吸收制亚硫酸钠
(3)为检验所得矿渣中是否含有FeO、Fe 2 O 3 、CuO、Al 2 O 3 、SiO 2 等氧化物,进行了以下实验:
①取一定量矿渣粉末,加入适量浓硫酸后加热,固体全部溶解,得溶液A;将产生的气体通人品红溶液中,溶液褪色。由此判断矿渣中一定含有_________ ,一定没有_________。
②将溶液A稀释后分成两份,取其中一份,加入过量NaOH 溶液,有沉淀产生,静置后取上层清液,通入过量的CO 2 , 溶液变浑浊。由此判断出矿渣中一定含有____________ ,写出通入过量的CO 2 所发生反应的离子方程式:_________________ 。
③另取一份溶液A加入过量的铁粉,充分反应后过滤,得到的固体中有红色物质,由此判断矿渣中有_____________ , 写出此步操作中得到红色物质所发生反应的离子方程式__________________。 为三留一手1年前1
为三留一手1年前1 -
 晨涵 共回答了17个问题
晨涵 共回答了17个问题 |采纳率100%(1)12.5
(2)bd
(3) ①FeO;SiO 2
②Al 2 O 3 ;AlO 2 - +CO 2 +2H 2 O==Al(OH) 3 ↓+HCO 3 -
③CuO; Fe+Cu 2+ ==Fe 2+ + Cu1年前查看全部
- 方解石,方铅石,黄铜矿,黄铁矿,磷灰石的主要成分
 wujiehk1年前1
wujiehk1年前1 -
 mingyunluo 共回答了12个问题
mingyunluo 共回答了12个问题 |采纳率75%方解石化学成分Ca[CO3],CaO56%,CO244%.
方铅石化学成分PbS
黄铜矿化学成分CuFeS2,含铜34.56%
黄铁矿化学成分FeS2
磷灰石化学成分3Ca3(PO4)2·CaF2.含氟约4%.1年前查看全部
- 12.5g黄铜矿经测含3.6g硫(杂质吧含硫),矿样中CuFeS2的质量分数为多少.请详解
 念念忘返1年前1
念念忘返1年前1 -
 飘零的天空幻 共回答了13个问题
飘零的天空幻 共回答了13个问题 |采纳率100%设,矿样中CuFeS2的质量是Xg
X*64/(64+56+32*2)*100%=3.6
X=10.35g
矿样中CuFeS2的质量分数为10.35/12.5*100%=82.8%1年前查看全部
- 黄铜矿(CuFeS 2 )是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
黄铜矿(CuFeS 2 )是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS 2 +21O 2 8Cu+4FeO+2Fe 2 O 3 +16SO 2
8Cu+4FeO+2Fe 2 O 3 +16SO 2
若CuFeS 2 中Fe的化合价为+2,反应中被还原的元素是______________(填元素符号)。
(2)上述冶炼过程产生大量SO 2 。下列处理方案中合理的是______________(填代号)。
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制NaSO 3 d.用浓硫酸吸收
(3)过二硫酸钾(K 2 S 2 O 8 )具有强氧化性,可I - 将氧化为I 2 :S 2 O 8 2- +2I - ==2SO 4 2- +I 2
通过改变反应途径,Fe 2+ 、Fe 3+ 均可催化上述反应。试用离子方程式表示Fe 3+ 对上述反应催化的过程
________________________,___________________________。(不必配平) 孤星毒狼1年前1
孤星毒狼1年前1 -
 非烦男人 共回答了23个问题
非烦男人 共回答了23个问题 |采纳率95.7%(1)Cu、O
(2)bc
(3)Fe 3+ +I - → Fe 2+ +I 2 ;S 2 O 8 2- +Fe 2+ → SO 4 2- +Fe 3+1年前查看全部
- 火法炼铜可以从黄铜矿(CuFeS2)或辉铜矿(Cu2S)中提取铜,发生如下反应:
火法炼铜可以从黄铜矿(CuFeS2)或辉铜矿(Cu2S)中提取铜,发生如下反应:
①2CuFeS2+4O2
Cu2S+3SO2+2FeO800℃ .
②2Cu2S+3O2
2Cu2O+2SO21200℃ .
③2Cu2O+Cu2S
6Cu+SO2↑1200℃ .
下列说法正确的是( )
A. 反应②、③中,Cu2S都只做还原剂
B. 1mol CuFeS2生成1molCu,理论上消耗2.5mol O2
C. 1mol Cu2S和O2反应生成2molCu转移的电子数为4mol
D. 反应①中,共转移的电子数为16mol,CuFeS2中铜元素的化合价为+2 moon_男孩1年前1
moon_男孩1年前1 -
 bgszcj 共回答了14个问题
bgszcj 共回答了14个问题 |采纳率100%解题思路:A.②中S元素的化合价升高,O元素的化合价降低;③中,Cu2S中Cu元素的化合价降低,S元素的化合价升高;
B.由反应可知,存在6Cu~3Cu2S~6CuFeS2~15O2,以此分析;
C.Cu元素由+1价降低为0,O元素的化合价降低,而S元素的化合价由-2价升高为+4价;
D.反应①中,Cu元素的化合价降低,O元素的化合价降低,S元素的化合价升高.A.②中S元素的化合价升高,O元素的化合价降低,Cu2S只做还原剂;③中,Cu2S中Cu元素的化合价降低,S元素的化合价升高,Cu2S既是还原剂又是氧化剂,故A错误;
B.由反应可知,存在6Cu~3Cu2S~6CuFeS2~15O2,则1mol CuFeS2生成1molCu,理论上消耗2.5molO2,故B正确;
C.Cu元素由+1价降低为0,O元素的化合价降低,而S元素的化合价由-2价升高为+4价,则转移的电子数为1mol×[4-(-2)]=6mol,故C错误;
D.反应①中,CuFeS2中铜元素的化合价为+2,Cu元素的化合价降低,O元素的化合价降低,S元素的化合价由-2价升高为+4价,2molCuFeS2反应转移电子为24mol,故D错误;
故选B.点评:
本题考点: 氧化还原反应的计算;氧化还原反应.
考点点评: 本题考查氧化还原反应及计算,明确反应中的元素的化合价变化是解答本题的关键,注意电子守恒、原子守恒的应用,选项D为易错点,题目难度较大.1年前查看全部
- 一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
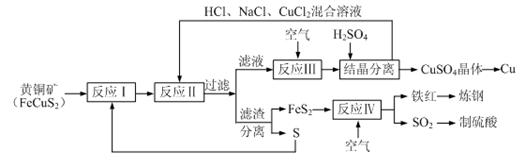
注:反应Ⅱ的离子方程式为Cu 2+ +CuS+4Cl — =2CuCl 2 - +S
请回答下列问题:
⑴反应Ⅰ的产物为(填化学式) ▲ 。
⑵反应Ⅲ的离子方程式为 ▲ 。
⑶一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是
▲ 。
⑷炼钢时,可将铁红投入熔融的生铁中,该过程中主要反应的化学方程式是 ▲ 。
⑸某硫酸厂为测定反应Ⅳ所得气体中SO 2 的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe 2 (SO 4 ) 3 溶液完全反应后,用浓度为0.02000 mol/L的K 2 Cr 2 O 7 标准溶液滴定至终点,消耗K 2 Cr 2 O 7 溶液25.00 mL 。
已知:Cr 2 O 7 2 - + Fe 2 + + H + →Cr 3+ +
3+ +  Fe 3 + + H 2 O(未配平)
Fe 3 + + H 2 O(未配平)
①SO 2 通入Fe 2 (SO 4 ) 3 溶液,发生反应的离子方程式为 ▲ 。
②反应Ⅳ所得气体中SO 2 的体积分数为 ▲ 。 文不渔1年前1
文不渔1年前1 -
 jianxionghe 共回答了19个问题
jianxionghe 共回答了19个问题 |采纳率84.2%⑴FeS 2 、CuS⑵4CuCl 2 - +O 2 +4H + =4Cu 2+ +8Cl - +2H 2 O⑶该温度下,硫酸铜的溶解度小于氯化铜⑷3C+Fe 2 O 3 2Fe+3CO⑸①SO 2 + 2Fe 3+ + 2H 2 O=SO 4 2- + 2Fe 2+ + 4H + ②12.00% ...1年前查看全部
- 以黄铜矿精矿为原料,制取金属铜的工艺如下所示:
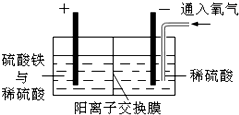 以黄铜矿精矿为原料,制取金属铜的工艺如下所示:
以黄铜矿精矿为原料,制取金属铜的工艺如下所示:
Ⅰ.将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎.
Ⅱ.采用如图所示装置进行电化学浸出实验.将精选黄铜矿粉加入电解槽的阳极区,恒速搅拌,使矿粉溶解.在阴极区通入氧气,并加入少量催化剂.
Ⅲ.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应:2RH(有机相)+Cu2+(水相)⇌R2Cu(有机相)+2H+(水相)分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生.
Ⅳ.电解硫酸铜溶液制得金属铜.
(1)黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应:
CuFeS2+4H+═Cu2++Fe2++2H2S↑2Fe3++H2S═2Fe2++S↓+2H+
阳极区硫酸铁的主要作用是______.
(2)阴极区,电极上开始时有大量气泡产生,后有红色固体析出,一段时间后红色固体溶解.写出析出红色固体的反应方程式______.
(3)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是______.
(4)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是______.
(5)步骤Ⅳ,若电解200mL0.5mol/L的CuSO4溶液,生成铜3.2g,此时溶液中离子浓度由大到小的顺序是______. 施耐德1年前1
施耐德1年前1 -
 丝芦花语 共回答了18个问题
丝芦花语 共回答了18个问题 |采纳率94.4%解题思路:(1)硫化氢有毒,直接排放会污染空气;
(2)首先氢离子放电生成氢气,反应一段时间,铜离子放电生成铜,再通入氧气的条件下Cu、氧气、硫酸反应生成硫酸铜;
(3)有机相和水相不互溶,分离有机相和水相通常利用分液的方法,使用的仪器为分液漏斗;
(4)增大氢离子浓度,根据平衡移动原理分析;
(5)电解uSO4溶液,发生反应2CuSO4+2H2O
2Cu+2H2SO4+O2↑,200mL 0.5mol/L的CuSO4溶液中n(CuSO4)=0.2L×0.5mol/L=0.1mol,生成铜3.2g,物质的量为[3.2g/64g/mol]=0.05mol,故生成H2SO40.1mol,溶液中CuSO4为0.1mol-0.05mol=0.05mol,电解后的溶液为CuSO4、H2SO4混合溶液,溶液中存在硫酸的电离、铜离子水解、水的电离等,据此判断.通电 .(1)由发生的反应可知,Fe3+氧化吸收硫化氢气体,防止环境污染,
故答案为:吸收硫化氢气体,防止环境污染;
(2)首先氢离子放电生成氢气,反应一段时间,铜离子放电生成铜,再通入氧气的条件下Cu、氧气、硫酸反应生成硫酸铜,发生的反应依次为:2H++2 e-=H2↑、Cu2++2e-=Cu、2Cu+O2+2H2SO4=2CuSO4+2H2O,析出红色固体的反应方程式Cu2++2e-=Cu,
故答案为:Cu2++2e-=Cu;
(3)有机相和水相不互溶,分离有机相和水相通常利用分液的方法,使用的仪器为分液漏斗,
故答案为:分液漏斗;
(4)向有机相中加入一定浓度的硫酸,增大H+浓度,使平衡2RH(有机相)+Cu2+(水相)⇌R2Cu(有机相)+2H+(水相)逆向移动,Cu2+进入水相得以再生,
故答案为:增大H+浓度,使平衡2RH(有机相)+Cu2+(水相)⇌R2Cu(有机相)+2H+(水相)逆向移动,Cu2+进入水相得以再生;
(5)电解uSO4溶液,发生反应2CuSO4+2H2O
通电
.
2Cu+2H2SO4+O2↑,200mL 0.5mol/L的CuSO4溶液中n(CuSO4)=0.2L×0.5mol/L=0.1mol,生成铜3.2g,物质的量为[3.2g/64g/mol]=0.05mol,故生成H2SO40.05mol,溶液中CuSO4为0.1mol-0.05mol=0.05mol,电解后的溶液为CuSO4、H2SO4混合溶液,溶液呈酸性,溶液中铜离子水解、水发生电离,故n(H+)>0.05mol×2=0.1mol,n(SO42-)=0.1mol,n(Cu2+)<0.05mol,溶液中氢氧根浓度很小,故c(H+)>c(SO42-)>c(Cu2+)>c(OH-),
故答案为:c(H+)>c(SO42-)>c(Cu2+)>c(OH-).点评:
本题考点: 电解原理;原电池和电解池的工作原理.
考点点评: 本题考查电解原理、对工艺原理的理解、常用化学用语、离子浓度比较等,题目综合性较大,是对所学知识的综合考查,需要学生具有知识的基础与分析、解决问题的能力,难度中等,(5)中注意根据物质的量判断离子大小.1年前查看全部
- 如图所示火法炼铜首先要焙烧黄铜矿……
如图所示火法炼铜首先要焙烧黄铜矿……

第三题,. 霉酸1年前3
霉酸1年前3 -
 东方狮 共回答了19个问题
东方狮 共回答了19个问题 |采纳率78.9%1年前查看全部
- 黄铜矿和硫磺哪个是金属矿物吗?找规律 3 15 35 63 99.第N个是多少 (用N表示)
 linminyisheng1年前2
linminyisheng1年前2 -
 10213000 共回答了27个问题
10213000 共回答了27个问题 |采纳率92.6%一、黄铜矿是金属矿物,硫磺是非金属矿物
二、N=(2n)^2-1(2倍n的平方减1) ,或者表达为4n^2-1(n的平方乘以4,再减去1)1年前查看全部
- 黄铜矿(主要成分CuFeS2)是提取铜的主要原料
黄铜矿(主要成分CuFeS2)是提取铜的主要原料
(1)取12.5g黄铜矿样品,经测定含3.60g硫(杂质不含硫),矿样中CuFeS2含量为______;
(2)已知2CuFeS2+4O2
Cu2S+3SO2+2FeO(炉渣)产物Cu2S在1200℃高温下继续反应:2Cu2S+3O2→2Cu2O+2SO2;2Cu2O+Cu2S→6Cu+SO2;800℃
假定各步反应都完全,完成下列计算:
①由6mol CuFeS2生成6mol Cu,求消耗O2的物质的量______;
②6mol CuFeS2和14.25mol O2反应,理论上可得到______摩尔铜;
③6mol CuFeS2和15.75mol O2反应,理论上可得到______摩尔铜. 772327681年前1
772327681年前1 -
 bw**83a_dv_25f2 共回答了12个问题
bw**83a_dv_25f2 共回答了12个问题 |采纳率100%解题思路:(1)m(样品)×ω(CuFeS2)×CuFeS2中S元素的质量分数=m(S);
(2)①由反应可知,最终CuFeS2与O2反应的最终成为FeO、Cu、SO2,根据原子守恒计算n(FeO)、n(SO2),根据O原子守恒可知2n(O2)=n(FeO)+n(SO2);
②③根据方程式计算6mol CuFeS2消耗O2的物质的量、生成Cu2S的物质的量,进而计算剩余O2的物质的量.根据2Cu2S+3O2=2Cu2O+2SO2计算反应的Cu2S的物质的量、生成Cu2O的物质的量,进而计算剩余Cu2S的物质的量,再根据2Cu2O+Cu2S→6Cu+SO2进行过量计算.(1)12.5g×ω(CuFeS2)×[64/64+56+64]=3.6g,解得ω(CuFeS2)=82.8%,
故答案为:82.8%;
(2)①由反应可知,最终CuFeS2与O2反应的最终成为FeO、Cu、SO2,根据原子守恒n(FeO)=n(CuFeS2)=6mol,n(SO2)=2n(CuFeS2)=mol,根据O原子守恒可知2n(O2)=n(FeO)+2n(SO2)=6mol+12mol×2,故n(O2)=15mol,
故答案为:15;
②2CuFeS2+4O2=Cu2S+3SO2+2FeO
6mol12mol 3mol
故剩余氧气为14.25mol-12mol=2.25mol,生成Cu2S为3mol,
2Cu2S+3O2=2Cu2O+2SO2;
3mol 4.5mol
故氧气不足,故氧气完全反应,生成Cu2O为2.25mol×[2/3]=1.5mol,剩余Cu2S为3mol-1.5mol=1.5mol,
2Cu2O+Cu2S=6Cu+SO2;
1.5mol 0.75mol
故氧化亚铜完全反应,生成铜1.5mol×[6/2]=4.5mol,
故答案为:4.5;
③2CuFeS2+4O2=Cu2S+3SO2+2FeO
6mol12mol 3mol
故剩余氧气为15.75mol-12mol=3.75mol,生成Cu2S为3mol,
2Cu2S+3O2=2Cu2O+2SO2;
3mol 4.5mol
故氧气不足,故氧气完全反应,生成Cu2O为3.75mol×[2/3]=2.5mol,剩余Cu2S为3mol-2.5mol=0.5mol,
2Cu2O+Cu2S=6Cu+SO2;
1mol 0.5mol
故氧化亚铜有剩余,生成铜0.5mol×6=3mol,
故答案为:3.点评:
本题考点: 有关混合物反应的计算;化学方程式的有关计算.
考点点评: 本题考查混合物的有关计算,题目过程复杂,计算量很大,为易错题目,对学生的心理素质有较高的要求,注意原子守恒计算与过量计算.1年前查看全部
- 工业上可用黄铜矿(CuFeS 2 )冶炼铜,同时还可得到多种物质。
工业上可用黄铜矿(CuFeS 2 )冶炼铜,同时还可得到多种物质。
工业冶炼铜的化学方程式是:
(1)CuFeS 2 中Fe的化合价为+2,反应中被还原的元素是氧元素和____________。
(2)用少量黄铜矿冶炼铜产生的炉渣(主要含Fe 2 O 3 、FeO、SiO 2 、Al 2 O 3 )模拟制铁红(Fe 2 O 3 ),进行如下实验。
①滤液中的阳离子有Fe 3+ 、Fe 2+ 、H + 、_____________。
②为确认滤液中含Fe 2+ ,下列实验方案和预期现象正确的是____(填序号)。实验方案 预期现象 a 加NaOH溶液 产生白色沉淀,变灰绿再变红褐 b 先加KSCN溶液,再加氯水 先无明显现象,后变红 C 加酸性KMnO 4 溶液 紫色褪去 d 先加氯水,再加KSCN溶液 溶液先变黄,再变红
③滤液在酸性条件下,与H 2 O 2 反应的离子方程式是
______________________________________________________________________。
(3)冶炼铜过程中产生大量的SO 2 可用于制硫酸,尾气可用纯碱溶液吸收。已知用1L1mol/L的纯碱溶液吸收SO 2 ,生成n(Na 2 SO 3 ):n(NaHSO 3 )=1:2,则吸收的SO 2 物质的量是_____________mol。 猪头方片五1年前1
猪头方片五1年前1 -
 筱茜0610 共回答了17个问题
筱茜0610 共回答了17个问题 |采纳率94.1%1年前查看全部
- 黄铜矿中如何确定元素化合价?
 chylchyl1年前1
chylchyl1年前1 -
 流浪之萤火虫 共回答了14个问题
流浪之萤火虫 共回答了14个问题 |采纳率92.9%CuFeS2
这个必须根据实际状况来,瞎猜是不行的.
首先Fe不可能是+3价
Fe3+氧化 S2- 或者-1价的S(关键点)
那么Fe +2价
S只能是-1或-2
因为-1的话,Cu就是0了,不可能
所以S是-2,Fe +2 Cu是+21年前查看全部
- 黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物.
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物.
(1)冶炼铜的反应为:
8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2高温 .
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是______(填元素符号).
(2)上述冶炼过程产生大量SO2.下列处理方案中合理的是______(填代号).
a.高空排放b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO4d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82-+2I-=2SO42-+I2.
通过改变反应途径,Fe3+、Fe2+均可催化上述反应.试用离子方程式表示Fe3+对上述反应催化的过程:______、______(不必配平)
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.方法为:
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3.
a.除去Al3+的离子方程式是______.
b.选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸稀硫酸KSCN溶液KMnO4溶液NaOH溶液碘水
所选试剂为______.证明炉渣中含有FeO的实验现象为______. sdu_xuhui1年前1
sdu_xuhui1年前1 -
 东巴龙 共回答了20个问题
东巴龙 共回答了20个问题 |采纳率100%解题思路:(1)反应中化合价降低的元素被还原;
(2)冶炼过程产生大量SO2,处理方案中合理的分析是二氧化硫是污染性气体,不能排放到空气中,可以吸收利用;
(3)三价铁具有氧化性,能将碘离子氧化;
(4)a、氧化铝是两性氧化物,能和强酸以及强碱反应;
b、亚铁离子能被高锰酸钾溶液氧化,使的高锰酸钾溶液褪色.(1)化合价降低的元素Cu、O,在反应中被还原,故答案为:Cu、O;
(2)冶炼过程产生大量SO2.分析下列处理方案:
a.二氧化硫是污染性气体,高空排放会污染空气,处理不合理,故a错误;
b.可以利用吸收二氧化硫生成硫酸,用于制备硫酸,故b合理;
c.用纯碱溶液吸收二氧化硫可以制Na2SO4,故c合理;
d.用浓硫酸不能吸收二氧化硫,故d不合理;
故答案为:b、c.
(3)三价铁具有氧化性,能将碘离子氧化,S2O82-能将亚铁离子氧化,原理为:2Fe3++2I-=2Fe2++I2,S2O82-+2Fe2+=2SO42-+2Fe3+,
故答案为:2Fe3++2I-=2Fe2++I2;S2O82-+2Fe2+=2SO42-+2Fe3+;
(4)a.氧化铝是两性氧化物,能和强酸以及强碱反应,6H++AI2O3=3H2O+2Al3+,除去铝离子的反应是利用过量氢氧化钠溶液和铝离子反应生成四羟基合铝,
故答案为:Al3++4OH-=2H2O+AlO2-;
b.高锰酸钾溶液能氧化亚铁离子,使得高锰酸钾溶液褪色,故答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色.点评:
本题考点: 铁的化学性质;含硫物质的性质及综合应用;制备实验方案的设计.
考点点评: 本题是对金属的化学性质的考查,要求学生熟记教材知识,学以致用,综合性较强,难度中等.1年前查看全部
- 如图所示是一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,该工艺的原料的综合利用率较高.
如图所示是一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,该工艺的原料的综合利用率较高.
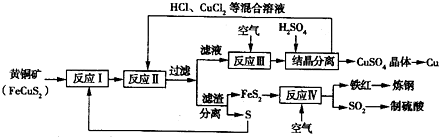
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl-═2[CuCl2]-+S
请回答下列问题:
(1)反应Ⅰ的产物为______(填化学式),反应Ⅲ的离子方程式为______.
(2)一定温度下,向反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是______.
(3)反应Ⅳ的主要反应为4FeS2+11O2═2Fe2O3+8SO2,其中氧化产物为______,当1.2g FeS2参与反应时,转移的电子数为______NA.
(4)某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe(SO4)3溶液完全反应后,用0.02000mol/L K2Cr2O7,标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL.已知:Cr2
+Fe2++H+→Cr3++Fe3++H2O(未配平)O 2−7
①SO2通入Fe(SO4)3溶液中,发生反应的离子方程式为______.
②反应Ⅳ所得气体中SO2的体积分数为______. gutangtang1年前1
gutangtang1年前1 -
 LY-christine 共回答了23个问题
LY-christine 共回答了23个问题 |采纳率95.7%解题思路:(1)由流程可知,黄铁矿分解生成的Fe、Cu均为+2价;反应Ⅲ中生成铜离子;
(2)相同条件下硫酸铜的溶解度小;
(3)反应中Fe、S的化合价均升高,n(FeS2)=[1.2g/120g/mol]=0.01mol,以此计算;
(4)①发生氧化还原反应生成硫酸亚铁;
②利用14H++Cr2O72-+6Fe2+═2Cr3++6Fe3++7H2O、SO2+2Fe3++2H2O=SO42-+2Fe2++4H+,可知,3SO2~Cr2O72-,以此计算.(1)由流程可知,黄铁矿分解生成的Fe、Cu均为+2价,则反应I的产物为FeS2、CuS,反应Ⅲ中生成铜离子,则离子反应为4CuCl2-+O2+4H+═4Cu2++8Cl-+2H2O,故答案为:FeS2、CuS;4CuCl2-+O2+4H+═4Cu2++8Cl-+2H2O;
(2)相同条件下硫酸铜的溶解度小,则该温度下,硫酸铜的溶解度小于氯化铜,所以向反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,
故答案为:该温度下,硫酸铜的溶解度小于氯化铜;
(3)反应中Fe、S的化合价均升高,氧化产物为Fe2O3、SO2,n(FeS2)=[1.2g/120g/mol]=0.01mol,
转移的电子为0.01mol×(3-2)+0.01mol×2×[4-(-1)]=0.11mol,个数为0.11NA个,
故答案为:Fe2O3、SO2;0.11;
(4)①发生氧化还原反应生成硫酸亚铁,离子反应为SO2+2Fe3++2H2O=SO42-+2Fe2++4H+,故答案为:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;
②利用14H++Cr2O72-+6Fe2+═2Cr3++6Fe3++7H2O、SO2+2Fe3++2H2O=SO42-+2Fe2++4H+,
可知,3SO2~Cr2O72-,
3 1
x 0.02mol/L×0.025L
解得x=0.0015mol,
反应Ⅳ所得气体中SO2的体积分数为[0.0015mol
0.28L/22.4L/mol]×100%=12.00%,故答案为:12.00%.点评:
本题考点: 离子方程式的书写;氧化还原反应;中和滴定.
考点点评: 本题以实际化工生产“黄铜矿的综合利用”为背景,考查了元素化合物知识,离子方程式和化学方程式的书写,题目更注重考查学生利用化学原理来解决实际问题的能力.1年前查看全部
- 火法炼铜首先要焙烧黄铜矿,主要涉及以下反应:
火法炼铜首先要焙烧黄铜矿,主要涉及以下反应:
①2CuFeS2+O2=Cu2S+2FeS+SO2
②Cu2S+O2=2Cu+SO2
下列说法正确的是( )
A.在反应①中:SO2既是氧化产物又是还原产物
B.在反应②中:Cu2S仅作还原剂,硫元素被氧化
C.在反应①中:每转移1.2 mol电子,有0.2 mol硫被氧化
D.在反应②中:每消耗1.0 molCu2S,有4.0 mol电子转移 二十四桥依旧1年前1
二十四桥依旧1年前1 -
 回头是岸吗 共回答了19个问题
回头是岸吗 共回答了19个问题 |采纳率100%解题思路:A、标注元素化合价变化,依据氧化还原反应的概念分析判断,还原剂被氧化生成氧化产物,氧化剂被还原生成氧化产物;
B、标注化合价分析判断;
C、依据化学方程式和电子守恒、化合价变化计算判断;
D、依据化学方程式和电子守恒、化合价变化计算判断;A、2CuFeS2+O2=Cu2S+2FeS+SO2中,Cu元素由+2价降低为+1价,S元素由-2价升高到+4价,氧气中O元素由0降低为-2价,则SO2既是氧化产物又是还原产物,故A正确;
B、Cu2S+O2=2Cu+SO2,铜元素化合价从+1价降到0价,氧元素化合价从 0价降低到-2价,硫元素化合价从-2价升高到+4价,则在反应②中:Cu2S即作氧化剂又做还原剂,硫元素被氧化,故B错误;
C、2CuFeS2+O2=Cu2S+2FeS+SO2中,硫元素化合价从-2价升高到+4价,所以生成1molSO2转移电子为6mol,被氧化的硫元素为1mol,每转移1.2 mol电子,有0.2 mol硫被氧化,故C正确;
D、Cu2S+O2=2Cu+SO2,铜元素化合价从+1价降到0价,氧元素化合价从 0价降低到-2价,硫元素化合价从-2价升高到+4价,消耗1molCu2S,电子转移6mol,故D错误;
故选AC.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查了氧化还原反应的概念应用,电子守恒的判断,化合价的升降分析判断概念的应用,转移电子的计算方法.1年前查看全部
- (1)以黄铜矿冶炼金属铜的过程中发生反应:2Cu 2 O+Cu 2 S 6Cu+SO 2 ↑,反应的氧化剂是______
(1)以黄铜矿冶炼金属铜的过程中发生反应:2Cu 2 O+Cu 2 S  6Cu+SO 2 ↑,反应的氧化剂是_________。
6Cu+SO 2 ↑,反应的氧化剂是_________。
(2)黄铜矿熔炼后得到的粗铜含少量Fe、Zn、Ag、Au等金属杂质,需进一步采用电解法精制。在电解精炼铜时,电解液中除了硫酸铜外,往往再加入一些硫酸,其作用是_____________________。
(3)在精炼铜的过程中,电解液中c(Cu 2+ )逐渐下降,c(Fe 2+ )、c(Zn 2+ )会逐渐增大,所以需定时除去其中的Fe 2+ 、Zn 2+ 。下表为几种物质的溶度积。
某同学设计了如下除杂方案 
试剂a是__________,其目的是______________________;根据溶度积该方案能够除去的杂质金属阳离子是______。操作①用到的玻璃仪器是____________。
(4)工业上通常用FeS除去废水中的Cu 2+ ,写出该沉淀转化离子方程式__________________。 月冷1年前1
月冷1年前1 -
 shuiaqi 共回答了17个问题
shuiaqi 共回答了17个问题 |采纳率94.1%(1)Cu 2 O、Cu 2 S
(2)增强电解液的导电性,抑制Cu 2+ 的水解
(3)H 2 O 2 ;将Fe 2+ 氧化成Fe 3+ ;Fe 2+ ;漏斗、烧杯、玻璃棒
(4)Cu 2+ (aq)+FeS(s)=CuS(s)+Fe 2+ (aq)1年前查看全部
- 黄铜矿(主要成分CuFeS2)是提取铜的主要原料. 问:已知2 CuFeS2+4O2===Cu 2S+3S O2+2Fe
黄铜矿(主要成分CuFeS2)是提取铜的主要原料. 问:已知2 CuFeS2+4O2===Cu 2S+3S O2+2Fe O 产物Cu S2在1
200度高温下继续反应:
2Cu S2+3 O2==== 2Cu2 O+2 S O2
2Cu2 O+ Cu2 S====6 Cu+ S O2
假设各步反应都完全,完成下列计算:
①由6mol CuFeS2生成6mol Cu,需消耗O2的物质的量是多少?
② 6 mol CuFeS2和14.25 mol O2反应,理论上可得到多少摩尔铜?
③ 6 mol CuFeS2和15.75 mol O2反应,理论上可得到多少摩尔铜? 134724106101年前1
134724106101年前1 -
 舞之魂200 共回答了21个问题
舞之魂200 共回答了21个问题 |采纳率85.7%①由第一个得 6mol和12mol O2生成3mol Cu2S6CuFeS2+12O2===3Cu2S+9SO2+6FeO2mol Cu2S和3mol O2生成2mol Cu2O2Cu2S+3O2===2Cu2O+2SO22mol Cu2O和1mol Cu2S最终生成6mol Cu2Cu2O+Cu2S===6Cu+SO2所以整个过程中共消耗O2...1年前查看全部
- 黄铜矿冶炼铜怎么配平 CuFeS2+O2=高温Cu+SO2+FeO+Fe2O3
 greatgrowing1年前2
greatgrowing1年前2 -
 zjh666zjh 共回答了16个问题
zjh666zjh 共回答了16个问题 |采纳率93.8%这个方程肯定不对
没办法配平
高温下有O2
怎么可能生成单质Cu和有还原性的FeO
下面的这个还差不多
2CuFeS2 + O2 = Cu2S + 2FeS + SO21年前查看全部
- 工业上用黄铜矿冶炼铜及对炉渣综合利用的一种工艺流程如下:
工业上用黄铜矿冶炼铜及对炉渣综合利用的一种工艺流程如下:

(1)冶炼过程中得到Cu 2 O和Cu的混合物称为“泡铜”,其与金属A1在高温条件下混合反应可得粗铜,反应化学方程式为________。粗铜精炼时应将粗铜连接在直流电源的____极,可在____极得到纯度较高的精铜。
(2)传统炼铜的方法主要是火法炼铜,其主要反应为: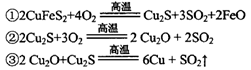
每生成1 mol Cu,共消耗____mol O 2 。反应③中的氧化剂是____。
(3)炼铜产生的炉渣(含 )可制备Fe 2 O 3 。根据流程回答下列问题:
)可制备Fe 2 O 3 。根据流程回答下列问题:
①加入适量NaClO溶液的目的是_______ (用离子方程式表示)。
②除去Al 3 + 的离子方程式是____。
③选用提供的试剂,设计实验验证炉渣中含有FeO。提供的试剂有:稀盐酸、稀硫酸、KSCN溶液、KMnO 4 溶液、NaOH溶液、碘水。所选试剂是____。实验设计:________。 我是谁bb1年前1
我是谁bb1年前1 -
 jxsddsy 共回答了18个问题
jxsddsy 共回答了18个问题 |采纳率94.4%1年前查看全部
- 黄铜矿CuFeS2可用于冶炼铜,冶炼原理为:2CuFeS2+2SiO2+5O2=2Cu+2FeSiO3+4SO2.
黄铜矿CuFeS2可用于冶炼铜,冶炼原理为:2CuFeS2+2SiO2+5O2=2Cu+2FeSiO3+4SO2.
(1)黄铜矿冶炼铜产生的炉渣中主要含Fe2O3、FeSiO3、SiO2、Al2O3等,请完成以下验证炉渣中含有+2价的铁的探究过程中的有关问题:
仅限选择的试剂有:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水
①应选用试剂为______.
②有关的实验现象为______.
(2)据报道,有一种叫ThibacillusFerroxidans的细菌在氧气存在下,酸性溶液中,将黄铜矿CuFeS2氧化成硫酸盐:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O.利用反应后的溶液,按如图所示流程可制备胆矾(CuSO4•5H2O):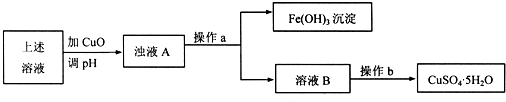
①操作a的名称是______,操作b的操作方法是______.
②检验溶液B中Fe3+是否被除尽的试剂是______,证明Fe3+已被除尽的现象是______.
③在实验室中,设计两个原理不同的方案,从溶液B中提炼金属铜(要求:一种方案只用一个反应来完成).写出两种方案的化学方程式:
方案一:______;
方案二:2CuSO4+2H2O
2Cu+O2↑+2H2SO4通电 .2CuSO4+2H2O.
2Cu+O2↑+2H2SO4通电 . 带着我飞1年前1
带着我飞1年前1 -
 cmwlg 共回答了22个问题
cmwlg 共回答了22个问题 |采纳率86.4%解题思路:(1)①亚铁离子能被高锰酸钾溶液氧化,高锰酸钾溶液被亚铁离子还原溶液褪色;
②选择硫酸和高锰酸钾溶液,可以和亚铁离子反应溶液褪色;
(2)①依据流程分析,操作a是得到氢氧化铁沉淀和溶液B,说明是过滤操作;操作b是溶液中得到晶体的方法,利用浓缩溶液结晶析出;
②依据铁离子的性质进行验证,铁离子遇到硫氰酸钾溶液变红色,若无红色出现这么铁离子除净;
③溶液B为硫酸铜溶液,可以加入铁粉置换铜得到,也可以通过电解硫酸铜溶液得到;(1)①高锰酸钾溶液酸性溶液中能氧化亚铁离子,使得高锰酸钾溶液褪色,
故答案为:①稀硫酸、KMnO4溶液;②稀硫酸浸取炉渣所得溶液使KMnO4 溶液褪色;
(2)①流程中操作a是通过过滤的方法得到氢氧化铁沉淀和滤液B,滤液B是硫酸铜溶液,操作b是溶液中得到CuSO4•5H2O晶体的实验方法,溶液中得到溶质晶体可以加热蒸发浓缩,冷却结晶得到;
故答案为:过滤;蒸发浓缩,冷却结晶;
②检验溶液B中Fe3+是否被除尽的试剂是KSCN溶液,加入KSCN溶液若变红证明含有铁离子,若加入后溶液不变红证明不含铁离子;
故答案为:KSCN溶液;溶液不变红;
③硫酸铜溶液得到金属铜的方法,可以加入铁粉置换铜反应的化学方程式为:CuSO4+Fe=FeSO4+Cu;也可以惰性电极通电电解硫酸铜溶液,反应的化学方程式为:2CuSO4+2H2O
通电
.
2Cu+O2↑+2H2SO4;
故答案为:CuSO4+Fe=FeSO4+Cu;2CuSO4+2H2O
通电
.
2Cu+O2↑+2H2SO4;点评:
本题考点: 性质实验方案的设计;制备实验方案的设计.
考点点评: 本题考查物质性质的实验设计和反应现象判断,实验流程的正确判断是解题关键,题目难度中等.1年前查看全部
- (2014•陕西一模)黄铜矿(CuFeS2)是炼钢和炼铜的主要原料.在高温下灼烧生成二氧化二铁和氧化亚铜.三氧化二铁和氧
(2014•陕西一模)黄铜矿(CuFeS2)是炼钢和炼铜的主要原料.在高温下灼烧生成二氧化二铁和氧化亚铜.三氧化二铁和氧化亚铜都是红色粉末.常用作颜料.某学校化学兴趣小组通过实验探究一红色粉末是Fe2O3、Cu2O或两者的混合物.探究过程如下:
查阅资料:Cu2O是一种碱性氧化物.溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO.
提出假设:
假设1:红色粉末是Fe2O3.
假设2:红色粉末是Cu2O.
假设3:红色粉末是Fe2O3和Cu2O的混合物.
设计探究实验:
取少量粉末放入足量稀硫酸中.在所得溶液中再滴加KSCN试剂.
(1)若假设1成立,则实验现象是______.
(2)滴加KSCN试剂后溶液不变红色.某同学认为原同体粉末中一定不含三氧化二铁.你认为这种说法合
理吗?______.简述你的理由(不需写出反应的化学方程式):______.
(3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色.则证明原同体粉末是______,写出发生的氧化还原反应的离子方程式:______.
探究延伸:
(4)经实验分析.确定红色粉末为Fe2O3和Cu2O的混合物.实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4•5H2O).经阅资料得知.在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表:
实验小组设汁如图实验方案:物质 Cu(OH)2 Fe(OH)2 Fe(OH)3 开始沉淀时的pH 6.0 7.5 1.4 完全沉淀时的pH 13 14 3.7 
①试剂Ⅰ为______.试剂2为______.(填字母)
A.氯水B.H2O2C.NaOH D.Cu2(OH)2CO3
②同体X的化学式为______.
③操作Ⅱ为______. 雪兰狐1年前1
雪兰狐1年前1 -
 seth1023 共回答了26个问题
seth1023 共回答了26个问题 |采纳率84.6%解题思路:(1)依据假设1为氧化铁,和实验工厂分析,固体溶解后生成硫酸铁,遇到硫氰酸钾会发生反应生成血红色溶液;
(2)滴加KSCN试剂后溶液不变红色,说明溶液中无铁离子,可能是氧化亚铜在酸中发生氧化还原反应生成氧化铜和铜,生成的铜能把铁离子还原为亚铁离子,使溶液遇到硫氰酸钾不变红色;
(3)固体完全溶解,无固体存在,说明固体含有氧化铁和氧化亚铜;反应生成的铜会和铁离子全部反应;
(4)①红色粉末为Fe2O3和Cu2O的混合物溶于硫酸后氧化亚铜反应生成的铜会还原铁离子为亚铁离子,加入氧化剂过氧化氢氧化亚铁离子为铁离子,调节溶液PH使铁离子全部沉淀;
②X推断为氢氧化铁沉淀;
③操作Ⅰ是溶液中得到溶质结晶水合物;是通过蒸发浓缩冷却结晶,过滤洗涤干燥得到晶体;(1)取少量粉末放入足量稀硫酸中.在所得溶液中再滴加KSCN试剂,若假设1成立,红色粉末是Fe2O3,则实验现象是固体完全溶解,溶液呈血红色;
故答案为:固体完全溶解,溶液呈血红色;
(2)滴加KSCN试剂后溶液不变红色,说明溶液中无铁离子,可能是氧化亚铜在酸中发生氧化还原反应生成氧化铜和铜,生成的铜能把铁离子还原为亚铁离子,使溶液遇到硫氰酸钾不变红色,所以滴加KSCN试剂后溶液不变红色,不能说明原混合物不含氧化铁;
故答案为:不合理;当原固体粉末为Fe2O3和Cu2O的混合物时,加入稀H2SO4后产生的Fe3+与Cu反应生成Fe2+,滴加KSCN溶液后也可能不变红色;
(3)固体完全溶解,无固体存在,说明固体含有氧化铁和氧化亚铜;反应生成的铜会和铁离子全部反应,反应的离子方程式为:Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+;
故答案为:Fe2O3和Cu2O;Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+;
(4)①红色粉末为Fe2O3和Cu2O的混合物溶于硫酸后氧化亚铜反应生成的铜会还原铁离子为亚铁离子,加入氧化剂过氧化氢氧化亚铁离子为铁离子,调节溶液PH使铁离子全部沉淀,为不引入杂质需要加入氧化铜或碱式碳酸铜调节溶液PH,AC会引入新的杂质;
故答案为:B;D;
②流程分析判断固体X为氢氧化铁沉淀;
故答案为:Fe(OH)3;
③操作Ⅰ是溶液中得到溶质结晶水合物;是通过蒸发浓缩冷却结晶,过滤洗涤干燥得到晶体;
故答案为:蒸发浓缩、冷却结晶;点评:
本题考点: 探究物质的组成或测量物质的含量.
考点点评: 本题考查了实验探究物质组成和性质的实验分析,物质的性质和转化关系,掌握基础,细心审题是解题关键,题目难度中等.1年前查看全部
- 金属铜的提炼多从黄铜矿开始.黄铜矿的焙烧过程中主要反应之一的化学方程式为:2CuFeS 2 +O 2 =
金属铜的提炼多从黄铜矿开始.黄铜矿的焙烧过程中主要反应之一的化学方程式为:2CuFeS 2 +O 2 = 
+2FeS+SO 2
下列说法不正确的是( )A.方框中的物质应为Cu 2 S B.O 2 只作氧化剂 C.SO 2 既是氧化产物又是还原产物 D.若有1molSO 2 生成,则反应中有4mol电子转移  kk1badq1年前1
kk1badq1年前1 -
 zvzv27 共回答了23个问题
zvzv27 共回答了23个问题 |采纳率82.6%A.由质量守恒定律可知,Cu、S原子守恒,则方框中的物质应为Cu 2 S,故A正确;
B.反应中O元素的化合价降低,则O 2 只作氧化剂,故B正确;
C.S元素由-1价升高到+4价,O元素0价降低为-2价,则SO 2 既是氧化产物又是还原产物,故C正确;
D.若有1molSO 2 生成,则反应中转移的电子为1mol×(4-(-2))=6mol,故D错误;
故选D.1年前查看全部
- (2012•润州区二模)以黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)为原料炼铜的方法分为高温炼铜和湿法炼铜两种
(2012•润州区二模)以黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)为原料炼铜的方法分为高温炼铜和湿法炼铜两种.近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐,某工厂运用该原理生产铜和绿矾(FeSO4的晶体,含结晶水).

回答下列问题:
(1)写出反应Ⅰ的化学反应方程式:______;
(2)欲从溶液中获得绿矾晶体,分离“操作2”应为蒸发浓缩、______、过滤. jackingyu1年前1
jackingyu1年前1 -
 没有dd 共回答了26个问题
没有dd 共回答了26个问题 |采纳率88.5%解题思路:(1)根据化学方程式的书写方法考虑;(2)根据固体溶质从溶液中结晶析出的方法是:蒸发溶剂,降温结晶,再过滤.(1)反应Ⅰ中的反应物是CuFeS2、O2、H2SO4三种物质,生成物是硫酸铁、硫酸铜和水,根据奇偶法配平,所以方程式是:4CuFeS2+17O2+2H2SO4═2Fe2(SO4)3+4CuSO4+2H2O;
(2)获得绿矾晶体时先蒸发浓缩,因为硫酸铁的溶解度随温度的升高而增大,所以降温溶解度减小,会析出晶体,最后过滤即可.
故答案为:(1)4CuFeS2+17O2+2H2SO4═2Fe2(SO4)3+4CuSO4+2H2O;(2)降温结晶.点评:
本题考点: 物质的相互转化和制备;结晶的原理、方法及其应用;金属的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题关键是要知道方程式的书写方法,熟悉溶液中溶质结晶析出的方法.1年前查看全部
- 由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:
(1)在反射炉中,把铜精矿砂和石英砂混合加热到l000℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物.该过程中两个主要反应的化学方程式分别是__________、__________,反射炉内生成炉渣的主要成分是__________;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%.转炉中,将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼.冰铜中的Cu2S被氧化为Cu2O.生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是__________、__________. 品牌小戴1年前0
品牌小戴1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:(1)气
工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:(1)气
手机看不了答案,求帮搜标题,一共五小题的,
顺便再搜下 下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示 庥琦1年前1
庥琦1年前1 -
 wending 共回答了23个问题
wending 共回答了23个问题 |采纳率100%第一题 C
第二题 Fe3+;加NaOH,有白色沉淀,沉淀颜色逐渐变深,最终变为红褐色.
第三题 啊氧化亚铜同铝反应的化学方程式,自己写吧,应该会吧.
第四题 D
第五提 氧气在酸的作用下变为水,自己写吧.
为了取得好成绩建议换部好手机1年前查看全部
- 黄铜矿(CuFeS 2 )是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物.
黄铜矿(CuFeS 2 )是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物.
(1)冶炼铜的反应为:8CuFeS 2 +21O 2 8Cu+4FeO+2Fe 2 O 3 +16SO 2 若CuFeS 2 中Fe的化合价为+2,反应中被还原的元素是________(填元素符号).
8Cu+4FeO+2Fe 2 O 3 +16SO 2 若CuFeS 2 中Fe的化合价为+2,反应中被还原的元素是________(填元素符号).
(2)上述冶炼过程产生大量SO 2 .下列处理方案中合理的是________(填代号).
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na 2 SO 3
d.用浓硫酸吸收
(3)过二硫酸钾(K 2 S 2 O 8 )具有强氧化性,可将I - 氧化为I 2 :S 2 O 8 2- +2I - ===2SO 4 2- +I 2 通过改变反应途径,Fe 3+ 、Fe 2+ 均可催化上述反应.试用离子方程式表示Fe 3+ 对上述反应催化的过程.________、________(不必配平)
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe 2 O 3 、FeO、SiO 2 、Al 2 O 3 )可制备Fe 2 O 3 .方法为:
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe 2 O 3 .
据以上信息回答下列问题:
a.除去Al 3+ 的离子方程式是________.
b.选用提供的试剂,设计实验验证炉渣中含有FeO. 提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO 4 溶液 NaOH溶液 碘水所选试剂为________.证明炉渣中含有FeO的实验现象为____________________________________. 观晨听宇1年前1
观晨听宇1年前1 -
 linvv00 共回答了27个问题
linvv00 共回答了27个问题 |采纳率81.5%(1)Cu、O (2)b、c (3)2Fe 3+ +2I - ===2Fe 2+ +I 2 ;S 2 O 8 2- +2Fe 2+ ===2SO 4 2- +2Fe 3+ (4)a.Al 3+ +4OH - ===AlO 2 - +2H 2 O;b.稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KM...1年前查看全部
- (2011•南京一模)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之,还可以制备硫以及铁的化合物.
(2011•南京一模)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之,还可以制备硫以及铁的化合物.
(1)近年来,湿法炼钢有了新进展.某工厂以一种叫Thibacillus ferroxidans的细菌为基体生产 铜和绿矾的工艺流程如下:
(1)试剂a为______,试剂b为______.(写名称)
(2)反应l的化学方程式为4CuFeS2+2H2SO4+17O2
4CuSO4+2Fe2(SO4)3+2H2O细菌 .4CuFeS2+2H2SO4+17O2
4CuSO4+2Fe2(SO4)3+2H2O细菌 .
(Ⅱ)以CuFeS2精矿为原料在沸腾炉中和02(空气)反应,生成物冷却后经溶解、除铁、结晶.得到 CuS04•5H2O.沸腾炉的温度与生成物主要成分的水溶性和酸溶性实验结果如图.
(1)沸腾炉生成物中的含铁物质主要成分为______.
(2)为获得最高的水溶性Cu(%),沸腾炉的温度应控制在______℃左右,高于该温度生成物中的水溶性 Cu(%)下降,可能原因是______. 予禾1年前1
予禾1年前1 -
 谁与争锋669 共回答了19个问题
谁与争锋669 共回答了19个问题 |采纳率94.7%解题思路:(Ⅰ)(1)得到的滤渣2是将三价铁沉淀下来的难溶物,可用硫酸来溶解,金属铁可以和三价铁化合为亚铁离子;加入稀硫酸溶解氢氧化铁生成硫酸铁,加入铁粉和硫酸铁反应生成硫酸亚铁;
(2)依据流程分析可知反应物为黄铜矿中加入硫酸和氧气反应硫酸铜、硫酸铁和水;
(Ⅱ)(1)从整个过程来看,CuFeS2最终变为Cu、FeO和SO2,即2CuFeS2+5O2=2Cu+4SO2+2FeO;
(2)据图象分析可知,600°C时水溶性铜最高;水溶性铜化合物为CuSO4•5H2O,酸溶性铜化合物为CuO,温度较高时,CuSO4•5H2O可分解生成CuO,则在600℃以上时水溶性铜化合物含量减少.(Ⅰ) (1)得到的滤渣2是将三价铁沉淀下来的难溶物,可用硫酸来溶解,再加入金属铁可以和三价铁化合为亚铁离子,而又不会引进杂质离子,故答案为:硫酸、过量的铁粉,故答案为:稀硫酸;铁粉;
(2)反应1的反应可以依据流程分析可知反应物为黄铜矿中加入硫酸和氧气反应硫酸铜、硫酸铁和水,反应的化学方程式为:4CuFeS2+2H2SO4+17O2
细菌
.
4CuSO4+2Fe2(SO4)3+2H2O,故答案为:4CuFeS2+2H2SO4+17O2
细菌
.
4CuSO4+2Fe2(SO4)3+2H2O;
(Ⅱ) (1)依据流程图,从整个过程来看,CuFeS2最终变为Cu、FeO和SO2,即2CuFeS2+5O2=2Cu+4SO2+2FeO;沸腾炉生成物中的含铁物质主要成分为铁的氧化物,
故答案为:铁的氧化物;
(2)CuFeS2与O2反应放热,依据图象分析可知,600°C时水溶性铜最高;水溶性铜化合物为CuSO4•5H2O,酸溶性铜化合物为CuO,温度较高时,CuSO4•5H2O可分解生成CuO,则在600℃以上时水溶性铜化合物含量减少,
故答案为:600;生成的CuSO4发生了分解生成酸溶性铜化合物.点评:
本题考点: 制备实验方案的设计;探究物质的组成或测量物质的含量.
考点点评: 本题考查考查较为综合,涉及物质的制备、检验和性质实验设计等问题,侧重于考查学生综合运用化学知识的能力,为高考常见题型,难度中等.1年前查看全部
- 取12.5克黄铜矿样品,经测定含3.6gliu(杂质中不含liu),矿样中CuFeS2含量为多少?
 蒲公英种子1年前1
蒲公英种子1年前1 -
 八面妖精 共回答了18个问题
八面妖精 共回答了18个问题 |采纳率94.4%因为杂质中不含中不含S; CuFeS2~2S 184 64 x g 3.6g x=10.35g CuFeS2%=10.35g/12.5g=82.8%1年前查看全部
- 以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
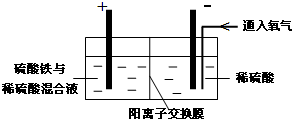 以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
Ⅰ.将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎
Ⅱ.采用如下装置进行电化学浸出实验将精选黄铜矿粉加入电解槽阳极区,恒速搅拌,使矿粉溶解.在阴极区通入氧气,并加入少量催化剂.
Ⅲ.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应:2RH(有机相)+Cu2+(水相)⇌R2Cu(有机相)+2H+(水相),分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生.
Ⅳ.电解硫酸铜溶液制得金属铜.
(1)黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应:
CuFeS2+4H+=Cu2++Fe2++2H2S
2Fe3++H2S=2Fe2++S↓+2H+
①阳极区硫酸铁的主要作用是______.
②电解过程中,阳极区Fe3+的浓度基本保持不变,原因是______.
(2)阴极区,电极上开始时有大量气泡产生,后有固体析出,一段时间后固体溶解.写出上述现象对应的反应式______.
(3)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是______;加入有机萃取剂的目的是______.
(4)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是______.
(5)步骤Ⅳ,若电解200mL 0.5mol/L的CuSO4溶液,生成铜3.2g,此时溶液中离子浓度由大到小的顺序是______. san2331年前1
san2331年前1 -
 jacksonlee 共回答了18个问题
jacksonlee 共回答了18个问题 |采纳率77.8%解题思路:(1)①硫化氢有毒,直接排放会污染空气;
②Fe3+被还原Fe2+,Fe2+在阳极放电又生成Fe3+;
(2)首先氢离子放电生成氢气,反应一段时间,铜离子放电生成铜,再通入氧气的条件下Cu、氧气、硫酸反应生成硫酸铜;
(3)有机相和水相不互溶,分离有机相和水相通常利用分液的方法,使用的仪器为分液漏斗;
加入有机萃取剂富集Cu2+,分离Cu2+与其它金属阳离子;
(4)增大氢离子浓度,根据平衡移动原理分析;
(5)电解uSO4溶液,发生反应2CuSO4+2H2O
2Cu+2H2SO4+O2↑,200mL 0.5mol/L的CuSO4溶液中n(CuSO4)=0.2L×0.5mol/L=0.1mol,生成铜3.2g,物质的量为[3.2g/64g/mol]=0.05mol,故生成H2SO40.1mol,溶液中CuSO4为0.1mol-0.05mol=0.05mol,电解后的溶液为CuSO4、H2SO4混合溶液,溶液中存在硫酸的电离、铜离子水解、水的电离等,据此判断.通电 .(1)①由发生的反应可知,Fe3+氧化吸收硫化氢气体,防止环境污染,故答案为:吸收硫化氢气体,防止环境污染;②Fe3+被还原Fe2+,Fe2+在阳极放电Fe2+-e-=Fe3+,又生成Fe3+,电解过程中,阳极区Fe3+的浓度基本保持不...
点评:
本题考点: 电解原理.
考点点评: 本题考查电解原理、对工艺原理的理解、常用化学用语、离子浓度比较等,题目综合性较大,是对所学知识的综合考查,需要学生具有知识的基础与分析、解决问题的能力,难度中等,(5)中注意根据物质的量判断离子大小.1年前查看全部
- 黄铜矿(CuFeS 2 )是制取铜及其化合物的主要原料之一.工业上以黄铜矿为原料,采用火法熔炼工艺生产铜时发生如下反应:
黄铜矿(CuFeS 2 )是制取铜及其化合物的主要原料之一.工业上以黄铜矿为原料,采用火法熔炼工艺生产铜时发生如下反应:2Cu 2 O+Cu 2 S
6Cu+SO 2 ↑.高温 .
Ⅰ.反应产生的SO 2 是大气污染物,可用NaOH溶液吸收得到NaHSO 3 .常温下,0.1mol•L -1 NaHSO 3 溶液的pH小于7,则溶液中c(H 2 SO 3 )______c(SO 3 2- )(填“>”、“=”或“<”),原因是______.
Ⅱ.黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制.
(1)请完成下列粗铜电解得到精铜的原理:电解池中______作阴极.
(2)精炼铜产生的废液中含有Fe 2+ 、Fe 3+ 、Cu 2+ 等金属阳离子.已知25℃时如下数据,请完成下列问题:
在25℃下,向浓度均为0.1mol•L -1 的FeCl 2 和CuCl 2 混合溶液中逐滴加入氨水,先生成______沉淀(填化学式),生成该沉淀的离子方程式为______.物质 Fe(OH) 2 Cu(OH) 2 Fe(OH) 3 Ksp 8.0×10 -16 2.2× -20 4.0×10 -38  里应外合21年前1
里应外合21年前1 -
 风雨相随哦 共回答了18个问题
风雨相随哦 共回答了18个问题 |采纳率94.4%Ⅰ.已知NaHSO 3 中的HSO 3 - 既能电离又能水HSO 3 - ⇌H + +SO 3 2- 电离显酸性,HSO 3 - +H 2 O⇌H 2 SO 3 +OH - 水解显碱性;常温下,0.1mol•L -1 NaHSO 3 溶液的pH小于7,
说明电离大于水解,故:c(SO 3 2- )>c(H 2 SO 3 ),
故答案为:<;NaHSO 3 溶液中HSO 3 - 电离程度大于水解程度;
Ⅱ.(1)精炼粗同时,粗铜为阳极,纯铜为阴极,故答案为:纯铜;
(2)Cu(OH) 2 因溶度积较小,则滴加氨水时首先生成Cu(OH) 2 沉淀,反应的离子方程式为Cu 2+ +2NH 3 •H 2 O=Cu(OH) 2 ↓+2NH 4 + ,
故答案为:Cu(OH) 2 ;Cu 2+ +2NH 3 •H 2 O=Cu(OH) 2 ↓+2NH 4 + .1年前查看全部
- (2013•德州模拟)黄铜矿的主要成分是CuFeS2(硫元素一2价,铁元素+2价).是工业炼铜的主要原料.已知黄铜矿在空
(2013•德州模拟)黄铜矿的主要成分是CuFeS2(硫元素一2价,铁元素+2价).是工业炼铜的主要原料.已知黄铜矿在空气中焙烧生成cu、FeS和S02,FeS+2Hcl=FeCl+H2S.H2S是一种剧毒气体.某科研小组设计以黄铜矿为原料涮取单质铜和氯化铁晶体(FeCl3•6H2O)的流程如下:

(1)92gCuFeS2在空气中焙烧生成Cu、FeS和S02转移电子的物质的量为______.
(2)请简述检验气体Ⅰ的操作步骤.
(3)在实验室中,欲用38%(密度为1.18g.mL-1)的盐酸配制30%的盐酸,需要的玻璃仪器主要有______.
(4)气体Ⅲ最好选用______(填写序号),其主要作用是______;
A.02B.H2C.Cl2D.N2
欲选用下列仪器在实验室中制取纯净干燥的该气体.
装置A中发生反应的离子方程式为MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O△ .MnO2+4H++2Cl-.
Mn2++Cl2↑+2H2O△ .
选用合适装置导管口的连接顺序为a接______.图中仪器G的名称是______;在使用该仪器时,应首先______. 景萱1年前1
景萱1年前1 -
 妮妮1111 共回答了16个问题
妮妮1111 共回答了16个问题 |采纳率93.8%解题思路:(1)根据n=[m/M]计算92gCuFeS2的物质的量,根据原子守恒计算Cu、FeS和SO2的物质的量,反应中只有生成SO2的硫元素化合价升高,由-2价升高为+4价,据此计算转移电子物质的量;
(2)由工艺流程可知,焙烧产生的气体Ⅰ为SO2,利用品红溶液进行检验;
(3)用38%(密度为1.18g.mL-1)的盐酸配制30%的盐酸,用量筒量取需要浓盐酸与水的体积,在烧杯中稀释,丙用玻璃棒搅拌;
(4)由工艺流程可知,过滤得到的滤液中主要为FeCl2,产品为FeCl3•6H2O,故通入的气体将Fe2+氧化为Fe3+,且不引入杂质,应为氯气最好;
制备干燥纯净的氯气:由发生装置可知,应是二氧化锰与浓盐酸加热制备,生成的氯气中含有HCl、水蒸气,利用饱和氯化钠溶液吸收氯气中的氯化氢气体;再利用浓硫酸除去氯气中的水蒸气,最后用氢氧化钠溶液吸收尾气中的氯气,连接时注意洗气与干燥装置导气管需要长进短出、收集装置应长进短出;
G是分液漏斗,使用之前应检查是否漏水.(1)92gCuFeS2的物质的量=[92g/184g/mol]=0.5mol,根据原子守恒可知生成Cu、FeS的物质的量分别为0.5mol、0.5mol,由硫原子守恒可知SO2的物质的量=0.5mol×2-0.5mol=0.5mol,反应中只有生成SO2的硫元素化合价升高,由-2价升高为+4价,故转移电子物质的量=0.5mol×[4-(-2)]=3mol,
故答案为:3mol;
(2)由工艺流程可知,焙烧产生的气体Ⅰ为SO2,利用品红溶液进行检验,具体操作为:收集适量气体Ⅰ通入品红溶液中,品红溶液褪色,加热溶液恢复红色,
故答案为:收集适量气体Ⅰ通入品红溶液中,品红溶液褪色,加热溶液恢复红色;
(3)用38%(密度为1.18g.mL-1)的盐酸配制30%的盐酸,用量筒量取需要浓盐酸与水的体积,在烧杯中稀释,丙用玻璃棒搅拌,故需要的仪器有:量筒、玻璃棒、烧杯,
故答案为:量筒、玻璃棒、烧杯;
(4)由工艺流程可知,过滤得到的滤液中主要为FeCl2,产品为FeCl3•6H2O,故通入的气体将Fe2+氧化为Fe3+,且不引入杂质,应为氯气最好;
制备干燥纯净的氯气:由发生装置可知,应是二氧化锰与浓盐酸加热制备,反应离子方程式为:MnO2+4H++2Cl-
△
.
Mn2++Cl2↑+2H2O;
生成的氯气中含有HCl、水蒸气,利用饱和氯化钠溶液吸收氯气中的氯化氢气体;再利用浓硫酸除去氯气中的水蒸气,最后用氢氧化钠溶液吸收尾气中的氯气,连接时注意洗气与干燥装置导气管需要长进短出、收集装置应长进短出,故连接顺序为aghefb;
G是分液漏斗,使用之前应检查是否漏水,
故答案为:C;将Fe2+氧化为Fe3+;MnO2+4H++2Cl-
△
.
Mn2++Cl2↑+2H2O;ghefb;分液漏斗;检查是否漏水.点评:
本题考点: 制备实验方案的设计;气体发生装置.
考点点评: 本题考查氧化还原反应、元素化合物性质、实验方案设计、氯气实验室制备等,侧重对化学基本操作与技能的考查,是对学生综合能力的考查,需要学生具备扎实的基础与灵活运用能力,题目难度中等.1年前查看全部
- 某同学为测定黄铜矿中硫的含量(主要成分为CuFeS 2 ,杂质不含硫)设计了如下实验:称取0.2g研细的黄铜矿样品,高温
某同学为测定黄铜矿中硫的含量(主要成分为CuFeS 2 ,杂质不含硫)设计了如下实验:称取0.2g研细的黄铜矿样品,高温下和氧气充分反应,产物有氧化铜、二氧化硫及某种铁的氧化物。
请回答下列问题:
(1)装置A中盛水的仪器名称是________,装置B的作用是_______
(2)固体X是淡黄色物质,其成分可能是_______,装置D中发生反应的化学方程式为________________
(3)反应后C中残留的固体呈黑色,某同学推测生成的铁的氧化物可能是FeO或Fe 3 O 4 中的一种。请设计实验,检验其成分____________________
(4)实验后将D中的溶液分为四等份转移至四个锥形瓶中,用0.4 mol/L的NaOH标准溶液滴定,达到终点时,消耗标准溶液的平均值为25. 00 mL,则该黄铜矿中硫的含量为________。 feelblue5201年前1
feelblue5201年前1 -
 oklawa 共回答了21个问题
oklawa 共回答了21个问题 |采纳率85.7%(1)分液漏斗;干燥氧气
(2)Na 2 O 2 ;SO 2 +H 2 O 2 =H 2 SO 4
(3)取少量黑色固体,溶于适量稀硫酸,向溶液中滴加KSCN溶液,若溶液呈红色,则铁的氧化物为
Fe 3 O 4 ,否则为FeO
(4)32%1年前查看全部
- 工业上用黄铜矿(CuFeS 工业上用黄铜矿(CuFeS 2 )炼铜的后期主要发生如下两个反应(假设两反应进行得很完全):
工业上用黄铜矿(CuFeS
工业上用黄铜矿(CuFeS 2 )炼铜的后期主要发生如下两个反应(假设两反应进行得很完全):2Cu 2 S+3O 2 =2Cu 2 O+2SO 2 、2Cu 2 O+Cu 2 S=6Cu+SO 2 根据以上两个化学反应,判断下列说法不正确的是 [ ] A.氧化剂与还原剂的质量之比为17:15
B.工业炼铜时应注意控制向炉内通入氧气的量
C.若制取3molCu,转移电子物质的量为9 mol
D.工业炼铜可以和硫酸工业联合建厂 gyang1140011年前1
gyang1140011年前1 -
 ee的那首歌 共回答了17个问题
ee的那首歌 共回答了17个问题 |采纳率88.2%A1年前查看全部
- (2014•陕西三模)火法炼铜首先要焙烧黄铜矿,反应为:2CuFeS2+O2→Cu2S+2FeS+SO2则下列说法正确的
(2014•陕西三模)火法炼铜首先要焙烧黄铜矿,反应为:2CuFeS2+O2→Cu2S+2FeS+SO2则下列说法正确的是( )
A.CuFeS2仅作还原剂,硫元素被氧化
B.每生成1mol Cu2S,有4 mol硫被氧化
C.SO2只是氧化产物,FeS只是还原产物
D.每转移1.2 mol电子,有0.2 mol硫被氧化 mingmei351年前1
mingmei351年前1 -
 qq海角1234 共回答了18个问题
qq海角1234 共回答了18个问题 |采纳率100%解题思路:反应2CuFeS2+O2=Cu2S+2FeS+SO2中,Cu元素由+2价降低为+1价,S元素由-2价升高到+4价,氧气中O元素由0降低为-2价,以此解答该题.A.Cu元素由+2价降低为+1价,S元素由-2价升高到+4价,CuFeS2既是氧化剂又是还原剂,故A错误;
B.由方程式可知,每生成1mol Cu2S,有1mol硫被氧化生成SO2,其它物质中的S元素化合价没有发生变化,故B错误;
C.生成FeS,元素化合价没有变化,FeS不是还原产物,也不是氧化产物,故C错误;
D.元素化合价升高的只有S元素,由-2价升高到+4价,变化6价,则每转移1.2mol电子,有0.2mol硫被氧化,故D正确.
故选D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力和计算能力的考查,注意元素化合价的判断,为解答该题的关键,从元素化合价的角度解答该类题目,难度不大.1年前查看全部
- (2013•河南模拟)火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2下列说法正确的
(2013•河南模拟)火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2下列说法正确的是( )
A.SO2既是氧化产物又是还原产物
B.CuFeS2仅作还原剂,硫元素被氧化
C.每生成1 molCu2S,有4mol硫被氧化
D.每转移1.2 mol电子,有0.1 mol硫被氧化 eleven-l1年前1
eleven-l1年前1 -
 雪河之子 共回答了24个问题
雪河之子 共回答了24个问题 |采纳率75%解题思路:2CuFeS2+O2→Cu2S+2FeS+SO2中,Cu元素的化合价由+2价降低为+1价,O元素的化合价由0降低为-2价,S元素的化合价由-2价升高为+4价,以此来解答.A.O元素的化合价由0降低为-2价,S元素的化合价由-2价升高为+4价,则SO2既是氧化产物又是还原产物,故A正确;
B.Cu元素的化合价降低,S元素的化合价升高,则CuFeS2既作还原剂又作还原剂,S元素被氧化,故B错误;
C.由反应可知,生成1 molCu2S,有1mol硫被氧化,故C错误;
D.由反应可知,1molS被氧化转移6mol电子,则每转移1.2 mol电子,有0.2mol硫被氧化,故D错误;
故选A.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,为高考常见题型,注意把握元素的化合价及反应中的变化为解答的关键,侧重基本概念的考查,题目难度不大.1年前查看全部
- 黄铜矿(CuFeS 2 )是制取铜及其化合物的主要原料之一,还可以制备硫、铁和镍的化合物。 回答下列问题。
黄铜矿(CuFeS 2 )是制取铜及其化合物的主要原料之一,还可以制备硫、铁和镍的化合物。 
回答下列问题。
(1) Cu 2 S熔炼过程发生的主要反应为:
2Cu 2 S(s)+3O 2 (g)=2Cu 2 O(s)+2SO 2 (g) △H=-768.2 kJ/mol
2Cu 2 O(s)+Cu 2 S(s)=6Cu(s)+SO 2 (g) △H=+116.0 kJ/mol
在熔炼过程中不需要持续加热,原因是____。
(2)熔炼过程中产生大量的___(填分子式),可进一步加工并作为上述流程中的原料加以循环利用。
(3)炉渣的主要成分是Fe 2 O 3 、FeO、Al 2 O 3 、SiO 2 ,为了得到铁红,需对上述滤液进行处理,处理过程涉及下列步骤中的___(填序号)。
A.氧化 B.还原 C.灼烧 D.加碱
(4)废电解液中含有较多的Ni 2+ ,从废电解液提取硫酸镍晶体,需要用电解法把电解液中的Cu 2+ 除去,电解的阳极可以采用___作为电极材料,阳极的电极反应式是____。
(5)从废电解液中除去Pb 2+ 的方法是往其中通入H 2 S至饱和,使Pb 2+ 转化为硫化铅沉淀,溶液的 pH对转化效果的影响是____。已知 ,饱和H 2 S溶液中c( H 2 S)为0.1 mol/L,NiS的Ksp=10-11,若废 电解液的pH =5,为保证不生成NiS沉淀,Ni 2+ 的浓度应控制在__以下。
,饱和H 2 S溶液中c( H 2 S)为0.1 mol/L,NiS的Ksp=10-11,若废 电解液的pH =5,为保证不生成NiS沉淀,Ni 2+ 的浓度应控制在__以下。  Rhett121年前1
Rhett121年前1 -
 chen634751028 共回答了21个问题
chen634751028 共回答了21个问题 |采纳率90.5%(1)Cu 2 S与O 2 反应的热化学方程式为:Cu 2 S(s)+O 2 (g)=2Cu(s)+SO 2 (g) △H= - 217.4kJ/mol,反应放出的热量足以维持反应的进行
(2) SO 2
(3)ACD
(4)惰性电极 ;4OH - -4e - =2H 2 O+O 2 ↑(或Ni - 2e - =Ni 2+ )
(5)溶液的pH越大,转化效果越好 ;1 mol/L1年前查看全部
- 黄铜矿(主要成分CuFeS2)是提取铜的主要原料. 问:已知2 CuFeS2+4O2===Cu 2S+3S O2+2Fe
黄铜矿(主要成分CuFeS2)是提取铜的主要原料. 问:已知2 CuFeS2+4O2===Cu 2S+3S O2+2Fe O
产物Cu S2在1200度高温下继续反应:
2Cu S2+3 O2==== 2Cu2 O+2 S O2
2Cu2 O+ Cu2 S====6 Cu+ S O2
假设各步反应都完全,由184gCuFeS2生成64gCu,求消耗氧气质量 wfqz1234561年前1
wfqz1234561年前1 -
 上海被骗 共回答了17个问题
上海被骗 共回答了17个问题 |采纳率88.2%2CuFeS2+5O2--2Cu+4SO2+2FeO,需要2.5mol氧气,2.5*32=80g1年前查看全部
- 【化学——选修化学与技术】(15分)现有一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流
【化学——选修化学与技术】(15分)现有一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
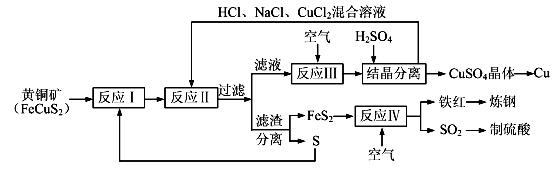
注:反应Ⅱ的离子方程式为Cu 2+ +CuS+4Cl — =2[CuCl 2 ] - +S
请回答下列问题:
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是 _____________________ ________、___________________________________ 。
(2)反应Ⅰ的产物为(填化学式) ___________________ 。
(3)反应Ⅲ的离子方程式为 ____________________________________________________ 。
(4)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是 ___________
(5)黄铜矿中Fe的化合价为+2,对于反应:8CuFeS 2 +21O 2 8Cu+4FeO+2Fe 2 O 3 +16SO 2 ,下列有关该反应的说法正确的是 ___________________ (填字母)。
8Cu+4FeO+2Fe 2 O 3 +16SO 2 ,下列有关该反应的说法正确的是 ___________________ (填字母)。
(6)某硫酸厂为测定反应Ⅳ所得气体中SO 2 的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe 2 (SO 4 ) 3 溶液完全反应后,用浓度为0.02000 mol/L的K 2 Cr 2 O 7 标准溶液滴定至终点,消耗K 2 Cr 2 O 7 溶液25.00 mL 。A.反应中被还原的元素只有氧 B.反应生成的SO 2 直接排放会污染环境 C.SO 2 既是氧化产物又是还原产物 D.当有8mol铜生成时,转移电子数目为100NA
已知:Cr 2 O 7 2 - + Fe 2 + + H + →Cr 3+ + Fe 3 + + H 2 O(未配平)
①SO 2 通入Fe 2 (SO 4 ) 3 溶液,发生反应的离子方程式为 ____________________________________ 。
②反应Ⅳ所得气体中SO 2 的体积分数为________________________________________________ 。 surpast1年前1
surpast1年前1 -
 dd的男人 共回答了19个问题
dd的男人 共回答了19个问题 |采纳率94.7%共15分。(1)SO 2 会导致大气污染(1分),同时要消耗大量的热能(1分)
(2)FeS 2 (1分)、CuS(1分) (3)4CuCl 2 - +O 2 +4H + =4Cu 2+ +8Cl - +2H 2 O(2分)
(4)该温度下,硫酸铜的溶解度小于氯化铜(2分)
(5)BCD(2分,漏选1个得1分,错选或漏选2个以上不得分)
(6)①SO 2 + 2Fe 3+ + 2H 2 O=SO 4 2- + 2Fe 2+ + 4H + (2分) ②12.00%(2分
1年前查看全部
- 高一离子反应在酸性溶液中,软锰矿(MnO2)和黄铜矿(CuFeS2)可以相互作用,生成铜盐、锰盐和铁盐.请写出反应的离子
高一离子反应
在酸性溶液中,软锰矿(MnO2)和黄铜矿(CuFeS2)可以相互作用,生成铜盐、锰盐和铁盐.请写出反应的离子方程式.
找不到答案.下面的是我写的...不知道对不对,若有错误,望高手指正.若无错误,请高手帮忙分析S为什么要到+6价而不是其它价态(我是靠经验和感觉写的SO4 2-...)好的追加分数
9MnO2 + 2Fe2+ + 2S2- + 20H+ ------ 9Mn2+ + 2Fe3+ + 2SO4 2- + 10H2O
回2L,在CUFES2中CU是不是+2价啊...我刚学氧化还原,只知道最简单的情形:要是CU是+1价的话,那FE就是+3价,这两个离子不是不能共存的啊.,难道固态的时候可以?所以我觉的CUFES2中CU是+2价...没变价,就不要写了... 止风静树1年前1
止风静树1年前1 -
 大唐王朝300年 共回答了28个问题
大唐王朝300年 共回答了28个问题 |采纳率96.4%你写的是有问题的.
首先,MnO2和CuFeS2都是不溶于水的.所以不能写成离子.(通常矿石都是不溶于水的,要不下场雨不就没矿石了么?这是常识哦)
第二,CuFeS2中,Cu是+1价,Fe是+3价.注意一个问题.也许老师会告诉你,Cu2+比Cu+稳定,但是注意,那是在水溶液中而不是在空气中!水溶液中稳定的原因是存在水化热.在空气中,Cu+比较稳定.而同样在空气中,Fe2+很溶液被氧化成Fe3+.另外,Cu+不能和Fe3+共存是热力学问题,而在矿石中还存在动力学问题,这不在高中学习范围内.
在酸性条件下,+4价的Mn的确可以将S氧化到+6价.所以总反应方程式是
2CuFeS2 + 17MnO2 + 36H+ = 2Cu2+ + 2Fe3+ + 17Mn2+ +4SO4 2- +18H2O1年前查看全部
- 黄铜矿主要成分CuFeS2是合金还是盐
 STENT1年前1
STENT1年前1 -
 huangxiong635188 共回答了18个问题
huangxiong635188 共回答了18个问题 |采纳率77.8%CuFeS2是盐 ,是化合物,不是混合物.1年前查看全部
- 黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物.
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物.
(1)冶炼铜的反应为8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2高温 .
若CuFeS2中Fe的化合价为+2,反应中被还原的元素______(填元素符号).
(2)上述冶炼过程中产生大量SO2.下列处理方案合理的是______(填代号).
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3
d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.方法为:
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧制得.
据以上信息回答下列问题:
选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸稀硫酸KSCN溶液KMnO4溶液NaOH溶液碘水
所选试剂为______.证明炉渣中含有FeO的实验现象为______. 花生乐橙搞联合1年前1
花生乐橙搞联合1年前1 -
 嘎嘎冷 共回答了16个问题
嘎嘎冷 共回答了16个问题 |采纳率100%解题思路:(1)8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2中,Fe元素的化合价升高,Cu、O元素的化合价降低;高温 .
(2)冶炼过程中产生大量SO2可制备硫酸或利用碱液吸收;
(3)设计实验验证炉渣中含有FeO,利用酸溶液后,根据亚铁离子具有还原性,选氧化剂发生明显的现象来解答.(1)8CuFeS2+21O2
高温
.
8Cu+4FeO+2Fe2O3+16SO2中,Fe元素的化合价升高,Cu、O元素的化合价降低,则Cu、O元素被还原,故答案为:Cu、O;
(2)冶炼过程中产生大量SO2可制备硫酸或利用碱液吸收,与浓硫酸不反应,也不能直接排放,故答案为:bc;
(3)设计实验验证炉渣中含有FeO,利用酸溶液后,根据亚铁离子具有还原性,选氧化剂发生明显的现象即可证明,因盐酸能被高锰酸钾氧化,则选择试剂为稀硫酸、KMnO4溶液,证明炉渣中含有FeO的实验现象为稀硫酸浸取炉渣所得溶液能使KMnO4溶液褪色,
故答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液能使KMnO4溶液褪色.点评:
本题考点: 氧化还原反应;物质的分离、提纯的基本方法选择与应用;物质的检验和鉴别的基本方法选择及应用.
考点点评: 本题考查氧化还原反应及应用,为高频考点,把握物质的性质、反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,(3)中易错选盐酸,题目难度不大.1年前查看全部
大家在问
- 1英语翻译第一段Part III.Translate English into Chinese.Directions:Fo
- 2关于能源的物理题?1太阳能是人类能源的宝库.太阳能集热器是直接利用太阳能的一种装置,它可以利用太阳能把水加热.太阳能集热
- 3当a=()时,算式(12-3a)*六分之五的值是10.当a= ( )时,算式(12-3a)*六分之五的值是0.
- 4将一张宽度相等的纸条按如图所示的方式折叠,则图中∠1的度数为( )
- 5我实在不会,望众高手教教我!甲,乙,丙三个人加工同样件数的服装,当甲完成任务时,乙还有五分之一未完成,丙还有20个零件未
- 6请英语高手翻译关于激发学生兴趣的一段话,谢谢!
- 7(2ll7•烟台三模)o个多面体的直观图(正视图、侧视图,俯视图)如图所示,他,N分别为A1B,B1C1的着点.
- 80.1,0.3,0.9,2.7,(),(),(),(). 16,15.4.14.8,14.2,(),(),(),()
- 9用“条形图”或“扇形图”描述数据,列举他们各有什么优点和不足
- 10唐代诗人李白的诗句:"黄河之水天上来,奔流到海不复回",这里的"天上"应指( )
- 11有一列数:3、5、9、17、33按这样的规律排列,第n个数是多少?
- 12的英文简介作者:马克吐温.(Mark Twain).【百万富翁】.尽量简短~
- 132y的二次方减y减2等于0,那4y的二次方减2y减5等于多少
- 14用12个棱长是1厘米的小正方体可以拼成()种不同的长方体
- 15抛掷一枚普通的正四面体的骰子,根据右栏对可能性大小的描述,选择左栏相应的随机事件与之相连:



