在中性溶液中Fe3+ Cl- NO3- Al3+为什么不能共存
 其实我明白2022-10-04 11:39:546条回答
其实我明白2022-10-04 11:39:546条回答
已提交,审核后显示!提交回复
共6条回复
 好名字都让狗占了 共回答了17个问题
好名字都让狗占了 共回答了17个问题 |采纳率76.5%- 标准的解释是:Fe3+、Al3+水解生成沉淀导致不共存.
跟NO3-没有任何关系!
但很难理解,可以这样理解这类问题.
Fe3+、Al3+水解导致溶液为酸性:
Fe3+ + 3 H2O ==可逆== Fe(OH)3 + H+
Al3+ + 3 H2O ==可逆== Al(OH)3 + H+
现在溶液却是中性,那么证明,一定向溶液中加入了碱,否则怎么会是中性呢?
既然加入了碱,Fe3+、Al3+都会沉淀了.
实际上,Fe3+在pH≈3,就会沉淀完全. - 1年前
 乱了乱了全乱了 共回答了18个问题
乱了乱了全乱了 共回答了18个问题 |采纳率83.3%- 应该可以大量共存,水解程度很小,而且无双水解
- 1年前
 gmpir 共回答了3个问题
gmpir 共回答了3个问题 |采纳率- 因为该溶液为中性,但是溶液中铁离子水解和铝离子水解使溶液呈酸性,与题意不符!沉淀到不至于!
- 1年前
 哨哨 共回答了4个问题
哨哨 共回答了4个问题 |采纳率- 铝离子结合氢氧根嘛,氢离子硝酸根他俩有还愿性,三甲铁还愿性,发生氧化还愿反应
- 1年前
 沈阳狂少 共回答了248个问题
沈阳狂少 共回答了248个问题 |采纳率- 本题并不是给出的四种离子的共存问题,关键是”中性溶液“
要知道Fe3+在pH=2.7左右的时候就可以开始产生沉淀了,到pH=5左右的时候,就已经沉淀完全了,因此中性溶液中Fe3+已经很少了,因此中性溶液中不可能大量存在Fe3+,Fe3+只能存在于强酸性溶液中。Al3+也是类似,也只能存在于酸性溶液中。... - 1年前
 shujianzhen 共回答了14319个问题
shujianzhen 共回答了14319个问题 |采纳率- 会发生水解生成氢氧化铝和氢氧化铁沉淀所以不能共存
- 1年前
相关推荐
- 面团在发酵的过程中产生的物质是什么?呈酸、碱还是中性?
 cheerya1年前3
cheerya1年前3 -
 就是赢 共回答了18个问题
就是赢 共回答了18个问题 |采纳率100%产生乳酸,和碱(碳酸钠)反应产生CO2,这是面包,馒头中气孔的由来!1年前查看全部
- 酸碱中和的计算常温下pH=11的苛性钠aL与pH=1的稀硫酸bL混合,若所得溶液为中性,则a:b=_____,若所得pH
酸碱中和的计算
常温下pH=11的苛性钠aL与pH=1的稀硫酸bL混合,若所得溶液为中性,则a:b=_____,若所得pH=2,则a:b=_____ 无亲情1年前1
无亲情1年前1 -
 琉璃妖妖 共回答了13个问题
琉璃妖妖 共回答了13个问题 |采纳率100%常温下pH=11的苛性钠aL与pH=1的稀硫酸bL混合,若所得溶液为中性,则a:b=1:100,若所得pH=2,则a:b=1:101年前查看全部
- 亚硫酸钠的水溶液呈碱性,食盐水溶液呈中性,怎样鉴定亚硫酸钠和食盐,选用什么试剂,如何操作
 cncr41年前1
cncr41年前1 -
 free_2010 共回答了21个问题
free_2010 共回答了21个问题 |采纳率76.2%(1)用酚酞,亚硫酸钠显红色,食盐水是无色
(2)紫色石蕊,亚硫酸钠为蓝色,食盐水仍是紫色
(3)H2SO4(HCl)共热,Na2SO3有刺激性气味气体(SO2)放出,而食盐水没有
(4)Ca(OH)2,Na2SO3有沉淀生成(CaSO3),食盐水没有1年前查看全部
- 某微粒核外有18个电子,当失去一个电子时呈电中性.问:此微粒的符号?
 苦苦的活着1年前1
苦苦的活着1年前1 -
 桃子妮妮 共回答了21个问题
桃子妮妮 共回答了21个问题 |采纳率90.5%失去一个电子时呈电中性,即为原子,可以判断出该元素为17号元素;
因此原微粒为原子加上一具负电荷,即Cl(-)1年前查看全部
- 某溶液是由体积相等的稀盐酸和氨水混合而成,且恰好中性,则混合前 C(HCL) 与C(氨水) 谁大
某溶液是由体积相等的稀盐酸和氨水混合而成,且恰好中性,则混合前 C(HCL) 与C(氨水) 谁大
混合前酸中的C(H离子) 和碱中的C(oh根) 谁大.求详解 烤糊的面包1年前2
烤糊的面包1年前2 -
 taotao4426 共回答了11个问题
taotao4426 共回答了11个问题 |采纳率81.8%这种题目这样来思考可能比较好一些:先假设盐酸与氨水的浓度是相同的,这样等体积混合后会完全反应生成氯化铵,而氯化铵溶液是显酸性的,所以二者混合要想呈中性,则需氨水多一点,所以C(HCl)<C(氨水).而比较c(H+)和c(O...1年前查看全部
- 赖氨酸在中性pH下,整个分子带什么电
赖氨酸在中性pH下,整个分子带什么电
说说具体的分析过程 jjf641年前2
jjf641年前2 -
 farun 共回答了24个问题
farun 共回答了24个问题 |采纳率95.8%带正电
赖氨酸是碱性氨基酸,等电点大于7,在等电点条件下赖氨酸呈电中性,而中性PH(PH=7)条件可看成是在赖氨酸等电点条件下加酸.由于赖氨酸中-NH2可以结合H+,所以加酸后赖氨酸带正电.1年前查看全部
- 所有的化合物都成电中性,为什么?
 yeejames1年前1
yeejames1年前1 -
 爱我一生哦 共回答了13个问题
爱我一生哦 共回答了13个问题 |采纳率84.6%之所以称之为化合物就是由两种或两种以上的物质结合,物质在结合的过程中正负抵消就成了电中性了1年前查看全部
- 赖氨酸在中性pH下,整个分子带什么电?
 john04081年前1
john04081年前1 -
 pazuochuan 共回答了18个问题
pazuochuan 共回答了18个问题 |采纳率83.3%带正电赖氨酸是碱性氨基酸
,等电点大于7,在等电点条件下赖氨酸呈电中性,而中性PH(PH=7)条件可看成是在赖氨酸等电点条件下加酸.由于赖氨酸中-NH2可以结合H+,所以加酸后赖氨酸带正电.1年前查看全部
- 原子呈中性是因为原子中的正负电荷数量相等还是因为原子中的正负电荷互相抵消了
 秋水葬花1年前2
秋水葬花1年前2 -
 刀三两 共回答了20个问题
刀三两 共回答了20个问题 |采纳率80%原子呈中性是因为原子中的正负电荷数量相等
它们没有相互接触,是不会互相抵消的1年前查看全部
- 碘和碘酸根在酸性,中性溶液中反应方程式
 lynn30031年前1
lynn30031年前1 -
 ymyee狼 共回答了18个问题
ymyee狼 共回答了18个问题 |采纳率94.4%酸性溶液
5I- + IO3- + 6H+ == 3I2 + 3H2O
中性溶液
5I- + IO3- + 3H2O== 3I2 + 6OH-1年前查看全部
- 下列说法正确的是( ) A.100℃时PH=2的盐酸与PH=12的KOH的体积混合,混合后的溶液为中性 B.对于0.
下列说法正确的是()
A.100℃时PH=2的盐酸与PH=12的KOH的体积混合,混合后的溶液为中性 B.对于0.1mol/L的NH 4 Cl溶液,温度不变,则 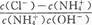 的比值不变
的比值不变C.丙烷分子的比例模型为: 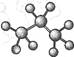
D.碱性氧化物由金属元素和氧元素组成,MgO、K 2 O、Na 2 O 2 、Mn 2 O 7 、Fe 2 O 3 中有四种为碱性氧化物  悠悠草草1年前1
悠悠草草1年前1 -
 stonexinqun 共回答了21个问题
stonexinqun 共回答了21个问题 |采纳率71.4%B
100℃是水的离子积常数是1×10 - 12 ,所以pH=12的氢氧化钾溶液的浓度是1.0mol/L,依次在反应中氢氧化钾是过量的,溶液显碱性,A不正确。C不正确,总是球棍模型。能和酸反应生成盐和水的氧化物是碱性氧化物,过氧化钠和酸反应还有氧气生成,不是碱性氧化物。Mn 2 O 7 是酸性氧化物,D不正确。所以正确的答案是B。1年前查看全部
- 100ml的pH值是1的溶液 用28%的氨水调节为中性 大约需要加多少ml氨水?()
 qiuqiutu511年前2
qiuqiutu511年前2 -
 喝粥吃山楂 共回答了14个问题
喝粥吃山楂 共回答了14个问题 |采纳率100%我算了下大约需要674mL!以下是计算过程!C(H+)=0.1MOL/L V(H+)=100ML 得:n(H+)=0.01MOLn(NH3)=0.01MOL m(NH3)=0.01*17=0.17g所需氨水的质量为:0.17/0.28=0.607g然后除以氨水的密度:0.607/0.9=0.674L最好自己算算...1年前查看全部
- 为什么胶粒带电荷而胶体都是电中性?
 foolp1年前1
foolp1年前1 -
 股怪柏麟 共回答了16个问题
股怪柏麟 共回答了16个问题 |采纳率100%胶体是分散系,相当于溶液,胶粒是分散质相当于溶质.
你可以这样想溶液中允许有带电的离子,但整个溶液是电中性的.
比如氯化钠溶液有钠离子和氯离子,刚好1:1
氢氧化铁胶体是因为氢氧化铁胶粒吸附了一定的三价铁离子带了正电,水溶液中还有多余的相应的氯离子,刚好整体中性1年前查看全部
- 层析用的氧化铝中性和碱性有什么区别
层析用的氧化铝中性和碱性有什么区别
用氧化铝层析石油醚的时候要求用中性氧化铝,化学试剂层析的氧化铝一般是碱性的,用碱性的氧化铝对层析有影响吗?中性的和碱性的对层析影响大吗?有什么区别吗? lucifer_mi1年前1
lucifer_mi1年前1 -
 caicai1001 共回答了21个问题
caicai1001 共回答了21个问题 |采纳率85.7%层析的时候最好是用中性的溶液,不过碱性的氧化铝问题不会太大(除非你的氧化铝中有太多的碱性杂质),建议尝试一下.
(失败了也没关系,失败为成功之母,学习到了知识就可以了.)1年前查看全部
- 酸性土壤怎么样才变中性?酸性土壤怎么样才能变成中性或碱性?中性或碱性的PH值各是多少?
 mansonzhu1年前1
mansonzhu1年前1 -
 shirleybevan 共回答了15个问题
shirleybevan 共回答了15个问题 |采纳率93.3%加氢氧化钙溶液
中性7 碱性 大于71年前查看全部
- “硫酸钾是化学中性、生理酸性肥料”这句话什么意思?
“硫酸钾是化学中性、生理酸性肥料”这句话什么意思?
什么叫“化学中性、生理酸性”?还有,“在淹水条件下,过多的硫酸根会被还原生成硫化氢”是怎么回事?能不能说明一下反应的原因和具体情况?(上面两句都是百度百科词条“硫酸钾”里的句子.) naxiong12341年前1
naxiong12341年前1 -
 caoeng 共回答了19个问题
caoeng 共回答了19个问题 |采纳率100%硫酸钾是点中性的 ,像硫酸就是显酸性,氢氧化钾是显碱性一样.在水溶液中硫酸根会被水中电离产生的氢离子还原生成硫化氢.1年前查看全部
- 【高一电学】判断一下这句话电现象的本质是电子的转移,呈中性的物体得到电子就一定显负电性,失去电子就一定显正电性
 9血之海91年前2
9血之海91年前2 -
 pannianlong 共回答了18个问题
pannianlong 共回答了18个问题 |采纳率83.3%从一般上看,是对的.
但是钻牛角尖看,是错的.
eg:HCl→H2+Cl2
HCl变成Cl2失去了H的电子和质子,但还是为电中性.╮(╯_╰)╭1年前查看全部
- 0.5molX元素的离子被还原成中性原子时,需得到6.02×10的23次方个电子;4gX的单质与足量盐酸充分反应放出0.
0.5molX元素的离子被还原成中性原子时,需得到6.02×10的23次方个电子;4gX的单质与足量盐酸充分反应放出0.2g氢气;X中质子数个中子数相等.Y元素的阴离子结构与氩原子结构相同它的气态氢化物的水溶液显强酸性.(1)通过计算说明X,Y的名称及其在周期表中的位置;(2)用化学方程式表示X最高价氧化物对应水化物与Y单质的反应.
 小小时候1年前1
小小时候1年前1 -
 奶牛rr 共回答了24个问题
奶牛rr 共回答了24个问题 |采纳率87.5%6.02×10^23=1mol,0.5molx元素需要1mole,所以x的离子为x2+,x+2h+=x2++h2,n(h2)=0.2/2=0.1mol,所以4gx为0.1mol,M(x)=40g/mol,x为Ca,第四周期,2A族;根据条件y是第三周期元素,气态氢化物为强酸性,应该是Cl,为第三周期7A族,2ca(oh)2+2cl2=ca(clo)2+cacl2+2h2o,把族数换成希腊数字就可以了,爪机打不粗.1年前查看全部
- 把PH从8中和到7,需加多少酸做的一个产品(醛类),本来显中性,但由于用了氢氧化钠作催化剂,反应完后PH=8,总共有12
把PH从8中和到7,需加多少酸
做的一个产品(醛类),本来显中性,但由于用了氢氧化钠作催化剂,反应完后PH=8,总共有1200KG(体积按1200L算吧),需加6MOL/L的盐酸多少进去,才能将PH值降到7? nh200805041年前4
nh200805041年前4 -
 empty3000 共回答了21个问题
empty3000 共回答了21个问题 |采纳率90.5%0.18ml理论上是.
如果溶液中有缓冲剂就不行了!
具体多少需要用酸碱滴定管滴一下样品,用滴出来的比例加.
滴定时最好用中性红作指示剂.1年前查看全部
- 某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40克,洗涤后的溶液呈中性,这一定量
某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40克,洗涤后的溶液呈中性,这一定量石油产品中含硫酸的质量是多少?
 飘荡的回忆wxm1年前1
飘荡的回忆wxm1年前1 -
 野性ff 共回答了16个问题
野性ff 共回答了16个问题 |采纳率93.8%由题可知NaOH的质量=40X15%=6g
设H2SO4的质量为X,
2NaOH+H2SO4=Na2SO4+2H2O
2X40 98
6g x
解得x=7.35g1年前查看全部
- 列举几个中性词,褒义,贬义词,口头语词,书面语词至少3个
 wenmyso1年前3
wenmyso1年前3 -
 hhhyyy6666 共回答了17个问题
hhhyyy6666 共回答了17个问题 |采纳率94.1%中性词:只字不提 少安毋躁 一衣带水
褒义词 奉公守法 博学多才,见多识广 才思敏捷,过目不忘,
贬义词 见利忘义 遗臭万年 臭名昭著
口头语词 粉丝 养眼 偶 拜拜 妈咪 爹地
书面语词 不啻 母亲 父亲 (比较正式的那些都算)1年前查看全部
- 小丽买中性笔和钢笔各1支,共付8.5元。如果一支钢笔换2支中性笔,还要付给售货员0.5元,中性笔和钢笔单价各是多少元?
 强强桃1年前1
强强桃1年前1 -
 梦想剧本 共回答了20个问题
梦想剧本 共回答了20个问题 |采纳率90%中3元,钢笔5.5元1年前查看全部
- 向硫酸氢那溶液中逐滴加入氢氧化钡溶液至中性,请写出发生反应的离子方程式
 yushihai101年前2
yushihai101年前2 -
 xzcyp 共回答了15个问题
xzcyp 共回答了15个问题 |采纳率86.7%2H+ + SO42- + Ba2+ + 2OH- ==2H20+BaSO4 (沉淀)
在高中阶段认为硫酸是二元强酸,是完全电离的.1年前查看全部
- 在PH3左右,氨基酸混合液(酸性,碱性,中性三类),经阳离子交换树脂被洗脱分离,这三类氨基酸的洗脱顺序
 love蝴蝶love1年前2
love蝴蝶love1年前2 -
 秋香美美 共回答了22个问题
秋香美美 共回答了22个问题 |采纳率100%原因:氨基酸与阳离子交换树脂的静电引力大小依次是 碱性氨基酸>中性氨基酸>酸性氨基酸,所以洗脱的顺序就
先是酸性氨基酸(负电荷最多),然后是中性氨基酸,最后是碱性氨基酸(带正电荷最多).
详见《生物化学》王镜岩 第三版 上册 153页1年前查看全部
- 为什么氯化钠显中性,碳酸钠显碱性
 乖乖的芹菜1年前1
乖乖的芹菜1年前1 -
 yorkyork 共回答了16个问题
yorkyork 共回答了16个问题 |采纳率87.5%氯化钠溶液中,Na离子是强碱离子,Cl是强酸酸根,所以两个离子在水中都不会发生水解反应,水中H+离子和OH-根离子浓度均未发生偏移,水溶液呈现中性;
碳酸钠溶液中,碳酸根是弱酸根,会与水发生水解反应:CO3 + H2O= HCO3- +OH- ,当然HCO3-也会与水发生反应 CO3- +H2O= H2CO3 + OH-,而Na是强碱离子,不发生水解,故溶液中HO-浓度高于H+浓度,溶液PH呈碱性.1年前查看全部
- 溶酶体内的酶最适PH为5左右.中性环境7时这些酶已经没有活性,那为什么细胞自溶是由溶酶体膜破裂造成的呢
 淡淡的爱今何在1年前1
淡淡的爱今何在1年前1 -
 wusiyin1 共回答了22个问题
wusiyin1 共回答了22个问题 |采纳率100%溶酶体内有大量酸性物质(溶酶体壁上还有很多质子泵),溶酶体破裂后细胞内部酸碱平衡被打破,显出酸性.而且,溶酶体内的酶不在最适环境下也是有一点作用的.1年前查看全部
- 等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”、“中性”或“碱性”)
等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”、“中性”或“碱性”)
醋酸和氢氧化钠可以完全反应,虽然醋酸是弱酸但是不断消耗H+,所以最后能成圣醋酸钠.但是醋酸钠水解后生成醋酸和OH-.那么他们就不能反应吗?为什么水解的醋酸不电离呢? 人鱼萝萝1年前3
人鱼萝萝1年前3 -
 我就是不登陆 共回答了15个问题
我就是不登陆 共回答了15个问题 |采纳率100%溶液呈碱性因为生成物醋酸钠是强碱弱酸盐、水溶液呈碱性
CH3COONA+H2O=CH3COOH+NA+ +OH-1年前查看全部
- 酯在碱性、酸性、中性下水解有什么不同
 小希20041年前1
小希20041年前1 -
 yll1219 共回答了15个问题
yll1219 共回答了15个问题 |采纳率93.3%中性不水解
碱性水解为酸钠
酸性水解为酸1年前查看全部
- 现有PH=a的醋酸和PH=b的NaOH溶液.将两种溶液等体积混合,混合成中性,则a+b的大小关系为大于14.为什么
 吃饭了没1年前1
吃饭了没1年前1 -
 itsoso 共回答了17个问题
itsoso 共回答了17个问题 |采纳率94.1%如果这个酸不是醋酸而是盐酸(设它的pH=a’),那么a‘+b=14;(根据氢氧根浓度=氢离子浓度)由于醋酸是弱酸,所以此时它的氢离子浓度应该小于盐酸,因为如果等于盐酸,那么反应过程中,促进醋酸电离,溶液最终显示酸性,不是PH=7;所以醋酸pH(氢离子负对数)a>a‘;所以a+b>14;1年前查看全部
- 我参加初中生物地理会考 在答题卡背面写了几个字(用黑色中性笔写的) 不知道会不会影响阅卷……
 mollyweiwei1年前1
mollyweiwei1年前1 -
 幻蓝nn 共回答了15个问题
幻蓝nn 共回答了15个问题 |采纳率93.3%不会影响的,放心
以后做题要小心,免得自己担心1年前查看全部
- 分类.煽动 阴谋 勇敢 风气 足智多谋 坚持不懈 诡计多端 横行霸道 川流不息 五湖四海 褒义词 贬义词 中性
 qwh1641年前1
qwh1641年前1 -
 wonderfulone 共回答了20个问题
wonderfulone 共回答了20个问题 |采纳率85%褒义词 勇敢 足智多谋 坚持不懈
贬义词 煽动 阴谋 诡计多端 横行霸道
中性 风气 川流不息 五湖四海1年前查看全部
- 欲确保含有盐酸的氯化钙溶液变为中性而不引入新的杂质,在不用指示剂的条件下,应加入的试剂是( )
欲确保含有盐酸的氯化钙溶液变为中性而不引入新的杂质,在不用指示剂的条件下,应加入的试剂是( )
A. 生石灰
B. 熟石灰
C. 石灰石粉末
D. 纯碱 宁惜惜1年前2
宁惜惜1年前2 -
 山海旅途俱乐部 共回答了13个问题
山海旅途俱乐部 共回答了13个问题 |采纳率92.3%解题思路:氯化钙溶液因含有盐酸显酸性要变为中性,即是要除去其中的盐酸.注意过程中不能增加其他可溶性的杂质,并要确实把盐酸反应掉,而不使用指示剂.A、生石灰的主要成分是氧化钙,能与水反应生成氢氧化钙,可以盐酸反应生成氯化钙,反应时无明显现象,不好控制加入的量.故本选项错误;
B、熟石灰的主要成分是氢氧化钙,能与盐酸反应生成氯化钙,反应时无明显现象不好控制加入的量.故本选项错误;
C、石灰石粉末的主要成分是碳酸钙能与盐酸反应生成氯化钙,且碳酸钙不溶于水,可加入过量的石灰石粉末以除去盐酸.故本选项正确;
D、纯碱的主要成分是碳酸钠,碳酸钠能与盐酸反应生成氯化钠,虽能除去盐酸但却增加了新的杂质氯化钠.故本选项错误;
故选C.点评:
本题考点: 物质除杂或净化的探究;酸的化学性质.
考点点评: 解答除杂相关问题时要把握如下原则:①选用的试剂要能将杂质除去但不能与要保留的物质反应;②在除杂的同时不能增加新的杂质.一般的方法是将杂质转化为要保留的物质.1年前查看全部
- 线圈中产生的正弦交变电流按i=10sin314tA变化,求出当线圈从中性面起转过30°、60°、90°、120°所需时间
线圈中产生的正弦交变电流按i=10sin314tA变化,求出当线圈从中性面起转过30°、60°、90°、120°所需时间及对应的电流值
 仝玲1年前1
仝玲1年前1 -
 分手才会有幸福 共回答了17个问题
分手才会有幸福 共回答了17个问题 |采纳率94.1%分析:在所给的电流规律表达式 i=10*sin(314t)安 中,(314 t )就是线圈平面与中性面的夹角.当线圈从中性面起转过 30度=(π / 6)弧度 时,所用时间为 t1,电流值为 i1 则314* t1=π / 6 ,得 t1=1 / 600=0.001667秒 i1=10* sin30度=5 安 当线圈从中性面起转过 60度=(π / 3)弧度 时,所用时间为 t2,电流值为 i2 则314* t2=π / 3 ,得 t2=1 / 300=0.003333秒 i2=10* sin60度=5 * 根号3=8.66 安 当线圈从中性面起转过 90度=(π / 2)弧度 时,所用时间为 t3,电流值为 i3 则314* t3=π / 2 ,得 t3=1 / 200=0.005 秒 i3=10* sin90度=10 安 当线圈从中性面起转过 120度=(2π / 3)弧度 时,所用时间为 t4,电流值为 i4 则314* t4=2π / 3 ,得 t4=1 / 150=0.00667秒 i4=10* sin120度=10* sin60度=5 * 根号3=8.66 安1年前查看全部
- (1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:______.
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:______.
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:______. 爱喝可乐的顽皮猫1年前3
爱喝可乐的顽皮猫1年前3 -
 远方的孤独 共回答了15个问题
远方的孤独 共回答了15个问题 |采纳率100%解题思路:(1)加入Ba(OH)2溶液至中性时,其反应式为:2NaHSO4+Ba(OH)2=BaSO4↓+Na2SO4+2H2O,以此书写离子方程式;
(2)至中性时溶液中溶质只有Na2SO4,加入Ba(OH)2溶液生成BaSO4沉淀.(1)NaHSO4是二元强酸的酸式盐,可以理解为全部电离.当反应后溶液呈中性时,其反应式为:2NaHSO4+Ba(OH)2=BaSO4↓+Na2SO4+2H2O,那么,
离子反应方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(2)此时溶液中溶质只有Na2SO4,加入Ba(OH)2的离子反应方程式为:Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓.点评:
本题考点: 离子方程式的书写.
考点点评: 本题考查离子方程式的书写,题目难度不大,注意根据物质的量判断反应的程度并书写相关离子方程式,注意与量有关的离子方程式的书写方法.1年前查看全部
- 阿司匹林含量测定中,已酰水杨酸晶体为什么要用中性乙醇溶解?
 维生素糖果1年前1
维生素糖果1年前1 -
 koujane 共回答了15个问题
koujane 共回答了15个问题 |采纳率93.3%检查是否有氯化物的存在,加入适量乙醇使其褪色!1年前查看全部
- 中性细胞数下降,中性细胞比率下降,淋巴细胞比率上升,身体是个什么情况才会出现?
中性细胞数下降,中性细胞比率下降,淋巴细胞比率上升,身体是个什么情况才会出现?
还有平均血小板体积、血小板分布宽度、大型血小板比例均上升是怎么回事? 意自闲1年前2
意自闲1年前2 -
 lxbo_7758 共回答了17个问题
lxbo_7758 共回答了17个问题 |采纳率94.1%首先无论是计数总数还是比率的下降都要看究竟下降了多少,如果只是轻微的改变并没有太明确的临床意义,但是有待观察.中性粒细胞比率下降,淋巴比率上身最常见的就是严重的病毒感染.至于血小板的部分,血小板计数并没有改变,应该没有大的问题,平均血小板体积、分布宽度、及大型血小板比例的上升均提示的是血小板体积不一,有大血小板存在,这个可能跟抽血过程有一定关系,可能抽血不顺畅,有部分凝集.当然也可以考虑有小红细胞的存在,这个要看你红细胞部分检查结果了.1年前查看全部
- 某温度下,向0.1mol/l的的NaHA中滴入0.1mol/l的KOH,使混合液呈中性
某温度下,向0.1mol/l的的NaHA中滴入0.1mol/l的KOH,使混合液呈中性
下列关系正确的是
A.C(H+)*C(OH-)=1*10^-14
B.C(Na+)+C(K+)=2C(A2-)+C(HA-)
C.C(K+) 大波仔1年前2
大波仔1年前2 -
 gyu1265 共回答了17个问题
gyu1265 共回答了17个问题 |采纳率82.4%B1年前查看全部
- 滔滔不绝是褒义?贬义?还是中性?
 qy88101年前1
qy88101年前1 -
 guojunpeng 共回答了19个问题
guojunpeng 共回答了19个问题 |采纳率89.5%要根据语境来判断的1年前查看全部
- 一份敞放于空气中氢氧化钠溶液,无论是否变质,逐滴加盐酸至溶液恰好为中性时,溶液中的溶质质量均相同.
 东方不怪1年前2
东方不怪1年前2 -
 叶子爱BB 共回答了14个问题
叶子爱BB 共回答了14个问题 |采纳率100%首先,一般认为氢氧化钠变质是因为与CO2反应生成Na2CO3或NaHCO3.滴加的HCl总会先跟Na2CO3或NaHCO3先反应,反应的计量数其实没有变,而且最终到了中性时,溶质都是NaCl,Na离子来自于氢氧化钠,质量自然相同1年前查看全部
- 光电效应的 金属板释放电子后变成什么状态?还是电中性的吗?金属会不会逐渐消耗掉?
 主儿71年前3
主儿71年前3 -
 wendy830214 共回答了14个问题
wendy830214 共回答了14个问题 |采纳率92.9%电子被激发到周围变成游离太,金属板因少了电子而带正电!
板的质量不会减少,电子的质量相对于物体来说太少了,忽略就可以啦1年前查看全部
- 碘与硫代硫酸钠反应应在中性或弱酸性溶液中进行; 高锰酸钾法只能在__溶液中进行,
碘与硫代硫酸钠反应应在中性或弱酸性溶液中进行; 高锰酸钾法只能在__溶液中进行,
高锰酸钾法只能在___________溶液中进行,酸度控制在________________. qyfv1年前2
qyfv1年前2 -
 风雨前缘 共回答了14个问题
风雨前缘 共回答了14个问题 |采纳率100%强酸性,酸度控制在 1mol/L (即pH=0).
这时候所用反应式为:
MnO4- + 5e + 8H+ ----- Mn2+ + 4H2O
高锰酸钾自身颜色变化无需加指示剂.
而在微酸性、中性或弱碱性溶液中,反应为:
MnO4- +2H2O+ 3e ------ MnO2↓+ 4OH-
反应后生成棕色的MnO2↓,妨碍终点的观察,这个反应在定量分析中很少应用.1年前查看全部
- 中性笔芯笔中墨水向笔尖流动的原因是什么?
 lxhy991年前1
lxhy991年前1 -
 天空永远的灰 共回答了25个问题
天空永远的灰 共回答了25个问题 |采纳率88%大气压的作用1年前查看全部
- 中性溶液能增加酸或降低碱溶液pH值吗?
中性溶液能增加酸或降低碱溶液pH值吗?
如氯化钠溶液能否使氢氧化钠pH值降低, 弹子云1年前7
弹子云1年前7 -
 celerylq 共回答了15个问题
celerylq 共回答了15个问题 |采纳率86.7%可以,因氯化钠溶液加入氢氧化钠溶液时体积增加而OH根量不变1年前查看全部
- 在一个电中性的原子中,一定含有的微粒是( )
在一个电中性的原子中,一定含有的微粒是( )
A. 质子、中子、电子
B. 质子、中子
C. 质子、电子
D. 中子、电子 拉度酱油1年前2
拉度酱油1年前2 -
 哈哈哈haha 共回答了18个问题
哈哈哈haha 共回答了18个问题 |采纳率83.3%解题思路:根据原子为电中性以及质子带正电、中子不带电、核外电子带负电来解答.根据原子呈电中性以及质子带正电、中子不带电、核外电子带负电可知,
原子中一定含有质子和电子,不一定有中子,如氢的一种同位素氕,它只有1个质子和1个电子构成.
故选C.点评:
本题考点: 原子构成.
考点点评: 本题主要考查了原子的构成以及组成粒子的电性,难度不大,根据课本知识即可完成.1年前查看全部
- 用同一个词造句,有贬义词,褒义词和中性词3个
 jg551年前1
jg551年前1 -
 mffk 共回答了11个问题
mffk 共回答了11个问题 |采纳率90.9%天真
你太天真了,连这个都信。
这个孩子天真地笑着。
今天真热。1年前查看全部
- 恍然顿悟是贬义词还是褒义词还是中性词.泄气呢?
 zhaodec241年前1
zhaodec241年前1 -
 liu_bens 共回答了19个问题
liu_bens 共回答了19个问题 |采纳率89.5%恍然大悟是褒义词
恍然大悟 【拼音】:huǎng rán dà wù
恍然:猛然清醒的样子;悟:心里明白.形容一下子明白过来.
【出处】:宋·释道原《景德传灯录》卷五:“简蒙指教,豁然大悟.”
【示例】:袁太守和庄太守听了,方才~,彼此相视而笑.★清·张春帆《宦海》第十七回
【近义词】:豁然开朗、如梦初醒、茅塞顿开
【反义词】:如坐云雾、大惑不解
【语法】:作谓语、定语、状语;形容人对某事突然明白
【英文】:tumble to
【日文】:はっと悟る
【法文】:comprendre,voir soudainement
【德文】:plǒtzlich Zusammenhǎnge begreifen1年前查看全部
- 寿终正寝 老师说这个词是贬义词 网上说这个词是褒义词 资料说这个词是中性词,也指事物的消亡,含有讽刺性.所以当它指一个人
寿终正寝
老师说这个词是贬义词 网上说这个词是褒义词 资料说这个词是中性词,也指事物的消亡,含有讽刺性.所以当它指一个人死去的时候是什么词性.. 冬季恋歌to香水1年前1
冬季恋歌to香水1年前1 -
 767859811 共回答了24个问题
767859811 共回答了24个问题 |采纳率87.5%寿终正寝应为中性词,或许为褒义词,但绝不会是贬义词.寿终正寝就是岁数大了,正常的、躺在床上死去了.怎么能够说是贬义词呢?那横死、扑街又算什么?寿终正寝本为中性,可是算上政治,那么就贬了.误人子弟啊.1年前查看全部
- 锂基酯的化学组成成分及性质锂基酯—中性笔芯后面的那层油
 45634567331年前1
45634567331年前1 -
 370181406 共回答了27个问题
370181406 共回答了27个问题 |采纳率92.6%随动密封剂(锂基酯)根据胶体与表面化学理论与实践经验研制成功的一种专用密封剂
,通称"锂基酯".适合作中性水笔笔芯的尾塞,即对笔管中的墨水密封,防止蒸发或倒流,
并随书写过程墨水因减少而随动跟进密封.因此可视为"液体活塞".
制笔使用的"锂基酯",要求与中性墨水互不相溶,界面清晰;无气泡,抗蒸发;高低温
稳定性好,随动触变流动性佳.使中性笔在气温变化较大的情况下,保持良好的保湿密封,
防止墨水蒸发或倒流溢出.并要求在快速书写时,密封剂能随时跟进,且少沾管壁,以保证
能跟进至墨水写完.1年前查看全部
- 醋酸和醋酸钠以什么比例混合时,溶液显中性?
 一小滴水1年前3
一小滴水1年前3 -
 快乐xx 共回答了16个问题
快乐xx 共回答了16个问题 |采纳率87.5%这道题的计算需要用到酸常数Ka,如果题目没有给的话,在这里取K=1.8×10^-5.
代入缓冲溶液pH计算公式:[H+]=Ka×a/b(a:acid,酸浓度;b:base,碱浓度)
即:10^-7(中性)=1.8*10^-5 ×a/b
解得:a/b=1:180
所以等浓度的醋酸和醋酸钠溶液以1:180混合所得的溶液呈中性.1年前查看全部
大家在问
- 1中性溶液:Fe3+、Al3+、NO3-、SO42-能否共存
- 26.离子共存:Fe3+与()双水解不能共存;Al3+与()双水解不能共存
- 3写东南西北风的诗句 各5句
- 4在托里拆利试验中,由于操作不慎,漏尽了一些空气,当大气压强为(75/76)^10^5Pa时,管内水银面差60CM,管内封
- 5懂 西语 的进,问几个单词.在听力中有几个单词听不懂,下面我把读音大概打出来.1.两个可能是人名:jiodacía li
- 6最后一份晚报 请写出与文章最贴近的一首古诗词,并标明作者
- 7Do you think people use will rather than would?
- 8如何理解声与人类社会息息相关?
- 9英语翻译Charles Fillmore的名言只有自己欣赏的事物,才能让我们进一步去提升。这是我的理解 你们仁者见仁
- 10400*(1-0.25)-32*0.125简便计算
- 11某学校的教学楼前直立一块面积为0.7平方米的平面镜,当镜面向着这幢楼时,则这幢教学楼能在平面镜中成( )
- 12学校有3根旗杆,第一根旗杆高度为10米,第二根旗杆的高度比第一根的5分之2还高1米,学校有
- 13当木块作匀速直线运动时,滑动摩擦力就会等于拉力
- 14The teacher says she will be a singer because she is a-----〔
- 15如何分离氯化铵和氯化锌
