2014二模数学啊 急 求指教吧
 czzzg2022-10-04 11:39:541条回答
czzzg2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 Xiujin118 共回答了16个问题
Xiujin118 共回答了16个问题 |采纳率87.5%- (1)在三角形AFC中FD垂直与AC且AD=DC
所以三角形AFC为等腰三角形,
所以 - 1年前
相关推荐
- (2009•大港区二模)如图①是一些大小相同的小正方体组成的几何体,其主视图如图②所示,则其俯视图是( )
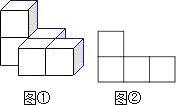 (2009•大港区二模)如图①是一些大小相同的小正方体组成的几何体,其主视图如图②所示,则其俯视图是( )
(2009•大港区二模)如图①是一些大小相同的小正方体组成的几何体,其主视图如图②所示,则其俯视图是( )
A.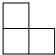
B.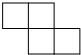
C.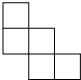
D.
 023502351年前1
023502351年前1 -
 无名看客246 共回答了23个问题
无名看客246 共回答了23个问题 |采纳率87%解题思路:找到从上面看所得到的图形即可.从上面看可得到从上往下两行正方形的个数依次为2,2,故选B.
点评:
本题考点: 简单组合体的三视图.
考点点评: 本题考查了三视图的知识,俯视图是从物体的上面看得到的视图.1年前查看全部
- (2013•嘉兴二模)固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2
(2013•嘉兴二模)固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:
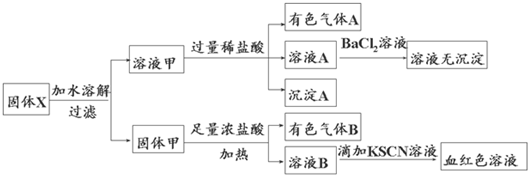
根据上述实验,以下说法正确的是( )
A. 溶液甲中一定含有K2SiO3、NaNO2、可能含有KAlO2、K2CO3
B. 由于在溶液甲中加入足量稀盐酸后再加入BaCl2溶液,因此无法判断溶液中是否有K2SO3
C. 气体A和气体B一定均为纯净物
D. 原混合物中一定含有Fe2O3 饵刀1年前4
饵刀1年前4 -
 梦血 共回答了18个问题
梦血 共回答了18个问题 |采纳率88.9%解题思路:有色气体A应为NO2,可能含有CO2气体,说明一定含有NaNO2,固体甲与浓盐酸反应生成有色气体B,B应为Cl2,则应含有MnO2,沉淀A应为H2SiO3,说明含有K2SiO3,则一定不含有MgCl2,溶液B加KSCN溶液呈血红色,说明含有Fe3+,则固体中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,以此解答该题.有色气体A应为NO2,可能含有CO2、SO2等气体,说明一定含有NaNO2,固体甲与浓盐酸反应生成有色气体B,B应为Cl2,则应含有MnO2,沉淀A应为H2SiO3,说明含有K2SiO3,则一定不含有MgCl2,溶液B加KSCN溶液呈血红色,说明含有Fe3+,则固体中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,
A.有以上分析可知一定含有K2SiO3、NaNO2,可能含有K2CO3,也可能含有KAlO2,加入过量盐酸生成AlCl3,与以上物质不反应,不能确定,故A正确;
B.因含有NaNO2,如含有K2SO3,二者在酸性条件下发生氧化还原反应生成SO42-,加入氯化钡生成硫酸钡沉淀,加入足量稀盐酸后再加入BaCl2溶液没有沉淀,则一定不含有K2SO3,故B错误;
C.有色气体A应为NO2,可能含有CO2气体,而浓盐酸易挥发,生成的氯气中一定含有HCl气体,故C错误;
D.溶液B加KSCN溶液呈血红色,说明含有Fe3+,则固体中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,故D错误.
故选A.点评:
本题考点: 物质的检验和鉴别的实验方案设计;物质的检验和鉴别的基本方法选择及应用.
考点点评: 本题考查物质的检验和鉴别的实验方案的设计,侧重于元素化合物知识的综合运用,题目难度中等,注意把握反应的现象,根据现象结合物质的性质进行判断,易错点为B和D,注意体会.1年前查看全部
- (2014•南开区二模)已知暗箱中开始有3个红球,2个白球(所有的球除颜色外其它均相同).现每次从暗箱中取出一个球后,再
(2014•南开区二模)已知暗箱中开始有3个红球,2个白球(所有的球除颜色外其它均相同).现每次从暗箱中取出一个球后,再将此球以及与它同色的5个球(共6个球)一起放回箱中.
(Ⅰ)求第二次取出红球的概率;
(Ⅱ)求第三次取出白球的概率;
(Ⅲ)设取出白球得5分,取出红球得8分,求连续取球3次得分的分布列和数学期望. kalar12111年前1
kalar12111年前1 -
 alvin422 共回答了14个问题
alvin422 共回答了14个问题 |采纳率92.9%解题思路:(Ⅰ)设第n次取出白球、红球的概率分别为Pn,Qn,利用互斥事件加法公式能求出第二次取出红球的概率.
(Ⅱ)三次取的过程共有以下情况:白白白、白红白、红白白、红红白,由此能求出第三次取出白球的概率.
(Ⅲ)连续取球三次,得分的情况共有8种:5+5+5,8+5+5,5+8+5,5+5+8,8+8+5,8+5+8,5+8+8,8+8+8,分别求出X=15,18,21,24的概率,由此能求出连续取球3次得分的分布列和数学期望.(Ⅰ)设第n次取出白球、红球的概率分别为Pn,Qn,
第二次取出红球的概率Q2=[2/5×
3
3+5+
3
5×
3+5
5+5]=[3/5].
(Ⅱ)三次取的过程共有以下情况:白白白、白红白、红白白、红红白,
∴第三次取出白球的概率是:
P3=[2/5×
2+5
5+5×
2+5+5
5+5+5]+[2/5×
3
3+5×
2+5
5+5+5]+[3/5×
2
5+5×
2+5
5+5+5]+[3/5×
3+5
5+5×
2
5+5+5]=[2/5].
(Ⅲ)连续取球三次,得分的情况共有8种:
5+5+5,8+5+5,5+8+5,5+5+8,8+8+5,8+5+8,5+8+8,8+8+8,
P(X=15)=[2/5×
2+5
5+5×
2+5+5
5+5+5]=[28/125],
P(X=18)=[2/5×
3
5+5×
2+5
5+5+5+
2
5×
2+5
5+5×
3
5+5+5]+[3/5×
2
5+5×
2+5
5+5+5][21/125],
P(X=21)=[3/5×
3+5
5+5×
2
5+5+5+
2
5×
3
5+5×
3+5
5+5+5]+
3
5×点评:
本题考点: 离散型随机变量的期望与方差;相互独立事件的概率乘法公式.
考点点评: 本题考查概率的求法,考查离散型随机变量的分布列和数学期望的求法,解题时要认真审题,是中档题.1年前查看全部
- (2012•唐山二模)执行如图所示的算法,若输出的结果y≥2,则输入的x满足( )
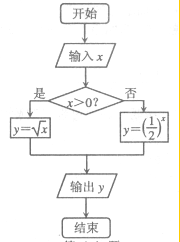 (2012•唐山二模)执行如图所示的算法,若输出的结果y≥2,则输入的x满足( )
(2012•唐山二模)执行如图所示的算法,若输出的结果y≥2,则输入的x满足( )
A.x≤-l或x≥4
B.x≤-l
C.-1≤x≤4
D.x≥4 AI_QIN1年前1
AI_QIN1年前1 -
 czg7871 共回答了19个问题
czg7871 共回答了19个问题 |采纳率94.7%解题思路:根据流程图所示的顺序,可知该程序的作用是计算分段函数的函数值,利用此分段函数的解析式求出相应的x的即可.由流程图可知,当x>0时,y=
x≥2,得x≥4,
当x≤0时,y=(
1
2)x≥2,得x≤-1,
综上可知输入的x的值是x≤-1或x≥4,
故选A点评:
本题考点: 选择结构.
考点点评: 题主要考查了选择结构、流程图等基础知识,算法是新课程中的新增加的内容,也必然是新高考中的一个热点,应高度重视.1年前查看全部
- (2011•盐城二模)如图所示,足够长的U型金属框架放置在绝缘斜面上,斜面倾角30°,框架的宽度l=1.0m
(2011•盐城二模)如图所示,足够长的U型金属框架放置在绝缘斜面上,斜面倾角30°,框架的宽度l=1.0m、质量M=1.0kg.导体棒ab垂直放在框架上,且可以无摩擦的运动.设不同质量的导体棒ab放置时,框架与斜面间的最大静摩擦力均为Fmax=7N.导体棒ab电阻R=0.02Ω,其余电阻一切不计.边界相距d的两个范围足够大的磁场Ⅰ、Ⅱ,方向相反且均垂直于金属框架,磁感应强度均为B=0.2T.导体棒ab从静止开始释放沿框架向下运动,当导体棒运动到即将离开Ⅰ区域时,框架与斜面间摩擦力第一次达到最大值;导体棒ab继续运动,当它刚刚进入Ⅱ区域时,框架与斜面间摩擦力第二次达到最大值.(g=10m/s2).求:
(1)磁场Ⅰ、Ⅱ边界间的距离d;
(2)欲使框架一直静止不动,导体棒ab的质量应该满足的条件;
(3)质量为1.6kg的导体棒ab在运动的全过程中,金属框架受到的最小摩擦力

分析:(1)导体棒即将离开Ⅰ时,金属框受到的安培力沿斜面向下,框架与斜面间摩擦力第一次达到最大值,根据平衡条件求出静摩擦力的最大值.根据安培力的表达式求出此时的速度.导体棒刚进入Ⅱ时,金属框受到的安培力沿斜面向上,根据平衡条件求出此时金属框受到的静摩擦力最大值.再由安培力表达式求出此时的速度.导体棒在两磁场边界之间做匀加速运动,由牛顿第二定律求出加速度,根据速度位移关系公式求出d.
在二区是安培力为什么向上,我判定几次了,结果都是向下
 xizmmdao1年前2
xizmmdao1年前2 -
 西来何往 共回答了10个问题
西来何往 共回答了10个问题 |采纳率90%进入二区时,磁通量的变化是向里增加,电流就应该反向了 即由a到b,用左手定则 手心向外,四指指向b 所以安培力是向上的1年前查看全部
- (2012•闵行区二模)硫酸铜是一种应用广泛的化工原料.实验室中可将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使
(2012•闵行区二模)硫酸铜是一种应用广泛的化工原料.实验室中可将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1所示).

(1)配制质量分数20%的硫酸需要100mL 98%的浓硫酸(密度为1.84g/cm3)和______mL蒸馏水.配制所需仪器除烧杯、量筒、胶头滴管外,还需要的仪器有______.
(2)图1中烧瓶中发生的离子反应方程式为______.
(3)图2是图1的改进装置,其优点有:①______;②______.
为符合绿色化学的要求,某研究性学习小组进行了如下设计:
方案1:以空气为氧化剂.将铜粉在某仪器A中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.反应后,过滤、蒸发、结晶等,用少量95%的酒精淋洗后晾干,得CuSO4•5H2O晶体.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加Fe2(SO4)3,即发生反应.反应完全后向其中先后加入物质甲、物质乙,取样检验后,过滤、蒸发、结晶,滤渣可循环使用.[已知Fe(OH)2、Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为9.6、3.7和6.4.]
(4)方案l中的A仅器名称是______.晶体采用酒精淋洗的优点是______.
(5)方案2中物质甲可以是______(选填答案编号,下同),物质乙可以是______.
a.Cub.CuCO3c.CuOd.氨水e.氯水f.双氧水
取样检验是为了确认Fe3+是否除净.有同学设计了以下两种方法:
方法①:取样于试管→滴加KSCN溶液;方法②:径向层析→喷KSCN溶液
指出你认为不合理的方法及存在的问题______.
(6)用铜粉制硫酸铜,上述方案1、方案2都不是十分理想,一种更符合绿色化学理念的是在氧气存在时用热稀硫酸与铜粉反应,其化学方程式是2Cu+O2+2H2SO4
2CuSO4+2H2O△ .2Cu+O2+2H2SO4.
2CuSO4+2H2O△ . kjh19821年前1
kjh19821年前1 -
 天堂衣 共回答了23个问题
天堂衣 共回答了23个问题 |采纳率91.3%解题思路:(1)根据配制溶液前后溶质的质量不变计算,浓硫酸配制稀硫酸注意利用玻璃棒不断搅拌;
(2)烧瓶中发生Cu与稀硝酸的氧化还原反应;
(3)图2中中间的装置可防止倒吸,并发生氮的氧化物与水的反应;
(4)由铜粉在某仪器A中反复灼烧,使铜与空气充分反应生成氧化铜分析;酒精与水互溶,除去晶体中的水并减少晶体溶解;
(5)加入的甲为氧化剂,能氧化亚铁离子;物质乙起调节pH的作用并除杂;确认Fe3+是否除净应注意铜离子的颜色造成的干扰;
(6)在氧气存在时用热稀硫酸与铜粉反应生成硫酸铜,以此书写化学反应方程式.(1)配制质量分数20%的硫酸需要100mL 98%的浓硫酸(密度为1.84g/cm3),设需要水xmL,
由配制溶液前后溶质的质量不变,则[100×1.84×98%/100×1.84+x×1]×100%=20%,解得x=717.6,浓硫酸稀释放出大量的热,应利用玻璃棒不断搅拌,
故答案为:717.6;玻璃棒;
(2)烧瓶中发生Cu与稀硝酸的氧化还原反应,离子反应为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
(3)由装置比较可知,装置2中多出的装置能①溶液不导管不直接接触,防止倒吸,②NO与氧气及碱反应,使有害气体能被完全吸收,故答案为:防止倒吸;有害气体能被完全吸收;
(4)由铜粉在某仪器A中反复灼烧,使铜与空气充分反应生成氧化铜,则A为坩埚,酒精与水互溶,除去晶体中的水并减少晶体溶解,则晶体采用酒精淋洗的优点是酒精与水互溶且极易挥发,减少晶体溶解,
故答案为:坩埚;酒精与水互溶且极易挥发,减少晶体溶解;
(5)由方案可知,Cu与Fe2(SO4)3反应,应除去亚铁离子,则加入f将亚铁离子氧化为铁离子,再利用bc促进铁离子水解转化为沉淀而除去,确认Fe3+是否除净的方法①中Cu2+的蓝色对检验有干扰,故答案为:f;bc;方法①中Cu2+的蓝色对检验有干扰;
(6)在氧气存在时用热稀硫酸与铜粉反应生成硫酸铜,该化学反应为2Cu+O2+2H2SO4
△
.
2CuSO4+2H2O,故答案为:2Cu+O2+2H2SO4
△
.
2CuSO4+2H2O.点评:
本题考点: 制备实验方案的设计;硝酸的化学性质;铜金属及其重要化合物的主要性质;配制一定物质的量浓度的溶液.
考点点评: 本题考查硫酸铜制备实验方案的设计,明确装置的作用及发生的氧化还原反应是解答本题的关键,注意除杂的方法及物质的成分、性质的差异、盐类水解的知识来解答,综合性较强,题目难度较大.1年前查看全部
- (2007•天河区二模)医疗上用的生理盐水是0.9%的氯化钠溶液.要配制0.9%的氯化钠溶液100g.下列配制过程正确的
(2007•天河区二模)医疗上用的生理盐水是0.9%的氯化钠溶液.要配制0.9%的氯化钠溶液100g.下列配制过程正确的是( )
A.只需要托盘天平和量筒两种仪器
B.用托盘天平称量,平衡时,左盘放0.9g氯化钠
C.用量筒量取100mL水
D.把食盐倒入装有100mL水的烧杯中,搅拌溶解 daijie09101年前1
daijie09101年前1 -
 一鬼卒 共回答了20个问题
一鬼卒 共回答了20个问题 |采纳率85%解题思路:根据使用固体配制溶液的操作过程为计算-称量-溶解,通过计算配制100g0.9%氯化钠溶液时所需要氯化钠和水的质量,判断配制过程所需要的仪器.A、配制溶液的步骤为计算、称量和溶解,称量时需要天平和量筒、胶头滴管,溶解时需要烧杯和玻璃棒,故需要的仪器为:托盘天平、玻璃棒、烧杯、量筒、胶头滴管,故A错误;
B、配制100g0.9%的氯化钠溶液时所需氯化钠质量=100g×0.9%=0.9g,称量时注意是左物右码,故应该在左盘放0.9g氯化钠,故B正确;
C、配制100g0.9%的氯化钠溶液所需要水的质量=100g-0.9g=99.1g,而水的密度为1g/mL,所以可以知道需要水的体积为99.1mL,所以应该用100mL的量筒来量取99.1mL水,故C错误;
D、根据C的判断可以知道,需要水的体积为99.1mL,故D错误.
故选B.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 通过回答本题知道了配制溶质质量分数一定的溶液的基本步骤和所用到的仪器,溶质和溶剂的计算方法,了解配制溶质质量分数一定的溶液的所用到的仪器.1年前查看全部
- (2005•宣武区二模)下列粒子示意图中,表示+3价阳离子的是( )
(2005•宣武区二模)下列粒子示意图中,表示+3价阳离子的是( )
A.
B.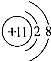
C.
D.
 世事难两全1年前1
世事难两全1年前1 -
 琉璃佛 共回答了24个问题
琉璃佛 共回答了24个问题 |采纳率95.8%解题思路:根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;+3价阳离子带有3的单位的正电荷;据此进行分析解答.+3价阳离子带有3的单位的正电荷.
A、质子数=核外电子数=10,为原子,故选项错误.
B、质子数=11,核外电子数=10,质子数>核外电子数,为阳离子;但该离子带有1个单位的正电荷,故选项错误.
C、质子数=12,核外电子数=10,质子数>核外电子数,为阳离子;但该离子带有2个单位的正电荷,故选项错误.
D、质子数=13,核外电子数=10,质子数>核外电子数,为阳离子;且该离子带有3个单位的正电荷,故选项正确.
故选D.点评:
本题考点: 原子结构示意图与离子结构示意图.
考点点评: 本题考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.1年前查看全部
- (2014•淄博二模)下列说法正确的是( )
(2014•淄博二模)下列说法正确的是( )
A.两种难溶物中溶解度小的物质其KSP不一定小
B.同种酸形成的酸式盐溶解度一定比正盐的溶解度大
C.因为Ksp(BaSO4)=1.08×l0-10,Ksp(BaCO3)=8.1×10-9,所以BaSO4沉淀不可能转化为BaCO3沉淀
D.相同温度下,将足量AgCl固体分别加入同体积的①0.1mo1•L-1盐酸、②0.1mo1•L-1氯化镁溶液、③0.1mo1•L-1硝酸银溶液中,c(Ag+):③>②>① lgzpp1年前1
lgzpp1年前1 -
 丝丝青烟 共回答了16个问题
丝丝青烟 共回答了16个问题 |采纳率87.5%解题思路:A.只有相同类型的难溶电解质,Ksp越小,溶解度可能会小;
B.碳酸氢钠的溶解度比碳酸钠小;
C.如生成沉淀,应满足Qc>Ksp;
D.根据溶解平衡AgCl(s)⇌Ag+(aq)+Cl-(aq)的影响因素判断.A.溶度积的大小与溶解度不一定是成正比的,如 BaSO4和Mg(OH)2两物质,溶解度BaSO4为2.4×10-4 g,Mg(OH)2为9×10-4 g,Mg(OH)2比BaSO4的溶解度大.溶度积Ksp(BaSO4)=1.1×10-10,而Ksp[Mg(OH)2]=1.8×10-...
点评:
本题考点: 难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查难溶电解质的溶解平衡,为高频考点,侧重于学生的分析能力的考查,注意Ksp的意义以及难溶电解质的溶解平衡的影响因素,难度不大.1年前查看全部
- (2014•宜宾二模)右面茎叶图表示的是甲、乙两人在5次综合测评中的成绩,其中一个数字被污损.则甲的平均成绩超过乙的平均
 (2014•宜宾二模)右面茎叶图表示的是甲、乙两人在5次综合测评中的成绩,其中一个数字被污损.则甲的平均成绩超过乙的平均成绩的概率为( )
(2014•宜宾二模)右面茎叶图表示的是甲、乙两人在5次综合测评中的成绩,其中一个数字被污损.则甲的平均成绩超过乙的平均成绩的概率为( )
A.[2/5]
B.[7/10]
C.[4/5]
D.[9/10] 原俗1年前1
原俗1年前1 -
 宇献枫玲 共回答了22个问题
宇献枫玲 共回答了22个问题 |采纳率100%解题思路:由已知的茎叶图,我们可以求出甲乙两人的平均成绩,然后求出
≤.甲
即甲的平均成绩不超过乙的平均成绩的概率,进而根据对立事件减法公式得到答案..乙 由已知中的茎叶图可得
甲的5次综合测评中的成绩分别为88,89,90,91,92,
则甲的平均成绩
.
甲=[88+89+90+91+92/5]=90
设污损数字为X,
则乙的5次综合测评中的成绩分别为83,83,87,99,90+X
则乙的平均成绩
.
乙=[83+83+87+99+90+X/5]=88.4+[x/5]
当X=8或9时,
.
甲≤
.
乙
即甲的平均成绩不超过乙的平均成绩的概率为[2/10]=[1/5]
则甲的平均成绩超过乙的平均成绩的概率P=1-[1/5]=[4/5]
故选C点评:
本题考点: 众数、中位数、平均数;茎叶图.
考点点评: 本题考查的知识点是平均数,茎叶图,古典概型概率计算公式,其中根据已知茎叶图求出数据的平均数是解答本题的关键.1年前查看全部
- (2006•昌平区二模)如图所示的太阳能热水器,水箱内装有120kg水,若水温由20℃升高到70℃,水吸收的热量是多少J
 (2006•昌平区二模)如图所示的太阳能热水器,水箱内装有120kg水,若水温由20℃升高到70℃,水吸收的热量是多少J?(4.2×103J/(kg•℃) )
(2006•昌平区二模)如图所示的太阳能热水器,水箱内装有120kg水,若水温由20℃升高到70℃,水吸收的热量是多少J?(4.2×103J/(kg•℃) )  红梦紫衣1年前1
红梦紫衣1年前1 -
 Oo漠漠oo 共回答了21个问题
Oo漠漠oo 共回答了21个问题 |采纳率81%解题思路:根据Q=cm(t-t0)求出水吸收的热量.已知:质量m=120kg,初温t0=20℃,末温t=70℃,比热c=4.2×103J/(kg•℃)
求:水吸收的热量Q=?
水吸收的热量:
Q=cm(t-t0)=4.2×103J/(kg•℃)×120 kg×(70℃-20℃)=2.52×107J.
答:水吸收的热量是2.52×107J.点评:
本题考点: 太阳能热水器中的热量计算.
考点点评: 此题主要考查的是学生对热量计算公式的理解和掌握,基础性题目.1年前查看全部
- (2012•大连二模)用酒精灯给烧杯里的水加热,把150g的水从20℃加热到100℃,燃烧了10g的酒精,设酒精完全燃烧
(2012•大连二模)用酒精灯给烧杯里的水加热,把150g的水从20℃加热到100℃,燃烧了10g的酒精,设酒精完全燃烧.已知酒精的热值为3×107J/kg,水的比热容为4.2×103J/(kg•℃).试求:
(1)水吸收的热量是多少?
(2)用酒精灯烧水时的效率是多少? jose234671年前1
jose234671年前1 -
 深圳高贵qq 共回答了19个问题
深圳高贵qq 共回答了19个问题 |采纳率84.2%解题思路:(1)水吸收的热量可用公式Q=cm△t来计算.
(2)酒精完全燃烧放出的热量可用Q放=qm来计算.对酒精灯来说,有用功为被水吸引的热量,总功为酒精完全燃烧放出的热量,酒精灯的效率可用公式η=
×100%来计算.W有用 W总 m水=150g=0.15kg,
(1)Q=cm(t末-t初)=4.2×103J/(kg•℃)×0.15kg×(100℃-20℃)=5.04×104J;
(2)Q放=qm=3.0×107J/kg×(10×10-3kg)=3×105J,
η=
W有用
W总×100%=
5.04×104J
3×105J×100%=16.8%
答:(1)水吸收的热量为5.04×104J;
(2)用酒精灯烧水时的效率是为16.8%.点评:
本题考点: 热平衡方程的应用.
考点点评: 考查了学生对吸热公式、燃料完全燃烧放热公式、效率公式的掌握和运用,知道酒精完全燃烧放出的热量不能完全被水吸收是本题的关键.1年前查看全部
- (2014•和平区二模)在△ABC中,AB=AC,以AB为直径的⊙O交BC于点D,交AC于点E,DF为⊙O的切线,
(2014•和平区二模)在△ABC中,AB=AC,以AB为直径的⊙O交BC于点D,交AC于点E,DF为⊙O的切线,

(1)如图①,求∠DFC的度数;
(2)如图②,过点A作BC的平行线交BE的延长线于点G,连接CG,当△ABC时等边三角形时,求∠AGC的度数. 永远的支持者1年前0
永远的支持者1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•临沂二模)下列有关四个电化学装置的叙述正确的是( )
(2014•临沂二模)下列有关四个电化学装置的叙述正确的是( )

A.图Ⅰ装置中MnO2作催化剂
B.图Ⅱ装置工作一段时间后,滴加少量K3[Fe(CN)6]溶液,无明显现象
C.图Ⅲ装置中Cu作阳极,为电解液提供Cu2+,保持溶液中Cu2+浓度恒定
D.图Ⅳ装置工作时,为平衡电荷,a烧杯中的Zn2+经盐桥移向b烧杯中 mywebpage1年前1
mywebpage1年前1 -
 hougao 共回答了15个问题
hougao 共回答了15个问题 |采纳率86.7%解题思路:A.二氧化锰作正极;
B.形成原电池反应,铁为负极,被氧化生成Fe2+;
C.为电镀装置,电解液浓度不变;
D.锌为负极,盐桥中阴离子向a移动,阳离子向b移动.A.该电池反应中二氧化锰得到电子被还原,为原电池的正极,故A错误;
B.形成原电池反应,铁为负极,被氧化生成Fe2+,滴加少量K3[Fe(CN)6]溶液,生成蓝色沉淀,故B错误;
C.为电镀装置,电解液浓度不变,故C正确;
D.锌为负极,盐桥中阴离子向a移动,阳离子向b移动,故D错误.
故选C.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查原电池和电解池原理,为高频考点,侧重于学生的分析能力的考查,明确电极上发生的反应是解本题关键,难度不大.1年前查看全部
- (2012•和平区二模)写出下列反应的化学方程式:
(2012•和平区二模)写出下列反应的化学方程式:
(1)实验室用过氧化氢制氧气2H2O2
2H2O+O2↑MnO2 .2H2O2;
2H2O+O2↑MnO2 .
(2)铜丝加入到硝酸银溶液中______;
(3)酒精燃烧C2H5OH+3O2
2CO2+3H2O点燃 .C2H5OH+3O2;
2CO2+3H2O点燃 .
(4)碳化钙(CaC2)与水反应生成氢氧化钙和乙炔(C2H2)气体______. taoyongjun08241年前1
taoyongjun08241年前1 -
 xzf007 共回答了25个问题
xzf007 共回答了25个问题 |采纳率84%解题思路:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.(1)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
MnO2
.
2H2O+O2↑.
(2)铜丝加入到硝酸银溶液中生成硝酸铜和银,反应的化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag.
(3)酒精燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2
点燃
.
2CO2+3H2O.
(4)碳化钙(CaC2)与水反应生成氢氧化钙和乙炔(C2H2)气体,反应的化学方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑.
故答案为:(1)2H2O2
MnO2
.
2H2O+O2↑;
(2)Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)C2H5OH+3O2
点燃
.
2CO2+3H2O;
(4)CaC2+2H2O═Ca(OH)2+C2H2↑.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.1年前查看全部
- (2010•卢湾区二模)如图,在平面直角坐标系xOy中,抛物线y=-[1/2]x2+bx+c经过点A(1,3),B(0,
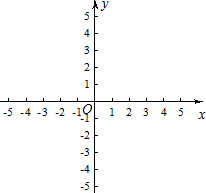 (2010•卢湾区二模)如图,在平面直角坐标系xOy中,抛物线y=-[1/2]x2+bx+c经过点A(1,3),B(0,1).
(2010•卢湾区二模)如图,在平面直角坐标系xOy中,抛物线y=-[1/2]x2+bx+c经过点A(1,3),B(0,1).
(1)求抛物线的表达式及其顶点坐标;
(2)过点A作x轴的平行线交抛物线于另一点C,
①求△ABC的面积;
②在y轴上取一点P,使△ABP与△ABC相似,求满足条件的所有P点坐标. 最love石头1年前0
最love石头1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•崇明县二模)如图所示的是酶、激素、蛋白质、抗体四者关系.下列有关叙述正确的是( )
(2014•崇明县二模)如图所示的是酶、激素、蛋白质、抗体四者关系.下列有关叙述正确的是( )

A.1、2、3分别表示激素、酶、蛋白质
B.能产生4的细胞一定能产生1
C.能产生3的细胞一定能产生4
D.物质1和3都具有专一性,属于高效能物质 水色鱼1年前1
水色鱼1年前1 -
 雨玲儿520 共回答了26个问题
雨玲儿520 共回答了26个问题 |采纳率92.3%解题思路:由题意知,1、2、3、4是激素、蛋白质、酶、抗体,绝大多数酶的本质是蛋白质,抗体属于蛋白质,大多数的激素的本质是蛋白质,蛋白质包括抗体、酶、激素等,因此分析题图可以看出:1是激素,2是蛋白质,3是酶,4是抗体.A、由题图知,1、2、3分别表示激素、蛋白质、酶,A错误;
B、激素是由专门的内分泌器官或细胞产生的,产生抗体的浆细胞不能产生激素,B错误;
C、所有的活细胞均能产生酶,抗体是由浆细胞产生的,产生酶的细胞不一定能产生抗体,C错误;
D、酶和激素的作用都具有专一性,且都是微量、高效的,D正确.
故选:D.点评:
本题考点: 酶的特性;蛋白质在生命活动中的主要功能.
考点点评: 对于酶、激素、蛋白质、抗体概念之间关系的理解、建构合理的概念图的能力是本题考查的重点.1年前查看全部
- (2011•普陀区二模)假设a、B为玉米的优良基因,现有AABB、aabb两个品种,控制两对相对性状的基因位于两对同源染
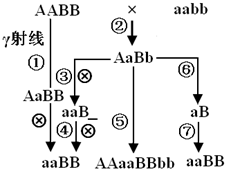 (2011•普陀区二模)假设a、B为玉米的优良基因,现有AABB、aabb两个品种,控制两对相对性状的基因位于两对同源染色体上,实验小组用不同方法进行了实验(见图),下列说法不正确的是( )
(2011•普陀区二模)假设a、B为玉米的优良基因,现有AABB、aabb两个品种,控制两对相对性状的基因位于两对同源染色体上,实验小组用不同方法进行了实验(见图),下列说法不正确的是( )
A.过程①育种方法运用的原理是基因突变,最大优点是能提高突变率,在短时间内获得更多的变异类型
B.过程②③④育种方法运用的原理是基因重组,基因型aaB_的类型经④后,子代中aaBB所占比例是5/6
C.过程⑥和⑦应用了单倍体育种的方法,最大的优点是明显缩短育种年限
D.过程⑤和⑦处理方法相同 第六根手指141年前1
第六根手指141年前1 -
 vincentcph 共回答了25个问题
vincentcph 共回答了25个问题 |采纳率96%解题思路:根据题意和图示分析可知:①是诱变育种,利用基因突变原理,最大优点是能提高突变率,在短时间内获得更多的优良变异类型;②③④是杂交育种,育种原理是基因重组,基因型aaB_的类型经④后,子代中aaBB所占比例是[1/2];②⑤是多倍体育种,原理是染色体变异,⑤过程是使用秋水仙素处理萌发的种子或幼苗,它可作用于正在分裂的细胞,抑制纺锤体的形成;②⑥⑦是单倍体育种,最大优点是明显缩短育种年限.A、图示①用r射线处理表示诱变育种,原理是基因突变,优点是能提高突变率,在短时间内获得更多的变异类型,大幅度改良生物性状,A正确;
B、②③④是典型的杂交育种,原理是基因重组,过程是杂交-自交-筛选-连续自交、筛选,基因型aaB_的组成中,aaBB占[1/3],aaBb占[2/3],则其自交后代中aaBB的比例是[1/3]+[2/3]×[1/4]=[1/2],B错误;
C、②⑥⑦表示的育种方法是单倍体育种,原理是染色体变异,方法是花药离体培养,其优点是明显缩短育种年限,C正确;
D、过程⑤和⑦都可用秋水仙素处理幼苗,抑制细胞有丝分裂过程中纺锤体的形成,使细胞染色体数目加倍,D正确.
故选:B.点评:
本题考点: 生物变异的应用;杂交育种;诱变育种.
考点点评: 本题以玉米为素材,综合考查诱变育种、杂交育种、多倍体育种和单倍体育种的相关内容,意在考查考生的识记能力、识图能力和理解应用能力.1年前查看全部
- (2014•泰安二模)以下命题:
(2014•泰安二模)以下命题:
①为了了解800名学生对学校某项教改试验的意见,打算从中抽取一个容量为40的样本,考虑用系统抽样,则分段的间隔k为40.
②线性回归直线方程
=
y
x+
b
恒过样本中心(
a
,.x
),且至少过一个样本点;.y
③复数z=(a-2i)i(a∈R,i为虚数单位)在复平面内对应的点为M,则“a<0“是“点M在第四象限”的充要条件.
其中真命题的个数为( )
A.0
B.1
C.2
D.3 小沙11年前1
小沙11年前1 -
 kid601 共回答了10个问题
kid601 共回答了10个问题 |采纳率80%解题思路:由系统抽样间隔号的求法求出间隔号判断①;
利用线性回归直线方程的意义,即恒过样本中心点但不一定过样本点判断②;
由充要条件的概念判断③.对于①,总体容量N=800,样本容量n=40,则用系统抽样的分段的间隔k=[800/40=20,命题①为假命题;
对于②,线性回归直线方程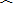
y]=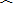
bx+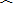
a恒过样本中心(
.
x,
.
y),但不一定过样本点,命题②为假命题;
对于③,∵复数z=(a-2i)在复平面内对应的点M(a,-2),
对于④,∵复数z=(a-2i)i=2+ai(a∈R,i为虚数单位)在复平面内对应的点为M,则“a<0“是“点M在第四象限”的充要条件.命题③为真命题.
∴真命题的个数为1.
故选:B.点评:
本题考点: 命题的真假判断与应用.
考点点评: 本题考查了命题的真假判断与应用,关键是对教材基础概念和基础知识的熟练掌握,是中档题.1年前查看全部
- (2011•昌平区二模)下列属于通过做功途径改变物体内能的是( )
(2011•昌平区二模)下列属于通过做功途径改变物体内能的是( )
A.在炉上烧水,水温升高
B.感冒发烧,用冷毛巾敷额头
C.冬天对手“哈气”,手感到暖和
D.冬天两手相互摩擦,手感到暖和 denny_ldy1年前1
denny_ldy1年前1 -
 xzren 共回答了16个问题
xzren 共回答了16个问题 |采纳率93.8%解题思路:改变物体内能有两种方式:做功和热传递.做功实质是能量的转化,热传递实质是内能从一个物体转移到另一个物体,或者是从一个物体的高温部分传到低温部分,有传导、对流和辐射三种方式,据此分析判断.在火炉上烧水时水温升高,感冒发烧时用冷毛巾敷额头,冬天对手“哈气”手感到暖和,都是热传递改变物体的内能,故A、B、C都不符合题意;
冬天两手相互摩擦,手感到暖和,是通过做功把机械能转化为内能,属于做功改变物体的内能.
故选D.点评:
本题考点: 做功改变物体内能;热传递改变物体内能.
考点点评: 本题主要考查学生对改变物体内能两种方法的了解与掌握,掌握做功和热传递的实质是关键,是中招的热点.1年前查看全部
- (2008•宝山区二模)A、B、C是平面内的三点,AB=1,BC=2,AC=3,则下列说法中正确的是( )
(2008•宝山区二模)A、B、C是平面内的三点,AB=1,BC=2,AC=3,则下列说法中正确的是( )
A.可以画一个圆,使A、B、C都在圆上
B.可以画一个圆,使A、B在圆上,C在圆内
C.可以画一个圆,使A、C在圆上,B在圆内
D.可以画一个圆,使B、C在圆上,A在圆内 chenzheng8881年前1
chenzheng8881年前1 -
 希望好运 共回答了19个问题
希望好运 共回答了19个问题 |采纳率89.5%解题思路:由已知可得AB+BC=AC,因而点B是线段AC上的点,进而可知可以画一个圆,使A,C在圆上,B在圆外.∵A,B,C是平面内的三点,AB=1,BC=2,AC=3,
∴AB+BC=AC,则B是线段AC上的点,
∴可以画一个圆,使A,C在圆上,B在圆外.
故选C.点评:
本题考点: 点与圆的位置关系.
考点点评: 本题考查了点与圆的位置关系,正确确定A、B、C三点的位置关系是解决本题的关键.1年前查看全部
- (2011•徐汇区二模)如图(a)所示,将两个底面削平的铅柱紧压在一起,下面吊一个重物也不能把它们拉开,说明分子间存在_
 (2011•徐汇区二模)如图(a)所示,将两个底面削平的铅柱紧压在一起,下面吊一个重物也不能把它们拉开,说明分子间存在______(选填“引力”或“斥力”);如图(b)所示,在一个配有活塞的厚玻璃筒里放一小团蘸了乙醚的棉花.把活塞迅速压下去,棉花燃烧起来.这说明活塞对气体______,增加了气体的内能,使气体的温度______.
(2011•徐汇区二模)如图(a)所示,将两个底面削平的铅柱紧压在一起,下面吊一个重物也不能把它们拉开,说明分子间存在______(选填“引力”或“斥力”);如图(b)所示,在一个配有活塞的厚玻璃筒里放一小团蘸了乙醚的棉花.把活塞迅速压下去,棉花燃烧起来.这说明活塞对气体______,增加了气体的内能,使气体的温度______.  哇里哈1年前1
哇里哈1年前1 -
 vivioops 共回答了15个问题
vivioops 共回答了15个问题 |采纳率93.3%解题思路:分子之间存在相互作用的引力和斥力.做功可以改变物体的内能,外界对物体做功,物体的内能增大,温度升高.两个底面削平的铅柱紧压在一起,下面吊一个重物也不能把它们拉开,说明分子之间存在相互作用的引力.
当活塞迅速压下去时,活塞对气体做功,使气体的内能增大,温度升高,达到棉花的着火点,因此棉花燃烧起来.
故答案为:引力;做功,升高.点评:
本题考点: 分子间的作用力;做功改变物体内能.
考点点评: 本题考查的知识点有两个:一是分子之间存在相互作用的引力和斥力;二是做功可以改变物体的内能,对物体做功,物体的内能增大,温度升高.1年前查看全部
- (2009•青岛二模)(1)关于分子运动和热现象的说法,正确的是______(填入正确选项前的字母)
 (2009•青岛二模)(1)关于分子运动和热现象的说法,正确的是______(填入正确选项前的字母)
(2009•青岛二模)(1)关于分子运动和热现象的说法,正确的是______(填入正确选项前的字母)
A.布朗运动是指液体或气体中悬浮微粒的运动
B.气体的温度升高,每个气体分子运动的速率都增加
C.一定量100℃的水变成100℃的水蒸汽,其分子之间的势能增加
D.空调机作为制冷机使用时,将热量从温度较低的室内送到温度较高的室外,所以制冷机的工作不遵循热力学第二定律
(2)图示为活塞式空压机的结构简图.某次往复运动中,活塞向右运动至气缸最右端时,吸气阀打开吸入压强为 p0 的空气,然后连杆推动活塞向左运动压缩空气,当压强达到3p0时排气阀打开排出空气,以保证产生符合要求的压力.若整个气缸内允许活塞往复运动的长度为L0,不考虑气体温度的变化,求活塞向左运动多少距离时空压机开始排气. bestrow1年前1
bestrow1年前1 -
 fighter2006 共回答了17个问题
fighter2006 共回答了17个问题 |采纳率76.5%解题思路:(1)A、布朗运动是悬浮在液体或气体中固体小颗粒的无规则运动;B、温度是分子平均动能的标志,温度高的物体分子平均动能大,并不是每个分子动能都大;C、温度相同分子平均动能相同,水汽化要吸收热量,内能增加,增加的内能转化为分子势能;D、空调机制冷并没有违反热力学第二定律,因为在制冷过程中空调机电流做了功.(2)气体温度不变,是等温变化,由玻意耳定律可以分析答题.(1)A、布朗运动是指液体或气体中悬浮微粒的运动,故A正确;
B、气体的温度升高,气体分子运动的平均速率增加,并不是每个分子的速率都增加,故B错误;
C、一定量100℃的水变成100℃的水蒸汽需要吸收热量,内能增加,由于温度不变,分子动能不变,则增加的内能转化为分子势能,其分子之间的势能增加,故C正确;
D、空调机作为制冷机使用时,空气压缩机做功,要消耗电能,制冷过程不是自发进行的,制冷时将热量从温度较低的室内送到温度较高的室外,所以制冷机的工作遵循热力学第二定律,故D错误;
故选AC.
(2)设活塞截面积为 S,开始排气时气体长度为 L,
由玻意耳定律得:p0L0S=3p0Ls,解得:L=
L0
3,
即活塞向左运动的距离d=L0-L=
2L0
3时空压机开始排气.
答:(1)AC.
(2)活塞向左运动的距离
2L0
3时空压机开始排气.点评:
本题考点: 理想气体的状态方程;热力学第二定律.
考点点评: (1)理解布朗运动的实质、掌握分子动理论内容与热力学第二定律内容即可正确解题,要注意基础知识的掌握.(2)理解题意,应用玻意耳定律即可正确解题.1年前查看全部
- (2013•资阳二模)在调查南方某块弃耕农田时,发现原来的田埂都淹没在杂草之中,只有零星的作物.调查中同学们观察到食草昆
 (2013•资阳二模)在调查南方某块弃耕农田时,发现原来的田埂都淹没在杂草之中,只有零星的作物.调查中同学们观察到食草昆虫、青蛙、蜘蛛和蛇类等动物.请回答以下问题:
(2013•资阳二模)在调查南方某块弃耕农田时,发现原来的田埂都淹没在杂草之中,只有零星的作物.调查中同学们观察到食草昆虫、青蛙、蜘蛛和蛇类等动物.请回答以下问题:
(1)在农田中,蛇的红外线感知器发现青蛙时,便快速移动进而准确捕食到青蛙,这说明信息传递在生态系统中具有______作用.农田中含碳元素最多的生物属生态系统成分中的______.
(2)生物防治农林害虫的方法之一是:在田间释放过量的人工合成性引诱剂,从而干扰害虫的正常交尾活动,使害虫种群的______下降,进而降低种群密度,降低对作物的危害.
(3)图1中曲线A表示该农田中群落所含能量的变化,则曲线______表示农田弃耕后植物的物种数变化.
(4)若在“植物→植食昆虫→…→蛇”这条食物链中,已知某营养级生物的同化量是a千焦,则其后面某营养级生物获得最多能量值的数学模型为______(…代表其中未写完的营养级,用b代表待求生物获得的能量、n和m分别代表待求的和已知同化量生物的营养级;模型成立的条件:相邻两个营养级之间能量的传递效率相同).
(5)同学们调查了农田中种植四种不同作物的土壤小动物数量.请完善图2采集土壤小动物的装置(在图中以图示或语言表示).______. 火凤凰啊1年前1
火凤凰啊1年前1 -
 大张水 共回答了17个问题
大张水 共回答了17个问题 |采纳率88.2%解题思路:1、信息传递在生态系统中的作用:
(1)个体:生命活动的正常进行,离不开信息的传递.
(2)种群:生物种群的繁衍,离不开信息的传递.
(3)群落和生态系统:能调节生物的种间关系,以维持生态系统的稳定.
2、昆虫的交配求偶就是通过性信息素的传递来实现的.所谓性信息素是指雌虫分泌到体外以引诱雄虫前去交配的微量化学物质.根据这一原理,利用高新技术,人工合成信息素即性引诱剂,制成对同种异性个体有较大吸引力的诱芯,结合诱捕器(水盆式、粘胶式)配套使用.在田间释放后,形成“假姑娘”(性引诱剂)引来“真小伙”(田间的雄虫),从而使得种群的性别比例失调,大幅度降低产卵量和孵化率(出生率),达到防治害虫目的.
3、群落演替过程中物种多样性增强,自我调节能力增强.
4、低营养级求高营养级,最少×10%,最多×20%.
5、图中在去底花盆中放一个金属网,将收集到的土壤样品放置在金属网上,然后,将花盆放在诱虫器上,再打开电灯,才可收集小动物.(1)在农田中,蛇的红外线感知器发现青蛙时,便快速移动进而准确捕食到青蛙,这说明信息传递在生态系统中具有调节种间关系,维持生态系统的稳定作用.农田中含碳元素最多的生物是生产者.
(2)利用人工合成的性引诱剂诱杀某种害虫的雄性个体,破坏害虫种群正常的性别比例,就会使很多雌性个体不能完成交配,从而使该害虫的种群密度明显降低,达到控制害虫数量的目的.
(3)图1中曲线A表示该农田中群落所含能量的变化,则曲线C表示农田弃耕后植物的物种数变化.
(4)能量传递率为10%-20%,在“植物→植食昆虫→…→蛇”这条食物链中,已知某营养级生物的同化量是a千焦,则其后面某营养级生物获得最多能量值的数学模型为b=a×(20%)n-m(b代表待求生物获得的能量、n和m分别代表待求的和已知同化量生物的营养级).
(5)土壤动物具有趋暗、趋湿、避高温的习性,为了探究该弃耕农田土壤小动物类群丰富度,应该在漏斗上方加一提供光源和热源的灯泡.
故答案为:
(1)调节种间关系,维持生态系统的稳定(答到“调节种间关系”即可);生产者;
(2)出生率;
(3)C;
(4)b=a×(20%)n-m;
(5)在漏斗上方加一(提供光源和热源的)灯泡
或者如图
点评:
本题考点: 生态系统中的信息传递;土壤中动物类群丰富度的研究;生态系统的结构.
考点点评: 本题考查生态系统的信息传递、种群特征、群落演替、生态系统能量流动、调查土壤小动物的物种丰富度,意在考查学生的识记和理解能力,属于中档题.1年前查看全部
- (2014•商丘二模)不用其他任何试剂就可以鉴别①NaOH②H2SO4③CuSO4④NaCl四种溶液,则鉴别出来的先后顺
(2014•商丘二模)不用其他任何试剂就可以鉴别①NaOH②H2SO4③CuSO4④NaCl四种溶液,则鉴别出来的先后顺序正确的是( )
A.①②③④
B.③①②④
C.②①③④
D.③②①④ yysbjb1年前1
yysbjb1年前1 -
 xwg1999 共回答了18个问题
xwg1999 共回答了18个问题 |采纳率94.4%解题思路:在不另加试剂就能鉴别的题目中,首先观察有无有特殊颜色的物质,若有,将有颜色的溶液鉴别出来,然后再借用这种溶液鉴别其它溶液把其它没有确定出的物质确定出来;若都没有颜色就将溶液两两混合,根据混合后的现象进行分析鉴别.①NaOH②H2SO4③CuSO4④NaCl四种溶液中,CuSO4溶液呈蓝色,首先鉴别出蓝色的CuSO4溶液;把CuSO4溶液与另外三种溶液混合,出现蓝色沉淀的溶液为NaOH溶液;再把剩余的两种溶液滴加到产生的蓝色沉淀中,能使沉淀溶解的是蓝色,无明显变化的是NaCl溶液;故将它们一一鉴别开来鉴别出来的先后顺序可能是③①②④或③①④②.
故选:B.点评:
本题考点: 酸、碱、盐的鉴别.
考点点评: 本题难度较大,解此类题的思路是:先用物理性质,一般先看颜色、闻气味;再用化学性质,用两两混合的方式,根据不同的实验现象进行鉴别.1年前查看全部
- (2012•黄浦区二模)(五)根据免疫知识,回答下列问题.
 (2012•黄浦区二模)(五)根据免疫知识,回答下列问题.
(2012•黄浦区二模)(五)根据免疫知识,回答下列问题.
如图为病原微生物侵入人体后的主要免疫过程.中的字母编号表示参与免疫的各种细胞或由它们产生的某些物质,数字表示生理作用过程.据图回答问题:
(1)图中A是______细胞,F是______细胞;B细胞的作用是______.
(2)图中表示细胞免疫的过程是______(用数字和箭头表示),其中过程______是非特异性免疫过程.
(3)B淋巴细胞与______细胞融合后,在体外培养可获得______. cd02liu1年前1
cd02liu1年前1 -
 yuehuang 共回答了20个问题
yuehuang 共回答了20个问题 |采纳率90%解题思路:本题重点是免疫过程,免疫包括非特异性免疫和特异性免疫,非特异性免疫是生来就有的,对多种病原体起作用,特异性免疫是后天形成的,只对特定的病原体琪作用,又包括细胞免疫和体液免疫.体液免疫:大多数病原体经吞噬细胞的摄取、处理,暴露出特有的抗原,将抗原呈递给T细胞,T细胞产生淋巴因子,在淋巴因子的作用下,T细胞将抗原传递B细胞,B细胞接受刺激开始增值分化大部分转化为浆细胞,产生抗体,小部分形成记忆细胞,抗体与病原体结合,抑制病原体繁殖或对人体细胞的黏附.记忆细胞可以在抗原消失后很长时间保持对这种抗原的记忆.当再接触这种抗原时,迅速增值分化形成浆细胞,产生大量抗体.
细胞免疫:T细胞接受抗原刺激后开始增值分化大部分转化为效应T细胞和部分记忆,效应T细胞与靶细胞接触,使靶细胞裂解死亡,病原体失去寄生的基础,从而被吞噬消灭.记忆细胞的作用是当再接触这种抗原时,迅速增值分化形成效应T细胞,参与免疫反应.
故答案应是:
(1)浆 巨噬 记忆入侵的抗原,当再次接受同一抗原刺激时,快速增殖分化,产生更多新的记忆B细胞与浆细胞参与免疫过程
(2)④-⑤-⑥-⑦-⑧④⑤
(3)骨髓瘤 单克隆抗体点评:
本题考点: 人体免疫系统在维持稳态中的作用.
考点点评: 本题 从题图入手,回忆细胞免疫与体液免疫的具体过程,确定序号及字母编号过程名称,直接作答.1年前查看全部
- (2014•陕西二模)如图,已知PA是⊙O的切线,A为切点.PC是⊙O的一条割线,交⊙O于B,C两点,点Q是弦BC的中点
(2014•陕西二模)如图,已知PA是⊙O的切线,A为切点.PC是⊙O的一条割线,交⊙O于B,C两点,点Q是弦BC的中点.若圆心O在∠APB内部,则∠OPQ+∠PAQ的度数为______.

 Haggis1年前0
Haggis1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 2010海淀二模数学14题怎么做
 lulangli1年前1
lulangli1年前1 -
 ciotopd 共回答了20个问题
ciotopd 共回答了20个问题 |采纳率95%这个题目关键是准确理解符号的含义
第一个条件,是说f(i)这一行的各个数组都不相等,第一行是1234...n,第二行也是1234...n,也就是说是一一映射.
第二个条件,f(1),f(2)...f(m)之中能够找到m,对应成表格就是除了1以外,2前面(或对应位置)有2,3前面有3,4前面有4...n前面有n
第一问,满足第二个条件的话第一空必须是2,后两个随便.
第二问,你可以列一个表试一下,如果第一个格是1,那么后面每一个格都和对应的i相等.所以第一个不是1,f(i)=i有6个解,也就是有6个i和f(i)对应,共有C6(9)=84种(1不能对应),之后1和剩下三个数不对应,只能排出一种(建议自己花个表试一下).所以这一空填84.1年前查看全部
- (2007•东城区二模)关于电流和电源,下列说法中正确的是( )
(2007•东城区二模)关于电流和电源,下列说法中正确的是( )
A.电路中只要有电源,就一定有电流
B.电流是由电荷的无规则运动形成的
C.在电源外部的电路中电流从电源的正极流向负极
D.金属导体中的电流方向,就是自由电子的定向移动方向 深南大道西1年前1
深南大道西1年前1 -
 badamazon 共回答了19个问题
badamazon 共回答了19个问题 |采纳率100%解题思路:根据以下知识分析答题:
(1)电路中有电流的条件是:电路闭合,且电路中有电源;
(2)电荷的定向移动形成电流,正电荷的定向移动方向是电流的方向;
(3)在电源外部,电流由正极流向负极.A、电路中有电源,如果电路没有闭合,则电路中没有电流,故A错误;
B、电荷的定向移动方向形成电流,电荷的无规则运动不会形成电流,故B错误;
C、在电源外部,电流由电源正极流向电源负极,故C正确;
D、电子带负电,金属导体中电流的方向与电子定向移动的方向相反,故D错误;
故选C.点评:
本题考点: 电流的方向;电流的形成.
考点点评: 本题考查了形成电流的条件、电流概念、电流方向等问题,熟练应用基础知识即可正确解题.1年前查看全部
- (2013•洛阳二模)下列运算正确的是( )
(2013•洛阳二模)下列运算正确的是( )
A.a2•a3=a6
B.(a-2)2=a2-4
C.−4a−2=1 4a2
D.(−
a2b)3=−1 2
a6b31 8  qshy19791年前1
qshy19791年前1 -
 newliving1979 共回答了18个问题
newliving1979 共回答了18个问题 |采纳率83.3%解题思路:A、原式利用同底数幂乘法法则计算得到结果,即可做出判断;
B、原式利用完全平方公式展开得到结果,即可做出判断;
C、原式利用负指数幂法则计算得到结果,即可做出判断;
D、原式利用积的乘方及幂的乘方运算法则计算得到结果,即可做出判断.A、a2•a3=a5,本选项错误;
B、(a-2)2=a2-4a+4,本选项错误;
C、-4a-2=-[4
a2,本选项错误;
D、(-
1/2]a2b)3=-[1/8]a6b3,本选项正确.
故选D.点评:
本题考点: 完全平方公式;同底数幂的乘法;幂的乘方与积的乘方;负整数指数幂.
考点点评: 此题考查了完全平方公式,同底数幂的乘法,幂的乘方及积的乘方,以及负指数幂,熟练掌握公式及法则是解本题的关键.1年前查看全部
- (2014•辽宁二模)下列说法正确的是( )
(2014•辽宁二模)下列说法正确的是( )
A.受迫振动的周期取决于驱动力的周期
B.未见其人先闻其声,是因为声波波长较长,容易发生衍射现象
C.声波频率的大小取决于在某种介质中传播的速度和波长的大小
D.偏振现象说明光是横波 jcyyp1年前1
jcyyp1年前1 -
 妖精小店 共回答了16个问题
妖精小店 共回答了16个问题 |采纳率100%解题思路:受迫振动的周期等于驱动力的周期;波长越长,越容易发生衍射;声波的频率由振动频率决定;偏振现象说明光是横波;根据光的折射定律,即可求解.A、受迫振动的周期取决于驱动力的周期,当振动周期等于固有周期时,会出现共振动现象,故A正确;
B、未见其人先闻其声,是因为声波波长较长,容易发生衍射现象,故B正确;
C、声波的频率由振动频率决定,与在某种介质中传播的速度和波长的大小无关,故C错误;
D、偏振现象说明光是横波,故D正确;
E、光线以入射角θ1从玻璃射入水中时的折射角为θ2,则玻璃相对水的折射率n=
sinθ2
sinθ1,故E错误;
故选:ABD.点评:
本题考点: 波的干涉和衍射现象;产生共振的条件及其应用;光的折射定律;光的偏振.
考点点评: 考查受迫振动的周期与什么有关,掌握波的明显衍射条件,认识偏振现象的作用,理解光的折射定律中,折射率始终大于1.1年前查看全部
- (2009•崇明县二模)实验室用氯化钠配制lOOg溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解;②称取氯化钠;
(2009•崇明县二模)实验室用氯化钠配制lOOg溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解;②称取氯化钠;③计算;④量取水;⑤装瓶贴标签.正确的操作顺序是( )
A.①②③④⑤
B.③②④①⑤
C.①③⑤②④
D.③②④⑤① intria1年前1
intria1年前1 -
 startle 共回答了19个问题
startle 共回答了19个问题 |采纳率89.5%解题思路:根据配制溶质质量分数一定的溶液的基本步骤考虑;配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放.
故选B.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 通过回答本题知道了配制溶质质量分数一定的溶液的基本步骤,要熟记它们并能灵活运用.1年前查看全部
- (2014•静安区二模)人的血液中存在H2CO3~HCO3-这样“一对”物质,前者的电离和后者的水解两个平衡使正常人血液
(2014•静安区二模)人的血液中存在H2CO3~HCO3-这样“一对”物质,前者的电离和后者的水解两个平衡使正常人血液的pH保持在7.35~7.45之间.血液中注射碱性物质时,上述电离和水解受到的影响分别是( )
A.促进、促进
B.促进、抑制
C.抑制、促进
D.抑制、抑制 hyf12051年前1
hyf12051年前1 -
 jp15823988 共回答了18个问题
jp15823988 共回答了18个问题 |采纳率100%解题思路:碳酸电离的离子方程式为:H2CO3 ⇌HCO3-+H+; 碳酸氢根水解的离子方程式为:HCO3-+H20⇌H2CO3+0H-,结合浓度对化学平衡移动的影响解答.向血液中注射碱性物质时,氢氧根离子浓度增大.
碳酸电离的离子方程式为:H2CO3⇌HCO3-+H+; 增大氢氧根离子浓度,消耗氢离子,平衡向正向移动,促进碳酸的电离;
碳酸氢根水解的离子方程式为:HCO3-+H20⇌H2CO3+0H-,增大氢氧根离子浓度,平衡向逆向移动,抑制碳酸氢根离子的水解,
故选:B.点评:
本题考点: 盐类水解的应用;弱电解质在水溶液中的电离平衡.
考点点评: 本题考查了弱电解的电离和盐类水解的影响因素,题目难度不大,熟悉弱电解质电离和盐类水解的实质,清楚浓度对化学平衡移动的影响是解题的关键.1年前查看全部
- (2013•内江二模)(3x−1x)6的二项展开式中,常数项为( )
(2013•内江二模)(3x−
)6的二项展开式中,常数项为( )1 x
A.-162
B.162
C.-540
D.540 骑着毛驴上高速1年前1
骑着毛驴上高速1年前1 -
 zhangsm2002 共回答了20个问题
zhangsm2002 共回答了20个问题 |采纳率95%解题思路:在二项展开式的通项公式中,令x的幂指数等于0,求出r的值,即可求得常数项.二项式(3x−
1
x)6的展开式的通项公式为 Tr+1=
Cr6•(3x)6-r•(-1)r•x-r=(−1)r•
C r6•36-r•x6-2r,
令6-2r=0,解得 r=3,
故常数项为 (−1)3•
C 36• 33=-540,
故选C.点评:
本题考点: 二项式系数的性质.
考点点评: 本题主要考查二项式定理的应用,二项展开式的通项公式,求展开式中某项的系数,属于中档题.1年前查看全部
- (2007•杭州二模)设A={x|2≤x≤π,x∈R},定义在集合A上的函数y=logax(a>0且a≠1)的最大值比最
(2007•杭州二模)设A={x|2≤x≤π,x∈R},定义在集合A上的函数y=logax(a>0且a≠1)的最大值比最小值大1,则底数a的值是[π/2]或[2/π][π/2]或[2/π].
 hh客5201年前1
hh客5201年前1 -
 MOUSEpan 共回答了18个问题
MOUSEpan 共回答了18个问题 |采纳率88.9%解题思路:先看单调性,再研究最值,当a>1时,函数是增函数,则2对应最小值,π对应最小值,再按条件求解;当0<a<1时,函数是减函数,则π对应最小值,2对应最小值,再按条件求解;两个结果取并集.当a>1时,函数是增函数,
根据题意有:logaπ-loga2=1
即:loga [π/2]=1
∴a=[π/2]
当0<a<1时,函数是减函数,
根据题意有:loga2-logaπ=1
即:loga [2/π]=1题
∴a=[2/π]
综上:a的值为:[π/2]或 [2/π]
故答案为:[π/2]或[2/π].点评:
本题考点: 对数函数的单调性与特殊点.
考点点评: 本题主要考查对数函数的最值,在研究最值时,一定要研究函数的单调性,还要注意函数的定义域.1年前查看全部
- (2011•湛江二模)下列有关生物学实验的描述正确的是( )
(2011•湛江二模)下列有关生物学实验的描述正确的是( )
A.粗提取的DNA加入二苯胺试剂后并加热,可观察到溶液变蓝
B.观察叶绿体中的DNA时,要换用高倍镜后观察
C.提取和分离叶绿体色素时,应加入CaCO3防止色素被破坏
D.分离纤维素分解菌时,培养基中的纤维素要用苏丹红染色 liulei23081年前0
liulei23081年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•吉州区二模)下列有关实验现象的描述,正确的是( )
(2014•吉州区二模)下列有关实验现象的描述,正确的是( )
A.打开盛浓盐酸的试剂瓶瓶盖,一会儿瓶口会产生白烟
B.镁在空气中燃烧发出耀眼的白光,放出热量,生成一种白色固体
C.铁丝在空气中剧烈燃烧时,火星四射,生成黑色固体
D.木炭在氧气中燃烧产生大量白烟 淡蓝色雪291年前1
淡蓝色雪291年前1 -
 hhfh1 共回答了18个问题
hhfh1 共回答了18个问题 |采纳率83.3%解题思路:A、根据浓盐酸具有挥发性进行解答;
B、根据镁在氧气中燃烧的现象进行分析判断.
C、根据铁丝在氧气中燃烧的现象进行分析判断.
D、根据木炭在氧气中燃烧的现象进行分析判断.A、浓盐酸具有挥发性,挥发出氯化氢气体,打开浓盐酸瓶塞,可看到大量白雾,故A错;
B、镁条是银白色固体,具有可燃性,在空气中点燃镁条,发出耀眼的白光,放出热量,生成一种白色的粉末,故正确;
C、铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体;铁丝在空气中不能燃烧,故错误.
D、木炭在氧气中燃烧时,发出白光,并能生成使澄清的石灰水变浑浊的气体. 故错误.
故选:B点评:
本题考点: 酸的物理性质及用途;氧气与碳、磷、硫、铁等物质的反应现象.
考点点评: 本题可结合的当时实验的现象来判断题目中的现象表述是否正确,在这里要注意:化学现象的概念和雾、烟的区别.1年前查看全部
- (2010•宣武区二模)小刚和小明在探究滑轮组的机械效率与哪些因素有关的实验中,使用几个规格相同的滑轮分别组成“一定一动
(2010•宣武区二模)小刚和小明在探究滑轮组的机械效率与哪些因素有关的实验中,使用几个规格相同的滑轮分别组成“一定一动”滑轮组和“两定两动”滑轮组做实验,记录的实验数据如下表.假设实验中滑轮轴的摩擦、绳重均忽略不计.请根据表格中的实验数据回答下列问题:
(1)请将表中数据补充完整.项目
滑轮组钩码重/N 钩码上升高度/m 绳端拉力/N 绳端上移的距离/m 机械效率 一定一动滑轮组 4 0.1 1.6 0.3 83.3% 6 0.1 2.2 0.3 90.9% 8 0.1 2.9 0.3 92.0% 两定两动滑轮组 4 0.1 1.1 0.5 72.7% 6 0.1 1.4 0.5 8 0.1 1.8 0.5 88.9%
(2)分析比较表中的数据,可以初步得到滑轮组机械效率与所提升的物体所受重力之间的定性关系是:使用同一滑轮组提升重物,滑轮组的机械效率随提升物体所受重力的增加而增大.除此之外,根据表中的实验数据你还可以得到的初步结论是:______. Jane_crystal9161年前1
Jane_crystal9161年前1 -
 你梦见的小兔子 共回答了13个问题
你梦见的小兔子 共回答了13个问题 |采纳率100%解题思路:(1)根据η=
×100%=[Gh/Fs]×100%计算出滑轮组的机械效率;W有用 W总
(2)掌握影响滑轮组机械效率的两个主要因素:提升的物重和动滑轮重.分析表格中重力相同而动滑轮不同的情况,比较滑轮组机械效率的大小得出结论.(1)由表格中数据知,η=
W有用
W总×100%=[Gh/Fs]×100%=[6N×0.1m/1.4N×0.5m]×100%=85.7%;
(2)由表格中1、4或2、5或3、6行数据知,被提升的物重相同,动滑轮的个数越多,滑轮组的机械效率越小,可得使用不同滑轮组提升相同的重物,滑轮组的机械效率随动滑轮重力的增加而减小.
故答案为:(1)85.7%;(2)使用不同滑轮组提升相同的重物,滑轮组的机械效率随动滑轮重力的增加而减小.点评:
本题考点: 滑轮(组)机械效率的测量实验.
考点点评: 此题是测量滑轮组机械效率实验,考查了机械效率的计算及影响滑轮组机械效率的两个主要因素.要学会用控制变量法对数据进行分析.1年前查看全部
- (2009•南汇区二模)请根据所学化学知识回答:
(2009•南汇区二模)请根据所学化学知识回答:
(1)写出编号的仪器名称:C:______、F:______.
(2)图G实验操作的目的是______,从该图观察到的实验现象中,你能得到的结论是______.
(3)实验室欲利用上述仪器完成氯酸钾与二氧化锰混合制取氧气的实验,还需要酒精灯,写出该反应的化学方程式2KClO3
2KCl+3O2↑MnO2 .△ 2KClO3.
2KCl+3O2↑MnO2 .△
(4)使用酒精灯时,有时会出现灯内有酒精却点不燃的现象,你认为可能的原因是______.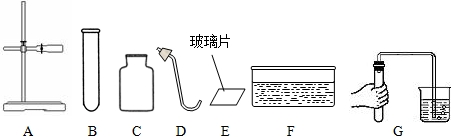
 菜鸟权威人士1年前1
菜鸟权威人士1年前1 -
 草一棵 共回答了13个问题
草一棵 共回答了13个问题 |采纳率100%解题思路:(1)C、F均为实验室常用的仪器,熟记常用仪器的名称即可轻松作答.
(2)从实验室制取气体的实验步骤和大气压的知识进行分析.
(3)熟记常用的化学方程式.
(4)根据酒精的挥发性进行分析.(1)熟记常用仪器的名称可知C为酒精灯,E为水槽.
(2)实验室制取气体前都要先检验装置的气密性,若装置漏气,会造成收集下的气体不纯或收集不下气体;把导管的一端浸入水中,两手紧握试管外壁,试管内的空气受热膨胀,气体压强增大,若装置不漏气会看到导管口有气泡冒出.
(3)氯酸钾以二氧化锰为催化剂加热生成氯化钾和氧气.
(4)不用酒精灯时要一直盖上灯帽,防止酒精挥发.
故答案为:(1)集气瓶、水槽.
(2)检查装置的气密性.该装置的气密性良好.
(3)2KClO3
MnO2
.
△2KCl+3O2↑
(4)未盖灯帽,酒精挥发,灯芯上有过多的水分.点评:
本题考点: 氧气的制取装置;常用仪器的名称和选用;实验室制取氧气的反应原理;书写化学方程式、文字表达式、电离方程式.
考点点评: 在实验室做实验时一定要严格按照实验步骤和实验操作规则进行,否则轻者会造成实验结果不准,重者会发生实验事故.1年前查看全部
- (2012•松江区二模)计算:2-2=[1/4][1/4].
 夜侵城1年前1
夜侵城1年前1 -
 天狗蚀月 共回答了22个问题
天狗蚀月 共回答了22个问题 |采纳率77.3%解题思路:根据负整数指数幂的定义求解:a-p=
(a≠0,p为正整数)1 ap 2-2=[1
22=
1/4],
故答案为[1/4].点评:
本题考点: 负整数指数幂.
考点点评: 本题考查了负整数指数幂的定义,解题时牢记定义是关键,此题比较简单,易于掌握.1年前查看全部
- (2009•兴化市二模)下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就能将它们一一鉴别出来
(2009•兴化市二模)下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就能将它们一一鉴别出来的是( )
A.NaCl、BaCl2、CuSO4、NaOH、KNO3
B.Ba(NO3)2、NaCl、Na2SO4、H2SO4、HCl
C.NaOH、FeCl3、MgSO4、BaCl2、KCl
D.AgNO3、HCl、Na2CO3、KCl、CaCl2 快乐为主1231年前1
快乐为主1231年前1 -
 qqq3334199 共回答了23个问题
qqq3334199 共回答了23个问题 |采纳率95.7%解题思路:先分析选项中有没有带色的物质,有带色物质的借助带色物质鉴别,没有带色物质的,借助表格列举出反应现象进行鉴别.A、先根据溶液的颜色鉴别出蓝色的溶液是硫酸铜,将剩余的四种物质分别滴加硫酸铜,会生成蓝色沉淀的是氢氧化钠,将硫酸铜滴入其余三份样品中,产生白色沉淀的原溶液为氯化钡.但是剩余的两种物质不会鉴别,故A错误,
B、
Ba(NO3)2 NaCl Na2SO4 H2SO4 HCl
Ba(NO3)2 ---- 无现象 沉淀 沉淀 无现象
NaCl 无现象 ------ 无现象 无现象
Na2SO4 沉淀 无现象 ------ 无现象 无现象
H2SO4 沉淀 无现象 无现象 ---- 无现象
HCl 无现象 无现象 无现象 无现象 ------分别有两组现象是相同的,不能鉴别,故B错误,
C、先根据溶液的颜色鉴别出黄色的溶液是氯化铁,然后在剩余的四种溶液中滴加氯化铁,会生成红褐色沉淀的是氢氧化钠,再将氢氧化钠滴入剩余的三种溶液中会生成白色沉淀的是硫酸镁,再将氯化镁滴入剩余的两种溶液中,会生成白色沉淀的是氯化钡,剩余的就是氯化钾,故C正确,
D、
AgNO3 HCl Na2CO3 KCl CaCl2
AgNO3 ---- 沉淀 沉淀 沉淀 沉淀
HCl 沉淀 ---- 气体 无现象 无现象
Na2CO3 沉淀 气体 ---- 无现象 沉淀
KCl 沉淀 无现象 无现象 ---- 无现象
CaCl2 沉淀 无现象 沉淀 无现象 ----五组中的现象是不同的,可以鉴别,故D正确,
故选CD.点评:
本题考点: 酸、碱、盐的鉴别.
考点点评: 在做物质的鉴别题时,主要分为两类:一类是选项中的有带色的离子,首先鉴别,然后再区别其他的物质,另一类是选项中的物质都是无色的,就需要借助表格进行鉴别,不管哪种,在鉴别时每组出现的现象不能完全相同.1年前查看全部
- (2014•肇庆二模)生命必需的水在化学中常用作溶剂和原料.
(2014•肇庆二模)生命必需的水在化学中常用作溶剂和原料.
(1)部分地下水含较多______物质称为硬水;酸雨中因含有______导致土壤酸化(填一种化学式);
(2)下列实验均用到水,其中仅作为溶剂的是______(填字母序号)
a.配制0.9%的生理盐水b.生石灰变成熟石灰
(3)下列两组固体物质用水即可鉴别的是______(填字母序号)
a.CuSO4,Na2SO4b.NaCl,Na2SO4
(4)4月11日,兰州法国威立雅自来水公司出厂水及自流沟水中检测出苯含量严重超标.苯的沸点80.10℃,可用煮沸蒸发和吸附过滤的方法清除水中的苯.已知苯的化学式C6H6,其中碳的百分含量是______(精确到0.1%). korla50g1年前1
korla50g1年前1 -
 我是ggvv 共回答了12个问题
我是ggvv 共回答了12个问题 |采纳率91.7%解题思路:根据水中含有钙离子、镁离子的多少可以把水分为硬水和软水,当雨水的pH小于5.6时称为酸雨,海水的主要成分是水,分子能够保持物质的化学性质;
水的用途很广泛;根据物质中某元素的质量分数=[碳元素相对原子质量×原子个数/物质相对分子质量]×100%,分别计算选项中含碳元素的质量分数,即可解答.(1)部分地下水含较多的可溶性钙、镁化合物,这种水属于硬水;二氧化硫、氮氧化物等物质溶解在雨水中,能和水反应生成亚硫酸、硫酸、硝酸等物质,这些物质进入土壤中,能使土壤酸化,硫酸的化学式是H2SO4;
故填:可溶性钙、镁化合物;H2SO4.
(2)配制0.9%的生理盐水时,水作为溶剂,起到溶解氯化钠的作用;生石灰变成熟石灰时,生石灰和水反应生成熟石灰,水是反应物.
故填:a.
(3)硫酸铜溶于水时,溶液是蓝色的,硫酸钠溶于水时,溶液是无色的,硫酸钠和硫酸铜用水就可以鉴别;而氯化钠和硫酸钠溶于水时,溶液都是无色的.
故填:a.
(4)已知苯的化学式C6H6,其中碳的百分含量是[12×6/12×6+1×6]×100%=92.3%.
故答案为:92.3%.点评:
本题考点: 硬水与软水;水的性质和应用;酸雨的产生、危害及防治;酸、碱、盐的鉴别;元素的质量分数计算.
考点点评: 能量之间可以相互转化,这为人类认识自然、改造自然提供了条件,因此能量转化方面的题目是考试热点之一.1年前查看全部
- (2012•黄浦区二模)函数f(x)=log12(2x+1)的定义域为(-[1/2],+∞)(-[1/2],+∞).
 眉山熊猫1年前1
眉山熊猫1年前1 -
 34789 共回答了15个问题
34789 共回答了15个问题 |采纳率73.3%解题思路:根据对数函数的性质可知对数函数的真数大于0,建立不等关系,解之即可求出所求.∵2x+1>0
∴x>-[1/2]
即函数f(x)=log
1
2(2x+1)的定义域为(-[1/2],+∞)
故答案为:(-[1/2],+∞)点评:
本题考点: 对数函数的定义.
考点点评: 本题主要考查了对数函数的定义域,掌握对数函数的性质是关键,属于基础题.1年前查看全部
- (2010•南汇区二模)如图(a)所示,弹簧测力计的最小分度值为______牛,在进行测量之前,首先要通过调节使指针__
(2010•南汇区二模)如图(a)所示,弹簧测力计的最小分度值为______牛,在进行测量之前,首先要通过调节使指针______.在水平平衡的杠杆两端分别挂上两组钩码后,发现杠杆不平衡,如图b所示,这时应______第二组钩码的个数(选填“增加”或“减少”)、或向______调节第二组钩码的位置(选填“左”或“右”),使杠杆水平平衡.

 水瓶月兔1年前1
水瓶月兔1年前1 -
 nibushaa 共回答了17个问题
nibushaa 共回答了17个问题 |采纳率82.4%解题思路:在进行测力计的读数时,注意测力计的分度值,在读数之前注意将指针调零;
掌握杠杆的平衡条件:F1L1=F2L2,要使杠杆平衡,应使两边力和力臂的乘积相等.由(a)知,测力计的分度值为0.2N;
在进行测量之前,首先要通过调节使指针指在零刻度线处;
由(b)知,杠杆的右端较低,根据杠杆平衡条件,要使杠杆平衡,应减小第二组的钩码个数或减小第二组的力臂,将第二组的钩码向左移动.
故答案为:0.2;指在零刻度线处;减少;左.点评:
本题考点: 探究杠杆的平衡条件实验.
考点点评: 此题是探究杠杆的平衡条件实验考查了测力计的使用及读数,同时考查了杠杆平衡条件的应用.1年前查看全部
- (2014•包头二模)如果执行如图所示的框图,输入N=5,则输出的数等于( )
(2014•包头二模)如果执行如图所示的框图,输入N=5,则输出的数等于( )

A.[25/42]
B.[25/21]
C.[19/21]
D.[2/21] vanf19801年前1
vanf19801年前1 -
 wangwang8666 共回答了20个问题
wangwang8666 共回答了20个问题 |采纳率85%解题思路:k=1,满足条件k<4,执行循环体,得S值,依此类推,k=3,满足条件k<4,执行循环体,当k=4,不满足条件k<4,退出循环体,最后利用裂项求和法求出所求即可.k=1,S=[1/3],满足条件k<4,
k=2,S=[1/3]+[1/8],满足条件k<4
k=3,S=[1/3]+[1/8]+[1/15],满足条件k<4,
k=4,S=[1/3]+[1/8]+[1/15]+[1/24],满足条件k<4,
k=5,S=[1/3]+[1/8]+[1/15]+[1/24]+[1/35],不满足条件k<4,退出循环,输出S=[25/42].
故答案为:A.点评:
本题考点: 循环结构.
考点点评: 根据流程图(或伪代码)写程序的运行结果,是算法这一模块最重要的题型,属于基础题.1年前查看全部
- (2008•沈阳二模)在如图所示的图中绕制螺线管,当S合上且变阻器滑片向左移动弹簧伸长.
 小越1年前0
小越1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 2010金山区初三语文二模试卷及答案
 蜀山少1年前1
蜀山少1年前1 -
 思冬 共回答了16个问题
思冬 共回答了16个问题 |采纳率87.5%问你老师去1年前查看全部
- 2011高三黄埔区化学二模 计算30题求解
 swee20021年前1
swee20021年前1 -
 摩根mm 共回答了13个问题
摩根mm 共回答了13个问题 |采纳率76.9%(1)代公式c=(1000*1.47*0.57)/98=8.55mol/l
(2)分别设加入的质量为m1 m2.式一 (m1*0.57)/(m1+m2)=0.27
式二 (m2*0.57)/(m1+m2)=0.3
两个式子一比,就只剩下m1.m2的关系比了.最终答案m1/m2=9/101年前查看全部
- 2011初中海淀二模数学18题肿么做额
 阿狄丽丝1年前4
阿狄丽丝1年前4 -
 falfred 共回答了16个问题
falfred 共回答了16个问题 |采纳率100%设租用甲种汽车x辆,则乙种(8-x)辆
由题意得 40x+30(8-x)大于等于290
10x+20(8-x)大于等于100
解得5小于等于x小于等于6
所以共有两种租车方案(1)甲5辆,乙3辆
(2)甲6辆,乙2辆
如有不懂,欢迎追问~1年前查看全部
大家在问
- 1问一道初中单位转换题?125cm= km?
- 2碘固体为什么不经液态就直接升华成碘蒸气?
- 3在提问一小时内解决,加到50分把一个两位数的个位与十位上的数字互相交换后,得到一个新的两位数等于原来的两位数的七分之四,
- 4已知x=2是一元二次方程ax^2;+bx-10=0的一个解a+1/2-3的值
- 5根据意思写出表示“看”的意思的成语:1.表示粗略地看()(含“看”字的)
- 6畜牧场养猪的头数比养牛头数多72,猪45% 牛5% 羊35% 马5%;求各牲畜的数量分别是多少?
- 7合唱团原有学生33人,后来又进来3个男生,此时男生人数比女生的2倍少6人,这个合唱团原有男生,女生各有多少人?
- 8自来水的TDS值是多少?今日用TDS测试自来水的TDS值是是100左右(中山市).还有矿泉水的TDS,和纯净水的TDS又
- 9访写下列这几句话燕子去了,有再来的时候;杨柳枯了,有再青的时候;桃花谢了,有再开的时候.
- 10奥巴马说过的一句箴言,大概意思是要珍惜时间,这句话是啥啊?
- 11为什么没装过滤器的水用TDS笔测是255ppm而装过滤的水测出值更高呢?
- 12“如饮甘醇,如食美珍,如沐春风”的意思是什么?
- 13英语,根据要求转换句子,每空一词.
- 14果园里有48棵苹果树,比桃树少2/5,桃树比苹果树多多少棵?
- 15已知关于x的方程x^2-(k+1)x+四分之一k^2+1=0的两根是一个矩形两边的长.当矩形对角线根五时求k的值
